Миастения гравис (МГ)— хроническое нейроиммунное заболевание, способное проявиться влюбом периоде жизни, но, как правило, поражающее лиц молодого, трудоспособного возраста. Известно, что дебют заболевания приходится на20–30 лет [1, 9, 13]. Патологические процессы при МГобусловлены нарушением нейромышечной передачи под действием аутоантител кацетилхолиновым рецепторам постсинаптической мембраны. Врезультате формируется аутоиммунный постсинаптический блок вследствие уменьшения числа рецепторов ацетилхолина инедостаточной чувствительности ихкмедиатору [1].
С каждым годом растет число описанных случаев сочетания МГ c демиелинизирующими заболеваниями (ДЗ) ЦНС. Среди последних отмечают миелит, ретробульбарный неврит, острый рассеянный энцефаломиелит, рассеянный склероз (РС), оптикомиелит [2, 3]. Однако, принимая во внимание небольшое число исследований в рамках описанной проблемы, низкую распространенность как МГ, так и ДЗ ЦНС, в настоящее время вопрос о сущности данной ассоциации остается открытым: случайное ли это сочетание или оно является частью неспецифической иммунной реакции и генетической предрасположенности.
Как МГ, так и ДЗ ЦНС имеют прогрессирующее течение, быстро приводят к снижению трудоспособности, инвалидизации, ухудшению качества жизни больных, что обусловливает высокую медицинскую и социальную значимость проблемы [4]. Сочетание этой патологии, с одной стороны, утяжеляет состояние пациентов, с другой — удлиняет диагностический поиск в силу недостаточного опыта ведения пациентов с сочетанной аутоиммунной патологией.
Учитывая новизну и малую освещенность данной проблемы в отечественной научной литературе, мы полагаем, что обсуждение этого вопроса важно для формирования адекватной тактики ведения пациентов. В данной статье описан зарегистрированный нами случай сочетания МГ и ДЗ ЦНС.
Клинический случай
Женщина, 36 лет, предъявляет жалобы на нарушение ходьбы, задержку мочи, запоры, головокружение, онемение в руках, стягивающие, сжимающие боли в туловище, ногах. В неврологическом статусе: полуптоз слева, нижний спастический парапарез, больше выраженный справа, гипалгезия по типу «куртки», горизонтальный нистагм при взгляде в стороны, тазовые нарушения по обструктивному типу.

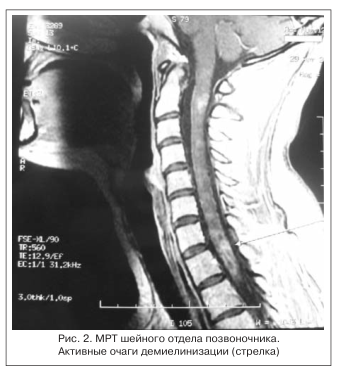
С 18-летнего возраста (после случая острого тонзиллита) развилась генерализованная форма МГ. Через 1,5 года от момента заболевания МГ проведена тимэктомия по причине недостаточного эффекта от проводимой терапии (антихолинэстеразные препараты, плазмаферез) и выявления гиперплазии тимуса при компьютерной томографии средостения, подтвержденной морфологически. Течение заболевания после оперативного лечения было стабильным, пациентка получала пиридостигмина бромид в дозе 120 мг/сут. В возрасте 29 лет остро развился поперечный миелит с синдромом выраженных опоясывающих болей в грудном и поясничном отделах позвоночника, нарушением функции тазовых органов. После курса пульс-терапии метилпреднизолоном по 1000 мг в/в № 5, прегабалином 150 мг 3 р./сут (в течение 3 нед.) в сочетании с нейропротективной терапией наблюдался регресс болевого синдрома, однако сохранялись ирритативные нарушения мочеиспускания. Рецидив миелита произошел через полгода с развитием умеренно выраженного нижнего спастического парапареза и расстройством чувствительности по проводниковому типу. Курс патогенетического лечения (пульс-терапия метилпреднизолоном в общей дозе 5000 мг, 3 сеанса плазмафереза) позволил добиться положительной динамики: отмечались увеличение мышечной силы, регресс чувствительных нарушений. В дальнейшем пациентка в течение 3 лет наблюдалась с диагнозом РС, получала лечение β-интерфероном-1в в дозе 8 млн МЕ. Следующий рецидив поперечного продольного миелита зарегистрирован через 3 года, проявлялся спастической параплегией, гипалгезией по типу «куртки», задержкой мочеиспускания. За 3 мес. до описанного рецидива β-интерферон-1в был отменен по причине «сочетания 2-х заболеваний: МГ и РС». После повторного курса гормонотерапии наблюдались стабилизация состояния, уменьшение степени пареза до 3 баллов в нижних конечностях, регрессировали тазовые нарушения, уменьшилась степень спастичности. Магнитно-резонансная томография (МРТ) головного мозга на протяжении всего времени с момента дебюта спинальных нарушений выявляла симметричные округлые очаги демиелинизации (до 7), наибольший — 4 мм в диаметре, в теменных долях с 2-х сторон — без накопления контрастного вещества и отрицательной динамики (рис. 1). Все эпизоды экзацербаций подтверждались нейровизуализацией грудного и шейного отделов позвоночника, которая выявила активные очаги демиелинизации, протяженные по длиннику спинного мозга более чем на 3 сегмента и занимающие 2/3 его диаметра (рис. 2). Исследование зрительных вызванных потенциалов не выявило патологии. Кроме того, на фоне рецидивов миелита наблюдалось ухудшение течения МГ, что требовало увеличения дозы антихолинэстеразных препаратов до 240 мг/сут.
Обсуждение
Таким образом, в представленном нами случае имело место развитие ДЗ ЦНС — рецидивирующего распространенного продольно-поперечного миелита на фоне диагностированной ранее МГ и последовавшей тимэктомии. Вопрос о влиянии тимэктомии на развитие ДЗ ЦНС у больных МГ является предметом, вызывающим повышенный интерес у специалистов [5]. Согласно тимогенной теории, возникновение МГ связывают с патологическими изменениями тимуса: гиперплазией, опухолью и др. [6]. Существуют неоспоримые данные, указывающие на участие дисфункции вилочковой железы в патогенезе МГ, однако ее структурные нарушения при этом заболевании довольно гетерогенны [6, 7]. В связи с этим тимэктомия является основным патогенетически обоснованным методом комплексного лечения больных МГ [4]. Результаты долгосрочных наблюдений оперативного лечения МГ как в отечественной, так и зарубежной литературе немногочисленны. Имеются сообщения об отсутствии патологии тимуса и неэффективности тимэктомии в отдельных клинических группах МГ, выделяют «тимус-независимые» формы заболевания [8]. Высказывается мнение, что дисрегуляция гуморального иммунитета, опосредованная тимэктомией, предрасполагает к развитию оптиконевромиелита и РС [9–12]. При отсутствии крупных проспективных исследований в настоящее время нельзя оценить последствия для пациента и степень риска развития ДЗ ЦНС после подобной операции.
Другим сценарием развития обсуждаемого сочетания заболеваний являются случаи МГ, развившейся на фоне уже существующего ДЗ ЦНС — РС. Необходимо отметить, что в некоторых случаях пациенты принимали лечение β-интерферонами-1а и -1в или глатирамера ацетатом [3, 12–14]. Возникновение патологии нейромышечной передачи на фоне терапии препаратами, изменяющими течение РС, может иметь следующие объяснения. Подобное лечение могло спровоцировать развитие аутоиммунного процесса посредством модуляции иммунного ответа: усиления Th2-клеточных реакций, увеличения продукции аутоантител [14]. С другой стороны, развитие 2-х заболеваний у одного пациента может быть спорадическим, возникшим вне зависимости от наличия иммуномодулирующей терапии [14].
Заключение
Изучение вопросов коморбидности МГ и ДЗ ЦНС имеет как теоретическую, так и практическую значимость. Определение распространенности сочетания этих 2-х состояний и тщательный сбор катамнеза пациентов после тимэктомии по поводу МГ помогут ответить на важный вопрос о природе данной ассоциации: случайность это или закономерность. Расшифровка иммунопатологических механизмов, лежащих в основе подобных сочетаний, внесет существенный вклад в понимание факторов риска, течения заболеваний, планирование их терапии и определение прогноза.














