Спастичность – результат повреждения кортикоспинальных путей головного и спинного мозга вследствие травмы головы, цереброваскулярных катастроф, опухолей мозга или других неврологических заболеваний, например, – рассеянного склероза. Появляющееся повышение мышечного тонуса неблагоприятно влияет на походку пациента, способность принимать и удерживать ту или иную позу, выполнять повседневные действия, а также затрудняет проведение физиотерапевтических процедур и уход за пациентами, прикованными к постели. Нелеченая спастичность приводит к контрактурам сухожилий, деформациям, боли и значительному нарушению физической активности. В связи с отсутствием эффективных методов лечения заболевания, лежащего в основе спастичности, применяются симптоматические средства – миорелаксанты и антиспастические препараты.
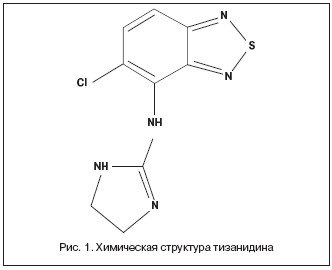
Тизанидин (Сирдалуд), a2–адренергический агонист–миорелаксант центрального действия, главной точкой приложения которого является спинной мозг. Отличается от других миорелаксантов по химической структуре (рис. 1) и механизму действия [1–3]. Он снижает повышенный мышечный тонус, вызванный гиперактивностью a– и g–моторных систем, подавляя проведение в полисинаптических путях активации мотонейронов. Миорелаксирующий эффект тизанидина, возможно, обусловлен пресинаптической модуляцией высвобождения аминокислот из спинальных интернейронов (вероятно, посредством центральных норадренергических механизмов, реализующихся через стимуляцию норадренергических a2–рецепторов) [2]. Предшествующие работы показали эффективность тизанидина в отношении снижения мышечного гипертонуса, спазма и клонуса [4–11], но при этом его стандартная таблетированная форма (СТФ) должна назначаться 3–4 раза в сутки. Сейчас появилась форма тизанидина в виде капсул с модифицированным высвобождением (ТМВ) – по 6 или 12 мг в капсуле.
Фармакология и фармакокинетика
Сравнительная биодоступность
Исследования показали сходную биодоступность при приеме капсул по 6 и 12 мг ТМВ и СТФ, кроме того, биодоступность не менялась при приеме пищи с высоким содержанием жиров. У здоровых добровольцев биодоступность ТМВ составила 98% от таковой при использовании СТФ по 2 мг 3 раза в сутки [12,13]. Аналогичные результаты получены и в другом исследовании на здоровых добровольцах при использовании 12 мг ТМВ и СТФ в дозе 4 мг 3 раза в сутки. Биодоступность препаратов обеих дозировок не различалась как при однократном, так и при постоянном приеме (рис. 2) [13].
Также выявлено, что у женщин, принимающих оральные контрацептивы, концентрация тизанидина в плазме более высокая, чем у мужчин, поэтому не исключена возможность взаимодействия препарата с оральными контрацептивами.
В другой работе изучено влияние пищи на биодоступность ТМВ. Препарат назначался через 4 часа после приема пищи, богатой жирами, или непосредственно перед едой. В последнем случае биодоступность составила 98,4% от таковой при приеме препарата за 4 часа до еды. Также было показано, что при приеме лекарства непосредственно перед едой, в плазме оно появлялось на 36 минут позже по сравнению с приемом за 4 часа до еды, что не имеет важного клинического значения.
Другие фармакокинетические показатели измерялись для оценки действия ТМВ in vivo [15]. Максимальная активность препарата обычно отмечается в период его наибольшей концентрации в плазме крови, а продолжительность активности зачастую связана с длительностью сохранения максимальной концентрации. Эта длительность была оценена с помощью половинной величины максимальной концентрации в плазме. Время, в течение которого в плазме крови сохранялась концентрация препарата, превышающая половину максимального значения, называется длительностью половинной концентрации (ДПК). При этом коэффициент ретардности (R) показывает, во сколько раз ДПК удлинена при использовании ТМВ по сравнению с СТФ.
В ходе описанных ранее исследований биодоступности однократной дозы препарата также изучалась фармакокинетика стандартной и модифицированной форм. В двух из этих исследований был вычислен R, и у ТМВ наблюдался приемлемый ретардный профиль. У ТМВ выявлены более низкие максимальные плазменные концентрации, достигаемые медленнее, чем при приеме СТФ, но площадь под кривой (Area under curve – AUC) была одинаковой для обеих форм. Относительная биодоступность капсул, содержащих 6 и 12 мг тизанидина, по сравнению с эквивалентными суточными дозами СТФ составила 98 и 105% соответственно. ДПК была выше для обеих дозировок ТМВ. Эти различия, отраженные в значении R, доказали отличные ретардные свойства препарата (табл. 1).
При регулярном приеме 12 мг ТМВ максимальная концентрация в плазме была ниже по сравнению с таковой при назначении СТФ по 4 мг три раза в сутки, но время достижения максимальных концентраций было сопоставимо (табл. 2).
Различий между AUC выявлено не было, однако ДПК значительно (р<0,01) удлинилась при приеме ТМВ, а значение коэффициента ретардности 2,02 подтвердило отличные характеристики нового ТМВ. Кроме того, минимальная плазменная концентрация ТМВ была достаточно высокой и в проценте от пиковой была значительно (р<0,01) выше, чем у СТФ, как при однократном, так и при постоянном приеме, что указывает на возможность достигать более стабильных плазменных концентраций при использовании МФТ. Однако один вопрос остается без ответа: будут ли плазменные концентрации, достигнутые при приеме МФТ, настолько же эффективны, как и при приеме СТФ? Проведено исследование среди здоровых добровольцев для оценки влияния 12 и 24 мг ТМВ по сравнению с приемом СТФ тизанидина по 4 мг три раза в сутки и плацебо на показатели электроэнцефалограммы, как непрямой показатель активности препарата [16]. Выявлено, что ответ на тизанидин напрямую зависел от его концентрации в плазме и не зависел от формы препарата.
Переносимость в группе
здоровых добровольцев
В другой работе исследовалась переносимость ТМВ в дозировках 6–24 мг [17]. Частота развития побочных эффектов была низкой, а в одном исследовании они не наблюдались вообще [14]. Как при однократном, так и при многократном приемах ТМВ во всех дозировках отмечалась хорошая переносимость по сравнению с плацебо и СТФ. Однако не представляется возможным точно определить частоту развития побочных эффектов в связи с малым числом включенных добровольцев, но наиболее распространенным побочным эффектом было чувство усталости, из–за которого из одного исследования выбыло 5 человек [13]. В целом частота и характер возникающих побочных эффектов одинаковы для ТМВ и СТФ. Также наблюдалось незначительное и преходящее снижение артериального давления, но это имело место преимущественно у пациентов, склонных к гипотонии или получающих гипотензивную терапию. Гематологические и биохимические показатели, как правило, оставались в пределах нормы, а изменения не имели клинической значимости.
Клинические исследования
Проведен ряд открытых несравнительных исследований с использованием ТМВ [18–22]. В связи с установленной эффективностью и хорошей переносимостью тизанидина, а также сложностями титрации индивидуальной дозы тизанидина 3 раза в сутки было решено не проводить сравнительные и слепые исследования. В целом в исследованиях приняло участие 80 пациентов (43 мужчины и 37 женщин) со спастичностью вследствие рассеянного склероза, различных поражений спинного мозга, цереброваскулярных заболеваний и поражения двигательных нейронов. Все пациенты получали от 6 до 24 мг ТМВ в сутки, но при этом не назначались другие антиспастические препараты или миорелаксанты.
Эффективность
В начале исследования спастичность оценивалась как тяжелая или очень тяжелая у 52 из 80 пациентов (65%), а общая недееспособность – у 48 из 80 пациентов (60%). По завершении исследования отмечено уменьшение спастичности у 75 (94%) пациентов, из них у 15% – значительное. Уменьшение общей недееспособности наблюдалось у 63 (79%) пациентов (у 9% – значительное). Уменьшение мышечного тонуса и клонусов наблюдалось в 82% случаев, уменьшение боли в руках и ногах – в 73%, улучшение функция мочевого пузыря – в 32% и способности к ходьбе в 66% случаев. Увеличение повседневной активности наблюдалось у 56 (70%) пациентов, но увеличение мышечной силы было небольшим, а степень улучшения других показателей колебалась от легкой до умеренной. Уменьшение общей спастичности (рис. 3) и недееспособности (рис. 4) было напрямую связано с продолжительностью лечения.
В целом терапия ТМВ оценивалась исследователями как эффективная у 71 (89%) пациентов, а сами пациенты считали ее эффективной в 69 (87%) случаях. Лечение СТФ и ТМВ было одинаково эффективно, и перевод со стандартной на модифицированную форму тизанидина не повлек за собой изменения эффективности [22]. Дозировка ТМВ была также сходна по сравнению с предшествующей терапией СТФ. Наиболее часто применяемая доза была 12 мг (40 пациентов), в то время как дозировка 24 мг потребовалась лишь 4 пациентам.
Побочные эффекты
Одной из главных целей исследований явилась оценка безопасности ТМВ. В течение исследования осуществлялся контроль массы тела, артериального давления, частоты сердечных сокращений, гематологических, биохимических показателей и анализа мочи, которые клинически значимо не менялись. Побочные эффекты возникли у 26 (33%) пациентов (табл. 3), из которых 35% составили мужчины и 30% – женщины. Наиболее частым побочным эффектом была мышечная слабость, развившаяся у 11 пациентов (14%). Чувство усталости, встречающееся у добровольцев, выявлено лишь у 7 (9%) пациентов. Гипотензия развилась у 1 пациента, однако изначально артериальное давление этого пациента было низким и изменилось незначительно. Головная боль и сердцебиение наблюдались у 1 пациента. Другие возникшие побочные эффекты были ожидаемы исходя из результатов исследования у добровольцев и опыта применения СТФ (табл. 3).
Число побочных эффектов было максимальным при использовании в дозе 18 мг и меньшим при применении дозы в 12 и 6 мг в сутки, и только один побочный эффект наблюдался при приеме 24 мг в сутки. Частота развития побочных эффектов была приблизительно одинакова при использовании ТМВ в дозе 6 и 12 мг в сутки, однако при использовании дозы в 18 мг в сутки она возрастала в 3 раза. В связи с малым числом пациентов, получавших 24 мг в сутки, значимых выводов сделать не удалось. В целом симптомы были мягкими и умеренными, преходящими и уменьшались при снижении дозы. Общая переносимость оценивалась как хорошая у 75 (94%) пациентов и у 4 (5%) пациентов как умеренно хорошая.
Выводы
Обычно у пациентов с заболеваниями ЦНС отмечается плохая переносимость препаратов центрального действия и миорелаксантов, однако, по данным клинических исследований, переносимость ТМВ была хорошей. Благодаря замедленному высвобождению препарата появилась возможность его назначения один раз в сутки, что является значительным преимуществом при длительном приеме для лечения хронических заболеваний. Кроме того, это ведет к улучшению комплаентности.
По результатам последних работ, тизанидин (3 раза в сутки в течение 7 дней) эффективен для лечения боли в нижней части спины, и при этом уменьшается необходимость применения анальгетиков [24].
Комбинация тизанидина и ибупрофена также показала большую эффективность по сравнению с ибупрофеном и плацебо [25]. Пациентам с болью в нижних отделах спины, сохраняющих повседневную активность, также удобно применение препарата один раз в сутки. Дальнейшее изучение клинических эффектов ТМВ будет основываться на базе этих начальных исследований.
Результаты исследований показывают, что ТМВ является безопасной и эффективной альтернативой СТФ для длительного лечения спастичности, возможно, обладающей преимуществом меньшей частоты развития побочных эффектов.
Реферат подготовлен Э.Р. Великовой
по материалам статьи D.R. Hutchinson
«Modified Release Tizanidine: a Review»
The Journal of International Medical Research
1989; 17: 565–573





Литература
1. Davies J: Selective depression of synaptic transmission of spinal neurones in the cat by a new centrally–acting muscle relaxant (DS 103 – 282). Br J Pharmacol 1982; 76: 473 – 481.
2. Davies J: Selective inhibition to responses to feline horn neurones to noxious cutaneous simuli by tizanidine (DS 103 – 282) and noradrenaline: involvement of alpha–2 adrenoreceptors. Neu–roscieme 1985: 16: 673 – 682.
3. Wiesendanger M: Neurophysiological investigations of tizanidine. In: Die klinische Wertung der Spatizitat (Conrad B, Benecke R. Bauer HJ. eds). Stuttgart: Schattauer Press, 1984; pp 39–55.
4. Hassan N, McLellan DL: Double blind comparison of single doses of DS 103 – 282, baclofen and placebo for the suppression of spasticity. J Neurol Newosurg Psychiatry 1980; 43: 1132 – 1136.
5. Newman PM, Nogues M, Newman PK, et ah Tizanidine in the treatment of spasticity. Eur J Clin Pharmacol 1982; 23: 31 – 35.
6. Taiti PG, Bavazzano A, Bevilacqua A: Tizanidine treatment of spasticity caused by CNS disorders. Preliminary observations. Biol Med 1984; 6: 149– 156.
7. Smolenski C: Vergleichsuntersuchung von Tiza–nidin und Baclofen bei der Behandlung der Spatizitat. In: Die klinische Wertung der Spatizitat (Conrad B, Benecke R, Bauer HJ, eds). Stuttgart: Schattauer Press, 1984; pp 101 – 110.
8. Jellinger K: Zur Behandlung der Spatizitat bei multiplier Sklerose. Ergebnisse einer Dop–pelblindstudie mit Tizanidine und Diazepam. In: Die klinische Wertung der Spatizitat (Conrad B, Benecke R, Bauer HJ, eds). Stuttgart; Schattauer Press, 1984; pp 171 – 190.
9. Gertstenbrand F, Williet J, Poewe W: Klinische Erfahrungen mit Tizanidin. In: Die klinische Wertung der Spatizitat (Conrad B, Benecke R, Nauer HJ, eds). Stuttgart: Schattauer Press, 1984; pp 191 –204.
10. Hoogstraten MC, van der Ploeg RJO, van der Burg W, el al: Tizanidine versus baclofen in the treatment of spasticity in multiple sclerosis patients. Acta Neurol Scand 1988; 77: 224–230.
11. Stein R, Nordal HJ, Oftedal SI, et al: The treatment of spasticity in multiple sclerosis: a double blind trial of a new antispastic drug, tizanidine, compated with baclofen. Acta Neurol Scand 1987; 75: 190– 194.
12. Galeazzi RL, Beveridge T, Nuesch t;. i’i al: Bioavailability study with DS 103 – 282 in num. Data on file, Sandoz Ltd. Basel. July 19X3.
13. Kutz K, Pirovino M. Abisch E: Bioavailability study with DS 103 – 282 in man under steady state conditions. Data on file. Sandoz Ltd. Basel. June 1986.
14. Hitzenberger H, Kutz K. Abisch E: Effect of food intake on the pharmacokinetics of DS 103 – 2X2 given once a day as an oral modified release formulation. Data on file, Sandoz Ltd. Basel. April 1986.
15. Meier J, Nuesch E. Schmidt R: Pharmacokinetic criteria for the evaluation of retard formulations. Eur J Clin Pharmacol 1974: 7: 429 – 432.
16. Irwin PM: Investigation in healthy volunteers of single dose effects of normal tablets and a delayed release formulation of tizanidine as compared to placebo. Data on file. Sando/. Ltd. Basel. January 1985.
17. Zollikofer H, Woodlti W: Safety and tolerability of single doses of Sirdalud Modified Release in healthy subjects. Data on file, Sandoz Ltd. Basel. June 1986.
18. Gonseite RE: An open trial of Sirdalud Modified Release in the treatment of spasticity caused by multiple sclerosis. Data on file. Sandoz Ltd, Basel. July 1986.
19. Pongratz D: An open trial of Sirdalud Modified Release in the treatment of spasticity due to CNS lesions. Data on file, Sandoz Ltd, Basel. August 1986.
20. VetterG: An open trial of Sirdalud Modified Release in the treatment of spasticity due to lesions in the CNS. Data on file, Sandoz Ltd, Basel. August, 1986.
21. Conrad B, Benecke R: An open trial of Sirdalud Modified Release in the treatment of spasticity due to CNS lesions. Data on file, Sandoz Ltd, Basel. June 1986.
22. Chantraine A, Van Ouwenaller C: Modified release tizanidine in the treatment of spasticity. J Int Med Res 1988; 16: 459 – 465.
23. Allan R, Lataste X, Braun P: DS 103 – 282, skeletal muscle relaxant. Clinical synopsis. Data on file, Sandoz Ltd, Basel. November 1981.
24. Berry H, Hutchinson DR: A multicentre placebo–controlled study in general practice to evaluate the efficacy and safety of tizanidine in acute low–back pain. J Int Med Res 1988; 16: 75 – 82.
25. Berry H, Hutchinson DR: Tizanidine and ibupro–fen in acute low–back pain; results of a double–blind multicentre study in general practice. J Int Med Res 1988; 16:83–91.












