–Ь–∞—В–µ—А–Є–∞–ї –Є –Љ–µ—В–Њ–і—Л
–Т –њ–µ—А–Є–Њ–і —Б –і–µ–Ї–∞–±—А—П 2007 –њ–Њ –Є—О–љ—М 2008 –≥–Њ–і–∞ –±—Л–ї–Є –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ—Л 48 –±–Њ–ї—М–љ—Л—Е. –Т—Б–µ–Љ –Є–Љ —А–∞–љ–µ–µ –љ–∞–Ј–љ–∞—З–∞–ї–Є—Б—М —В—А–Є–њ—В–∞–љ—Л (—Б—Г–Љ–∞—В—А–Є–њ—В–∞–љ – 41 —З–µ–ї., –Ј–Њ–ї–Љ–Є—В—А–Є–њ—В–∞–љ – 4 —З–µ–ї., —Н–ї–µ—В—А–Є–њ—В–∞–љ – 3 —З–µ–ї.). –Я–Њ —А–∞–Ј–ї–Є—З–љ—Л–Љ –њ—А–Є—З–Є–љ–∞–Љ –±–Њ–ї—М–љ—Л–µ —А–∞–љ–µ–µ –Њ—В–Ї–∞–Ј–∞–ї–Є—Б—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –і–∞–љ–љ—Л–є —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –Ї–ї–∞—Б—Б –≤ –Ї–∞—З–µ—Б—В–≤–µ –љ–µ–Њ—В–ї–Њ–ґ–љ–Њ–є —В–µ—А–∞–њ–Є–Є. –Т–Њ–њ—А–Њ—Б –Њ—В–Ї–∞–Ј–∞ –Њ—В —В—А–Є–њ—В–∞–љ–Њ–≤ –±—Л–ї —Б–Њ–≥–ї–∞—Б–Њ–≤–∞–љ —Б –ї–µ—З–∞—Й–Є–Љ –≤—А–∞—З–Њ–Љ (20 —З–µ–ї.), –Є–ї–Є —В–∞–Ї–Њ–µ —А–µ—И–µ–љ–Є–µ —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ –њ—А–Є–љ–Є–Љ–∞–ї–Њ—Б—М —Б–∞–Љ–Є–Љ –±–Њ–ї—М–љ—Л–Љ (28 —З–µ–ї.). –Ф–Є–∞–≥–љ–Њ–Ј —В–Є–њ–∞ –≥–Њ–ї–Њ–≤–љ–Њ–є –±–Њ–ї–Є —Г—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–ї—Б—П –њ–Њ –Ї—А–Є—В–µ—А–Є—П–Љ –Ь–µ–ґ–і—Г–љ–∞—А–Њ–і–љ–Њ–є –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є–Є –≥–Њ–ї–Њ–≤–љ—Л—Е –±–Њ–ї–µ–є 2003 –≥–Њ–і–∞ [5]. –Ъ—А–Є—В–µ—А–Є–Є –Є—Б–Ї–ї—О—З–µ–љ–Є—П: —В–µ–Ї—Г—Й–Є–µ –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є–µ –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Є —Н–љ–і–Њ–≥–µ–љ–љ—Л–µ –њ—Б–Є—Е–Є—З–µ—Б–Ї–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є—Б—М —Б–ї–µ–і—Г—О—Й–Є–µ –Љ–µ—В–Њ–і—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –Ъ–ї–Є–љ–Є–Ї–Њ––љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є – –њ–Њ–і—А–Њ–±–љ—Л–є —Б–±–Њ—А –ґ–∞–ї–Њ–± –Є –∞–љ–∞–Љ–љ–µ–Ј–∞, –Њ–±—Й–µ—Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–µ –Є –Ї–ї–Є–љ–Є–Ї–Њ––љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ —В–µ—Б—В–Є—А–Њ–≤–∞–љ–Є–µ, –≤–µ–і–µ–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є –і–љ–µ–≤–љ–Є–Ї–Њ–≤ –≥–Њ–ї–Њ–≤–љ–Њ–є –±–Њ–ї–Є. –Я—Б–Є—Е–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Њ–µ —В–µ—Б—В–Є—А–Њ–≤–∞–љ–Є–µ – –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ —В—П–ґ–µ—Б—В–Є –Љ–Є–≥—А–µ–љ–Є –њ–Њ —И–Ї–∞–ї–µ MIDAS –Є –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –њ–Њ —В–µ—Б—В—Г –°–Р–Э. –Я–Њ—Б–ї–µ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—П –і–Є–∞–≥–љ–Њ–Ј–∞ –Љ–Є–≥—А–µ–љ—М –Є —Г—В–Њ—З–љ–µ–љ–Є—П –µ–µ —В–µ—З–µ–љ–Є—П (—Н–њ–Є–Ј–Њ–і–Є—З–µ—Б–Ї–∞—П –Є–ї–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–∞—П –Љ–Є–≥—А–µ–љ—М), –Є–Ј—Г—З–∞–ї–∞—Б—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Ј–Њ–ї–Љ–Є—В—А–Є–њ—В–∞–љ–∞ (–Ч–Њ–Љ–Є–≥) –≤ –і–Њ–Ј–µ 2,5 –Љ–≥ –њ—А–Є —В—А–µ—Е –њ—А–Є—Б—В—Г–њ–∞—Е –≥–Њ–ї–Њ–≤–љ–Њ–є –±–Њ–ї–Є. –С–Њ–ї—М–љ—Л–µ –≤ –і–љ–µ–≤–љ–Є–Ї–∞—Е –≥–Њ–ї–Њ–≤–љ–Њ–є –±–Њ–ї–Є –Њ—В–Љ–µ—З–∞–ї–Є –≤—А–µ–Љ—П –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –њ—А–Є—Б—В—Г–њ–∞, –µ–≥–Њ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М, –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –Њ—Б–љ–Њ–≤–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ (–Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М, —В–Њ—И–љ–Њ—В–∞, —А–≤–Њ—В–∞, —Б–≤–µ—В–Њ––Ј–≤—Г–Ї–Њ–±–Њ—П–Ј–љ—М) –і–Њ –љ–∞—З–∞–ї–∞ –њ—А–Є–µ–Љ–∞ –Ј–Њ–ї–Љ–Є—В—А–Є–њ—В–∞–љ–∞, —З–µ—А–µ–Ј 1, 2, 4, 24 —З–∞—Б–∞ –њ–Њ—Б–ї–µ –µ–≥–Њ –њ—А–Є–µ–Љ–∞. –°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–∞—П –Њ–±—А–∞–±–Њ—В–Ї–∞ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М —Б –њ–Њ–Љ–Њ—Й—М—О –њ–∞–Ї–µ—В–∞ –њ—А–Є–Ї–ї–∞–і–љ—Л—Е –њ—А–Њ–≥—А–∞–Љ–Љ Statistica 6 —Д–Є—А–Љ—Л «Stat Soft».
–†–µ–Ј—Г–ї—М—В–∞—В—Л
–Т —А–µ–Ј—Г–ї—М—В–∞—В–µ —В—Й–∞—В–µ–ї—М–љ–Њ–≥–Њ –Ї–ї–Є–љ–Є–Ї–Њ––љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е —А–∞–љ–µ–µ –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е —В—А–Є–њ—В–∞–љ—Л, –±—Л–ї–Є —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ—Л —Б–ї–µ–і—Г—О—Й–Є–µ –і–Є–∞–≥–љ–Њ–Ј—Л: –Љ–Є–≥—А–µ–љ—М –±–µ–Ј –∞—Г—А—Л (–Ь–С–Р) – 16 —З–µ–ї., –Љ–Є–≥—А–µ–љ—М —Б –∞—Г—А–Њ–є (–Ь–Р) – 2 —З–µ–ї., —Е—А–Њ–љ–Є—З–µ—Б–Ї–∞—П –Љ–Є–≥—А–µ–љ—М (–•–Ь) – 26 —З–µ–ї. –£ 4 —З–µ–ї. —Е–∞—А–∞–Ї—В–µ—А —Ж–µ—Д–∞–ї–≥–Є–Є –љ–Њ—Б–Є–ї —В–Є–њ–Є—З–љ—Л–µ —З–µ—А—В—Л –≥–Њ–ї–Њ–≤–љ–Њ–є –±–Њ–ї–Є –љ–∞–њ—А—П–ґ–µ–љ–Є—П –±–µ–Ј —Е–∞—А–∞–Ї—В–µ—А–љ—Л—Е –Љ–Є–≥—А–µ–љ–Њ–Ј–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Ї—А–Њ–Љ–µ —Д–Њ—В–Њ—Д–Њ–±–Є–Є –љ–∞ –≤—Л—Б–Њ—В–µ –њ—А–Є—Б—В—Г–њ–∞. –†–µ—В—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Л–є –∞–љ–∞–Љ–љ–µ–Ј –њ—А–Є—Б—В—Г–њ–Њ–≤ –≥–Њ–ї–Њ–≤–љ–Њ–є –±–Њ–ї–Є, –њ–Њ –њ–Њ–≤–Њ–і—Г –Ї–Њ—В–Њ—А—Л—Е –±—Л–ї–Є –љ–∞–Ј–љ–∞—З–µ–љ—Л —В—А–Є–њ—В–∞–љ—Л, —В–∞–Ї–ґ–µ –љ–µ –≤—Л—П–≤–Є–ї –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–љ–Њ—Б—В—М —В–∞–Ї–Њ–≥–Њ –≤–Є–і–∞ –љ–µ–Њ—В–ї–Њ–ґ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Є, —Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –ї–Њ–≥–Є—З–љ–Њ –Њ–±—К—П—Б–љ—П–µ—В –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Њ–є –њ—А–Њ—В–Є–≤–Њ–Љ–Є–≥—А–µ–љ–Њ–Ј–љ–Њ–є —В–µ—А–∞–њ–Є–Є. –≠—В–Њ–є –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е –±—Л–ї —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ –і–Є–∞–≥–љ–Њ–Ј: —З–∞—Б—В–∞—П —Н–њ–Є–Ј–Њ–і–Є—З–µ—Б–Ї–∞—П –≥–Њ–ї–Њ–≤–љ–∞—П –±–Њ–ї—М –љ–∞–њ—А—П–ґ–µ–љ–Є—П, —Б–Њ—З–µ—В–∞—О—Й–∞—П—Б—П —Б –љ–∞–њ—А—П–ґ–µ–љ–Є–µ–Љ –њ–µ—А–Є–Ї—А–∞–љ–Є–∞–ї—М–љ—Л—Е –Љ—Л—И—Ж – 3 —З–µ–ї. –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–∞—П –≥–Њ–ї–Њ–≤–љ–∞—П –±–Њ–ї—М –љ–∞–њ—А—П–ґ–µ–љ–Є—П, –љ–µ —Б–Њ—З–µ—В–∞—О—Й–∞—П—Б—П —Б –љ–∞–њ—А—П–ґ–µ–љ–Є–µ–Љ –њ–µ—А–Є–Ї—А–∞–љ–Є–∞–ї—М–љ—Л—Е –Љ—Л—И—Ж – 1 —З–µ–ї., –Є –Њ–љ–Є –±—Л–ї–Є –Є—Б–Ї–ї—О—З–µ–љ—Л –Є–Ј –і–∞–ї—М–љ–µ–є—И–µ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –Р–љ–∞–ї–Є–Ј —Е–∞—А–∞–Ї—В–µ—А–∞ –њ—А–Є—Б—В—Г–њ–∞ –Є —Б–±–Њ—А –∞–љ–∞–Љ–љ–µ–Ј–∞ –њ–Њ–Ј–≤–Њ–ї–Є–ї —В–∞–Ї–ґ–µ —Г—В–Њ—З–љ–Є—В—М –њ—А–Є—З–Є–љ—Г –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Њ–і–љ–Њ–≥–Њ –Є–Ј —В—А–Є–њ—В–∞–љ–Њ–≤ —Г 2 —З–µ–ї., —Б—В—А–∞–і–∞—О—Й–Є—Е –Ь–С–Р. –Т—Л—П—Б–љ–µ–љ–Њ, —З—В–Њ –љ–∞–Ї–∞–љ—Г–љ–µ –њ—А–Є—Б—В—Г–њ–∞ –У–С —Н—В–Є –±–Њ–ї—М–љ—Л–µ —Г–њ–Њ—В—А–µ–±–ї—П–ї–Є –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –љ–µ–±–Њ–ї—М—И—Г—О –і–Њ–Ј—Г –ї–µ–≥–Ї–Њ–≥–Њ –∞–ї–Ї–Њ–≥–Њ–ї—М–љ–Њ–≥–Њ –љ–∞–њ–Є—В–Ї–∞. –Э–Њ—З—М—О —А–∞–Ј–≤–Є–ї—Б—П –њ—А–Є—Б—В—Г–њ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–є –њ—Г–ї—М—Б–Є—А—Г—О—Й–µ–є –і–≤—Г—Е—Б—В–Њ—А–Њ–љ–љ–µ–є –У–С, –Ї–Њ—В–Њ—А—Л–є –љ–µ –±—Л–ї –Ї—Г–њ–Є—А–Њ–≤–∞–љ —Н–љ—В–µ—А–∞–ї—М–љ—Л–Љ –њ—А–Є–µ–Љ–Њ–Љ —В—А–Є–њ—В–∞–љ–∞. –Т —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є–Љ–Є –Ї—А–Є—В–µ—А–Є—П–Љ–Є –Ь–Ъ–У–С 2003 –≥. [5] –і–∞–љ–љ—Л–µ –њ—А–Є—Б—В—Г–њ—Л –±—Л–ї–Є —А–∞—Б—Ж–µ–љ–µ–љ—Л –Ї–∞–Ї –Њ—В—Б—А–Њ—З–µ–љ–љ–∞—П –≥–Њ–ї–Њ–≤–љ–∞—П –±–Њ–ї—М, –≤—Л–Ј–≤–∞–љ–љ–∞—П –∞–ї–Ї–Њ–≥–Њ–ї–µ–Љ. –Ф–≤–Њ–µ –±–Њ–ї—М–љ—Л—Е, —Б—В—А–∞–і–∞—О—Й–Є—Е –Ь–С–Р, –≤ —В–µ—З–µ–љ–Є–µ –њ–Њ—Б–ї–µ–і–љ–Є—Е —В—А–µ—Е –Љ–µ—Б—П—Ж–µ–≤ —Б—В—А–∞–і–∞–ї–Є –њ—А–Є—Б—В—Г–њ–∞–Љ–Є —Б —З–∞—Б—В–Њ—В–Њ–є 1 —А–∞–Ј –≤ –Љ–µ—Б—П—Ж, —Б—В–µ–њ–µ–љ—М —В—П–ґ–µ—Б—В–Є –њ–Њ —И–Ї–∞–ї–µ MIDAS —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Њ–≤–∞–ї–Њ 1 —Б—В–µ–њ–µ–љ–Є (5 –±–∞–ї–ї–Њ–≤). –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –њ—А–Є—Б—В—Г–њ—Л –Ї—Г–њ–Є—А–Њ–≤–∞–ї–Є—Б—М –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –Э–Я–Т–Я. –Ґ–Њ –µ—Б—В—М, –Є–Ј–љ–∞—З–∞–ї—М–љ–Њ, –љ–µ –±—Л–ї–Њ –њ—А–µ–і–њ–Њ—Б—Л–ї–Њ–Ї –і–ї—П –љ–∞–Ј–љ–∞—З–µ–љ–Є—П —В—А–Є–њ—В–∞–љ–Њ–≤. –≠—В–Є –±–Њ–ї—М–љ—Л–µ —В–∞–Ї–ґ–µ –±—Л–ї–Є –Є—Б–Ї–ї—О—З–µ–љ—Л –Є–Ј –і–∞–ї—М–љ–µ–є—И–µ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П.
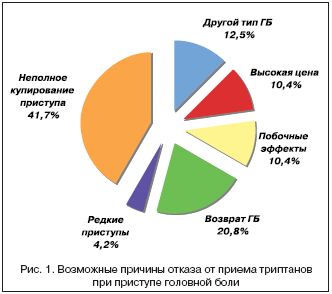
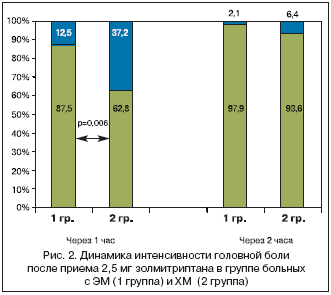
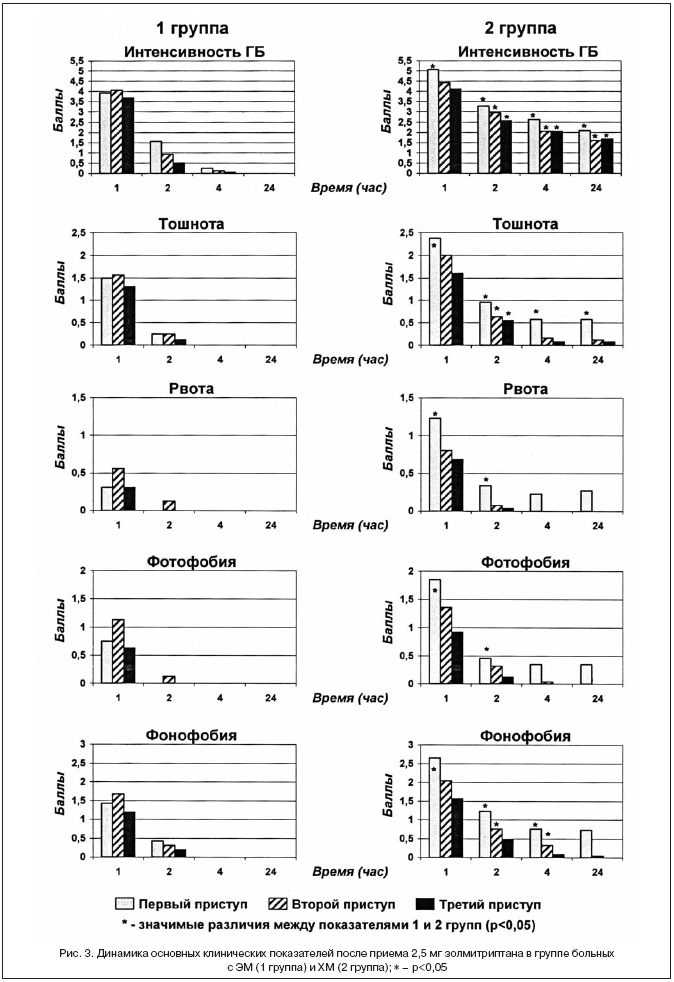
–°—А–µ–і–Є –і—А—Г–≥–Є—Е –Њ—Б–љ–Њ–≤–љ—Л—Е –њ—А–Є—З–Є–љ –Њ—В–Ї–∞–Ј–∞ –Њ—В –њ—А–Є–µ–Љ–∞ —В—А–Є–њ—В–∞–љ–Њ–≤ —Г –±–Њ–ї—М–љ—Л—Е —Б —Н–њ–Є–Ј–Њ–і–Є—З–µ—Б–Ї–Є–Љ–Є —Д–Њ—А–Љ–∞–Љ–Є –Љ–Є–≥—А–µ–љ–Є (–Ь–С–Р, –Ь–Р) –Є –•–Ь –±—Л–ї–Є –љ–∞–Ј–≤–∞–љ—Л —Б–ї–µ–і—Г—О—Й–Є–µ –≤–∞—А–Є–∞–љ—В—Л (—А–Є—Б. 1): –њ—А–Є—Б—В—Г–њ—Л –љ–µ –њ–Њ–ї–љ–Њ—Б—В—М—О –Ї—Г–њ–Є—А—Г—О—В—Б—П (41,7%), –≤–Њ–Ј–≤—А–∞—В –У–С (20,8%), –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л (10,4%), –≤—Л—Б–Њ–Ї–∞—П —Ж–µ–љ–∞ (10,4%), —А–µ–і–Ї–Є–µ –њ—А–Є—Б—В—Г–њ—Л (4,2%). –Ф–ї—П –±–Њ–ї–µ–µ –і–µ—В–∞–ї—М–љ–Њ–≥–Њ –∞–љ–∞–Љ–љ–µ–Ј–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —В—А–Є–њ—В–∞–љ–Њ–≤ —Г 42 —З–µ–ї., —Б—В—А–∞–і–∞—О—Й–Є—Е –Љ–Є–≥—А–µ–љ—М—О –Є–Ј—Г—З–∞–ї–∞—Б—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Ј–Њ–ї–Љ–Є—В—А–Є–њ—В–∞–љ–∞ 2,5 –Љ–≥ –≤ —В—А–µ—Е –њ—А–Є—Б—В—Г–њ–∞—Е. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –±—Л–ї–Њ –њ—А–Њ–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–Њ 126 –њ—А–Є—Б—В—Г–њ–Њ–≤ –њ–Њ –Њ—Б–љ–Њ–≤–љ—Л–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ –њ—А–Њ—П–≤–ї–µ–љ–Є—П–Љ: –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М –У–С (–Т–Р–® –Њ—В 0 –і–Њ 10 –±–∞–ї–ї–Њ–≤), —В–Њ—И–љ–Њ—В–∞, —А–≤–Њ—В–∞, —Д–Њ—В–Њ–—Д–Њ–љ–Њ—Д–Њ–±–Є—П (–Њ—В 0 –і–Њ 5 –±–∞–ї–ї–Њ–≤). –Я–Њ –і–љ–µ–≤–љ–Є–Ї–∞–Љ, –Є–Ј—Г—З–∞–ї–∞—Б—М –У–С –Є –µ–µ –Њ—Б–љ–Њ–≤–љ—Л–µ —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є–µ —Б–Є–Љ–њ—В–Њ–Љ—Л —З–µ—А–µ–Ј —Б–ї–µ–і—Г—О—Й–Є–µ –≤—А–µ–Љ–µ–љ–љ—Л–µ –Є–љ—В–µ—А–≤–∞–ї—Л: 1, 2, 4, 24 —З–∞—Б–∞. –Т –Ї–∞—З–µ—Б—В–≤–µ –Њ—Б–љ–Њ–≤–љ–Њ–≥–Њ –Ї—А–Є—В–µ—А–Є—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї—Б—П –Њ—В–≤–µ—В –≤ –≤–Є–і–µ —Г–Љ–µ–љ—М—И–µ–љ–Є—П –У–С —З–µ—А–µ–Ј 2 —З–∞—Б–∞ –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ 2,5 –Љ–≥ –Ј–Њ–ї–Љ–Є—В—А–Є–њ—В–∞–љ–∞ –Њ—В –Њ—З–µ–љ—М —Б–Є–ї—М–љ–Њ–є –Є —Б–Є–ї—М–љ–Њ–є –±–Њ–ї–Є –і–Њ —Б—А–µ–і–љ–µ–є –Є–ї–Є –µ–µ –њ–Њ–ї–љ–Њ–≥–Њ –Њ—В—Б—Г—В—Б—В–≤–Є—П. –Т—Б–µ–Љ –±–Њ–ї—М–љ—Л–Љ –±—Л–ї —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ –њ—А–Є–µ–Љ –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–≥–Њ —В—А–Є–њ—В–∞–љ–∞ –≤ –љ–∞—З–∞–ї–µ –њ—А–Є—Б—В—Г–њ–∞ –У–С –њ—А–Є –њ–Њ—П–≤–ї–µ–љ–Є–Є —Е–∞—А–∞–Ї—В–µ—А–љ–Њ–є –њ—Г–ї—М—Б–∞—Ж–Є–Є –Њ–і–љ–Њ—Б—В–Њ—А–Њ–љ–љ–µ–є (85%) –Є–ї–Є –і–≤—Г—Е—Б—В–Њ—А–Њ–љ–љ–µ–є –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є (15%). –Я–Њ–ї—Г—З–µ–љ–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л —Б—А–∞–≤–љ–Є–≤–∞–ї–Є—Б—М –≤ –і–≤—Г—Е –≥—А—Г–њ–њ–∞—Е –±–Њ–ї—М–љ—Л—Е (—Н–њ–Є–Ј–Њ–і–Є—З–µ—Б–Ї–Є–µ —Д–Њ—А–Љ—Л –Љ–Є–≥—А–µ–љ–Є (–Ь–С–Р –Є –Ь–Р) – 16 —З–µ–ї. –Є –•–Ь – 26 —З–µ–ї. –Т—Б–µ –±–Њ–ї—М–љ—Л–µ –њ—А–Њ—Е–Њ–і–Є–ї–Є –њ—Б–Є—Е–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Њ–µ —В–µ—Б—В–Є—А–Њ–≤–∞–љ–Є–µ –њ–Њ —И–Ї–∞–ї–µ MIDAS –і–ї—П –Њ—Ж–µ–љ–Ї–Є —Б—В–µ–њ–µ–љ–Є –Љ–Є–≥—А–µ–љ–Є –Є —И–Ї–∞–ї–µ –°–Р–Э –і–Њ –Є –њ–Њ—Б–ї–µ –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –і–ї—П –Њ—Ж–µ–љ–Ї–Є –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є. –°—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В –±–Њ–ї—М–љ—Л—Е –≤ –≥—А—Г–њ–њ–µ –≠–Ь —Б–Њ—Б—В–∞–≤–Є–ї 38,5±6,7 –ї–µ—В, —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є–µ –ґ/–Љ 3:1, –≤–Њ–Ј—А–∞—Б—В –і–µ–±—О—В–∞ 21,0±3,7 –≥–Њ–і–∞., —Б—В–µ–њ–µ–љ—М —В—П–ґ–µ—Б—В–Є –Љ–Є–≥—А–µ–љ–Є –њ–Њ —И–Ї–∞–ї–µ MIDAS – 10,9±1,8 –±–∞–ї–ї–∞. –Т –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е –•–Ь —Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В —Б–Њ—Б—В–∞–≤–Є–ї 43,85±4,2 –≥–Њ–і–∞, —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є–µ –ґ/–Љ 4:1, –≤–Њ–Ј—А–∞—Б—В –і–µ–±—О—В–∞ 19,0±4,1 –≥–Њ–і–∞, –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П 3,6±0,8 –≥–Њ–і–∞, —Б—В–µ–њ–µ–љ—М —В—П–ґ–µ—Б—В–Є –Љ–Є–≥—А–µ–љ–Є –њ–Њ —И–Ї–∞–ї–µ MIDAS – 19,7±4,4 –±–∞–ї–ї–∞. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Є–µ–Љ–∞ 2,5 –Љ–≥ –Ј–Њ–ї–Љ–Є—В—А–Є–њ—В–∞–љ–∞ —З–µ—А–µ–Ј 1 –Є 2 —З–∞—Б–∞ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –љ–∞ —А–Є—Б—Г–љ–Ї–µ 2. –Ш–Ј –љ–µ–≥–Њ –≤–Є–і–љ–Њ, —З—В–Њ –њ–Њ–ї–љ–Њ–µ –Њ—В—Б—Г—В—Б—В–≤–Є–µ –У–С –Є–ї–Є —Б–љ–Є–ґ–µ–љ–Є–µ –µ–µ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є –±–Њ–ї–µ–µ —З–µ–Љ –≤–њ–Њ–ї–Њ–≤–Є–љ—Г –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —Г 87,5% –±–Њ–ї—М–љ—Л—Е —Б –≠–Ь –Є 62,8% –±–Њ–ї—М–љ—Л—Е —Б –•–Ь (p=0,006). –Я—А–Є —Н—В–Њ–Љ –њ–Њ–ї–љ–Њ–µ –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є–µ –њ—А–Є—Б—В—Г–њ–∞ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Г 72% –±–Њ–ї—М–љ—Л—Е —Б –≠–Ь –Є 48,5% –±–Њ–ї—М–љ—Л—Е —Б –•–Ь. –І–µ—А–µ–Ј 2 —З–∞—Б–∞ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є —А–µ–Ј—Г–ї—М—В–∞—В –ї–µ—З–µ–љ–Є—П –≤–Њ–Ј—А–Њ—Б –≤ –њ–µ—А–≤–Њ–є –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е –і–Њ 97,9% –Є –≤–Њ –≤—В–Њ—А–Њ–є –≥—А—Г–њ–њ–µ –і–Њ 93,6% (—Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –≤ –≥—А—Г–њ–њ–∞—Е –љ–µ –њ–Њ–ї—Г—З–µ–љ–Њ). –Я—А–Є —Н—В–Њ–Љ –њ—А–Њ—Ж–µ–љ—В –±–Њ–ї—М–љ—Л—Е —Б –њ–Њ–ї–љ—Л–Љ –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є–µ–Љ –њ—А–Є—Б—В—Г–њ–∞ –≤ –≥—А—Г–њ–њ–µ –≠–Ь —Б–Њ—Б—В–∞–≤–Є–ї 82%, –∞ –≤ –≥—А—Г–њ–њ–µ –•–Ь – 76,5%. –Ф–Є–љ–∞–Љ–Є–Ї–∞ –Њ—Б–љ–Њ–≤–љ—Л—Е —А–µ–≥–Є—Б—В—А–Є—А—Г–µ–Љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –≤ –Њ–±–µ–Є—Е –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л—Е –≥—А—Г–њ–њ–∞—Е –њ—А–Є–≤–µ–і–µ–љ–∞ –љ–∞ —А–Є—Б—Г–љ–Ї–µ 3. –Ш–Ј –љ–µ–≥–Њ –≤–Є–і–љ–Њ, —З—В–Њ –≤ –≥—А—Г–њ–њ–µ –≠–Ь –Ј–∞ —А–µ–≥–Є—Б—В—А–Є—А—Г–µ–Љ—Л–µ –Є–љ—В–µ—А–≤–∞–ї—Л –≤—А–µ–Љ–µ–љ–Є –њ—А–Њ–Є–Ј–Њ—И–µ–ї –њ–Њ–ї–љ—Л–є —А–µ–≥—А–µ—Б—Б –У–С, –Є —В–∞–Ї–ґ–µ –љ–µ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М –≤–Њ–Ј–≤—А–∞—В–∞ –У–С. –Т –≥—А—Г–њ–њ–µ –•–Ь —В–∞–Ї–ґ–µ –њ—А–Њ–Є–Ј–Њ—И–µ–ї —А–µ–≥—А–µ—Б—Б –њ—А–Є—Б—В—Г–њ–Њ–Њ–±—А–∞–Ј–љ–Њ–є –У–С –Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є –±–Њ–ї–Є —Б–љ–Є–Ј–Є–ї–Є—Б—М –і–Њ —Д–Њ–љ–Њ–≤–Њ–≥–Њ —Г—А–Њ–≤–љ—П. –£ 2 –±–Њ–ї—М–љ—Л—Е –≤ –і–∞–љ–љ–Њ–є –≥—А—Г–њ–њ–µ –≤ –Њ–і–љ–Њ–Љ –Є–Ј –њ—А–Є—Б—В—Г–њ–Њ–≤ –Њ—В–Љ–µ—З–∞–ї—Б—П –≤–Њ–Ј–≤—А–∞—В –У–С —Б–њ—Г—Б—В—П 4 —З–∞—Б–∞, —З—В–Њ –њ–Њ—В—А–µ–±–Њ–≤–∞–ї–Њ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ 2,5 –Љ–≥ –Ј–Њ–ї–Љ–Є—В—А–Є–њ—В–∞–љ–∞ –і–ї—П –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П –њ—А–Є—Б—В—Г–њ–∞. –Т –Њ–±–µ–Є—Е –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л—Е –≥—А—Г–њ–њ–∞—Е –Њ—В–Љ–µ—З–∞–ї—Б—П —А–µ–≥—А–µ—Б—Б —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤, –љ–Њ —В–µ–Љ–њ—Л –Є—Е –±—Л–ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –≤—Л—И–µ —Г –±–Њ–ї—М–љ—Л—Е —Б –≠–Ь (p<0,05). –Я–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ј–Њ–ї–Љ–Є—В—А–Є–њ—В–∞–љ–∞ —А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–ї–Є—Б—М –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –±–Њ–ї—М–љ—Л—Е. –Т—Б–µ–≥–Њ –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –љ–∞–±–ї—О–і–∞–ї–Є—Б—М —Г 28% –±–Њ–ї—М–љ—Л—Е, –±—Л–ї–Є –Ї—А–∞—В–Ї–Њ–≤—А–µ–Љ–µ–љ–љ—Л–Љ–Є –Є –љ–µ —В—А–µ–±–Њ–≤–∞–ї–Є –Ї–∞–Ї–Њ–є–—В–Њ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є. –Э–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М –≥–Њ–ї–Њ–≤–Њ–Ї—А—Г–ґ–µ–љ–Є–µ 22%, —В–Њ—И–љ–Њ—В–∞ – 21%, —Б—Г—Е–Њ—Б—В—М –≤–Њ —А—В—Г – 11%, —В–Њ—И–љ–Њ—В–∞ – 10%, —З—Г–≤—Б—В–≤–Њ «–њ—А–Є–ї–Є–≤–∞ –Ї –ї–Є—Ж—Г» – 8%, —Б–Њ–љ–ї–Є–≤–Њ—Б—В—М – 6%. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –њ—А–Є—Б—В—Г–њ–Њ–≤ –Љ–Є–≥—А–µ–љ–Њ–Ј–љ–Њ–є —Ж–µ—Д–∞–ї–≥–Є–Є —Г–ї—Г—З—И–Є–ї–Є—Б—М –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –њ–Њ —В–µ—Б—В—Г –°–Р–Э –≤ –Њ–±–µ–Є—Е –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л—Е –≥—А—Г–њ–њ–∞—Е. –Ґ–∞–Ї –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М —Б–∞–Љ–Њ—З—Г–≤—Б—В–≤–Є—П –њ—А–Є –≠–Ь –≤–Њ–Ј—А–Њ—Б —Б 3,6±0,6 –±–∞–ї–ї–∞ –і–Њ 4,3±0,5 –±–∞–ї–ї–∞ (p<0,05), –≤ –≥—А—Г–њ–њ–µ –•–Ь —Б 2,5±1,1 –±–∞–ї–ї–∞ –і–Њ 3,2 –±–∞–ї–ї–∞, –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Г–≤–µ–ї–Є—З–Є–ї—Б—П –≤ –≥—А—Г–њ–њ–µ –≠–Ь —Б 4,0±0,5 –і–Њ 4,8 –±–∞–ї–ї–∞ (p<0,05), –≤ –≤—В–Њ—А–Њ–є –≥—А—Г–њ–њ–µ —Б 3,0±0,9 –і–Њ 4,2 –±–∞–ї–ї–∞ (p<0,05). –Э–∞–Ї–Њ–љ–µ—Ж –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –љ–∞—Б—В—А–Њ–µ–љ–Є—П —Г–≤–µ–ї–Є—З–Є–ї—Б—П –≤ –њ–µ—А–≤–Њ–є –≥—А—Г–њ–њ–µ —Б 4,7±0,4 –±–∞–ї–ї–∞ –і–Њ 4,8±0,1 –±–∞–ї–ї–∞ –Є –≤ –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е —Б –•–Ь – —Б 3,6±0,8 –і–Њ 4,1±0,9 –±–∞–ї–ї–∞. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –љ–∞–Љ–Є –Њ—В–Љ–µ—З–µ–љ –≤—Л—Б–Њ–Ї–Є–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ј–Њ–ї–Љ–Є—В—А–Є–њ—В–∞–љ–∞ (–Ч–Њ–Љ–Є–≥) –≤ –і–Њ–Ј–Є—А–Њ–≤–Ї–µ 2,5 –Љ–≥ –≤ –Њ–±–µ–Є—Е —Б—А–∞–≤–љ–Є–≤–∞–µ–Љ—Л—Е –≥—А—Г–њ–њ–∞—Е –њ—А–Є –Њ–±—Й–µ–є —Е–Њ—А–Њ—И–µ–є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –Є –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л—Е –Ї—А–∞—В–Ї–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–∞—Е.
–Ю–±—Б—Г–ґ–і–µ–љ–Є–µ
–Я—А–Њ–≤–µ–і–µ–љ–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ —Г—Б—В–∞–љ–Њ–≤–Є—В—М —Ж–µ–ї—Л–є —А—П–і –≤–Њ–Ј–Љ–Њ–ґ–љ—Л—Е –њ—А–Є—З–Є–љ –љ–µ—Г–і–∞—З –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —В—А–Є–њ—В–∞–љ–Њ–≤ –≤ –∞–±–Њ—А—В–Є–≤–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є –Љ–Є–≥—А–µ–љ–Є. –Т 2003 –≥–Њ–і—Г –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–≥–Њ –Љ–∞—Б—И—В–∞–±–љ–Њ–≥–Њ –Ї–ї–Є–љ–Є–Ї–Њ–—Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П [4] –±—Л–ї–∞ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–∞ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –≤ –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ–Њ–є –њ–Њ–њ—Г–ї—П—Ж–Є–Є –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –і–ї—П –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П –Љ–Є–≥—А–µ–љ–Њ–Ј–љ–Њ–≥–Њ –њ—А–Є—Б—В—Г–њ–∞ –Є, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, —В—А–Є–њ—В–∞–љ–Њ–≤. –Ч–∞ –њ—А–Њ—И–µ–і—И–Є–µ –≥–Њ–і—Л —Б–Ї–ї–∞–і—Л–≤–∞–µ—В—Б—П –≤–њ–µ—З–∞—В–ї–µ–љ–Є–µ –Њ –±–Њ–ї–µ–µ —З–∞—Б—В–Њ–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є —Н—В–Њ–є —Б–∞–Љ–Њ–є —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є –≥—А—Г–њ–њ—Л —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є, —З—В–Њ –Љ–Њ–ґ–µ—В –±—Л—В—М —Б–≤—П–Ј–∞–љ–Њ —Б —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є–Љ —А–Њ—Б—В–Њ–Љ –≤ —Ж–µ–ї–Њ–Љ –≤ —Б—В—А–∞–љ–µ, —Г—Б–Є–ї–Є—П–Љ–Є –†–Њ—Б—Б–Є–є—Б–Ї–Њ–≥–Њ –Ю–±—Й–µ—Б—В–≤–∞ –≥–Њ–ї–Њ–≤–љ—Л—Е –±–Њ–ї–µ–є –Є —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Ї–Њ–Љ–њ–∞–љ–Є–є –њ–Њ –Є–љ—Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—О –≤—А–∞—З–µ–є –Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –њ–Њ–і—Е–Њ–і–∞—Е –Ї –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –Є –ї–µ—З–µ–љ–Є—О –У–С. –Ю–і–љ–∞–Ї–Њ, –Ї—А–Њ–Љ–µ –Ј–љ–∞–љ–Є—П –Њ —Б—Г—Й–µ—Б—В–≤–Њ–≤–∞–љ–Є–Є –і–∞–љ–љ–Њ–≥–Њ –Ї–ї–∞—Б—Б–∞ –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Є—Е –њ—А–∞–≤–Є–ї—М–љ–Њ –љ–∞–Ј–љ–∞—З–∞—В—М –Є –Ї–Њ–љ—В—А–Њ–ї–Є—А–Њ–≤–∞—В—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М. –Я—А–Њ–≤–µ–і–µ–љ–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ –Ї—А–Њ–Љ–µ –Њ—И–Є–±–Њ–Ї –≤ –њ–Њ—Б—В–∞–љ–Њ–≤–Ї–µ —Б–∞–Љ–Њ–≥–Њ –і–Є–∞–≥–љ–Њ–Ј–∞ –Љ–Є–≥—А–µ–љ–Є, –Ї—А–∞–є–љ–µ –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –њ—А–Њ—Б—В–∞—П –Є –Є–љ—Д–Њ—А–Љ–∞—В–Є–≤–љ–∞—П —И–Ї–∞–ї–∞ MIDAS –і–ї—П –Њ—Ж–µ–љ–Ї–Є —В—П–ґ–µ—Б—В–Є –Љ–Є–≥—А–µ–љ–Є (5%). –Я—А–µ–і–њ–Њ—З—В–µ–љ–Є—П –њ—А–∞–Ї—В–Є–Ї—Г—О—Й–Є—Е –≤—А–∞—З–µ–є –≤ –њ—А–Є–љ—Ж–Є–њ–µ –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П –Љ–Є–≥—А–µ–љ–Є –Њ—В–і–∞–µ—В—Б—П –љ–µ —Б—В—А–∞—В–Є—Д–Є–Ї–∞—Ж–Є–Њ–≤–∞–љ–љ–Њ–Љ—Г, –∞ —Б—В—Г–њ–µ–љ—З–∞—В–Њ–Љ—Г –њ–Њ–і—Е–Њ–і—Г –љ–µ–Њ—В–ї–Њ–ґ–љ–Њ–є —В–µ—А–∞–њ–Є–Є (90%). –Ф–∞–љ–љ—Л–є –њ–Њ–і—Е–Њ–і –≤–Њ –Љ–љ–Њ–≥–Њ–Љ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є–µ –Ј–∞—В—А–∞—В—Л –Њ—В –ї–µ—З–µ–љ–Є—П, —З–∞—Й–µ –њ—А–Є–≤–Њ–і–Є—В—М –Ї —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—О –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ –Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ—Л—Е –≥–Њ–ї–Њ–≤–љ—Л—Е –±–Њ–ї–µ–є [1,16,20]. –С–Њ–ї—М–љ—Л–Љ, —Б—В—А–∞–і–∞—О—Й–Є–Љ –Љ–Є–≥—А–µ–љ—М—О, —А–µ–і–Ї–Њ –њ—А–Њ–≤–Њ–і–Є—В—Б—П —А–∞–Ј—К—П—Б–љ–Є—В–µ–ї—М–љ–∞—П —А–∞–±–Њ—В–∞ –Њ –≤—А–µ–Љ–µ–љ–Є –њ—А–Є–µ–Љ–∞ —В—А–Є–њ—В–∞–љ–Њ–≤. –Ґ–∞–Ї 88% —Г—З–∞—Б—В–≤–Њ–≤–∞–≤—И–Є—Е –≤ –љ–∞—И–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –±–Њ–ї—М–љ—Л—Е, —А–∞–љ–µ–µ –њ—А–Є–љ–Є–Љ–∞–ї–Є —В—А–Є–њ—В–∞–љ—Л —Г–ґ–µ –≤ —А–∞–Ј–≤–µ—А–љ—Г—В—Г—О —Б—В–∞–і–Є—О –њ—А–Є—Б—В—Г–њ–∞. –Ґ–Њ –µ—Б—В—М –њ–Њ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–Љ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є—П–Љ –Њ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–µ –Љ–Є–≥—А–µ–љ–Є, —Б —Г—З–µ—В–Њ–Љ —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є —Б–µ–љ—Б–Є—В–Є–Ј–∞—Ж–Є–Є —П–≤–ї—П–µ—В—Б—П –Љ–µ—В–Њ–і–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –Њ—И–Є–±–Ї–Њ–є [1,9,12]. –Ґ–∞–Ї–ґ–µ –њ—А–µ–і–≤–∞—А–Є—В–µ–ї—М–љ–Њ —Б –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –љ–µ –Њ–±—Б—Г–ґ–і–∞—О—В—Б—П –≤–µ—А–Њ—П—В–љ—Л–µ –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —В—А–Є–њ—В–∞–љ–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –≤ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є «–њ—Г–≥–∞—О—В» –±–Њ–ї—М–љ—Л—Е, —З–µ–Љ —А–µ–∞–ї—М–љ–Њ —Б–љ–Є–ґ–∞—О—В —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —В–µ—А–∞–њ–Є–Є. –°–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –њ–∞—А–∞–ї–ї–µ–ї—М–љ–Њ —Б –љ–∞–Ї–Њ–њ–ї–µ–љ–Є–µ–Љ –љ–∞—Г—З–љ—Л—Е –Ј–љ–∞–љ–Є–є –Њ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–µ –Љ–Є–≥—А–µ–љ–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Б–Њ–≤–µ—А—И–µ–љ—Б—В–≤–Њ–≤–∞—В—М –Љ–µ—В–Њ–і–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –њ–Њ–і—Е–Њ–і—Л –≤ —В–∞–Ї—В–Є–Ї–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –њ—А–Њ—В–Є–≤–Њ–Љ–Є–≥—А–µ–љ–Њ–Ј–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤.
–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –Р–Љ–µ–ї–Є–љ –Р. –Т., –Ш–≥–љ–∞—В–Њ–≤ –Ѓ.–Ф., –°–Ї–Њ—А–Њ–Љ–µ—Ж –Р.–Р. –Ь–Є–≥—А–µ–љ—М (–њ–∞—В–Њ–≥–µ–љ–µ–Ј, –Ї–ї–Є–љ–Є–Ї–∞, –ї–µ—З–µ–љ–Є–µ). // –°–∞–љ–Ї—В––Я–µ—В–µ—А–±—Г—А–≥—Б–Ї–Њ–µ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–µ –Є–Ј–і–∞—В–µ–ї—М—Б—В–≤–Њ 2001.
2. –У–∞–љ–ґ—Г–ї–∞ –Я.–Р., –®–Є–љ–Ї–∞—А–µ–≤ –°.–Т. –°–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є—П –Њ –Љ–Є–≥—А–µ–љ–Є –Є –ї–µ—З–µ–љ–Є–Є –Љ–Є–≥—А–µ–љ–Њ–Ј–љ–Њ–≥–Њ –њ—А–Є—Б—В—Г–њ–∞. –§–∞—А–Љ–∞—В–µ–Ї–∞. 17 – 2005. – –°. 35–39.
3. –Ъ—Г—Ж–µ–Љ–µ–ї–Њ–≤ –Ш.–С. –Ъ–ї–Є–љ–Є–Ї–Њ–—Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј –њ–µ—А–≤–Є—З–љ—Л—Е –≥–Њ–ї–Њ–≤–љ—Л—Е –±–Њ–ї–µ–є –≤–Ј—А–Њ—Б–ї–Њ–≥–Њ –≥–Њ—А–Њ–і—Б–Ї–Њ–≥–Њ –љ–∞—Б–µ–ї–µ–љ–Є—П: –Р–≤—В–Њ—А–µ—Д. –і–Є—Б. … –Ї–∞–љ–і. –Љ–µ–і. –љ–∞—Г–Ї. –Ь 2005.
4. –Ъ—Г—Ж–µ–Љ–µ–ї–Њ–≤ –Ш. –С., –Ґ–∞–±–µ–µ–≤–∞ –У. –†. –≠–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—П –њ–µ—А–≤–Є—З–љ–Њ–є –≥–Њ–ї–Њ–≤–љ–Њ–є –±–Њ–ї–Є (–њ–Њ –і–∞–љ–љ—Л–Љ –њ–Њ–њ—Г–ї—П—Ж–Є–Њ–љ–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤–Ј—А–Њ—Б–ї–Њ–≥–Њ –љ–∞—Б–µ–ї–µ–љ–Є—П –≥. –†–Њ—Б—В–Њ–≤–∞––љ–∞––Ф–Њ–љ—Г). –Ц—Г—А–љ–∞–ї «–С–Њ–ї—М» – 2004. – 4(5). – –°.25–31.
5. –Ь–µ–ґ–і—Г–љ–∞—А–Њ–і–љ–∞—П –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є—П –≥–Њ–ї–Њ–≤–љ–Њ–є –±–Њ–ї–Є, 2––µ –Є–Ј–і. –Ь–µ–ґ–і—Г–љ–∞—А–Њ–і–љ–Њ–µ –Њ–±—Й–µ—Б—В–≤–Њ –≥–Њ–ї–Њ–≤–љ–Њ–є –±–Њ–ї–Є, 2003. –Я–µ—А. –Т.–Т. –Ю—Б–Є–њ–Њ–≤–Њ–є, –Ґ.–У. –Т–Њ–Ј–љ–µ—Б–µ–љ—Б–Ї–Њ–є. –У–µ–і–µ–Њ–љ –†–Є—Е—В–µ—А 2003.
6. –Ю—Б–Є–њ–Њ–≤–∞ –Т.–Т. –Ь–Є–≥—А–µ–љ—М: –Ї–ї–Є–љ–Є–Ї–Њ––њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј, –Ї–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є, –Ї–Њ–Љ–Њ—А–±–Є–і–љ–Њ—Б—В—М, —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–µ –њ–Њ–і—Е–Њ–і—Л. –Ф–Є—Б—Б….–і–Њ–Ї—В. –Љ–µ–і. –љ–∞—Г–Ї. –Ь. - 2003.
7. –Я—А–µ—Б—Б–—А–µ–ї–Є–Ј. - World Headache Alliance, 2004; —Б. 1–4.
8. –†–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞, —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б –≥–Њ–ї–Њ–≤–љ–Њ–є –±–Њ–ї—М—О, –Є –Њ–±—Й–µ—Б—В–≤–µ–љ–љ–Њ–µ –Ј–і—А–∞–≤–Њ–Њ—Е—А–∞–љ–µ–љ–Є–µ. - WHO/MSD/009, 2004; —Б. 1–10.
9. –Ґ–∞–±–µ–µ–≤–∞ –У.–†., –Р–Ј–Є–Љ–Њ–≤–∞ –Ѓ.–≠. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —Б—Г–Љ–∞–Љ–Є–≥—А–µ–љ–∞ –њ—А–Є –µ–≥–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –≤ —А–∞–љ–љ–µ–Љ –Є –њ–Њ–Ј–і–љ–µ–Љ –њ–µ—А–Є–Њ–і–∞—Е —А–∞–Ј–≤–Є—В–Є—П –Љ–Є–≥—А–µ–љ–Њ–Ј–љ–Њ–≥–Њ –њ—А–Є—Б—В—Г–њ–∞. –Ц—Г—А–љ–∞–ї –Э–µ–≤—А–Њ–ї–Њ–≥–Є–Є –Є –њ—Б–Є—Е–Є–∞—В—А–Є–Є, 8 – 2007. – –°.29–33.
10. Cheung R.T. Prevalence of migraine, tension–type headache, and other headaches in Hong Kong. // Headache. 2000 Jun; 40(60): 473–9.
11. Da–Costa M.Z, Soares C.B., Heinisch L.M., Heinisch R.H. Frequency of headache in the medical students of Santa Catarina‘s Federal University. // Headache. 2000 Oct; 40 (9): 740–4.
12. Ferrari M.D. Should we advise patients to treat migraine attacks early: methodologic issues. Eur Neurol 2005; 53: Suppl 1: 17–21.
13. Gobel H., Buschmann P., Heinze A., Heinze–Kuhn K. Epidemiologie und sozioekonomische Konsequenzen von Migraine und Kopfschmerzerkrankungen. // Versicherungsmedizin.2000 Mar 1; 52(1): 19–23.
14. Linde M., Mellberg A., Dahlof C. The natural course of migraine attacks. A prospective analysis of untreated attacks compared with attacks treated with atriptan. Cephalalgia 2006; 26: 712–721.
15. Lipton R.B, Hamelsky SW, Kolodner KB, Steiner TJ, Stewart WF. Migraine, quality of life, and depression: a population–based case–control study. Neurology. 2000 Sep 12; 55(5):629–35.
16. Mathew N.T. Transformed migraine, analgetic rebound, and other chronic daily headaches. Neurol Clin, 1997; 15(1): 167–186.
17. Rasmussen B. K. Epidemiology and socio–economic impact of headache. Cephalalgia 1999; 19 Suppl 25: 20–23.
18. Sakai F., Igarashi H. Prevalence of migraine in Japan: a nationwide survey. // Cephalalgia 1997; 17:15–22.
19. Scher A.I, Stewart W.F, Lipton R.B. Migraine and headache: A meta–analytic approach. In Epidemiology of pain (I Crombie, Ed.). IASP Press Seattle.
20. Silberstein S, Lipton R. Chronic daily headache including transformed migraine, chronic tension–type headache and medication overuse. In: Silberstein S, Lipton R and Dalessio D (eds.) Wolff’s headache and other head pain. Oxford University Press, 2001.
21. Wang S.J., Fuh J.L., Young Y.H., Lu S.R., Shia B.C. Prevalence of migraine in Taipei, Taiwan: a population–based survey. // Cephalalgia. 2000 Jul; 20(6): 566–72.












