Нарушение когнитивных функций является очень важным симптомом для оценки состояния пациента, определения локализации повреждения мозга и нозологического диагноза. Когнитивные расстройства оказывают крайне негативное воздействие на качество жизни как самого пациента, так и его ближайшего окружения, и поэтому нуждаются в коррекции. Все это обусловливает важность диагностики и правильного анализа характера и выраженности когнитивных расстройств у каждого конкретного пациента [4,9,12].
Объективизация когнитивных нарушений
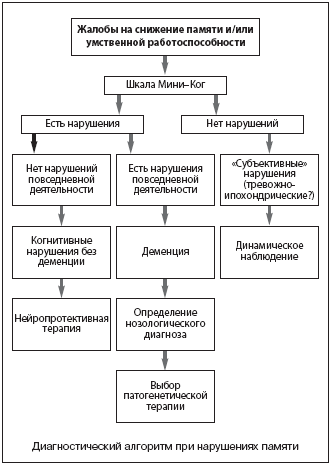
Подозрение на наличие когнитивных нарушений обычно базируется на активных жалобах пациента на повышенную забывчивость, снижение умственной работоспособности или концентрации внимания. Следует отметить, что пациент не всегда в состоянии правильно оценить состояние своей памяти и когнитивных функций. Практический опыт свидетельствует, что приблизительно в половине случаев жалобы пациента на снижение памяти не подтверждаются объективными методами исследования. Исключительно «субъективный» характер забывчивости при нормальных показателях нейропсихологических тестов чаще всего связан с расстройствами личности тревожно-ипохондрического ряда [6].
В связи с вышесказанным важным представляется беседа с ближайшими родственниками пациента. Информация от родственников необходима для уточнения анамнеза заболевания, который невозможно выяснить при наличии у больного мнестических расстройств. Следует также оценить степень самостоятельности больного в повседневной жизни: его способность продолжать профессиональную деятельность, поддерживать контакты с другими людьми, пользоваться бытовой техникой, обслуживать себя в быту. Выявление даже небольшого ограничения повседневной активности свидетельствует о наличии у пациента деменции [6,10,12,28,29].
В любом случае подозрение на наличие когнитивных нарушений является показанием для проведения нейропсихологического исследования. При невозможности проведения такого исследования в полном объеме, можно ограничиться скрининговыми шкалами деменции. Скрининговые шкалы представляют собой простейшие нейропсихологические методики, которые не требуют наличия психологической квалификации у исследователя, не занимают много времени и не вызывают затруднений при интерпретации результатов. Одной из таких шкал, которую можно рекомендовать для широкого применения на практике, является шкала Мини-Ког (табл. 1) [19].
Дифференциальный диагноз когнитивных нарушений
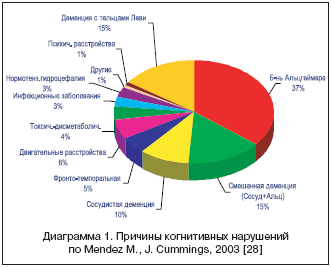
Существуют более 100 различных заболеваний, которые могут приводить к когнитивным нарушениям и деменции [3,6,29]. Наиболее распространенные из них показаны на диаграмме 1.
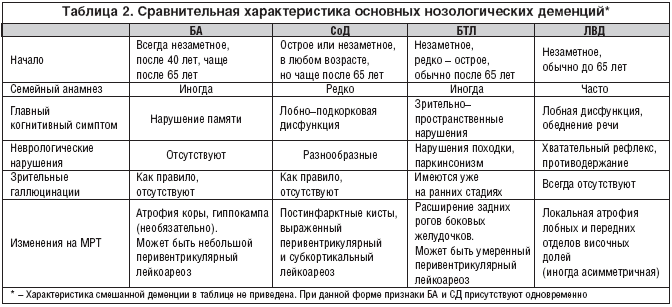
Дифференциальный диагноз между различными процессами, приводящими к деменции, базируется на совокупности данных клинических, нейропсихологических и инструментальных методов исследования. Особые трудности возникают при установлении точного нозологического диагноза на стадии недементных (легких и умеренных) когнитивных нарушений или на стадии тяжелой деменции. В этих случаях различия особенностей когнитивных расстройств могут быть незаметны из-за незначительности или, напротив, крайней степени выраженности нарушений в целом. На стадии легкой и умеренной деменции качественные особенности расстройств обычно более яркие и определяемые (табл. 2).
Самым распространенным заболеванием, приводящим к когнитивным расстройствам и деменции, является болезнь Альцгеймера (БА). Болезнь Альцгеймера представляет собой нейродегенеративное заболевание, в основе которого лежит прогрессирующая гибель нейронов, в первую очередь гиппокампа и височно-теменных отделов коры. Клиническая картина характеризуется постепенным началом, преобладанием на ранних этапах болезни прогрессирующей забывчивости с последующим присоединением афазии, апраксии и агнозии, отсутствием очаговой неврологической симптоматики. Изменения при МРТ отсутствуют или выявляется атрофический процесс, наиболее выраженный в височно-теменных отделах головного мозга [1,3,4,6,8,28,29].
Сосудистая деменция (СоД) может начинаться остро (постинсультная деменция) или постепенно. Ведущими нарушениями являются замедленность мышления, трудности формально-логических операций, снижение критики, эмоциональная лабильность. Практически во всех случаях выявляется очаговая неврологическая симптоматика в виде псевдобульбарного, экстрапирамидного и пирамидного синдромов, нарушений походки. Обязательным условием диагностики СоД являются доказательства сосудистого поражения мозга по данным КТ или МРТ [2-4,6,28,29].
Не менее чем в 15% случаев деменции определяется одновременное сосуществование клинических и морфологических признаков БА и СоД. Клинический диагноз в этих случаях формулируется как смешанная (сосудисто-дегенеративная) деменция. Столь частое сочетание двух нозологических форм деменции объясняется общностью факторов риска, таких как пожилой возраст и наличие заболеваний сердечно-сосудистой системы [3,4,8].
Третьей по частоте причиной деменции является болезнь с телецами Леви (БТЛ). Это заболевание, как и БА, относится к группе нейродегенеративных и характеризуется постепенной гибелью нейронов преимущественно задних отделов головного мозга и подкорковых базальных ганглиев. Специфической особенностью данного заболевания являются повторяющиеся зрительные галлюцинации, которые, однако, присутствуют не у всех пациентов. В когнитивном статусе доминируют нарушения пространственного гнозиса и праксиса обычно в сочетании с умеренными расстройствами памяти. Характерны также экстрапирамидные нарушения. Изменения на МРТ характеризуются симметричным расширением задних рогов боковых желудочков [10,29].
Относительно распространенной причиной деменции, начинающейся в среднем возрасте, является лобно-височная дегенерация (ЛВД). Лобно-височная дегенерация обычно дебютирует на шестом десятилетии жизни поведенческими или речевыми нарушениями. Среди поведенческих нарушений основным является снижение критики, что приводит к неадекватным поступкам. Речевые нарушения проявляются по типу либо акустико-мнестической, либо динамической афазии. В неврологическом статусе выявляются примитивные рефлексы: орального автоматизма, хватательные и др. Изменения на МРТ характеризуются локальной атрофией лобных и/или височных долей головного мозга, часто асимметричной [4,29].
Основные дифференциально-диагностические различия наиболее распространенных форм деменций суммированы в таблице 2.
Лечение когнитивных нарушений
Обязательным мероприятием при когнитивных нарушениях любой выраженности является клинический, лабораторный и инструментальный скрининг так называемой «потенциально обратимой» деменции. По статистике не менее чем в 5% случаев деменции можно добиться значительного регресса нарушений [8,28,29]. Основными причинами «потенциально обратимых» деменций являются дисметаболические расстройства, связанные с заболеваниями печени, почек, щитовидной железы, дефицитом витамина В12 или фолиевой кислоты, интоксикациями, побочными действиями лекарственных препаратов (холинолитики, трициклические антидепрессанты, нейролептики, бензодиазепины). Частично обратимы также когнитивные нарушения при нейрохирургической патологии, такой как опухоль мозга или нормотензивная гидроцефалия. Рекомендуемый минимум клинико-лабораторных и инструментальных исследований при наличии когнитивных расстройств указан в таблице 3.
Всем пациентам с когнитивными нарушениями безусловно показано адекватное лечение заболеваний сердечно-сосудистой системы, которые в настоящее время рассматриваются в качестве факторов риска не только сосудистой, но и первичной дегенеративной деменции. Международные рандомизированные исследования свидетельствуют о профилактическом эффекте длительной антигипертензивной терапии в отношении заболеваемости деменцией. Однако нормализация артериального давления должна быть планомерной и постепенной, так как слишком быстрое снижение АД может приводить к ухудшению перфузии головного мозга. Особенно опасно выраженное снижение АД у лиц с атеросклеротическим стенозом магистральных артерий головы [2-4,9,28,32].
Весьма распространенной причиной когнитивных нарушений в пожилом возрасте является депрессия, которая может быть как ситуативно обусловленной, так и связанной с органическим поражением головного мозга. Депрессия наиболее характерна для хронической сосудистой мозговой недостаточности, болезни Паркинсона и других заболеваний с преимущественным поражением подкорковых базальных ганглиев. Нередко депрессия встречается и при БА.
В случае одновременного наличия как эмоциональных, так и когнитивных нарушений лечение следует начинать с коррекции депрессии. В лечении депрессии в пожилом возрасте следует избегать препаратов с клинически значимым холинолитическим эффектом, таких как трициклические антидепрессанты поскольку они оказывают негативное воздействие на когнитивные функции. Напротив, селективные антагонисты обратного захвата серотонина или селективные антагонисты обратного захвата серотонина и норадреналина способствуют улучшению высшей нервной деятельности [6,9,28]. Для лечения депрессии у пациентов с когнитивными нарушениями также полезным может быть назначение мапротилина (Людиомила) – антидепрессанта тетрациклической структуры, у которого в силу его фармакологических особенностей холинолитические эффекты незначительны [7].
Коррекцию дисметаболических нарушений, лечение сердечно-сосудистой патологии и устранение депрессии можно отнести к «неспецифической терапии» когнитивных расстройств, так как данные мероприятия показаны при любой выраженности и этиологии нарушений.
В отличие от этого, выбор специфического лечения когнитивных нарушений определяется как стадией, так и с особенностями патологического процесса.
На сегодняшний день не существует общепринятого протокола ведения больных с недементными (легкими и умеренными) когнитивными нарушениями. Теоретически приоритетными являются препараты с нейропротективными свойствами, назначение которых может предотвратить или отсрочить наступление деменции. Однако на практике нейропротективный эффект того или иного препарата доказать очень трудно, поскольку это требует многолетнего сравнительного наблюдения за параллельными группами пациентов с плацебо–контролем. Проведение таких исследований не всегда оправдано с экономической и этической точек зрения. Эмпирически при легких и умеренных когнитивных нарушениях различной этиологии чаще всего назначают препараты с вазоактивным и/или метаболическим эффектами [5,6,11,26,27].
В отличие от недементных когнитивных нарушений, деменция легкой и умеренной выраженности имеет общепринятый стандарт терапии, который базируется на результатах международных рандомизированных исследований. В большинстве случаев приоритетным является воздействие на ацетилхолинергическую систему, так как именно недостаточность этой системы лежит в основе наиболее распространенных форм деменции в пожилом возрасте (табл. 4). С целью коррекции ацетилхолинергической медиации используются ингибиторы холинэстераз, приникающие через гематоэнцефалический барьер (ипидакрин, ривастигмин, донепизил, галантамин). Кроме того, на стадии умеренной и тяжелой деменции доказан положительный эффект глутаматергического препарата мемантина [5,17,23,28,29].
К ингибиторам ацетилхолинестреразы, избирательно действующим на головной мозг и имеющим малую вероятность развития периферических холинергических эффектов, относится Экселон (ривастигмин) Эффективность Экселона (ривастигмина) при основных нозологических формах деменции была неоспоримо доказана в крупных, многоцентровых, рандомизированных и плацебо-контролируемых клинических исследованиях на более чем 3300 пациентов. Экселон отличается от прочих селективных ингибиторов ацетилхолинэстеразы, использующихся в клинической практике, тем, что ингибирует не только ацетилхолинэстеразу, но и бутирилхолинэстеразу. Двойной механизм действия препарата лежит в основе не только высокого симптоматического эффекта Экселона в отношении уменьшения выраженности психических расстройств, но также обеспечивает замедление прогрессирования заболевания. В пользу последнего предположения свидетельствует полиморфизм гена, кодирующего бутирилхолинэстеразу у пациентов с быстро прогрессирующей деменций [13,15,16,18,20,24,30,31,33].
Было показано, что на фоне применения Экселона отмечается уменьшение выраженности когнитивных расстройств, нормализация поведения пациента, улучшение адаптации в повседневной жизни, снижается нагрузка на ухаживающих лиц (табл. 5). Указанные эффекты приводят, в конечном счете, к увеличению времени активной жизни пациентов с деменцией, улучшению качества жизни как самих пациентов, так и их родственников [13,15,16,18,20,24,30,31,33].
Следует также отметить, что Экселон является единственным препаратом с доказанной эффективностью не только при БА, сосудистой и смешанной деменции, но и при деменции с тельцами Леви, а также при болезни Паркинсона с деменцией. При заболеваниях с преимущественным поражением подкорковых базальных ганглиев двойной механизм действия Экселона особенно важен, так как в подкорковых структурах концентрация бутирилхолинэстеразы максимальна [10,18,22].
Таким образом, комплексная оценка соматического и нервно-психического статуса пациента, точный нозологический диагноз позволяют оказать эффективную помощь пациенту в большинстве случаев деменции. Возможности эффективной помощи существуют на всех стадиях патологического процесса, но наиболее выраженный эффект отмечается при начале терапии на стадии легких и умеренных когнитивных нарушений. Основной задачей практических врачей является своевременная диагностика возможности развития когнитивных нарушений. А основным направлением разработки перспективных препаратов следует признать поиск эффективного нейропротективного лечения, которое при назначении на стадии недементных когнитивных нарушений, могло бы надежно предотвратить наступление деменции.




Литература
1. Гаврилова С.И. Фармакотерапия болезни Альцгеймера. //Москва: изд-во «Пульс». –2003. –С.109-115.
2. Дамулин И.В. Сосудистая деменция. //Неврологический журнал. –1999. –Т.4. № 3. –С. 4-11.
3. Дамулин И.В. Болезнь Альцгеймера и сосудистая деменция. //Под ред. Н.Н.Яхно. –М. –2002. –С.85.
4. Дамулин И.В., Яхно Н.Н. Дегенеративные заболевания с когнитивными расстройствами. //В кн. «Болезни нервной системы. Руководство для врачей». Под ред. Н.Н.Яхно, Д.Р.Штульмана. –2003. –Т.2. –С.189-207.
5. Захаров В.В., И.В.Дамулин, Н.Н.Яхно. Медикаментозная терапия деменций. //Клиническая фармакология и терапия. –1994. –Т.3. –№ 4. –С. 69-75.
6. Захаров В.В., Яхно Н.Н. Нарушения памяти. //Москва: ГеотарМед. –2003. –С.150.
7. Мосолов С.Н. Место традиционны антидепрессантов в современной терапии депрессивных и тревожных расстройств (на примере препаратов кломипрамин и мапротилин) // М. – 2005 – С.28.
8. Мхитарян Э.А., Преображенская И.С. Болезнь Альцгеймера и цереброваскулярные расстройства. //Неврологический журнал. –2006. –Т.11. –Приложение 1. –С.31-36.
9. Яхно Н.Н. Гериатрические аспекты заболеваний нервной системы. //В кн. «Болезни нервной системы. Руководство для врачей». Под ред. Н.Н.Яхно, Д.Р.Штульман, П.В.Мельничук. М.: Медицина. –1995. Т.2ю –С.465-490.
10. Яхно Н.Н., Преображенская И.С. Деменция с тельцами Леви. //Неврологический журнал. –2003. –Т.8. № 6. –С.4-12.
11. Яхно Н.Н., Захаров В.В. Легкие когнитивные нарушения в пожилом возрасте. //Неврологический журнал. –2004. –№ 1. –С.3-9.
12. Яхно Н.Н. Когнитивные расстройства в неврологической клинике. //Неврологический журнал. –2006. –Т.11. –Приложение № 1. –С.4-12.
13. Agid Y., Dubois B., Anand R., Charabawi G. Efficacy and tolerability of rivastigmine in patients with dementia of Alzheimer’s type. //Curr Res Clin Thep Exp. –1998. –V.59. –P.837-845.
14. Amaducci L., L.Andrea. The epidemiology of the dementia in Europe. //In: “New concepts in vascular dementia”. A.Culebras, J.Matias Cuiu, G.Roman (eds). –Barselona: Prous Science Publishers. –1993. –P.19-27.
15. Anand R., Hartman R., Gharabawi G. Therapeutic effect of Exelon in the treatment of patients with Alzheimer’s disease.
16. Anand R., Hartman R., Gharabawi G. Worldwide clinical experience with Exelon, a new generation of cholinesterase inhibitor in the treatment of Alzheimer’s disease. //Eur J Neurol. –1997. –Vol.4, Suppl.1.-P.S.37.
17. Birks J. Cholinesterase inhibitors for Alzheimer’s disease. // Cochrane Database Syst Rev. –2006.-V.25. –N.1. CD005593.
18. Birks J., Grimley E.J., Iakovidou V., Tsolaki M. Rivastigmine for Alzheimer’s disease. //In: The Cochrane Library. Issue I. Chichester John Willey. –2004.
19. Borson S., Scanlan J., Brush M. et al. The mini-cog: a cognitive ‘vital signs’ measure for dementia in multi-lingual elderly. //Int J Psych. –2000. –V.15. –N.1021-1027.
20. Corey-Bloom J., Anand R., Veach J. A randomized trial evaluating the efficacy and safety of ENA 713 (rivastigmine tartate), a new acetylcholinesterase inhibitor in patients with mild to moderate severe Alzheimers disease. //Int J Ger Psychopharm. –1998. –V.1. –P.55-65.
21. DiCarlo A., Baldereschi M., Amaducci L. Et al. Cognitive impairment without dementia in older people: prevalence, vascular risk factors, impact on disability. The Italian Longitudinal Study on Aging. //J Am Ger Soc. –2000. –V.48. –P.775-782.
22. Emre M., Aarsland D., Albaneo A. et al. Rivastigmine for dementia associated with Parkinson’s disease. //N Engl J Med. –2004. –V.351. –N.24. –P.2509-2518.
23. Erkinjuntti T., Roman G., Gauthier S. Treatment of vascular dementia-evidence from clinical trials with cholinesterase inhibitors. //J Neurol Sci. –2004. –Vol.226. –P.63-66.
24. Forrete F., Anand R., Gharebawi G. A phase II study in patients with Alzheimer’s disease to assess the preliminary efficacy and maximum tolerated dose of rivastigmine. //Eur J Neurology. –1999. –V.6. –P.423-429.
25. Graham J.E., Rockwood K., Beattie E.L. et al. Prevalence and severity of cognitive impairment with and without dementia in an elderly population. //Lancet. –1997. –V.349. –V.1793-1796.
26. Knopman D.S. Current treatment of mild cognitive impairment and Alzheimer’s disease. //Curr Neurol Nerosci Rep. –2006. –V.6. –N.5. –P.365-371.
27. Kurshner H.S. Mild cognitive impairment: to treat or not to treat? //Curr Neurol Neurosci Rep. –2205. –V.5. –N.6. –P.455-457.
28. Lovenstone S., Gauthier S. Management of dementia. London: Martin Dunitz, 2001.
29. Mendez M., Cummings J. Dementia: a clinical approach. //Philadelphia: Elsevier Science. –2003. –534 P.
30. Morreti R., Torre P., Antonello R.M. et al. Rivastigmine in subcortical vascular dementia: an open 22 months study. //J Neurol Sci. –2002. –V.203-204. –P.141-146.
31. Rosler R., Anand R., Cicin-Saine A. et al. Efficacy and safety of rivastigmine in patients with Alzheimer’s disease: International randomized controlled trial. //BMJ. –1999. –V.318. –P.633-638.
32. Skoog I., Gustafson D. Clinical trials for primary prevention in dementia. //In: “Dementia therapeutic research”. K.Rockwood, S.Gauthier (eds). –London a New York: Taylor a Francis. –2006. –P.189-212.
33. Wilkikson D.G., Passmore A.P., Bullock R. et al. A multinational randomized 12 week comparative study of donepizil and rivastigmine in patient with mild to moderate Alzheimer’s disease. //Int J Clin Pract. –2002. –V.56. –P.441-446.












