–¶–µ–ї—М—О –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —П–≤–Є–ї—Б—П —Д–∞—А–Љ–∞–Ї–Њ—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П –Ґ–Є–Њ–Ї—В–∞—Ж–Є–і–Њ–Љ –С–Т –±–Њ–ї—М–љ—Л—Е —Б —А–∞–Ј–љ—Л–Љ–Є —Б—В–∞–і–Є—П–Љ–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Ж–µ—А–µ–±—А–∞–ї—М–љ–Њ–є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є. –Т –Ј–∞–і–∞—З–Є —А–∞–±–Њ—В—Л –≤—Е–Њ–і–Є–ї–Њ: –Є–Ј—Г—З–µ–љ–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ґ–Є–Њ–Ї—В–∞—Ж–Є–і–∞ –С–Т —Г –±–Њ–ї—М–љ—Л—Е –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–Њ–є –Є –≤—Л—П–≤–ї–µ–љ–Є–µ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –Ф–≠ –Є –µ–µ –Є—Б—Е–Њ–і–Њ–≤ —Г –±–Њ–ї—М–љ—Л—Е –Њ—Б–љ–Њ–≤–љ–Њ–є –Є –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ. –Ю—Б–Њ–±–µ–љ–љ–Њ—Б—В—М—О —А–∞–±–Њ—В—Л –±—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Є–µ —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ–є –Њ—Ж–µ–љ–Ї–Є —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ґ–Є–Њ–Ї—В–∞—Ж–Є–і–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –≥—А—Г–њ–њ–Њ–є –Ї–Њ–љ—В—А–Њ–ї—П.
–Ь–∞—В–µ—А–Є–∞–ї –Є –Љ–µ—В–Њ–і—Л
–Э–∞–±–ї—О–і–∞–ї–Є 128 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ф–≠, –Ї–Њ—В–Њ—А—Л–µ —Б–Њ—Б—В–∞–≤–Є–ї–Є –Њ—Б–љ–Њ–≤–љ—Г—О –≥—А—Г–њ–њ—Г. –≠—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –±—Л–ї–Є: –∞—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—В–Њ–љ–Є—П (–Р–У) – —Г 52 (40,6%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј – —Г 36 (28,1%), —Б–Њ—З–µ—В–∞–љ–Є–µ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞ –Є –Р–У – —Г 40 (31,3%). –Т 13,7% —Б–ї—Г—З–∞–µ–≤ –±—Л–ї–Є –і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞–љ—Л –љ–∞—А—Г—И–µ–љ–Є—П —А–Є—В–Љ–∞ —Б–µ—А–і—Ж–∞, —Б–Њ—З–µ—В–∞–≤—И–Є–µ—Б—П —Б —В–µ–Љ –Є–ї–Є –Є–љ—Л–Љ –Њ—Б–љ–Њ–≤–љ—Л–Љ —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ. –†–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ —Б—В–∞–і–Є—П–Љ –Ф–≠ –±—Л–ї–Њ —Б–ї–µ–і—Г—О—Й–Є–Љ: –Ф–≠ I – 43, –Ф–≠ II – 51, –Ф–≠ III – 34.
–С–Њ–ї—М–љ—Л–µ –Њ—Б–љ–Њ–≤–љ–Њ–є –Є –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ –ї–µ—З–Є–ї–Є—Б—М –∞–Љ–±—Г–ї–∞—В–Њ—А–љ–Њ. –Я–∞—Ж–Є–µ–љ—В—Л –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л—Е –≥—А—Г–њ–њ –љ–∞–±–ї—О–і–∞–ї–Є—Б—М –≤ —В–µ—З–µ–љ–Є–µ –≥–Њ–і–∞. –Ю–љ–Є –±—Л–ї–Є –Њ—Б–Љ–Њ—В—А–µ–љ—Л –і–Њ –љ–∞—З–∞–ї–∞ –ї–µ—З–µ–љ–Є—П, –Ј–∞—В–µ–Љ –≤ –Ї–Њ–љ—Ж–µ 1––≥–Њ, 3––≥–Њ, 6––≥–Њ, 7––≥–Њ –Є 12––≥–Њ –Љ–µ—Б—П—Ж–µ–≤. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –Њ—В–Ї—А—Л—В–Њ. –Я—А–Є –љ–∞–±–Њ—А–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є –Љ–µ—В–Њ–і —А–∞–љ–і–Њ–Љ–Є–Ј–∞—Ж–Є–Є. –Я–∞—Ж–Є–µ–љ—В—Л –Ї–∞–Ї –Њ—Б–љ–Њ–≤–љ–Њ–є, —В–∞–Ї –Є –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ –њ–Њ–ї—Г—З–∞–ї–Є –±–∞–Ј–Њ–≤—Г—О —В–µ—А–∞–њ–Є—О, –Ї–Њ—В–Њ—А–∞—П –±—Л–ї–∞ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ —Г–љ–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–∞ –Є –≤–Ї–ї—О—З–∞–ї–∞ –њ—А–Є–µ–Љ –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л (100 –Љ–≥/—Б—Г—В.), –і–Є–њ–Є—А–Є–і–∞–Љ–Њ–ї–∞ (150 –Љ–≥/—Б—Г—В.), –≥–ї–Є—Ж–Є–љ–∞ (900 –Љ–≥/—Б—Г—В.) –Є —Н–љ–∞–ї–∞–њ—А–Є–ї–∞. –Я–Њ—Б–ї–µ–і–љ–Є–є –љ–∞–Ј–љ–∞—З–∞–ї—Б—П –≤ –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ–Њ–є –і–Њ–Ј–µ –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Б—В–∞–і–Є–Є –Р–У –Є –Є—Б—Е–Њ–і–љ–Њ–≥–Њ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П. –Ъ–Њ—А—А–µ–Ї—Ж–Є—П –њ–Њ—Б–ї–µ–і–љ–µ–≥–Њ –і–Њ—Б—В–Є–≥–∞–ї–∞ —Г—А–Њ–≤–љ—П 120/70 – 140/80 –Љ–Љ —А—В.—Б—В. –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є —В–µ—З–µ–љ–Є—П –Р–У, —Б—В–µ–њ–µ–љ–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –њ–µ—А—Д—Г–Ј–Є–Њ–љ–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ –Є –Є—Б—Е–Њ–і–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П – –≤ –љ–∞—З–∞–ї–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –Я—А–Є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ–Љ —Н—Д—Д–µ–Ї—В–µ —Н–љ–∞–ї–∞–њ—А–Є–ї–∞ –≤ –њ–ї–∞–љ–µ —Б–љ–Є–ґ–µ–љ–Є—П –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –µ–≥–Њ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–ї–Є —Б –Є–љ–і–∞–њ–∞–Љ–Є–і–Њ–Љ (2,5 –Љ–≥/—Б—Г—В.). –Ш–Ј–Љ–µ–љ–µ–љ–Є—П —Б—В–Њ–Є–Љ–Њ—Б—В–Є —Б—В–∞–љ–і–∞—А—В–∞ –ї–µ—З–µ–љ–Є—П —Г—З–Є—В—Л–≤–∞–ї–Є –≤ –Ї–∞–ґ–і–Њ–Љ –Ї–Њ–љ–Ї—А–µ—В–љ–Њ–Љ —Б–ї—Г—З–∞–µ. –Ґ–Є–Њ–Ї—В–∞—Ж–Є–і –С–Т –љ–∞–Ј–љ–∞—З–∞–ї—Б—П –њ–µ—А–Њ—А–∞–ї—М–љ–Њ –≤ —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј–µ 600 –Љ–≥ 2 —А–∞–Ј–∞/—Б—Г—В. –≤ —В–µ—З–µ–љ–Є–µ 7 –і–љ–µ–є —Б –њ–µ—А–µ—Е–Њ–і–Њ–Љ –љ–∞ 600 –Љ–≥ 1 —А–∞–Ј/c—Г—В. –≤ —В–µ—З–µ–љ–Є–µ 23 –і–љ–µ–є –Ј–∞ 30 –Љ–Є–љ –і–Њ –µ–і—Л. –Т —В–µ—З–µ–љ–Є–µ –≥–Њ–і–∞ –±–Њ–ї—М–љ—Л–µ –њ–Њ–ї—Г—З–∞–ї–Є –і–≤–∞ –Ї—Г—А—Б–∞ –ї–µ—З–µ–љ–Є—П –Ґ–Є–Њ–Ї—В–∞—Ж–Є–і–Њ–Љ –С–Т – –љ–∞ 1––є –Є 6––є –Љ–µ—Б—П—Ж—Л. –Т –≥—А—Г–њ–њ—Г –Ї–Њ–љ—В—А–Њ–ї—П –≤–Њ—И–ї–Є 118 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ф–≠, –њ–Њ–ї—Г—З–∞–≤—И–Є–µ «–±–∞–Ј–Њ–≤—Г—О» —В–µ—А–∞–њ–Є—О. –Ю—Б–љ–Њ–≤–љ–∞—П –Є –Ї–Њ–љ—В—А–Њ–ї—М–љ–∞—П –≥—А—Г–њ–њ—Л –±—Л–ї–Є —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ—Л –њ–Њ –њ–Њ–ї—Г, –≤–Њ–Ј—А–∞—Б—В—Г, —Н—В–Є–Њ–ї–Њ–≥–Є–Є –Є —В—П–ґ–µ—Б—В–Є —В–µ—З–µ–љ–Є—П –±–Њ–ї–µ–Ј–љ–Є.
–Я—А–Є –Є–Ј—Г—З–µ–љ–Є–Є –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—В–∞—В—Г—Б–∞ –њ—А–Є–Љ–µ–љ—П–ї–Є—Б—М —Б–ї–µ–і—Г—О—Й–Є–µ —И–Ї–∞–ї—Л: MFI–20, MCA:FMA (Motor Clab Assessment: Functional Movement Activities), —И–Ї–∞–ї–∞ –Ґ–Є–љ–љ–µ—В—В–Є, —И–Ї–∞–ї–∞ —В—А–µ–≤–Њ–≥–Є –°–њ–Є–ї–±–µ—А–≥–µ—А–∞, —И–Ї–∞–ї–∞ –У–∞–Љ–Є–ї—М—В–Њ–љ–∞ (HAM–D), —Б–Ї—А–Є–љ–Є–љ–≥––Њ—Ж–µ–љ–Ї–∞ –њ—Б–Є—Е–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П –њ–Њ —И–Ї–∞–ї–µ MMSE, –Њ–њ—А–Њ—Б–љ–Є–Ї «–Т–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ –ї–Њ–Ї—Г—Б–∞ –Ї–Њ–љ—В—А–Њ–ї—П», –Љ–Њ–і–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ–∞—П —И–Ї–∞–ї–∞ –†—Н–љ–Ї–Є–љ –і–ї—П –Њ—Ж–µ–љ–Ї–Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –њ–Њ—Б–ї–µ–і—Б—В–≤–Є–є –Є–љ—Б—Г–ї—М—В–∞. –Т–≤–Є–і—Г —А–∞–Ј–љ–Њ–Љ–∞—Б—И—В–∞–±–љ–Њ—Б—В–Є –Є —А–∞–Ј–љ–Њ–љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ—Б—В–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–љ—Л—Е —И–Ї–∞–ї –і–ї—П —Г–і–Њ–±—Б—В–≤–∞ –Є–Ј–ї–Њ–ґ–µ–љ–Є—П –Є –≤–Њ—Б–њ—А–Є—П—В–Є—П –Љ–∞—В–µ—А–Є–∞–ї–∞ –Љ—Л —Б–Њ—З–ї–Є —Г–і–Њ–±–љ—Л–Љ –Њ–њ–Є—Б—Л–≤–∞—В—М –і–Є–љ–∞–Љ–Є–Ї—Г –±–∞–ї–ї—М–љ–Њ–є –Њ—Ж–µ–љ–Ї–Є —Г–њ–Њ–Љ—П–љ—Г—В—Л—Е —И–Ї–∞–ї –≤ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л—Е –њ—А–Њ—Ж–µ–љ—В–∞—Е, –≥–Њ–≤–Њ—А—П –Њ –њ—А–Њ—Ж–µ–љ—В–µ —Г–ї—Г—З—И–µ–љ–Є—П/—Г—Е—Г–і—И–µ–љ–Є—П —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–µ–≥–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –њ–Њ –Њ—В–љ–Њ—И–µ–љ–Є—О –Ї –µ–≥–Њ –Є—Б—Е–Њ–і–љ–Њ–Љ—Г –Ј–љ–∞—З–µ–љ–Є—О.
–Я–Њ–Љ–Є–Љ–Њ –њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л—Е –њ–Њ–і—Е–Њ–і–Њ–≤, –њ—А–Є –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –±–Њ–ї—М–љ—Л—Е –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є —В—А–∞–і–Є—Ж–Є–Њ–љ–љ—Л–µ –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л–µ –Є –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ—Л–µ –Љ–µ—В–Њ–і—Л, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –Є –љ–µ–є—А–Њ–≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є–Њ–љ–љ—Л–µ (–Ъ–Ґ, –Ь–†–Ґ).
–†–µ–Ј—Г–ї—М—В–∞—В—Л
–Т —В–∞–±–ї–Є—Ж–µ 1 –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –±–∞–ї–ї—М–љ–∞—П –Њ—Ж–µ–љ–Ї–∞ –њ–Њ –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л–Љ —И–Ї–∞–ї–∞–Љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –Є –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ –Ї –Ї–Њ–љ—Ж—Г –љ–∞–±–ї—О–і–µ–љ–Є—П (12––є –Љ–µ—Б—П—Ж). –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ф–≠ I —Б—В–∞–і–Є–Є –њ—А–Є –ї–µ—З–µ–љ–Є–Є –Ґ–Є–Њ–Ї—В–∞—Ж–Є–і–Њ–Љ –С–Т –Њ–Ї–∞–Ј—Л–≤–∞–ї–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ —А–µ–≥—А–µ—Б—Б –∞—Б—В–µ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ (–Ф–Ш 90%), –≤–µ—Б—В–Є–±—Г–ї—П—А–љ–Њ–є –∞—В–∞–Ї—Б–Є–Є (–Ф–Ш 90%) –Є –∞–Ї—Б–Є–∞–ї—М–љ—Л—Е —А–µ—Д–ї–µ–Ї—Б–Њ–≤ (–Ф–Ш 95%). –£ –±–Њ–ї—М–љ—Л—Е —Б –Ф–≠ II, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Ґ–Є–Њ–Ї—В–∞—Ж–Є–і, –Њ—В–Љ–µ—З–µ–љ–Њ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –µ–≥–Њ –≤–ї–Є—П–љ–Є—П –љ–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є —И–Ї–∞–ї—Л «–і–≤–Є–ґ–µ–љ–Є–µ», –∞—В–∞–Ї—Б–Є–Є (–Ф–Ш 90%) –Є –њ—Б–µ–≤–і–Њ–±—Г–ї—М–±–∞—А–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞. –°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Г–ї—Г—З—И–∞–ї–∞—Б—М –±–∞–ї–ї—М–љ–∞—П –Њ—Ж–µ–љ–Ї–∞ –њ–Њ —И–Ї–∞–ї–∞–Љ —В—А–µ–≤–Њ–≥–Є, –і–µ–њ—А–µ—Б—Б–Є–Є –Є —Б–Ї—А–Є–љ–Є–љ–≥–Њ–≤–Њ–є –Њ—Ж–µ–љ–Ї–Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є (MMSE) (–Ф–Ш 90%). –£ –±–Њ–ї—М–љ—Л—Е —Б –Ф–≠ III —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–µ–µ –≤–ї–Є—П–љ–Є–µ —Б–Њ—Е—А–∞–љ—П–ї–Њ—Б—М –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –≤—Б–µ—Е —И–Ї–∞–ї. –Я—А–µ–њ–∞—А–∞—В —В–∞–Ї–ґ–µ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ –≤–ї–Є—П–ї –љ–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є —И–Ї–∞–ї—Л «–і–≤–Є–ґ–µ–љ–Є–µ», –∞—В–∞–Ї—Б–Є–Є (–ї–Њ–±–љ–Њ–є –Є –Љ–Њ–Ј–ґ–µ—З–Ї–Њ–≤–Њ–є) –Є –њ—Б–µ–≤–і–Њ–±—Г–ї—М–±–∞—А–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, –Ї–Њ—В–Њ—А–Њ–µ —Б–Њ—Е—А–∞–љ—П–ї–Њ—Б—М –і–Њ 12––≥–Њ –Љ–µ—Б—П—Ж–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П. –Я—А–Є –ї–µ—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е —Б –Ф–≠ III –њ–Њ–Љ–Є–Љ–Њ —Н—В–Є—Е –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–є –Ґ–Є–Њ–Ї—В–∞—Ж–Є–і –С–Т —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ –≤–ї–Є—П–ї –љ–∞ –і–Є–љ–∞–Љ–Є–Ї—Г –±–∞–ї–ї—М–љ–Њ–є –Њ—Ж–µ–љ–Ї–Є –∞–Љ–Є–Њ—Б—В–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ (–Ф–Ш 95%).
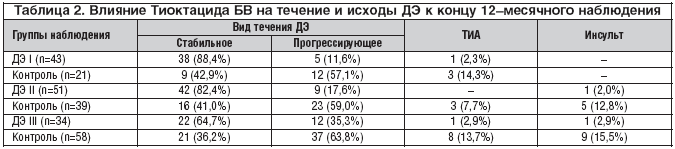
–Т –њ—А–Њ—Ж–µ—Б—Б–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е –Њ—Б–љ–Њ–≤–љ–Њ–є –Є –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ –Њ—Ж–µ–љ–Є–≤–∞–ї–Є —А–Є—Б–Ї –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –Ф–≠, –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –Ґ–Ш–Р –Є –Є–љ—Б—Г–ї—М—В–Њ–≤. –£—З–Є—В—Л–≤–∞–ї–Њ—Б—М —З–Є—Б–ї–Њ –±–Њ–ї—М–љ—Л—Е —Б–Њ —Б—В–∞–±–Є–ї—М–љ—Л–Љ –Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–Є–Љ —В–µ—З–µ–љ–Є–µ–Љ –Ф–≠. –Т –Њ—В–љ–Њ—И–µ–љ–Є–Є —А–Є—Б–Ї–Њ–≤ —А–∞–Ј–≤–Є—В–Є—П –Њ–±–Њ—Б—В—А–µ–љ–Є–є –≤ —В–µ—З–µ–љ–Є–Є –Ф–≠ – –Ґ–Ш–Р –Є –Є–љ—Б—Г–ї—М—В–Њ–≤ –ї–µ—З–µ–љ–Є–µ –Ґ–Є–Њ–Ї—В–∞—Ж–Є–і–Њ–Љ –С–Т –Њ–Ї–∞–Ј–∞–ї–Њ—Б—М –≤–µ—Б—М–Љ–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ (—В–∞–±–ї. 2).
–Я—А–Є –ї–µ—З–µ–љ–Є–Є –Ґ–Є–Њ–Ї—В–∞—Ж–Є–і–Њ–Љ –С–Т –Њ—В–Љ–µ—З–µ–љ–Њ –µ–≥–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ—А–Є –≤—Б–µ—Е —Б—В–∞–і–Є—П—Е –Ф–≠. –Я—А–Є —Н—В–Њ–Љ –Ґ–Є–Њ–Ї—В–∞—Ж–Є–і –С–Т –Њ–Ї–∞–Ј—Л–≤–∞–ї –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –Є –љ–∞ —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Є–љ—Б—Г–ї—М—В–∞ –Є –Ґ–Ш–Р.
–Ґ–Є–Њ–Ї—В–∞—Ж–Є–і –Ј–∞—А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–ї —Б–µ–±—П –Ї–∞–Ї –±–µ–Ј–Њ–њ–∞—Б–љ—Л–є –њ—А–µ–њ–∞—А–∞—В –њ—А–Є –ї–µ—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е —Б –Ф–≠. –Т –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–є –≥—А—Г–њ–њ–µ (128 —З–µ–ї–Њ–≤–µ–Ї) —Г –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Ґ–Є–Њ–Ї—В–∞—Ж–Є–і –С–Т, –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –Ј–∞—Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ—Л —Г 9 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (7,03%), –Ї–Њ—В–Њ—А—Л–µ –±—Л–ї–Є –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ –≤–Є–і–µ –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ (—В–Њ—И–љ–Њ—В–∞, –≥–Њ—А–µ—З—М –Є —Б—Г—Е–Њ—Б—В—М –≤–Њ —А—В—Г), –њ—А–Є —Н—В–Њ–Љ —Г 3 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ—В–Љ–µ—З–∞–ї–Є—Б—М —В—П–ґ–µ—Б—В—М –Є –±–Њ–ї—М –≤ –њ—А–∞–≤–Њ–Љ –њ–Њ–і—А–µ–±–µ—А—М–µ. –Ф–∞–љ–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –≤–Њ–Ј–љ–Є–Ї–∞–ї–Є –њ—А–Є –њ—А–Є–µ–Љ–µ –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –і–Њ–Ј–µ 1200 –Љ–≥/—Б—Г—В. –Я–Њ —Б—В–µ–њ–µ–љ–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –±—Л–ї–Є –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л. –£ 6 –±–Њ–ї—М–љ—Л—Е –≤–Њ–Ј–љ–Є–Ї—И–Є–µ –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –љ–µ –њ–Њ—В—А–µ–±–Њ–≤–∞–ї–Є –Њ—В–Љ–µ–љ—Л –њ—А–µ–њ–∞—А–∞—В–∞, –∞ –њ—А–Є –њ–µ—А–µ—Е–Њ–і–µ –љ–∞ –њ—А–Є–µ–Љ 600 –Љ–≥/—Б—Г—В. —А–µ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–ї–Є. –Ю–і–љ–Њ–≥–Њ –±–Њ–ї—М–љ–Њ–є –њ—А–µ–Ї—А–∞—В–Є–ї –њ—А–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–∞ –Є –≤—Л–±—Л–ї –Є–Ј –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤ –Ї–Њ–љ—Ж–µ –њ—А–Њ–≤–µ–і–µ–љ–Є—П –≤—В–Њ—А–Њ–≥–Њ –Ї—Г—А—Б–∞ –ї–µ—З–µ–љ–Є—П. –Т—Б–µ 128 —З–µ–ї–Њ–≤–µ–Ї, –≤–Њ—И–µ–і—И–Є–µ –≤ –Є—Б—Б–ї–µ–і—Г–µ–Љ—Г—О –≥—А—Г–њ–њ—Г, –Њ—Ж–µ–љ–Є–ї–Є —А–µ–Ј—Г–ї—М—В–∞—В—Л –ї–µ—З–µ–љ–Є—П –Ї–∞–Ї «–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–µ»: 27 –±–Њ–ї—М–љ—Л—Е –Ї–∞–Ї «–Њ—В–ї–Є—З–љ—Л–µ», 18 –Ї–∞–Ї «—Е–Њ—А–Њ—И–Є–µ» –Є 4 –њ–∞—Ж–Є–µ–љ—В–∞ –Ї–∞–Ї «—Г–і–Њ–≤–ї–µ—В–≤–Њ—А–Є—В–µ–ї—М–љ—Г—О».
–§–∞—А–Љ–∞–Ї–Њ—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј
–Т –њ—А–Њ–≤–µ–і–µ–љ–љ—Л—Е —Д–∞—А–Љ–∞–Ї–Њ—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є—Е —А–∞—Б—З–µ—В–∞—Е —Г—З–Є—В—Л–≤–∞–ї–Є—Б—М –њ—А—П–Љ—Л–µ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–µ –Є –љ–µ–Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–µ –Ј–∞—В—А–∞—В—Л: –љ–∞ –∞–Љ–±—Г–ї–∞—В–Њ—А–љ–Њ–µ –Є —Б—В–∞—Ж–Є–Њ–љ–∞—А–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ – –Ї–Њ–љ—Б—Г–ї—М—В–∞—Ж–Є–Є —Б–њ–µ—Ж–Є–∞–ї–Є—Б—В–Њ–≤, –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, —Б—В–Њ–Є–Љ–Њ—Б—В—М –Ї–Њ–є–Ї–Њ––і–љ—П, —Б—В–Њ–Є–Љ–Њ—Б—В—М –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П, – –∞ —В–∞–Ї–ґ–µ –њ—А—П–Љ—Л–µ –љ–µ–Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–µ –Ј–∞—В—А–∞—В—Л. –Ь–µ–ґ–±–Њ–ї—М–љ–Є—З–љ—Л–µ —А–∞–Ј–ї–Є—З–Є—П –≤ —В–∞—А–Є—Д–∞—Е –ї–µ—З–µ–љ–Є—П –љ–µ —Г—З–Є—В—Л–≤–∞–ї–Є—Б—М. –Я—А–Є –њ–Њ–і–±–Њ—А–µ —Ж–µ–љ–Њ–≤—Л—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ—Л —Б–ї–µ–і—Г—О—Й–Є–µ –Є—Б—В–Њ—З–љ–Є–Ї–Є: –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Њ–љ–љ—Л–є –±—О–ї–ї–µ—В–µ–љ—М «–Ь–µ–і–Є—Ж–Є–љ–∞ (–Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–µ –њ—А–µ–њ–∞—А–∞—В—Л, –Њ–±–Њ—А—Г–і–Њ–≤–∞–љ–Є—П, —Г—Б–ї—Г–≥–Є)» –∞–≥–µ–љ—В—Б—В–≤–∞ «–Ь–Њ–±–Є–ї–µ», «–§–∞—А–Љ–∞—Ж–µ–≤—В–Є—З–µ—Б–Ї–Є–є –±—О–ї–ї–µ—В–µ–љ—М», «–Ґ–∞—А–Є—Д—Л –љ–∞ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–µ —Г—Б–ї—Г–≥–Є, –њ—А–µ–і–Њ—Б—В–∞–≤–ї—П–µ–Љ—Л–µ –≤–Ј—А–Њ—Б–ї–Њ–Љ—Г –љ–∞—Б–µ–ї–µ–љ–Є—О –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –Ь–Њ—Б–Ї–Њ–≤—Б–Ї–Њ–є –≥–Њ—А–Њ–і—Б–Ї–Њ–є –њ—А–Њ–≥—А–∞–Љ–Љ–Њ–є –Њ–±—П–Ј–∞—В–µ–ї—М–љ–Њ–≥–Њ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–≥–Њ —Б—В—А–∞—Е–Њ–≤–∞–љ–Є—П» [1]. –°—В–Њ–Є–Љ–Њ—Б—В—М –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–Њ–≥–Њ –Є –љ–µ–Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –≤–Ј—П—В–∞ –µ–і–Є–љ—Л–Љ –≤—А–µ–Љ–µ–љ–љ—Л–Љ —Б—А–µ–Ј–Њ–Љ –љ–∞ –і–µ–Ї–∞–±—А—М 2009 –≥. –Є –њ–µ—А–µ–≤–µ–і–µ–љ–∞ –≤ –∞–Љ–µ—А–Є–Ї–∞–љ—Б–Ї–Є–µ –і–Њ–ї–ї–∞—А—Л –њ–Њ –Ї—Г—А—Б—Г 1 —Г.–µ.= 29,0 —А—Г–±.
–†–∞—Б—Б—З–Є—В–∞–љ–∞ —Б—В–Њ–Є–Љ–Њ—Б—В—М –Ї–∞–ґ–і–Њ–є –µ–і–Є–љ–Є—Ж—Л –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Б—А–µ–і—Б—В–≤–∞ (—В–∞–±–ї–µ—В–Ї–∞, –Ї–∞–њ—Б—Г–ї–∞, —Д–ї–∞–Ї–Њ–љ, –∞–Љ–њ—Г–ї–∞ –Є —В.–і.) –і–ї—П –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П —А–∞—Б—Е–Њ–і–Њ–≤ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ —Г—Б–ї–Њ–≤–Є—П—Е —Б—В–∞—Ж–Є–Њ–љ–∞—А–∞ –Є –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –∞–Љ–±—Г–ї–∞—В–Њ—А–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П (—В–∞–±–ї–Є—Ж–∞ –њ—А–Є–ї–Њ–ґ–µ–љ–Є—П). –Ч–∞—В–µ–Љ —Б—В–Њ–Є–Љ–Њ—Б—В—М –Ї–∞–ґ–і–Њ–є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–є –µ–і–Є–љ–Є—Ж—Л —Г–Љ–љ–Њ–ґ–∞–ї–∞—Б—М –љ–∞ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ—Л—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –µ–і–Є–љ–Є—Ж, –і–∞–ї–µ–µ —Б—В–Њ–Є–Љ–Њ—Б—В—М –≤—Б–µ—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤ —Б–Ї–ї–∞–і—Л–≤–∞–ї–∞—Б—М –Є –і–µ–ї–Є–ї–∞—Б—М –љ–∞ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –±–Њ–ї—М–љ—Л—Е.
–Ю–њ—А–µ–і–µ–ї–µ–љ–Є–µ —Б—В–Њ–Є–Љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —А–∞–Ј–љ—Л–Љ–Є —Б—В–∞–і–Є—П–Љ–Є –Ф–≠, –≤—Е–Њ–і—П—Й–Є—Е –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ—Г—О –≥—А—Г–њ–њ—Г (–±–µ–Ј —Г—З–µ—В–∞ –ї–µ—З–µ–љ–Є—П —А–∞—Б—Е–Њ–і–Њ–≤ –љ–∞ –ї–µ—З–µ–љ–Є–µ —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–µ–є —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є): –љ–∞ 1 –±–Њ–ї—М–љ–Њ–≥–Њ (–Ј–∞–Ї–Њ–љ—З–µ–љ–љ—Л–є —Б–ї—Г—З–∞–є) —Б—З–Є—В–∞–ї–Є –Ј–∞—В—А–∞—В—Л –љ–∞ –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –±–∞–Ј–Њ–≤–Њ–є —В–µ—А–∞–њ–Є–Є, –љ–∞ –ї–µ—З–µ–љ–Є–µ –≤–Њ–Ј–љ–Є–Ї—И–Є—Е –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є «–±–∞–Ј–Њ–≤–Њ–є —В–µ—А–∞–њ–Є–Є» –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤, –љ–∞ –ї–µ—З–µ–љ–Є–µ –Ґ–Ш–Р, —Ж–µ—А–µ–±—А–∞–ї—М–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ї—А–Є–Ј–Њ–≤ –Є –Є–љ—Б—Г–ї—М—В–Њ–≤ –Ј–∞ –≤—Б–µ –≤—А–µ–Љ—П –љ–∞–±–ї—О–і–µ–љ–Є—П, –∞ —В–∞–Ї–ґ–µ –њ—А—П–Љ—Л–µ –љ–µ–Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–µ –Ј–∞—В—А–∞—В—Л.
–Ґ–∞–Ї –і–ї—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ф–≠ I —Б—В–∞–і–Є–Є –Њ–±—Й–∞—П —Б—В–Њ–Є–Љ–Њ—Б—В—М –Ї–Њ–љ—Б—Г–ї—М—В–∞—Ж–Є–є –љ–∞ –Њ–і–љ–Њ–≥–Њ –±–Њ–ї—М–љ–Њ–≥–Њ –≤ –≥–Њ–і —Б–Њ—Б—В–∞–≤–Є–ї–∞ 13,6$. –Ю–±—Й–∞—П —Б—В–Њ–Є–Љ–Њ—Б—В—М –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –љ–∞ –Њ–і–љ–Њ–≥–Њ –±–Њ–ї—М–љ–Њ–≥–Њ –≥–Њ–і —Б–Њ—Б—В–∞–≤–Є–ї–∞ 41,1$.
–Ю–њ—А–µ–і–µ–ї–µ–љ–Є–µ —Б—В–Њ–Є–Љ–Њ—Б—В–Є «–±–∞–Ј–Њ–≤–Њ–є —В–µ—А–∞–њ–Є–Є» —Г –±–Њ–ї—М–љ—Л—Е –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л —Б —А–∞–Ј–љ—Л–Љ–Є —Б—В–∞–і–Є—П–Љ–Є –Ф–≠ –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ —Б—А–µ–і–љ–Є–µ –Ј–∞—В—А–∞—В—Л –љ–∞ –њ—А–Њ–≤–µ–і–µ–љ–Є–µ «–±–∞–Ј–Њ–≤–Њ–є —В–µ—А–∞–њ–Є–Є» —Б–Њ—Б—В–∞–≤–Є–ї–Є:
20145,75/118 = 170,7$.
–Т –Њ—Б–љ–Њ–≤–љ–Њ–Љ –Ї—Г—А—Б –ї–µ—З–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є, –≤—Е–Њ–і—П—Й–Є–Љ–Є –≤ «–±–∞–Ј–Њ–≤—Г—О —В–µ—А–∞–њ–Є—О», –љ–∞ –≤—Б–µ–Љ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є –љ–∞–±–ї—О–і–µ–љ–Є—П –њ–µ—А–µ–љ–Њ—Б–Є–ї—Б—П –±–Њ–ї—М–љ—Л–Љ–Є —Е–Њ—А–Њ—И–Њ. –Я–Њ–±–Њ—З–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є –≤–Њ –≤—А–µ–Љ—П –Ї—Г—А—Б–∞ –ї–µ—З–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є, –≤—Е–Њ–і—П—Й–Є–Љ–Є –≤ «–±–∞–Ј–Њ–≤—Г—О —В–µ—А–∞–њ–Є—О», –≤–Њ–Ј–љ–Є–Ї–ї–Є —Г 2 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (1,7%). –Я–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –≤–Ї–ї—О—З–∞–ї–Є –≤ —Б–µ–±—П –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –Ї–∞—И–ї—П (1 –њ–∞—Ж–Є–µ–љ—В), –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –≥–Є–њ–Њ—В–Њ–љ–Є–Є –≤ –љ–∞—З–∞–ї–µ –ї–µ—З–µ–љ–Є—П (1 –њ–∞—Ж–Є–µ–љ—В). –Э–Є –≤ –Њ–і–љ–Њ–Љ —Б–ї—Г—З–∞–µ –Ї—Г—А—Б «–±–∞–Ј–Њ–≤–Њ–є —В–µ—А–∞–њ–Є–Є» –љ–µ –±—Л–ї –Њ—В–Љ–µ–љ–µ–љ –Є–Ј––Ј–∞ –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П, –Є –±–Њ–ї—М–љ—Л–µ –љ–µ –±—Л–ї–Є –Є—Б–Ї–ї—О—З–µ–љ—Л –Є–Ј –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П.
–Я—А–Є –∞–љ–∞–ї–Є–Ј–µ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –ї–µ—З–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л –≤—Л—П—Б–љ–µ–љ–Њ, —З—В–Њ –њ—А–Њ—Ж–µ–љ—В –±–Њ–ї—М–љ—Л—Е, –њ–µ—А–µ–љ–µ—Б—И–Є—Е –Є–љ—Б—Г–ї—М—В –≤ —В–µ—З–µ–љ–Є–µ –≥–Њ–і–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П, —Б–Њ—Б—В–∞–≤–Є–ї 11,9% (14 –±–Њ–ї—М–љ—Л—Е) –Є –њ–µ—А–µ–љ–µ—Б—И–Є—Е –Ґ–Ш–Р – 11,9% (14 –±–Њ–ї—М–љ—Л—Е) (—В–∞–±–ї. 2).
–°—А–µ–і–љ—П—П —Б—В–Њ–Є–Љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П –±–Њ–ї—М–љ—Л—Е —Б –Ґ–Ш–Р —А–∞–≤–љ—П–ї–∞—Б—М 476,71$, –∞ —Б—В–Њ–Є–Љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–∞ —Б –Є–љ—Б—Г–ї—М—В–Њ–Љ – 667,0$.
–°—А–µ–і–љ—П—П —Б—В–Њ–Є–Љ–Њ—Б—В—М –њ—А—П–Љ—Л—Е –љ–µ–Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е –Ј–∞—В—А–∞—В –љ–∞ 1 –њ–∞—Ж–Є–µ–љ—В–∞ –≤ –≥–Њ–і —Б–Њ—Б—В–∞–≤–Є–ї–∞: —Г –±–Њ–ї—М–љ—Л—Е —Б –Ґ–Ш–Р – 10,57$, —Г –±–Њ–ї—М–љ—Л—Е —Б –Є–љ—Б—Г–ї—М—В–Њ–Љ – 226,9$.
–Ш—В–Њ–≥–Њ: —Б—А–µ–і–љ—П—П —Б—В–Њ–Є–Љ–Њ—Б—В—М –њ—А—П–Љ—Л—Е –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е –Є –љ–µ–Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е –Ј–∞—В—А–∞—В –љ–∞ –ї–µ—З–µ–љ–Є–µ –Њ–і–љ–Њ–≥–Њ –њ–∞—Ж–Є–µ–љ—В–∞ –≤ –≥–Њ–і —Б –Ґ–Ш–Р —Б–Њ—Б—В–∞–≤–Є–ї–∞ – 487,3, –∞ —Б –Є–љ—Б—Г–ї—М—В–Њ–Љ – 893,9$.
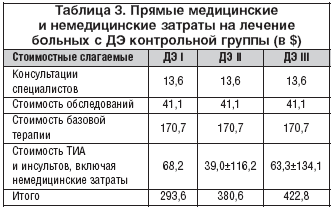
–Т —В–∞–±–ї–Є—Ж–µ 3 –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л —Б—В–Њ–Є–Љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П (–њ—А—П–Љ—Л–µ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–µ –Є –љ–µ–Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–µ –Ј–∞—В—А–∞—В—Л) –Ф–≠ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л.
–Ш—В–∞–Ї, –Њ–±—Й–∞—П —Б—В–Њ–Є–Љ–Њ—Б—В—М –Ф–≠ —А–∞–Ј–љ—Л—Е —Б—В–∞–і–Є–є, –≤–Ї–ї—О—З–∞—П —Б—В–Њ–Є–Љ–Њ—Б—В—М –Ї–Њ–љ—Б—Г–ї—М—В–∞—Ж–Є–є, –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –±–∞–Ј–Њ–≤–Њ–є —В–µ—А–∞–њ–Є–Є, –∞ —В–∞–Ї–ґ–µ —Б—В–Њ–Є–Љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П –Ґ–Ш–Р, –Є–љ—Б—Г–ї—М—В–Њ–≤, –≤–Њ–Ј–љ–Є–Ї–∞—О—Й–Є—Е –≤ —В–µ—З–µ–љ–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –≤–Ї–ї—О—З–∞—П –Є —Б—В–Њ–Є–Љ–Њ—Б—В—М –њ—А—П–Љ—Л—Е –љ–µ–Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е –Ј–∞—В—А–∞—В, —Б–Њ—Б—В–∞–≤–Є–ї–Є: –Ф–≠ I – 293,6$; –Ф–≠ II – 380,6$; –Ф–≠ III – 422,8$.
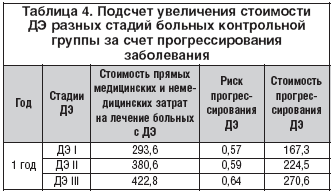
–Я–Њ—Б–ї–µ –њ–Њ–і—Б—З–µ—В–∞ —Б—В–Њ–Є–Љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е —Б —А–∞–Ј–љ—Л–Љ–Є —Б—В–∞–і–Є—П–Љ–Є –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л –Љ—Л –Љ–Њ–ґ–µ–Љ –њ–Њ–і—Б—З–Є—В–∞—В—М —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —А–∞—Б—Е–Њ–і–Њ–≤ –љ–∞ –ї–µ—З–µ–љ–Є–µ –±–Њ–ї—М–љ—Л—Е –Ј–∞ —Б—З–µ—В –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –±–Њ–ї—М–љ—Л–µ, –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—П –њ–Њ —Б—В–∞–і–Є—П–Љ –Ф–≠ —В—А–µ–±—Г—О—В –±–Њ–ї—М—И–Є—Е –і–µ–љ–µ–ґ–љ—Л—Е –≤–ї–Њ–ґ–µ–љ–Є–є –≤ –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–µ –ї–µ—З–µ–љ–Є–µ (—В–∞–±–ї. 4).
–Ш—В–∞–Ї, –Њ–±—Й–∞—П —Б—В–Њ–Є–Љ–Њ—Б—В—М –њ—А—П–Љ—Л—Е –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е –Є –љ–µ–Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е –Ј–∞—В—А–∞—В –љ–∞ –ї–µ—З–µ–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є —Б—В–∞–і–Є—П–Љ–Є –Ф–≠ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л —Б —Г—З–µ—В–Њ–Љ –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –±–Њ–ї–µ–Ј–љ–Є —Б–Њ—Б—В–∞–≤–Є–ї–∞:
–Ф–≠ I – 293,6 + 167,3 = 460,9$;
–Ф–≠ II – 380,6 + 224,5 = 605,1$;
–Ф–≠ III – 422,8 + 270,6 = 693,4$.
–Я—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є —Б—В–Њ–Є–Љ–Њ—Б—В–љ–Њ–—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ –ї–µ—З–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ—Л, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ–Њ–і—Б—З–Є—В–∞—В—М —Б—В–Њ–Є–Љ–Њ—Б—В—М –Ј–∞—В—А–∞—В –љ–∞ –њ—А–Њ–≤–µ–і–µ–љ–Є–µ —Б–∞–Љ–Њ–є –љ–µ–є—А–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Ґ–Є–Њ–Ї—В–∞—Ж–Є–і–Њ–Љ, —З—В–Њ –њ—А–Є–≤–µ–і–µ–љ–Њ –≤ —В–∞–±–ї–Є—Ж–µ 5.
–°—В–Њ–Є–Љ–Њ—Б—В—М –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –Ї–Њ–љ—Б—Г–ї—М—В–∞—Ж–Є–є, «–±–∞–Ј–Њ–≤–Њ–є —В–µ—А–∞–њ–Є–Є» –Є —Б—В–Њ–Є–Љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П –Ґ–Є–Њ–Ї—В–∞—Ж–Є–і–Њ–Љ –С–Т –±–Њ–ї—М–љ—Л—Е —Б —А–∞–Ј–љ—Л–Љ–Є —Б—В–∞–і–Є—П–Љ–Є –Ф–≠ –њ–Њ –≤—Л–±—А–∞–љ–љ–Њ–є —Б—Е–µ–Љ–µ –≤ —В–µ—З–µ–љ–Є–µ 30 –і–љ–µ–є (2 –Ї—Г—А—Б–∞ –ї–µ—З–µ–љ–Є—П –≤ –≥–Њ–і) —Б–Њ—Б—В–∞–≤–Є–ї–∞ 170,7$.
–Ч–љ–∞—П —З–Є—Б–ї–Њ –≤–Њ–Ј–љ–Є–Ї—И–Є—Е –Ґ–Ш–Р –Є –Є–љ—Б—Г–ї—М—В–Њ–≤ –≤ —В–µ—З–µ–љ–Є–µ –≥–Њ–і–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П, –Є—Е —Б—В–Њ–Є–Љ–Њ—Б—В—М, –∞ —В–∞–Ї–ґ–µ —Б—В–Њ–Є–Љ–Њ—Б—В—М –њ—А—П–Љ—Л—Е –љ–µ–Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е –Ј–∞—В—А–∞—В, –Љ—Л –Љ–Њ–ґ–µ–Љ —А–∞—Б—Б—З–Є—В–∞—В—М –Њ–±—Й—Г—О —Б—В–Њ–Є–Љ–Њ—Б—В—М –њ—А—П–Љ—Л—Е –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е –Є –љ–µ–Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е –Ј–∞—В—А–∞—В –љ–∞ –ї–µ—З–µ–љ–Є–µ –Њ–і–љ–Њ–≥–Њ –њ–∞—Ж–Є–µ–љ—В–∞ –≤ –≥–Њ–і —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є —Б—В–∞–і–Є—П–Љ–Є –Ф–≠ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –Ґ–Є–Њ–Ї—В–∞—Ж–Є–і–Њ–Љ –С–Т. –Ю–±—Й–∞—П —Б—В–Њ–Є–Љ–Њ—Б—В—М –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –Ї–Њ–љ—Б—Г–ї—М—В–∞—Ж–Є–є, «–±–∞–Ј–Њ–≤–Њ–є —В–µ—А–∞–њ–Є–Є», —Б—В–Њ–Є–Љ–Њ—Б—В—М —Б–∞–Љ–Њ–є —В–µ—А–∞–њ–Є–Є —Б–Њ–ї–Ї–Њ–Љ–µ—А–Є–ї–Њ–Љ, –∞ —В–∞–Ї–ґ–µ —Б —Г—З–µ—В–Њ–Љ —Б—В–Њ–Є–Љ–Њ—Б—В–Є –Ґ–Ш–Р –Є –Є–љ—Б—Г–ї—М—В–Њ–≤, –≤–Њ–Ј–љ–Є–Ї—И–Є—Е –Ј–∞ –≥–Њ–і –љ–∞–±–ї—О–і–µ–љ–Є—П, –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –≤ —В–∞–±–ї–Є—Ж–µ 6.
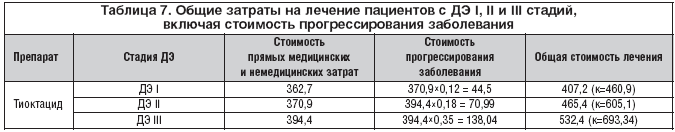
–°—Г–Љ–Љ–Є—А—Г—П —Б—В–Њ–Є–Љ–Њ—Б—В—М –Ї–Њ–љ—Б—Г–ї—М—В–∞—Ж–Є–є, –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –±–∞–Ј–Њ–≤–Њ–є —В–µ—А–∞–њ–Є–Є –Є —Б–∞–Љ–Њ–≥–Њ –Ґ–Є–Њ–Ї—В–∞—Ж–Є–і–∞ –С–Т, –∞ —В–∞–Ї–ґ–µ —Б—В–Њ–Є–Љ–Њ—Б—В—М –¶–°–Ъ/–Ґ–Ш–Р –Є –Є–љ—Б—Г–ї—М—В–Њ–≤, –≤–Њ–Ј–љ–Є–Ї—И–Є—Е –Ј–∞ –≤—А–µ–Љ—П –љ–∞–±–ї—О–і–µ–љ–Є—П (–≤–Ї–ї—О—З–∞—П –љ–µ–Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–µ –Ј–∞—В—А–∞—В—Л) —Г –±–Њ–ї—М–љ—Л—Е —Б —А–∞–Ј–љ—Л–Љ–Є —Б—В–∞–і–Є—П–Љ–Є –Ф–≠, –Љ—Л –њ–Њ–ї—Г—З–Є–ї–Є —Б—В–Њ–Є–Љ–Њ—Б—В—М –њ—А—П–Љ—Л—Е –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е –Є –љ–µ–Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е –Ј–∞—В—А–∞—В –љ–∞ –ї–µ—З–µ–љ–Є–µ –Њ–і–љ–Њ–≥–Њ –њ–∞—Ж–Є–µ–љ—В–∞ –≤ –≥–Њ–і, –Ї–Њ—В–Њ—А—Л–µ —Б–Њ—Б—В–∞–≤–Є–ї–Є:
–Ф–≠ I – 362,7$;
–Ф–≠ II – 370,9$;
–Ф–≠ III – 394,4$.
–Т —В–∞–±–ї–Є—Ж–µ 7 –њ—А–Є–≤–µ–і–µ–љ—Л —Ж–Є—Д—А—Л —Б —Г—З–µ—В–Њ–Љ —Б—В–Њ–Є–Љ–Њ—Б—В–Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Љ–Њ–ґ–љ–Њ –Ї–Њ–љ—Б—В–∞—В–Є—А–Њ–≤–∞—В—М, —З—В–Њ –ї–µ—З–µ–љ–Є–µ –Ґ–Є–Њ–Ї—В–∞—Ж–Є–і–Њ–Љ –С–Т —Г –±–Њ–ї—М–љ—Л—Е —Б –Ф–≠ –њ—А–Є–≤–Њ–і–Є—В –Ї –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ—Г –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–Љ—Г —Г–ї—Г—З—И–µ–љ–Є—О, —Б–љ–Є–ґ–∞–µ—В —А–Є—Б–Ї –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –Є–љ—Б—Г–ї—М—В–Њ–≤ –≤ —В–µ—З–µ–љ–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є —Г–Љ–µ–љ—М—И–∞–µ—В –њ—А–Њ—Ж–µ–љ—В –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е —Б –Ф–≠ I –Є II —Б—В–∞–і–Є–є. –Я—А–µ–њ–∞—А–∞—В –Є–Љ–µ–µ—В –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–є –њ—А–Њ—Ж–µ–љ—В –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤, —Е–Њ—А–Њ—И–Њ –њ–µ—А–µ–љ–Њ—Б–Є—В—Б—П –±–Њ–ї—М–љ—Л–Љ–Є, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –Є –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є —Б—В–∞—А—И–Є—Е –≤–Њ–Ј—А–∞—Б—В–љ—Л—Е –≥—А—Г–њ–њ.
–Ґ–µ—А–∞–њ–Є—П –Ґ–Є–Њ–Ї—В–∞—Ж–Є–і–Њ–Љ –С–Т –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ–∞ —Б —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Њ–є —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б–Њ —Б—В–Њ–Є–Љ–Њ—Б—В—М—О –ї–µ—З–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Г—О –Є –∞–љ—В–Є—В—А–Њ–Љ–±–Њ—В–Є—З–µ—Б–Ї—Г—О —В–µ—А–∞–њ–Є—О, —З—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –µ–≥–Њ –≤—Л—Б–Њ–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О –≤–ї–Є—П–љ–Є—П –љ–∞ —А–Є—Б–Ї –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –Ґ–Ш–Р –Є –Є–љ—Б—Г–ї—М—В–Њ–≤ –Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –Ф–≠, –њ—А–Є–≤–Њ–і—П—Й–µ–є —Б –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ—Г —Г–Љ–µ–љ—М—И–µ–љ–Є—О –Ј–∞—В—А–∞—В –љ–∞ –ї–µ—З–µ–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Н—В–Є—Е –≥—А—Г–њ–њ.



–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –Т–Њ—А–Њ–±—М–µ–≤ –Я.–Р., –Р–≤–Ї—Б–µ–љ—В—М–µ–≤–∞ –Ь.–Т., –Ѓ—А—М–µ–≤ –Р.–°. –Є –і—А. –Ъ–ї–Є–љ–Є–Ї–Њ–—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј. –Ь. «–Э—М—О–і–Є–∞–Љ–µ–і»: 2004; 403 —Б.
2. –У—Г—Б–µ–≤ –Х.–Ш. –°–Ї–≤–Њ—А—Ж–Њ–≤–∞ –Т.–Ш. –Ш—И–µ–Љ–Є—П –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ –Ь –Ь–µ–і–Є—Ж–Є–љ–∞ 2001, –°. 248.
3. –°–Є–≤–Њ—Г—Б –У.–Ш. –Р–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ–∞—П —В–µ—А–∞–њ–Є—П –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –њ–Њ–ї–Є–љ–µ–≤—А–Њ–њ–∞—В–Є–Є —Г –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ α––ї–Є–њ–Њ–µ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л // –§—А–Љ–∞—В–µ–Ї–∞.2004. вДЦ9/10. –°.55–59.
4. –І—Г–Ї–∞–љ–Њ–≤–∞ –Х.–Ш. –Ф–Є—Б—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–∞—П —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є—П (–Ї–ї–Є–љ–Є–Ї–∞, –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Є –ї–µ—З–µ–љ–Є–µ). –Ф–Є—Б—Б –і–Љ–љ. –Ь. 2004.
5. Goldstein L.B., Adams R., Becker K. et al. Primary prevention of ischemic stroke: a statement for healthcare professionals from the Stroke Council of the American Heart Association. // Stroke 2001; 32: 280–299.
6. Sands M.L., Shetterly S.M., Frankin G.M., et al. Incidence of distal symmetric (sensory) neuropathy in NIDDM/ The Sun Luis Vallery Diabetes Study. Diabetes Care 1997; 20(3): p/322–29
7. Pepine C., Celermajer D., Drexler H. Vascular health as a therapeutic target in cardiovascular disease. University of Florida 1998; p.42.
8. Plum F. Neuroprotection in acute ischemic stroke. // JAMA, 2001, 285, 1–4.












