Для мешотчатых внутричерепных аневризм (ВА), которые представляют собой аномальные локальные расширения просвета сосудов головного мозга, характерны высокая частота встречаемости и смертность. За последние годы представления о патогенезе, а также методах лечения этого заболевания претерпели значительные изменения. Традиционные представления о клиническом течении аневризм и высоком риске разрыва той или иной аневризмы сегодня ставятся под сомнение [1,2].
Ранее, в 1997 г., когда подобная проблема уже обсуждалась на страницах «New England Journal of Medicine» в рубрике «Medical Progress», пациентам, у которых по тем или иным причинам не проводилось оперативное вмешательство, был предложен новый экспериментальный малоинвазивный эндоваскулярный метод хирургического лечения ВА – эмболизация [3]. Десятилетний опыт активного применения этой технологии свидетельствует о ее безопасности. Она стала альтернативой традиционным открытым нейрохирургическим операциям с наложением клипсы (клипированием), при которых необходима трепанация черепа. Сегодня в ряде клиник при выборе тактики хирургического лечения ВА предпочтение отдается именно эмболизации, а не клипированию. С 1995 г., когда микроспирали Джуглиелми были одобрены Управлением по контролю за продуктами и лекарствами (FDA), проведено уже около 150 тыс. операций с их использованием [4,5]. В представленном ниже обзоре проанализированы результаты исследований, посвященных изучению этого во-проса.
Эпидемиология и патофизиология
ВА встречаются достаточно часто. Так, по данным аутопсии их распространенность среди взрослого населения составляет от 1 до 5% [2], то есть аневризмы выявляются у 10–12 млн. жителей США [3]. К счастью, в большинстве случаев аневризмы имеют небольшой размер, а 50–80% не подвержены разрыву [6]. Считается, что ВА появляются спорадически, хотя описаны и редко встречающиеся наследственные формы этого заболевания [3]. С возникновением аневризм ассоциированы поликистозная болезнь почек, наследуемая по аутосомно–доминантному типу, фибромышечная дисплазия, синдром Марфана, синдром Элерса–Данло IV типа и артериовенозные мальформации головного мозга. ВА выявляются у 5–40% пациентов с аутосомно–доминантной поликистозной болезнью почек [3,7], причем в 10–30% случаев эти аневризмы множественные [3]. При наличии ВА у двух близких родственников и всем больным с поликистозной болезнью почек показан скрининг – проведение магнитно–резонансной внутричерепной ангиографии [3,8,9]. Если пациент страдает поликистозной болезнью почек, ему рекомендуют повторный скрининг, хотя окончательно необходимость его повторного проведения определяется в зависимости от того, есть ли ВА у родственников [8].
Частота субарахноидальных кровоизлияний (СК) вследствие разрыва ВА в США составляет примерно 1:10000. Разрывом аневризмы обусловлено около 27000 СК в год [3,5], которые чаще наблюдаются у женщин, чем у мужчин (2:1) [10], достигая максимума в возрасте 55–60 лет [11]. С разрывом внутричерепных аневризм связывают 5–15% инсультов [12]. Смертность к 30–му дню от момента возникновения СК из аневризмы (одна из разновидностей геморрагического инсульта) достигает 45%, а 30% выживших становятся инвалидами [13].
Причины, способствующие появлению, росту и разрыву аневризм, изучены достаточно плохо; по–видимому, ключевую роль играют артериальная гипертония и спровоцированные курением изменения сосудистой стенки [3]. Гистологически выявляется истончение tunica media (средней оболочки артерии). В комбинации с гемодинамическими изменениями структурные дефекты вызывают локальное аневризматическое расширение участка артерии, которое «выпячивается» в субарахноидальное пространство в области основания мозга (рис. 1) [3].
Клиническое течение
аневризм и риск разрыва
Наиболее часто ВА манифестируют при разрывах, что проявляется симптомами СК [11]. В настоящее время благодаря большей доступности высокочувствительных неинвазивных методов визуализации аневризмы можно диагностировать и до разрыва. Неразорвавшаяся аневризма может протекать бессимптомно, и обнаруживают ее при случайном обследовании, или же она вызывает развитие клинической симптоматики, обусловленной наличием объемного образования в полости черепа (паралич черепных нервов или признаки сдавления ствола мозга) [6]. Одним из характерных симптомов является внезапный паралич III пары черепных нервов, возникающий на фоне увеличения размеров аневризмы задней соединительной артерии [3].
СК вследствие разрыва аневризм зачастую рецидивируют. В 2–4% случаев повторное кровоизлияние происходит в первые 24 часа, а в 15–20% – в первые две недели [11]. При наличии неврологической симптоматики (паралич черепных нервов, нарушение деятельности ствола мозга) риск разрыва аневризмы особенно велик (до 6% в год), поэтому таких пациентов необходимо регулярно обследовать и лечить [6]. Риск разрыва случайно обнаруженной ВА, из которой не было кровотечения, существенно ниже, поэтому они не требуют непрерывного наблюдения. Раньше считалось, что для любой внутричерепной аневризмы характерен высокий риск разрыва – 1–2% в год [15–18]. До появления микроспиралей для предотвращения разрыва ВА в большинстве случаев предпочитали клипировать хирургическим путем.
Но после опубликования в 1998 г. результатов ретроспективного исследования, проведенного на базе 53 медицинских учреждений и включившего анализ историй болезни 2621 пациента, традиционные представления о риске разрыва ВА изменились [1]. Выяснилось, что в когорте больных с неразорвавшимися аневризмами, отобранными для консервативного лечения, частота разрывов небольших (до 10 мм в диаметре) аневризм не превышала 0,05% в год. Среди пациентов с анамнестическими кровотечениями из аневризмы риск кровоизлияния оказался в 10 раз выше по сравнению с испытуемыми без кровотечений в анамнезе. Риск разрыва крупных аневризм (10 и более мм в диаметре), аневризм сосудов основания мозга и аневризм задней соединительной артерии еще больше. Аналогичные данные были получены при проведении проспективного этапа исследования (Международное исследование по неразорвавшимся ВА), в котором было задействовано 1692 пациента, отобранных для консервативной терапии. Однако стратификация носила несколько иной характер: за пятилетний срок наблюдений разрывов небольших (до 7 мм в диаметре) аневризм – а больных с такими аневризмами оказалось 62% – вообще не было [2]. Однако результаты этого многоцентрового исследования нельзя считать достаточно объективными, поскольку изначально лица, принявшие участие в нем, были отсеяны хирургами, как подлежащие динамическому наблюдению вследствие невысокого риска разрыва аневризмы [22,23]. Дальнейшие испытания выявили больший риск разрыва ВА [24,25].
Диагностика и тактика лечения
субарахноидальных кровоизлияний
Клиническая картина и диагностика
В большинстве случаев при СК возникают внезапные необычайно интенсивные головные боли, описываемые пациентом, как «сильнейшая головная боль в моей жизни». Однако еще до начала лечения около 10% больных погибают, многие впадают в кому, у других развивается тяжелая неврологическая симптоматика [5]. Неврологический статус оценивается по специальным критериям, которые позволяют достаточно точно спрогнозировать исход, например, по классификации Ханта и Хесса (табл. 1) [26,27]. При подозрении на СК диагностическим методом выбора остается компьютерная томография (КТ) без введения контрастного вещества. При проведении КТ без контрастного усиления объем кровопотери оценивается по 4–балльной шкале Фишера, значения показателей которой коррелируют с выраженностью вазоспазма [28]. В 5% случаев, когда КТ не выявляет патологических изменений, выполняется люмбальная пункция, даже несмотря на симптомы СК [11]. Наличие примеси крови в спинномозговой жидкости, которая не осаждается при отстаивании, может свидетельствовать о СК. Ксантохромия (желтоватое окрашивание спинномозговой жидкости), обусловленная разрушением гемоглобина и появлением билирубина, даже более патогномонична, чем наличие крови. Если СК произошло более чем за 12 часов до проведения люмбальной пункции, то будет наблюдаться ксантохромия спинномозговой жидкости, в то время как при свежем кровотечении (например, в случае повреждения сосуда иглой для люмбальной пункции) ксантохромия отсутствует [29].
После окончательной постановки диагноза СК необходимо определить, стал ли его причиной именно разрыв аневризмы. Для этого выбирают наиболее подходящий для данного конкретного случая метод визуализации.
Методы и режимы визуализации
Для выявления ВА, оценки их размеров и морфологических особенностей используют КТ ангиографию (КТА) с внутривенным введением контраста, магнитно–резонансную ангиографию (МРА), ангиографию с прямой катетеризацией артерии (катетеризационная ангиография), которая до сих пор считается точкой отсчета. В ряде исследований проводилось сравнительное изучение диагностических возможностей КТА, МРА, КТА + МРА и катетеризационной ангиографии и/или интраоперационной визуализации ВА [30–35].
КТА позволяет получить оцифрованное трехмерное изображение сосудов головного мозга, построенное на основе тонких срезов благодаря КТ с контрастным усилением. Такое изображение, реконструируемое всего за несколько минут, можно ротировать и оценить расположение сосудов относительно структур головного мозга и основания черепа, что позволяет определить хирургическую тактику. При диагностике ВА чувствительность КТА составляет 0,77–0,97, а специфичность – 0,87–1,00 [12,30,31,33,36,37]. В случае небольшого размера аневризм чувствительность этого метода резко снижается: так, если диаметр аневризмы меньше 3 мм, то чувствительность КТА не превышает 0,4–0,91 [30,32,38]. Поскольку при проведении КТА вводится большой объем контраста, у пациентов с нарушенной функцией почек этот метод визуализации надо применять с осторожностью.
Выполнение МРА занимает гораздо больше времени, чем КТА (от 30 до 60 мин.), и поэтому использовать ее в ургентной ситуации нецелесообразно. При диагностике ВА МРА характеризуется высокой чувствительностью (0,69–0,99) и специфичностью (1,00) [12,33,35,36]. В случае мелких аневризм чувствительность МРА может снижаться до 0,38 [28].
В 1998 г. была апробирована технология трехмерной катетеризационной ангиографии, позволяющей ротировать отформатированное изображение. Основное преимущество этого метода, получившего название трехмерной катетеризационной ангиографии, перед двухмерной катетеризационной ангиографией заключается в том, что она дает возможность оценить положение аневризмы относительно кровеносных сосудов в трех измерениях, делая изображение более информативным [39,40]. Катетеризационная ангиография, с возможностью трехмерной реконструкции или без нее, является более дорогостоящим и более инвазивным исследованием, чем МРА или КТА. Учитывая, какую опасность для жизни больного представляют ВА, степень риска осложнений этого метода обследования, особенно если его проводит опытный специалист, весьма мала (неврологические осложнения встречаются в 1–2,5% случаев, а стойкая симптоматика сохраняется у 0,1–0,5% больных) [41–44]. Прочие осложнения – повреждения стенки бедренной артерии (0,05–0,55%), гематома в паху (6,9–10,7%), нарушение функций почек на фоне введения контрастного вещества и аллергические реакции (1–2%) – обычно носят транзиторный характер [45]. У пациентов пожилого возраста с атеросклерозом чаще встречаются тромбоэмболии, а при нарушении функций почек – нефротоксические явления [3].
Клинические аспекты визуализации
Катетеризационная ангиография высокого разрешения обладает большой точностью, а потому является методом выбора для диагностики СК [12], хотя раньше таким методом считалась КТА [41]. Для диагностики неразорвавшихся аневризм на первом этапе рекомендуется использовать малоинвазивные КТА и МРА.
При наличии СК в 10–20% случаев с помощью ангиографии аневризму обнаружить не удается. Если ангиография дала отрицательные результаты, то через 1–6 недель исследование повторяют [26,46]. Этиология СК при отсутствии верифицированной аневризмы неизвестна. Одним из гипотетических механизмов может быть разрыв мелкой артерии или вены, вызванный резким подъемом давления. Для исключения тромбоза аневризмы, кровотечения из опухоли, артерио–венозных мальформаций спинного мозга и дуральных артерио–венозных фистул при первом посещении врача проводится МРТ головного и шейного отдела спинного мозга с контрастным усилением, хотя в этих случаях ее диагностическая ценность невелика.
Непосредственные исходы
субарахноидальных кровоизлияний
У 15–20% пациентов на фоне СК развивается гидроцефалия [11]. Тактика лечения при симптоматической гидроцефалии – вентрикулостомия с шунтированием спинномозговой жидкости.
Церебральный ангиоспазм – основная причина смертности и инвалидизации пациентов с СК – представляет собой сужение просвета внутричерепных кровеносных сосудов, которое происходит в сроки от 3 до 12 дней с момента кровоизлияния. Причина такого ангиоспазма неизвестна; даже при проведении активной терапии он может спровоцировать инсульт и летальный исход [11]. Диагностировать ангиоспазм помогает неинвазивная транскраниальная допплерография.
Консервативная терапия
Основу медикаментозного лечения составляет нимодипин в таблетках (60 мг каждые 4 часа в течение 21 дня); применение этого препарата улучшает исходы СК [47]. При повышении кровотока в сосудах головного мозга по данным транскраниальной допплерографии или в случае нарастания неврологического дефицита с появлением новой симптоматики начинают так называемую «три–Г терапию» (гипертония, гиперволемия, гемодилюция). Ее задачи – обеспечить поддержание гематокрита на уровне 30% и центрального венозного давления на уровне 8–12 мм рт.ст., а также создать искусственную гипертонию с целью предотвратить или купировать неврологическую симптоматику [5,11,26]. Выраженность неврологического дефицита зачастую зависит от того, бассейн какой артерии пострадал в результате ангиоспазма, и варьирует от незначительного снижения уровня активности до развития гемипарезов. С учетом возможных осложнений три–Г терапии (в частности, нарушения сердечной деятельности) для подтверждения результатов транскраниальной допплерографии может потребоваться катетеризационная ангиография.
Если вновь возникшая неврологическая симптоматика сохраняется достаточно длительно, а ответа на лечение нет, для верификации ангиоспазма срочно проводят катетеризационную ангиографию, после чего выполняют ангиопластику спазмированных сосудов или внутриартериальное введение гладкомышечных спазмолитиков, таких как папаверин [48,49]. В подавляющем большинстве случаев (90–98%) баллонная ангиопластика и введение спазмолитиков способствуют расширению просвета артерии, визуализируемому ангиографически [49,50]. Однако результаты радиографии не всегда коррелируют с улучшением клинической картины. По некоторым данным, неврологический статус улучшается у 61–70% больных, в то время как другие данные свидетельствуют об отсутствии преимуществ такой тактики лечения по сравнению с три–Г терапией [49,51,52].
Нарушение сердечной деятельности после СК встречается достаточно часто и проявляется изменениями на электрокардиограмме (25–100%) [53,54], повышением уровня сердечных ферментов (тропонина – в 17–28% случаев, МВ–изофермента креатинкиназы – в 37% случаев) [53,55–57], а также дисфункцией левого желудочка (8–30%) [58,59]. Возникновение этих симптомов, в совокупности получивших название «оглушенного» миокарда, обусловлено мощным выбросом катехоламинов в ответ на СК. Верифицировать диагноз позволяет резкое снижение фракции выброса в сочетании с ухудшением сократительной способности стенок желудочка, не соответствующее по своей выраженности признакам сосудистой ишемии по данным электрокардиографии [56,59]. Содержание МВ–изофермента креатинкиназы и тропонина обычно повышено, однако по сравнению с истинной ишемией миокарда уровень тропонина в 10 раз ниже [56]. У большинства пациентов состояние «оглушения» миокрада носит транзиторный характер, некроз сердечной мышцы происходит редко и не зависит от сроков начала лечения [53].
Тактика ведения
Существует три подхода к тактике ведения больных с внутричерепными аневризмами: динамическое наблюдение, трепанация черепа с наложением клипсы (клипирование) (рис. 2) и эндовазальная окклюзия аневризмы микроспиралями (эмболизация) (рис. 3). При разрыве аневризмы (I–IV степень по классификации Ханта и Хесса) оперативное лечение проводят как можно раньше, желательно в первые 72 часа. Единого мнения о том, как вести наиболее тяжелых пациентов (V степень по классификации Ханта и Хесса), нет. Поскольку клинический опыт свидетельствует о высокой частоте неблагоприятных исходов несмотря на лечение, таких пациентов предлагают вести консервативно до наступления клинического улучшения. Однако результаты недавних исследований говорят в пользу активной тактики ведения большинства больных и выполнения, например, дренирования желудочков или окклюзии аневризмы путем клипирования или эмболизации [26]. В таких ситуациях, когда ткань головного мозга уже значительно пострадала, более физиологичным считается использование микроспиралей, а не клипс [26].
Бессимптомные аневризмы, аневризмы, обнаруженные при случайном обследовании, наблюдают в динамике или оперируют выборочно в зависимости от желания пациента, а также размера и состояния аневризмы. Динамическое наблюдение подразумевает периодические осмотры лечащего врача и проведение обследования с использованием одного из методов визуализации. Трепанация черепа и клипирование аневризмы проводится под общей анестезией в условиях нейрохирургической операционной. Постоянную клипсу, изготовленную из немагнитного материала, накладывают поперек шейки аневризмы, выключая ее таким образом из циркуляции (рис. 2).
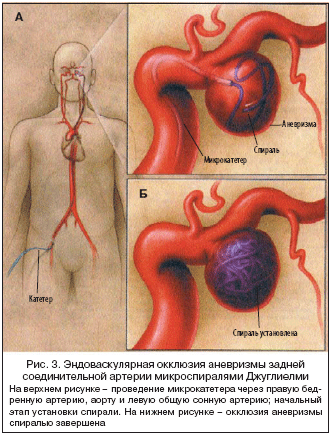
Эндоваскулярную эмболизацию осуществляет интервенционный нейрорадиолог, нейрохирург или невролог, получивший специальную подготовку по интервенционной радиологии [60]. Операцию обычно выполняют под наркозом, хотя в некоторых медицинских учреждениях предпочитают вводить только седативные препараты, что позволяет контролировать неврологический статус пациента в ходе процедуры [61]. Еще одна возможность отследить изменения в неврологическом статусе при проведении эмболизации – нейрофизиологический мониторинг [62]. Под контролем ангиографии к зоне локализации аневризмы подводят микрокатетер, через который в полость аневризмы вводят микроспирали различных размеров и формы, ограничивая или прекращая поступление в нее крови (рис. 3).
Клипирование и эмболизация:
сравнение
Осложнения клипирования
Согласно результатам крупного одноцентрового исследования и данным мета–анализа, показатели заболеваемости и смертности, ассоциированных с клипированием неразорвавшихся аневризм, составляют 4,0–10,9 и 1,0–3,0, соответственно [19–21]. Хотя успешно выполненное клипирование практически исключает вероятность разрыва аневризмы, всегда остается незначительный риск возникновения технических трудностей, неполного закрытия просвета шейки аневризмы (5,2%) [63], ее рецидива (1,5%) и кровотечения (0,26%) [64], о чем свидетельствуют длительные наблюдения.
В ходе международного исследования по неразорвавшимся ВА оценивался риск осложнений, связанных с хирургическим клипированием неразорвавшихся аневризм. Он составил 15,7%, что превышает результаты более ранних исследований [1]. Однако согласно данным другого одноцентрового исследования, значения этого показателя составили 3–7% [6]. Как бы то ни было, результаты международного исследования по неразорвавшимся внутричерепным аневризмам в значительной степени изменили подходы к тактике ведения неразорвавшихся аневризм [65,66]. Большинство пациентов с аневризмами теперь наблюдают в динамике. Рекомендации по тактике ведения неразорвавшихся внутричерепных аневризм сформулированы экспертами Комитета по инсультам Американской кардиологической ассоциации в 2000 г. [12].
Осложнения эмболизации
Введение в полость аневризмы микроспиралей ассоциировано с развитием аллергических реакций на контрастный материал, появлением гематомы в паху и псевдоаневризм, инфицированием, то есть тех же самых осложнений, которые характерны для катетеризационной ангиографии, однако их риск минимален [67]. Наиболее велика вероятность прободения стенки артерии (0,7%), окклюзии несущей артерии (2%) и тромбоэмболии (2,4%) [68]. Одно из самых опасных осложнений – интраоперационный разрыв аневризмы в процессе подведения к ней катетера или установки микроспирали. Частота встречаемости этого осложнения составляет от 1,4 до 2,7%, а смертность достигает 30–40% [68–70]. По данным другого исследовательского центра, риск интраоперационного разрыва аневризмы ниже (1%), при этом заболеваемость составляет 17%, а смертность – 0%. По–видимому, это объясняется все более широким внедрением технологии эмболизации в клиническую практику с момента их утверждения FDA в 1995 г. [71]. В среднем же значения показателей интраоперационной заболеваемости и смертности в ходе проведения эмболизации находятся в пределах 3,7–5,3% и 1,1–1,5% соответственно [72,73]. В 5–14,5% случаев осуществить эмболизацию не удается [68,74] из–за чрезмерной извитости сосудов, что затрудняет доступ к аневризме, или из–за формы самой аневризмы.
Внедрение современных технологических новинок, в том числе микроспиралей, которые можно вводить в атипичные по морфологии аневризмы, баллонов [75] и внутричерепных стентов, применяемых с 2002 г. (рис. 4) [76,77], заметно снизило количество случаев, когда проведение эмболизации по стандартной методике невозможно. Следует отметить, что частичная окклюзия чаще происходит после эмболизации, чем хирургического клипирования. Согласно результатам трехцентрового исследования, к которому было привлечено 2868 пациентов с прооперированными путем эмболизации внутричерепными аневризмами, успешная окклюзия по данным ангиографии (закрытие аневризмы на 90–95% или визуализация только ее шейки) наблюдается в 85–90,4% случаев. Окклюзия более крупных аневризм или аневризм с широкими шейками происходит менее успешно [68,72,78].
Аневризмы, прооперированные с использованием микроспиралей, могут рецидировать, и в случае рецидива возникает опасность кровотечения. Со временем микроспираль сдавливается током крови внутри аневризмы. Этот процесс получил название компресии. В результате аневримзма вновь начинает заполняться кровью, т.е. происходит ее реканализация (рис. 4). Реканализация встречается в 20,9–33,6% случаев [79]. Неизвестно, значима ли реканализация клинически; также непонятно, предотвращает ли реканализацию частичная эмболизация. Чтобы подтвердить факт реканализации аневризмы, проводят контрольную ангиографию [78,79], поскольку в этих ситуациях может быть показана повторная эмболизация, являющаяся достаточно безопасной процедурой (из 53 повторных эмболизаций не было зафиксировано ни одного осложнения) [80]. Таким образом, риск кровотечения из аневризмы, прооперированной с использованием микроспиралей, выше, чем из клипированной аневризмы, но все же остается очень низким; при наблюдении на протяжении 31,32±24,96 месяцев в среднем он составляет, по данным крупного исследования, 0,8% [79].
Одним из перспективных решений проблемы реканализации аневризмы после эмболизации является применение биологически активных микроспиралей, импрегнированных соединениями, взаимодействующими с эндотелием сосудов и формирующими коллагеновую массу, которая закрывает вход в аневризму [81]. Опыты на животных свидетельствуют о том, что использование микроспиралей нового поколения [77,82], расширяющихся при введении в полость аневризмы (что обеспечивает более плотное расположение петель), снижает вероятность компрессии [83]. Еще одна возможность избежать реканализацию – применение гибких саморасширяющихся нитиноловых стентов (стент Neuroform, Target Therapeutics/Boston Scientific), устанавливаемые с помощью микрокатетера (рис. 4). Такие внутричерепные стенты, недавно одобренные FDA, устанавливают в артерию, от которой отходит аневризма, тем самым обтурируя ее [76,77].
Относительный риск осложнений
эмболизации и клипирования
Согласно результатам сразу нескольких ретроспективных исследований [84–86], по меньшей мере в раннем послеоперационном периоде использование микроспиралей в хирургии разорвавшихся и неразорвавшихся ВА более безопасно, чем клипирование, даже несмотря на возможность развития осложнений, связанных с установкой микроспиралей. При анализе баз данных консорциума 60 университетов, входящих в систему институтов охраны здоровья США [86], базы данных больниц по штату Калифорния [85] и базы данных госпиталя Калифорнийского университета в Сан–Франциско [84] выяснилось, что исходы клипирования хуже, чем эмболизации. Кроме того, применение микроспиралей позволяет снизить больничную летальность, уменьшить сроки госпитализации и сократить затраты на лечение [84–86].
Самые убедительные доказательства большей безопасности микроспиралей по сравнению с клипсами в хирургии аневризм, манифестирующих СК, были получены после завершения крупного многоцентрового проспективного исследования, проводившегося в Англии [87]. В ходе международного исследования по субарахноидальным аневризмам 2143 пациента были рандомизированы для выполнения клипирования или эмболизации [88]. Плановый промежуточный анализ, проведенный комиссией по мониторингу данных, показал, что в той группе, где выполнялось эндоваскулярное вмешательство, неврологическая симптоматика и даже летальные исходы регистрировались с частотой 23,7% против 30,6% в группе прооперированных открытым способом. Исследование было досрочно прекращено, поскольку уже не вызывало сомнений, что относительный (22,6%) и абсолютный (6,9%) риск развития неврологической симптоматики и летальных исходов после эмболизации ниже, чем после клипирования. Эти данные были получены в течение года до прекращения исследования [88].
Результаты указанного исследования в значительной степени изменили взгляды на тактику лечения внутричерепных аневризм [89,90]. Выводы исследования были обсуждены на заседании Американского общества интервенционной и терапевтической нейрорадиологии [91] и Американской нейрохирургической ассоциации [92], итогом чего стало опубликование программного документа и изменение рекомендаций по ведению таких пациентов [89,90]. Следует, однако, упомянуть и о недостатках этого исследования. Так, в нем было задействовано 9559 пациентов с СК, спровоцированными разрывами аневризм, однако критериям включения соответствовала лишь часть больных, которые и были отобраны на эмболизацию или клипирование. Рандомизации было подвергнуто только 2143 человека (22,4%). У большинства испытуемых (более 90%) отмечалось благоприятное клиническое течение аневризм, их источником служили преимущественно сосуды передних отделов головного мозга, и примерно в 95% случаев аневризмы имели диаметр меньше 10 мм. Приняв во внимание результаты международного исследования по субарахноидальным аневризмам, эксперты Американского общества интервенционной и терапевтической нейрорадиологии сформулировали следующие рекомендации: всех пациентов с разорвавшимися внутричерепными аневризмами следует проконсультировать у специалиста, владеющего техникой установки микроспиралей [91]. Американская нейрохирургическая ассоциация предложила рассматривать хирургическое клипирование как метод выбора, если квалифицированный сосудистый нейрохирург считает его наиболее целесообразным для данного конкретного пациента [92].
Объем выполненных хирургических вмешательств и его влияние
на исходы операции
Анализ исходов оперативного лечения аневризм отдельно взятым хирургом, интервенционным радиологом или в конкретном медицинском учреждении свидетельствует о том, что чем больше процедур провел специалист, тем лучше результаты [93–96]. Сообщения в основном сделаны врачами, которые выполнили большой объем вмешательств. Вероятность благоприятного исхода выше у хирургов, проводящих более 30 трепанаций черепа по поводу аневризмы в год [97]. Поэтому некоторые аналитики предлагают осуществить регионализацию оперативного лечения ВА.
Выбор оптимальной
тактики лечения аневризм
Четких рекомендаций по выбору оптимальной тактики лечения разорвавшихся и неразорвавшихся ВА нет. Согласно сведениям научной литературы, необходимо принимать во внимание показания как к клипированию, так и к эмболизации. В некоторых случаях равнозначны оба метода, и тогда решение принимают с учетом, например, пожеланий пациента или опыта и квалификации хирурга.
Выбор тактики ведения конкретного пациента с ВА – динамическое наблюдение, хирургическое вмешательство на открытом черепе или эндоскопическая процедура – также активно дискутируется. Разорвавшуюся аневризму оперируют по экстренным показаниям, чтобы не допустить смертельно опасного рецидива кровотечения; в этом случае более целесообразна эмболизация, как менее инвазивный метод. Проводить хирургическое вмешательство по поводу ВА, выявленной при случайном обследовании, необязательно. Также предстоит установить, компенсирует ли более длительный срок службы клипс тот высокий риск, с которым сопряжено клипирование по сравнению с эмболизацией.
Эндоваскулярные вмешательства, хотя и проводятся пока реже, выводят технологии хирургического лечения ВА на качественно новый этап. Уже идущие клинические испытания, такие как международное исследование по субарахноидальным аневризмам и международное исследование по неразорвавшимся внутричерепным аневризмам, а также рандомизированные испытания, запланированные на будущее и ставящие целью сравнить клипирование и эмболизацию с клинической точки зрения, помогут не только пролить свет на клиническое течение ВА, но и просчитать риск осложнений и преимущества различных подходов к тактике ведения таких больных, будь то динамическое наблюдение, эмболизация или клипирование.
Реферат подготовлен Е.Б. Третьяк
по материалам статьи
J.L. Brisman, J.K. Song, D. Newell
«Cerebral Aneurysms»
The New England Journal of Medicine
Vol. 355, No. 9, August 2006




Литература
1. The International Study of Unruptured Intracranial Aneurysm Investigators. Unruptured intracranial aneurysms Ч risk of rupture and risks of surgical intervention. N Engl J Med 1998;339:1725–33. [Erratum, N Engl J Med 1999;340:744J
2. Wiebers DO, Whisnant JP, Huston J III, et al. Unruptured intracranial aneurysms: natural history, clinical outcome, and risks of surgical and endovascular treatment. Lancet 2003;362:103–10.
3. Schievink WI. Intracranial aneurysms. N Engl J Med 1997;336:28–40. [Erratum, N Engl J Med 1997;336:1267J
4. Endovascular repair of intracranial aneurysms. Medtech Insight. Vol. 7. No. 2. February 2005:47–52 (newsletter).
5. Wijdicks EF, Kallmes DF, Manno EM, Fulgham JR, Piepgras DG. Subarachnoid hemorrhage: neurointensive care and aneurysm repair. Mayo Clin Proc 2005;80: 550–9.
6. Connolly ES, Solomon RA. Management of unruptured aneurysms. In: Le Roux PD, Winn HR, Newell DW, eds. Management of cerebral aneurysms. Philadelphia: Saunders, 2004:271–85.
7. Yanaka K, Nagase S, Asakawa H, Mat–sumaru Y, Koyama A, Nose T. Management of unruptured cerebral aneurysms in patients with polycystic kidney disease. Surg Neurol 2004;62:538–45.
8. Butler WE, Barker FG II, Crowell RM.
Patients with polycystic kidney disease would benefit from routine magnetic resonance angiographic screening for intracerebral aneurysms: a decision analysis. Neurosurgery 1996;38:506–15.
9. The Magnetic Resonance Angiography in Relatives of Patients with Subarachnoid Hemorrhage Study Group. Risks and benefits of screening for intracranial aneurysms in first–degree relatives of patients with sporadic subarachnoid hemorrhage. N Engl J Med 1999;341:1344–50.
10. Stapf C, Mohr JP. Aneurysms and subarachnoid hemorrhage Ч epidemiology. In: Le Roux PD, Winn HR, Newell DW, eds. Management of cerebral aneurysms. Philadelphia: Saunders, 2004:183–7.
11. Greenberg MS. SAH and aneurysms. In: Greenberg MS, ed. Handbook of neurosurgery. 5th ed. New York: Thieme Medical, 2000:754–803.
12. Bederson JB, Awad IA, Wiebers DO, et al. Recommendations for the management of patients with unruptured intracranial aneurysms: a statement for healthcare professionals from the Stroke Council of the American Heart Association. Stroke 2000;31:2742–50.
13. Johnston SC, Selvin S, Gress DR. The burden, trends, and demographics of mortality from subarachnoid hemorrhage. Neurology 1998;50:1413–8.
14. Wiebers DO, Whisnant JP, Sundt TM
Jr, O’Fallon WM. The significance of unruptured intracranial saccular aneurysms. J Neurosurg 1987;66:23–9.
15. Juvela S, Porras M, Heiskanen O. Natural history of unruptured intracranial aneurysms: a long–term follow–up study. J Neurosurg 1993;79:174–82.
16. Wiebers DO, Whisnant JP, O’Fallon WM. The natural history of unruptured intracranial aneurysms. N Engl J Med 1981;304:696–8.
17. Mount LA, Brisman R. Treatment of multiple aneurysms Ч symptomatic and asymptomatic. Clin Neurosurg 1974;21: 166–70.
18. Winn HR, Almaani WS, Berga SL, Jane JA, Richardson AE. The long–term outcome in patients with multiple aneurysms: incidence of late hemorrhage and implications for treatment of incidental aneurysms. J Neurosurg 1983;59:642–51.
19. Raaymakers TW, Rinkel GJ, Limburg M, Algra A. Mortality and morbidity of surgery for unruptured intracranial aneurysms: a meta–analysis. Stroke 1998;29: 1531–8.
20. KingJTJr, Berlin JA, Flamm ES. Morbidity and mortality from elective surgery for asymptomatic, unruptured, intracranial aneurysms: a meta–analysis. J Neurosurg 1994;81:837–42.
21. Solomon RA, Fink ME, Pile–Spellman J. Surgical management of unruptured
intracranial aneurysms. J Neurosurg 1994; 80:440–6.
22. Kobayashi S, Orz Y, George B, et al. Treatment of unruptured cerebral aneurysms. Surg Neurol 1999;51:355–62.
23. Ausman JI. The New England Journal of Medicine report on unruptured intracranial aneurysms: a critique. Surg Neurol 1999;51:227–9.
24. Tsutsumi K, Ueki K, Morita A, Kirino T. Risk of rupture from incidental cerebral aneurysms. J Neurosurg 2000;93:550–3.
25. Juvela S, Porras M, Poussa K. Natural history of unruptured intracranial aneurysms: probability of and risk factors for aneurysm rupture. J Neurosurg 2000;93: 379–87.
26. Le Roux PD, Winn HR. Management of the ruptured aneurysm. In: Le Roux PD, Winn HR, Newell DW, eds. Management of cerebral aneurysms. Philadelphia: Saunders, 2004:303–33.
27. Hunt WE, Hess RM. Surgical risk as related to time of intervention in the repair of intracranial aneurysms. J Neurosurg 1968;28:14–20.
28. Fisher CM, Kistler JP, Davis JM. Relation of cerebral vasospasm to subarachnoid hemorrhage visualized by computerized tomographic scanning. Neurosurgery 1980;6:1–9.
29. Edlow JA, Caplan LR. Avoiding pitfalls in the diagnosis of subarachnoid hemorrhage. N Engl J Med 2000;342:29–36.
30. Dammert S, Krings T, Moller–Hart–mann W, et al. Detection of intracranial aneurysms with multislice CT: comparison with conventional angiography. Neuroradiology 2004;46:427–34.
31. Chappell ET, Moure FC, Good MC. Comparison of computed tomographic angiography with digital subtraction angiography in the diagnosis of cerebral aneurysms: a meta–analysis. Neurosurgery 2003;52:624–31.
32. White PM, Wardlaw JM, Easton V. Can noninvasive imaging accurately depict intracranial aneurysms? A systematic review. Radiology 2000;217:361–70.
33. White PM, Teasdale EM, Wardlaw JM, Easton V. Intracranial aneurysms: CT angiography and MR angiography for detection prospective blinded comparison in a large patient cohort. Radiology 2001;219: 739–49.
34. Kouskouras C, Charitanti A, Giavro–glou C, et al. Intracranial aneurysms: evaluation using CTA and MRA: correlation with DSA and intraoperative findings. Neuroradiology 2004;46:842–50.
35. Okahara M, Kiyosue H, Yamashita M, et al. Diagnostic accuracy of magnetic resonance angiography for cerebral aneurysms in correlation with 3D–digital subtraction angiographic images: a study of 133 aneurysms. Stroke 2002;33:1803–8.
36. Harrison MJ, Johnson BA, Gardner GM, Welling BG. Preliminary results on the management of unruptured intracra–
nial aneurysms with magnetic resonance angiography and computed tomographic angiography. Neurosurgery 1997;40:947–55.
37. Kangasniemi M, Makela T, Koskinen S, Porras M, Poussa K, Hernesniemi J. Detection of intracranial aneurysms with two–dimensional and three–dimensional multislice helical computed tomographic angiography. Neurosurgery 2004;54:336–40.
38. Tipper G, U–King–Im JM, Price SJ, et al. Detection and evaluation of intracranial aneurysms with 16–row multislice CT angiography. Clin Radiol 2005;60:565–72.
39. Anxionnat R, Bracard S, Ducrocq X, et al. Intracranial aneurysms: clinical value of 3D digital subtraction angiography in the therapeutic decision and endovascular treatment. Radiology 2001;218:799–808.
40. Tanoue S, Kiyosue H, Kenai H, Naka–mura T, Yamashita M, Mori H. Three–dimensional reconstructed images after rotational angiography in the evaluation of intracranial aneurysms: surgical correlation. Neurosurgery 2000;47:866–71.
41. Hoh BL, Cheung AC, Rabinov JD, Pryor JC, Carter BS, Ogilvy CS. Results of a prospective protocol of computed tomographic angiography in place of catheter angiography as the only diagnostic and pretreatment planning study for cerebral aneurysms by a combined neurovascular team. Neurosurgery 2004;54:1329–40.
42. Heiserman JE, Dean BL, Hodak JA, et al. Neurologic complications of cerebral angiography. AJNR Am J Neuroradiol 1994;15:1401–7.
43. Dion JE, Gates PC, Fox AJ, Barnett HJ, Blom RJ. Clinical events following neuro–angiography: a prospective study. Stroke 1987;18:997–1004.
44. Connors JJ III, Sacks D, Furlan AJ, et al. Training, competency, and credential–ing standards for diagnostic cervicocere–bral angiography, carotid stenting, and cerebrovascular intervention: a joint statement from the American Academy of Neurology, the American Association of Neurological Surgeons, the American Society of Interventional and Therapeutic Neuroradiology, the American Society of Neuroradiology, the Congress of Neurological Surgeons, the AANS/CNS Cerebrovascular Section, and the Society of Interventional Radiology. Neurology 2005;64:190–8.
45. Morris P. Practical neuroangiography. Baltimore: Williams & Wilkins, 1997.
46. van Gijn J, Rinkel GJ. Subarachnoid haemorrhage: diagnosis, causes and management. Brain 2001;124:249–78.
47. Barker FG II, Ogilvy CS. Efficacy of prophylactic nimodipine for delayed ischemic deficit after subarachnoid hemorrhage: a metaanalysis. J Neurosurg 1996; 84:405–14.
48. Elliott JP, Newell DW, Lam DJ, et al. Comparison of balloon angioplasty and papaverine infusion for the treatment of
vasospasm following aneurysmal subarachnoid hemorrhage. J Neurosurg 1998; 88:277–84.
49. Rosenwasser RH, Armonda RA, Thomas JE, Benitez RP, Gannon PM, Har–rop J. Therapeutic modalities for the management of cerebral vasospasm: timing of endovascular options. Neurosurgery 1999; 44:975–9.
50. Rabinstein AA, Friedman JA, Nichols DA, et al. Predictors of outcome after endovascular treatment of cerebral vasospasm. AJNR Am J Neuroradiol 2004;25: 1778–82.
51. Polin RS, Coenen VA, Hansen CA, et al. Efficacy of transluminal angioplasty for the management of symptomatic cerebral vasospasm following aneurysmal subarachnoid hemorrhage. J Neurosurg 2000; 92:284–90.
52. Eskridge JM, McAuliffe W, Song JK, et al. Balloon angioplasty for the treatment of vasospasm: results of first 50 cases. Neurosurgery 1998;42:510–6.
53. Zaroff JG, Rordorf GA, Newell JB, Ogilvy CS, Levinson JR. Cardiac outcome in patients with subarachnoid hemorrhage and electrocardiographic abnormalities. Neurosurgery 1999;44:34–9.
54. Jain R, Deveikis J, Thompson BG. Management of patients with stunned myocardium associated with subarachnoid hemorrhage. AJNR Am J Neuroradiol 2004;25:126–9.
55. Deibert E, Barzilai B, Braverman AC, et al. Clinical significance of elevated troponin I levels in patients with nontraumatic subarachnoid hemorrhage. J Neurosurg 2003;98:741–6.
56. Bulsara KR, McGirt MJ, Liao L, et al. Use of the peak troponin value to differentiate myocardial infarction from reversible neurogenic left ventricular dysfunction associated with aneurysmal subarachnoid hemorrhage. J Neurosurg 2003;98:524–8.
57. Tung P, Kopelnik A, Banki N, et al. Predictors of neurocardiogenic injury after subarachnoid hemorrhage. Stroke 2004; 35:548–51.
58. Khush K, Kopelnik A, Tung P, et al. Age and aneurysm position predict patterns of left ventricular dysfunction after subarachnoid hemorrhage. J Am Soc Echo–cardiogr 2005;18:168–74.
59. Zaroff JG, Rordorf GA, Ogilvy CS, Picard MH. Regional patterns of left ventricular systolic dysfunction after subarachnoid hemorrhage: evidence for neu–rally mediated cardiac injury. J Am Soc Echocardiogr 2000;13:774–9.
60. Friedman DP, Maitino AJ. Endovascular interventional neuroradiologic procedures: who is performing them, how often, and where? A survey of academic and non–academic radiology practices. AJNR Am J Neuroradiol 2003;24:1772–7.
61. Qureshi Al, Suri MF, Khan J, et al. Endovascular treatment of intracranial aneurysms by using Guglielmi detachable
coils in awake patients: safety and feasibility. J Neurosurg 2001;94:880–5.
62. Liu AY, Lopez JR, Do HM, Steinberg GK, Cockroft K, Marks MP. Neurophysi–ological monitoring in the endovascular therapy of aneurysms. AJNRAm J Neuro–radiol 2003;24:1520–7.
63. Thornton J, Bashir Q, Aletich VA, De–brun GM, Ausman JI, Charbel FT. What percentage of surgically clipped intracranial aneurysms have residual necks? Neurosurgery 2000;46:1294–8.
64. David CA, Vishteh AG, Spetzler RF, Lemole M, Lawton MT, Partovi S. Late angiographic follow–up review of surgically treated aneurysms. J Neurosurg 1999;91: 396–401.
65. Tummala RP, Baskaya MK, Heros RC. Contemporary management of incidental intracranial aneurysms. Neurosurg Focus 2005;18(l):e9.
66. Johnston SC, Higashida RT, Barrow DL, et al. Recommendations for the endovascular treatment of intracranial aneurysms: a statement for healthcare professionals from the Committee on Cerebrovascular Imaging of the American Heart Association Council on Cardiovascular Radiology. Stroke 2002;33:2536–44.
67. Friedman JA, Nichols DA, Meyer FB, et al. Guglielmi detachable coil treatment of ruptured saccular cerebral aneurysms: retrospective review of a 10–year single–center experience. AJNRAm J Neuroradiol 2003;24:526–33.
68. Murayama Y, Nien YL, Duckwiler G, et al. Guglielmi detachable coil embolization of cerebral aneurysms: 11 years, experience. J Neurosurg 2003;98:959–66.
69. Tummala RP, Chu RM, Madison MT, Myers M, Tubman D, Nussbaum ES. Outcomes after aneurysm rupture during endovascular coil embolization. Neurosurgery 2001;49:1059–66.
70. Cloft HJ, Kallmes DF. Cerebral aneurysm perforations complicating therapy with Guglielmi detachable coils: a metaanalysis. AJNRAm J Neuroradiol 2002;23: 1706–9.
71. Brisman JL, Niimi Y, Song JK, Beren–stein A. Aneurysmal rupture during coiling: low incidence and good outcomes at a single large volume center. Neurosurgery 2005;57:1103–9.
72. Henkes H, Fischer S, Weber W, et al. Endovascular coil occlusion of 1811 intracranial aneurysms: early angiographic and clinical results. Neurosurgery 2004;54: 268–80.
73. Brilstra EH, Rinkel GJ, van der Graaf Y, van Rooij WJ, Algra A. Treatment of intracranial aneurysms by embolization with coils: a systematic review. Stroke 1999;30: 470–6.
74. Shanno GB, Armonda RA, Benitez RP,
Rosenwasser RH. Assessment of acutely unsuccessful attempts at detachable coiling in intracranial aneurysms. Neurosurgery 2001;48:1066–72.
75. Moret J, Cognard C, Weill A, Castaings L, Rey A. Reconstruction technic in the treatment of wide–neck intracranial aneurysms: long–term angiographic and clinical results: apropos of 56 cases. J Neuroradiol 1997;24:30–44. (In French.)
76. Lylyk P, Ferrario A, Pasbon B, Miranda C, Doroszuk G. Buenos Aires experience with the Neuroform self–expanding stent for the treatment of intracranial aneurysms. J Neurosurg 2005;102:235–41.
77. Brisman JL, Song JK, Niimi Y, Beren–stein A. Treatment options for wide–necked intracranial aneurysms using a self–expandable hydrophilic coil and a self–expandable stent combination. AJNR Am J Neuroradiol 2005;26:1237–40.
78. Thornton J, Debrun GM, Aletich VA, Bashir Q, Charbel FT, Ausman J. Follow–up angiography of intracranial aneurysms treated with endovascular placement of Guglielmi detachable coils. Neurosurgery 2002;50:239–49.
79. Raymond J, Guilbert F, Weill A, et al. Long–term angiographic recurrences after selective endovascular treatment of aneurysms with detachable coils. Stroke 2003; 34:1398–403.
80. Slob MJ, Sluzewski M, van Rooij WJ, Roks G, Rinkel GJ. Additional coiling of previously coiled cerebral aneurysms: clinical and angiographic results. AJNR Am J Neuroradiol 2004;25:1373–6.
81. Murayama Y, Tateshima S, Gonzalez NR, Vinuela F. Matrix and bioabsorbable polymeric coils accelerate healing of intracranial aneurysms: long–term experimental study. Stroke 2003;34:2031–7.
82. Cloft HJ, Kallmes DF. Aneurysm packing with HydroCoil Embolic System versus platinum coils: initial clinical experience. AJNR Am J Neuroradiol 2004;25: 60–2.
83. Yoshino Y, Niimi Y, Song JK, Silane M, Berenstein A. Endovascular treatment of intracranial aneurysms: comparative evaluation in a terminal bifurcation aneurysm model in dogs. J Neurosurg 2004;101:996–1003.
84. Johnston SC, Wilson CB, Halbach VV, et al. Endovascular and surgical treatment of unruptured cerebral aneurysms: comparison of risks. Ann Neurol 2000;48:11–9.
85. Johnston SC, Zhao S, Dudley RA, Ber–man MF, Gress DR. Treatment of unruptured cerebral aneurysms in California. Stroke 2001;32:597–605.
86. Johnston SC, Dudley RA, Gress DR, Ono L. Surgical and endovascular treatment of unruptured cerebral aneurysms at university hospitals. Neurology 1999; 52:1799–805.
87. Molyneux A, Kerr R, Stratton I, et al. International Subarachnoid Aneurysm Trial (ISAT) of neurosurgical clipping versus endovascular coiling in 2143 patients with ruptured intracranial aneurysms: a randomised trial. Lancet 2002;360:1267–74.
88. Molyneux AJ, Kerr RS, Yu LM, et al. International Subarachnoid Aneurysm Trial (ISAT) of neurosurgical clipping versus endovascular coiling in 2143 patients with ruptured intracranial aneurysms: a randomised comparison of effects on survival, dependency, seizures, rebleeding, subgroups, and aneurysm occlusion. Lancet 2005;366:809–17.
89. Lindsay KW. The impact of the International Subarachnoid Aneurysm Treatment Trial (ISAT) on neurosurgical practice. Acta Neurochir (Wien) 2003;145:97–9.
90. Maurice–Williams RS. Aneurysm surgery after the International Subarachnoid Aneurysm Trial (ISAT). J Neurol Neurosurg Psychiatry 2004;75:807–8.
91. Derdeyn CP, Barr JD, Berenstein A, et al. The International Subarachnoid Aneurysm Trial (ISAT): a position statement from the Executive Committee of the American Society of Interventional and Therapeutic Neuroradiology and the American Society of Neuroradiology. AJNRAm J Neuroradiol 2003;24:1404–8.
92. Harbaugh RE, Heros RC, Hadley MN. Position statement on the International Subarachnoid Aneurysm Trial (ISAT). (Accessed August 4, 2006, at http://www.aans. org/Library/Article.aspx?ArticleId=9703.)
93. Barker FG II, Amin–Hanjani S, Butler WE, Ogilvy CS, Carter BS. In–hospital mortality and morbidity after surgical treatment of unruptured intracranial aneurysms in the United States, 1996–2000: the effect of hospital and surgeon volume. Neurosurgery 2003;52:995–1007.
94. Berman MF, Solomon RA, Mayer SA, Johnston SC, Yung PP. Impact of hospital–related factors on outcome after treatment of cerebral aneurysms. Stroke 2003;34: 2200–7.
95. Bardach NS, Zhao S, Gress DR, Lawton MT, Johnston SC. Association between subarachnoid hemorrhage outcomes and number of cases treated at California hospitals. Stroke 2002;33:1851–6.
96. Johnston SC. Effect of endovascular services and hospital volume on cerebral aneurysm treatment outcomes. Stroke 2000;31:111–7.
97. Solomon RA, Mayer SA, Tarmey JJ. Relationship between the volume of craniotomies for cerebral aneurysm performed at New York state hospitals and in–hospital mortality. Stroke 1996;27:13–7.












