Несмотря на разнонаправленные многолетние исследования, изучение различных аспектов рассеянного склероза (РС) остается актуальной проблемой, медицинская и социальная значимость которой обусловлена высокой частотой встречаемости, заболеваемостью лиц молодого трудоспособного возраста, возможностью быстрого развития стойкой инвалидизации при недостаточной эффективности в ряде случаев существующих терапевтических средств.
На современном этапе наличие унифицированных критериев постановки диагноза РС способствует раннему назначению специфического патогенетического лечения, направленного как на купирование симптомов экзацербации, так и на модулирование течения болезни, что стало возможным благодаря значительному прогрессу в понимании механизмов развития патологического процесса при РС, а также биотехнологическим методам создания новых лекарственных средств.
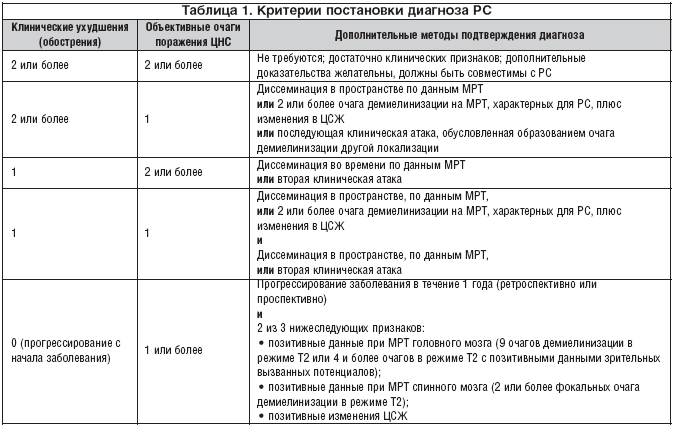
В настоящее время при РС общепринятыми являются критерии постановки диагноза, предложенные W. McDonald и соавт. в 2001 г. и уточненные в 2005 г. [Polman C.H. et al., 2005] (табл. 1).
Согласно представленным в таблице 1 критериям, положительными данными при МРТ считаются 3 из 4 нижеследующих признаков:
• 1 очаг, накапливающий контрастное вещество, в головном или спинном мозге или 9 гиперинтенсивных очагов в режиме Т2 в головном и/или спинном мозга при отсутствии контрастирующихся очагов;
• 1 или более инфратенториальный очаг в головном или в спинном мозге;
• 1 или более юкстакортикальных очага;
• 3 или более перивентрикулярных очага.
Доказательством диссеминации во времени при МРТ считаются:
• наличие накапливающего контрастное вещество очага по меньшей мере через 3 мес. после начала первого клинического ухудшения, расположенного в другом, отличном от первого обострения месте,
или
• в случае наличия нового очага в режиме Т2 при сканировании, сделанном в любое время, относительно исследования, выполненного по меньшей мере через 30 дней после первого клинического ухудшения.
К позитивным изменениям в цереброспинальной жидкости (ЦСЖ) относятся олигоклональные цепи IgG в ЦСЖ (при отсутствии в сыворотке) или повышенный индекс IgG. Положительным изменением зрительных вызванных потенциалов является увеличение латентности волн при сохранности их формы.
Исключение альтернативных диагнозов особенно необходимо при ранних клинических проявлениях заболевания, когда еще нет типичного ремиттирующего течения [Berger T., 2009]. Различные комбинации неврологических симптомов и данных МРТ могут наблюдаться у пациентов при клинически изолированном синдроме (КИС), который в настоящее время определяется как монофазно развившаяся симптоматика, вызванная предположительно воспалительным демиелинизирующим заболеванием. При этом монофазность подразумевает впервые развившийся отдельный клинический эпизод с относительно быстрым началом. Возможно одновременное выявление множественных клинических/параклинических проявлений, однако диссеминация во времени не должна быть очевидной. В связи с этим в современной классификации КИС выделяются следующие варианты: тип 1 — клинически монофокальный; по меньшей мере 1 асимптомный МРТ–очаг; тип 2 – клинически мультифокальный; по меньшей мере 1 асимптомный МРТ–очаг; тип 3 — клинически монофокальный; МРТ может быть без патологии; нет асимптомных МРТ–очагов; тип 4 — клинически мультифокальный; МРТ может быть без патологии; нет асимптомных МРТ–очагов; тип 5 — нет клинических проявлений, предполагающих демиелинизирующее заболевание, но есть наводящие МРТ–данные [Miller D.H. et al., 2008].
Как видно из критериев, приведенных W. McDonald и соавт. (2005), для постановки диагноза РС у пациентов с КИС необходимо подтверждение диссеминации патологического процесса в пространстве и времени. В последующем J.K. Swanton и соавт. (2006) предложили новые МРТ–критерии РС, согласно которым диссеминация в пространстве подтверждается при выявлении одного или более субклинических очагов в режиме Т2, локализующихся по меньшей мере в двух из четырех характерных для РС областей по критериям W. McDonald (юкстакортикальная, перивентрикулярная, инфратенториальная области, а также спинной мозг). В то же время для верификации диссеминации во времени необходимо выявление нового очага в режиме Т2 на более поздних изображениях, независимо от времени проведения более ранней МРТ [Swanton J.K. et al., 2006]. По сравнению с критериями W. McDonald и соавт., эти МРТ–критерии также высокоспецифичны для клинически достоверного РС, более чувствительны и не требуют выявления очагов, накапливающих контрастное вещество; с другой стороны, для подтверждения диссеминации во времени необходимо по меньшей мере двухкратное проведение МРТ–исследования, при этом соблюдение минимального интервала между началом клинических симптомов и МРТ не является необходимым [Swanton J.K. et al., 2007; Tur C. et al., 2008; Rovira A. et al., 2009].
В критериях W. McDonald и соавт. временной интервал в 3 мес. был выбран для исключения острого рассеянного энцефаломиелита (ОРЭМ), обычно монофазного заболевания, при котором, однако, может наблюдаться появление новых очагов на более поздних МРТ во время периода восстановления с наличием смешанного паттерна контрастирующихся и неконтрастирующихся очагов. Однако ОРЭМ редко встречается у взрослых и имеется ряд клинических и МРТ–особенностей, которые могут быть использованы в дифференциальной диагностике ОРЭМ и РС. В связи с этим результаты исследования, представленного A. Rovira и соавт. (2009), послужили основой для концепции, согласно которой одновременное присутствие как накапливающих, так и не накапливающих контрастное вещество очагов в веществе головного мозга на единственной МРТ, выполненной в течение первых 3 мес. после начала КИС, предполагает различные стадии их эволюции и, следовательно, подтверждает диссеминацию во времени. По мнению авторов, данные должны быть приняты во внимание при дальнейшей модификации МРТ–диагностических критериев РС с целью оптимизации исследования в плане «легкости, простоты и стоимости».
Однако учитывая значительные трудности при постановке диагноза РС в атипичных случаях, в НЦН РАМН проведено клинико–морфологическое исследование при псевдотуморозном течении РС и острой очаговой демиелинизации. Наблюдались 43 пациента; из них 32 больным диагноз уточнен на основании гистологического исследования операционного материала, полученного в ходе стереотаксической биопсии или оперативного вмешательства. Были выделены группы с псевдотуморозным моноочаговым процессом, с сочетанием псевдотуморозного очага субклинической многоочаговой демиелинизации, с развитием псевдотуморозного течения при обострении достоверного РС. Одиннадцати пациентам диагноз поставлен в результате проведения комплексного исследования и динамического наблюдения.
Выделены следующие клинические особенности псевдотуморозного течения демиелинизирующего процесса: возраст начала болезни типичен для рассеянного склероза, выявлена одинаковая частота встречаемости у мужчин и у женщин, характерна преимущественно полушарная локализация псевдотуморозного очага с подострым течением заболевания.
При морфологическом исследовании биопсийного и операционного материала были выявлены изменения ткани мозга, характерные для острого очагового демиелинизирующего процесса, основными признаками которого являются деструкция миелиновых волокон белого вещества с уборкой продуктов их распада липофагами, пролиферация и гипертрофия астроцитов, продуцирующих глиальные волокна, воспалительные периваскулярные инфильтраты, состоящие из лимфоцитов, моноцитов и немногочисленных плазматических клеток, гиперемия мелких сосудов и капилляров, отек ткани мозга. Установлено, что распад аксонов в очаге демиелинизации возникает уже на самых ранних этапах развития демиелинизирующего заболевания.
Полученные данные позволили уточнить алгоритм обследования больных с псевдотуморозным типом течения патологического процесса и определенные подходы тактики ведения данных пациентов. Так, при выявлении спорных данных КТ и МРТ в дебюте псевдотуморозного демиелинизирующего заболевания рекомендовано комплексное дообследование пациента, включая выполнение высокопольной МРТ головного мозга, шейного, грудного отделов позвоночника, регистрацию вызванных потенциалов мозга для исключения «диссеминации патологического процесса в пространстве». В случае развития псевдотуморозного варианта течения болезни в рамках КИС при многоочаговом поражении мозга или при достоверном РС целесообразно проведение пульс–терапии метилпреднизолоном и в случае отсутствия реакции на данное лечение показана биопсия. Несмотря на то, что стереотаксическая операция с целью получения биопсии имеет важное диагностическое значение при выявлении псевдотуморозного очага, расширение возможностей обследования данных больных позволяет избежать в ряде случаев ее проведения.
Еще одним атипичным симптомом при РС, как считалось ранее, являются слуховые нарушения. В ходе проведенного анализа кохлеарных нарушений при РС было обследовано 70 пациентов, из которых у 35 отмечались жалобы на снижение слуха; контрольную группу составили 18 чел.
Отмеченными клиническими особенностями слуховых нарушений при РС явился широкий диапазон жалоб, которые варьировали от явлений раздражения, таких как заложенность, шум в ухе, гиперакузия, до явлений выпадения, вплоть до остро возникшей односторонней глухоты. Обращал на себя внимание разнообразный спектр слуховых жалоб: появление слуховых нарушений то с одной, то с другой стороны, сочетание снижения слуха с головокружением, шумом в ухе, а также появление слуховых нарушений в дебюте или при обострении заболевания. Иногда пациенты указывали на какие–либо нарушения слуха только лишь при акцентированном расспросе.
Проведенное комплексное аудиологическое обследование позволило исключить кондуктивную форму тугоухости у большинства обследованных пациентов с РС. Так, по результатам аудиометрии, как тональной пороговой, так и в расширенном диапазоне частот (высокочастотной), у пациентов с РС с кохлеарными жалобами на стороне хуже слышащего уха и на противоположной стороне, а также и в группе пациентов без подобных жалоб по сравнению с контрольной группой выявлено повышение порога восприятия звука на всех частотах, однако более выраженное повышение порогов воздушной проводимости отмечено для высоких частот, что характерно для нейросенсорной тугоухости. Кроме этого, при тимпанометрии, оценивающей акустический импеданс среднего уха, получены результаты, свидетельствующие об отсутствии патологии среднего уха и нормальном функционировании слуховой трубы.
Наконец, при акустической рефлексометрии, которая является ценным диагностическим тестом для топической диагностики нарушений слуха (в частности, дает возможность разграничения кохлеарных и ретрокохлеарных нарушений) при РС зафиксировано значительное повышение абсолютных и относительных порогов акустического рефлекса, а также частое его выпадение, что является характерным для ретрокохлеарного поражения. Важно отметить, что при акустической рефлексометрии как у пациентов с жалобами на нарушение слуха, так и у пациентов с РС с головокружением выявлены признаки одно–двустороннего поражения слухового нерва и слуховых центров продолговатого мозга и моста, более типичное для пациентов с кохлеарными нарушениями. Полученные данные подтверждают, с одной стороны, чувствительность акустической рефлексометрии при выявлении патологии слухового нерва при РС, а с другой, высокую частоту вовлечения в патологический процесс не только центральных структур, но и ретрокохлеарного неврального поражения даже у пациентов без слуховых нарушений; при этом подчеркивают роль подобного сочетанного поражения в развитии кохлеарных нарушений при РС.
В связи с представленными данными с практической точки зрения важно рассмотреть следующий аспект слуховых нарушений при РС: при обращении к отоларингологам пациентов с жалобами на снижение слуха при выявлении сенсоневральной тугоухости неясного генеза при проведении дифференциальной диагностики необходимо учитывать возможность демиелинизирующего характера процесса, поскольку своевременная постановка диагноза РС и выявление признаков его активности имеют принципиальное значение для адекватной терапии.
В последние годы в связи с достаточно большим выбором препаратов, модулирующих течение РС, и необходимостью их индивидуального назначения подходы к патогенетической терапии РС претерпевают определенные изменения.
Предлагается целый ряд терапевтических алгоритмов. Обсуждаются эскалационный (возрастающий) и индукционный подходы: эскалационная схема предполагает начало лечения с более безопасных препаратов с переходом в случае их неэффективности к более агрессивным; индукционный подход подразумевает первоначально более агрессивное влияние на иммунную систему, однако использование данного вида терапии может быть ограничено возможностью развития целого спектра побочных эффектов [Comi G., 2008; Freedman M.S., 2008].
Multiple Sclerosis Treatment Consensus Group (MSTCG) предложена интегрированная схема, основанная на разделении базовой и эскалационной терапии [Wiendl H. et al., 2008]. Согласно данному алгоритму, первоначально необходимо соответствующее лечение обострения с последующим максимально ранним назначением иммуномодуляторов первой линии. При недостаточно эффективном контроле активности болезни необходима эскалация в сторону более интенсивной терапии. К рекомендуемым базовым препаратам первой линии относятся глатирамера ацетат и интерфероны–b (ИФН–b), а при определенных обстоятельствах также натализумаб. При неэффективности лечения или плохой переносимости возможны переводы с одного из этих классов на другой или на натализумаб [Berger T., 2009]. Согласно рекомендациям MSTCG, необходимо динамическое наблюдение за пациентами, включающее как клиническую оценку, так и ряд лабораторных и инструментальных обследований.
Как уже указывалось, к модулирующим течение РС препаратам первой линии относятся ИФН–b и глатирамера ацетат. В настоящее время в России зарегистрированы следующие препараты ИФН–b: ИФН–b1а для подкожного введения (ребиф, генфаксон); ИФН–b1а для внутримышечного введения (авонекс, синновекс); ИФН–b1b (бетаферон, экставиа, ронбетал), которые отличаются между собой по источнику получения, химической структуре, а также по способу и частоте введения.
Терапевтические эффекты ИФН–b предположительно связаны с влиянием на презентирование антигенов и угнетением пролиферации и активации воспалительных клеток; угнетением продукции провоспалительных цитокинов и изменением цитокинового профиля в сторону противовоспалительного фенотипа, а также уменьшением поступления лейкоцитов в центральную нервную систему через гематоэнцефалический барьер за счет влияния на молекулы адгезии, хемокины и матриксные металлопротеиназы [Yong V.W. et al., 1998; Johnson K.P., Calabresi P.A., 2001; Clanet M., Montalban X., 2006]. Вследствие вышеперечисленного уменьшается поражение нейронов. Кроме этого, ИФН–b индуцирует синтез фактора роста нервов астроцитами [Boutros T. et al., 1997], а также усиливает секрецию данного нейротрофина эндотелиальными клетками при их взаимодействии с Т–лимфоцитами (т.е. на уровне гематоэнцефалического барьера), что также определяет его иммуномодулирующее влияние и, возможно, обусловливает непосредственное воздействие на нейрональные клетки [Biernacki K. et al. 2005].
Механизмы действия глатирамера ацетата включают конкурентное с основным белком миелина связывание с молекулой II класса главного комплекса гистосовместимости, участвующей в презентировании антигенов, а также активацию Th2–фенотипа CD4+–Т–клеток, пересекающих гематоэнцефалический барьер и секретирующих противовоспалительные цитокины (интерлейкины–4, интерлейкин–10, интерлейкин–13, трансформирующий фактор роста – b), что приводит к угнетению аутоиммунного ответа на множественные антигены миелина [Panitch H., 2001]. Кроме этого показано, что глатирамера ацетат–специфичные Т–клетки экспрессируют нейротрофический фактор мозгового происхождения и трансформирующий фактор роста – b [Aharoni R. et al., 2003]. Результаты, полученные на модели экспериментального аллергического энцефаломиелита, позволяют предположить, что глатирамера ацетат способствуют нейрогенезу [Aharoni R. et al., 2005].
Для бетаферона, ребифа, авонекса и глатирамера ацетата при ремиттирующем РС проведены двойные слепые плацебо–контролируемые испытания, продемонстрировавшие их положительное влияние на активность патологического процесса как по клиническим, так и по нейровизуализационным данным [The IFNB Multiple Sclerosis Study Group, 1993; Johnson K.P. et al., 1995; Jacobs L.D. et al., 1996; PRISMS Study Group, 1998]. Кроме этого, для ребифа и авонекса при ремиттирующем РС показано замедление прогрессирования неврологического дефицита по шкале EDSS. При исследовании эффективности глатирамера ацетата и бетаферона также отмечено замедление нарастания неврологических нарушений, однако указанные изменения в данных исследованиях не были статистически значимыми.
При вторично–прогрессирующем РС проведены двойные слепые плацебо–контролируемые исследования эффективности ребифа и бетаферона, продемонстрировавшие снижение числа обострений и уменьшение выраженности иммуно–воспалительных реакций по результатам МРТ. Также при назначении бетаферона показано замедление темпов нарастания инвалидизации пациентов (по шкале EDSS) независимо от исходной степени неврологических нарушений и наличия обострений до или во время исследования [European Study Group on Interferon beta–1b in Secondary Progressive MS, 1998]. При лечении ребифом отмечен меньший процент пациентов с прогрессированием симптомов при наличии обострений в течение последних 2 лет (в отличие от больных без обострений) [SPECTRIMS Study Group, 2001].
Важно отметить, что при обобщении результатов длительной иммуномодулирующей терапии РС бетафероном, ребифом, авонексом, глатирамера ацетатом получены данные, свидетельствующие об ее эффективности и безопасности.
Несмотря на противоречивые данные о роли нейтрализующих антител при терапии ИФН–b, нельзя исключить снижение клинической эффективности лечения под их влиянием: было показано четкое отрицательное влияние данных антител на клинические (частота обострений) и нейровизуализационные показатели активности РС, а также на прогрессирование инвалидизации [Giovannoni G., Goodman A., 2005; Sorensen P.S. et al., 2005]. В связи с этим в настоящее время разработаны рекомендации EFNS по оценке антител к ИФН–b и клиническому применению измерения нейтрализующих антител. В частности, тесты на нейтрализующие антитела должны выполняться через 12 и 24 мес. от начала терапии; измерение нейтрализующих антител должно быть прекращено при их отсутствии в этот период, однако необходимо возобновить исследования при нарастании активности болезни; при выявлении нейтрализующих антител исследование должно быть повторено через 3–6 мес.; терапия ИФН–b должна быть прекращена у пациентов с высокими титрами нейтрализующих антител, выявляющимися при повторном изменении с 3–6–месячными интервалами [Sorensen P.S. et al., 2005].
В то же время на фоне терапии глатирамера ацетатом у большинства пациентов также вырабатываются связывающие антитела к препарату, что наблюдается уже в первые 3–4 мес. после начала лечения [Dhib–Jalbut S., 2003]. Однако эти антитела не оказывают влияния на эффективность терапии [Brenner T. et al., 2001].
Важно отметить, что частота встречаемости данных антител отличается при лечении различными препаратами ИФН–b, кроме этого, ИФН–b характеризуются различной иммуногенностью (титром продуцируемых нейтрализующих антител). По данным различных исследователей, при использовании авонекса отмечается наименьшая частота встречаемости нейтрализующих антител и наименьшая иммуногенность по сравнению с другими препаратами ИФН–b [Gneiss C. et al. 2006; Goodin D.S. et al., 2007].
Также необходимо подчеркнуть, что в последние годы формула ребифа модифицирована, что привело к снижению иммуногенности и меньшему числу побочных эффектов.
В связи с большим выбором модулирующих течение РС препаратов первой линии достаточно актуальным является сопоставление их клинической эффективности. В ходе проведенного в НЦН РАМН сравнительного анализа иммуномодулирующей терапии рассеянного склероза за 3 года лечения 400 больных РС ИФН–b1b (бетафероном), ИФН–b1a для подкожного введения (ребифом) в дозе 22 мкг или глатирамера ацетатом показана одинаковая высокая эффективность исследуемых препаратов в отношении снижения числа экзацербаций как при ремиттирующем, так и при вторично–прогрессирующем РС. Продемонстрировано предупреждение нарастания выраженности неврологических нарушений при ремиттирующем РС во всех трех терапевтических группах, при вторично–прогресирующем РС – при назначении ребифа–22 мкг и глатирамера ацетата. На фоне терапии глатирамера ацетатом отмечена меньшая частота встречаемости побочных эффектов на всем протяжении 3 лет терапии по сравнению с подгруппами, получавшими лечение ИФН–b [Завалишин И.А. и др., 2007].
Полученные данные согласуются с результатами недавно завершившихся мультицентровых исследований. Так, при сопоставлении эффективности ребифа и глатирамера ацетата при ремитирующем РС (REGARD) через 96 нед. терапии не выявлены отличия первично оцениваемого показателя — времени до наступления первого обострения. Вторичные критерии (количество и изменение объема активных очагов в режиме Т2 по данным МРТ, изменения объема очагов, накапливающих контрастное вещество) также не отличались между двумя терапевтическими группами. Небольшое число обострений за время исследования в отличие от ожидаемого позволило авторам высказать предположение, что низкая активность заболевания во включенной в исследование популяции пациентов ограничила возможность выявления клинического превосходства того или иного препарата. В другом исследовании (BEYOND) при анализе первичного критерия — риска развития обострений за 2 года терапии также не выявлено отличий при назначении бетаферона и глатирамера ацетата [Mikol D.D. et al., 2008].
Обсуждая вопросы терапии, модулирующей течение РС, необходимо отметить, что большое внимание уделяется раннему назначению подобного лечения. Так, ряд проведенных исследований показал терапевтическую эффективность бетаферона, ребифа, авонекса и глатирамера ацетата при КИС [Coyle P.K., 2008].
Важной с практической точки зрения является возможность назначения данных препаратов в детском возрасте, в связи с чем необходимо подчеркнуть, что ребиф разрешен к применению с 12 лет, авонекс – с 16 лет.
В 2009 г. в России зарегистрирован и разрешен к применению другой ИФН–b1b – экставиа, при этом активная субстанция экставиа и бетаферона поступает от одного производителя, таким образом, препараты абсолютно идентичны по своему составу и качеству [Шмидт Т.Е., Яхно Н.Н., 2010].
Также в 2009 г. зарегистрирован отечественный ИФН–b – ронбетал, активным веществом в составе которого является ИФН–1b человеческий рекомбинантный. Препарат показан для уменьшения частоты и тяжести обострений у больных с рецидивирующе–ремиттирующим течением РС, для замедления темпов прогрессирования заболевания у больных с вторично–прогрессирующим течением РС.
Результаты, полученные в ходе проведенного многоцентрового проспективного рандомизированного сравнительного клинического исследования с включением пациентов с ремиттирующим и вторично–прогрессирующим (с обострениями) течением РС, показали сопоставимость данных о безопасности и переносимости оригинального препарата ИФН–b1b бетаферона и его биоаналога ронбетала, а также позволили сделать предварительное заключение об их сопоставимой эффективности [Байдина Е.В. и др., 2010]. Так, за 7,5 мес. приема препаратов наблюдавшиеся нежелательные явления, включая отклонения лабораторных показателей, в группе, получавшей ронбетал, соответствовали таковым для оригинального препарата. Выявленное в данном исследовании статистически значимое различие частоты развития гриппоподобного синдрома между группами, проходившими терапию ронбеталом и бетафероном (значительно меньшая частота развития выявлена в группе, получавшей ронбетал), требует уточнения в дальнейших исследованиях. Полученные данные о снижении риска развития обострений на фоне применения ронбетала соответствовала результатам многоцентровых клинических исследований по применению ИФН–β. В ходе исследования статистически значимого нарастания балла по шкале EDSS не отмечено, различий средних значений EDSS между группами ни в начале исследования, ни в динамике отмечено не было. Наблюдавшаяся в данном исследовании динамика количества и объема очагов демиелинизации по данным МРТ при терапии препаратами ИФН–β была аналогична данным международных многоцентровых исследований.
Также в 2010 г. в России зарегистрированы следующие ИФН–β1а — генфаксон (для подкожного применения), а также синновекс (для внутримышечного введения).
В России в 2010 г. для пациентов с ремиттирующим РС зарегистрирован целый ряд препаратов с другими механизмами действия и способами введения: Тизабри (натализумаб), Мовектро® (кладрибин), Гилениа (финголимод).
Так, натализумаб относится к моноклональным антителам, является селективным ингибитором молекул адгезии. Натализумаб связывается с ά4–субъединицей человеческого интегрина, в большом количестве экспрессирующегося на поверхности всех лейкоцитов, за исключением нейтрофилов. В частности, препарат специфически связывается с ά4β1–интегрином, блокируя при этом взаимодействие с соответствующим рецептором, адгезивной молекулой клеток сосудов (VCAM–1). В связи с этим антитела к молекулам адгезии ингибируют один из основных этапов патогенеза РС — взаимодействие с эндотелиальными клетками и миграцию лимфоцитов через гематоэнцефалический барьер. Дальнейший механизм действия натализумаба может быть обусловлен подавлением воспалительных реакций в пораженных тканях путем подавления взаимодействия ά4–экспрессирующих лейкоцитов с их лигандами. Таким образом, натализумаб может подавлять воспалительную активность в пораженных тканях и дальнейшее привлечение иммунных клеток к очагу воспаления.
Высокая эффективность терапии натализумабом при ремиттирующем РС была продемонстрирована в следующих рандомизированных плацебо–контролируемых исследованиях III фазы. Так, при использовании натализумаба в качестве монотерапии по сравнению с группой плацебо было показано значительное снижение среднегодовой частоты обострений, образования новых или увеличивающихся очагов на МРТ в режиме Т2 и среднего количества накапливающих контрастное вещество очагов, а также уменьшение прогрессирования заболевания [Polman C.H. et al, 2006]. Также была продемонстрирована значительно бо́льшая эффективность комбинации натализумаба и авонекса по сравнению с монотерапией авонексом [Rudick R.A. et al., 2006].
В настоящее время препарат натализумаб показан для монотерапии ремиттирующей формы рассеянного склероза следующим группам больных: пациентам с активным течением заболевания, несмотря на лечение ИФН–β; пациентам с быстро прогрессирующим тяжелым ремиттирующим РС. Противопоказаниями к его назначению являются: гиперчувствительность к натализумабу или любому из вспомогательных веществ; прогрессирующая многоочаговая лейкоэнцефалопатия (ПМЛ); повышенный риск инфекции условно–патогенными микроорганизмами, в том числе иммунодефицитные состояния; одновременное применение ИФН–β или глатирамера ацетата; злокачественные новообразования, за исключением базальноклеточного рака кожи; детский и подростковый возраст. Не следует назначать натализумаб во время беременности без крайней необходимости; если пациентка забеременеет во время приема, терапию следует прекратить; пациентки, получающие препарат, должны прекратить кормление грудью. Применение натализумаба у пациентов старше 65 лет не рекомендуется из–за отсутствия данных о безопасности для этой категории больных [Инструкция по медицинскому применению препарата тизабри].
Препарат применяется в виде внутривенных инфузий 1 раз в 4 нед.
Однако при использовании натализумаба необходимо помнить о возможности развития различных побочных эффектов. В частности, его применение может повысить риск развития такого опасного нежелательного явления, как прогрессирующая мультифокальная лейкоэнцефалопатия (ПМЛ), при этом опасность увеличивается по мере продолжительности терапии, особенно при лечении препаратом более 2 лет. При назначении данного препарата необходимо тщательное наблюдение за пациентами, в том числе мониторинг побочных эффектов: инфекций, включая ПМЛ и инфекции условно–патогенными микроорганизмами; развития гиперчувствительности на введение препарата; побочного влияния на функцию печени и др. В связи с этим разрабатываются специальные программы наблюдения за лицами, получающими натализумаб; препарат назначается только после соответствующего информирования пациента, при этом врач и пациент должны в индивидуальном порядке рассмотреть соотношение пользы и риска при лечении препаратом.
Следующие два новых препарата для лечения ремитирующего РС – Гилениа (финголимод) и Мовектро®Ò (кладрибин), предназначены для перорального приема.
Финголимод является модулятором рецепторов сфингозин–1–фосфата. После фосфорилирования финголимод действует как функциональный антагонист рецепторов сфингозин–1 фосфата 1–го типа, вызывая их смещение с внешней мембраны лимфоцитов на внутреннюю, что делает Т– и В–лимфоциты невосприимчивыми к сигналам, стимулирующим их выход из вторичной лимфоидной ткани [Brinkmann V. et al., 2002; Schwab S.R., Cyster J.G., 2007]. Возникающее в результате этого перераспределение лимфоцитов в лимфоузлы и предотвращение их миграции из лимфоузлов уменьшает поступление аутоагрессивных лимфоцитов в ЦНС [Pinschewer D.D. et al., 2000; Mandala S. et al., 2002; Matloubian M. et al., 2004]. Благодаря липофильности финголимод проникает через гематоэнцефалический барьер и проходит фосфорилизрование в ЦНС [Foster C.A. et al., 2007]. Показано также, что финголимод может оказывать нейропротективное действие и способствует ремиелинизации в ЦНС путем взаимодействия с рецепторами сфингозин–1 фосфата на нейронах [Coelho R.P. et al., 2007; Foster C.A. et al., 2007; Barske C. et al., 2008; Miron V.E. et al., 2008].
В двух проведенных исследованиях финголимод использовался в двух суточных дозах: 1,25 или 0,5 мг. В одном из исследований показано преимущество финголимода в обеих указанных дозах в сравнении с ИФН–b1а для внутримышечного введения по таким параметрам эффективности, как частота обострений, и данным МРТ (меньшее количество новых или увеличивающихся гиперинтенсивных очагов в режиме Т2; очагов, накапливающих контрастное вещество в режиме Т1; процент уменьшения объема мозга от исходного уровня). Два случая инфекций с летальным исходом были зарегистрированы в группе, получавшей 1,25 мг финголимода: диссеминированная первичная инфекция, вызванная вирусом Varicellazoster, и энцефалит, вызванный вирусом простого герпеса. Другие нежелательные явления у пациентов, получавших финголимод, включали нефатальные случаи герпетической инфекции, брадикардию и атриовентрикулярную блокаду, артериальную гипертонию, отек макулы, рак кожи и повышение активности печеночных ферментов [Cohen J.A. et al., 2010].
В другом исследовании пациенты получали финголимод в одной из указанных доз или плацебо. Препарат в обеих дозах значительно снижал риск нарастания инвалидизации; МРТ–показатели активности болезни (появление новых или увеличение старых очагов в режиме Т2, очагов, накапливающих контрастное вещество, атрофии мозга). Причинами отмены препарата и нежелательными явлениями, связанными с приемом финголимода, были брадикардия и атриовентрикулярная блокада в начале лечения, отек макулы, повышение печеночных ферментов и легкая артериальная гипертония [Kappos L. et al., 2010].
Надо отметить, что зарегистрированной дозой гилении (финголимода гидрохлорида) является 0,5 мг перорально 1 раз/сут.; показанием для ее назначения — ремиттирующий РС, для уменьшения частоты клинических обострений болезни и снижения риска прогрессирования нетрудоспособности. Препарат противопоказан при гиперчувствительности к финголимоду или любому другому его компоненту, беременности и в период грудного вскармливания. Эффективность и безопасность применения препарата гилениа у детей и подростков в возрасте до 18 лет не установлены. Существует также целый ряд состояний, при которых данный препарат назначается с осторожностью. В связи с этим необходимо тщательное обследование пациента перед назначением препарата, наблюдение за приемом первой дозы, а также динамическое наблюдение на фоне приема препарата и контроль нежелательных явлений.
Механизм действия кладрибина связан с тем, что внутриклеточная аккумуляция его активного метаболита, 2–хлородезоксиаденозина трифосфата, приводит к нарушению клеточного метаболизма, угнетению синтеза и репарации ДНК и, соответственно, апоптозу [Beutler E., 1992]. Кладрибин преимущественно действует на лимфоциты. Накопление нуклеотидов кладрибина вызывает быстрое и длительное уменьшение количества CD4+ и CD8+ клеток, а также обладает быстрым, но более преходящим влиянием на CD19+ B–клетки с относительной сохранностью других иммунных клеток [Beutler E., 1992; Rice G.P. et al., 2000; Guarnaccia J.B. et al., 2008; Giovannoni G. et al., 2010]. Также кладрибин уменьшает уровень провоспалительных цитокинов и хемокинов в сыворотке и цереброспинальной жидкости, экспрессию молекул адгезии, миграцию мононуклеарных клеток [Janiec K. et al., 2001; Niezgoda A. et al., 2001; Bartosik–Psujek H. et al., 2004; Kopadze T. et al., 2009].
В плацебо–контролируемом исследовании у пациентов с ремиттирующим РС, перорально получавших кладрибин в дозе 3,5 мг или 5,25 мг на 1 кг массы тела, по сравнению с группой плацебо отмечено значительное снижение частоты обострений, более высокая доля пациентов без экзацербаций, более низкий риск устойчивого на протяжении 3 мес. прогрессирования инвалидизации, а также значительное уменьшение количества очагов в головном мозге, по данным МРТ. Нежелательными явлениями, которые чаще отмечались в группах, получавших кладрибин, включали лимфоцитопению, инфекцию herpes zoster [Giovannoni G. et al., 2010].
Зарегистрированный препарат Мовектро® в таблетках, содержащих активное вещество кладрибин (10,00 мг в 1 табл.), показан к применению для лечения РС рецидивирующего (ремитирующего) течения. Противопоказаниями для назначения являются: повышенная чувствительность к кладрибину и другим компонентам препарата; острое инфекционное заболевание или обострение хронического заболевания; снижение иммунитета в связи с заболеванием или вследствие приема иммунодепрессантов, включая циклоспорин, метотрексат, митоксантрон, натализумаб, или длительного применения глюкокортикостероидов; вакцинация в течение предшествующих лечению 3 мес. аттенуированной вакциной (живые или ослабленные вакцины); беременность, период лактации; возраст до 18 лет (недостаточно клинических данных). В связи с тем, что Мовектро®Ò содержит сорбитол, у пациентов с непереносимостью фруктозы его применение не рекомендуется. Также существует ряд состояний, при которых данный препарат назначается с осторожностью.
Терапия Мовектро® проводится курсами; каждый курс состоит в применении одной или двух таблеток в течение первых 4 или 5 дней периода в 4 нед. (расчет дозы проводится на основании необходимых курсов лечения и массы тела пациента). Обычно лечение препаратом начинают с 2 лечебных курсов. В зависимости от выраженности заболевания может быть рекомендовано 4 курса лечения сразу. Эти 2 или 4 курса называют «Начальная терапия». Интервал между курсами лечения Мовектро® в рамках «Начальной терапии» составляет 4 нед. Начальная терапия, включающая 4 последовательных курса, рекомендуется пациентам с выраженной активностью заболевания. Дополнительные курсы начинают через 48 и 52 нед. после завершения начальной терапии. Эти 2 курса называют «Повторная терапия». Как перед началом терапии, так и в период терапии Мовектро® необходимо выполнение определенных обследований с целью мониторинга состояния пациента.
При вторично–прогрессирующем и ремиттирующем РС при быстром прогрессировании заболевания и неэффективности средств первой линии, изменяющих течение РС, широко используется цитостатический препарат митоксантрон с целью снижения частоты и тяжести обострений и замедления темпа прогрессирования заболевания. Однако при использовании митоксантрона, как и других цитостатических препаратов, необходимо учитывать возможность развития побочных эффектов, в частности миелосупрессии и кардиотоксичности, что требует тщательного отбора пациентов и мониторирования соответствующих показателей. Согласно публикации Multiple Sclerosis Therapy Consensus Group [Wiendl H. et al., 2008], рекомендуется также снижение максимальной кумулятивной дозы до 100 мг на 1 м2 поверхности тела (в ряде случаев возможно достижение суммарной дозы 140 мг на 1 м2 поверхности тела); проведение эхокардиографии перед каждым введением митоксантрона. Продолжение курса препарата возможно только в случае чувствительности пациента к проводимому лечению и сохранении признаков активности заболевания. При назначении препарата молодым женщинам необходимо учитывать возможность развития длительной или постоянной аменореи. Кроме этого, препарат может влиять и на фертильность у мужчин.
Таким образом, за последние годы отмечается значительное расширение спектра препаратов для лечения РС, что обусловлено не только появлением ряда дженериков давно известных лекарственных препаратов ИФН–b и биоаналога ИФН–b1b, но и регистраций средств с другими механизмами действия. С одной стороны, это увеличивает возможности современной терапии, модулирующей течение РС, с другой стороны, требует индивидуального подхода к подбору лечения с тщательным анализом показаний/противопоказаний и состояний, требующих осторожности, возможных побочных явлений, также необходим тщательный мониторинг состояния пациентов в период лечения с целью оценки как эффективности, так и безопасности назначенной терапии.
Литература
1. Байдина Е.В., Бойко А.Н., Брюхов В.В. и др. Результаты клинического исследования российского биоаналога интерферона–бета–1В // Неврологический вестник. 2010. Т. XLII. Вып. 1. С. 41–48.
2. Завалишин И.А., Переседова А.В., Стойда Н.И. и др. Сравнительный анализ эффективности иммуномодулирующей терапии рассеянного склероза ребифом–22 мкг, бетафероном и копаксоном (результаты 3 лет лечения) // Журнал неврологии и психиатрии им. С.С. Корсакова. 2007. Вып. 4. Рассеянный склероз. С. 99–105.
3. Шмидт Т.Е., Яхно Н.Н. Рассеянный склероз: руководство для врачей. 2–е изд. М.: МЕДпресс–информ, 2010. 272 с.
4. Aharoni R., Arnon R., Eilam R. Neurogenesis and neuroprotection induced by peripheral immunomodulatory treatment of experimental autoimmune encephalomyelitis. J. Neurosci. 2005; 25: 8217–8228.
5. Aharoni R., Kayhan B., Eilam R. et al. Glatiramer acetate–specific T cells in the brain express T helper 2/3 cytokines and brain–derived neurotrophic factor in situ. Proc. Natl. Acad. Sci. USA. 2003; 100: 14157–14162.
6. Barske C., Osinde M., Klein C. et al. FTY720 (fingolimod) and S1P–receptor 1 and 5 specific agonists increase the number of oligodendrocytes in vitro. Neurology. 2008; 70: Suppl.1: A28. abstract.
7. Bartosik–Psujek H., Belniak E., Mitosek–Szewczyk K. et al. Interleukin–8 and RANTES levels in patients with relapsing–remitting multiple sclerosis (RR–MS) treated with cladribine. Acta Neurol. Scand. 2004; 109: 390–392.
8. Berger T. Current therapeutic recommendations in multiple sclerosis. J. Neurol. Sci. 2009; 287 S1: S37–S45.
9. Beutler E. Cladribine (2–chlorodeoxyadenosine). Lancet 1992; 340: 952–956.
10. Biernacki K., Antel J.P., Blain M. et al. Interferon beta promotes nerve growth factor secretion early in the course of multiple sclerosis. Arch. Neurol. 2005; 62 (4): 563–568.
11. Boutros T., Croze E., Yong V.W. Interferon–b is a potent promoter of nerve growth factor production by astrocytes. J. Neurochem. 1997; 69: 939–946.
12. Brenner T., Arnon R., Sela M. et al. Humoral and cellular immune responses to Copolymer 1 in multiple sclerosis patients treated with Copaxone. J. Neuroimmunol. 2001; 115: 152–160.
13. Brinkmann V., Davis M.D., Heise C.E.et al. The immune modulator FTY720 targets sphingosine 1–phosphate receptors. J. Biol. Chem. 2002; 277: 21453–21457.
14. Clanet M., Montalban X. (chairmen). The future of multiple sclerosis therapies. — PAREXEL MMS Europe Ltd. 2006; 51 p.
15. Coelho R.P., Payne S.G., Bittman R. et al. The immunomodulator FTY720 has a direct cytoprotective effect in oligodendrocyte progenitors. J. Pharmacol. Exp. Ther. 2007; 323: 626–635.
16. Cohen J.A. , Barkhof F., Comi G. et al. Oral fingolimod or intramuscular interferon for relapsing multiple sclerosis. N. Engl. J. Med. 2010; 362 (5): 402–415.
17. Comi G. Induction vs. escalating therapy in multiple sclerosis: practical implications. Neurol. Sci. 2008; 29 Suppl. 2: P. 253–255.
18. Coyle P.K. Early treatment of multiple sclerosis to prevent neurologic damage. Neurology 2008; 71 (24 Suppl. 3): P. 3–7.
19. Dhib–Jalbut S. Glatiramer acetate (Copaxone®) therapy for multiple sclerosis. Pharmacol. Ther. 2003; 98: 245–255.
20. European Study Group on Interferon beta–1b in Secondary Progressive MS. Placebo–controlled multicenter randomized trial of interferon b–1b in treatment of secondary progressive multiple sclerosis. Lancet. 1998; 352: 1491–1497.
21. Foster C.A., Howard L.M., Schweitzer A. et al. Brain penetration ot the oral immunomodulatory drug FTY720 and its phosphorylation in the central nervous system during experimental autoimmune encephalomyelitis: consequences for mode of action in multiple sclerosis. J. Pharmacol. Exp. Ther. 2007; 323: 469–475.
22. Freedman M.S. Induction vs. escalation of therapy for relapsing multiple sclerosis: the evidence. Neurol. Sci. 2008; 29 Suppl. 2: S250–252.
23. Giovannoni G., Comi G., Cook S. et al. A placebo–controlled trial of oral cladribine for relapsing multiple sclerosis. N. Engl. J. Med. 2010; 362 (5): 416–426.
24. Giovannoni G., Goodman A. Neutralizing anti–IFN–b antibodies, How much more evidence do we need to use them in practice? Neurology 2005; 65: 6–8.
25. Gneiss C., Tripp P., Reichartseder F. et al. Differing immunogenic potentials of interferon beta preparations in multiple sclerosis patients. Mult. Scler. 2006; 12 (6): 731–737.
26. Goodin D.S., Frohman E.M., Hurwitz B. et al. Neutralizing antibodies to interferon beta: assessment of their clinical and radiographic impact: an evidence report: report of the Therapeutics and Technology Assessment Subcommittee of the American Academy of Neurology. Neurology 2007; 68 (13): 977–984.
27. Guarnaccia J.B., Rinder H., Smith B. Preferential depletion of lymphocyte sub–populations by cladribine in a phase III clinical trial in multiple sclerosis. In: Program and abstracts of the World Congress on Treatment and Research in Multiple Sclerosis, Montreal, September 17–20, 2008 (poster).
28. Jacobs L.D., Cookfair D.L., Rudick R.A. et al. Intramuscular interferon beta–1a for disease progression in exacerbating–remitting multiple sclerosis. Ann. Neurol. 1996; 39: 285–294.
29. Janiec K., Wajgt A., Kondera–Anasz Z. Effect of immunosuppressive cladribine treatment on serum leucocytes system in two–year clinical trial in patients with chronic progressive multiple sclerosis. Med Sci. Monit. 2001; 7: 93–98.
30. Johnson K.P., Brooks B.R., Cohen J.A. et al. Copolymer 1 reduces relapse rate and improves disability in relapsing–remitting multiple sclerosis: results of a phase III multicenter, double–blind, placebo–controlled trial. Neurology. 1995; 45: 1268–1276.
31. Johnson K.P., Calabresi P.A. Interferon–b–1b: prophylactic therapy in multiple sclerosis. Handbook of multiple sclerosis. Ed. S.D.Cook. 3nd ed. Marcel Dekker Inc. 2001: 503–518.
32. Kappos L., Radue E.W., O’Connor P. et al. A placebo–controlled trial of oral fingolimod in relapsing multiple sclerosis. N. Engl. J. Med. 2010; 362 (5): 387–401.
33. Kopadze T., Dobert M., Leussink V.I. et al. Cladribine impedes in vitro migration of mononuclear cells: a possible implication for treating multiple sclerosis. Eur. J. Neurol. 2009; 16: 409–412.
34. Mandala S., Hajdu R., Bergstrom J. et al. Alteration of lymphocyte trafficking by sphingosine–1–phosphate receptor agonists. Science. 2002; 296: 346–349.
35. Matloubian M., Lo C.G., Cinamon G. et al. Lymphocyte egress from thymus and peripheral lymphoid organs is dependent on S1p receptor 1. Nature. 2004; 427: 355–360.
36. Mikol D.D., Barkhof F., Chang P. et al. Comparison of subcutaneous interferon beta–1a with glatiramer acetate in patients with relapsing multiple sclerosis (the REbif vs Glatiramer Acetate in Relapsing MS Disease [REGARD] study): a multicentre, randomised, parallel, open–label trial. Lancet Neurol. 2008; 7 (10): 903–914.
37. Miller D.H., Weinshenker B.G., Filippi M. et al. Diffential diagnosis of suspected multiple sclerosis: a consensus approach. Mult. Scler. 2008; 14: 1157–1174.
38. Miron V.E., Jung C.G., Kim H.J. et al. FTY720 modulates human oligodendrocyte progenitor process extension and survival. Ann. Neurol. 2008; 63: 61–71.
39. Niezgoda A., Losy J., Mehta P.D. Effect of cladribine treatment on beta–2 micro–globulin and soluble intercellular adhesion molecule 1 (ICAM–1) in patients with multiple sclerosis. Folia Morphol. (Warsz) 2001; 60: 225–228.
40. Panitch H. Prophylactic therapy — glatiramer acetate (Copaxone). Handbook of multiple sclerosis. Ed. S.D.Cook. 3nd ed. Marcel Dekker Inc. 2001; 541–560.
41. Pinschewer D.D., Ochsenbein A.F., Odermatt B. et al. FTY720 immunosuppression impairs effector T cell peripheral homing without affecting induction, expansion, and memory. J. Immunol. 2000; 164: 5761–5770.
42. Polman C.H., O’Connor P.W., Havrdova E. et al. A randomized, placebo–controlled trial of natalizumab for relapsing multiple sclerosis. N. Engl. J. Med. 2006; 354 (22): 2387–2389.
43. Polman C.H., Reingold S.C., Edan G. et. al. Diagnostic criteria for multiple sclerosis: 2005 revisions to the “McDonald Criteria”. Ann. Neurol. 2005; 58 (6): 840–846.
44. PRISMS Study Group. Randomized double–blind placebo–controlled study of interferon b–1a in relapsing–remitting multiple sclerosis. Lancet. 1998; 352: 1498–1504.
45. Rice G.P., Filippi M., Comi G. Cladribine and progressive MS: clinical and MRI outcomes of a multicenter controlled trial. Neurology 2000; 54: 1145–1155.
46. Rovira A., Swanton J., Tintore M. et al. A single, early magnetic resonance imaging study in the diagnosis of multiple sclerosis. Arch. Neurol. 2009; 66 (5): 587–592.
47. Rudick R.A., Stuart W.H., Calabresi P.A. et al. Natalizumab plus interferon beta–1a for relapsing multiple sclerosis. N. Engl. J. Med. 2006; 354 (9): 911–923.
48. Schwab S.R., Cyster J.G. Finding a way out: lymphocyte egress from lymphoid organs. Nat. Immunol. 2007; 8: 1295–1301.
49. Sorensen P.S., Deisenhammer F., Duda P. Et al. Guidelines on use of anti–IFN–b antibody measurements in multiple sclerosis: report of an EFNS Task Force on IFN–b antibodies in multiple sclerosis. Europ. J. Neurol. 2005; 12: 817–827.
50. SPECTRIMS Study Group. Randomized controlled trial of interferon–beta–1a in secondary progressive MS. Clinical results. Neurology. 2001; 56: 1496–1504.
51. Swanton J.K., Fernando K., Dalton C.M. et al. Modification of MRI criteria for multiple sclerosis in patients with clinically isolated syndromes. J. Neurol. Neurosurg. Psychiatry. 2006; 77 (7): 830–833.
52. Swanton J.K., Rovira A., Tintore M. et al. MRI criteria for multiple sclerosis in patients presenting with clinically isolated syndromes: a multicentre retrospective study. Lancet Neurol. 2007; 6 (8): 677–686.
53. The IFNB Multiple Sclerosis Study Group. Interferon beta–1b is effective in relapsing–remitting multiple sclerosis: I. Clinical results of a multicentral, randomized double bind, placebo–controlled trial. Neurology. 1993; 43: 655–661.
54. Tur C., Tintore M., Rovira A. et al. Very early scans for demonstrating dissemination in time in multiple sclerosis. Mult. Scler. 2008; 14 (5): 631–635.
55. Wiendl H., Toyka K.V., Rieckman P. et al. Basic and escalating immunomodulatory treatments in multiple sclerosis: current therapeutic recommendations. J. Neurol. 2008; 255: 1449–1463.
56. Yong V.W., Chabot S., Stuve O., Williams G. Interferon beta in the treatment of multiple sclerosis: mechanisms of action. Neurology 1998; 51: 682–689.












