Риск развития ОНМК у таких пациентов определяется характером и тяжестью основного сердечно–сосудистого заболевания (ИБС, артериальная гипертензия, мерцательная аритмия и т.д.), степенью (величина и протяженность стеноза) и характером (тип и расположение атеросклесклеротической бляшки, особенности экстравазальной компрессии, наличие аномалий развития и т.д.) поражения сосудистого русла, а также возможностью обеспечения коллатерального кровообращения головного мозга.
Принято разделять недостаточность кровообращения в каротидном и ВББ, однако необходимо учитывать, что во многих случаях даже полное прекращение кровотока по одной из четырех магистральных артерий может не давать значимых клинических проявлений за счет перетока из бассейнов смежных артерий. В то же время подобное пераспределение приводит к обкрадыванию в бассейне артерии–донора и клинические проявления могут возникать в бассейне именно этой артерии. Эта особенность существенно затрудняет клиническую диагностику, требуя применения современных инструментальных методов обследования. Клиническая картина поражения артерий каротидного и вертебро–базилярного бассейнов различна.
Характерными проявлениями поражения сонных артерий являются:
1. Преобладание различных умеренно выраженных очаговых изменений корковых функций (афазия, алексия, аграфия, пространственная агнозия).
2. Когнитивные нарушения, редко достигающие степени деменции.
Характерными клиническими проявлениями поражения артерий ВББ являются:
• зрительные и глазодвигательные расстройства,
• нарушения статики и координации движений,
• вестибулярные нарушения,
• транзиторная глобальная амнезия,
• зрительная агнозия,
• внезапные падения (drop attacks),
• синкопальный вертебрально–базилярный синдром,
• нарушения сна и бодрствования,
• вегетативно–висцеральные расстройства.
При поражении любой преобладающей локализации могут наблюдаться нарушения сна, синдромы паркинсонизма, мозжечковой недостаточности и т.д. Головная боль, часто сопровождающая эти симптомы, обычно обусловлена нарушением венозного оттока различного генеза и/или миофасциальными синдромами, что в большинстве случаев требует самостоятельной терапии.
При этом из–за особенностей анатомического строения одной из наиболее сложных задач является обеспечение полноценной диагностики патологии артерий ВББ. ВБН является одним из наиболее распространенных диагнозов как в амбулаторной, так и стационарной неврологической практике, объединяющим различные по своему происхождению и механизмам развития ишемические расстройства мозгового кровообращения в этой сосудистой системе. Вариабельность клинических проявлений ВБН, объективные трудности диагностики, клиническое сходство с целым рядом других патологических состояний нередко приводят к ошибочной гипо– и гипердиагностике данного состояния.
Основную роль в диагностике (особенно скрининге) клинически значимых изменений церебрального кровотока в настоящее время играет ультразвуковая диагностика, что обусловлено неинвазивностью и сравнительной дешевизной исследования [5]. Однако она имеет ряд технических ограничений, в частности, при необходимости обследования интравертебральных и интракраниальных отделов сосудистого русла. В связи с этим все большее значение в диагностике этой патологии приобретают магнитно–резонансная ангиография (МРА) и мультиспиральная компьютерная томография (МСКТ). Важной особенностью МРА является возможность проведения обследования сосудистого русла без введения контраста, что позволяет применять эту технологию у лиц с непереносимостью контрастных препаратов, а также в качестве дополнительного метода скринингового обследования. МСКТ, напротив, требует применения контрастирования, однако позволяет получить наиболее точные и достоверные данные, которые в настоящее время можно считать «золотым стандартом» обследования при решении вопроса об оперативном или консервативном ведении пациента с клинической картиной вертебрально–базилярной или каротидной недостаточности.
Патогенез ВБН может затрагивать очень широкий спектр патологических и компенсаторных изменений. Наряду с уже упомянутой патологией сосудов ВББ (петлеобразование, стенозы и окклюзии), большую роль играет влияние экстравазальных факторов. Так, тромбоз позвоночной артерии зачастую обусловлен ее диссекцией вследствие повреждения при хлыстовой или иной травме шеи, неадекватных мануальных манипуляциях на шейном отделе позвоночника, компрессии сосуда вследствие наличия грыжи межпозвонкового диска или врожденной аномалии. Типичным примером такого состояния является аномалия Киммерли, при которой на рентгенограмме краниовертебральной зоны в сагиттальной проекции дифференцируется костная перемычка, соединяющая задний край боковой массы и заднюю дужку атланта, из–за наличия которой при повороте головы происходит перегиб и компрессия позвоночной артерии с возможной ее травматизацией. Важной особенностью аномалии Киммерли является зависимость гемодинамики и клинической картины от положения головы и шеи, поэтому при проведении ЦДС, МРА и МСКТ без функциональных проб весьма вероятно получение ложноотрицательного результата. В последнем случае они могут быть устранены путем проведения 3D–реконструкции костных структур, однако до настоящего времени наиболее надежным и дешевым методом диагностики является классическая рентгенография шейного отдела позвоночника в боковой проекции. В тяжелых случаях требуется хирургическое устранение костной дужки, в остальных случаях показано консервативное лечение.
Серьезное влияние на кровоток в ВББ могут оказывать и такие аномалии развития, как аномалия Клиппеля–Фейля–Шпренгеля, аномалия Арнольда–Киари, незаращение задней дужки атланта, седловидная гиперплазия боковых масс атланта, недоразвитие суставных отростков шейных позвонков, шейные ребра и ряд других.
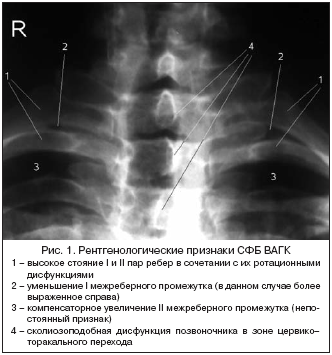
Еще одним распространенным, но сложным в диагностике состоянием, вызывающим клиническую картину ВБН, является синдром функционального блока верхней апертуры грудной клетки (СФБ ВАГК) [2]. При его наличии имеет место сочетанное ухудшение церебрального артериального и венозного кровотока за счет мультифокальной, часто диффузной экстравазальной компрессии. Для него характерны визуально определяемые укорочение и утолщение шеи; глубокие кожные складки на шее, преимущественно по задней поверхности (на уровне функциональных блоков позвоночно–двигательных сегментов) и на уровне выйных линий; деформация зоны цервико–торакального перехода по типу «жирового холмика»; одутловатость лица, нередко гиперемия кожных покровов головы и шеи; укорочение надплечий за счет гипертонуса трапециевидных и надостных мышц; высокое стояние рукоятки грудины, выбухание надключичных ямок; высокое стояние ключиц и лопаток и ряд других симптомов [2]. В случае если у пациента имеется вышеописанная симптоматика, рекомендуется проведение рентгенографической диагностики. При выявлении представленных на рисунке 1 изменений, а также гиперлордоза шейного отдела позвоночника на уровне верхних сегментов в сочетании со сглаженностью средних и нижних в боковой проекции, больным показано ношение воротниковой шины Шанца, стандартная ноотропная и сосудистая терапия, при возможности и в отсутствие противопоказаний – консультация мануального терапевта для решения вопроса о коррекции биомеханических дисфункций. Также на позвоночные артерии могут влиять и другие патобиомеханические изменения, приводя к формированию, например, вертеброгенного синдрома позвоночной артерии [8].
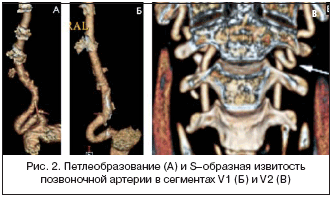
В целом при определении тактики лечения ВБН важнейшее значение имеют течение заболевания и его патогенез. В случае остро возникшего и/или нарастающего неврологического дефицита (альтернирующие синдромы, мозжечковая недостаточность, «негативные» скотомы и т.д.) пациент должен быть в экстренном порядке госпитализирован в неврологическое отделение (при наличии возможности – отделение нейрореанимации), т.к. имеется высокий риск витально опасных осложнений. В остальных случаях обычно возможно лечение в амбулаторных условиях. При определении тактики ведения пациента большую роль играют визуализационные методы исследования. На рисунке 2 показаны гемодинамически значимое петлеобразование проксимального (сегмент V1) отдела позвоночной артерии, подлежащее оперативному лечению (А), и S–образная извитость того же отдела, которая в большинстве случаев не нуждается в хирургической коррекции (Б), а коррекция петли, расположенной в интравертебральном отделе позвоночной артерии между II и III позвонками (сегмент V2) в большинстве случаев невозможна. Кроме петлеобразования и извитости, в сегменте V1 нередко может выявляться диссекция, как спонтанная, так и травматического генеза, являющаяся маркером клинически значимых гемодинамических изменений и высокого риска восходящего тромбоза позвоночной артерии. В случае выявления показаний к оперативному лечению пациент должен быть незамедлительно осмотрен сосудистым хирургом. При отсутствии таких показаний или невозможности оперативного вмешательства проводится консервативная терапия, основной целью которой является профилактика развития ОНМК.
Одним из основных направлений профилактики инсульта у пациентов с хроническими нарушениями мозгового кровообращения, особенно перенесших ТИА, является применение антиагрегантной терапии. По результатам международных мультицентровых контролируемых исследований, наиболее эффективными препаратами для вторичной профилактики ишемических нарушений мозгового кровообращения являются: ацетилсалициловая кислота (АСК), дипиридамол, тиклопидин и клопидогрел.
При этом «золотым стандартом» до настоящего времени остается АСК [7]. Весьма важным является вопрос дозирования АСК. Многочисленные клинические исследования, в частности, Antithrombotic Trialists’ Collaboration [10], показали, что оптимальным является прием АСК в дозе 75–150 мг в сутки., т.к. в отличие от роста побочных эффектов не существует достоверной положительной зависимости эффективности приема АСК от увеличения ее дозы. При этом весьма важным является вопрос профилактики осложнений терапии, к числу которых относятся в первую очередь гастриты, язвы желудка и 12–перстной кишки, а также иная гастроинтестинальная патология. В этом плане является важным соблюдение режима приема препарата, а также одновременное назначение антацидов в виде самостоятельной лекарственной формы или комплексного препарата, например, АСК с невсасывающимся антацидом, действующим на всем протяжение ЖКТ – гидроокисью магния). Следует иметь в виду, что от 25 до 30% пациентов могут быть вообще резистентны к антиагрегационным эффектам ацетилсалициловой кислоты [7].
В случае непереносимости или неэффективности АСК в терапевтических дозах возможными заменами могут быть сочетание АСК (25 мг) и дипиридамола (200 мг) дважды в сутки, клопидогрел (75 мг/сут) или монотерапия дипиридамолом (200 мг дважды в сутки). Необходимо отметить, что применение комбинации АСК с дипиридамолом может сопровождаться головной болью. Также с осторожностью необходимо относиться к его использованию у пациентов со стенокардией напряжения и документированным тяжелым стенозом коронарных артерий из–за риска осложнений. Во всех случаях применение альтернативных схем лечения требует более частого (в том числе лабораторного) мониторинга состояния пациента.
Если у пациента с клинической картиной ВБН имеет место дислипидемия, а по данным ЦДС или МСКТ – хотя бы одна атеросклеротическая бляшка (I–III типы по Gray–Weale), то может быть поставлен вопрос о назначении статинов, например, аторвастатина в малой терапевтической дозе 10 мг в сутки. Противопоказаниями к назначению являются активное заболевание печени, тяжелая недостаточность функции печени с повышенной активностью трансаминаз и т.д. Снижение холестерина на 1,0 ммоль/л приводит к снижению риска всех инсультов на 10%, а на 1,8 ммоль/л – на 17%. В целом, по данным ряда исследований (SSSS, 1995; HPS, 2001), применение статинов в течение 3–5 лет позволяет снизить риск инсульта на 24–36% [11].
Следующим важным направлением лечения пациентов с ВБН является применение нейрометаболических и вазоактивных препаратов. К их числу можно отнести препараты комплексного действия (Актовегин, инстенон, винпоцетин, Цераксон), преимущественно нейротропные препараты (пирацетам, глицин, Энцефабол), препараты, преимущественно влияющие на мозговой кровоток (циннаризин, ницерголин, ксантинола никотинат), препараты, улучшающие микроциркуляцию (пентоксифиллин), препараты, обладающие преимущественно нейротрофическим действием (церебролизин). В клинической практике в большинстве случаев оптимальным является применение препаратов комплексного действия, т.к. это позволяет снизить фармакологическую нагрузку на больного и увеличить его приверженность терапии. Одним из таких препаратов является Актовегин, обладающий широким спектром фармакологических эффектов: антигипоксантным, антиоксидантным, препарат способствует процессам репарации и регенерации, оказывает нейротрофическое действие, способствует реваскуляризации зоны ишемии. Актовегин не только улучшает транспорт глюкозы и поглощение кислорода, но и стимулирует их утилизацию, что улучшает кислородный метаболизм даже в условиях гипоксии [1]. Эта особенность обусловлена в том числе его инсулиноподобным действием. Несомненным достоинством Актовегина является хорошая переносимость, возможность длительного применения даже в относительно высоких дозировках [3,6]. Побочные эффекты в виде аллергических реакций (крапивница, отеки, лихорадка), тошноты, ощущения жара и усталости наблюдаются достаточно редко [9,12].
Оптимальная схема применения Актовегина при хронической форме ВБН на амбулаторном этапе: 200–400 мг (по 1–2 таблетки) 3 раза/сут в течение 4–6 недель. Кроме того, возможны курсы в/в вливаний препарата в дозе от 200 до 800 мг в/в капельно по 10–15 вливаний курсами 2–4 раза в год, предпочтительно в условиях стационара. При остром нарушении кровообращения в ВББ Актовегин назначается в дозе 1000–2000 мг в/в капельно 10–14 дней с последующим назначением таблетированной формы 200–400 мг (по 1–2 таблетки) 3 раза/сут в течение 4–6 недель.
Для мониторинга эффективности проводимой терапии наиболее часто применяется классический неврологический осмотр, однако современные диагностические методики позволяют получить более точные и достоверные результаты. Например, для оценки стато–локомоторых функций наиболее эффективно использование компьютерной стабилометрии, а применение перфузионной компьютерной томографии и позитронно–эмиссионной томографии позволяет точно оценить влияние проводимой терапии на кровоснабжение и метаболизм тканей мозга и обеспечить максимально точный подбор препаратов.
В качестве иллюстрации приводим два типичных клинических примера пациентов, нуждающихся в консервативном и оперативном лечении.
Консервативная терапия
Больной К, 48 лет, предъявляет жалобы на диффузную головную боль давящего характера больше в затылке, усиливающуюся утром и в процессе работы, снижение зрения («мушки»), выраженную утомляемость, снижение памяти, нарушение сна, эпизоды головокружения, периодический легкий шум в ушах, обычно сочетающийся с головокружением, эпизоды подъема АД до 150/90 мм рт.ст.
В анамнезе: данные жалобы беспокоят на протяжении не менее 5 лет, постепенно нарастая. ОНМК, ЧМТ отрицает. Работа сидячая с эпизодическими физическими нагрузками (системный администратор компьютерной сети). Вредные привычки – курение до 20–30 сигарет в день, алкоголь – умеренно, но регулярно (преимущественно пиво). Эпизоды ухудшения самочувствия связывает с перегрузками на работе.
Объективно: конституция гиперстеническая, рост 173 см, вес 109 кг. Шея укорочена, визуально–клиническая картина СФБ ВАГК. В легких дыхание диффузно ослаблено, отмечаются распространенные свистящие хрипы, единичные мелкопузырчатые, тоны сердца приглушены. ЧСС 88, ритмично, АД 130/85 мм рт.ст. Живот мягкий, б/б. Кожа чистая. Отмечается умеренная пастозность голеней.
В неврологическом статусе: в сознании, контактен, адекватен, ориентирован. ЧМН: легкий птоз левого века, незначительный двусторонний нистагм при взгляде в сторону, в остальном патологии не выявлено. Парезов и параличей нет. Чувствительных нарушений нет. Сухожильные рефлексы живые, D=S, патологических нет. В позе Ромберга пошатывание, п.н.п. и п.к.п. выполняет удовлетворительно.
ЭКГ – горизонтальное положение ЭОС, синусовый ритм, ЧСС 90.
R–графия грудной клетки: диффузный пневмосклероз, дисфункции ребер, характерные для СФБ ВАГК.
R–графия шейного отдела п–ка: гиперлордоз на уровне C1–C2, C2–C3, сглаженность с тенденцией к кифозированию C3–C4, C4–C5, при функциональных пробах элементы нестабильности C3–C4, C4–C5.
МСКТ– ангио: гемодинамически значимых изменений не выявлено.
Пациент проконсультирован мануальным терапевтом, подтвержден диагноз СФБ ВАГК, проведен курс мягкотканной мануальной коррекции с выраженным положительным эффектом. Даны рекомендации по ношению воротниковой шины Шанца, режиму труда и отдыха.
Фармакологическая терапия: курс в/в вливаний Актовегина в дозе 800 мг в/в капельно медленно № 10 через день, затем в таблетках 2 таб. (400 мг) 3 раза/сут в течение месяца; Цераксон 3 мл 3 раза/сут в течение месяца; бетагистин 24 мг в сутки в течение месяца.
На фоне проводимой терапии уже к концу 3–й недели лечения описанная симптоматика полностью купирована, пациент жалоб не предъявляет. Рекомендованы повторные курсы 2 раза в год.
Хирургическое лечение
Больной Ж., 51 год, активно жалоб не предъявляет, при опросе – иногда головокружение.
В анамнезе – профессиональный водитель, при очередном предрейсовом осмотре выявлено повышение АД. Пациент был направлен на консервативное лечение гипертензии без эффекта. В течение полутора недель отмечается выраженная нестабильность артериального давления в течение дня (от 90/50 до 130/80 мм рт.ст.), в норме пациент склонен к гипотонии. При очередном осмотре случайно выявлена разница в давлении на руках – слева на 25 мм рт.ст. ниже, после чего пациент обратился за консультацией к неврологу. Несколько месяцев назад имело место ДТП, в результате которого оставалась гематома от ремня безопасности.
Объективно: конституция нормостеническая, АД 130/85 мм рт.ст. Болезненность и отечность левого грудино–ключичного сочленения.
В неврологическом статусе: в сознании, контактен, адекватен, ориентирован. ЧМН: легкий горизонтальный нистагм при взгляде в стороны, в остальном без патологии, парезов и параличей нет, сухожильные рефлексы симметричны, патологических не выявляется. Чувствительных нарушений не выявлено. Отмечается диффузный миофасциальный синдром паравертебральных мышц на всех уровнях.
ЦДС МАГ: Ретроградный кровоток по левой позвоночной артерии.
С диагнозом «Синдром подключичного обкрадывания» пациент направлен к сосудистому хирургу для дообследования и решения вопроса об оперативном лечении. Запрещено управление транспортными средствами.
Таким образом, своевременная комплексная диагностика и адекватное патогенетически обоснованное лечение позволяют получить достичь хорошего клинического эффекта в сочетании с минимизацией побочных действий и фармакологической нагрузки на пациента, а также обеспечить профилактику вторичных осложнений, в частности, травматического характера.
Литература
1. Беневольская Н.Г., Евсеев В.Н., Румянцева С.А.. Антигипоксанты в реаниматологии и неврологии // Русск.мед.журн. – 2004 – Т.12, №22 – стр.1263–1267.
2. Васильева В.В., Васильев А.С. Шмырев В.И. Клинико–диагностическое значение, патогенез и возможности мануальной коррекции синдрома функционального блока верхней апертуры грудной клетки. – Ж. «Кремлевская медицина. Клинический вестник», №3, 2007, с. 81–84.
3. Гудкова В.В., Стаховская Л.В., Кирильченко Т.Д. и др. Применение Актовегина на разных этапах лечения больных с ишемическим инсультом. Ж. CONSILIUM MEDICUM / ТОМ 9 / № 8. – с. 22–25.
4. Гусев Е.И. Белоусов Ю.Б., Бойко А.Н. и др. Общие принципы проведения фармакоэкономических исследований в неврологии. Метод. рекомендации. – М. Издатель Е. Разумова, 2003. – 56с.
5. Дифференциальная диагностика нервных болезней: Руководство для врачей / под ред. Г.А. Акимова и М.М. Одинака. Изд. 3–е. – СПб.: Гиппократ+, 2004. – 744с.
6. Камчатнов П.Р., Чугунов А.В., Воловец С.А., Умарова Х.Я. Комбинированная терапия дис циркуляторной энцефалопатии. Сonsilium medicum. 2005; 7 (8): 686–92.
7. Пирадов М.А. Антиагрегантная терапия в профилактике повторных ишемических инсультов Русский медицинский журнал, 2003 г, том 11, № 12 с. 696–698.
8. Шмидт И.Р. Вертеброгенный синдром позвоночной артерии. – Новосибирск, Издатель, 2001. –299с.
9. Янсен В., Брукнер Г.В. Лечение хронической цереброваскулярной недостаточности с использованием драже Актовегин форте. Рос. мед. журн. 2002; 10 (12): 1–4.
10. Collaborative meta–analysis of randomised trials of antiplatelet therapy for prevention of death, myocardial infarction, and stroke in high risk patients. BMJ 2002 Jan 19;324(7330):141.
11. Law M R, Wald N J, Rudnicka A R, Quantifying effect of statins on low density lipoprotein cholesterol, ischaemic heart disease, and stroke: systematic review and meta–analysis. BMJ. 2003 Jun 28;326(7404):1423:
12. Letzel H, Schictiger U. Применение Актовегина у пожилых пациентов с органическим синдромом. Мультицентровое исследование 1549 пациентов. Рос.мед.журн. 2003; 11 (21): 3–6.












