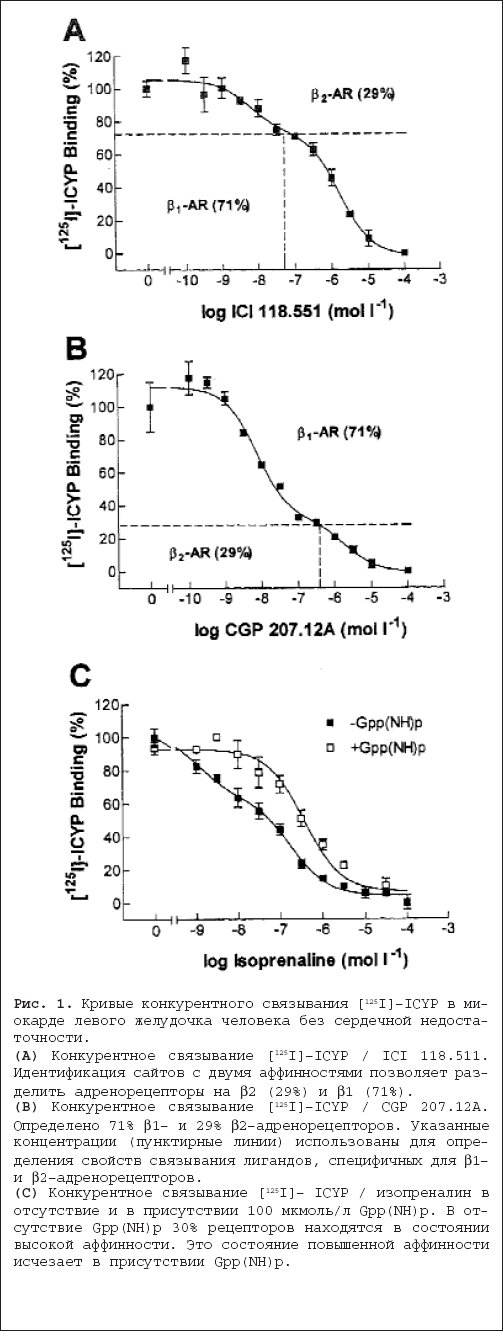
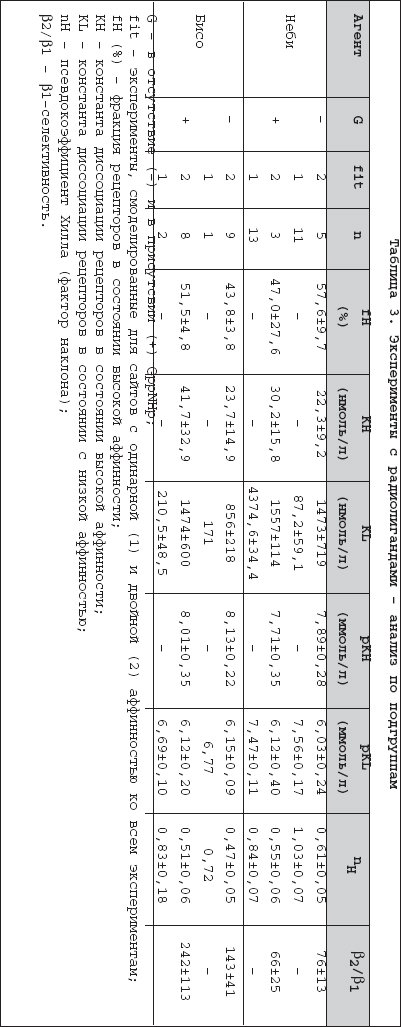
–£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О ќ≤вАУ–±–ї–Њ–Ї–∞—В–Њ—А—Л –Њ–Ї–∞–Ј—Л–≤–∞—О—В –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –љ–∞ —Д—Г–љ–Ї—Ж–Є—О –ґ–µ–ї—Г–і–Њ—З–Ї–Њ–≤ –Є –љ–∞ –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В—М. –≠—В–Є–Љ–Є –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є –Њ–±–ї–∞–і–∞—О—В ќ≤1вАУ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ ќ≤вАУ–±–ї–Њ–Ї–∞—В–Њ—А—Л –≤—В–Њ—А–Њ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П (–±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї, CIBIS II, 1999; –Љ–µ—В–Њ–њ—А–Њ–ї–Њ–ї, MERITвАУHF, 1999) –Є –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ ќ≤вАУ–±–ї–Њ–Ї–∞—В–Њ—А—Л —В—А–µ—В—М–µ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П ( –Ї–∞—А–≤–µ–і–Є–ї–Њ–ї , Packerr et al., 1996). –Т –Њ—В–ї–Є—З–Є–µ –Њ—В –љ–Є—Е –Ї—Б–∞–Љ–Њ—В–µ—А–Њ–ї, –њ–∞—А—Ж–Є–∞–ї—М–љ—Л–є –∞–≥–Њ–љ–Є—Б—В, –њ—А–Є–≤–Њ–і–Є–ї –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О —Б–Љ–µ—А—В–љ–Њ—Б—В–Є (Nicholas, 1990). –Э–µ–і–∞–≤–љ–µ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Б –±—Г—Ж–Є–љ–і–Њ–ї–Њ–ї–Њ–Љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О (–Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ BEST) –±—Л–ї–Њ –њ—А–µ–Ї—А–∞—Й–µ–љ–Њ –Є–ЈвАУ–Ј–∞ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–∞ [Bristow, 2000]. –Ф–Њ –љ–∞—Б—В–Њ—П—Й–µ–≥–Њ –≤—А–µ–Љ–µ–љ–Є –Њ–±—Б—Г–ґ–і–∞–µ—В—Б—П –≤–Њ–њ—А–Њ—Б –Њ —В–Њ–Љ, –Љ–Њ–ґ–µ—В –ї–Є –љ–µ–≥–∞—В–Є–≤–љ—Л–є —А–µ–Ј—Г–ї—М—В–∞—В —Н—В–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –±—Л—В—М –Њ–±—К—П—Б–љ–µ–љ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –≤—Л—Б–Њ–Ї–Њ–є –≤–љ—Г—В—А–µ–љ–љ–µ–є –Љ–Є–Љ–µ—В–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О –±—Г—Ж–Є–љ–і–Њ–ї–Њ–ї–∞, –Ї–Њ—В–Њ—А–∞—П –±—Л–ї–∞ –Њ–±–љ–∞—А—Г–ґ–µ–љ–∞ –≤ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞—Е –љ–∞ –ґ–Є–≤–Њ—В–љ—Л—Е [Willette et al., 1998] –Є –≤ –Љ–Є–Њ–Ї–∞—А–і–µ —З–µ–ї–Њ–≤–µ–Ї–∞ [Maack et al., 2000]. –≠—В–Є –і–∞–љ–љ—Л–µ –≥–Њ–≤–Њ—А—П—В –Њ —В–Њ–Љ, —З—В–Њ –њ—А–Є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є ќ≤вАУ–±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤ –і–Њ–ї–ґ–љ–∞ —Г—З–Є—В—Л–≤–∞—В—М—Б—П –Є—Е –≤–љ—Г—В—А–µ–љ–љ—П—П –Љ–Є–Љ–µ—В–Є—З–µ—Б–Ї–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М . –Э–µ–±–Є–≤–Њ–ї–Њ–ї –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є ќ≤вАУ–±–ї–Њ–Ї–∞—В–Њ—А —В—А–µ—В—М–µ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П, —П–≤–ї—П—П—Б—М —А–∞—Ж–µ–Љ–Є—З–µ—Б–Ї–Њ–є —Б–Љ–µ—Б—М—О —А–∞–≤–љ—Л—Е –Ї–Њ–ї–Є—З–µ—Б—В–≤ –Є–Ј–Њ–Љ–µ—А–Њ–≤ dвАУ(SRRRвАУ) –Є IвАУ(RSSSвАУ) –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞ . DвАУ–Є–Ј–Њ–Љ–µ—А —П–≤–ї—П–µ—В—Б—П –±–Њ–ї–µ–µ —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–Љ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є ќ≤1вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, —З—В–Њ –±—Л–ї–Њ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–Њ –љ–∞ —А–∞–Ј–ї–Є—З–љ—Л—Е –ґ–Є–≤–Њ—В–љ—Л—Е –Є –Ї–ї–µ—В–Њ—З–љ—Л—Е –Љ–Њ–і–µ–ї—П—Е [Pauwels et al., 1989;1991], –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї IвАУ–Є–Ј–Њ–Љ–µ—А –Њ—В–≤–µ—З–∞–µ—В –Ј–∞ –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—Ж–Є–Њ–љ–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л, –Њ–њ–Њ—Б—А–µ–і–Њ–≤–∞–љ–љ—Л–µ –≤—Л—А–∞–±–Њ—В–Ї–Њ–є –Њ–Ї—Б–Є–і–∞ –∞–Ј–Њ—В–∞ [Mangrella et al., 1998]. –Ю—Б–Њ–±–µ–љ–љ–Њ—Б—В—М—О –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞ —П–≤–ї—П–µ—В—Б—П —В–Њ, —З—В–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Б–µ—А–і–µ—З–љ–ЊвАУ—Б–Њ—Б—Г–і–Є—Б—В—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є, –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –Ї–ї–∞—Б—Б–Є—З–µ—Б–Ї–Є—Е ќ≤вАУ–±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤, –µ–≥–Њ –Њ–і–љ–Њ–Ї—А–∞—В–љ—Л–є –њ—А–Є–µ–Љ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –Є –њ–Њ–і–і–µ—А–ґ–∞–љ–Є–µ–Љ —Д—А–∞–Ї—Ж–Є–Є –≤—Л–±—А–Њ—Б–∞ –њ—А–Є —Б–љ–Є–ґ–µ–љ–Є–Є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П [Storelu et al., 1993]. –Я–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ –і–∞–љ–љ—Л–Љ –љ–µ–ї—М–Ј—П –Є—Б–Ї–ї—О—З–Є—В—М —В–Њ–≥–Њ, —З—В–Њ, –њ–Њ–Љ–Є–Љ–Њ –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—Ж–Є–Є, –Ј–∞ –Њ—Б—В—А–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Д—А–∞–Ї—Ж–Є–Є –≤—Л–±—А–Њ—Б–∞ –Љ–Њ–ґ–µ—В –Њ—В–≤–µ—З–∞—В—М –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є –Є–љ–Њ—В—А–Њ–њ–љ—Л–є, –Є–ї–Є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ—Л–є –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–є –Є–љ–Њ—В—А–Њ–њ–љ—Л–є —Н—Д—Д–µ–Ї—В –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞. –Ш–љ–Њ—В—А–Њ–њ–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –ї–Є–≥–∞–љ–і–Њ–≤ ќ≤вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –Њ–±—Л—З–љ–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ—Л –Є—Е –≤–љ—Г—В—А–µ–љ–љ–µ–є –Љ–Є–Љ–µ—В–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О. –Ф–ї—П –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞ –љ–µ –±—Л–ї–Њ –њ–Њ–ї—Г—З–µ–љ–Њ –і–∞–љ–љ—Л—Е –Њ –њ—А–Њ—П–≤–ї–µ–љ–Є–Є –≤–љ—Г—В—А–µ–љ–љ–µ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –≤ –Љ–Є–Њ–Ї–∞—А–і–µ —З–µ–ї–Њ–≤–µ–Ї–∞. –Т —Б–≤–Њ–µ–Љ—Б–≤–Њ–±–Њ–і–љ–Њ–Љ —Б–Њ—Б—В–Њ—П–љ–Є–Є ќ≤вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А —Б—Г—Й–µ—Б—В–≤—Г–µ—В –≤ —А–∞–≤–љ–Њ–≤–µ—Б–љ–Њ–Љ —Б–Њ—Б—В–Њ—П–љ–Є–Є –Љ–µ–ґ–і—Г –∞–Ї—В–Є–≤–љ–Њ–є (R*) –Є –љ–µ–∞–Ї—В–Є–≤–љ–Њ–є (R) –Ї–Њ–љ—Д–Њ—А–Љ–∞—Ж–Є—П–Љ–Є. –Я—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є–µ –∞–≥–Њ–љ–Є—Б—В–∞ –Є–љ–і—Г—Ж–Є—А—Г–µ—В –Ї–Њ–љ—Д–Њ—А–Љ–∞—Ж–Є–Њ–љ–љ—Л–µ –њ—А–µ–≤—А–∞—Й–µ–љ–Є—П –≤ —Б—В–Њ—А–Њ–љ—Г R*, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –Њ–±—А–∞—В–љ—Л–є –∞–≥–Њ–љ–Є—Б—В —Б—В–∞–±–Є–ї–Є–Ј–Є—А—Г–µ—В –љ–µ–∞–Ї—В–Є–≤–љ—Г—О —Д–Њ—А–Љ—Г —А–µ—Ж–µ–њ—В–Њ—А–∞ [Bond et al., 1995]. R*вАУ–Ї–Њ–љ—Д–Њ—А–Љ–∞—Ж–Є—П —А–µ—Ж–µ–њ—В–Њ—А–∞ –і–µ–ї–∞–µ—В –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–Љ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–µ —А–µ—Ж–µ–њ—В–Њ—А–∞ —Б–Њ —Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–Є–Љ GвАУ–њ—А–Њ—В–µ–Є–љ–Њ–Љ (Gs). –Я–Њ—Б–ї–µ–і—Г—О—Й–µ–µ –Њ—В—Б–Њ–µ–і–Є–љ–µ–љ–Є–µ ќ≤вАУ—Б—Г–±—К–µ–і–Є–љ–Є—Ж—Л –Њ—В ?ќ≤вАУ—Б—Г–±—К–µ–і–Є–љ–Є—Ж Gs —Б—В–Є–Љ—Г–ї–Є—А—Г–µ—В –∞–і–µ–љ–Є–ї–∞—В—Ж–Є–Ї–ї–∞–Ј—Г. –Т –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Е–∞—А–∞–Ї—В–µ—А–∞ —А–µ—Ж–µ–њ—В–Њ—А–љ—Л—Е —Б–Є—Б—В–µ–Љ –Є —Г—Б–ї–Њ–≤–Є–є —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞ (–љ–∞–њ—А–Є–Љ–µ—А, —А–∞–Ј–ї–Є—З–љ–∞—П —Б—В–µ—Е–Є–Њ–Љ–µ—В—А–Є—П —А–µ—Ж–µ–њ—В–Њ—А–∞/GвАУ–±–µ–ї–Ї–∞, —А–∞–Ј–ї–Є—З–љ—Л–µ —Б–Њ—Б—В–Њ—П–љ–Є—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є —А–µ—Ж–µ–њ—В–Њ—А–∞, –Є —В.–і.) –Њ–і–Є–љ –Є —В–Њ—В –ґ–µ –ї–Є–≥–∞–љ–і –Љ–Њ–ґ–µ—В –≤–µ—Б—В–Є —Б–µ–±—П –Ї–∞–Ї –Њ–±—А–∞—В–љ—Л–є –∞–≥–Њ–љ–Є—Б—В, –љ–µ–є—В—А–∞–ї—М–љ—Л–є –∞–љ—В–∞–≥–Њ–љ–Є—Б—В –Є–ї–Є –і–∞–ґ–µ –Ї–∞–Ї —З–∞—Б—В–Є—З–љ—Л–є –∞–≥–Њ–љ–Є—Б—В [De Light et al., 2000; Chidiac et al., 1996]. –Т –љ–∞—Б—В–Њ—П—Й–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –≤ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞—Е —Б –ї–Є–≥–∞–љ–і–∞–Љ–Є, –Љ–µ—З–µ–љ—Л–Љ–Є [ 125 I]вАУ–є–Њ–і–Њ—Ж–Є–∞–љ–Њ–њ–Є–љ–і–Њ–ї–Њ–ї–Њ–Љ, –Є–Ј—Г—З–∞–ї–Њ—Б—М –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–µ ќ≤вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–∞ –Є GвАУ–±–µ–ї–Ї–∞ –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ –љ–Њ–≤–Њ–≥–Њ ќ≤вАУ–±–ї–Њ–Ї–∞—В–Њ—А–∞ –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞ –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї–Њ–Љ, –≤ –Њ—В—Б—Г—В—Б—В–≤–Є–µ –Є –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є –≥—Г–∞–љ–Є–ї–Є–ї–Є–Љ–Є–і–Њ–і–Є—Д–Њ—Б—Д–∞—В–∞ (Gpp(Nh)p). –С–Њ–ї–µ–µ —В–Њ–≥–Њ, –≤ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞—Е –љ–∞ –Љ–Є–Њ–Ї–∞—А–і–µ —З–µ–ї–Њ–≤–µ–Ї–∞ —Б—А–∞–≤–љ–Є–≤–∞–ї–∞—Б—М –≤–љ—Г—В—А–µ–љ–љ—П—П –Љ–Є–Љ–µ—В–Є—З–µ—Б–Ї–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞ –Є –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї–∞, –Љ–µ—В–Њ–њ—А–Њ–ї–Њ–ї–∞, –Ї–∞—А–≤–µ–і–Є–ї–Њ–ї–∞ –Є –±—Г—Ж–Є–љ–і–Њ–ї–Њ–ї–∞. –Т —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞—Е –љ–∞ –ґ–Є–≤–Њ—В–љ—Л—Е –Є –љ–∞ –Ї–ї–µ—В–Њ—З–љ—Л—Е –Ї—Г–ї—М—В—Г—А–∞—Е –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –љ–µ–±–Є–≤–Њ–ї–Њ–ї –Њ–±–ї–∞–і–∞–µ—В –≤—Л—Б–Њ–Ї–Њ–є ќ≤1вАУ—Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О [Pauwels et al., 1989; 1991]. –Ю–і–љ–∞–Ї–Њ –і–Њ –љ–∞—Б—В–Њ—П—Й–µ–≥–Њ –≤—А–µ–Љ–µ–љ–Є –њ—А—П–Љ–Њ–є –Њ—Ж–µ–љ–Ї–Є —Б–≤—П–Ј—Л–≤–∞–љ–Є—П –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞ —Б ќ≤1вАУ –Є ќ≤2вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–∞–Љ–Є –Љ–Є–Њ–Ї–∞—А–і–∞ —З–µ–ї–Њ–≤–µ–Ї–∞ –љ–µ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М. –Т –љ–∞—Б—В–Њ—П—Й–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –∞—Д—Д–Є–љ–љ–Њ—Б—В—М –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞ –Є –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї–∞ –Ї ќ≤1вАУ –Є ќ≤2вАУ–∞–і–Њ—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–∞–Љ –Њ—Ж–µ–љ–Є–≤–∞–ї–∞—Б—М –≤ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞—Е —Б —А–∞–і–Є–Њ–∞–Ї—В–Є–≤–љ–Њ –Љ–µ—З–µ–љ—Л–Љ–Є –ї–Є–≥–∞–љ–і–∞–Љ–Є, –≤ –Њ—В—Б—Г—В—Б—В–≤–Є–µ –Є –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є ICI 118.551 –Є CGP 207.12A —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ. –С–Њ–ї–µ–µ —В–Њ–≥–Њ, —А–µ–Ј—Г–ї—М—В–∞—В—Л —Н—В–Є—Е —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–Њ–≤ –љ–∞ –Љ–Є–Њ–Ї–∞—А–і–µ —З–µ–ї–Њ–≤–µ–Ї–∞ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П–Љ–Є –љ–∞ –Ї–ї–µ—В–Ї–∞—Е COSвАУ7, —Б–Њ–і–µ—А–ґ–∞—Й–Є—Е —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–µ ќ≤1вАУ –Є ќ≤2вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А—Л. –Ь–µ—В–Њ–і—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Ґ–Ї–∞–љ—М –Љ–Є–Њ–Ї–∞—А–і–∞ –≠–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В—Л –њ—А–Њ–≤–Њ–і–Є–ї–Є—Б—М –љ–∞ —В–Ї–∞–љ–Є —В—А–∞–±–µ–Ї—Г–ї–ї—Л –Є–Ј –њ—А–∞–≤–Њ–≥–Њ –њ—А–µ–і—Б–µ—А–і–Є—П —З–µ–ї–Њ–≤–µ–Ї–∞, –њ–Њ–ї—Г—З–µ–љ–љ–Њ–є –≤ —Е–Њ–і–µ –Њ–њ–µ—А–∞—Ж–Є–є –њ–Њ —И—Г–љ—В–Є—А–Њ–≤–∞–љ–Є—О –љ–∞ –Њ—В–Ї—А—Л—В–Њ–Љ —Б–µ—А–і—Ж–µ, –Є –љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞—Е –Љ—Л—И–µ—З–љ–Њ–є –њ–Њ–ї–Њ—Б–Ї–Є –Є–Ј –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞, –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е –Њ—В —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ —Б–Њ—Б—В–Њ—П—В–µ–ї—М–љ—Л—Е –Є –љ–µ—Б–Њ—Б—В–Њ—П—В–µ–ї—М–љ—Л—Е —Б–µ—А–і–µ—Ж –≤ —Е–Њ–і–µ –Њ–њ–µ—А–∞—Ж–Є–є –њ–Њ —В—А–∞–љ—Б–њ–ї–∞–љ—В–∞—Ж–Є–Є —Б–µ—А–і—Ж–∞. –Ґ–Ї–∞–љ–Є –љ–µ–Љ–µ–і–ї–µ–љ–љ–Њ –і–Њ—Б—В–∞–≤–ї—П–ї–Є—Б—М –≤ –ї–∞–±–Њ—А–∞—В–Њ—А–Є—О –Є –њ–Њ–і–≥–Њ—В–∞–≤–ї–Є–≤–∞–ї–Є—Б—М –і–ї—П –њ—А–Њ–≤–µ–і–µ–љ–Є—П —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞. –Ю–±—А–∞–Ј—Ж—Л —В–Ї–∞–љ–µ–є –і–ї—П —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–Њ–≤ –њ–Њ —Б–≤—П–Ј—Л–≤–∞–љ–Є—О —Б —А–µ—Ж–µ–њ—В–Њ—А–∞–Љ–Є –і–Њ –∞–љ–∞–ї–Є–Ј–∞ —Е—А–∞–љ–Є–ї–Є—Б—М –њ—А–Є —В–µ–Љ–њ–µ—А–∞—В—Г—А–µ вАУ80¬∞–°. –§—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ –љ–µ—Б–Њ—Б—В–Њ—П—В–µ–ї—М–љ—Л–є –Љ–Є–Њ–Ї–∞—А–і –±—Л–ї –њ–Њ–ї—Г—З–µ–љ –Њ—В 17 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —В–µ—А–Љ–Є–љ–∞–ї—М–љ–Њ–є —Б—В–∞–і–Є–µ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є (–њ–Њ –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є–Є –Р–Љ–µ—А–Є–Ї–∞–љ—Б–Ї–Њ–є –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Њ–≤, IV –Ї–ї–∞—Б—Б NYHA), —А–∞–Ј–≤–Є–≤—И–µ–є—Б—П –≤ –Є—Б—Е–Њ–і–µ –ї–Є–±–Њ –Є–і–Є–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є (n=7), –ї–Є–±–Њ –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–є (n=10) –Ї–∞—А–і–Є–Њ–Љ–Є–Њ–њ–∞—В–Є–Є (15 –Љ—Г–ґ—З–Є–љ, 2 –ґ–µ–љ—Й–Є–љ—Л; –≤–Њ–Ј—А–∞—Б—В 55¬±1 –≥–Њ–і). –Ґ–Ї–∞–љ—М —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ —Б–Њ—Б—В–Њ—П—В–µ–ї—М–љ—Л—Е —Б–µ—А–і–µ—Ж –±—Л–ї–∞ –њ–Њ–ї—Г—З–µ–љ–∞ –Њ—В –њ—П—В–Є –і–Њ–љ–Њ—А–Њ–≤, —З—М–Є —Б–µ—А–і—Ж–∞ –љ–µ –Љ–Њ–≥–ї–Є –±—Л—В—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ—Л –і–ї—П —В—А–∞–љ—Б–њ–ї–∞–љ—В–∞—Ж–Є–Є (4 –Љ—Г–ґ—З–Є–љ, 1 –ґ–µ–љ—Й–Є–љ–∞; –≤–Њ–Ј—А–∞—Б—В 45¬±4 –≥–Њ–і–∞). –Т –њ–Њ—Б–ї–µ–і–љ–µ–є –≥—А—Г–њ–њ–µ –љ–Њ—А–Љ–∞–ї—М–љ–∞—П —Б–Њ–Ї—А–∞—В–Є—В–µ–ї—М–љ–∞—П —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –±—Л–ї–∞ –і–Њ–Ї–∞–Ј–∞–љ–∞ —Н—Е–Њ–Ї–∞—А–і–Є–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є. –Я–∞—Ж–Є–µ–љ—В—Л —Б –Ї–Њ—А–Њ–љ–∞—А–љ—Л–Љ —И—Г–љ—В–Є—А–Њ–≤–∞–љ–Є–µ–Љ (—Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В 67¬±2 –≥–Њ–і–∞, 17 –Љ—Г–ґ—З–Є–љ, 6 –ґ–µ–љ—Й–Є–љ) –љ–µ –Є–Љ–µ–ї–Є –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –і–Є–ї–∞—В–∞—Ж–Є–Є –њ—А–µ–і—Б–µ—А–і–Є–є –Є–ї–Є –њ—А–µ–і—Б–µ—А–і–љ—Л—Е –∞—А–Є—В–Љ–Є–є, –∞ —В–∞–Ї–ґ–µ –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞. –Т—Б–µ –њ–∞—Ж–Є–µ–љ—В—Л –њ–µ—А–µ–і –њ—А–Њ–≤–µ–і–µ–љ–Є–µ–Љ –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–≥–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ –і–∞–ї–Є –Є–љ—Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–љ–Њ–µ –њ–Є—Б—М–Љ–µ–љ–љ–Њ–µ —Б–Њ–≥–ї–∞—Б–Є–µ –љ–∞ –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –±–Є–Њ–њ—Б–Є–Є. –Я–Њ—Б–Ї–Њ–ї—М–Ї—Г –љ–µ–±–Є–≤–Њ–ї–Њ–ї –Є –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї —Б—А–∞–≤–љ–Є–≤–∞–ї–Є—Б—М –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –љ–∞ –Њ–±—А–∞–Ј—Ж–∞—Е —В–Ї–∞–љ–Є –Њ—В –Њ–і–љ–Є—Е –Є —В–µ—Е –ґ–µ —Б–µ—А–і–µ—Ж (—Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В—Л –Є —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В—Л –њ–Њ —Б–≤—П–Ј—Л–≤–∞–љ–Є—О –ї–Є–≥–∞–љ–і–Њ–≤), —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –њ–Њ –њ–Њ–ї—Г, –≤–Њ–Ј—А–∞—Б—В—Г –Є –њ—А–Є–љ–Є–Љ–∞–µ–Љ—Л–Љ –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–∞–Љ –Љ–µ–ґ–і—Г —Н—В–Є–Љ–Є –і–≤—Г–Љ—П –≥—А—Г–њ–њ–∞–Љ–Є –љ–µ –±—Л–ї–Њ. –Я—А–µ–њ–∞—А–∞—В—Л —В–Ї–∞–љ–µ–є –і–ї—П —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–Њ–≤ –Є –њ—А–µ–њ–∞—А–∞—В—Л –Љ–µ–Љ–±—А–∞–љ –і–ї—П —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–Њ–≤ –њ–Њ —Б–≤—П–Ј—Л–≤–∞–љ–Є—О –ї–Є–≥–∞–љ–і–Њ–≤ –Њ–њ–Є—Б–∞–љ—Л –≤ –і—А—Г–≥–Є—Е –њ—Г–±–ї–Є–Ї–∞—Ж–Є—П—Е [Maack et al., 2000; Boehm et al., 1990b]. –Я–Њ–і–≥–Њ—В–Њ–≤–Ї–∞ –Є–Ј–Њ–ї–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ–Њ–ї–Њ—Б —Б–µ—А–і–µ—З–љ–Њ–є –Љ—Л—И—Ж—Л –Є –Є–Ј–Љ–µ—А–µ–љ–Є–µ —Б–Є–ї—Л —Б–Њ–Ї—А–∞—Й–µ–љ–Є—П –Ш–Ј–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–∞—П —Б–Є–ї–∞ —Б–Њ–Ї—А–∞—Й–µ–љ–Є–є –Њ–њ—А–µ–і–µ–ї—П–ї–∞—Б—М –љ–∞ –Є–Ј–Њ–ї–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ–Њ–ї–Њ—Б–∞—Е –Љ–Є–Њ–Ї–∞—А–і–∞ –њ–Њ –Њ–њ–Є—Б–∞–љ–љ–Њ–є —А–∞–љ–µ–µ –Љ–µ—В–Њ–і–Є–Ї–µ [Boehm et al., 1990b]. –†–∞—Б—В–≤–Њ—А –і–ї—П –њ—А–µ–њ–∞—А–∞—В–∞ —Б–Њ–і–µ—А–ґ–∞–ї—Б—П –њ—А–Є —В–µ–Љ–њ–µ—А–∞—В—Г—А–µ 37¬∞–° –Є –њ—А–Є —А–Э 7,4, –∞ —В–∞–Ї–ґ–µ –∞—Н—А–Є—А–Њ–≤–∞–ї—Б—П —Б–Љ–µ—Б—М—О –Є–Ј 95% –Ї–Є—Б–ї–Њ—А–Њ–і–∞ –Є 5% —Г–≥–ї–µ–Ї–Є—Б–ї–Њ–≥–Њ –≥–∞–Ј–∞. –Ь—Л—И—Ж—Л —Б—В–∞–љ–і–∞—А—В–љ–Њ–≥–Њ —А–∞–Ј–Љ–µ—А–∞ (–і–ї–Є–љ–Њ–є 5вАУ6 –Љ–Љ –Є —В–Њ–ї—Й–Є–љ–Њ–є 1вАУ2 –Љ–Љ) –±—Л–ї–Є —А–∞—Б—В—П–љ—Г—В—Л –і–Њ –і–ї–Є–љ—Л, –њ—А–Є –Ї–Њ—В–Њ—А–Њ–є —Б–Є–ї–∞ —Б–Њ–Ї—А–∞—Й–µ–љ–Є–є –±—Л–ї–∞ –±—Л –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є (5вАУ8 –Љ–Э). –Т —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞—Е —Б –Є–љ–Њ—В—А–Њ–њ–љ–Њ–є –њ—А–µ–і—Б—В–Є–Љ—Г–ї—П—Ж–Є–µ–є –њ–Њ–ї–Њ—Б—Л –Љ—Л—И–µ—З–љ–Њ–є —В–Ї–∞–љ–Є –њ—А–µ–і–≤–∞—А–Є—В–µ–ї—М–љ–Њ –≤—Л–і–µ—А–ґ–Є–≤–∞–ї–Є—Б—М –≤ —В–µ—З–µ–љ–Є–µ 30 –Љ–Є–љ—Г—В –≤ —А–∞—Б—В–≤–Њ—А–µ –Є–Ј–Њ–њ—А–µ–љ–∞–ї–Є–љ–∞ (1 –Љ–Ї–Љ–Њ–ї—М/–ї, ќ≤–Х–°90), –∞ –Ј–∞—В–µ–Љ –≤ —А–∞—Б—В–≤–Њ—А–µ —Д–Њ—А—Б–Ї–Њ–ї–Є–љ–∞ (0,3 –Љ–Ї–Љ–Њ–ї—М/–ї, ќ≤–Х–°50) –≤ —В–µ—З–µ–љ–Є–µ –њ–Њ –Ї—А–∞–є–љ–µ–є –Љ–µ—А–µ 45 –Љ–Є–љ—Г—В. –Р–љ—В–∞–≥–Њ–љ–Є—Б—В—Л ќ≤вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –љ–µ–±–Є–≤–Њ–ї–Њ–ї (1вАУ10 000 –љ–Љ–Њ–ї—М/–ї), –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї (1вАУ10 000 –љ–Љ–Њ–ї—М/–ї), –±—Г—Ж–Є–љ–і–Њ–ї–Њ–ї (0,11вАУ1000 –љ–Љ–Њ–ї—М/–ї), –Ї–∞—А–≤–µ–і–Є–ї–Њ–ї (0,1вАУ1000 –љ–Љ–Њ–ї—М/–ї) –Є –Љ–µ—В–Њ–њ—А–Њ–ї–Њ–ї (1вАУ100 000 –љ–Љ–Њ–ї—М/–ї) –Ї—Г–Љ—Г–ї—П—В–Є–≤–љ–Њ –і–Њ–±–∞–≤–ї—П–ї–Є—Б—М –≤ –≤–∞–љ–љ–Њ—З–Ї—Г —Б –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –љ–∞ 30 –Љ–Є–љ—Г—В –і–ї—П –Ї–∞–ґ–і–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є. –Х—Б–ї–Є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П ќ≤вАУ–±–ї–Њ–Ї–∞—В–Њ—А–∞ –Њ–±–Њ–Ј–љ–∞—З–∞–ї–∞—Б—М –Ї–∞–Ї Ki –Є–ї–Є 100 x Ki (–≥–Є—Б—В–Њ–≥—А–∞–Љ–Љ—Л), —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ–Њ–ї—Г—З–∞–ї–Є—Б—М –Є–Ј —Н—В–Є—Е –Ї—Г–Љ—Г–ї—П—В–Є–≤–љ—Л—Е –Ї—А–Є–≤—Л—Е ¬Ђ–і–Њ–Ј–∞вАУ—А–µ–∞–Ї—Ж–Є—П¬ї. –Т –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ –±–µ–Ј –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П ќ≤вАУ–±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤ –µ—Б—В–µ—Б—В–≤–µ–љ–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Є–ї—Л —Б–Њ–Ї—А–∞—В–Є–Љ–Њ—Б—В–Є –Њ–њ—А–µ–і–µ–ї—П–ї–Њ—Б—М –љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞—Е –Љ–Є–Њ–Ї–∞—А–і–∞ –њ—А–µ–і—Б–µ—А–і–Є–є. –°–љ–Є–ґ–µ–љ–Є–µ —Б–Њ–Ї—А–∞—В–Є–Љ–Њ—Б—В–Є –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–µ–≥–Њ ќ≤вАУ–±–ї–Њ–Ї–∞—В–Њ—А–∞ —Б–Њ–њ–Њ—Б—В–∞–≤–ї—П–ї–Њ—Б—М —Б–Њ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —Б–Њ–Ї—А–∞—В–Є–Љ–Њ—Б—В–Є –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ. –Т –Љ–Є–Њ–Ї–∞—А–і–µ –њ—А–µ–і—Б–µ—А–і–Є–є –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л —Б–Є–ї–∞ —Б–Њ–Ї—А–∞—Й–µ–љ–Є–є –Њ—Б—В–∞–≤–∞–ї–∞—Б—М –њ–Њ—Б—В–Њ—П–љ–љ–Њ–є. –Ъ—Г–ї—М—В—Г—А–∞ –Ї–ї–µ—В–Њ–Ї –Є —В—А–∞–љ—Б—Д–µ–Ї—Ж–Є—П –Ъ–ї–µ—В–Ї–Є COSвАУ7 –Ї—Г–ї—М—В–Є–≤–Є—А–Њ–≤–∞–ї–Є—Б—М –Є –њ–Њ–і–≤–µ—А–≥–ї–Є—Б—М —В—А–∞–љ—Б—Д–µ–Ї—Ж–Є–Є —Б—В–∞–љ–і–∞—А—В–љ—Л–Љ —А–µ–∞–≥–µ–љ—В–Њ–Љ (Pomega, Heidelberg, Germany) –њ–Њ –Њ–њ–Є—Б–∞–љ–љ–Њ–є —А–∞–љ–µ–µ –Љ–µ—В–Њ–і–Є–Ї–µ [Schnabel et al., 1993]. –Я—А–µ–њ–∞—А–∞—В—Л –Љ–µ–Љ–±—А–∞–љ –≥–Њ—В–Њ–≤–Є–ї–Є—Б—М, –Ї–∞–Ї –Њ–њ–Є—Б–∞–љ–Њ —А–∞–љ–µ–µ [Schnabel et al., 1993] –Ј–∞ –Є—Б–Ї–ї—О—З–µ–љ–Є–µ–Љ —В–Њ–≥–Њ, —З—В–Њ –Ї–Њ–Љ–Њ—З–Ї–Є —В–Ї–∞–љ–Є –±—Л–ї–Є –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ –њ–Њ–і–≤–µ—А–≥–љ—Г—В—Л —Б—Г—Б–њ–µ–љ–Ј–Є—А–Њ–≤–∞–љ–Є—О –≤ –±—Г—Д–µ—А–µ, —Б–Њ–і–µ—А–ґ–∞—Й–µ–Љ 50 –Љ–Љ–Њ–ї—М/–ї Tris/HCl, pH 7,4 –Є 10 –Љ–Љ–Њ–ї—М/–ї MgCl2. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б–≤—П–Ј—Л–≤–∞–љ–Є—П —Б ќ≤вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–∞–Љ–Є ќ≤вАУ—А–µ—Ж–µ–њ—В–Њ—А—Л —Б–µ—А–і–µ—З–љ–Њ–є —В–Ї–∞–љ–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–ї–Є—Б—М —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —А–∞–і–Є–Њ–∞–Ї—В–Є–≤–љ–Њ –Љ–µ—З–µ–љ–Њ–≥–Њ –ї–Є–≥–∞–љ–і–∞ [ 125 I]вАУ–є–Њ–і–Њ—Ж–Є–∞–љ–Њ–њ–Є–љ–і–Њ–ї–Њ–ї–∞ (ICYP). –°–≤—П–Ј—Л–≤–∞—О—Й–∞—П —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —Е–Њ–ї–Њ–і–љ–Њ–≥–Њ –ї–Є–≥–∞–љ–і–∞ –Є–Ј–Љ–µ—А—П–ї–∞—Б—М –њ–Њ –Ї—А–Є–≤—Л–Љ –Ї–Њ–љ–Ї—Г—А–µ–љ—Ж–Є–Є ICYPвАУ–ї–Є–≥–∞–љ–і–∞ —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ ICYP –≤ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є 37,5 –Љ–Љ–Њ–ї—М/–ї –і–ї—П –њ–Њ–і–і–µ—А–ґ–∞–љ–Є—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є —А–∞–і–Є–Њ–ї–Є–≥–∞–љ–і–∞ –љ–∞ —Г—А–Њ–≤–љ–µ Kd . –Р–љ–∞–ї–Є–Ј –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–ї—Б—П –≤ –Њ–±—Й–µ–Љ –Њ–±—К–µ–Љ–µ 250 –Љ–Ї–ї. –Ю–±—Й–µ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–љ–Њ–≥–Њ –њ—А–Њ—В–µ–Є–љ–∞ —Б–Њ—Б—В–∞–≤–ї—П–ї–Њ 20вАУ30 –Љ–Ї–≥. –Ъ–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –њ—А–Њ—В–µ–Є–љ–∞ –Њ–њ—А–µ–і–µ–ї—П–ї–∞—Б—М –њ–Њ –Љ–µ—В–Њ–і—Г –Ы–∞—Г—А–Є [Lowry et al., 1951]. –Ф–ї—П –Ј–∞–≤–µ—А—И–µ–љ–Є—П —Н–Ї–≤–Є–ї–Є–±—А–∞—Ж–Є–Є ќ≤вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ —Б —А–∞–і–Є–Њ–ї–Є–≥–∞–љ–і–Њ–Љ –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М –Є–љ–Ї—Г–±–∞—Ж–Є—П –њ—А–Є 25¬∞–° –≤ —В–µ—З–µ–љ–Є–µ 60 –Љ–Є–љ—Г—В. –†–µ–∞–Ї—Ж–Є—П –њ—А–µ–Ї—А–∞—Й–∞–ї–∞—Б—М –њ—Г—В–µ–Љ –±—Л—Б—В—А–Њ–є –≤–∞–Ї—Г—Г–Љ–љ–Њ–є —Д–Є–ї—М—В—А–∞—Ж–Є–Є —З–µ—А–µ–Ј —Д–Є–ї—М—В—А—Л –Т–∞—В–Љ–∞–љ–∞ GF/C (Whatman Inc., Cifton, NJ, USA). –§–Є–ї—М—В—А—Л –љ–µ–Љ–µ–і–ї–µ–љ–љ–Њ –њ—А–Њ–Љ—Л–≤–∞–ї–Є—Б—М 3 —А–∞–Ј–∞ 6 –Љ–ї –Њ—Е–ї–∞–ґ–і–µ–љ–љ–Њ–≥–Њ –≤–Њ –ї—М–і—Г –Є–љ–Ї—Г–±–∞—Ж–Є–Њ–љ–љ–Њ–≥–Њ –±—Г—Д–µ—А–∞. –Т—Б–µ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В—Л –њ—А–Њ–≤–Њ–і–Є–ї–Є—Б—М —В—А–Є–ґ–і—Л. –°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј –†–µ–≥—А–µ—Б—Б–Є–Њ–љ–љ—Л–є –∞–љ–∞–ї–Є–Ј –њ—А–Њ–≤–Њ–і–Є–ї—Б—П —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–Њ–є –њ—А–Њ–≥—А–∞–Љ–Љ—Л GraphPadPrism (GraphPad Software, SanDiego, CA, USA). –Э–∞–Ї–ї–Њ–љ –Ї–Њ–љ–Ї—Г—А–µ–љ—В–љ–Њ–є –Ї—А–Є–≤–Њ–є (–њ—Б–µ–≤–і–Њ–Ї–Њ—Н—Д—Д–Є—Ж–Є–µ–љ—В –•–Є–ї–ї–∞, nH), –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П, –њ—А–Є –Ї–Њ—В–Њ—А–Њ–є –Ј–∞–љ–Є–Љ–∞–ї–Њ—Б—М 50% –≤—Б–µ—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ (–Х–°50) –Є –њ—А–Њ—Ж–µ–љ—В —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –≤ —Б–Њ—Б—В–Њ—П–љ–Є—П—Е –≤—Л—Б–Њ–Ї–Њ–є –∞—Д—Д–Є–љ–љ–Њ—Б—В–Є (%RH) –Є –љ–Є–Ј–Ї–Њ–є –∞—Д—Д–Є–љ–љ–Њ—Б—В–Є (%RL) –Њ–њ—А–µ–і–µ–ї—П–ї–Є—Б—М –њ—Г—В–µ–Љ –љ–µ–ї–Є–љ–µ–є–љ–Њ–≥–Њ —А–µ–≥—А–µ—Б—Б–Є–Њ–љ–љ–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞, —Б–Њ–њ–Њ—Б—В–∞–≤–ї—П—П –њ–Њ–ї—Г—З–µ–љ–љ—Г—О –Ї—А–Є–≤—Г—О —Б –Њ–і–љ–Є–Љ –Є–Ј –і–≤—Г—Е —Б–Њ—Б—В–Њ—П–љ–Є–є —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –≤ FвАУ—В–µ—Б—В–µ. –Ъ–Њ–љ—Б—В–∞–љ—В—Л –і–Є—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є —Е–Њ–ї–Њ–і–љ–Њ–≥–Њ –ї–Є–≥–∞–љ–і–∞ –і–ї—П —Б–Њ—Б—В–Њ—П–љ–Є—П –≤—Л—Б–Њ–Ї–Њ–є –∞—Д—Д–Є–љ–љ–Њ—Б—В–Є (KH) –Є–ї–Є –љ–Є–Ј–Ї–Њ–є –∞—Д—Д–Є–љ–љ–Њ—Б—В–Є (KL) —А–∞—Б—Б—З–Є—В—Л–≤–∞–ї–Є—Б—М –њ–Њ –Љ–µ—В–Њ–і—Г –І–µ–љ–≥–∞ –Є –Я—А—Г—Б—Б–Њ–≤–∞ [Cheng & Prussoff, 1973]. –Ч–љ–∞—З–µ–љ–Є—П –Ъi —А–∞—Б—Б—З–Є—В—Л–≤–∞–ї–Є—Б—М –Є–Ј –Ј–љ–∞—З–µ–љ–Є–є –Х–°50, –Ї–Њ—В–Њ—А—Л–µ –Њ–њ—А–µ–і–µ–ї—П–ї–Є—Б—М –њ—Г—В–µ–Љ —Б–Њ–њ–Њ—Б—В–∞–≤–ї–µ–љ–Є—П —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Ї–Њ–љ–Ї—Г—А–µ–љ—В–љ—Л—Е —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–Њ–≤ —Б –љ–µ–ї–Є–љ–µ–є–љ—Л–Љ —А–µ–≥—А–µ—Б—Б–Є–Њ–љ–љ—Л–Љ –∞–љ–∞–ї–Є–Ј–Њ–Љ, —Г—З–Є—В—Л–≤–∞—П —В–Њ–ї—М–Ї–Њ –Њ–і–љ–Њ —Б–Њ—Б—В–Њ—П–љ–Є–µ —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, –Є –≤–љ–µ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —В–Њ–≥–Њ, –Њ—В—А–∞–ґ–∞—О—В –ї–Є –Њ–љ–Є –Њ–і–љ–Њ –Є–ї–Є –і–≤–∞ —Б–Њ—Б—В–Њ—П–љ–Є—П –∞—Д—Д–Є–љ–љ–Њ—Б—В–Є. –Х—Б–ї–Є –Њ—Б–Њ–±–Њ –љ–µ —Г–Ї–∞–Ј–∞–љ–Њ, —В–Њ —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ –≤–Є–і–µ —Б—А–µ–і–љ–Є—Е –Ј–љ–∞—З–µ–љ–Є–є ¬± —Б—В. –Њ—И–Є–±–Ї–∞ —Б—А–µ–і–љ–µ–≥–Њ. –Ф–ї—П –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ—Л—Е —Б—А–∞–≤–љ–µ–љ–Є–є –њ—А–Њ–≤–Њ–і–Є–ї—Б—П –Љ—Г–ї—М—В–Є–≤–∞—А–Є–∞–љ—В–љ—Л–є –∞–љ–∞–ї–Є–Ј ANOVA. –Т –і—А—Г–≥–Є—Е —Б–ї—Г—З–∞—П—Е —Г—А–Њ–≤–µ–љ—М —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–є –Ј–љ–∞—З–Є–Љ–Њ—Б—В–Є –Њ–њ—А–µ–і–µ–ї—П–ї—Б—П –њ—А–Є –њ–Њ–Љ–Њ—Й–Є —В–µ—Б—В–Њ–≤ –Ь–∞–љ–љ–∞вАУ–£–Є—В–љ–Є –Є–ї–Є –Т–Є–ї–Ї–Њ–Ї—Б–Њ–љ–∞. –Ч–љ–∞—З–Є–Љ—Л–Љ —Б—З–Є—В–∞–ї–Њ—Б—М –Ј–љ–∞—З–µ–љ–Є–µ p< 0,05. –†–µ–Ј—Г–ї—М—В–∞—В—Л –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ —Б–≤—П–Ј—Л–≤–∞–љ–Є—О —А–∞–і–Є–Њ–ї–Є–≥–∞–љ–і–∞ –Э–∞ —А–Є—Б—Г–љ–Ї–µ 1 –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л —А–µ–њ—А–µ–Ј–µ–љ—В–∞—В–Є–≤–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–Њ–≤ –њ–Њ –Ї–Њ–љ–Ї—Г—А–Є—А–Њ–≤–∞–љ–Є—О –ї–Є–≥–∞–љ–і–Њ–≤ ќ≤вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ ICI 118.551, GCP 207.12A –Є –Є–Ј–Њ–њ—А–µ–љ–∞–ї–Є–љ–∞ –≤ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ —Б–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ–Љ –Љ–Є–Њ–Ї–∞—А–і–µ —З–µ–ї–Њ–≤–µ–Ї–∞. –Т—Л—Б–Њ–Ї–Њ —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ –ї–Є–≥–∞–љ–і—Л ICI 118.551 ( ќ≤2вАУ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–є, —А–Є—Б. 1–Р) –Є CGP 207.12A ( ќ≤1вАУ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–є, —А–Є—Б. 1–Т) –њ–Њ–Ї–∞–Ј–∞–ї–Є –і–≤—Г—Д–∞–Ј–љ—Л–µ –Ї—А–Є–≤—Л–µ —Б–≤—П–Ј—Л–≤–∞–љ–Є—П, —А–∞–Ј–і–µ–ї–Є–≤ –≤—Б—О –њ–Њ–њ—Г–ї—П—Ж–Є—О –∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –љ–∞ 70% ќ≤1вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –Є 30% ќ≤2вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤. –Т–Њ –≤—А–µ–Љ—П –њ—А–Њ–≤–µ–і–µ–љ–Є—П —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–Њ–≤ –њ–Њ —Б–≤—П–Ј—Л–≤–∞–љ–Є—О –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є —Г–Ї–∞–Ј–∞–љ–љ—Л—Е –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–є ICI 118.551–Є GCP 207.12A, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є —Б–≤—П–Ј—Л–≤–∞–љ–Є—П –і–ї—П –Є–Ј—Г—З–∞–µ–Љ—Л—Е –ї–Є–≥–∞–љ–і–Њ–≤ (–љ–µ–±–Є–≤–Њ–ї–Њ–ї –Є–ї–Є –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї) –Љ–Њ–≥–ї–Є –±—Л—В—М –Њ–њ—А–µ–і–µ–ї–µ–љ—Л —Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ –њ–Њ ќ≤1вАУ –Є –њ–Њ ќ≤2вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–∞–Љ. –Т –Љ–Є–Њ–Ї–∞—А–і–Є–∞–ї—М–љ—Л—Е –Љ–µ–Љ–±—А–∞–љ–∞—Е —В–µ—Е –ґ–µ —Б–µ—А–і–µ—Ж –∞–≥–Њ–љ–Є—Б—В –Є–Ј–Њ–њ—А–µ–љ–∞–ї–Є–љ –њ–Њ–Ї–∞–Ј–∞–ї –і–≤—Г—Е—Д–∞–Ј–љ—Г—О –Ї—А–Є–≤—Г—О —Б–≤—П–Ј—Л–≤–∞–љ–Є—П, –Њ—В—А–∞–ґ–∞—О—Й—Г—О –Љ–µ—Б—В–∞ –≤—Л—Б–Њ–Ї–Њ–є –Є –љ–Є–Ј–Ї–Њ–є —Б–≤—П–Ј—Л–≤–∞—О—Й–µ–є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є (–∞—Д—Д–Є–љ–љ–Њ—Б—В–Є) (—А–Є—Б. 1–°). –Т –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є –≥—Г–∞–љ–Є–ї–Є–ї–Є–Љ–Є–і–Њ–і–Є—Д–Њ—Б—Д–∞—В–∞ (Gpp(Nh)p), –љ–µ–≥–Є–і—А–Њ–ї–Є–Ј–Є—А—Г–µ–Љ–Њ–≥–Њ –≥—Г–∞–љ–Є–љ–Њ–≤–Њ–≥–Њ –љ—Г–Ї–ї–µ–Њ—В–Є–і–∞, —Б–≤—П–Ј—Л–≤–∞–љ–Є–µ —Б—В–∞–ї–Њ –Љ–Њ–љ–Њ—Д–∞–Ј–љ—Л–Љ, –Њ–њ—А–µ–і–µ–ї—П—П —В–Њ–ї—М–Ї–Њ –Њ–і–љ–Њ –Љ–µ—Б—В–Њ —Б–≤—П–Ј—Л–≤–∞–љ–Є—П (—Б –љ–Є–Ј–Ї–Њ–є –∞—Д—Д–Є–љ–љ–Њ—Б—В—М—О). –Ъ–∞–Ї —Б–ї–µ–і—Б—В–≤–Є–µ, —Д–∞–Ї—В–Њ—А –љ–∞–Ї–ї–Њ–љ–∞ (nH) –≤–Њ–Ј—А–Њ—Б —Б 0,43 –і–Њ 0,67. –≠—В–Њ –Њ–Ј–љ–∞—З–∞–µ—В, —З—В–Њ –≤ –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л—Е —Б–µ—А–і—Ж–∞—Е 30%вАУ—П —Д—А–∞–Ї—Ж–Є—П ќ≤вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –љ–∞—Е–Њ–і–Є–ї–∞—Б—М –≤ —Б–Њ—Б—В–Њ—П–љ–Є–Є –≤—Л—Б–Њ–Ї–Њ–є –∞—Д—Д–Є–љ–љ–Њ—Б—В–Є –Є, —В–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –±—Л–ї–∞ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ–є –і–ї—П –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –Љ–Є–Љ–µ—В–Є—З–µ—Б–Ї–Є—Е —Б–≤–Њ–є—Б—В–≤ –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л—Е ќ≤вАУ–±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤. –Ю–±—Й–µ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ ќ≤вАУ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –≤ —Б–Њ—Б—В–Њ—П–љ–Є–Є –≤—Л—Б–Њ–Ї–Њ–є –∞—Д—Д–Є–љ–љ–Њ—Б—В–Є —Б–Њ—Б—В–∞–≤–Є–ї–Њ 16¬±5% (–љ–µ –њ–Њ–Ї–∞–Ј–∞–љ–Њ). –Э–∞ —А–Є—Б—Г–љ–Ї–µ 2 –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є —Б–≤—П–Ј—Л–≤–∞–љ–Є—П –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞ (–ї–µ–≤–∞—П –њ–∞–љ–µ–ї—М) –Є –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї–∞ (–њ—А–∞–≤–∞—П –њ–∞–љ–µ–ї—М) –≤ –Љ–Є–Њ–Ї–∞—А–і–µ —Б —Б–Њ—Е—А–∞–љ–µ–љ–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О. –Т —В–∞–±–ї–Є—Ж–µ 1 –њ—А–Є–≤–µ–і–µ–љ—Л –Њ–±—Й–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л. –Т –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–Њ–≤ (–≤ 11 –Є–Ј 16), –љ–µ–±–Є–≤–Њ–ї–Њ–ї –њ–Њ–Ї–∞–Ј–∞–ї –Њ–і–љ–Њ—Б—В–Њ—А–Њ–љ–љ—О—О –Ї—А–Є–≤—Г—О —Б–≤—П–Ј—Л–≤–∞–љ–Є—П (—А–Є—Б. 2–Р). –§–∞–Ї—В–Њ—А –љ–∞–Ї–ї–Њ–љ–∞ –≤ 0,90¬±0,07 –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Є–≥ –µ–і–Є–љ–Є—Ж—Л, —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—П –Њ–± –Њ–і–Є–љ–∞–Ї–Њ–≤—Л—Е –Ї–Њ–љ—Б—В–∞–љ—В–∞—Е –і–Є—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞ –і–ї—П ќ≤1вАУ –Є ќ≤2вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤. –Т –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є Gpp(Nh)p –≤ –і–≤—Г—Е —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞—Е –Ї—А–Є–≤–∞—П —Б–≤—П–Ј—Л–≤–∞–љ–Є—П, —Е–∞—А–∞–Ї—В–µ—А–љ–∞—П –і–ї—П –і–≤–Њ–є–љ–Њ–≥–Њ —Б—А–Њ–і—Б—В–≤–∞, –њ—А–µ–≤—А–∞—В–Є–ї–∞—Б—М –≤ –Љ–Њ–љ–Њ—Д–∞–Ј–љ—Г—О –Ї—А–Є–≤—Г—О (—В–∞–±–ї. 1). –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –љ–Є —Д–∞–Ї—В–Њ—А –љ–∞–Ї–ї–Њ–љ–∞, –љ–Є –Ј–љ–∞—З–µ–љ–Є—П p Ki –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є Gpp(Nh)p –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –љ–µ –Є–Ј–Љ–µ–љ–Є–ї–Є—Б—М. –Ґ–∞–±–ї–Є—Ж–∞ 2 –њ–Њ–Ї–∞–Ј—Л–≤–∞–µ—В, —З—В–Њ –Љ–µ–ґ–і—Г —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞ —Б–≤—П–Ј—Л–≤–∞—В—М—Б—П —Б ќ≤вАУ—А–µ—Ж–µ–њ—В–Њ—А–∞–Љ–Є –≤ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ —Б–Њ—Е—А–∞–љ–љ–Њ–Љ –Є –≤ –њ–Њ—А–∞–ґ–µ–љ–љ–Њ–Љ –Љ–Є–Њ–Ї–∞—А–і–µ –љ–µ –±—Л–ї–Њ –Ї–∞–Ї–Є—ЕвАУ–ї–Є–±–Њ —А–∞–Ј–ї–Є—З–Є–є. –Т –њ—А–Њ—В–Є–≤–Њ–њ–Њ–ї–Њ–ґ–љ–Њ—Б—В—М –љ–µ–±–Є–≤–Њ–ї–Њ–ї—Г, –≤ 9 –Є–Ј 10 —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–Њ–≤ –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї –њ–Њ–Ї–∞–Ј–∞–ї –і–≤–µ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —А–∞–Ј–ї–Є—З–∞—О—Й–Є–µ—Б—П –њ–Њ —Б—А–Њ–і—Б—В–≤—Г –Ї—А–Є–≤—Л–µ, –Ї–∞–Ї –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є, —В–∞–Ї –Є –≤ –Њ—В—Б—Г—В—Б—В–≤–Є–µ Gpp(Nh)p (—А–Є—Б. 2–Т, —В–∞–±–ї. 1). –Т –Њ–±–Њ–Є—Е —Б–ї—Г—З–∞—П—Е —Д–∞–Ї—В–Њ—А—Л –љ–∞–Ї–ї–Њ–љ–∞ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –Њ—В–ї–Є—З–∞–ї–Є—Б—М –Њ—В –µ–і–Є–љ–Є—Ж—Л, –∞ —В–∞–Ї –ґ–µ –Њ—В —Д–∞–Ї—В–Њ—А–Њ–≤ –љ–∞–Ї–ї–Њ–љ–∞ –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞. –Э–Є –Ј–љ–∞—З–µ–љ–Є—П p Ki , –љ–Є —Д–∞–Ї—В–Њ—А—Л –љ–∞–Ї–ї–Њ–љ–∞ –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї–∞ –љ–µ –Є–Ј–Љ–µ–љ—П–ї–Є—Б—М –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є Gpp(Nh)p. –•–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є —Б–≤—П–Ј—Л–≤–∞–љ–Є—П –≤ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ —Б–Њ—Е—А–∞–љ–љ–Њ–Љ –Є –њ–Њ—А–∞–ґ–µ–љ–љ–Њ–Љ –Љ–Є–Њ–Ї–∞—А–і–µ —В–∞–Ї–ґ–µ –љ–µ —А–∞–Ј–ї–Є—З–∞–ї–Є—Б—М –Љ–µ–ґ–і—Г —Б–Њ–±–Њ–є (—В–∞–±–ї. 2). –Т –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є ICI 118.551–Є GCP 207.12A, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, —Г –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞ –Ї—А–Є–≤—Л–µ —Б–≤—П–Ј—Л–≤–∞–љ–Є—П –≤—Л—П–≤–Є–ї–Є –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –±–Њ–ї—М—И–Є–µ –Ј–љ–∞—З–µ–љ–Є—П p Ki –і–ї—П ќ≤1вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, —З–µ–Љ –і–ї—П ќ≤2вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ (—А–Є—Б. 2–°, –Х; —В–∞–±–ї. 1). –†–∞—Б—Б—З–Є—В–∞–љ–љ–Њ–µ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є–µ ќ≤2вАУ/ ќ≤1вАУ, –≤—Л—А–∞–ґ–∞—О—Й–µ–µ ќ≤1вАУ—Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В—М, –≤ –Њ—В—Б—Г—В—Б—В–≤–Є–µ Gpp(Nh)p —Б–Њ—Б—В–∞–≤–Є–ї–Њ 2,8¬±0,8, –∞ –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є —Н—В–Њ–≥–Њ –≤–µ—Й–µ—Б—В–≤–∞ вАУ 4,5¬±2,2 (—В–∞–±–ї. 1). –§–∞–Ї—В–Њ—А—Л –љ–∞–Ї–ї–Њ–љ–∞ –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є ICI 118.551 –Є GCP 207.12A, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, –љ–µ –Є–Ј–Љ–µ–љ—П–ї–Є—Б—М. –Т –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–Њ–≤ —Б –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї–Њ–Љ, –љ–∞–њ—А–Њ—В–Є–≤, –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є ICI 118.551–Є–ї–Є GCP 207.12A, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, –Ї—А–Є–≤—Л–µ —Б–≤—П–Ј—Л–≤–∞–љ–Є—П –њ–µ—А–µ—И–ї–Є –≤ –Љ–Њ–љ–Њ—Д–∞–Ј–љ—Л–µ. –§–∞–Ї—В–Њ—А—Л –љ–∞–Ї–ї–Њ–љ–∞ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –≤–Њ–Ј—А–Њ—Б–ї–Є –≤–њ–ї–Њ—В—М –і–Њ –µ–і–Є–љ–Є—Ж—Л, –∞ –Ј–љ–∞—З–µ–љ–Є—П p Ki –Љ–µ–ґ–і—Г ќ≤1вАУ –Є ќ≤2вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–∞–Љ–Є –Ј–љ–∞—З–Є–Љ–Њ —А–∞–Ј–ї–Є—З–∞–ї–Є—Б—М (—В–∞–±–ї. 1). –†–∞—Б—Б—З–Є—В–∞–љ–љ–Њ–µ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є–µ ќ≤2/ ќ≤1 –≤ –Њ—В—Б—Г—В—Б—В–≤–Є–µ Gpp(Nh)p —Б–Њ—Б—В–∞–≤–Є–ї–Њ 19,7¬±9,7, –∞ –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є вАУ 15,6¬±5,8, —З—В–Њ –Њ–Ї–∞–Ј–∞–ї–Њ—Б—М –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –±–Њ–ї—М—И–µ, —З–µ–Љ –і–ї—П –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞. –Т –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є ICI 118.551 –Є–ї–Є GCP 207.12A, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, Gpp(Nh)p –љ–µ –Є–Ј–Љ–µ–љ–Є–ї —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є –љ–Є –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї–∞, –љ–Є –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞. –Ф—А—Г–≥–Є–Љ —Б–њ–Њ—Б–Њ–±–Њ–Љ —А–∞—Б—З–µ—В–∞ ќ≤1вАУ—Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –≤–µ—Й–µ—Б—В–≤–∞ —П–≤–ї—П–µ—В—Б—П –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ –Ї–Њ–љ—Б—В–∞–љ—В –і–Є—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є –Љ–µ—Б—В –≤—Л—Б–Њ–Ї–Њ–є –Є –љ–Є–Ј–Ї–Њ–є –∞—Д—Д–Є–љ–љ–Њ—Б—В–Є –њ–Њ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є–Љ –і–≤—Г—Б—В–Њ—А–Њ–љ–љ–Є–Љ –Ї—А–Є–≤—Л–Љ —Б–≤—П–Ј—Л–≤–∞–љ–Є—П . –Т —В–∞–±–ї–Є—Ж–µ 3 –њ—А–Є–≤–µ–і–µ–љ—Л —А–µ–Ј—Г–ї—М—В–∞—В—Л —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–Њ–≤ —Б –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ–Љ –Љ–µ—Б—В –Њ–±–µ–Є—Е –Є–ї–Є —В–Њ–ї—М–Ї–Њ –Њ–і–љ–Њ–є –∞—Д—Д–Є–љ–љ–Њ—Б—В–µ–є. –°–Њ–≥–ї–∞—Б–љ–Њ –≤—Л—З–Є—Б–ї–µ–љ–Є—П–Љ ќ≤1вАУ—Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ–Њ –Љ–µ—Б—В–∞–Љ —Б–≤—П–Ј—Л–≤–∞–љ–Є—П —Б –≤—Л—Б–Њ–Ї–Њ–є –Є –љ–Є–Ј–Ї–Њ–є –∞—Д—Д–Є–љ–љ–Њ—Б—В—М—О –і–ї—П –Њ–±–Њ–Є—Е –≤–µ—Й–µ—Б—В–≤ ќ≤1вАУ—Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Њ–Ї–∞–Ј–∞–ї–∞—Б—М –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –≤—Л—И–µ, —З–µ–Љ –њ–Њ –≤—Л—З–Є—Б–ї–µ–љ–Є—П–Љ, –і–∞–љ–љ—Л–Љ –≤ —В–∞–±–ї–Є—Ж–µ 1. –Ш –≤–љ–Њ–≤—М –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї –±–Њ–ї—М—И—Г—О ќ≤1вАУ—Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В—М, —З–µ–Љ –љ–µ–±–Є–≤–Њ–ї–Њ–ї, –Ї–∞–Ї –≤ –Њ—В—Б—Г—В—Б—В–≤–Є–µ (143 vs 76), —В–∞–Ї –Є –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є Gpp(Nh)p (242 vs 66). –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –Є–ЈвАУ–Ј–∞ –Њ–≥—А–∞–љ–Є—З–µ–љ–љ–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–Њ–≤ –≤ –≥—А—Г–њ–њ–µ –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞ —Н—В–Є —А–∞–Ј–ї–Є—З–Є—П –Њ–Ї–∞–Ј–∞–ї–Є—Б—М —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –љ–µ–Ј–љ–∞—З–Є–Љ—Л–Љ–Є. –Ю–і–љ–∞–Ї–Њ —Б–ї–µ–і—Г–µ—В —Г—З–Є—В—Л–≤–∞—В—М, —З—В–Њ –љ–µ–±–Є–≤–Њ–ї–Њ–ї –њ–Њ–Ї–∞–Ј–∞–ї –і–≤—Г—Б—В–Њ—А–Њ–љ–љ–µ–µ —Б–≤—П–Ј—Л–≤–∞–љ–Є–µ –≤ –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–Њ–≤, –∞ –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї вАУ–≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–Њ–≤. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Н—В–Є –і–∞–љ–љ—Л–µ –њ–Њ —Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –љ–µ –Њ—В—А–∞–ґ–∞—О—В —Б—Г–Љ–Љ–∞—А–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –≤—Б–µ—Е —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–Њ–≤. –Т —В–∞–±–ї–Є—Ж–µ 4 –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –Ј–љ–∞—З–µ–љ–Є—П p Ki , –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ –≤ —Е–Њ–і–µ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–Њ–≤ –њ–Њ —Б–≤—П–Ј—Л–≤–∞–љ–Є—О –љ–∞ –Ї–ї–µ—В–Ї–∞—Е COSвАУ7, —Б–Њ–і–µ—А–ґ–∞—Й–Є—Е —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–µ ќ≤1вАУ –Є ќ≤2вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А—Л. –Ю—В–љ–Њ—И–µ–љ–Є—П ќ≤2/ ќ≤1 –і–ї—П –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞ (3,0) –Є –і–ї—П –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї–∞ (15,1) —Б–Њ–≥–ї–∞—Б—Г—О—В—Б—П —Б —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є—П–Љ–Є —Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є, –њ–Њ–ї—Г—З–µ–љ–љ—Л–Љ–Є –≤ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞—Е –љ–∞ –Љ–Є–Њ–Ї–∞—А–і–µ —З–µ–ї–Њ–≤–µ–Ї–∞ (—В–∞–±–ї. 1). –§—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Ф–ї—П —В–Њ–≥–Њ, —З—В–Њ–±—Л –Њ—Ж–µ–љ–Є—В—М –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ ќ≤вАУ—А–µ—Ж–µ–њ—В–Њ—А–љ–Њ–є —Б–≤—П–Ј—Л–≤–∞—О—Й–µ–є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞ –Є –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї–∞ –љ–∞ —Б–Њ–Ї—А–∞—В–Є—В–µ–ї—М–љ—Г—О —Д—Г–љ–Ї—Ж–Є—О –Љ–Є–Њ–Ї–∞—А–і–∞, –±—Л–ї–Є –њ—А–Њ–≤–µ–і–µ–љ—Л —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В—Л –љ–∞ –њ–Њ–ї–Њ—Б–Ї–∞—Е –Љ—Л—И–µ—З–љ–Њ–є —В–Ї–∞–љ–Є –Є–Ј –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ –Є –њ—А–∞–≤–Њ–≥–Њ –њ—А–µ–і—Б–µ—А–і–Є—П —Б–µ—А–і–µ—Ж —Б –љ–∞—А—Г—И–µ–љ–љ–Њ–є –Є —Б–Њ—Е—А–∞–љ–љ–Њ–є —Б–Њ–Ї—А–∞—В–Є—В–µ–ї—М–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–µ–є. –Т —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞—Е –њ–Њ —Б–Њ–Ї—А–∞—В–Є–Љ–Њ—Б—В–Є –Љ—Л—И–µ—З–љ—Л–µ –њ–Њ–ї–Њ—Б–Ї–Є —А–∞—Б—В—П–≥–Є–≤–∞–ї–Є—Б—М –і–Њ —В–∞–Ї–Њ–є –і–ї–Є–љ—Л, –њ—А–Є –Ї–Њ—В–Њ—А–Њ–є —Б–Є–ї–∞ —Б–Њ–Ї—А–∞—Й–µ–љ–Є—П –±—Л–ї–∞ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є. –Т–Њ –≤—Б–µ—Е —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞—Е —Б –Љ–Є–Њ–Ї–∞—А–і–Њ–Љ –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ –Є –њ—А–∞–≤–Њ–≥–Њ –њ—А–µ–і—Б–µ—А–і–Є—П –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–µ –љ–∞–њ—А—П–ґ–µ–љ–Є–µ –љ–µ —А–∞–Ј–ї–Є—З–∞–ї–Њ—Б—М –Љ–µ–ґ–і—Г –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л–Љ–Є –≥—А—Г–њ–њ–∞–Љ–Є (–љ–µ –њ–Њ–Ї–∞–Ј–∞–љ–Њ). –Т –≤–µ–љ—В—А–Є–Ї—Г–ї—П—А–љ–Њ–Љ –Љ–Є–Њ–Ї–∞—А–і–µ —З–µ–ї–Њ–≤–µ–Ї–∞ –њ—А–Є –љ–∞–љ–µ—Б–µ–љ–Є–Є 1 –Љ–Ї–Љ–Њ–ї—М/–ї –Є–Ј–Њ–њ—А–µ–љ–∞–ї–Є–љ–∞ –Є—Б—Е–Њ–і–љ–∞—П —Б–Є–ї–∞ —Б–Њ–Ї—А–∞—Й–µ–љ–Є—П —Г–≤–µ–ї–Є—З–Є–≤–∞–ї–∞—Б—М –љ–∞ 123¬±16% (n=11). –Я–Њ—Б–ї–µ —Н–Ї–≤–Є–ї–Є–±—А–∞—Ж–Є–Є –≤ –≤–∞–љ–љ–Њ—З–Ї—Г —Б –Љ—Л—И–µ—З–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –і–Њ–±–∞–≤–ї—П–ї–Є—Б—М –Ї—Г–Љ—Г–ї—П—В–Є–≤–љ—Л–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞ –Є –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї–∞. –Ь–µ–ґ–і—Г –і–≤—Г–Љ—П –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –љ–µ –±—Л–ї–Њ –њ–Њ–ї—Г—З–µ–љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л—Е –Њ—В–ї–Є—З–Є–є –њ–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—О –Ї–∞–Ї –љ–∞ –±–∞–Ј–∞–ї—М–љ—Г—О, —В–∞–Ї –Є –љ–∞ —Б—В–Є–Љ—Г–ї–Є—А–Њ–≤–∞–љ–љ—Г—О –Є–Ј–Њ–њ—А–µ–љ–∞–ї–Є–љ–Њ–Љ —Б–Њ–Ї—А–∞—В–Є–Љ–Њ—Б—В—М (—В–∞–±–ї. 5). –Т –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–µ–є —Б–≤—П–Ј—Л–≤–∞–љ–Є—О —Б 50% ( Ki ) –Є —Б–Њ 100% (100 x Ki ) ќ≤вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, –Њ–±–∞ ќ≤вАУ–±–ї–Њ–Ї–∞—В–Њ—А–∞ –Ј–љ–∞—З–Є–Љ–Њ –њ—А–µ–њ—П—В—Б—В–≤–Њ–≤–∞–ї–Є –Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–Љ—Г –Є–Ј–Њ–њ—А–µ–љ–∞–ї–Є–љ–Њ–Љ —Г—Б–Є–ї–µ–љ–Є—О —Б–Є–ї—Л —Б–Њ–Ї—А–∞—Й–µ–љ–Є—П (—А–Є—Б—Г–љ–Ї–Є 3–Р, 3–Т). –Ф–ї—П –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –≤–љ—Г—В—А–µ–љ–љ–µ–є –Љ–Є–Љ–µ—В–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Њ–±–Њ–Є—Е –∞–≥–µ–љ—В–Њ–≤ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–µ ќ≤вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ —Б –∞–і–µ–љ–Є–ї–∞—В—Ж–Є–Ї–ї–∞–Ј–Њ–є —Б—В–Є–Љ—Г–ї–Є—А–Њ–≤–∞–ї–Њ—Б—М —Д–Њ—А—Б–Ї–Њ–ї–Є–љ–Њ–Љ (0,3 –Љ–Ї–Љ–Њ–ї—М/–ї). –≠—В–Є–Љ –Љ–µ—В–Њ–і–Њ–Љ –Љ–Њ–ґ–љ–Њ –Њ–њ—А–µ–і–µ–ї–Є—В—М –Ї–∞–Ї –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —З–∞—Б—В–Є—З–љ–Њ–≥–Њ –∞–≥–Њ–љ–Є—Б—В–∞ [Boehm et al., 1990b], —В–∞–Ї –Є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Њ–±—А–∞—В–љ–Њ–≥–Њ –∞–≥–Њ–љ–Є—Б—В–∞ [Mewes et al., 1993]. –§–Њ—А—Б–Ї–Њ–ї–Є–љ –њ–Њ–≤—Л—Б–Є–ї —Б–Є–ї—Г —Б–Њ–Ї—А–∞—В–Є–Љ–Њ—Б—В–Є –љ–∞ 81¬±20% (n=16). –Э–µ–±–Є–≤–Њ–ї–Њ–ї –Є –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї –≤ –љ–∞—А–∞—Б—В–∞—О—Й–Є—Е –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П—Е –Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–ї–Є —Б—Е–Њ–і–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Њ–Ї—А–∞—В–Є–Љ–Њ—Б—В–Є (—А–Є—Б. 3–°). –°–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, –µ—Б–ї–Є —Б–Њ–њ–Њ—Б—В–∞–≤–Є—В—М —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Њ–Ї—А–∞—В–Є–Љ–Њ—Б—В–Є —Б–Њ –Ј–љ–∞—З–µ–љ–Є—П–Љ–Є Ki , —В–Њ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ —Б–Њ–Ї—А–∞—В–Є–Љ–Њ—Б—В–Є –і–ї—П –Њ–±–Њ–Є—Е –∞–≥–µ–љ—В–Њ–≤ –љ–µ —А–∞–Ј–ї–Є—З–∞—О—В—Б—П –Љ–µ–ґ–і—Г —Б–Њ–±–Њ–є (—А–Є—Б. 3D). –Т –Љ–Є–Њ–Ї–∞—А–і–µ, –љ–µ –Њ–±—А–∞–±–∞—В—Л–≤–∞–≤—И–µ–Љ—Б—П —Д–Њ—А—Б–Ї–Њ–ї–Є–љ–Њ–Љ –Є–ї–Є –Є–Ј–Њ–њ—А–µ–љ–∞–ї–Є–љ–Њ–Љ, –∞–љ–∞–ї–Њ–≥–Є—З–љ–Њ, —Б–Њ–Ї—А–∞—В–Є–Љ–Њ—Б—В—М –±—Л–ї–∞ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–Љ–µ–љ—М—И–µ–љ–∞ –њ–Њ–і –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ–Љ –Њ–±–Њ–Є—Е –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л—Е ќ≤вАУ–±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤ (—А–Є—Б. 4). –Я—А–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –≤–љ—Г—В—А–µ–љ–љ–µ–є –Љ–Є–Љ–µ—В–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–≤ ќ≤вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –≤–∞–ґ–љ–Њ —Б—А–∞–≤–љ–Є–≤–∞—В—М —А–∞–Ј–ї–Є—З–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –љ–∞ –Њ–і–љ–Њ–є –Є —В–Њ–є –ґ–µ —Б–Є—Б—В–µ–Љ–µ, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –≤–љ—Г—В—А–µ–љ–љ—П—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –ї–Є–≥–∞–љ–і–Њ–≤ —Б–Є–ї—М–љ–Њ –Ј–∞–≤–Є—Б–Є—В –Њ—В —В–Є–њ–∞ —В–Ї–∞–љ–µ–є [de Ligt et al., 2000]. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Љ—Л —Б—А–∞–≤–љ–Є–≤–∞–ї–Є –≤–љ—Г—В—А–µ–љ–љ—О—О –Љ–Є–Љ–µ—В–Є—З–µ—Б–Ї—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞ –Є –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї–∞ —Б –±—Г—Ж–Є–љ–і–Њ–ї–Њ–ї–Њ–Љ, –Ї–∞—А–≤–µ–і–Є–ї–Њ–ї–Њ–Љ –Є –Љ–µ—В–Њ–њ—А–Њ–ї–Њ–ї–Њ–Љ –љ–∞ –Љ–Є–Њ–Ї–∞—А–і–µ –њ—А–µ–і—Б–µ—А–і–Є—П —З–µ–ї–Њ–≤–µ–Ї–∞. –Э–∞ —А–Є—Б—Г–љ–Ї–µ 5 —Н—Д—Д–µ–Ї—В—Л –≤—Б–µ—Е –∞–≥–µ–љ—В–Њ–≤ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —Б–Њ–Ї—А–∞—В–Є–Љ–Њ—Б—В–Є —Б—А–∞–≤–љ–Є–≤–∞—О—В—Б—П –≤ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П—Е —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —Б–Њ–Њ—В–≤–µ—В—Б–≤—Г—О—Й–Є—Е —Б–≤—П–Ј—Л–≤–∞–љ–Є—О —Б 50% (—А–Є—Б. 5–Р) –Є —Б–Њ 100% (—А–Є—Б. 5–Т) ќ≤вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤. –Я—А–Є –Њ–±–Њ–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є—П—Е –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї –Є –љ–µ–±–Є–≤–Њ–ї–Њ–ї –њ–Њ–Ї–∞–Ј–∞–ї–Є –Ј–љ–∞—З–Є–Љ–Њ –±–Њ–ї—М—И–Є–є –Њ–±—А–∞—В–љ—Л–є –∞–≥–Њ–љ–Є–Ј–Љ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –±—Г—Ж–Є–љ–і–Њ–ї–Њ–ї–Њ–Љ –Є –Љ–µ–љ—М—И–Є–є вАУ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Љ–µ—В–Њ–њ—А–Њ–ї–Њ–ї–Њ–Љ. –Ъ–∞—А–≤–µ–і–Є–ї–Њ–ї –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –љ–µ–±–Є–≤–Њ–ї–Њ–ї–Њ–Љ –Є –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї–Њ–Љ –њ—А–Њ—П–≤–Є–ї –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –Љ–µ–љ–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ—Л–є –Њ–±—А–∞—В–љ—Л–є –∞–≥–Њ–љ–Є–Ј–Љ. –Т —Ж–µ–ї–Њ–Љ ќ≤вАУ–±–ї–Њ–Ї–∞—В–Њ—А—Л —Б–Њ —Б–≤—П–Ј—Л–≤–∞—О—Й–µ–є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О, –Љ–Њ–і–µ–ї–Є—А—Г–µ–Љ–Њ–є –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ–Љ Gpp(Nh)p, —В–∞–Ї–Є–µ –Ї–∞–Ї –±—Г—Ж–Є–љ–і–Њ–ї–Њ–ї –Є –Ї–∞—А–≤–µ–і–Є–ї–Њ–ї [Yoshikawa et al., 1996; –Ь aack et al., 2000], –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї–Є –Љ–µ–љ—М—И—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –≤ –Ї–∞—З–µ—Б—В–≤–µ –Њ–±—А–∞—В–љ—Л—Е –∞–≥–Њ–љ–Є—Б—В–Њ–≤, —З–µ–Љ –њ—А–µ–њ–∞—А–∞—В—Л, –љ–µ –Њ–±–ї–∞–і–∞—О—Й–Є–µ —В–∞–Ї–Њ–є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О. –Ґ–Є–њ–Є—З–љ–Њ–є —З–µ—А—В–Њ–є –Њ–±—А–∞—В–љ–Њ–≥–Њ –∞–≥–Њ–љ–Є—Б—В–∞ —П–≤–ї—П–µ—В—Б—П —В–Њ, —З—В–Њ –µ–≥–Њ –љ–µ–≥–∞—В–Є–≤–љ—Л–µ –Є–љ–Њ—В—А–Њ–њ–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –Љ–Њ–≥—Г—В –±—Л—В—М –∞–љ—В–∞–≥–Њ–љ–Є–Ј–Є—А–Њ–≤–∞–љ—Л –ї–Є–≥–∞–љ–і–∞–Љ–Є —Б –љ–Є–Ј–Ї–Њ–є –Њ–±—А–∞—В–љ–Њ–є –∞–≥–Њ–љ–Є—Б—В–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О (–≤ –Є–і–µ–∞–ї–µ, –љ–µ–є—В—А–∞–ї—М–љ—Л–Љ –∞–≥–Њ–љ–Є—Б—В–Њ–Љ). –Э–∞ —А–Є—Б—Г–љ–Ї–µ 6 –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –≤ –Љ–Є–Њ–Ї–∞—А–і–µ —З–µ–ї–Њ–≤–µ–Ї–∞, –њ—А–µ–і–≤–∞—А–Є—В–µ–ї—М–љ–Њ –Њ–±—А–∞–±–Њ—В–∞–љ–љ–Њ–≥–Њ —Д–Њ—А—Б–Ї–Њ–ї–Є–љ–Њ–Љ, –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–є –Є–љ–Њ—В—А–Њ–њ–љ—Л–є —Н—Д—Д–µ–Ї—В –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞ –±—Л–ї –∞–љ—В–∞–≥–Њ–љ–Є–Ј–Є—А–Њ–≤–∞–љ –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є –±—Г—Ж–Є–љ–і–Њ–ї–Њ–ї–∞. –Ю–±—Б—Г–ґ–і–µ–љ–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Ю—Б–љ–Њ–≤–љ–Њ–є –љ–∞—Е–Њ–і–Ї–Њ–є —Н—В–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —П–≤–ї—П–µ—В—Б—П —В–Њ—В —Д–∞–Ї—В, —З—В–Њ –≤ –Љ–Є–Њ–Ї–∞—А–і–µ —З–µ–ї–Њ–≤–µ–Ї–∞ –љ–µ–±–Є–≤–Њ–ї–Њ–ї –Є –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї –≤–µ–і—Г—В —Б–µ–±—П –Ї–∞–Ї –Њ–±—А–∞—В–љ—Л–µ –∞–≥–Њ–љ–Є—Б—В—Л. –Я–Њ —Б—В–µ–њ–µ–љ–Є –Њ–±—А–∞—В–љ–Њ–≥–Њ –∞–≥–Њ–љ–Є–Ј–Љ–∞ –≤ –Љ–Є–Њ–Ї–∞—А–і–µ —З–µ–ї–Њ–≤–µ–Ї–∞ –њ—А–µ–њ–∞—А–∞—В—Л —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ—Л –≤ —Б–ї–µ–і—Г—О—Й–µ–Љ –њ–Њ—А—П–і–Ї–µ: –Љ–µ—В–Њ–њ—А–Њ–ї–Њ–ї > –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї = –љ–µ–±–Є–≤–Њ–ї–Њ–ї ќ≤–Ї–∞—А–≤–µ–і–Є–ї–Њ–ї > –±—Г—Ж–Є–љ–і–Њ–ї–Њ–ї. –С–Њ–ї–µ–µ —В–Њ–≥–Њ, –љ–µ–±–Є–≤–Њ–ї–Њ–ї —П–≤–ї—П–µ—В—Б—П –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–Љ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є ќ≤1вАУ –Є ќ≤2вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –Љ–Є–Њ–Ї–∞—А–і–∞, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї ќ≤1вАУ—Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї–∞ –≤ 16вАУ20 —А–∞–Ј –≤—Л—И–µ . –Т–љ—Г—В—А–µ–љ–љ—П—П –Љ–Є–Љ–µ—В–Є—З–µ—Б–Ї–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Я–Њ –љ–µ–Ї–Њ—В–Њ—А—Л–Љ –њ—А–Є—З–Є–љ–∞–Љ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ –≤–љ—Г—В—А–µ–љ–љ–µ–є –Љ–Є–Љ–µ—В–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –љ–∞ –Є–љ—В–∞–Ї—В–љ–Њ–Љ –Љ–Є–Њ–Ї–∞—А–і–µ —З–µ–ї–Њ–≤–µ–Ї–∞ —П–≤–ї—П–µ—В—Б—П —Б–ї–Њ–ґ–љ–Њ–є –Ј–∞–і–∞—З–µ–є. –Т –Љ–Є–Њ–Ї–∞—А–і–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —Б—В—А–∞–і–∞—О—Й–Є—Е —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О, –њ–ї–Њ—В–љ–Њ—Б—В—М ќ≤вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ —Б–љ–Є–ґ–µ–љ–∞ [Bristow et al., 1982], –∞ –Њ—Б—В–∞–≤—И–Є–µ—Б—П —А–µ—Ж–µ–њ—В–Њ—А—Л –љ–∞—Е–Њ–і—П—В—Б—П –≤–љ–µ —Б–≤—П–Ј–Є —Б Gs [Hausdorff et al., 1990]. –Ъ—А–Њ–Љ–µ —Н—В–Њ–≥–Њ, –њ–Њ–≤—Л—И–µ–љ–љ–Њ–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –≤ –Љ–µ–Љ–±—А–∞–љ–µ ќ≤вАУ—Б—Г–±—К–µ–і–Є–љ–Є—Ж –Є–љ–≥–Є–±–Є—В–Њ—А–љ–Њ–≥–Њ GвАУ –њ—А–Њ—В–µ–Є–љ–∞ [Boehm et al., 1990a] —В–∞–Ї–ґ–µ –Љ–Њ–ґ–µ—В —Г–Љ–µ–љ—М—И–∞—В—М –Њ—В–≤–µ—В –љ–∞ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –њ–∞—А—Ж–Є–∞–ї—М–љ–Њ–≥–Њ –Є–ї–Є –Њ–±—А–∞—В–љ–Њ–≥–Њ –∞–≥–Њ–љ–Є—Б—В–Њ–≤. –°–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В—Л –њ–Њ –Є–Ј—Г—З–µ–љ–Є—О —Б–Њ–Ї—А–∞—В–Є–Љ–Њ—Б—В–Є –њ—А–Њ–≤–Њ–і–Є–ї–Є—Б—М –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є —Д–Њ—А—Б–Ї–Њ–ї–Є–љ–∞, –і–Є—В–µ—А–њ–µ–љ–∞, –Њ–±–ї–∞–і–∞—О—Й–µ–≥–Њ —Б–≤–Њ–є—Б—В–≤–Њ–Љ —Б–≤—П–Ј—Л–≤–∞—В—М Gs ќ≤—Б –∞–і–µ–љ–Є–ї–∞—ВвАУ—Ж–Є–Ї–ї–∞–Ј–Њ–є. –≠—В–Є–Љ –Љ–µ—В–Њ–і–Њ–Љ –Љ–Њ–ґ–љ–Њ –Њ–њ—А–µ–і–µ–ї–Є—В—М —Н—Д—Д–µ–Ї—В—Л –њ–∞—А—Ж–Є–∞–ї—М–љ—Л—Е –Є –Њ–±—А–∞—В–љ—Л—Е –∞–≥–Њ–љ–Є—Б—В–Њ–≤ [Boehm et al., 1990b]. –≠—В–Є–Љ –Љ–µ—В–Њ–і–Њ–Љ –≤ –љ–µ–і–∞–≤–љ–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Љ—Л –Њ–њ—А–µ–і–µ–ї—П–ї–Є –≤–љ—Г—В—А–µ–љ–љ—О—О –Љ–Є–Љ–µ—В–Є—З–µ—Б–Ї—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –±—Г—Ж–Є–љ–і–Њ–ї–Њ–ї–∞, –Ї–∞—А–≤–µ–і–Є–ї–Њ–ї–∞ –Є –Љ–µ—В–Њ–њ—А–Њ–ї–Њ–ї–∞ [Maack et al., 2000]. –Т —Г–њ–Њ–Љ—П–љ—Г—В–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Љ–µ—В–Њ–њ—А–Њ–ї–Њ–ї –≤–µ–ї —Б–µ–±—П –Ї–∞–Ї —Б–Є–ї—М–љ—Л–є –Њ–±—А–∞—В–љ—Л–є –∞–≥–Њ–љ–Є—Б—В, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –±—Г—Ж–Є–љ–і–Њ–ї–Њ–ї –Є –Ї–∞—А–≤–µ–і–Є–ї–Њ–ї –њ—А–Њ—П–≤–Є–ї–Є —Б–≤—П–Ј—Л–≤–∞—О—Й—Г—О —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М, –Љ–Њ–і—Г–ї–Є—А—Г–µ–Љ—Г—О Gpp(Nh)p, –Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –Љ–µ–љ—М—И—Г—О –Њ–±—А–∞—В–љ—Г—О –∞–≥–Њ–љ–Є—Б—В–Є—З–µ—Б–Ї—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М, —З–µ–Љ –Љ–µ—В–Њ–њ—А–Њ–ї–Њ–ї. –Т —З–∞—Б—В–Є —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–Њ–≤ –±—Г—Ж–Є–љ–і–Њ–ї–Њ–ї –њ–Њ–≤–µ–ї —Б–µ–±—П –і–∞–ґ–µ –Ї–∞–Ї –њ–∞—А—Ж–Є–∞–ї—М–љ—Л–є –∞–≥–Њ–љ–Є—Б—В. –Я–Њ—Б–Ї–Њ–ї—М–Ї—Г –≤ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е [Willette et al., 1998; 1999; Trochu et al., 1999; Maack et al., 2000] –±—Г—Ж–Є–љ–і–Њ–ї–Њ–ї –њ—А–Њ—П–≤–Є–ї —Н—Д—Д–µ–Ї—В—Л —З–∞—Б—В–Є—З–љ–Њ–≥–Њ –∞–≥–Њ–љ–Є—Б—В–∞, —Е–Њ—В—П –Є –љ–µ –≤–Њ –≤—Б–µ—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е [Hershberger et al., 1990; Bristow et al., 1992], –≤–љ—Г—В—А–µ–љ–љ—П—П –Љ–Є–Љ–µ—В–Є—З–µ—Б–Ї–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М ќ≤вАУ–±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤ –Љ–Њ–ґ–µ—В –±—Л—В—М —Б–Є—Б—В–µ–Љ–Њ–Ј–∞–≤–Є—Б–Є–Љ–Њ–є. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –љ–∞ —Б–Њ–±–∞–Ї–∞—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —А–µ–Ј–µ—А–њ–Є–љ, –Є —Г –Ї—А—Л—Б —Б–Њ —Б–њ–Њ–љ—В–∞–љ–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–µ–є —Г –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞ –љ–µ –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ –њ–∞—А—Ж–Є–∞–ї—М–љ–Њ–є –∞–≥–Њ–љ–Є—Б—В–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є [Janssens et al., 1989]. –Т —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞—Е –љ–∞ –Ї—А—Л—Б–∞—Е —Б —А–∞–Ј—А—Г—И–µ–љ–љ—Л–Љ —Б–њ–Є–љ–љ—Л–Љ –Љ–Њ–Ј–≥–Њ–Љ (—Б–њ–Є–љ–∞–ї—М–љ—Л—Е –Ї—А—Л—Б–∞—Е) —Г –Ј–і–Њ—А–Њ–≤—Л—Е –ґ–Є–≤–Њ—В–љ—Л—Е –Є —Г –ґ–Є–≤–Њ—В–љ—Л—Е —Б —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї —В–∞–Ї–ґ–µ –љ–µ –њ—А–Њ—П–≤–Є–ї –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —З–∞—Б—В–Є—З–љ–Њ–≥–Њ –∞–≥–Њ–љ–Є—Б—В–∞ [Willette et al., 1999]. –Т –љ–∞—Б—В–Њ—П—Й–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В—Л –њ–Њ –Є–Ј—Г—З–µ–љ–Є—О —Б–Њ–Ї—А–∞—В–Є–Љ–Њ—Б—В–Є –Љ–Є–Њ–Ї–∞—А–і–∞ —З–µ–ї–Њ–≤–µ–Ї–∞ –±—Л–ї–Є –њ—А–Њ–≤–µ–і–µ–љ—Л –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є —Д–Њ—А—Б–Ї–Њ–ї–Є–љ–∞. –°—В–Є–Љ—Г–ї–Є—А–Њ–≤–∞–љ–Є–µ –∞–і–µ–љ–Є–ї–∞—ВвАУ—Ж–Є–Ї–ї–∞–Ј—Л —Д–Њ—А—Б–Ї–Њ–ї–Є–љ–Њ–Љ –Ј–∞–≤–Є—Б–Є—В –Њ—В –љ–∞–ї–Є—З–Є—П Gs ќ≤[Darfler et al., 1982], –љ–Њ –і–Є—Б—Б–Њ—Ж–Є–∞—Ж–Є—П Gs ќ≤–Њ—В ?ќ≤вАУ—Б—Г–±—К–µ–і–Є–љ–Є—Ж GвАУ–±–µ–ї–Ї–∞ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В —В–Њ–ї—М–Ї–Њ —В–Њ–≥–і–∞, –Ї–Њ–≥–і–∞ —А–µ—Ж–µ–њ—В–Њ—А –љ–∞—Е–Њ–і–Є—В—Б—П –≤ –∞–Ї—В–Є–≤–Є—А–Њ–≤–∞–љ–љ–Њ–Љ —Б–Њ—Б—В–Њ—П–љ–Є–Є (R*). –Ю—В—А–Є—Ж–∞—В–µ–ї—М–љ–Њ–µ –Є–љ–Њ—В—А–Њ–њ–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞ –Є –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї–∞ –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є —Д–Њ—А—Б–Ї–Њ–ї–Є–љ–∞ –Љ–Њ–ґ–µ—В –Њ—В—А–∞–ґ–∞—В—М —Б–љ–Є–ґ–µ–љ–љ—Г—О GsвАУ–Ј–∞–≤–Є—Б–Є–Љ—Г—О —Б—В–Є–Љ—Г–ї—П—Ж–Є—О –∞–і–µ–љ–Є–ї–∞—ВвАУ—Ж–Є–Ї–ї–∞–Ј—Л, —З—В–Њ, –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М, –Њ–Ј–љ–∞—З–∞–µ—В, —З—В–Њ –Њ–±–∞ —Н—В–Є—Е ќ≤вАУ–±–ї–Њ–Ї–∞—В–Њ—А–∞ —П–≤–ї—П—О—В—Б—П –Њ–±—А–∞—В–љ—Л–Љ–Є –∞–≥–Њ–љ–Є—Б—В–∞–Љ–Є, –Є—Б—Е–Њ–і–љ–Њ —Б—В–∞–±–Є–ї–Є–Ј–Є—А—Г—О—Й–Є–Љ–Є –љ–µ–∞–Ї—В–Є–≤–љ—Г—О –Ї–Њ–љ—Д–Њ—А–Љ–∞—Ж–Є—О ќ≤вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–∞ (R). –Т —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б —Н—В–Є–Љ –љ–Є –љ–µ–±–Є–≤–Њ–ї–Њ–ї, –љ–Є –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї –љ–µ –Є–љ–і—Г—Ж–Є—А—Г—О—В –і–Є—Б—Б–Њ—Ж–Є–∞—Ж–Є—О Gs ќ≤–Њ—В ?ќ≤вАУ—Б—Г–±—К–µ–і–Є–љ–Є—Ж GвАУ–±–µ–ї–Ї–∞, —З—В–Њ –±—Л–ї–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Њ –≤ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞—Е —Б —А–∞–і–Є–Њ–ї–Є–≥–∞–љ–і–∞–Љ–Є –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –Є –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є Gpp(Nh)p. –Я—А–Є –Є–Ј—Г—З–µ–љ–Є–Є –Њ–±—А–∞—В–љ–Њ–є –∞–≥–Њ–љ–Є—Б—В–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є ќ≤вАУ–±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤ –љ–∞ –Є–љ—В–∞–Ї—В–љ–Њ–є —В–Ї–∞–љ–Є –≤–∞–ґ–љ–Њ –Є—Б–Ї–ї—О—З–Є—В—М –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л—Е –Є–љ–Њ—В—А–Њ–њ–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤—Б–ї–µ–і—Б—В–≤–Є–µ –њ—А–Є—Б—Г—В—Б—В–≤–Є—П —Н–љ–і–Њ–≥–µ–љ–љ—Л—Е –Ї–∞—В–µ—Е–Њ–ї–∞–Љ–Є–љ–Њ–≤. –≠—В–Њ –Љ–Њ–ґ–љ–Њ —Б–і–µ–ї–∞—В—М –њ—Г—В–µ–Љ –њ—А–Њ–≤–µ–і–µ–љ–Є—П —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–Њ–≤ –њ–Њ —Б–Њ–Ї—А–∞—В–Є–Љ–Њ—Б—В–Є –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є —Б–ї–∞–±–Њ–≥–Њ –Њ–±—А–∞—В–љ–Њ–≥–Њ –∞–≥–Њ–љ–Є—Б—В–∞ (–≤ –Є–і–µ–∞–ї–µ ¬Ђ–љ–µ–є—В—А–∞–ї—М–љ–Њ–≥–Њ –∞–≥–Њ–љ–Є—Б—В–∞¬ї). –Т –љ–∞—И–Є—Е —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞—Е –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–є –Є–љ–Њ—В—А–Њ–њ–љ—Л–є —Н—Д—Д–µ–Ї—В –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞ –Љ–Њ–ґ–µ—В –±—Л—В—М —Б–≤—П–Ј–∞–љ —Б –µ–≥–Њ –і–µ–є—Б—В–≤–Є–µ–Љ –љ–∞ ќ≤вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А—Л, –∞ –љ–µ —Б–Њ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Љ–Є–Њ—Д–Є–ї–∞–Љ–µ–љ—В–Њ–≤ –Ї –Ї–∞–ї—М—Ж–Є—О [Zeit et al., 2000] –Є–ї–Є –і—А—Г–≥–Є–Љ–Є –љ–µ—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–Љ–Є —Н—Д—Д–µ–Ї—В–∞–Љ–Є. –°–Њ—Б—В–Њ—П–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є ќ≤вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–∞ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –≤–ї–Є—П–љ–Є–µ –љ–∞ —А–µ–≥—Г–ї—П—Ж–Є—О —А–µ—Ж–µ–њ—В–Њ—А–∞. Benovic et al. (1988) –љ–∞–±–ї—О–і–∞–ї–Є –Ї–Њ—А—А–µ–ї—П—Ж–Є—О –≤–љ—Г—В—А–µ–љ–љ–µ–є –Љ–Є–Љ–µ—В–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —З–∞—Б—В–Є—З–љ—Л—Е –Є –њ–Њ–ї–љ—Л—Е –∞–≥–Њ–љ–Є—Б—В–Њ–≤ —Б–Њ —Б—В–µ–њ–µ–љ—М—О —Д–Њ—Б—Д–Њ—А–Є–ї–Є—А–Њ–≤–∞–љ–Є—П —А–µ—Ж–µ–њ—В–Њ—А–∞, –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–µ–Љ–Њ–≥–Њ –Ї–Є–љ–∞–Ј–Њ–є ќ≤вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ ( ќ≤вАУ–Р–†–Ъ) –Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ–≥–Њ –і–ї—П –і–µ—Б–µ–љ—Б–µ–±–Є–ї–Є–Ј–∞—Ж–Є–Є –Є –њ–Њ–і–∞–≤–ї–µ–љ–Є—П –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —А–µ—Ж–µ–њ—В–Њ—А–∞ [Hausdorff et al., 1990]. –£ –Љ—Л—И–µ–є —Б –∞–Ї—В–Є–≤–љ—Л–Љ–Є –Љ—Г—В–∞–љ—В–∞–Љ–Є ќ≤2вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Њ–±—А–∞—В–љ–Њ–≥–Њ –∞–≥–Њ–љ–Є—Б—В–∞ ICI 118.551 –њ—А–Є–≤–µ–ї–Њ –Ї 50вАУ–Ї—А–∞—В–љ–Њ–Љ—Г —Г–≤–µ–ї–Є—З–µ–љ–Є—О –њ–ї–Њ—В–љ–Њ—Б—В–Є ќ≤вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –≤ –Љ–Є–Њ–Ї–∞—А–і–µ [Samana et al., 1997]. –°–ї–µ–і—Г—П —Н—В–Є–Љ –і–∞–љ–љ—Л–Љ, –Љ–Њ–ґ–љ–Њ –њ—А–µ–і–њ–Њ–ї–Њ–ґ–Є—В—М, —З—В–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О —Д–Њ—Б—Д–Њ—А–Є–ї–Є—А–Њ–≤–∞–љ–Є–µ ќ≤вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ —Д–µ—А–Љ–µ–љ—В–Њ–Љ ќ≤вАУ–Р–†–Ъ –Є –њ–Њ—Б–ї–µ–і—Г—О—Й–∞—П –і–µ—Б–µ–љ—Б–Є–±–Є–ї–Є–Ј–∞—Ж–Є—П –Є–ї–Є –њ–Њ–і–∞–≤–ї–µ–љ–Є–µ ќ≤вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –Љ–Њ–ґ–µ—В –±—Л—В—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Њ –њ—А–Є–µ–Љ–Њ–Љ –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞ –Є–ї–Є –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї–∞. –Ф–µ–є—Б—В–≤–Є—В–µ–ї—М–љ–Њ, —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–і–≤–µ—А–≥–∞—О—Й–Є—Е—Б—П –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–Љ—Г —И—Г–љ—В–Є—А–Њ–≤–∞–љ–Є—О, –і–ї–Є—В–µ–ї—М–љ–∞—П —В–µ—А–∞–њ–Є—П –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї–Њ–Љ–њ—А–Є–≤–Њ–і–Є—В –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О –њ–ї–Њ—В–љ–Њ—Б—В–Є ќ≤1вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –≤ –Љ–Є–Њ–Ї–∞—А–і–µ [Motomur –∞ et al., 1990]. –Ф–∞–љ–љ—Л—Е –Њ –≤–ї–Є—П–љ–Є–Є –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞ –љ–∞ ќ≤вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А—Л –љ–µ —Б—Г—Й–µ—Б—В–≤—Г–µ—В. ќ≤1вАУ—Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Ф—А—Г–≥–Њ–є –≤–∞–ґ–љ–Њ–є —З–µ—А—В–Њ–є ќ≤вАУ–±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤ —П–≤–ї—П–µ—В—Б—П –Є—Е —Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є ќ≤1вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤. –Э–µ–±–Є–≤–Њ–ї–Њ–ї —З–∞—Б—В–Њ –Њ–±–Њ–Ј–љ–∞—З–∞–µ—В—Б—П –Ї–∞–Ї ќ≤1вАУ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–є –њ—А–µ–њ–∞—А–∞—В. –Ф–µ–є—Б—В–≤–Є—В–µ–ї—М–љ–Њ, –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є van de Water –Є —Б–Њ–∞–≤—В . (1988) –љ–µ–±–Є–≤–Њ–ї–Њ–ї –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї 293вАУ–Ї—А–∞—В–љ—Г—О ќ≤1вАУ—Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В—М. –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –≤ —Н—В–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –і–ї—П –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –Ї–Њ–љ—Б—В–∞–љ—В –і–Є—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї—Б—П –∞–љ–∞–ї–Є–Ј –®–Є–ї–і–∞ (Schild) –і–ї—П –Є–љ–≥–Є–±–Є—В–Њ—А–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є ќ≤вАУ–∞–і—А–µ–љ–µ—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ—В–≤–µ—В–∞ –≤ –њ—А–∞–≤–Њ–Љ –њ—А–µ–і—Б–µ—А–і–Є–Є ( ќ≤1) –Є –≤ —В—А–∞—Е–µ–∞–ї—М–љ–Њ–є ( ќ≤2) —В–Ї–∞–љ–Є –Љ–Њ—А—Б–Ї–Є—Е —Б–≤–Є–љ–Њ–Ї. Pauwels –Є —Б–Њ–∞–≤—В. (1989) –њ—А–Њ–≤–µ–ї–Є —А—П–і –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —Б —А–∞–і–Є–Њ–ї–Є–≥–∞–љ–і–∞–Љ–Є –љ–∞ ќ≤1вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–∞—Е –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –Ї—А–Њ–ї–Є–Ї–Њ–≤ –Є ќ≤2вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–∞—Е –ї–µ–≥–Ї–Є—Е –Ї—А—Л—Б –Є –љ–∞–±–ї—О–і–∞–ї–Є 48вАУ55 –Ї—А–∞—В–љ—Г—О ќ≤1вАУ—Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е —Б —А–∞–і–Є–Њ–ї–Є–≥–∞–љ–і–∞–Љ–Є –љ–∞ CHOвАУ–Ї–ї–µ—В–Ї–∞—Е, —Б–Њ–і–µ—А–ґ–∞—Й–Є—Е —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–µ ќ≤1вАУ –Є ќ≤2вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А—Л, —В–∞ –ґ–µ –≥—А—Г–њ–њ–∞ —Г—З–µ–љ—Л—Е [–†auwels et al., 1991] –Њ–±–љ–∞—А—Г–ґ–Є–ї–Є —В–Њ–ї—М–Ї–Њ 10вАУ–Ї—А–∞—В–љ—Г—О ќ≤1вАУ—Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞. –Т –љ–∞—Б—В–Њ—П—Й–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є ќ≤1вАУ—Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞ –≤ –Љ–Є–Њ–Ї–∞—А–і–µ —З–µ–ї–Њ–≤–µ–Ї–∞ –Њ–Ї–∞–Ј–∞–ї–∞—Б—М 2вАУ4 –Ї—А–∞—В–љ–Њ–є, —З—В–Њ –±–Њ–ї–µ–µ –Є–ї–Є –Љ–µ–љ–µ–µ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є. ќ≤1вАУ—Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞ –≤ –Ї–ї–µ—В–Ї–∞—Е COSвАУ7, —Б–Њ–і–µ—А–ґ–∞—Й–Є—Е —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–µ ќ≤1вАУ –Є ќ≤2вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А—Л, —В–∞–Ї–ґ–µ –Њ–Ї–∞–Ј–∞–ї–∞—Б—М –ї–Є—И—М 3вАУ–Ї—А–∞—В–љ–Њ–є. –Т –Њ—В–ї–Є—З–Є–µ –Њ—В –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞ ќ≤1вАУ—Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї–∞ –≤ –Љ–Є–Њ–Ї–∞—А–і–µ —З–µ–ї–Њ–≤–µ–Ї–∞ –±—Л–ї–∞ 16вАУ20вАУ–Ї—А–∞—В–љ–Њ–є, –∞ –≤ –Ї–ї–µ—В–Ї–∞—Е COS вАУ 7вАУ15вАУ–Ї—А–∞—В–љ–Њ–є . –Т–∞–ґ–љ–Њ—Б—В—М ќ≤1вАУ—Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –≤ —В–µ—А–∞–њ–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П –љ–µ–Њ–і–љ–Њ–Ј–љ–∞—З–љ–Њ–є. –Ю–±–∞ ќ≤1вАУ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–∞ –±–Є—Б–Њ–њ—А–Њ–ї–Њ–ї (CIBIS II, 1999) –Є –Љ–µ—В–Њ–њ—А–Њ–ї–Њ–ї (MERITвАУHF, 1999), –∞ —В–∞–Ї–ґ–µ –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–є –Ї–∞—А–≤–µ–і–Є–ї–Њ–ї [Packer et al., 1996] –і–Њ–Ї–∞–Ј–∞–ї–Є —Б–≤–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В—М –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О. –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –Ї–∞—А–≤–µ–і–Є–ї–Њ–ї –Њ–±–ї–∞–і–∞–µ—В –µ—Й–µ –Є ќ≤вАУ–±–ї–Њ–Ї–Є—А—Г—О—Й–Є–Љ–Є [Bristow et al., 1992] –Є –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ—Л–Љ–Є —Н—Д—Д–µ–Ї—В–∞–Љ–Є [Yue et al., 1992], —В—А—Г–і–љ–Њ –Њ—В–і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–∞—В—М, –Ї–∞–Ї–Є–µ –Є–Љ–µ–љ–љ–Њ –µ–≥–Њ —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Б–≤–Њ–є—Б—В–≤–∞ –Њ–Ї–∞–Ј–∞–ї–Є –±–ї–∞–≥–Њ—В–≤–Њ—А–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О. –°—Г–Љ–Љ–∞—А–љ—Л–µ –і–∞–љ–љ—Л–µ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є in vivo –Є in vitro –≥–Њ–≤–Њ—А—П—В –Њ —В–Њ–Љ, —З—В–Њ –±–ї–Њ–Ї–∞–і–∞ –њ–µ—А–µ–і–∞—З–Є –≤—Б–µ—Е –∞–і—А–µ–љ–µ—А–≥–Є—З–µ—Б–Ї–Є—Е —Б–Є–≥–љ–∞–ї–Њ–≤ –Љ–Њ–ґ–µ—В –Є–Љ–µ—В—М –Њ—Б–Њ–±–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –≤ —В–µ—А–∞–њ–Є–Є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є [Bristow, 2000]. –Т –і–≤—Г—Е –Љ–µ—В–∞вАУ–∞–љ–∞–ї–Є–Ј–∞—Е —Н—Д—Д–µ–Ї—В–Њ–≤ ќ≤вАУ–±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ—Б–ї–µ –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ —Б–Љ–µ—А—В–љ–Њ—Б—В—М —Г–Љ–µ–љ—М—И–∞–ї–Є –Ї–∞–Ї —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ, —В–∞–Ї –Є –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ ќ≤вАУ–±–ї–Њ–Ї–∞—В–Њ—А—Л [Soriano et al., 1997; Freemantle et al., 1999]. –Э–∞–њ—А–Њ—В–Є–≤, –њ—А–µ–њ–∞—А–∞—В—Л —Б –≤–љ—Г—В—А–µ–љ–љ–µ–є —Б–Є–Љ–њ–∞—В–Њ–Љ–Є–Љ–µ—В–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О (–Т–°–Р) –Њ–±–ї–∞–і–∞–ї–Є –Љ–µ–љ—М—И–Є–Љ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —А–Є—Б–Ї–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –±–µ–Ј –Т–°–Р. –≠—В–Є –і–∞–љ–љ—Л–µ –≥–Њ–≤–Њ—А—П—В –Њ —В–Њ–Љ, —З—В–Њ —Б—А–µ–і–Є —А–∞–Ј–ї–Є—З–љ—Л—Е —Б–≤–Њ–є—Б—В–≤ ќ≤вАУ–±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤ –Є–Љ–µ–љ–љ–Њ –≤–љ—Г—В—А–µ–љ–љ—П—П —Б–Є–Љ–њ–∞—В–Њ–Љ–Є–Љ–µ—В–Є—З–µ—Б–Ї–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М (–∞ –љ–µ ќ≤1вАУ—Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В—М) –Є–Љ–µ–µ—В –Ј–љ–∞—З–µ–љ–Є–µ –і–ї—П –њ—А–Њ–≥–љ–Њ–Ј–∞ –њ—А–Є —Б–µ—А–і–µ—З–љ–ЊвАУ—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е . –Я–Њ–Љ–Є–Љ–Њ ќ≤вАУ–∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Є—З–µ—Б–Ї–Є—Е —Н—Д—Д–µ–Ї—В–Њ–≤, –љ–µ–±–Є–≤–Њ–ї–Њ–ї –Њ–±–ї–∞–і–∞–µ—В –њ—А—П–Љ—Л–Љ –≤–∞–Ј–Њ–і–Є–ї–∞—В–Є—А—Г—О—Й–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ, –Њ–њ–Њ—Б—А–µ–і–Њ–≤–∞–љ–љ—Л–Љ –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є–µ–Љ –Є–Ј —Н–љ–і–Њ—В–µ–ї–Є—П –Њ–Ї—Б–Є–і–∞ –∞–Ј–Њ—В–∞ [Bowman et al., 1994; Cockeroft et al., 1995]. –Э–µ–і–∞–≤–љ–µ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ —Н—В–Є —Н—Д—Д–µ–Ї—В—Л –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ—Л –Њ—В—З–∞—Б—В–Є –і–µ–є—Б—В–≤–Є–µ–Љ –∞–Ї—В–Є–≤–љ—Л—Е –Љ–µ—В–∞–±–Њ–ї–Є—В–Њ–≤ –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В –Њ–Ї–∞–Ј—Л–≤–∞—В—М —Б–≤–Њ–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ —З–µ—А–µ–Ј —Б—В–Є–Љ—Г–ї—П—Ж–Є—О —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ—Л—Е ќ≤2вАУ–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ [Broeders et al., 2000]. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Н—Д—Д–µ–Ї—В—Л –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞ in vivo –Љ–Њ–≥—Г—В –љ–µ–Љ–љ–Њ–≥–Њ –Њ—В–ї–Є—З–∞—В—М—Б—П –Њ—В —Н—Д—Д–µ–Ї—В–Њ–≤ in vitro . –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –≤ –љ–∞—Б—В–Њ—П—Й–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Є–Ј—Г—З–∞–ї–∞—Б—М –≤–љ—Г—В—А–µ–љ–љ—П—П –Љ–Є–Љ–µ—В–Є—З–µ—Б–Ї–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М ќ≤вАУ–±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤ –≤–љ–µ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Б–Є—Б—В–µ–Љ–љ—Л—Е –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є—Е —Н—Д—Д–µ–Ї—В–Њ–≤. –Т —Н—В–Њ–є —Б–≤—П–Ј–Є —Н—В–Є —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В—Л –Љ–Њ–≥—Г—В –Њ–±–ї–∞–і–∞—В—М –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞–Љ–Є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–Љ–Є in vivo . –†–µ–Ј—Г–ї—М—В–∞—В—Л —Н—В–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤–њ–µ—А–≤—Л–µ –Њ—Е–∞—А–∞–Ї—В–µ—А–Є–Ј–Њ–≤–∞–ї–Є ќ≤вАУ–∞–і—А–µ–љ–µ—А–≥–Є—З–µ—Б–Ї–Є–µ —Н—Д—Д–µ–Ї—В—Л –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞ –≤ –Љ–Є–Њ–Ї–∞—А–і–µ —З–µ–ї–Њ–≤–µ–Ї–∞. –Э–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П —Б GвАУ–±–µ–ї–Ї–Њ–Љ, –∞ —В–∞–Ї–ґ–µ –Њ–±—А–∞—В–љ—Л–є –∞–≥–Њ–љ–Є–Ј–Љ —П–≤–ї—П—О—В—Б—П –ґ–µ–ї–∞—В–µ–ї—М–љ—Л–Љ–Є —Н—Д—Д–µ–Ї—В–∞–Љ–Є ќ≤вАУ–±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤ –≤ —В–µ—А–∞–њ–Є–Є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є. –Э–∞–±–ї—О–і–µ–љ–Є–µ —В–Њ–≥–Њ, —З—В–Њ –≤ –Љ–Є–Њ–Ї–∞—А–і–µ —З–µ–ї–Њ–≤–µ–Ї–∞ –љ–µ–±–Є–≤–Њ–ї–Њ–ї —П–≤–ї—П–µ—В—Б—П –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–Љ, –њ—А–Њ–ї–Є–≤–∞–µ—В —Б–≤–µ—В –љ–∞ —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Б–≤–Њ–є—Б—В–≤–∞ —Н—В–Њ–≥–Њ –≤–µ—Й–µ—Б—В–≤–∞. –Э–µ–Њ–±—Е–Њ–і–Є–Љ—Л –і–∞–ї—М–љ–µ–є—И–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –і–ї—П –Є–Ј—Г—З–µ–љ–Є—П –Њ—Б–Њ–±–Њ–≥–Њ –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Д–Є–ї—П –љ–µ–±–Є–≤–Њ–ї–Њ–ї–∞.
–Ю–±–Ј–Њ—А –њ–Њ–і–≥–Њ—В–Њ–≤–ї–µ–љ –њ–Њ –Љ–∞—В–µ—А–Є–∞–ї–∞–Љ British Journal of Pharmacology 2001; 132: 1817вАУ1826