В статье представлены результаты
временной двухкамерной
электрокардиостимуляции у 9
больных гипертрофической
кардиомиопатией. Сделаны выводы о
целесообразности предварительного
проведения временной
электрокардиостимуляции с оценкой
гемодинамических параметров в
покое и при нагрузке для
прогнозирования результатов
постоянной
электрокардиостимуляции.
The paper presents the outcomes of dual chambered pacing in 9
patients with hypertrophic cardiomyopathy. It is concluded that
is very important temporary pacing, by estimating hemodynamic
parameters at rest and during exercise for prediction of the
outcomes of permanent pacing.
Key words: Hypertrophic cardiomyopathy, temporary pacing.
Н. А. Мазур.
Доктор мед. наук,
профессор, зав. кафедрой
кардиологии Российской
медицинской академии
последипломного образования,
Москва.
А.М.Жданов.
Доктор мед.
наук,руководитель отделения
хирургии нарушений проводимости и
ритма сердца Института хирургии
им.А.В.Вишневского РАМН,
Московского центра
электрокардиостимуляции.
В. В. Чигинева, С. А.
Термосесов.
Кафедра кардиологии
Российской медицинской академии
последипломного образования,
Москва.
Отделение хирургии
нарушений проводимости и ритма
сердца Института хирургии им.
А. В. Вишневского РАМН,
Московский центр
электрокардиостимуляции.
Prof. N.A. Mazur.
Head, Department of Cardiology, Russian Medical Academy of
Postgraduate Training;
A.M. Zhdanov.
Head, Department of Surgery for Cardiac
Conduction and Rhythm Disturbances, A.V. Vishnevsky Institute of
Surgery, Russian Academy of Medical Sciences, Moscow Cardiac
Pacing Center.
V.V. Chigineva, S.A. Termosesov
Department of Cardiology, Russian Medical Academy of Postgraduate
Training, Moscow.
Department of Surgery for Cardiac Conduction and Rhythm
Disturbances, A.V. Vishnevsky Institute of Surgery, Russian
Academy of Medical Sciences, Moscow Cardiac Pacing Center.
Correspondence to: V.V. Chigineva, Department of Cardiology,
Russian Cardiology Research and Production Center, 3rd
Cherepkovskaya St. 15a, Build. 9, Moscow 121552, Tel. 414-68-58
Введение
Обструкция выносящего тракта
левого желудочка (ЛЖ) - один из
важнейших механизмов, ведущих к
появлению различных симптомов
заболевания и ограничивающих
физическую активность, встречается
у 25% пациентов с гипертрофической
кардиомиопатией (ГКМП) [1]. Н. Newman и
соавт. [2] доказали, что наличие
обструкции выносящего тракта в
покое, превышающее 20 мм рт. ст.,
является предвестником
прогрессирования симптомов
заболевания, но не влияет на
частоту внезапной смерти в этой
группе больных.
Для уменьшения симптомов
заболевания, таких как одышка при
физической нагрузке, боли в левой
половине грудной клетки, обмороки
или предобморочные состояния, в
течение более 30 лет применяют
b-блокаторы, верапамил, дилтиазем,
дизопирамид и амиодарон. Несмотря
на это, некоторые больные все же
остаются рефрактерными к
проводимой терапии или у них
наблюдаются побочные реакции на
данные препараты. В подобных
случаях альтернативной является
миосептэктомия или имплантация
митрального клапана (МК) с целью
уменьшения градиента давления. По
данным разных авторов летальность
во время операции составляет от 1,3 -
2 до 14 - 17% [3 - 5]. После операции у
части больных наблюдаются такие
осложнения, как полная
предсердно-желудочковая блокада,
блокада левой ножки пучка Гиса,
перфорация межжелудочковой
перегородки (МЖП). Некоторые
больные отказываются от проведения
операции на "открытом" сердце.
Поэтому требуются другие подходы к
их лечению.
В 1975 г. Р. Hassenstein и соавт. впервые
опубликовали результаты
проведения
электрокардиостимуляции (ЭКС) у
пациентов с обструктивной формой
ГКМП. Позже в целом ряде других
работ было показано, что
двухкамерная ЭКС может уменьшать
градиент давления в выносящем
тракте ЛЖ и таким образом улучшать
самочувствие больных [6 - 16]. Такой
подход основывается на мнении, что
возбуждение МЖП при проведении
Р-синхронизированной ЭКС правого
желудочка или последовательной
предсердно-желудочковой ЭКС
вызывает парадоксальное движение
МЖП в сторону от задней стенки ЛЖ во
время систолы, в результате чего
размеры выносящего тракта ЛЖ
увелчиваются и скорость кровотока
в нем снижается. Учитывая
вышеизложенное, нами была
проведена временная ЭКС больным
гипертрофической кардиомиопатией
для оценки влияния ее на показатели
гемодинамики в течение короткого
курса.
Пациенты и методы. В исследование
было включено 9 пациентов с ГКМП (5
мужчин и 4 женщины), средний возраст
пациентов составил 38,2 года (от 14 - до
59 лет). Диагноз ГКМП был установлен
на основании обнаружения утолщения
МЖП или свободной стенки ЛЖ при
нормальных размерах ЛЖ и
отсутствии у пациентов
артериальной гипертензии,
приобретенных или врожденных
пороков сердца, а также других
заболеваний, которые могли бы
привести к гипертрофии миокарда ЛЖ.
У 5 пациентов для установления
точного диагноза и исключения
сопутствующей патологии была
проведена
коронаровентрикулография, при
которой были обнаружены
непораженные коронарные артерии.
Большинство пациентов относились к
III и IV функциональному классу (ФК) по
NYHA. Обструкция выносящего тракта ЛЖ
с градиентом давления в выносящем
тракте ЛЖ в покое более 30 мм рт. ст.
наблюдалась у 5 пациентов и
составляла в среднем 50,3 + 28,0 мм рт.
ст., у 4 пациентов обструкции в покое
не было. Средняя длительность
заболевания до проведения
манипуляции составила 15,3 + 9 лет. У
половины пациентов заболевание
было выявлено случайно - при
медицинском осмотре был обнаружен
шум; 2 пациента из-за наличия на ЭКГ
изменений по типу "рубцовых"
были направлены для дальнейшего
обследования; у 3 больных дебютом
явилось возникновение загрудинных
болей при ходьбе.
У всех пациентов имеются
родственники, больные ГКМП, причем
у 6 пациентов в семьях были случаи
внезапной смерти в молодом
возрасте.
При поступлении в стационар все
пациенты жаловались на одышку при
физической нагрузке, у 7 больных
наблюдались перебои в работе
сердца и приступы сердцебиений, у
половины были обмороки. При
объективном осмотре у всех
выслушивался грубый систолический
шум изгнания с максимумом в 5-й
точке. При холтеровском
мониторировании были выявлены
следующие нарушения ритма сердца: у
7 больных - желудочковая
экстрасистолия, причем у 2
пациентов куплеты; у 1 пациентки -
пробежки неустойчивой
желудочковой тахикардии, у 1 -
пароксизмы мерцательной аритмии.
При эхокардиографическом (ЭхоКГ)
исследовании толщина МЖП в среднем
составила 2,5 + 0,7 см, задней стенки ЛЖ
(ЗСЛЖ) - 1,3 + 0,2 см, соотношение
МЖП/ЗСЛЖ равнялось 2; митральная
регургитация наблюдалась у 8
больных, пролапс - митрального
клапана у 3, ни у одного пациента не
было кальциноза митрального
клапана и обструкции выносящего
тракта правого желудочка. Фракция
выброса по данным ЭхоКГ в среднем
составила 79,6 + 6,9 % (табл. 1).
До поступления в стационар
большинство пациентов в течение 3,8 +
2,5 года получали анаприлин в
средней дозе 102 + 27,1 мг/день (от 60 до
120 мг); часть больных получала
верапамил в дозе 360 + 214,1 мг/день (от
120 до 640 мг) в течение 5,3 + 3,3 года; 1
пациентка принимала ранитек по 5
мг/день; все больные отмечали
неэффективность терапии.
Показанием к проведению временной
ЭКС было сохранение высокого
градиента в выносящем тракте ЛЖ,
несмотря на последовательное
применение максимально
переносимых доз атенолола,
верапамила и ритмилена, а у 4
пациентов с необструктивной формой
ГКМП - наличие сопутствующей
предсердно-желудочковой блокады I -
II степени, степень которой
нарастала при назначении даже
малых, неэффективных доз данных
препаратов. До начала ЭКС все
лекарства были отменены на срок,
равный 5 периодам полувыведения.
Пациенты прошли общеклиническое
обследование, у них регистрировали
ЭКГ в 12 отведениях, проводили
24-часовое холтеровское
мониторирование ЭКГ,
велоэргометрию (ВЭМ) и ЭхоКГ до
оперативного лечения без приема
медикаментов; в конце курса ЭКС, в
1-й день установки параметров
стимуляции, проводились
контрольные электро- и
эхокардиографическое
исследования. Все пациенты дали
информированное согласие на
проведение манипуляции.
Больные оценивали каждый симптом
заболевания (боль, одышка,
сердцебиения, головокружения) по
4-балльной шкале: 0 - полное
отсутствие симптома; 1 - слабая
степень выраженности, т. е. симптом
не появляется при обычной
физической активности, а возникая,
протекает легко, не вызывая
изменений в общем состоянии
пациента; 2 - умеренная
выраженность, т. е. обычная
физическая нагрузка вызывает
появление симптомов, из-за которых
состояние пациента ухудшается; 3 -
значительная выраженность
симптома, т.е. любая физическая
активность вызывает
дискомфорт,симптомы появляются
даже в покое.
ВЭМ. Для оценки толерантности к
физической нагрузке проводили ВЭМ
в положении лежа на спине,
использовался протокол непрерывно
возрастающих нагрузок [17], нагрузки
прекращались при появлении
приступа стенокардии, повышении
диастолического АД более 120 мм рт.
ст., депрессии сегмента ST [18], а также
при появлении слабости,
головокружения, нарастании одышки,
гипотонии.
Таблица 1. Клинические характеристика больных ГКМП
Число больных
| Жалобы: | |
| одышка | 9 |
| сердцебиения и перебои в работе сердца | 7 |
| обмороки | 5 |
| боли за грудиной | 7 |
| слабость | 3 |
| ФК по NYHA | 2,7± 0,7 |
| НРС: | |
| желудочковая экстрасистолия | 7 |
| пробежки ЖТ | 1 |
| пароксизмы МА | 1 |
| ПЖБ I - III степени | 4 |
| ЭхоКГ: | |
| обструкция выносящего тракта ЛЖ | 5 |
| наличие митральной регургитации | 8 |
| пролапс МК | 3 |
П р и м е ч а н и е . НРС - нарушения
ритма сердца,
ЖТ - желудочковая тахикардия, МА -
мерцательная аритмия,
МК - митральный клапан; ПЖБ -
предсердно-желудочковая блокада.
| Средняя минимальная частота | 55 импульсов |
| стимуляции предсердий | в минуту |
| Средний порог стимуляции желудочков, мВ | 0,7 |
| Средняя амплитуда импульсов желудочков, В | 5 |
| Средний порог стимуляции предсердий, мВ | 0,9 |
| Средняя амплитуда импульсов предсердий, В | 4,4 |
| Средняя продолжительность P - Q, мс | 236 |
| Средняя продолжительность предсердно-желудочковой задержки, мс | 166 |
Таблица 3. Динамика показателей на временной ЭКС
| Уровень | Изменения, % | ||
| исходный | на временный ЭКС | ||
| Градиент давления у больных с обструкцией, n = 5 | 50 | 46 | -8* |
| Средняя скорость кровотока в выносящем тракте ЛЖ по всей группе, n = 9 | 2,5 (1,1) | 2,3 (1,2) | -13** |
| Средняя скорость кровотока в выносящем тракте ЛЖ у больных с предсердно желудочковой задержкой более 160 мс, n = 5 | 1,7 (0,6) | 1,3 (0,5) | -36** |
| ФК по NYHA, средние значения | 2,7 | 2,3 | |
p<0,01;** p<0,05.
ЭхоКГ. Исследование проводили на аппарате 70 А-SAL фирмы "Toshiba" в режиме реального времени ультразвуковым датчиком 2,5 МГц. При исследовании из апикальной позиции определяли скорость кровотока в выносящем тракте на подклапанном уровне. Градиент в выносящем тракте рассчитывали по модифицированной формуле Бернулли [19].
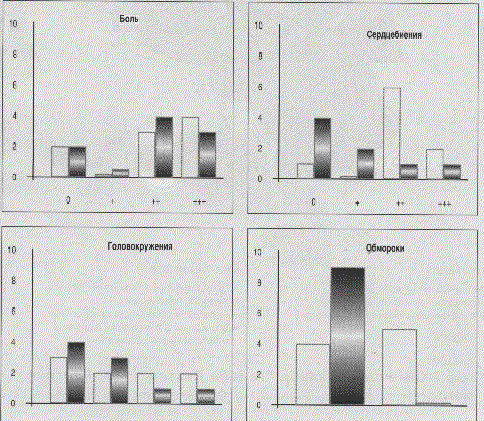
Рис. 1. Динамика клинических
симптомов на фоне временной ЭКС, 0-
отсутствиесимптомов, +- слабая
выраженность симптома, +++-
значительная выраженность
симптома.

Временная ЭКС. Для проведения ЭКС
использовали временный
двухкамерный кардиостимулятор
модели 3070 фирмы "Pacesetter" (США),
позволяющий навязывать ритм в
режиме DDD. Под местной анестезией по
методике Seldinger проводили пункцию
подключичной вены, через просвет
которой под рентгеновским
контролем вводили два электрода.
Электрод ПЭЭФ (электрод с активной
фиксацией, типа
"буравчик",производства
Украины) фиксировали в области ушка
правого предсердия. Второй
электрод LES 165 (производства Чехии)
устанавливали в области верхушки
правого желудочка. Стимуляцию
проводили в монополярном режиме,
при этом индифферентные электроды
в виде булавок укрепляли на коже
пациента в подключичной области.
Особенность процедуры состояла в
том, что для временной стимуляции
были использованы электроды для
постоянной стимуляции. Это было
обусловлено тем, что требовалось
объективно оценить изменение
физических возможностей пациента
через 5 - 7 дней, в течение которых
пациенты вели активный образ жизни,
а в конце срока наблюдения всем
проводилась ВЭМ.
Порог стимуляции и амплитуду
внутрисердечного сигнала
определяли с помощью прибора ЕRА-20
фирмы "Biotronic" (Германия).
Задаваемые параметры стимуляции
были следующими: режим - DDD
(универсальный сенквециальный
режим или двух-камерная стимуляция
сердца); минимальная частота
стимуляции от 50 до 55 имп/мин;
средняя амплитуда импульсов по
желудочкам составила 5 В,
длительность стимулирующего
импульса - 0,5 мс; средняя амплитуда
импульсов по предсердиям - 5 В,
длительность стимулирующего
импульса - 0,5 мс, рефрактерный
период по предсердиям - 250 мс,
рефрактерный период по желудочкам -
325 мс, гистерезис - 0.
Предсердно-желудочковая задержка
программировалась в зависимости от
исходной величины интервала Р - Q,
который в среднем составил 236,8 мс,
причем минимальное значение ее
было 112 мс, максимальное - 400 мс.
Предсердно-желудочковый интервал
подбирали опытным путем, он
соответствовал максимально
возможному по величине интервалу,
вызывающему предвозбуждение
желудочков без появления сливных
сокращений; на ЭКГ при этом после
стимула появлялся уширеный
комплекс QRS, напоминающий по виду
блокаду левой ножки пучка Гиса. Он
составил в среднем 166 мс, т.е. 70% от
исходной длительности PQ (табл.
2).
Статистическую обработку данных
производили с помощью пакета
программ "Supercalc 5.0",
использовали критерий Стьюдента.
Для средних величин в скобках
указана величина стандартного
отклонения.
Результаты. За время наблюдения в
течение 6,3 + 1,7 дня (от 8 ч до 8 сут)
только у 1 пациента субъективно
отмечалось ухудшение самочувствия
- усилились сердцебиение и одышка; у
него ЭКС была досрочно прекращена
на 3-й день. Другой пациентке по
экстренным показаниям была
выполнена имплантация постоянного
ЭКС из-за остро развившейся
предсердно-желудочковой блокады III
степени с приступом МЭС через 8 ч
наблюдения. Остальные пациенты
отметили улучшение самочувствия:
уменьшилась одышка, у 5 пациентов
уменьшился болевой синдром, за
время наблюдения не было
зарегистрировано ни одного
обморока, 4 пациента отметили
уменьшение головокружений (рис. 1).
Однако 2 пациента обратили внимание
на усиление болевых ощущений в
левой половине грудной клетки. ФК
по NYHA улучшился на 1 ступень у 5
пациентов, остался без изменения у 3
и у 1 возрос до IV (у него ЭКС была
досрочно прекращена). В среднем по
группе ФК по NYHA уменьшился с 2,7 до 2,3
(рис. 2).Скорость кровотока в
выносящем тракте ЛЖ по данным
допплерографии снизилась у 7
пациентов, у 2 осталась на прежнем
уровне; в среднем по группе
отмечалось достоверное снижение на
13% от исходного уровня,в подгруппе
пациентов с обструкцией на 8%. У
пациентов с величиной
предсердно-желудочковой задержки
более 160 мс, отмечалось более
значительное снижение скорости
кровотока по сравнению с
остальными (на 36%; табл. 3).
Ограничения в увеличении
предсердно-желудочковой задержки
были связаны с тем, что у
большинства пациентов интервал P - Q
исходно составлял менее 150 мс и для
проведения эффективной ЭКС
приходилось программировать
предсердно-желудочковую задержку
на величину, в среднем на 30% меньшую
исходного P - Q, что в свою очередь
приводило к укорочению систолы
предсердий.
При проведении ВЭМ не было выявлено
достоверного прироста пороговой
мощности и времени нагрузки, не
было различий в частоте
возникновения болевого синдрома
при нагрузке, появления
желудочковых экстрасистол как во
время нагрузки, так и в
восстановительном периоде. Однако
при одинаковом уровне пороговой
мощности на фоне проведения ЭКС
максимальная частота сердечных
сокращений (ЧСС) была достоверно
ниже, но и время ее восстановления
было достоверно продолжительнее.
При суточном мониторировании ЭКГ
было отмечено уменьшение
количества желудочковых
экстрасистол в среднем на 61% по
сравнению с исходным уровнем.
По результатам временной
стимуляции 4 пациентам была
выполнена имплантация двух
камерных аппаратов Synchrony III фирмы
"Pacesetter".
Обсуждение. Опыт проведения ЭКС у
больных ГКМП показал, что при ЭКС
происходит достоверное снижение
градиента давления в выносящем
тракте ЛЖ по сравнению с исходным
уровнем без изменения ЧСС. Эффект
снижения градиента был тем
значительнее, чем больше по
величине была
предсердно-желудочковая задержка,
что в свою очередь зависело от
исходной длительности интервала P -
Q. В то же время при ЭКС необходимо
добиваться достаточного
предвозбуждения желудочков с
появлением уширенного комплекса QRS
по типу блокады левой ножки пучка
Гиса при отсутствии "сливных"
комплексов, что обеспечивает
наибольшее снижение градиента за
счет парадоксального движения МЖП.
Это важно и потому, что значение
величины градиента прямо
пропорционально времени контакта
створок митрального клапана с МЖП
[20]. Таким образом,чем более будет
выражено парадоксальное движение
МЖП, тем дальше отойдут створки МК
от МЖП. В то же время значительное
уменьшение
предсердно-желудочковой задержки
при двухкамерной стимуляции ведет
к укорочению систолы предсердий и
уменьшению вклада предсердий в
наполнение ЛЖ [21]. Так, в
исследовании L. Fananapazir и соавт. [22]
наблюдалось ухудшение
самочувствия у пациентов с
необструктивной формой ГКМП в
отдаленные сроки после имплантации
ЭКС, потребовавшее дополнительного
назначения лекарственных средств,
что может быть связано с нарушением
диастолической функции ЛЖ. Для
предотвращения этого
рекомендуется удлинение интервала
P - Q с помощью лекарственных средств
[23].
Ряд авторов [11,14,15] наблюдали
достоверное увеличение времени
нагрузки на тредмиле по сравнению с
исходным уровнем. В нашей подгруппе
при проведении ВЭМ в положении лежа
подобных изменений не наблюдалось,
однако при одинаковой выполненой
пороговой нагрузке при ЭКС
наблюдалось достоверное снижение
ЧСС на высоте нагрузки по сравнению
с исследованием без применения
медикаментов.
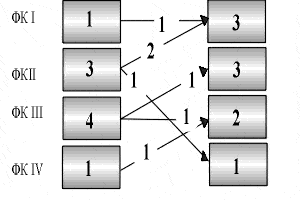
Рис 2. Изменения ФК по NYHA при проведении временной электрокардиостимуляции у больных ГКМП (цифры в прямоугольниках - число ,больных перешедших из одного ФК в другой.
Как и другие авторы [11,12,14,15], мы
отмечали значительное уменьшение
одышки и головокружений при ЭКС. У
части больных появились неприятные
болевые ощущения в левой половине
грудной клетки. Подобные ощущения
обычно появляются в первые недели
после имплантации
кардиостимулятора из-за
травматизации миокарда головками
электродов, после их инкапсуляции
симптомы исчезают.
Вопрос о показаниях к имплантации
ЭКС при ГКМП до сих пор однозначно
не решен. Наблюдаемое нами, а также
другими авторами снижение
градиента не достигало критической
величины 30 мм рт. ст. В то же время R.
Morh [3] было показано, что остаточный
градиент выше 15 мм рт. ст. после
миосептэктомии является
предвестником смертности после
операции. Таким образом, необходимы
длительные исследования для
изучения этого вопроса в отношении
как ЭКС, так и основных применяемых
при ГКМП лекарственных средств, тем
более что и при медикаментозной
терапии часто не наблюдается
значительного (менее 30 мм рт. ст.)
снижения градиента.
Выводы. 1.Целесообразно
предварительное проведение
временной ЭКС с оценкой
гемодинамических параметров в
покое и при нагрузке для
прогнозорования результатов
постоянной ЭКС.
2. Наилучшие ближайшие
положительные результаты
наблюдаются у больных, у которых
интервал P - Q больше 160 мс.
3. У больных с исходно коротким
интервалом P - Q или в тех случаях,
когда имеет место эффективная
стимуляция при
предсердно-желудочковой задержке
менее 160 мс, рекомендуется
обеспечить удлинение интервала P - Q
с помощью лекарственных
препаратов.
Литература:
1. Pierce GE, Morrow BJ, Braunwald E. Idiopatic hypertrophic
subaortic stenosis. Circulation 1964;30 (suppl 4): IV-152-IV-213.
2. NewmanH, Sugrue D, Oakley CM, et al. Relation of left
ventricular function and prognosis in hypertrophic
cardiomyopathy: an angiographic study. J Am Coll Cardiol
1985;5:1064-74.
3. Mohr R, Schaff HV, Danielson GK, et al. The outcome of cal
treatment of hypertrophic obstructive cardiomyopathy. J Thorac
Cardiovasc Surg 1989;97:666-74.
4. Roberts WC. Operative treatment of hypertrophic obstructive
cardiomyopathy: The case against mitral valve replacement. Am J
Cardiol 1973;32:377-81.
5. Seiler C, Hess OM, Schoenberh M, et al. Long-term follow-up of
medical versus surgical therapy for hypertrophic cardiomyopathy:
A retrospective study. J Am Coll Cardiol 1991;17:634-42.
6. Hassenstein P, Walther H, Dittrich J. Haemodynamische
Veranderungen durch einfach und gekoppelte Stimulation bei
Patienten mit obstruktiver Kardiomyopathie. Verh Dtsch Ges Inn
Med 1975;81:170-3.
7. Hassenstein P, Storch HH, Schmitz W. Erfahrungen mit der
Schrittmacherdauerbehandlung bei Patienten mit obstrucktiver
Kardiomyopathie. Thoraxchirurgie 1975;23:496-9
8. Jonson AD, Daily PO. Hypertrophic subaortic stenosis
complicated by high degree heart block: Successful treatment with
atrial synchronous ventricular pacemaker. Chest 1975;67:491-4.
9. Duck HJ, Hutschemeiter W, Paneau H, Trenckmann H.
Atrioventricular stimulation with reduced AV-delay time as a
therapeutic principle in hypertrophic obstructive cardiomyopathy.
Z Gesamte Inn Med 1984;39:437-47.
10. Jusgen W. Therapie der hypertroph-obstruktiven
Kardiomyopathie mit AV-sequentiellen Herzschrittmachersystemen,
in Weiki A (ed): Physiologische Stimulation des Herzens. Perimed,
Erlangen, 1984.
11. McDonald K, McWilliams E, O'Keeffe B, Maurer B. Functional
assessment of patients treated with permanent dual chamber pacing
as a primary treatment for hypertrophic cardiomyopathy. Eur Heart
J 1988;9:893-8.
12. Fananapazir L, Winkler J, Schenke B, et al. Reducing left
ventricular outflow tract obstruction in patients with
hypertrophic cardiomyopathy by pacing-induced interventricular
septal preexcitation (abstract). J Am Coll Cardiol 1989;13:117A.
13. Richter T, Cserhalmi M, Lengyel M, et al. Changes in left
ventricular hemodynamics of hypertrophic obstructive
cardiomyopathy (HOCM) patients treated with VAT sequential
pacing, in Baroldi G, Camerini F, Goodwin JF (eds): Advances in
Cardiomyopathies. New York, Springer-Verlag, 1990;168-74.
14. Fananapazir L, Cannon RO III, Tripodi D, Panza JA. Impact of
dual-chamber permanent pacing in patients with obstructive
hypertrophic cardiomyopathy with symptoms refractory to verapamil
and b-adrenergic blocker therapy. Circulation 1992;85:2149-61.
15. Jeanremaud X, Goy J-J, Kappenberger L. Effect of dual-chamber
pacing in hypertrophic obstructive cardiomyopathy. Lancet
1992;339:1318-23.
16. Tascon J, Albarran A, Perez-Carasa MA, et al. The treatment
of hypertrophic obstructive cardiomyopathy refractory to medical
treatment by DDD pacing. Rev Esp Cardiol 1994;47 (5):294-302.
17. Counihan P.J., Frenneaux M.P., Webb D.J., Mc Kenna W.J.
Abnormal vascular responses to supine exercise in hypertrophic
cardiomyopathy. Circulation 1991;84:686-96.
18. Aронов Д.М., Лупанов В.П., Михеева
Т.Г. Функциональные пробы в
кардиологии. Лекции III, IV.
Кардиология. - 1995. - № 12. - C. 83-93.
19. Hatle L, Andelsen B: Doppler ultrasound in cardiology.
Physical principles and clinical applications. Philadelphia, Lea
& Febiger, 1985;205-17.
20. Pollich C., Rakowcki H, Wigle E.D.. Muscular subaortic
stenosis: the quantitative relationship between systolic anterior
motion and the pressure gradient. Circulation 1984;69:43-9.
21. В.В. Желнов, И.Ф. Павлова, В.И.
Симонов, и др.
Доплер-эхокардиографическое
исследование диастолической
фукции левого желудочка у больных
ишемической болезнью сердца при
временной одно- и двукамерной
электрокардиостимуляции.
Кардиология. - 1995. - № 6. - С. 43-45.
22. Cannon RD III, Tripodi D, Dilsizian V, Panza JA, Fananapazir
L: Result of permanent dual-chamber pacing in symptomatic
nonobstructive hypertrophic cardiomyopathy. Am J Cardiol
1994;73:571-6.
23. Gras D, de Place C, Le Breton H, et al. Importance of
atrioventricular synchrony in hypertrophic obstructive
cardiomyopathy treated by cardiac pacing. Arch Mal Coeur Vaiss
1995;88 (2):215-23.








