Клинические проявления старческого амилоидоза крайне разнообразны: нарушения функций миокарда, инсулиннезависимый сахарный диабет, пресенильная и сенильная деменция, катаракта, глаукома, сенильная макулярная дистрофия и др. Однако при жизни старческий амилоидоз распознается крайне редко.
The paper shows the evolution of knowledge of senile amyloidosis in the past quarter of the century. Schwartz’s tetrad has generally stopped existing as a clinical and morphological substrate of senile amyloidosis. Both systemic and local types of the disease are revealed. Their morphology and pathogenesis are examined. Clinical and morphological characteristics of each type are given.
В. В. Серов,
Московская медицинская академия
им. И. М. Сеченова
V. V. Serov, I. M. Sechenov Moscow Medical Academy
В 1970 г. немецкий патолог
Ph. Schwartz [1] описал характерную для
старческого амилоидоза тетраду –
содружественное поражение сердца,
аорты, головного мозга и островков
поджелудочной железы. Он считал,
что эта тетрада лежит в основе
физической и психической
деградации в старческом возрасте и
встречается у стариков чуть ли не
постоянно.
Раскрыть и
расширить рамки тетрады Шварца
стало возможным совсем недавно,
когда амилоидоз был разделен на
генерализованные и локальные формы
и появились сообщения о различных
предшественниках белка фибрилл
амилоида. Среди генерализованных
форм амилоидоза (АА, AL, FAР) был
выделен четвертый тип – старческий
системный амилоидоз (SSA), а среди
локальных форм старческого
амилоидоза – эндокринный и
неэндокринный [2, 3]. Первый
представлен изолированным
амилоидозом предсердий и
амилоидозом островков
поджелудочной железы, второй –
амилоидозом аорты, церебральным
амилоидозом, амилоидозом глаза,
амилоидозом простаты и семенных
пузырьков.
При
генерализованных формах
предшественники фибрилл белка
амилоида циркулируют в крови
(сывороточные предшественники) и
для их преформации в фибриллярный
белок амилоида требуется участие
эффекторных клеток (макрофага,
плазматической, миеломной клетки и
др.) или клеток, к которым имеется
сродство предшественника. При
локальных же формах амилоидоза
предшественник “синтезирует” та
же клетка, которая строит из него
амилоидные фибриллы, и среди этих
клеток особое место занимают
представители диффузной
эндокринной системы – апудоциты.
Исключение составляет
церебральный амилоидоз, при
котором предшественник белка
фибрилл амилоида циркулирует в
спинномозговой жидкости.
Предшественники фибриллярного
белка амилоида представлены в
таблице.
Старческий
системный амилоидоз. Частота SSA
по различным оценкам составляет от
3,6 до 46,0% [4] среди умерших старше 70
лет; несколько чаще он встречается
у мужчин, хотя это мнение разделяют
далеко не все авторы.
Предшественником
белка фибрилл амилоида – ASC1 –
является транстиретин
(преальбумин, см. таблицу), не
идентичный таковому при ряде форм
генерализованного наследственного
и локального амилоидоза, что
доказано иммуногистохимически. Ряд
авторов считают, что ASC1 отражает
эволюцию старческого варианта
преальбумина и представляет собой
мутантный белок [5]. P. Westermark и соавт.
[6] обратили внимание на депрессию
сывороточного преальбумина при SSA и
корреляцию с уровнем сывороточных
ретинолсвязаных белков. Эти
исследования позволили
предположить, что в пожилом
возрасте имеются нарушения
метаболизма преальбумина и
повышенная склонность к
амилоидообразованию, чем и
объясняется снижение концентрации
преальбумина в сыворотке.
Механизм
образования амилоидного белка из
циркулирующего в крови
предшественника изучен плохо. Не
исключено сродство
предшественника к мышечной ткани.
Вероятно, этим объясняется тот
факт, что в качестве амилоидобласта
в миокарде выступает кардиомиоцит,
а в сосудах – гладкомышечная
клетка [4, 7].
SSA –
кардиоваскулярный амилоидоз.
Поэтому большинство авторов
отмечают его сходство с системным
AL-амилоидозом по
распространенности, локализации
амилоидных отложений (сердце,
сосуды, прежде всего легких,
кишечника), а также выраженности
поражения сердца, не достигающей,
однако, такой степени, как при AL. Для
SSA, в отличие от AL, типичны
очаговость и малая концентрация
амилоидных отложений, а также
начало болезни в более позднем
возрасте, нередкое сочетание с
атеросклерозом.
Патология
сердца при SSA является ведущей.
Вовлечение в патологический
процесс предсердий отмечается у 71%
больных, желудочков – у 67%,
коронарных сосудов – у 50%, из них у
40% с сужением просвета, что
симулирует ишемическую болезнь
сердца и образование
псевдоинфарктных очагов.
Существенна и частота нарушения
функции возбудимости сердца.
Обнаруживается
корреляция между степенью и типом
отложений амилоида в сердце. При I и
II степени находят узелковые
отложения в миокарде, реже в мелких
сосудах, при III и IV степени амилоид
имеет вид россыпи с обязательным
вовлечением сосудов. Возможно
тотальное поражение сердца или
только предсердий, только
желудочков или клапанов.
Среди причин
летального исходa при SSA основное
место занимает сердечная
недостаточность. Наши данные
показывают, что половина бльных SSA
умирает от сердечной
недостаточности и половина – от
ишемического инсульта. У больных SSA
инфаркт миокарда выявляется чаще,
чем у больных того же возраста без
амилоидоза.
Диагностика SSA
основывается на полиморфной
клинической картине и данных
биопсии органов, вовлеченных в
патологический процесс. При этом
учитываются методы идентификации
белка ASC1: неспецифические и
специфический
иммуногистохимический с
использованием антисыворотки к ASC1.
При сочетании SSA с амилоидозом
аорты, простаты,
семенных пузырьков амилоидные
массы в этих органах не реагируют с
сывороткой к ASC1.
Предшественники фибриллярного белка амилоида при различных формах старческого амилоидоза
| Форма заболевания | Предшественник белка фибрилл амилоида |
| Старческий системный амилоидоз | Транстиретин (“депрессивный” сывороточный преальбумин) |
| Изолированный амилоидоз предсердий | Предсердный натрий- уретический фактор |
| Амилоидоз островков поджелудочной железы | Амилин |
| Амилоидоз аорты | Преальбумин |
| Церебральный амилоидоз | b-Протеин |
| Амилоидоз глаза | Псевдоэксфолиативный материал, деградирующие фоторецепторные диски |
| Амилоидоз простаты и семенных пузырьков | ? |
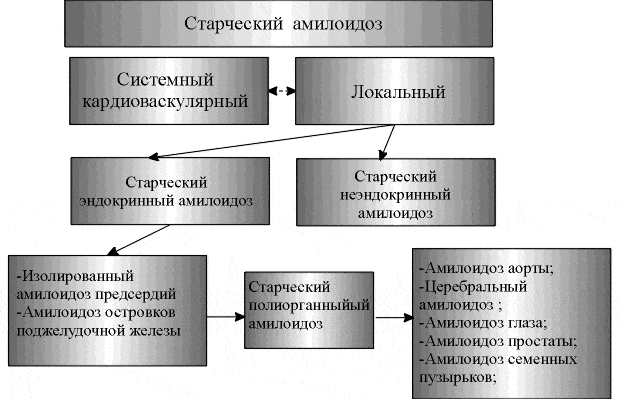
Старческий
локальный амилоидоз, как уже
говорилось, гетерогенен: одну
группу его составляет старческий
эндокринный, другую – старческий
неэндокринный амилоидоз. Помимо
моноорганных проявлений в каждой
из этих групп возможны
полиорганные проявления, что
позволяет говорить о группе
полиорганного старческого
амилоидоза (см. рисунок). Каждая из
этих групп требует, естественно,
отдельного анализа.
Старческий
локальный эндокринный амилоидоз
– наиболее частое проявление
эндокринного амилоидоза, если не
считать амилоидоз опухолей
APUD-системы. Он представлен
изолированным амилоидозом
предсердий и амилоидозом островков
поджелудочной железы.
Изолированный
амилоидоз предсердий (IAA)
составляет почти 1/3 всех случаев
старческого локального амилоидоза
[7]. Предшественником белка фибрилл
амилоида является пептидный гормон
– предсердный натрийуретический
фактор [8]. Строят фибриллы амилоида
предсердные кардиомиоциты с
секреторными гранулами, открытые B.
Kisch [9] еще в 1956 г.
Поражаются оба
предсердия и межпредсердная
перегородка. Важно отметить, что
амилоид при IAA имеет характерные
антигенные и биохимические
свойства: не реагирует с белком ASC1
– предшественником белка фибрилл
– при генерализованном старческом
амилоидозе, не содержит триптофана
[10]. Эти признаки подтверждают
самостоятельность IAA среди
локальных форм амилоидоза.
О причастности
этой формы эндокринного амилоидоза
к старческому свидетельствует
высокая частота встречаемости ее у
пожилых и старых людей. Так, G. Cornwell и
соавт. [10] находили IAA у умерших
после 80 лет в 78 – 95% случаев. По
нашим данным [11], пик встречаемости
IAA приходится на возраст от 70 до 79
лет, причем у женщин его
обнаруживают в 3 раза чаще.
При жизни IAA
практически не диагностируется,
так как в половине случаев он
сочетается с атеросклерозом,
гипертонической болезнью,
ревматизмом и другой патологией, т.
е. представляет собой одно из
проявлений полипатий у старых
людей. Но несомненно, что он повинен
в нарушениях функции прежде всего
возбудимости миокарда
(мерцательная аритмия, предсердные
политопные экстрасистолии),
которые связывают с атеросклерозом
или гипертонической болезнью.
Основная причина смерти при IAA –
сердечная недостаточность.
Амилоидоз
островков поджелудочной железы
(АОПЖ) составляет 1/4 случаев
локального старческого амилоидоза,
т. е. встречается несколько реже,
чем IAA [4, 7]. Бытовавшее до недавнего
времени мнение о том, что
предшественником белка амилоидных
фибрилл являются дериваты
инсулина, в настоящее время
опровергнуто. Установлено, что
предшественник белка фибрилл
амилоида представлен аналогом
нейропептида человека –
кальцитонингенсвязанным пептидом-1
– 2. После того, как было доказано,
что этот пептид обладает
гормональной активностью и
содержится в панкреатических
островках не только при
инсулиннезависимом диабете, но и в
норме, его стали называть амилином
[6, 12, 13]. Иммуногистохимически
амилин обнаруживается в тех же
гранулах b-клеток островков, что и
инсулин [14].
О значении
возраста в развитии АОПЖ
свидетельствует тот факт, что
средний возраст больных этой
формой амилоидоза превышает 70 лет
(вне зависимости от пола), а частота
и степень амилоидоза островков
резко резко возрастают после 80 лет
[7].
Клиника АОПЖ
типична: примерно у 70% больных
развивается инсулиннезависимый
сахарный диабет, причем отмечается
связь тяжести сахарного диабета со
степенью амилоидоза островков [7, 15].
В связи с этим дискуссию о
взаимоотношениях сахарного
диабета с АОПЖ, начатую с первого его описания
еще в 1900 г., можно считать
законченной – речь идет не о
диабетическом амилоидозе
островков, а об амилоидном диабете
[3].
Диагностируется
старческий амилоидный диабет, как и
IAA, к сожалению, постмортально, хотя
достижения современной
медицинской инструментальной
техники позволяют делать это и
прижизненно.
Закономерен
вопрос, почему более половины
случаев старческого локального
амилоидоза представлены
эндокринным амилоидозом, т. е.
связаны с APUD-системой. На наш
взгляд, это объясняется тем, что
диффузная система биогенных
моноаминов, работая там, где
встречаются потоки метаболизма [16],
первая служит гомеостазу и поэтому
первая подвергается разрушению при
нарастающей старческой
брадитрофии. Причем это разрушение
имеет прежде всего
“конформационный характер” (в
основе формирования фибриллярного
белка амилоида лежит b-кросс-конформация).
Старческий
локальный неэндокринный амилоидоз
представлен амилоидозом аорты,
церебральным амилоидозом,
амилоидозом глаза и довольно редко
амилоидозом простаты и/или
семенных пузырьков. Заслуживают
внимания преимущественно первые
три локализации.
Старческий
амилоидоз аорты (САА) составляет не
более 1/5 всех случаев локального
старческого амилоидоза. Его
находят у 95 – 100% умерших старше 80
лет [10]. По нашим данным [17], частота
САА в последнем десятилетии жизни
(80 – 89 лет) возрастает в 5 раз по
сравнению с предпоследним (70 – 79
лет), т. е. подобно взрыву, и это мало
объяснимо.
Предшественником
белка фибрилл амилоида считают
преальбумин (см. таблицу), при
деградации (конформации) которого
на цитолемме гладкомышечных клеток
аорты образуются амилоидные
фибриллы [17, 18]. Поэтому амилоид
локализуется в средней оболочке
аорты, но в субинтимальном ее слое,
что определяет комбинации
(сочетания) амилоидоза и
атеросклероза. Сам амилоид
уникален по антигенным свойствам –
его белки не реагируют с
антисыворотками к белкам фибрилл
амилоида при генерализованных
формах амилоидоза и содержат
триптофан, что позволяет исключить
его из группы эндокринного
амилоидоза [19, 20].
Поражается
преимущественно не брюшной отдел
аорты, как при атеросклерозе, а
грудной, что ставит под сомнение
роль гемодинамического фактора в
амилоидогенезе. Но в подавляющем
большинстве случаев имеется
сочетание амилоидоза и
атеросклероза в одних и тех же
отделах аорты. Причем это сочетание
в разные периоды старости носит
различный характер: до 80 лет –
редкое, от 80 до 89 лет – возможное, но
корреляции отсутствуют, старше 90
лет – частое, причем доминирует
амилоидоз [21]. Сочетание амилоидоза
и атеросклероза аорты в старости не
имеет однозначных
патогенетических оценок и в его
основе лежат биологические, точнее,
геронтологические закономерности
[22]. Не исключено, что атеросклероз
аорты, способствуя конформационным
превращениям плазменных белков,
“прокладывает
дорогу” амилоидозу.
Случаи
прижизненной диагностики САА
неизвестны.
Старческий
церебральный амилоидоз (СЦА)
встречается довольно редко: среди
форм старческого локального
амилоидоза он составляет не более
13% [7]. По мере старения частота СЦА
прогрессивно возрастает: если у
умерших до 80 лет его находят всего в
2,4% случаев, то после 80 лет – в 30 – 65%
[4, 23]. При этом распространенность
амилоидоза в структурах мозга и его
оболочках увеличивается.
Морфологическим
субстратом СЦА являются старческие
(амилоидные) бляшки, конгофильные
нейрофибриллярные сплетения и
амилоид внутримозговых сосудов,
сосудов мозговых оболочек и
сосудистых сплетений. Во всех этих
образованиях фибриллы строятся не
из преальбумина, как раньше считали
[24], а из сывороточного
предшественника b-протеина [3]. Недавно Н.
В. Кудиновой [25] показано, что b-протеин,
ассоциированный с липопротеидами
высокой плотности, циркулирует в
растворимой форме в спинномозговой
жидкости здоровых людей. Это
наблюдение позволяет предположить,
что патогенез церебрального
амилоидоза близок патогенезу
амилоидоза АА, если будет доказано
увеличение продукции b-протеина
в старости.
Образование
основного слагаемого СЦА –
старческой бляшки – связывают с
разными структурами мозга:
нейронами, глиальными клетками,
дендритами, капиллярами головного
мозга [26]. Результаты наших
исследований [4, 7] позволяют
считать, что к построению
старческой бляшки причастен
нейрон, в нем же образуются и
нейрофибриллярные структуры;
фибриллы сосудистого амилоида
формируются на цитолемме
гладкомышечных клеток.
Особого
рассмотрения требуют
взаимоотношения СЦА с пресенильной
(болезнь Альцгеймера) и сенильной
деменцией. Поскольку при этих
сенильных заболеваниях
церебральный амилоидоз находят в
100% случаев [7, 26], его следует считать
морфологическим субстратом этих
заболеваний.
Наши данные [3, 7],
как и данные многих зарубежных
авторов, свидетельствуют о том, что
имеется прямая зависимость
развития пресенильной и сенильной
деменции от степени развития
амилоидоза головного мозга. Причем
при болезни Альцгеймера (средний
возраст 66,6 года) амилоидоз мозга
выражен сильнее, чем при сенильной
деменции (средний возраст 80,3 гoда).
Это касается как количества
амилоидных бляшек,
нейрофибриллярных сплетений,
сохранных нейронов, так и степени
амилоидоза сосудистых структур
мозга.
Важно отметить,
что пресенильная и сенильная
деменция клинически в подавляющем
большинстве случаев протекают под
маской атеросклероза,
постмортальный же диагноз СЦА в
этих случаях возможен в 78,6% [7].
Старческий
амилоидоз глаза (САГ), как
показали исследования последних
лет [27, 28], гетерогенен. Выделяют
амилоидоз с преимущественным
поражением переднего либо заднего
отдела газа, морфогенез которого и
клинические проявления различны.
При изолированном амилоидозе с
преимущественным поражением
переднего отдела глаза, частота
которого возрастает после 70 лет,
амилоид представлен
псевдоэксфолиативным материалом
[27, 29]. Клинически он проявляется
псевдоэксфолиативным синдромом,
катарактой и глаукомой.
При
изолированном амилоидозе с
преимущественным поражением
заднего отдела глаза с пиком
встречаемости на десятом
десятилетии жизни, амилоид
строится, вероятно, из материала
деградирующих фоторецепторных
дисков [28], клиническим же
прявлением этого вида амилоидоза
глаза становится
сенильная макулярная дистрофия.
С большой долей
вероятности можно предположить,
что и при старческом локальном
неэндокринном амилоидозе в основе
формирования фибриллярного белка
амилоида прежде всего нарушения
конформационного характера.
Сывороточные предшественники при
САА (преальбумин) и СЦА
(спинномозговой b-протеин, а, возможно, и
сывороточный преальбумин), как и
белки материала передней
(псевдоэксфолиативный материал) и
задней (материал фоторецепторных
дисков) камер глаза, будучи
естественными составляющими тела,
способны, как это было показано, к b-кросс-конформации.
При старческом амилоидозе
различные белки тела под влиянием
нарастающей брадитрофии
приобретают новое качество,
качество особого фибриллярного
белка, причем в основе этого
процесса лежат рекомбинантные
преобразования на основе
конформации.
Старческий
полиорганный амилоидоз. Наш опыт
[4, 17] свидетельствует о том, что
полная тетрада Шварца практически
не встречается, а в редуцированном
виде ее находят не более чем в 5,5%
вскрытий умерших в старческом
возрасте (средний возраст 72 года).
Чаще всего старческий полиорганный
амилоидоз представлен сочетанием
IAA, САА и АОПЖ или АОПЖ, СЦА и САГ.
Поскольку глаз – это “окно во
внешний мир” зрительного
анализатора головного мозга, при
последнем сочетании САГ можно
рассматривать как проявление СЦА
[30].
Литература:
1. Schwartz Ph. Causes and Manifestation
of Senile Degeneration. Warren, 1970.
2. Серов
В. В. // Арх. патол. – 1989. – Вып. 10. – С.
3 – 11.
3. Серов
В. В. // Клин. геронт. – 1995. – №1. – С. 3
– 8.
4. Серов
В. В., Зыкова Л. Д. // Тер. архив. – 1987.
– №8. – С. 14–20.
5. Glenner G. N Engl J Med 1980;302:1283–92; 1333–42.
6. Westermark P, Pitkanen P, Benson J, et al. Lab Invest
1985;52:314–8.
7.
Зыкова Л. Д. Старческий амилоидоз:
клинико-морфологический аспект
проблемы. – Автореф. дис. докт. мед.
наук. – М. – 1989.
8. Kayl GG, Butler MG, d`Ardenn A, et al. Brit Heart J
1986;56:317–20.
9. Kisch B. Exp med Surg 1956;14:99–112.
10.Cornwell GG, Kyle PA, Westermark P, et al. Am J Med
1983;75(4):618–23.
11. Серов
В. В., Зыкова Л. Д., Виноградова О. М. и
др. // Арх. патол. – 1988. – Вып. 8. – С.
3–12.
12. Cooper G, Willis A, Clarc A. Proc Nat Acad Sci USA
1987;84:8628–32.
13. Westermark P, Wernstedt C, Wilander E, et al. Biochem
Biophys Res Commun 1986;140:837–41.
14. Cooper G, Gay A, Willis A, et al. Biochem Biophys Acta
1989;1014;247-58.
15. Howard C. Diabetologia 1986;29:301–6.
16.
Райхлин Н. Т., Кветной И. М., Осадчук
М. А. APUD-система (общепатологические
и онкологические аспекты) – часть I
и II – Обнинск, 1993.
17.
Зыкова Л. Д., Серов В. В., Секамова С.
М. // Сов. мед. – 1989. – №9. – С. 74–8.
18. Storkel S, Bohl J, Schneider H.–M. Virch Arch Pathol
Anat 1983;44:145–61.
19. Breathnach SM, Melrose SM, Bhoga CB, et al. Nature
1981;293:652–4.
20. Cornwell GG, Westermark P, Murdoch W, et al. Amer J
Path 1982;108:135–9.
21. Vincent J, Choinet C, Durand M, et al. Ann Invest Med
1982;133:160–3.
22.
Давыдовский И. В. Геронтология. – М.,
1966.
23. Divry P. J Neurol Psychiatr 1927;27:643–57.
24.Shirachama T, Skinner M, Westermasrk P, et al. Am J Path
1982;107:41–50.
25.
Кудинова Н. В. Амилоид бета и
липидный метаболизм. Автореф. дисс.
канд. мед. наук. – М., 1996.
26. Ойфа
А. И. Церебральный амилоидоз при
сенильных заболеваниях. Автореф.
дисс. докт. мед. наук. – М., 1983.
27.
Ермилов В. В. // Арх. патол. – 1993. –
Вып. 6. – С. 43–5.
28.
Ермилов В. В., Серов В. В. // Арх. патол.
– 1994. – Вып. 4. – С. 10–4.
29. Ringvold A, Husy G. Ex Eye Res 1973;17:284–99.
30. Ермилов
В. В. // Арх. патол. – 1993. – Вып. 6. – С.
39–42.








