–Т —А—П–і–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –ї–Є–њ–Є–і—Б–љ–Є–ґ–∞—О—Й–Є–µ —Б—А–µ–і—Б—В–≤–∞ (–Ы–°–°) –Љ–Њ–≥—Г—В —Г–Љ–µ–љ—М—И–∞—В—М –Њ—В–і–∞–ї–µ–љ–љ—Г—О –ї–µ—В–∞–ї—М–љ–Њ—Б—В—М —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б–Њ —Б—В–∞–±–Є–ї—М–љ–Њ–є –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–є –±–Њ–ї–µ–Ј–љ—М—О —Б–µ—А–і—Ж–∞ (–Ъ–С–°) [1-3] –Є–ї–Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є —А–Є—Б–Ї–∞ [4,5]. –Э–Њ –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –Є–Ј —Н—В–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –Є—Б–Ї–ї—О—З–∞–ї–Є –±–Њ–ї—М–љ—Л—Е —Б –Њ—Б—В—А—Л–Љ –Ї–Њ—А–Њ–љ–∞—А–љ—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ (–Ю–Ъ–°) –≤ —В–µ—З–µ–љ–Є–µ 3-6 –Љ–µ—Б—П—Ж–µ–≤ –і–Њ –≤–Ї–ї—О—З–µ–љ–Є—П –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, —В–Њ –Њ—Б—В–∞–µ—В—Б—П –љ–µ —П—Б–љ—Л–Љ, –і–∞–µ—В –ї–Є –ї–Є–њ–Є–і—Б–љ–Є–ґ–∞—О—Й–∞—П —В–µ—А–∞–њ–Є—П (–Ы–°–Ґ) –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Г—О –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О –≤—Л–≥–Њ–і—Г, –µ—Б–ї–Є –Њ–љ–∞ –љ–∞—З–∞—В–∞ —Б—А–∞–Ј—Г –њ–Њ—Б–ї–µ —Н–њ–Є–Ј–Њ–і–∞ –љ–µ—Б—В–∞–±–Є–ї—М–љ–Њ–є –Ъ–С–°. –І–∞—Б—В–Њ—В–∞ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є (—Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Б–Њ–±—Л—В–Є–є) –њ–Њ—Б–ї–µ –Њ—Б—В—А–Њ–≥–Њ –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –≤—Л—И–µ, —З–µ–Љ –њ—А–Є —Б—В–∞–±–Є–ї—М–љ–Њ–є –Ъ–С–°; –њ–Њ—Н—В–Њ–Љ—Г –µ—Б–ї–Є –ї–Є–њ–Є–і—Б–љ–Є–ґ–∞—О—Й–∞—П —В–µ—А–∞–њ–Є—П –Њ–Ї–∞–Ј–∞–ї–∞—Б—М –±—Л —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є –≤ –Њ—Б—В—А–Њ–є —Б–Є—В—Г–∞—Ж–Є–Є, –Њ–љ–∞ –Љ–Њ–≥–ї–∞ –±—Л –њ—А–µ–і–Њ—В–≤—А–∞—В–Є—В—М –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–µ —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л–µ —Б–Њ–±—Л—В–Є—П.
–Э—Л–љ–µ—И–љ–Є–µ —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–∞ –Р–Љ–µ—А–Є–Ї–∞–љ—Б–Ї–Њ–≥–Њ –Ї–Њ–ї–ї–µ–і–ґ–∞ –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Є–Є –Є –Р–Љ–µ—А–Є–Ї–∞–љ—Б–Ї–Њ–є –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є –њ–Њ –≤–µ–і–µ–љ–Є—О –Њ—Б—В—А—Л—Е –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е —Б–Є–љ–і—А–Њ–Љ–Њ–≤ —Г–Ї–∞–Ј—Л–≤–∞—О—В, —З—В–Њ –њ–Њ–Ї–∞ –Љ–∞–ї–Њ –∞—А–≥—Г–Љ–µ–љ—В–Њ–≤ –≤ –њ–Њ–ї—М–Ј—Г —А–∞–љ–љ–µ–≥–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Ы–°–Ґ, –Є —А–µ–Ї–Њ–Љ–µ–љ–і—Г—О—В –љ–∞—З–Є–љ–∞—В—М —Б –і–Є–µ—В–Њ—В–µ—А–∞–њ–Є–Є [6,7]. –Я–Њ—Б–Ї–Њ–ї—М–Ї—Г –ї–Є–њ–Є–і—Б–љ–Є–ґ–∞—О—Й–Є–µ —Б—А–µ–і—Б—В–≤–∞ –Љ–Њ–≥—Г—В –≤ –Њ—Б—В—А–Њ–Љ –Њ–њ—Л—В–µ —Г–ї—Г—З—И–∞—В—М —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ—Г—О —Д—Г–љ–Ї—Ж–Є—О [8,9], —Г–Љ–µ–љ—М—И–∞—В—М –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ [10,11] –Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ [12,13], —В–Њ –Є—Е –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –≤—Б–Ї–Њ—А–µ –њ–Њ—Б–ї–µ –љ–∞—З–∞–ї–∞ –Њ—Б—В—А–Њ–≥–Њ –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –Љ–Њ–≥–ї–Њ –±—Л —Г–Љ–µ–љ—М—И–Є—В—М —А–∞–љ–љ—О—О –ї–µ—В–∞–ї—М–љ–Њ—Б—В—М.
H.D. Aronow, E.J. Topol, M.T. Roe et al. –≤ –Њ–±—Б–µ—А–≤–∞—Ж–Є–Њ–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є [14], –Њ –Ї–Њ—В–Њ—А–Њ–Љ —А–µ—З—М –њ–Њ–є–і–µ—В –љ–Є–ґ–µ, —Б—В—А–µ–Љ–Є–ї–Є—Б—М –≤—Л—П—Б–љ–Є—В—М, –±—Л–ї–Њ –ї–Є –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –ї–Є–њ–Є–і—Б–љ–Є–ґ–∞—О—Й–Є—Е —Б—А–µ–і—Б—В–≤ –њ—А–Є –≤—Л–њ–Є—Б–Ї–µ –Є–Ј —Б—В–∞—Ж–Є–Њ–љ–∞—А–∞ —Б–Њ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —А–∞–љ–љ–µ–є –ї–µ—В–∞–ї—М–љ–Њ—Б—В–Є —Б—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –≤–Ї–ї—О—З–µ–љ–љ—Л—Е –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П GUSTO IIb [15] –Є PURSUIT [16]. –Т —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П GUSTO IIb (Global Use of Streptokinase or t-PA for Occluded Coronary Arteries - –У–ї–Њ–±–∞–ї—М–љ–Њ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ —Б—В—А–µ–њ—В–Њ–Ї–Є–љ–∞–Ј—Л –Є–ї–Є —В–Ї–∞–љ–µ–≤–Њ–≥–Њ –∞–Ї—В–Є–≤–∞—В–Њ—А–∞ –њ–ї–∞–Ј–Љ–Є–љ–Њ–≥–µ–љ–∞ –њ—А–Є –Њ–Ї–Ї–ї—О–Ј–Є–Є –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е –∞—А—В–µ—А–Є–є) –Є PURSUIT (Platelet Glycoprotein IIb/IIIa in Unstable Angina: Receptor Suppression Using Integrilin Therapy - –Ґ—А–Њ–Љ–±–Њ—Ж–Є—В–∞—А–љ—Л–є –≥–ї–Є–Ї–Њ–њ—А–Њ—В–µ–Є–і IIb/IIIa –њ—А–Є –љ–µ—Б—В–∞–±–Є–ї—М–љ–Њ–є —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є: –њ–Њ–і–∞–≤–ї–µ–љ–Є–µ —А–µ—Ж–µ–њ—В–Њ—А–∞ —Б –њ–Њ–Љ–Њ—Й—М—О —В–µ—А–∞–њ–Є–Є –Є–љ—В–µ–≥—А–Є–ї–Є–љ–Њ–Љ) –≤–Ї–ї—О—З–∞–ї–Є—Б—М –њ–∞—Ж–Є–µ–љ—В—Л —Б –Њ—Б—В—А—Л–Љ–Є –Ї–Њ—А–Њ–љ–∞—А–љ—Л–Љ–Є —Б–Є–љ–і—А–Њ–Љ–∞–Љ–Є. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ GUSTO IIb –≤–Ї–ї—О—З–∞–ї–Є—Б—М –њ–∞—Ж–Є–µ–љ—В—Л —Б —Н–ї–µ–≤–∞—Ж–Є–µ–є –Є –±–µ–Ј —Н–ї–µ–≤–∞—Ж–Є–Є ST-—Б–µ–≥–Љ–µ–љ—В–∞ –љ–∞ —Н–ї–µ–Ї—В—А–Њ–Ї–∞—А–і–Є–Њ–≥—А–∞–Љ–Љ–µ (–≠–Ъ–У), –∞ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ PURSUIT - —В–Њ–ї—М–Ї–Њ —Б –Ю–Ъ–° –±–µ–Ј —Н–ї–µ–≤–∞—Ж–Є–Є ST-—Б–µ–≥–Љ–µ–љ—В–∞.
–Ь–µ—В–Њ–і—Л
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ GUSTO IIb –≤–Ї–ї—О—З–∞–ї–Є—Б—М –њ–∞—Ж–Є–µ–љ—В—Л —Б –і–Є—Б–Ї–Њ–Љ—Д–Њ—А—В–Њ–Љ –≤ –≥—А—Г–і–Є –Є –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–Љ–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ–Є –љ–∞ –≠–Ъ–У –і–∞–≤–љ–Њ—Б—В—М—О –і–Њ 12 —З–∞—Б–Њ–≤. –Р–љ–∞–ї–Њ–≥–Є—З–љ–Њ, –Ї—А–Є—В–µ—А–Є–µ–Љ –≤–Ї–ї—О—З–µ–љ–Є—П –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ PURSUIT –±—Л–ї–Њ –љ–∞–ї–Є—З–Є–µ —Н–њ–Є–Ј–Њ–і–∞ –±–Њ–ї–Є –≤ –≥—А—Г–і–Є –і–∞–≤–љ–Њ—Б—В—М—О –і–Њ 24 —З–∞—Б–Њ–≤ –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–Љ–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ–Є –љ–∞ –≠–Ъ–У –≤ —В–µ—З–µ–љ–Є–µ 12 —З–∞—Б–Њ–≤ –і–Њ –Є–ї–Є 12 —З–∞—Б–Њ–≤ –њ–Њ—Б–ї–µ –њ–Њ—П–≤–ї–µ–љ–Є—П –±–Њ–ї–µ–є, –Є–ї–Є —Б —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –Ї—А–µ–∞—В–Є–љ—Д–Њ—Б—Д–Њ–Ї–Є–љ–∞–Ј—Л –Ь–Т –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –≤—Л—И–µ –≤–µ—А—Е–љ–µ–є –≥—А–∞–љ–Є—Ж—Л –љ–Њ—А–Љ—Л. –Т –∞–љ–∞–ї–Є–Ј –≤–Ї–ї—О—З–∞–ї–Є —В–Њ–ї—М–Ї–Њ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –≤—Л–ґ–Є–≤—И–Є—Е –і–Њ –≤—Л–њ–Є—Б–Ї–Є –Є–Ј —Б—В–∞—Ж–Є–Њ–љ–∞—А–∞. –Т —Ж–µ–ї–Њ–Љ 68% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є–Љ–µ–ї–Є –Є–љ—Д–∞—А–Ї—В –Љ–Є–Њ–Ї–∞—А–і–∞ (–Ш–Ь) –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ –Є–ї–Є –њ—А–Є –≤–Ї–ї—О—З–µ–љ–Є–Є –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ.
–Ы–µ—З–µ–љ–Є–µ
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є GUSTO IIb –њ–∞—Ж–Є–µ–љ—В–∞–Љ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ –љ–∞–Ј–љ–∞—З–∞–ї–Є –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ –±–Њ–ї—О—Б–љ–Њ –Є –Є–љ—Д—Г–Ј–Є–Њ–љ–љ–Њ –љ–µ—Д—А–∞–Ї—Ж–Є–Њ–љ–Є—А–Њ–≤–∞–љ–љ—Л–є –≥–µ–њ–∞—А–Є–љ –Є–ї–Є —А–µ–Ї–Њ–Љ–±–Є–љ–∞–љ—В–љ—Л–є –≥–Є—А—Г–і–Є–љ –≤ —В–µ—З–µ–љ–Є–µ 3-5 –і–љ–µ–є. –†–µ—И–µ–љ–Є–µ –Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є —В—А–Њ–Љ–±–Њ–ї–Є—В–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є (–Є–ї–Є —Б—В—А–µ–њ—В–Њ–Ї–Є–љ–∞–Ј–Њ–є, –Є–ї–Є —В–Ї–∞–љ–µ–≤—Л–Љ –∞–Ї—В–Є–≤–∞—В–Њ—А–Њ–Љ –њ–ї–∞–Ј–Љ–Є–љ–Њ–≥–µ–љ–∞) –њ—А–Є –Ш–Ь —Б —Н–ї–µ–≤–∞—Ж–Є–µ–є ST-—Б–µ–≥–Љ–µ–љ—В–∞ –њ—А–Є–љ–Є–Љ–∞–ї –ї–µ—З–∞—Й–Є–є –≤—А–∞—З. –Ы–µ—З–µ–љ–Є–µ –≥–Є—А—Г–і–Є–љ–Њ–Љ –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–ї–Њ—Б—М —Б–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–Љ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ–Љ —З–∞—Б—В–Њ—В—Л –љ–µ—Д–∞—В–∞–ї—М–љ–Њ–≥–Њ –Ш–Ь –Ї 30-–Љ—Г –і–љ—О, –Є –ї–Є—И—М —Б —В–µ–љ–і–µ–љ—Ж–Є–µ–є –Ї —Г–Љ–µ–љ—М—И–µ–љ–Є—О —З–∞—Б—В–Њ—В—Л –њ–µ—А–≤–Є—З–љ–Њ–є –Ї–Њ–љ–µ—З–љ–Њ–є —В–Њ—З–Ї–Є (–љ–µ—Д–∞—В–∞–ї—М–љ–Њ–≥–Њ –Ш–Ь –Є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є).
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є PURSUIT –њ–∞—Ж–Є–µ–љ—В–∞–Љ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ –љ–∞–Ј–љ–∞—З–∞–ї–Є –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ –±–Њ–ї—О—Б–љ–Њ –Є –Є–љ—Д—Г–Ј–Є–Њ–љ–љ–Њ —Н–њ—В–Є—Д–Є–±–∞—В–Є–і –Є–ї–Є –њ–ї–∞—Ж–µ–±–Њ –і–Њ –≤—Л–њ–Є—Б–Ї–Є, –љ–Њ –љ–µ –і–Њ–ї—М—И–µ 3 –і–љ–µ–є. –≠–њ—В–Є—Д–Є–±–∞—В–Є–і –њ—А–Є–≤–µ–ї –Ї –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ—Г —Б–љ–Є–ґ–µ–љ–Є—О —З–∞—Б—В–Њ—В—Л –љ–µ—Д–∞—В–∞–ї—М–љ–Њ–≥–Њ –Ш–Ь –Є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –Ї 30-–Љ—Г –і–љ—О.
–Т –Њ–±–Њ–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –Њ—Б—В–∞–ї—М–љ—Л–µ –ї–µ–Ї–∞—А—Б—В–≤–∞ –љ–∞–Ј–љ–∞—З–∞–ї –ї–µ—З–∞—Й–Є–є –≤—А–∞—З. –Т —З–∞—Б—В–љ–Њ—Б—В–Є, –њ—А–∞–≤–Є–ї–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –љ–µ —А–µ–≥–ї–∞–Љ–µ–љ—В–Є—А–Њ–≤–∞–ї–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –ї–Є–њ–Є–і—Б–љ–Є–ґ–∞—О—Й–µ–є —В–µ—А–∞–њ–Є–Є. H.D. Aronow et al. –∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–ї–Є —В–µ—А–∞–њ–Є—О –њ—А–Є –≤—Л–њ–Є—Б–Ї–µ, –Њ–і–љ–∞–Ї–Њ –і–∞–љ–љ—Л–µ –Њ –Ї–Њ–љ–Ї—А–µ—В–љ—Л—Е –Ї–ї–∞—Б—Б–∞—Е –љ–∞–Ј–љ–∞—З–µ–љ–љ—Л—Е –Ы–°–° –љ–µ –±—Л–ї–Є –і–Њ—Б—В—Г–њ–љ—Л. –Я–µ—А–≤–Є—З–љ–Њ–є –Ї–Њ–љ–µ—З–љ–Њ–є —В–Њ—З–Ї–Њ–є —Н—В–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –±—Л–ї–∞ 6-–Љ–µ—Б—П—З–љ–∞—П –ї–µ—В–∞–ї—М–љ–Њ—Б—В—М –Њ—В –≤—Б–µ—Е –њ—А–Є—З–Є–љ, –Ї–∞–Ї –љ–∞–Є–±–Њ–ї–µ–µ –Њ–±—К–µ–Ї—В–Є–≤–љ—Л–є –Ї—А–Є—В–µ—А–Є–є –Њ—Ж–µ–љ–Ї–Є [17]. –Т—В–Њ—А–Є—З–љ—Л–µ –Ї–Њ–љ–µ—З–љ—Л–µ —В–Њ—З–Ї–Є –≤–Ї–ї—О—З–∞–ї–Є 30-–і–љ–µ–≤–љ—Г—О –ї–µ—В–∞–ї—М–љ–Њ—Б—В—М –Њ—В –≤—Б–µ—Е –њ—А–Є—З–Є–љ, –Є —Б–Њ–≤–Њ–Ї—Г–њ–љ–Њ—Б—В—М –ї–µ—В–∞–ї—М–љ–Њ—Б—В–Є –Є –љ–µ—Д–∞—В–∞–ї—М–љ–Њ–≥–Њ –Є–љ—Д–∞—А–Ї—В–∞ –Ј–∞ 6 –Љ–µ—Б—П—Ж–µ–≤. –С—Л–ї–Њ –Њ—В—Б–ї–µ–ґ–µ–љ–Њ 99,9% –±–Њ–ї—М–љ—Л—Е.
–°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј
–Ф–ї—П —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є—Б—М –Љ–µ—В–Њ–і—Л –Ь–∞–љ–љ–∞-–£–Є—В–љ–Є, —В–Њ—З–љ—Л–є —В–µ—Б—В –§–Є—И–µ—А–∞, –Ї—А–Є—В–µ—А–Є–є c2 –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –Є—Е –њ—А–Є–Љ–µ–љ–Є–Љ–Њ—Б—В—М—О. –Ф–ї—П –Њ—Ж–µ–љ–Ї–Є –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є –∞–љ–∞–ї–Є–Ј –Ъ–∞–њ–ї–∞–љ–∞-–Ь–µ–є–µ—А–∞ –Є –Љ–µ—В–Њ–і –Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є—П —А–Є—Б–Ї–Њ–≤ –Ъ–Њ–Ї—Б–∞. –Я–Њ—Б–Ї–Њ–ї—М–Ї—Г –њ–∞—Ж–Є–µ–љ—В—Л –±—Л–ї–Є –њ—А–Њ—Б–ї–µ–ґ–µ–љ—Л –≤ —В–µ—З–µ–љ–Є–µ –љ–µ—А–∞–≤–љ—Л—Е –њ–µ—А–Є–Њ–і–Њ–≤, –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–µ —А–Є—Б–Ї–Є –±—Л–ї–Є –Њ—Ж–µ–љ–µ–љ—Л –Є –≤—Л—А–∞–ґ–µ–љ—Л —Б 95% –і–Њ–≤–µ—А–Є—В–µ–ї—М–љ—Л–Љ–Є –Є–љ—В–µ—А–≤–∞–ї–∞–Љ–Є (–Ф–Ш 95%). –Ф–ї—П –∞–љ–∞–ї–Є–Ј–∞ –њ–Њ –њ–Њ–і–≥—А—Г–њ–њ–∞–Љ –±–Њ–ї—М–љ—Л—Е —А–∞–Ј–і–µ–ї–Є–ї–Є –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –≤–Њ–Ј—А–∞—Б—В–∞, –њ–Њ–ї–∞, –≥–Є–њ–µ—А–ї–Є–њ–Є–і–µ–Љ–Є–Є, –љ–∞–ї–Є—З–Є—П —Б–∞—Е–∞—А–љ–Њ–≥–Њ –і–Є–∞–±–µ—В–∞, –Ї—Г—А–µ–љ–Є—П, —В–Є–њ–∞ –Њ—Б—В—А–Њ–≥–Њ –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, –љ–∞–ї–Є—З–Є—П –ї—О–±–Њ–≥–Њ –Ш–Ь (–≤ –∞–љ–∞–Љ–љ–µ–Ј–µ –Є–ї–Є –њ—А–Є –≤–Ї–ї—О—З–µ–љ–Є–Є –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ), –Њ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –ї–Є–њ–Є–і—Б–љ–Є–ґ–∞—О—Й–Є—Е —Б—А–µ–і—Б—В–≤ –і–Њ –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є—П, –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–є —З—А–µ—Б–Ї–Њ–ґ–љ–Њ–є –Є–ї–Є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–є –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–є —А–µ–≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є–Є, –Њ–±–ї–∞—Б—В–Є –њ—А–Њ–ґ–Є–≤–∞–љ–Є—П –Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П.
–Т –Њ—В–ї–Є—З–Є–µ –Њ—В —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –≤ –Ї–Њ—В–Њ—А—Л—Е –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Њ–і–љ–Њ–≥–Њ –Є–Ј –і–≤—Г—Е –≤–Є–і–Њ–≤ –ї–µ—З–µ–љ–Є—П –љ–µ –Ј–∞–≤–Є—Б–Є—В –Њ—В –Ї–∞–Ї–Є—Е-–ї–Є–±–Њ —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤, –љ–∞ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ —В–µ—А–∞–њ–Є–Є –≤ –Њ–±—Б–µ—А–≤–∞—Ж–Є–Њ–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Њ–±—Л—З–љ–Њ –≤–ї–Є—П—О—В –≤–љ–µ—И–љ–Є–µ —Д–∞–Ї—В–Њ—А—Л. –І—В–Њ–±—Л –Љ–Є–љ–Є–Љ–Є–Ј–Є—А–Њ–≤–∞—В—М –њ–Њ–≥—А–µ—И–љ–Њ—Б—В–Є, —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б –≤–ї–Є—П–љ–Є–µ–Љ –њ—А–Є–≤—Е–Њ–і—П—Й–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤ –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –Ы–°–Ґ –њ—А–Є –≤—Л–њ–Є—Б–Ї–µ, –њ–µ—А–µ–і —Б—В–∞–љ–і–∞—А—В–љ–Њ–є –Љ–љ–Њ–≥–Њ—Д–∞–Ї—В–Њ—А–љ–Њ–є —А–µ–≥—А–µ—Б—Б–Є–µ–є –±—Л–ї –њ—А–Њ–≤–µ–і–µ–љ –∞–љ–∞–ї–Є–Ј –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ—Б—В–Є [18]. –Р–љ–∞–ї–Є–Ј –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ—Б—В–Є [19] –Є–і–µ–љ—В–Є—Д–Є—Ж–Є—А—Г–µ—В –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —Б—Е–Њ–ґ–Є—Е –і—А—Г–≥ —Б –і—А—Г–≥–Њ–Љ –њ–Њ –≤—Б–µ–Љ –њ–∞—А–∞–Љ–µ—В—А–∞–Љ, –Ї—А–Њ–Љ–µ –љ–∞–Ј–љ–∞—З–µ–љ–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П, –Є —В–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ –Є–Љ–Є—В–Є—А—Г–µ—В —Г—Б–ї–Њ–≤–Є—П —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є. –°–љ–∞—З–∞–ї–∞ –±—Л–ї–∞ —А–∞–Ј—А–∞–±–Њ—В–∞–љ–∞ –Љ–љ–Њ–≥–Њ—Д–∞–Ї—В–Њ—А–љ–∞—П –ї–Њ–≥–Є—Б—В–Є—З–µ—Б–Ї–∞—П –Љ–Њ–і–µ–ї—М —А–µ–≥—А–µ—Б—Б–Є–Є –і–ї—П –Њ—Ж–µ–љ–Ї–Є –≤–µ—А–Њ—П—В–љ–Њ—Б—В–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В—Г –њ—А–Є –≤—Л–њ–Є—Б–Ї–µ –Ы–°–Ґ. –≠—В–∞ –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М –љ–∞–Ј—Л–≤–∞–µ—В—Б—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–Љ –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ—Б—В–Є. –Ф–µ–Љ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є–µ –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ–µ—А–µ–Љ–µ–љ–љ—Л–µ –Љ–Њ–і–µ–ї–Є —А–µ–≥—А–µ—Б—Б–Є–Є –≤–Ї–ї—О—З–∞–ї–Є: –≤–Њ–Ј—А–∞—Б—В, –њ–Њ–ї, –≤–µ—Б, —А–Њ—Б—В, —А–∞—Б—Г, –≥–Є–њ–µ—А—В–Њ–љ–Є—О, –і–Є–∞–±–µ—В, –≥–Є–њ–µ—А–ї–Є–њ–Є–і–µ–Љ–Є—О, –њ–Њ—А–∞–ґ–µ–љ–Є–µ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –∞—А—В–µ—А–Є–є, –Ї—Г—А–µ–љ–Є–µ, —Б–µ–Љ–µ–є–љ—Л–є –∞–љ–∞–Љ–љ–µ–Ј –Ъ–С–°, –Ї–ї–∞—Б—Б —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є; –љ–∞–ї–Є—З–Є–µ –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ –Ј–∞—Б—В–Њ–є–љ–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є, –Ш–Ь, —З—А–µ—Б–Ї–Њ–ґ–љ–Њ–є –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–є –∞–љ–≥–Є–Њ–њ–ї–∞—Б—В–Є–Ї–Є (–І–Ъ–Р), –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–≥–Њ —И—Г–љ—В–Є—А–Њ–≤–∞–љ–Є—П (–Ъ–®), –Є–љ—Б—Г–ї—М—В–∞ –Є–ї–Є —В—А–∞–љ–Ј–Є—В–Њ—А–љ–Њ–є –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–є –∞—В–∞–Ї–Є. –Ф–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ —Г—З–Є—В—Л–≤–∞–ї–Є—Б—М —З–∞—Б—В–Њ—В–∞ —Б–µ—А–і–µ—З–љ—Л—Е —Б–Њ–Ї—А–∞—Й–µ–љ–Є–є, —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–µ –Є –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–µ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–µ –і–∞–≤–ї–µ–љ–Є–µ (–Р–Ф), —В–Є–њ –Њ—Б—В—А–Њ–≥–Њ –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –њ—А–Є –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–Є (–љ–µ—Б—В–∞–±–Є–ї—М–љ–∞—П —Б—В–µ–љ–Њ–Ї–∞—А–і–Є—П, –Є–љ—Д–∞—А–Ї—В –Љ–Є–Њ–Ї–∞—А–і–∞ —Б —Н–ї–µ–≤–∞—Ж–Є–µ–є ST-—Б–µ–≥–Љ–µ–љ—В–∞ –Є–ї–Є –Є–љ—Д–∞—А–Ї—В –Љ–Є–Њ–Ї–∞—А–і–∞ –±–µ–Ј —Н–ї–µ–≤–∞—Ж–Є–Є ST-—Б–µ–≥–Љ–µ–љ—В–∞), –≥–µ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–∞—П –Њ–±–ї–∞—Б—В—М –Є –і–∞—В–∞ –≤–Ї–ї—О—З–µ–љ–Є—П. –Э–∞–Ї–Њ–љ–µ—Ж, —Г—З–Є—В—Л–≤–∞–ї–Є—Б—М –њ—А–Є–µ–Љ –ї–µ–Ї–∞—А—Б—В–≤ –і–Њ –Є–ї–Є –њ—А–Є –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–Є –Є –њ—А–Є –≤—Л–њ–Є—Б–Ї–µ (–ї–Є–њ–Є–і—Б–љ–Є–ґ–∞—О—Й–Є–µ —Б—А–µ–і—Б—В–≤–∞, b-–±–ї–Њ–Ї–∞—В–Њ—А—Л, –Є–љ–≥–Є–±–Є—В–Њ—А—Л –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–њ—А–µ–≤—А–∞—Й–∞—О—Й–µ–≥–Њ —Д–µ—А–Љ–µ–љ—В–∞ (–Р–Я–§) –Є–ї–Є –±–ї–Њ–Ї–∞—В–Њ—А—Л –Ї–∞–ї—М—Ж–Є–µ–≤—Л—Е –Ї–∞–љ–∞–ї–Њ–≤), –њ—А–Њ–≤–µ–і–µ–љ–љ—Л–µ –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ –І–Ъ–Р –Є–ї–Є –Ъ–®, –љ–∞–Ј–љ–∞—З–µ–љ–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ (–≥–µ–њ–∞—А–Є–љ –љ–∞—В—А–Є—П, –≥–Є—А—Г–і–Є–љ, —Н–њ—В–Є—Д–Є–±–∞—В–Є–і –Є–ї–Є –њ–ї–∞—Ж–µ–±–Њ) –Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ.
–Я–Њ–њ—Г–ї—П—Ж–Є—П –±—Л–ї–∞ —А–∞–Ј–і–µ–ї–µ–љ–∞ –љ–∞ –і–µ—Ж–Є–ї–Є (10-–њ—А–Њ—Ж–µ–љ—В–љ—Л–µ –Є–љ—В–µ—А–≤–∞–ї—Л) –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–Љ –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ—Б—В–Є. –Т –Ї–∞–ґ–і–Њ–Љ –і–µ—Ж–Є–ї–µ –њ–∞—Ж–Є–µ–љ—В—Л –±—Л–ї–Є —А–∞–Ј–і–µ–ї–µ–љ—Л –љ–∞ —В–µ—Е, –Ї–Њ–Љ—Г –љ–∞–Ј–љ–∞—З–Є–ї–Є –њ—А–Є –≤—Л–њ–Є—Б–Ї–µ –ї–Є–њ–Є–і—Б–љ–Є–ґ–∞—О—Й–Є–µ —Б—А–µ–і—Б—В–≤–∞ –Є —В–µ—Е, –Ї–Њ–Љ—Г –Ы–°–° –љ–µ –љ–∞–Ј–љ–∞—З–Є–ї–Є. –°—А–∞–≤–љ–µ–љ–Є–µ —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї –њ—А–Њ–≤–Њ–і–Є–ї–Є –≤ –Ї–∞–ґ–і–Њ–Љ –і–µ—Ж–Є–ї–µ [20,21]. –Ф–µ—Ж–Є–ї–Є, –≤ –Ї–Њ—В–Њ—А—Л—Е –і–µ–Љ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є–µ, –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є –Є –ї–µ—З–µ–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–ї–Њ—Е–Њ —Б–Њ–≥–ї–∞—Б–Њ–≤–∞–ї–Є—Б—М, –±—Л–ї–Є –Є—Б–Ї–ї—О—З–µ–љ—Л –Є–Ј –Ј–∞–Ї–ї—О—З–Є—В–µ–ї—М–љ–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞.
–†–µ–Ј—Г–ї—М—В–∞—В—Л
–Ш–Ј 20809 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 20 –і–Њ 96 –ї–µ—В (–Љ–µ–і–Є–∞–љ–∞ 64 –≥–Њ–і–∞; –Љ—Г–ґ—З–Є–љ 68%) –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е GUSTO IIb –Є PURSUIT, 3653 –±–Њ–ї—М–љ—Л–Љ (18%) –±—Л–ї–Є –љ–∞–Ј–љ–∞—З–µ–љ—Л –њ—А–Є –≤—Л–њ–Є—Б–Ї–µ –ї–Є–њ–Є–і—Б–љ–Є–ґ–∞—О—Й–Є–µ —Б—А–µ–і—Б—В–≤–∞. –Ш–Љ–µ–ї–Є—Б—М –љ–µ–Ї–Њ—В–Њ—А—Л–µ —А–∞–Ј–ї–Є—З–Є—П –≤ –Є—Б—Е–Њ–і–љ—Л—Е —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–∞—Е –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є (—Б –љ–∞–Ј–љ–∞—З–µ–љ–љ–Њ–є –Ы–°–Ґ –Є –±–µ–Ј –Ы–°–Ґ). –Т –≥—А—Г–њ–њ–µ –Ы–°–Ґ –Є–Љ–µ–ї—Б—П –±–Њ–ї—М—И–Є–є –њ—А–Њ—Ж–µ–љ—В –ґ–µ–љ—Й–Є–љ, —Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В –±—Л–ї –Љ–µ–љ—М—И–µ, –Њ—В–Љ–µ—З–∞–ї–∞—Б—М –≤—Л—Б–Њ–Ї–∞—П —З–∞—Б—В–Њ—В–∞ –Њ–ґ–Є—А–µ–љ–Є—П, –≥–Є–њ–µ—А—В–Њ–љ–Є–Є, –і–Є–∞–±–µ—В–∞, –≥–Є–њ–µ—А–ї–Є–њ–Є–і–µ–Љ–Є–Є, –њ–Њ—А–∞–ґ–µ–љ–Є—П –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –∞—А—В–µ—А–Є–є –Ш–Ь, —З—А–µ—Б–Ї–Њ–ґ–љ–Њ–є –Є–ї–Є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–є –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–є —А–µ–≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є–Є –Є —В—П–ґ–µ–ї–Њ–є —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ. –Ґ–∞–Ї–ґ–µ –≤ —Н—В–Њ–є –≥—А—Г–њ–њ–µ —З–∞—Й–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є—Б—М –Ы–°–° –і–Њ –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є—П, –Є —Н—В–Є–Љ –њ–∞—Ж–Є–µ–љ—В–∞–Љ —З–∞—Й–µ –љ–∞–Ј–љ–∞—З–∞–ї–Є –њ–Њ—Б–ї–µ –≤—Л–њ–Є—Б–Ї–Є, –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –Є b-–±–ї–Њ–Ї–∞—В–Њ—А—Л.
–Ы–°–° –Є —А–∞–љ–љ—П—П –ї–µ—В–∞–ї—М–љ–Њ—Б—В—М
–Т —В–µ—З–µ–љ–Є–µ 6 –Љ–µ—Б—П—Ж–µ–≤ –љ–∞–±–ї—О–і–µ–љ–Є—П –њ—А–Њ–Є–Ј–Њ—И–ї–Њ 668 —Б–ї—Г—З–∞–µ–≤ –ї–µ—В–∞–ї—М–љ–Њ–≥–Њ –Є—Б—Е–Њ–і–∞. –Р–љ–∞–ї–Є–Ј –Ъ–∞–њ–ї–∞–љ–∞-–Ь–µ–є–µ—А–∞ –њ–Њ–Ї–∞–Ј–∞–ї –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ –Є —А–∞–љ–љ–µ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В–Є, —Б–≤—П–Ј–∞–љ–љ–Њ–µ —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –ї–Є–њ–Є–і—Б–љ–Є–ґ–∞—О—Й–Є—Е —Б—А–µ–і—Б—В–≤ –њ–Њ—Б–ї–µ –≤—Л–њ–Є—Б–Ї–Є (—А–Є—Б. 1). –£–ґ–µ —З–µ—А–µ–Ј 30 –і–љ–µ–є –≤ –≥—А—Г–њ–њ–µ –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Ы–°–° –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М –Љ–µ–љ—М—И–µ –ї–µ—В–∞–ї—М–љ—Л—Е –Є—Б—Е–Њ–і–Њ–≤, —З–µ–Љ –≤ –≥—А—Г–њ–њ–µ –±–µ–Ј –Ы–°–°: 17 (0,5%) –њ—А–Њ—В–Є–≤ 179 (1,0%), –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–є —А–Є—Б–Ї 0,44 (–Ф–Ш 95% 0,27-0,73), p=0,001. –Ъ 6 –Љ–µ—Б—П—Ж—Г —Б–љ–Є–ґ–µ–љ–Є–µ –Њ–±—Й–µ–є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –≤ –≥—А—Г–њ–њ–µ –Ы–°–° —Б–Њ—Е—А–∞–љ—П–ї–Њ—Б—М: 63 (1,7%) –њ—А–Њ—В–Є–≤ 605 (3,5%), –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–є —А–Є—Б–Ї 0,48 (0,37-0,63), p < 0,0001. –≠—В–∞ –Ј–∞–Ї–Њ–љ–Њ–Љ–µ—А–љ–Њ—Б—В—М –≤—Л—П–≤–ї—П–ї–∞—Б—М –≤–Њ –≤—Б–µ—Е –њ–Њ–і–≥—А—Г–њ–њ–∞—Е.
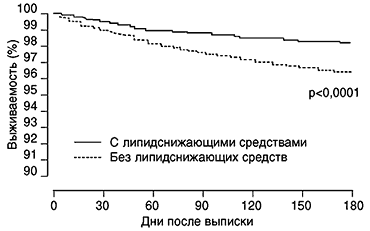
–†–Є—Б. 1. –Ъ—А–Є–≤—Л–µ –Ъ–∞–њ–ї–∞–љ–∞-–Ь–µ–є–µ—А–∞ 6-–Љ–µ—Б—П—З–љ–Њ–є –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В–Є –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –ї–µ—З–µ–љ–Є—П –Ы–°–° –њ–Њ—Б–ї–µ –≤—Л–њ–Є—Б–Ї–Є
–Р–љ–∞–ї–Є–Ј –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ—Б—В–Є–Ч–∞–Ї–ї—О—З–Є—В–µ–ї—М–љ—Л–є —А–µ–≥—А–µ—Б—Б–Є–Њ–љ–љ—Л–є –∞–љ–∞–ї–Є–Ј –≤–Ї–ї—О—З–∞–ї –≤—Б–µ –Ј–љ–∞—З–Є–Љ—Л–µ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–µ –њ—А–µ–і–Є–Ї—В–Њ—А—Л –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Ы–°–°: –і–Є–∞–≥–љ–Њ–Ј –≥–Є–њ–µ—А–ї–Є–њ–Є–і–µ–Љ–Є–Є; –ї–µ—З–µ–љ–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –Р–Я–§ –Є–ї–Є b-–±–ї–Њ–Ї–∞—В–Њ—А–∞–Љ–Є –і–Њ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є; –Ъ–® –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ; –±–Њ–ї–µ–µ –Љ–Њ–ї–Њ–і–Њ–є –≤–Њ–Ј—А–∞—Б—В; –ґ–µ–љ—Б–Ї–Є–є –њ–Њ–ї; –Њ—В—Б—Г—В—Б—В–≤–Є–µ –≥–Є–њ–µ—А—В–Њ–љ–Є–Є; –Ш–Ь –±–µ–Ј —Н–ї–µ–≤–∞—Ж–Є–Є ST –њ—А–Є –≤–Ї–ї—О—З–µ–љ–Є–Є –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ; –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Е—А–Є–њ–Њ–≤ –њ—А–Є –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–Є; –±–Њ–ї–µ–µ –њ–Њ–Ј–і–љ—П—П –і–∞—В–∞ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є; –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –І–Ъ–Р –Є –Њ—В—Б—Г—В—Б—В–≤–Є–µ –Ъ–® –≤–Њ –≤—А–µ–Љ—П –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є. –Ъ—А–Њ–Љ–µ —Н—В–Њ–≥–Њ, –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ—Б—В—М –Ї –ї–µ—З–µ–љ–Є—О –Ы–°–° –≤–∞—А—М–Є—А–Њ–≤–∞–ї–∞ –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –≥–µ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Њ–є –Њ–±–ї–∞—Б—В–Є. –Я–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –°–µ–≤–µ—А–љ–Њ–є –Р–Љ–µ—А–Є–Ї–Њ–є, –њ–∞—Ж–Є–µ–љ—В—Л –≤ –¶–µ–љ—В—А–∞–ї—М–љ–Њ–є –Р–Љ–µ—А–Є–Ї–µ, –Т–Њ—Б—В–Њ—З–љ–Њ–є –Є –Ч–∞–њ–∞–і–љ–Њ–є –Х–≤—А–Њ–њ–µ –Є–Љ–µ–ї–Є –Љ–µ–љ—М—И—Г—О –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Ы–°–° (–њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ—Б—В–Є) –њ—А–Є –≤—Л–њ–Є—Б–Ї–µ, –∞ –≤ –Р–≤—Б—В—А–∞–ї–Є–Є –Є –Э–Њ–≤–Њ–є –Ч–µ–ї–∞–љ–і–Є–Є - –±–Њ–ї—М—И—Г—О. –Ь–Њ–і–µ–ї—М –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ—Б—В–Є —Е–Њ—А–Њ—И–Њ –Њ–њ–Є—Б—Л–≤–∞–ї–∞ —А–∞–Ј–ї–Є—З–Є—П –Љ–µ–ґ–і—Г –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є, –Ї–Њ—В–Њ—А—Л–Љ –љ–∞–Ј–љ–∞—З–∞–ї–Є—Б—М –Ы–°–°, –Є —В–µ–Љ–Є, –Ї–Њ–Љ—Г –Њ–љ–Є –љ–µ –±—Л–ї–Є –љ–∞–Ј–љ–∞—З–µ–љ—Л. –Я–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ—Б—В–Є –±—Л–ї–Є —Б—Е–Њ–і–љ—Л–Љ–Є –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є—Е –і–µ—Ж–Є–ї—П—Е –Њ–±–µ–Є—Е –≥—А—Г–њ–њ. –Ю–і–љ–∞–Ї–Њ –Є—Б—Е–Њ–і–љ—Л–µ —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є –љ–µ –±—Л–ї–Є —Е–Њ—А–Њ—И–Њ —Б–±–∞–ї–∞–љ—Б–Є—А–Њ–≤–∞–љ—Л –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є –≤ 1, 2 –Є 3-–Љ –і–µ—Ж–Є–ї—П—Е (–≤ –≥—А—Г–њ–њ–µ –Ы–°–° –±–Њ–ї—М–љ—Л–µ –±—Л–ї–Є –љ–∞–Љ–љ–Њ–≥–Њ –Љ–Њ–ї–Њ–ґ–µ; –Њ–љ–Є —З–∞—Й–µ –њ–Њ–і–≤–µ—А–≥–∞–ї–Є—Б—М –І–Ъ–Р –Є–ї–Є –Ъ–®, —З–µ–Љ –≤ –≥—А—Г–њ–њ–µ –±–µ–Ј –Ы–°–°), –≤ —Б–≤—П–Ј–Є —Б —З–µ–Љ —Н—В–Є –њ–∞—Ж–Є–µ–љ—В—Л (n=6242) –±—Л–ї–Є –Є—Б–Ї–ї—О—З–µ–љ—Л –Є–Ј –Ј–∞–Ї–ї—О—З–Є—В–µ–ї—М–љ–Њ–≥–Њ –Љ–љ–Њ–≥–Њ—Д–∞–Ї—В–Њ—А–љ–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞.
–Ь–љ–Њ–≥–Њ—Д–∞–Ї—В–Њ—А–љ—Л–є –∞–љ–∞–ї–Є–Ј 6-–Љ–µ—Б—П—З–љ–Њ–є –ї–µ—В–∞–ї—М–љ–Њ—Б—В–Є
–Я–Њ—Б–ї–µ –њ–Њ–њ—А–∞–≤–Ї–Є –љ–∞ –њ—А–Є–≤—Е–Њ–і—П—Й–Є–µ —Д–∞–Ї—В–Њ—А—Л –Є –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ—Б—В—М –Ї –љ–∞–Ј–љ–∞—З–µ–љ–Є—О –Ы–°–°, –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –ї–Є–њ–Є–і—Б–љ–Є–ґ–∞—О—Й–µ–≥–Њ —Б—А–µ–і—Б—В–≤–∞ –њ—А–Є –≤—Л–њ–Є—Б–Ї–µ –Њ—Б—В–∞–ї–Њ—Б—М —Д–∞–Ї—В–Њ—А–Њ–Љ, –њ—А–Њ–≥–љ–Њ–Ј–Є—А—Г—О—Й–Є–Љ –±–Њ–ї–µ–µ –љ–Є–Ј–Ї—Г—О 6-–Љ–µ—Б—П—З–љ—Г—О –ї–µ—В–∞–ї—М–љ–Њ—Б—В—М. –Э–∞–Ј–љ–∞—З–µ–љ–Є–µ –Ы–°–° –Њ—Б—В–∞–ї–Њ—Б—М –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–Љ –Є –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–Љ –њ—А–µ–і–Є–Ї—В–Њ—А–Њ–Љ –±–Њ–ї–µ–µ –љ–Є–Ј–Ї–Њ–є 6-–Љ–µ—Б—П—З–љ–Њ–є –ї–µ—В–∞–ї—М–љ–Њ—Б—В–Є –і–∞–ґ–µ –њ–Њ—Б–ї–µ –њ—А–Њ–≤–µ–і–µ–љ–Є—П –∞–љ–∞–ї–Є–Ј–∞ —В–Њ–ї—М–Ї–Њ —Б—А–µ–і–Є 4-10-–≥–Њ –і–µ—Ж–Є–ї–µ–є –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ—Б—В–Є (n=14567): –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–є —А–Є—Б–Ї 0,67 (–Ф–Ш 95% 0,47-0,95), p=0,023. –Ю—В–Њ–±—А–∞–љ–љ—Л–µ –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–µ –њ—А–µ–і–Є–Ї—В–Њ—А—Л 6-–Љ–µ—Б—П—З–љ–Њ–є –ї–µ—В–∞–ї—М–љ–Њ—Б—В–Є –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –љ–∞ —А–Є—Б—Г–љ–Ї–µ 2.
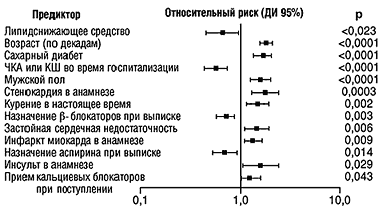
–†–Є—Б. 2. –Э–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–µ –њ—А–µ–і–Є–Ї—В–Њ—А—Л 6-–Љ–µ—Б—П—З–љ–Њ–є –ї–µ—В–∞–ї—М–љ–Њ—Б—В–Є —Б—А–µ–і–Є —Г—А–∞–≤–љ–µ–љ–љ—Л—Е –њ–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—О –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ—Б—В–Є –Ї –љ–∞–Ј–љ–∞—З–µ–љ–Є—О –Ы–°–° –њ–∞—Ж–Є–µ–љ—В–Њ–≤
–Ь–љ–Њ–≥–Њ—Д–∞–Ї—В–Њ—А–љ—Л–є –∞–љ–∞–ї–Є–Ј –ї–µ—В–∞–ї—М–љ—Л—Е –Є—Б—Е–Њ–і–Њ–≤ –Є –љ–µ—Д–∞—В–∞–ї—М–љ—Л—Е –Є–љ—Д–∞—А–Ї—В–Њ–≤ –Љ–Є–Њ–Ї–∞—А–і–∞–І–µ—А–µ–Ј 6 –Љ–µ—Б—П—Ж–µ–≤ 1242 –њ–∞—Ж–Є–µ–љ—В–∞ —Г–Љ–µ—А–ї–Є –Є–ї–Є –њ–µ—А–µ–љ–µ—Б–ї–Є –љ–µ—Д–∞—В–∞–ї—М–љ—Л–є –Є–љ—Д–∞—А–Ї—В –Љ–Є–Њ–Ї–∞—А–і–∞: 1057 (6,2%) —Б—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –≤—Л–њ–Є—Б–∞–љ–љ—Л—Е –±–µ–Ј –Ы–°–° –Є 185 (5,1%) —Б—А–µ–і–Є –≤—Л–њ–Є—Б–∞–љ–љ—Л—Е —Б –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ–Љ –Ы–°–°. –Я–Њ—Б–ї–µ —Г—А–∞–≤–љ–Є–≤–∞–љ–Є—П –њ–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—О –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ—Б—В–Є –Ї –љ–∞–Ј–љ–∞—З–µ–љ–Є—О –Ы–°–°, —З–∞—Б—В–Њ—В–∞ –Ї–Њ–љ–µ—З–љ–Њ–є —В–Њ—З–Ї–Є (—Б–Љ–µ—А—В—М –Є–ї–Є –љ–µ—Д–∞—В–∞–ї—М–љ—Л–є –Ш–Ь –≤ —В–µ—З–µ–љ–Є–µ 6 –Љ–µ—Б—П—Ж–µ–≤) –±—Л–ї–∞ –љ–Є–ґ–µ –≤ –≥—А—Г–њ–њ–µ —Б –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ–Љ –Ы–°–°: –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–є —А–Є—Б–Ї 0,80 (–Ф–Ш 95% 0,65-0,98), p=0,035. –Ґ–∞–Ї–Є–Љ –ґ–µ –њ—А–µ–і–Є–Ї—В–Њ—А–Њ–Љ –љ–Є–Ј–Ї–Њ–≥–Њ —А–Є—Б–Ї–∞ —П–≤–ї—П–ї–Њ—Б—М –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Ы–°–° –њ—А–Є –∞–љ–∞–ї–Є–Ј–µ —В–Њ–ї—М–Ї–Њ —Б—А–µ–і–Є 4-10-–≥–Њ –і–µ—Ж–Є–ї–µ–є –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ—Б—В–Є: –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–є —А–Є—Б–Ї 0,79 (0,64-0,99), p=0,037. –Ф–ї—П —Г—В–Њ—З–љ–µ–љ–Є—П, –љ–∞ –Ї–∞–Ї—Г—О —Б–Њ—Б—В–∞–≤–ї—П—О—Й—Г—О –Ї–Њ–љ–µ—З–љ–Њ–є —В–Њ—З–Ї–Є (—Б–Љ–µ—А—В—М –Є–ї–Є –Є–љ—Д–∞—А–Ї—В –Љ–Є–Њ–Ї–∞—А–і–∞) –і–µ–є—Б—В–≤—Г—О—В –Ы–°–°, –±—Л–ї –њ—А–Њ–≤–µ–і–µ–љ –∞–љ–∞–ї–Є–Ј –Ї–Њ–љ–Ї—Г—А–Є—А—Г—О—Й–Є—Е —А–Є—Б–Ї–Њ–≤ [22]. –Я—А–Є —Н—В–Њ–Љ –љ–µ –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є –Љ–µ–ґ–і—Г –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Ы–°–° –њ–Њ—Б–ї–µ –≤—Л–њ–Є—Б–Ї–Є –Є —А–Є—Б–Ї–Њ–Љ –Ш–Ь. –Я–Њ—Н—В–Њ–Љ—Г —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л—Е –Є—Б—Е–Њ–і–Њ–≤, –≤–µ—А–Њ—П—В–љ–Њ, —Б–≤—П–Ј–∞–љ–Њ —Б –Є–Ј–Њ–ї–Є—А–Њ–≤–∞–љ–љ—Л–Љ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –ї–µ—В–∞–ї—М–љ–Њ—Б—В–Є.
–Ю–±—Б—Г–ґ–і–µ–љ–Є–µ
–•–Њ—В—П —Н—В–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –љ–µ –±—Л–ї–Њ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–Љ, –Є –µ–≥–Њ —А–µ–Ј—Г–ї—М—В–∞—В—Л –і–Њ–ї–ґ–љ—Л —А–∞—Б—Ж–µ–љ–Є–≤–∞—В—М—Б—П –ї–Є—И—М –Ї–∞–Ї –і–∞—О—Й–Є–µ –љ–∞—З–∞–ї–Њ –≥–Є–њ–Њ—В–µ–Ј–µ, –Њ–і–љ–∞–Ї–Њ —Б–≤—П–Ј–∞–љ–љ–Њ–µ —Б –Ы–°–Ґ –∞–±—Б–Њ–ї—О—В–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —А–Є—Б–Ї–∞ —Б–Љ–µ—А—В–Є –љ–∞ 1,8% –Њ–Ј–љ–∞—З–∞–µ—В —Б–Њ—Е—А–∞–љ–µ–љ–Є–µ –Њ–і–љ–Њ–є –ґ–Є–Ј–љ–Є –љ–∞ –Ї–∞–ґ–і—Л–µ 56 –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ—А–Њ–ї–µ—З–µ–љ–љ—Л—Е –Ы–°–° –≤ —В–µ—З–µ–љ–Є–µ 6 –Љ–µ—Б—П—Ж–µ–≤. –£–Љ–µ–љ—М—И–µ–љ–Є–µ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ–≥–Њ —А–Є—Б–Ї–∞ —Б–Љ–µ—А—В–Є –љ–∞ 33% —Б–Њ–≥–ї–∞—Б—Г–µ—В—Б—П —Б —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ–Є –њ—А–µ–і—Л–і—Г—Й–Є—Е —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –ї–Є–њ–Є–і—Б–љ–Є–ґ–∞—О—Й–µ–є —В–µ—А–∞–њ–Є–Є —Г –±–Њ–ї—М–љ—Л—Е —Б–Њ —Б—В–∞–±–Є–ї—М–љ–Њ–є –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–є –±–Њ–ї–µ–Ј–љ—М—О [1вАУ3]. –≠—В–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ –ї–Є–њ–Є–і—Б–љ–Є–ґ–∞—О—Й–∞—П —В–µ—А–∞–њ–Є—П –Љ–Њ–ґ–µ—В –њ—А–Є–Љ–µ–љ—П—В—М—Б—П –Є –≤ –Њ—Б—В—А–Њ–є —Б–Є—В—Г–∞—Ж–Є–Є.
–Р–≤—В–Њ—А—Л –љ–µ –≤—Л—П–≤–Є–ї–Є —П–≤–љ–Њ–є –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є –Љ–µ–ґ–і—Г –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Ы–°–° –њ–Њ—Б–ї–µ –≤—Л–њ–Є—Б–Ї–Є –Є —А–Є—Б–Ї–Њ–Љ –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ –ї–Є–њ–Є–і—Б–љ–Є–ґ–∞—О—Й–Є–µ —Б—А–µ–і—Б—В–≤–∞ –Љ–Њ–≥—Г—В –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞—В—М —Б–Љ–µ—А—В—М, –љ–Њ –љ–µ –Є–љ—Д–∞—А–Ї—В –Љ–Є–Њ–Ї–∞—А–і–∞ –≤ —В–µ—З–µ–љ–Є–µ –њ–µ—А–≤—Л—Е 6 –Љ–µ—Б—П—Ж–µ–≤ –њ–Њ—Б–ї–µ –Њ—Б—В—А–Њ–≥–Њ –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞; –Њ–і–љ–∞–Ї–Њ –Њ–љ–Є –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞—О—В –Ш–Ь —Г –±–Њ–ї—М–љ—Л—Е —Б–Њ —Б—В–∞–±–Є–ї—М–љ–Њ–є –Ъ–С–° —З–µ—А–µ–Ј 1-2 –≥–Њ–і–∞ –ї–µ—З–µ–љ–Є—П [1-3]. –Ф—А—Г–≥–Њ–µ –Њ–±—К—П—Б–љ–µ–љ–Є–µ –Њ—В—Б—Г—В—Б—В–≤–Є—О —В–∞–Ї–Њ–є –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є - –њ–Њ–≥—А–µ—И–љ–Њ—Б—В–Є –њ—А–Є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –Ш–Ь. –Я–Њ–ї—Г—З–∞—О—Й–Є–µ –Ы–°–° –њ–∞—Ж–Є–µ–љ—В—Л –Є–ї–Є –Є—Е –≤—А–∞—З–Є –Љ–Њ–≥–ї–Є –±—Л—В—М –±–Њ–ї–µ–µ –љ–∞—Б—В–Њ—А–Њ–ґ–µ–љ–љ—Л–Љ–Є –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –±–Њ–ї—М—И–µ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ —Б–ї—Г—З–∞–µ–≤ –Ш–Ь –Љ–Њ–≥–ї–Њ –±—Л—В—М –Є–і–µ–љ—В–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–Њ —Б—А–µ–і–Є –њ–Њ–ї—Г—З–∞—О—Й–Є—Е –Ы–°–Ґ, —З–µ–Љ —Б—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±–µ–Ј –Ы–°–Ґ, –∞ –Є—Б—В–Є–љ–љ–∞—П –≤—Л–≥–Њ–і–∞ –ї–Є–њ–Є–і—Б–љ–Є–ґ–∞—О—Й–µ–є —В–µ—А–∞–њ–Є–Є –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –Ш–Ь –±—Л–ї–∞ –±—Л –њ–Њ—Н—В–Њ–Љ—Г –Ј–∞–Љ–∞—Б–Ї–Є—А–Њ–≤–∞–љ–∞.
–Я–Њ–Ї–∞ –Љ–∞–ї–Њ –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –ї–Є–њ–Є–і—Б–љ–Є–ґ–∞—О—Й–µ–є —В–µ—А–∞–њ–Є–Є –њ—А–Є –Њ—Б—В—А–Њ–Љ –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–Љ —Б–Є–љ–і—А–Њ–Љ–µ. –Т –Њ–±—Б–µ—А–≤–∞—Ж–Є–Њ–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –®–≤–µ–і—Б–Ї–Њ–≥–Њ —А–µ–≥–Є—Б—В—А–∞ –Ї–∞—А–і–Є–∞–ї—М–љ–Њ–є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ —Б—В–∞—В–Є–љ–Њ–≤ –і–Њ –Є–ї–Є —Б –Љ–Њ–Љ–µ–љ—В–∞ –≤—Л–њ–Є—Б–Ї–Є –Є–Ј —Б—В–∞—Ж–Є–Њ–љ–∞—А–∞ –њ–Њ—Б–ї–µ –Њ—Б—В—А–Њ–≥–Њ –Ш–Ь —Б–≤—П–Ј–∞–љ–Њ —Б–Њ –Ј–љ–∞—З–Є–Љ—Л–Љ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ–≥–Њ —А–Є—Б–Ї–∞ —Б–Љ–µ—А—В–Є –≤ —В–µ—З–µ–љ–Є–µ 1 –≥–Њ–і–∞ –љ–∞ 25% [23]. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є MIRACL [24] –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –љ–∞ 16 –љ–µ–і–µ–ї—М –∞—В–Њ—А–≤–∞—Б—В–∞—В–Є–љ–∞ —Г 3086 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б—А–∞–Ј—Г –њ–Њ—Б–ї–µ –љ–µ—Б—В–∞–±–Є–ї—М–љ–Њ–є —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –Є–ї–Є –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ –±–µ–Ј –Ј—Г–±—Ж–∞ Q –±—Л–ї–Њ —Б–≤—П–Ј–∞–љ–Њ —Б–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–Љ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ–≥–Њ —Б—Г–Љ–Љ–∞—А–љ–Њ–≥–Њ —А–Є—Б–Ї–∞ —Б–Љ–µ—А—В–Є, –љ–µ—Д–∞—В–∞–ї—М–љ–Њ–≥–Њ –Ш–Ь, —А–µ–∞–љ–Є–Љ–∞—Ж–Є–Є –њ—А–Є –≤–љ–µ–Ј–∞–њ–љ–Њ–є –Ї–∞—А–і–Є–∞–ї—М–љ–Њ–є —Б–Љ–µ—А—В–Є –Є–ї–Є —Н–Ї—Б—В—А–µ–љ–љ–Њ–є –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є —Б –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–µ–є —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–µ–є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–ї–∞—Ж–µ–±–Њ (14,8% –њ—А–Њ—В–Є–≤ 17,4%, –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–є —А–Є—Б–Ї 0,84 (–Ф–Ш 95% 0,701-0,999), p=0,048. –£–Љ–µ–љ—М—И–µ–љ–Є–µ –ї–µ—В–∞–ї—М–љ–Њ—Б—В–Є –љ–µ –±—Л–ї–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ (4,4% –њ—А–Њ—В–Є–≤ 4,2%). –Ю–і–љ–∞–Ї–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ MIRACL –љ–µ –Є–Љ–µ–ї–Њ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ–є —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–є —Б–Є–ї—Л, —З—В–Њ–±—Л –Њ–±–љ–∞—А—Г–ґ–Є—В—М —В–∞–Ї–Є–µ –Љ–∞–ї—Л–µ —А–∞–Ј–ї–Є—З–Є—П, –Ї–∞–Ї –Њ–њ–Є—Б—Л–≤–∞–µ–Љ—Л–µ –≤–µ—А—Е–љ–Є–Љ–Є –≥—А–∞–љ–Є—Ж–∞–Љ–Є –і–Њ–≤–µ—А–Є—В–µ–ї—М–љ—Л—Е –Є–љ—В–µ—А–≤–∞–ї–Њ–≤ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є H.D. Aronow et al. –Є –®–≤–µ–і—Б–Ї–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є. –†–Њ–ї—М —Б—В–∞—В–Є–љ–Њ–≤ –≤ —Н—В–Є—Е —Г—Б–ї–Њ–≤–Є—П—Е —В—А–µ–±—Г–µ—В –і–∞–ї—М–љ–µ–є—И–µ–≥–Њ –Є–Ј—Г—З–µ–љ–Є—П.
–Э–µ—Б–Ї–Њ–ї—М–Ї–Њ –њ—А–Њ–і–Њ–ї–ґ–∞—О—Й–Є—Е—Б—П —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –Є–Ј—Г—З–∞—О—В –≤–ї–Є—П–љ–Є–µ —Б—В–∞—В–Є–љ–Њ–≤ –љ–∞ —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л–µ —Б–Њ–±—Л—В–Є—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б–Њ —Б–≤–µ–ґ–Є–Љ–Є –Њ—Б—В—А—Л–Љ–Є –Ї–Њ—А–Њ–љ–∞—А–љ—Л–Љ–Є —Б–Є–љ–і—А–Њ–Љ–∞–Љ–Є. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ Aggrastat to Zocor (A to Z) –њ–Њ—Б–≤—П—Й–µ–љ–Њ —Н—Д—Д–µ–Ї—В—Г —Б–Є–Љ–≤–∞—Б—В–∞—В–Є–љ–∞ –љ–∞ –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–µ —Б–Њ–±—Л—В–Є—П –њ–Њ—Б–ї–µ –Ю–Ъ–° –±–µ–Ј —Н–ї–µ–≤–∞—Ж–Є–Є ST, –∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П PRINCESS (–Я—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є–µ —А–µ–Є–љ—Д–∞—А–Ї—В–∞ –њ—А–Є —А–∞–љ–љ–µ–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є —Ж–µ—А–Є–≤–∞—Б—В–∞—В–Є–љ–∞) –Є –†–Р–°–Ґ (–Я—А–∞–≤–∞—Б—В–∞—В–Є–љ –њ—А–Є –Њ—Б—В—А–Њ–Љ –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–Љ —Б–Є–љ–і—А–Њ–Љ–µ) –Є–Ј—Г—З–∞—О—В –≤–ї–Є—П–љ–Є–µ —Б—В–∞—В–Є–љ–Њ–≤ –њ—А–Є –љ–µ–і–∞–≤–љ–µ–Љ –Ш–Ь —Б —Н–ї–µ–≤–∞—Ж–Є–µ–є ST.
–Т –њ—А–µ–і—Л–і—Г—Й–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –Ы–°–° –њ—А–Є —Б—В–∞–±–Є–ї—М–љ–Њ–є –Ъ–С–° –Ї—А–Є–≤—Л–µ –≤—Л–ґ–Є–≤–∞–љ–Є—П –љ–µ —А–∞–Ј–і–µ–ї—П–ї–Є—Б—М –і–Њ 1-2 –ї–µ—В –њ–Њ—Б–ї–µ –љ–∞—З–∞–ї–∞ —В–µ—А–∞–њ–Є–Є [1-3]. –Т –Њ–њ–Є—Б—Л–≤–∞–µ–Љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б–Њ —Б–≤–µ–ґ–µ–є –љ–µ—Б—В–∞–±–Є–ї—М–љ–Њ–є —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–µ–є –Є–ї–Є –Є–љ—Д–∞—А–Ї—В–Њ–Љ –Љ–Є–Њ–Ї–∞—А–і–∞ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —Б–љ–Є–ґ–µ–љ–Є–µ –ї–µ—В–∞–ї—М–љ–Њ—Б—В–Є –Ї 30 –і–љ—П–Љ, –њ—А–Є—З–µ–Љ —Н—В–Њ —А–∞–Ј–ї–Є—З–Є–µ —Г–≤–µ–ї–Є—З–Є–≤–∞–ї–Њ—Б—М –Ї 6 –Љ–µ—Б—П—Ж–∞–Љ. –†–∞–љ–љ–µ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –њ—А–Є –Ы–°–Ґ –њ—А–Њ–Є–Ј–Њ—И–ї–Њ –Є —Г –±–Њ–ї—М–љ—Л—Е —Б –Ш–Ь –≤ –®–≤–µ–і—Б–Ї–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є [23].
–Я–Њ–Ї–∞ —В–Њ—З–љ–Њ –љ–µ –Њ–њ—А–µ–і–µ–ї–µ–љ–Њ, –Ї–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ —Б—В–∞—В–Є–љ—Л —Б–љ–Є–ґ–∞—О—В —А–Є—Б–Ї –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л—Е –Є—Б—Е–Њ–і–Њ–≤ –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –Є—Е —Б—А–∞–Ј—Г –њ–Њ—Б–ї–µ –Њ—Б—В—А–Њ–≥–Њ –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, –љ–Њ –µ—Б—В—М –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –≤–µ—А–Њ—П—В–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤, –≤ —В.—З. –≤–ї–Є—П–љ–Є–µ –Є—Е –љ–∞ —Д—Г–љ–Ї—Ж–Є–Є —Н–љ–і–Њ—В–µ–ї–Є—П –Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤, –∞ —В–∞–Ї–ґ–µ –љ–∞ –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є RECIFE (–°–љ–Є–ґ–µ–љ–Є–µ —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞ –њ—А–Є –Є—И–µ–Љ–Є–Є –Є —Д—Г–љ–Ї—Ж–Є—П —Н–љ–і–Њ—В–µ–ї–Є—П) [8] —В–µ—А–∞–њ–Є—О —Б—В–∞—В–Є–љ–∞–Љ–Є –љ–∞—З–Є–љ–∞–ї–Є —Б—А–∞–Ј—Г –њ–Њ—Б–ї–µ –Ю–Ъ–°, –Є —Г–ї—Г—З—И–µ–љ–Є–µ —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М –Ї 6 –љ–µ–і–µ–ї–µ. –Ф—А—Г–≥–Є–µ –∞–≤—В–Њ—А—Л –Њ—В–Љ–µ—З–∞–ї–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є —Г–ґ–µ —З–µ—А–µ–Ј 2 –љ–µ–і–µ–ї–Є –њ–Њ—Б–ї–µ –Љ–Њ–і–Є—Д–Є–Ї–∞—Ж–Є–Є –ї–Є–њ–Є–і—Б–љ–Є–ґ–∞—О—Й–µ–є —В–µ—А–∞–њ–Є–Є [9]. –Т –Њ–њ—Л—В–∞—Е in vitro —Б—В–∞—В–Є–љ—Л —Г–≤–µ–ї–Є—З–Є–≤–∞—О—В –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ–Њ–є NO-—Б–Є–љ—В–∞–Ј—Л —З–µ—А–µ–Ј 48 —З–∞—Б–Њ–≤ –њ–Њ—Б–ї–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П [25]. –°—В–∞—В–Є–љ—Л —В–Њ—А–Љ–Њ–Ј—П—В –∞–Ї—В–Є–≤–∞—Ж–Є—О —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ —З–µ—А–µ–Ј 4 –љ–µ–і–µ–ї–Є [11] –Є —Г–Љ–µ–љ—М—И–∞—О—В —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ —В—А–Њ–Љ–±–Њ—Ж–Є—В–∞—А–љ–Њ–≥–Њ —В—А–Њ–Љ–±–∞ –≤ —Б—А–µ–і–љ–µ–Љ —З–µ—А–µ–Ј 2,5 –Љ–µ—Б—П—Ж–∞ —В–µ—А–∞–њ–Є–Є [10]. –Э–∞–Ї–Њ–љ–µ—Ж, —Б—В–∞—В–Є–љ—Л —В–Њ—А–Љ–Њ–Ј—П—В –Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ—Г—О g-–Є–љ—В–µ—А—Д–µ—А–Њ–љ–Њ–Љ –∞–Ї—В–Є–≤–∞—Ж–Є—О T-–ї–Є–Љ—Д–Њ—Ж–Є—В–Њ–≤ [26], —Г–Љ–µ–љ—М—И–∞—О—В –∞–і–≥–µ–Ј–Є–≤–љ—Л–µ —Б–≤–Њ–є—Б—В–≤–∞ –Љ–Њ–љ–Њ—Ж–Є—В–Њ–≤ —З–µ—А–µ–Ј 6 –љ–µ–і–µ–ї—М –ї–µ—З–µ–љ–Є—П [12]; –∞ —В–∞–Ї–ґ–µ —Б–љ–Є–ґ–∞—О—В –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О C-—А–µ–∞–Ї—В–Є–≤–љ–Њ–≥–Њ –њ—А–Њ—В–µ–Є–љ–∞ –≤ –Ї—А–Њ–≤–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≥–Є–њ–µ—А–ї–Є–њ–Є–і–µ–Љ–Є–µ–є —З–µ—А–µ–Ј 3-4 –Љ–µ—Б—П—Ж–∞ –ї–µ—З–µ–љ–Є—П [13].
–Ъ–Њ–≥–і–∞ –Ї –Є—Б—Е–Њ–і–љ–Њ–є –Љ–Њ–і–µ–ї–Є 6-–Љ–µ—Б—П—З–љ–Њ–є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –±—Л–ї–Є –і–Њ–±–∞–≤–ї–µ–љ—Л –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–µ –њ–µ—А–µ–Љ–µ–љ–љ—Л–µ, –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–є —А–Є—Б–Ї —Г–≤–µ–ї–Є—З–Є–ї—Б—П –Њ—В 0,48 –і–Њ 0,60, —З—В–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ —Б—Г—Й–µ—Б—В–≤–Њ–≤–∞–≤—И–µ–Љ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ —З–Є—Б–ї–µ —Д–∞–Ї—В–Њ—А–Њ–≤ –Њ—И–Є–±–Ї–Є. –Ю–і–љ–∞–Ї–Њ –Ї–Њ–≥–і–∞ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–µ –њ–µ—А–µ–Љ–µ–љ–љ—Л–µ –±—Л–ї–Є –і–Њ–±–∞–≤–ї–µ–љ—Л –Ї –Љ–Њ–і–µ–ї–Є —Б –≤–љ–µ—Б–µ–љ–љ–Њ–є –њ–Њ–њ—А–∞–≤–Ї–Њ–є –љ–∞ –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ—Б—В—М –Ї –љ–∞–Ј–љ–∞—З–µ–љ–Є—О –Ы–°–°, –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–є —А–Є—Б–Ї —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –љ–µ –Є–Ј–Љ–µ–љ–Є–ї—Б—П. –≠—В–Њ –Њ–Ј–љ–∞—З–∞–µ—В, —З—В–Њ –њ—А–Є –∞–љ–∞–ї–Є–Ј–µ –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ—Б—В–Є —Г–ґ–µ –±—Л–ї–Њ —Г—З—В–µ–љ–Њ –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ —Д–∞–Ї—В–Њ—А–Њ–≤ –Њ—И–Є–±–Ї–Є. –Э–∞–Њ–±–Њ—А–Њ—В, –Ї–Њ–≥–і–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ—Б—В–Є –±—Л–ї –і–Њ–±–∞–≤–ї–µ–љ –Ї –Љ–Њ–і–µ–ї–Є, –≤–Ї–ї—О—З–∞–≤—И–µ–є –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–µ –њ–µ—А–µ–Љ–µ–љ–љ—Л–µ, –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–є —А–Є—Б–Ї —Г–≤–µ–ї–Є—З–Є–ї—Б—П –Њ—В 0,60 –і–Њ 0,67. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –∞–љ–∞–ї–Є–Ј –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ—Б—В–Є –њ–Њ–Ј–≤–Њ–ї—П–µ—В –≤–љ–µ—Б—В–Є –њ–Њ–њ—А–∞–≤–Ї—Г –љ–∞ —А—П–і —Д–∞–Ї—В–Њ—А–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –љ–µ —Г—З–Є—В—Л–≤–∞—О—В—Б—П —Б—В–∞–љ–і–∞—А—В–љ—Л–Љ–Є –Љ–љ–Њ–≥–Њ—Д–∞–Ї—В–Њ—А–љ—Л–Љ–Є –Љ–µ—В–Њ–і–∞–Љ–Є –∞–љ–∞–ї–Є–Ј–∞. –С–µ–Ј —Г—З–µ—В–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ—Б—В–Є –Є—Б—В–Є–љ–љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –ї–µ—В–∞–ї—М–љ–Њ—Б—В–Є –Љ–Њ–≥–ї–Њ –±—Л—В—М –Ј–∞–≤—Л—И–µ–љ–Њ.
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є H.D. Aronow et al. –Є–Љ–µ–µ—В—Б—П –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ—Л—Е –Њ–≥—А–∞–љ–Є—З–µ–љ–Є–є. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±—Л–ї–Њ –Њ–±—Б–µ—А–≤–∞—Ж–Є–Њ–љ–љ—Л–Љ: –ї–Є–њ–Є–і—Б–љ–Є–ґ–∞—О—Й–∞—П —В–µ—А–∞–њ–Є—П –љ–µ –љ–∞–Ј–љ–∞—З–∞–ї–∞—Б—М –њ–∞—Ж–Є–µ–љ—В–∞–Љ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ. –•–Њ—В—П —А—П–і –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–µ–є –Є—Б–њ–Њ–ї—М–Ј—Г—О—В —Б—В–∞–љ–і–∞—А—В–љ—Л–µ –Љ–µ—В–Њ–і—Л –Љ–љ–Њ–≥–Њ—Д–∞–Ї—В–Њ—А–љ–Њ–є —А–µ–≥—А–µ—Б—Б–Є–Є –і–ї—П –≤–љ–µ—Б–µ–љ–Є—П –њ–Њ–њ—А–∞–≤–Њ–Ї –љ–∞ –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–µ –Є—Б—В–Њ—З–љ–Є–Ї–Є –њ–Њ–≥—А–µ—И–љ–Њ—Б—В–µ–є [27-29], –µ—Б—В—М –Љ–љ–µ–љ–Є–µ –Њ –љ–µ–Є–Ј–±–µ–ґ–љ–Њ—Б—В–Є –Њ—И–Є–±–Ї–Є –њ—А–Є –Њ—Ж–µ–љ–Ї–µ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л—Е —А–Є—Б–Ї–Њ–≤ –≤ —Н—В–Є—Е —Б–ї—Г—З–∞—П—Е [18]. –Р–љ–∞–ї–Є–Ј –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ—Б—В–Є —Б–њ–Њ—Б–Њ–±–µ–љ –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ –Є –∞–і–µ–Ї–≤–∞—В–љ–Њ –≤–љ–Њ—Б–Є—В—М –њ–Њ–њ—А–∞–≤–Ї–Є –і–ї—П –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ—Л—Е –њ–µ—А–µ–Љ–µ–љ–љ—Л—Е [19], –љ–Њ –і–∞–ґ–µ —Н—В–Њ—В –Љ–µ—В–Њ–і –љ–µ –Љ–Њ–ґ–µ—В —Г—З–µ—Б—В—М –љ–µ–Є–Ј–≤–µ—Б—В–љ—Л–µ –Є–ї–Є –љ–µ–Є–Ј–Љ–µ—А—П–µ–Љ—Л–µ —Д–∞–Ї—В–Њ—А—Л (–љ–∞–њ—А–Є–Љ–µ—А, –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є —Б–Є—Б—В–µ–Љ—Л –Ј–і—А–∞–≤–Њ–Њ—Е—А–∞–љ–µ–љ–Є—П). –Ґ–Њ–ї—М–Ї–Њ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Б–њ–Њ—Б–Њ–±–љ–Њ –њ—А–Њ–Є–Ј–≤–µ—Б—В–Є –≤—Л—А–∞–≤–љ–Є–≤–∞–љ–Є–µ –≥—А—Г–њ–њ –њ–Њ –≤—Б–µ–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ. –Я–Њ—Н—В–Њ–Љ—Г, –љ–µ—Б–Љ–Њ—В—А—П –љ–∞ –≤–Ї–ї—О—З–µ–љ–Є–µ –≤ –∞–љ–∞–ї–Є–Ј –≤ –Ї–∞—З–µ—Б—В–≤–µ –њ–µ—А–µ–Љ–µ–љ–љ—Л—Е –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –∞—Б–њ–Є—А–Є–љ–∞, b-–±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤ –Є –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –њ—А–Є –≤—Л–њ–Є—Б–Ї–µ, –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Ы–°–° –њ—А–Є –≤—Л–њ–Є—Б–Ї–µ –Љ–Њ–ґ–µ—В –±—Л—В—М –њ—А–Њ—Б—В–Њ –њ—А–Њ—П–≤–ї–µ–љ–Є–µ–Љ –і–µ–є—Б—В–≤–Є—П –і—А—Г–≥–Є—Е –љ–µ–Є–Ј–Љ–µ—А—П–µ–Љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –Њ—В—А–∞–ґ–∞—О—В –±–Њ–ї–µ–µ –∞–≥—А–µ—Б—Б–Є–≤–љ—Г—О —Б—В—А–∞—В–µ–≥–Є—О –ї–µ—З–µ–љ–Є—П.
–Ф–∞–љ–љ—Л–µ –Њ –њ—А–Є–≤–µ—А–ґ–µ–љ–љ–Њ—Б—В–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ї –Ы–°–Ґ –≤ —В–µ—З–µ–љ–Є–µ –њ–µ—А–Є–Њ–і–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П –љ–µ –±—Л–ї–Є –і–Њ—Б—В—Г–њ–љ—Л. –І–∞—Б—В—М –±–Њ–ї—М–љ—Л—Е, –≤—Л–њ–Є—Б–∞–љ–љ—Л—Е –±–µ–Ј –Ы–°–Ґ, –Љ–Њ–≥–ї–Є –≤–њ–Њ—Б–ї–µ–і—Б—В–≤–Є–Є –љ–∞—З–∞—В—М –њ—А–Є–µ–Љ –Ы–°–°, –Є –љ–∞–Њ–±–Њ—А–Њ—В, –љ–µ–Ї–Њ—В–Њ—А—Л–µ –±–Њ–ї—М–љ—Л–µ, –≤—Л–њ–Є—Б–∞–љ–љ—Л–µ —Б —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ–Є –њ—А–Є–љ–Є–Љ–∞—В—М –Ы–°–°, –Љ–Њ–≥–ї–Є –њ—А–µ–Ї—А–∞—В–Є—В—М –ї–µ—З–µ–љ–Є–µ. –Ю–і–љ–∞–Ї–Њ —В–∞–Ї–∞—П –њ–Њ–≥—А–µ—И–љ–Њ—Б—В—М –њ—А–Є–≤–µ–ї–∞ –±—Л –Ї –љ–µ–і–Њ–Њ—Ж–µ–љ–Ї–µ, –∞ –љ–µ –Ї –њ–µ—А–µ–Њ—Ж–µ–љ–Ї–µ —Б–≤—П–Ј–Є –Љ–µ–ґ–і—Г –ї–Є–њ–Є–і—Б–љ–Є–ґ–∞—О—Й–µ–є —В–µ—А–∞–њ–Є–µ–є –Є –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В—М—О.
–Ф–∞–љ–љ—Л–µ –Њ –ї–Є–њ–Є–і–љ–Њ–Љ –њ—А–Њ—Д–Є–ї–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —В–∞–Ї–ґ–µ –±—Л–ї–Є –љ–µ–і–Њ—Б—В—Г–њ–љ—Л. –•–Њ—В—П —Г–Љ–µ–љ—М—И–µ–љ–Є–µ —З–Є—Б–ї–∞ —Б–Њ–±—Л—В–Є–є –љ–µ –Ј–∞–≤–Є—Б–µ–ї–Њ –Њ—В –љ–∞–ї–Є—З–Є—П –≥–Є–њ–µ—А–ї–Є–њ–Є–і–µ–Љ–Є–Є, –љ–µ–Є–Ј–≤–µ—Б—В–љ–Њ, –Ј–∞–≤–Є—Б–Є—В –ї–Є —Н—В–Њ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Њ—В –Є—Б—Е–Њ–і–љ—Л—Е —Г—А–Њ–≤–љ–µ–є –ї–Є–њ–Є–і–љ—Л—Е —Д—А–∞–Ї—Ж–Є–є –Є–ї–Є –Њ—В –Є—Е –і–Є–љ–∞–Љ–Є–Ї–Є –Є —Б—Г—Й–µ—Б—В–≤—Г–µ—В –ї–Є –њ–Њ—А–Њ–≥–Њ–≤—Л–є —Н—Д—Д–µ–Ї—В.
–Э–∞–Ї–Њ–љ–µ—Ж, –љ–µ—П—Б–љ–Њ, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –ї–Є –Њ—В–љ–µ—Б—В–Є —А–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П H.D. Aronow et al. –Ї –њ–∞—Ж–Є–µ–љ—В–∞–Љ, –њ–Њ–ї—Г—З–∞—О—Й–Є–Љ –њ–Њ—Б–ї–µ –Ю–Ъ–° –ї—О–±–Њ–є —В–Є–њ –ї–Є–њ–Є–і—Б–љ–Є–ґ–∞—О—Й–µ–є —В–µ—А–∞–њ–Є–Є. –Т –њ—А–Є–љ—Ж–Є–њ–µ —В–µ—А–Љ–Є–љ вАЬ–ї–Є–њ–Є–і—Б–љ–Є–ґ–∞—О—Й–Є–µ —Б—А–µ–і—Б—В–≤–∞вАЭ - –Ј–∞–Љ–µ–љ–Є—В–µ–ї—М —В–µ—А–Љ–Є–љ–∞ вАЬ—Б—В–∞—В–Є–љ—ЛвАЭ [30], –Њ–і–љ–∞–Ї–Њ —Н—В–Њ –љ–µ —Б–Њ–≤—Б–µ–Љ —В–∞–Ї. –Ы–°–° –љ–µ—Б—В–∞—В–Є–љ–Њ–≤–Њ–є –њ—А–Є—А–Њ–і—Л —В–∞–Ї–ґ–µ —Б–љ–Є–ґ–∞—О—В —З–Є—Б–ї–Њ —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Б–Њ–±—Л—В–Є–є [31], –∞ –µ—Б–ї–Є –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е GUSTO IIb –Є PURSUIT –Є –љ–∞–Ј–љ–∞—З–∞–ї–Є—Б—М –Ы–°–° —Б –љ–µ–і–Њ–Ї–∞–Ј–∞–љ–љ–Њ–є –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Б–Њ–±—Л—В–Є–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О, —В–Њ –Є—Б—В–Є–љ–љ—Л–є —А–∞–Ј–Љ–µ—А –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –≤—Л–≥–Њ–і—Л –Њ—В –Ы–°–Ґ –±—Л–ї —В–Њ–ї—М–Ї–Њ –љ–µ–і–Њ–Њ—Ж–µ–љ–µ–љ.
–Э–µ—Б–Љ–Њ—В—А—П –љ–∞ —Н—В–Є –Њ–≥—А–∞–љ–Є—З–µ–љ–Є—П, —А–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П H.D. Aronow et al. –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—В –≥–Є–њ–Њ—В–µ–Ј—Г, —З—В–Њ —А–∞–љ–љ–µ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –ї–Є–њ–Є–і—Б–љ–Є–ґ–∞—О—Й–µ–є —В–µ—А–∞–њ–Є–Є –њ–Њ—Б–ї–µ –Њ—Б—В—А–Њ–≥–Њ –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –њ—А–Є–≤–Њ–і–Є—В –Ї —Б–љ–Є–ґ–µ–љ–Є—О –ї–µ—В–∞–ї—М–љ–Њ—Б—В–Є —Г–ґ–µ –≤ —В–µ—З–µ–љ–Є–µ –њ–µ—А–≤—Л—Е –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –љ–µ–і–µ–ї—М –Є–ї–Є –Љ–µ—Б—П—Ж–µ–≤ –ї–µ—З–µ–љ–Є—П. –С–ї–∞–≥–Њ–і–∞—А—П —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–љ–Њ–є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –Є —Е–Њ—А–Њ—И–µ–є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –ї–Є–њ–Є–і—Б–љ–Є–ґ–∞—О—Й–Є—Е —Б—А–µ–і—Б—В–≤ [32] –Є –Є—Е —Д–∞—А–Љ–∞–Ї–Њ—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –і–ї—П –≤—В–Њ—А–Є—З–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є [33], –Є—Е —А—Г—В–Є–љ–љ–Њ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –њ—А–Є –Ю–Ъ–° —П–≤–ї—П–µ—В—Б—П –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–љ—Л–Љ. –Я—А–Њ–≤–Њ–і–Є–Љ—Л–µ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Є –±—Г–і—Г—Й–Є–µ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–µ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –і–Њ–ї–ґ–љ—Л –њ—А–Є–≤–µ—Б—В–Є –Ї —В–Њ—З–љ–Њ–Љ—Г –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є—О –Њ–± –∞–±—Б–Њ–ї—О—В–љ—Л—Е –Є –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л—Е –≤—Л–≥–Њ–і–∞—Е –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Њ—В–і–µ–ї—М–љ—Л—Е –ї–Є–њ–Є–і—Б–љ–Є–ґ–∞—О—Й–Є—Е —Б—А–µ–і—Б—В–≤ –њ—А–Є —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є.
1. The LIPID Investigators. Prevention of cardiovascular events and death with pravastatin in patients with coronary heart disease and a broad range of initial cholesterol levels. // N Engl J Med, 1998; 339: 1349-57.
2. The 4S Investigators. Randomised trial of cholesterol lowering in 4444 patients with coronary heart disease: the Scandinavian Simvastatin Survival Study (4S). // Lancet, 1994; 344: 1383-89.
3. Sacks FM, Pfeffer MA, Moye LA, et al. The effect of pravastatin on coronary events after myocardial infarction in patients with average cholesterol levels. // N Engl J Med, 1996; 335: 1001-09.
4. Downs JR, Clearfield M, Weis S, et al. Primary prevention of acute coronary events with lovastatin in men and women with average cholesterol levels: results of AFCAPS/TexCAPS. Air Force/Texas Coronary Atherosclerosis Prevention Study. // JAMA, 1998; 279: 1615-22.
5. Shepherd J, Cobbe SM, Ford I, et al. Prevention of coronary heart disease with pravastatin in men with hypercholesterolemia. // N Engl J Med, 1995; 333: 1301-07.
6. Braunwald E, Antman EM, Beasley JW, et al. ACC/AHA guidelines for the management of patients with unstable angina and non-ST-segment elevation myocardial infarction: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Committee on the Management of Patients With Unstable Angina). // J Am Coll Cardiol, 2000; 36: 970-1062.
7. Ryan TJ, Antman EM, Brooks NH, et al. 1999 update: ACC/AHA Guidelines for the Management of Patients With Acute Myocardial Infarction: Executive Summary and Recommendations: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Committee on Management of Acute Myocardial Infarction). // Circulation, 1999; 100: 1016-30.
8. Dupuis J, Tardif JC, Cernacek P, Theroux P. Cholesterol reduction rapidly improves endothelial function after acute coronary syndromes: the RECIFE (reduction of cholesterol in ischemia and function of the endothelium) trial. Circulation, 1999; 99: 3227-33.
9. Stroes ES, Koomans HA, de Bruin TW, Rabelink TJ. Vascular function in the forearm of hypercholesterolaemic patients off and on lipid-lowering medication. // Lancet, 1995; 346: 467-71.
10. Lacoste L, Lam JY, Hung J, Letchacovski G, Solymoss CB, Waters D. Hyperlipidemia and coronary disease: correction of the increased thrombogenic potential with cholesterol reduction. // Circulation, 1995; 92: 3172-77.
11. Notarbartolo A, Davi G, Averna M, et al. Inhibition of thromboxane biosynthesis and platelet function by simvastatin in type IIa hypercholesterolemia. // Arterioscler Thromb, 1995; 15: 247-51.
12. Weber C, Erl W, Weber KS, Weber PC. HMG-CoA reductase inhibitors decrease CD11b expression and CD11b-dependent adhesion of monocytes to endothelium and reduce increased adhesiveness of monocytes isolated from patients with hypercholesterolemia. // J Am Coll Cardiol, 1997; 30: 1212-17.
13. Kluft C, de Maat MP, Gevers Leuven JA, Potter van Loon BJ, Mohrschladt MF. Statins and C-reactive protein. // Lancet, 1999; 353: 1274.
14. Herbert D Aronow, Eric J Topol, Matthew T Roe, et al. Effect of lipid-lowering therapy on early mortality after acute coronary syndromes: an observational study. // Lancet, 2001; 357: 1063-68
15. The GUSTO IIb Investigators. A comparison of recombinant hirudin with heparin for the treatment of acute coronary syndromes. // N Engl J Med, 1996; 335: 775-82.
16. Harrington RA. Design and methodology of the PURSUIT trial: evaluating eptifibatide for acute ischemic coronary syndromes. Platelet Glycoprotein IIb-IIIa in Unstable Angina: Receptor Suppression Using Integrilin Therapy. // Am J Cardiol, 1997; 80: 34B-38B.
17. Lauer MS, Blackstone EH, Young JB, Topol EJ. Cause of death in clinical research: time for a reassessment? // J Am Coll Cardiol, 1999; 34: 618-20.
18. Rubin DB. Estimating causal effects from large data sets using propensity scores. // Ann Intern Med, 1997; 127: 757-63.
19. Joffe MM, Rosenbaum PR. Invited commentary: propensity scores. // Am J Epidemiol, 1999; 150: 327-33.
20. Boersma E, Pieper KS, Steyerberg EW, et al. Predictors of outcome in patients with acute coronary syndromes without persistent ST-segment elevation: results from an international trial of 9461 patients. // Circulation, 2000; 101: 2557-67.
21. Lee KL, Woodlief LH, Topol EJ, et al. Predictors of 30-day mortality in the era of reperfusion for acute myocardial infarction: results from an international trial of 41,021 patients. // Circulation, 1995; 91: 1659-68.
22. Kalbfleisch JD, Prentice RL. Competing risks: the statistical analysis of failure time data. New York: John Wiley & Sons, 1980: 163-88.
23. Stenestrand U, Wallentin L. Early statin treatment following acute myocardial infarction and 1-year survival. // JAMA, 2001; 285: 430-36.
24. Schwartz GG, Oliver MF, Ezekowitz MD, et al. Rationale and design of the Myocardial Ischemia Reduction with Aggressive Cholesterol Lowering (MIRACL) study that evaluates atorvastatin in unstable angina pectoris and in non-Q-wave acute myocardial infarction. // Am J Cardiol, 1998; 81: 578-81.
25. Laufs U, La Fata V, Plutzky J, Liao JK. Upregulation of endothelial nitric oxide synthase by HMG CoA reductase inhibitors. // Circulation, 1998; 97: 1129-35.
26. Kwak B, Mulhaupt F, Myit S, Mach F. Statins as a newly recognized type of immunomodulator. // Nat Med, 2000; 6: 1399-402.
27. Krumholz HM, Radford MJ, Wang Y, Chen J, Marciniak TA. Early beta-blocker therapy for acute myocardial infarction in elderly patients. // Ann Intern Med, 1999; 131: 648-54.
28. Benson K, Hartz AJ. A comparison of observational studies and randomized, controlled trials. // N Engl J Med, 2000; 342: 1878-86.
29. Concato J, Shah N, Horwitz RI. Randomized, controlled trials, observational studies, and the hierarchy of research designs. // N Engl J Med, 2000; 342: 1887-92.
30. Siegel D, Lopez J, Meier J. Use of cholesterol-lowering medications in the United States from 1991 to 1997. // Am J Med, 2000; 108: 496-99.
31. Rubins HB, Robins SJ, Collins D, et al. Gemfibrozil for the secondary prevention of coronary heart disease in men with low levels of high-density lipoprotein cholesterol. // N Engl J Med, 1999; 341: 410-18.
32. Knopp RH. Drug treatment of lipid disorders. // N Engl J Med 1999; 341: 498-511.
33. Prosser LA, Stinnett AA, Goldman PA, et al. Cost-effectiveness of cholesterol-lowering therapies according to selected patient characteristics. // Ann Intern Med, 2000; 132: 769-79.
–Ь–∞—В–µ—А–Є–∞–ї –њ–Њ–і–≥–Њ—В–Њ–≤–ї–µ–љ –Ї.–Љ.–љ. –Ѓ.–Я. –Я–∞–≤–ї–Њ–≤—Л–Љ
–°–Є–Љ–≤–∞—Б—В–∞—В–Є–љ вАУ –Ч–Њ–Ї–Њ—А (—В–Њ—А–≥–Њ–≤–Њ–µ –љ–∞–Ј–≤–∞–љ–Є–µ)











