FGU «2nd сentral military сlinical нospital named after Mandryka P.V.»
Moscow
Modern algorithm of glaucoma treatment hasn’t undergone any essential changes during the last years, in spite of useful increase of arsenal of anti–glaucoma drugs. Now medication groups include β–blockers, prostaglandin analogs, carboanhydrase inhibitors (CAI’s), miotics, sympathomimetics and combine medicines. The role of combined drug forms is very important, because it has more evident efficacy than monotherapy. Literary review summarizes some independent clinical trials around the world, and shows the effectiveness of combination of anti–glaucoma medicines, including the long–term effects on intraocular pressure, retrobulbar blood flow, and the speed of progression of visual damage in patients with primary open–angle glaucoma.
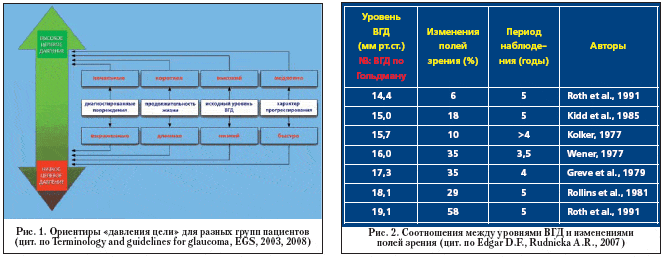
Принципы назначения гипотензивной терапии при лечении глаукомы, хотя и не претерпели значительных изменений на протяжении последнего десятилетия, тем не менее заслуживают более широкого обсуждения в связи с появлением новых фармацевтических продуктов и внедрением в клиническую практику комбинированных препаратов. Дифференцированные подходы к лечению основаны, на мой взгляд, на нескольких составляющих, среди которых принципиальное значение имеют: необходимость активного понижения уровня внутриглазного давления (ВГД) для достижения т.н. «целевого давления»; пожизненная необходимость применения глазных капель; хронический и проградиентно текущий характер болезни, и, наконец, необходимость и возможность оплачивать лечение на протяжении длительного времени с соблюдением параметров заданного режима. Среди приведенных параметров «целевое давление» является наиболее непростым ориентиром, т.к. до настоящего времени не разработано удовлетворительных и точных методик его определения [11,17,21]. Вместе с тем определены некоторые критерии, которые следует использовать для достижения безопасных уровней ВГД [34,35] (рис. 1).
Продолжительные наблюдения за больными с глаукомой убедили большинство исследователей, что низкий уровень ВГД является определяющим фактором стабилизации зрительных функций (рис. 2).
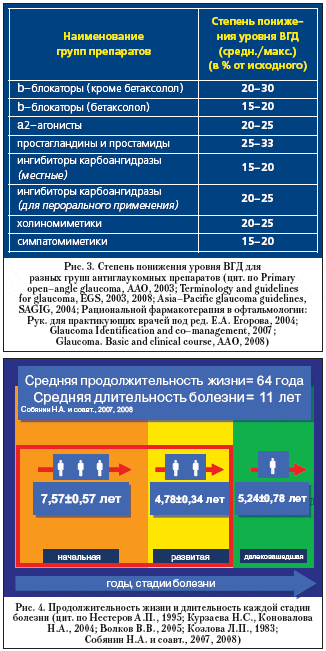
Принятыми и одобренными ориентирами снижения ВГД сегодня стали некоторые условные цифры: от 20 до 40% в зависимости от стадии болезни и ряда факторов, которые, как полагают, могут способствовать более быстрому прогрессированию болезни, а достижение приемлемых показателей офтальмотонуса предопределено в том числе и эффективностью гипотензивных лекарственных средств при монотерапии (рис. 3).
Вместе с тем глаукомная оптическая нейропатия (ГОН) отмечается и у пациентов с контролируемым уровнем ВГД. Эта доказанная клиническая особенность глаукомы свидетельствует о том, что пациенты, вероятно, обладают разной чувствительностью к повышенному уровню ВГД, или о том, что существуют иные характеристики давления, влияющие на прогрессирование болезни. Кроме этого, заявленные в рекомендациях эффективные характеристики гипотензивных препаратов значительно отличаются в каждом конкретном клиническом случае [33,36]. Так, Козлова Л.П. и соавт. (1981) указали, что на ранних стадиях болезни уровень ВГД играет роль индикатора болезни (глаукома прогрессирует даже при низких уровнях ВГД); состояние больных и ухудшение зрительных функций наступает после 50–59–летнего возраста пациента, т.е. когда болезнь продолжается от 10 и более лет. Чернявский Г.Д. и соавт. (1980) подтвердили, что при адекватном лечении и мониторинге почти у 60% пациентов зрительные функции сохраняются на протяжении более 10 лет наблюдений. Интересно, что определены такие параметры, как длительность болезни в зависимости от продолжительности жизни пациентов, свидетельствующие, что в среднем болезнь продолжается около 11 лет при длительности жизни около 64 лет [13] (рис. 4).
Такие результаты вместе с недавно опубликованными оптимальными рекомендациями Европейского глаукомного общества (2008) о приоритетах выбора терапии первой линии на усмотрение лечащего врача лишь подчеркивают необходимость более активного индивидуального мониторинга на начальных стадиях болезни, т.е. не протяжении первых 10–12 лет и пересмотра стратегии назначения препаратов т.н. первой линии. Следует также отметить, что на развитой и далекозашедшей стадиях болезни обратимые изменения структуры диска зрительного нерва маловероятны [1,2,9,10]. Наглядной иллюстрацией этому может быть информация о совокупных морфометрических изменениях архитектуры ДЗН у больных с начальной и развитой стадиями глаукомы на фоне проводимого лечения (рис. 5).
Есть и еще один аспект: нельзя не отметить и информацию о контингенте пациентов с впервые выявленной глаукомой: среди этой группы больных более 60% – это пациенты с развитой и далекозашедшей стадиями болезни. Как сообщает В.П. Еричев (2008), рассчитывать на успех монотерапии у таких больных вряд ли возможно [4]. Именно поэтому для повышения эффективности медикаментозного лечения и улучшения качества жизни был разработан ряд комбинированных препаратов, содержащих вещества, которые обладают различным механизмом гипотензивного действия и при одновременном применении которых наблюдается аддитивный эффект [8]. Наибольшее распространение получили комбинации, одной из составляющие которой стали β–адреноблокаторы, и, в частности тимолола малеат (рис. 6).
Среди указанных комбинаций важное место, в связи выраженной гипотензивной активностью, занимает сочетание β–адреноблокатора и ингибитора карбоангидразы, которое было разработано почти 12 лет назад. В настоящее время такая фиксированная комбинация, известная под названием косопт (тимолола малеат 0,5% и дорзоламид 2%, MSD, США) получила регистрацию в России. Этот антиглаукомный препарат понижает офтальмотонус в среднем на 30% от базового, а максимальное уменьшение уровня ВГД достигает 43%. Снижение ВГД начинается через 1 час после однократной инстилляции, достигает максимума через 4–6 ч и сохраняется в течение 24 ч. Рекомендуемый режим применения – 2 р/день [12].
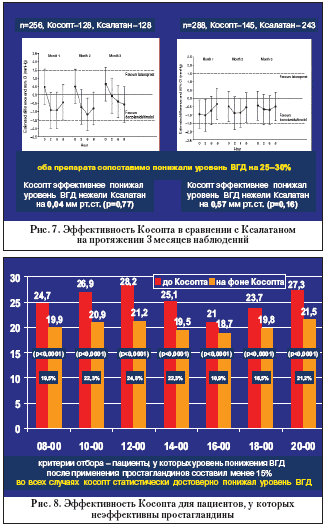
При изучении гипотензивной эффективности Косопта по сравнению с раздельным применением компонентов входящих в его состав в одном из исследований был установлен сопоставимый уровень снижения ВГД [Hutzelmann J. et al., 1998] [22]. В другом случае Bacharach J. и соавт. (2003) обнаружили, что Косопт дополнительно снизил уровень ВГД, в среднем на 1,5 мм рт.ст. (p<0,001) [16]. По данным авторов, статистически значимое усиление гипотензивного эффекта было отмечено в 83% случаев всех назначений препарата. Подтверждена эффективность косопта для снижения офтальмотонуса у пациентов с исходно высоким уровнем ВГД. Так, Henderer J.D. и соавт. (2005) указали, что при исходном уровне 37,5±1,0 мм рт.ст. (здесь и далее уровень ВГД по Гольдману) через 60 суток терапии ВГД снизилось до 21,1±0,9 мм рт.ст., т.е. более чем на 40%. В другой работе Pajic B. (2003) обнаружил, что назначение Косопта пациентам с впервые выявленной глаукомой позволило снизить офтальмотонус на 12,5 мм рт.ст. (38%) [29]. Этот же автор установил, что в случаях, если пациенты (n=891) предварительно получали монотерапию β–блокаторами или даже комбинированное лечение другими препаратами, дополнительное достоверное снижение уровня ВГД составило 5,6 и 3,4 мм рт.ст. соответственно. Автор также обобщил результаты применения максимально возможной комбинированной терапии современного этапа: он установил, что назначение комбинации Косопта с латанопростом 0,005% (Ксалатан, Пфайзер, США) привело к снижению уровня ВГД у пациентов с впервые выявленной глаукомой, не получавших до этого никакого лечения на 27 мм рт.ст. (43%). В случае, если пациенты уже применяли тимолол, то уровень ВГД снизился на 41%, а при ранее используемом Ксалатане – на 17%. Безусловный интерес представляют работы, в которых назначение Косопта сравнивается с эффективностью монотерапии препаратами простагландинового ряда, как препаратов выбора. Так, Fechtner R.D. и соавт. (2004) провели исследования в 2 группах пациентов (n=544) и установили, что Косопт лучше понижает уровень ВГД, нежели Ксалатан (на 0,04 и 0,57 мм рт.ст.). При этом авторы не нашли достоверных различий в полученных результатах (р=0,77 и р=0,16 соответственно) (рис. 7).
Ozturk F. и соавт. (2007) также не обнаружили статистически достоверных различий в окончательных параметрах офтальмотонуса у пациентов (n=65), получавших Косопт и биматопрост 0,03% (Люмиган, Аллерган, США) в течение 3 месяцев [28]. Уровень ВГД был понижен на 6,5±2,3 и 6,2±1,8 мм рт.ст., соответственно. Konstas A.G.P. и соавт. (2008) проводили многократные суточные измерения офтальмотонуса у пациентов (n=38), получавших Косопт и Ксалатан, и через 6 месяцев терапии не обнаружили статистически значимой разницы в показателях ВГД между обеими группами, при этом Косопт обладал более выраженным гипотензивным эффектом по состоянию на 10–00 и 22–00. В свою очередь, Martinez A., Sanchez M. (2007) назначали Косопт пациентам (n=31), у которых примененные ранее простагландины недостаточно эффективно понизили уровень ВГД (менее чем на 15% от исходного уровня) [26]. Во всех случаях наблюдений Косопт статистически достоверно понижал уровень ВГД (p<0,0001), что составило от 11 до 25% от первоначального уровня (рис. 8).
По мнению многих авторов, наиболее востребованной является фиксированная комбинация β–адреноблокатора и препаратов простагландинового ряда. Объяснение такой популярности в хорошей гипотензивной эффективности препаратов. Сегодня на мировом рынке представлены такие препараты, как Ксалаком (латанопрост 0,005% и тимолола малеат 0,5%, Пфайзер, США); Дуотрав (травопрост 0,004% и тимолола малеат 0,5%, Алкон, США); Ганфорт (биматопрост 0,03% и тимолола малеат 0,5%, Аллерган, США) [8]. Эти комбинации были зарегистрированы на фармацевтическом рынке несколько позднее, нежели Косопт, в связи с чем понятно желание исследователей провести сравнение гипотензивной эффективности таких лекарственных препаратов между собой.
Так, Shin D.H. и соавт. (2004) установили, что Ксалаком был более эффективен нежели Косопт при измерении уровня ВГД в 08–00, 12–00 и 16–00 на протяжении 90 суток наблюдения (n=253; р<0,025) [31]. В другом исследовании [Siesky B. и соавт., 2006], где пациенты (n=17) получали тимолол и на фоне недостаточного понижения офтальмотонуса были переведены на Косопт и Ксалаком [32], уровень ВГД был дополнительно понижен на 13,9 и 12,5% соответственно. Статистически значимой разницы между обеими группами отмечено не было (p=0,5533). В то же время Косопт достоверно увеличил объем кровенаполнения в центральной артерии сетчатки (ЦАС) (p=0,0168). Martinez A., Sanchez M. (2006) подтвердили сопоставимую степень понижения офтальмотонуса у пациентов, получавших Косопт и Ксалаком (6,9±2,9 против 6,9±3,2 мм рт.ст., p=0,766) [25]. При этом Косопт достоверно увеличил объем кровенаполнения и систолический объем в центральной и задней цилиарной артериях в отличие от Ксалакома (p=0,0001 против р=0,018).
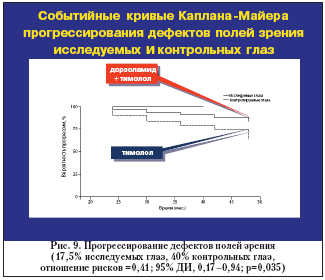
Большинство исследователей склоняются к мнению, что при лечении больных с глаукомой необходимо стремиться к улучшению кровоснабжения глаза с помощью медикаментозных средств. Такими свойствами могут обладать как дополнительные препараты (нейропротекторная терапия?), так и антиглаукомные глазные капли. Так, например, после применения дорзоламида исследователи отмечали увеличение скорости кровотока в сосудах сетчатки, поверхностных сосудах на диске зрительного нерва и в ретробульбарных сосудах, а также увеличение амплитуды глазного пульса. Противоположные результаты – отсутствие влияния дорзоламида на глазной кровоток, представленные в других исследованиях, могли быть результатом применения различных методов и дизайнов исследований [23]. Важность таких работ становится понятной вследствие необходимости прогнозирования течения болезни. Martinez A., Sanchez M. (2008) изучали эффективность влияния комбинации дорзодамида 2% и тимолола 0,5% на уровень ВГД и ретробульбарную гемодинамику в течение 4–летнего проспективного периода наблюдения у 80 пациентов с глаукомой, ранее получавших в качестве монотерапии лишь тимолол [27]. Было установлено, что при дополнительном назначении дорзоламида эффективно изменился ряд весьма важных показателей (в отличие от результатов контрольной группы). Во–первых, были получены достоверные данные дополнительного снижения уровня ВГД (на 1,1 мм рт.ст., или 5,73%; p<0,001 против контрольной группы p=0,644); во–вторых, достоверно изменился индекс резистентности в a. ophthalmica, ЦАС и короткой задней цилиарной артерии (p<0,001); и, наконец, прогрессирование болезни, т.е. изменения периферического зрения были отмечены в 17,5% в исследуемой группе в отличие от почти 40% в контрольной группе (p=0,035) (рис. 9).
Следует отметить, что обе группы пациентов относились к первой стадии болезни, а базовые показатели светочувствительности сетчатки в группе дорзоламид + тимолол были хуже, нежели в контрольной группе (–4,05 dB против –2,63dB) Такие результаты подтверждают высказанное выше предположение о необходимости назначения комбинированной терапии у пациентов с начальной стадией болезни и соответственно – более агрессивного лечения глаукомы.
Подводя итоги данного обзора, следует отметить, что достижение «целевого давления» является приоритетом современной гипотензивной терапии. Фиксированная комбинация дорзоламида 2% и тимолола малеата 0,5% обладает выраженной гипотензивной эффективностью (при назначении Косопта пациентам, не получавшим ранее другого лечения, уровень ВГД понижается на 35–40% от исходного). Кроме этого, Косопт способен дополнительно снизить уровень ВГД (на 12–25%) в случаях, когда простагландины неэффективны. Он также обладает аддитивным действием по отношению к простагландинам в том случае, если простагландины работают эффективно. Указанная комбинация обладает доказанным действием на гемодинамические показатели, стабилизация которых, как доказано, способствуют замедлению прогрессирования ГОН.

Литература
1. Волков В.В., Журавлев А.И. Диск зрительного нерва при глаукоме // Офтальм. журн.– 1982.– №5.– С. 272–276.
2. Волков В.В. Глаукома при псевдонормальном давлении. – М.: Медицина, 2001.– 350 с.
3. Волков В.В. Типичные для открытоугольной глаукомы структурно–функциональные нарушения в глазу – основа для построения ее современной классификации // Вестн. офтальмол.– 2005.– №4.– С. 35–38
4. Еричев В.П. Современные принципы гипотензивной терапии глаукомы // Сб. научн. ст. Глаукома: реальность и перспективы.– М., 2008.– С. 220–223.
5. Козлова Л.П., Спорова Н.А., Леонов С.А. и соавт. Факторы, влияющие на переход I стадии открытоугольной глаукомы в последующие // Вестн. офтальмол.– 1981. –№5. – С. 16–19.
6. Козлова Л.П., Спорова Н.А., Леонов С.А. Характеристика течения I стадии открытоугольной глаукомы // Вестн. офтальмол.–1983.– №2.– С. 14–15.
7. Курзаева Н. С., Коновалова Н. А. Динамика течения глаукомы и её использование в прогнозе эффективности диспансеризации // Сб. научн. ст. Глаукома: проблемы и решения.– М., 2004.– С. 422–423.
8. Куроедов А.В. Перспективы применения комбинированных антиглаукомных препаратов (обзор литературы) // Клин. офтальмол.– 2007.– № 4.– С. 176–181.
9. Нестеров А.П., Бунин А.Я., Кацнельсон Л.А. // Внутриглазное давление. Физиология и патологи.– М.: Наука, 1974.– 381 с.
10. Нестеров А.П., Егоров Е.А. О патогенезе глаукоматозной атрофии зрительного нерва // Офтальмол. журнал.– 1979. – №7.– С. 419–422.
11. Нестеров А.П. Глаукома.– М.: ООО «Медицинское информационное агентство», 2008.– 360 с.
12. Рациональная фармакотерапия в офтальмологии: Рук. для практикующих врачей / Е.А. Егоров, В.Н. Алексеев, Ю.С. Астахов, В.В. Бржевский, А.Ф. Бровкина и др.; под общ. ред. Е.А. Егорова. – М.: Литтерра, 2004. – 954 с.
13. Собянин Н.А., Максимов А.Г., Гаврилова Т.В. Методика оценки длительности болезненности на примере заболеваний глаукомой // Воен.–мед. журн.– 2007.– №2.– С.62–63.
14. Чернявский Г.Д., Супрун А.В., Федорова С.М. и соавт. Результаты длительного наблюдения за больными с начальной стадией первичной глаукомы // Вестн. офтальмол.– 1980.– №6.– С. 8–11.
15. Asia–Pacific glaucoma guidelines // South East Asia Glaucoma Interest Group. – 2004. – 92 p.
16. Bacharach J., Delgado M.F., Iwach A.G. Comparison of efficacy of the fixed–combination timolol/dorzolamide versus concomitant administration of timolol and dorzolamide // Ocul. Pharm. Ther.– 2003.– Vol. 19.– P. 93–96.
17. Edgar D.F., Rudnicka A.R. Glaucoma identification and co–management // Elsevier.– 2007.– 197 p.
18. Fechtner R.D., Airaksinen P.J., Getson A.J. et al. Efficacy and tolerability of the dorzolamide 2%/timolol 0.5% combination (COSOPT) versus latanoprost 0.005% (XALATAN) in the treatment of ocular hypertension or glaucoma: results from two randomized clinical trials // Acta Ophthalmol. Scand.– 2004.– Vol. 82.– P. 42–48.
19. Glaucoma. Basic and clinical course // Am. Acad. Ophthalmol. – 2008. – 258 p.
20. Henderer J.D., Wilson R.P., Moster M.R. et al. Timolol/dorzolamide combination therapy as initial treatment for intraocular pressure over 30 mm hg // J. Glaucoma.– 2005.– Vol. 14.– P. 267–270.
21. Higginbotham E.J., Lee D.A. Clinical guide to glaucoma management // Elsevier.– 2004.– 607 p.
22. Hutzelmann J., Owens S., Shedden A. et al. Comparison of safety and efficacy of fixed combination of dorzolamide/timolol and the concomitant administration of dorzolamide and timolol: a clinical equivalence study // Br. J. Opthalmol.– 1998.– Vol. 82.– P. 1249–1253.
23. Kaup M., Plange N., Niegel M., Remky A., Arend O. Effects of brinzolamide on jcular hemodynamics in healthy volunteers // Br. J. Ophthalmol.– 2004.– Vol.88.– P.257–262.
24. Konstas A.G.P., Kozobolis V.P., Tsironi S. et al. Comparison of the 24–hour intraocular pressure–lowering effects of latanoprost and dorzolamide/timolol fixed combination after 2 and 6 months of treatment ophthalmology. – 2008.– Vol. 115.– P. 99–103.
25. Martinez A., Sanchez M. A comparison of the effects of 0.005% latanoprost and fixed combination dorzolamide/timolol on retrobulbar haemodynamics in previously untreated glaucoma patients // Cur. Med. Res. Opin.–2006.– Vol. 22.– P. 67–73.
26. Martinez A., Sanchez M. Intraocular pressure lowering effect of dorzolamide/timolol fixed combination in patients with glaucoma who were unresponsive to prostaglandin analogs/prostamides Cur. Med. Res. Opin.–2007.– Vol. 23.– P. 595–600.
27. Martinez A., Sanchez M. Effects of dorzolamide 2% added to timolol maleate 0,5% on intraocular pressure, retrobulbar blood flow, and the progression of visual field damage in patients with primary open–angle glaucoma: a single–center, 4–year, open–label study // Clin. Ther. – 2008.– Vol. 30.– P. 1120–1134.
28. Ozturk F., Ermis S.S., Inan U.U. Comparison of the ocular hypotensive effects of bimatoprost and imololdorzolamide combination in patients with elevated intraocular pressure: a 6–month study // Acta Ophthalmol. Scand. – 2007.– Vol. 85.– P. 80–83.
29. Pajic B. Experience with Cosopt, the fixed combination of timolol and dorzolamide, gained in Swiss ophthalmologists offices // Cur. Med. Res. Opin.–2003.– Vol. 19.– P. 95–101.
30. Primary open–angle glaucoma. Preferred practice pattern. Limited revision // American Academy of Ophthalmology. – 2003. – 38 p.
31. Shin D.H. Feldman R.M., Sheu W–P., et al. Efficacy and safety of the fixed combination latanoprost/timolol versus dorzolamide/timolol in patients with elevated intraocular pressure // Ophthalmology.– 2004.– Vol. 111.– P. 276–282.
32. Siesky B., Harris A., Sines D., et al. A comparative fnalysis of the effects of the fixed combination of timolol and dorzolamide versus latanoprost plus timolol on ocular hemodynamics and visual function in patients with primary open–angle glaucoma // J. Ocul. Pharm. Ther.– 2006.– Vol. 22.– P. 353–362.
33. Stewart W.C., Konstas A.G.P., Nelson L.A., Kruft B. Meta–analysis of 24–hour intraocular pressure studies evaluating the efficacy of glaucoma medicines // Ophthalmology.– 2008.– Vol. 115.– № 7.– P. 1117–1122.
34. Terminology and guidelines for glaucoma // European Glaucoma Society. – 2003. – 85 p.
35. Terminology and guidelines for glaucoma // European Glaucoma Society. – 2008. – 184 p.
36. Varma R., Hwang L–J., Grunden J.W., Bean G.W. Inter–visit intraocular pressure range: an alternative parameter for assessing intraocular pressure control in clinical trials // Am. J. Ophthalmol.– 2008.–Vol. 145.– N.2.– P. 336–342.












