Yu.S. Astahov, E.L. Akopov,
N.N.Grigoreva, F.E. Shadrichev
St.–Petersburg state medical university named after I.P. Pavlov
Heidelberg retinal tomograph (HRT II) represents confocal scanning laser system intended for shooting and the analysis of three–dimensional images of researched sites of an eye bottom. The software of the device includes programs of estimation of optic nerve disc and macular zone. It is necessary to note especially, that at carrying out of research on retinal tomograph in overwhelming majority of cases there is no necessity for dilatation of a pupil, there is no flare of an eye during research. Experience of use of a tomograph enables to recommend the given device for equipment glaucoma cabinets, diabetic centers and ophthalmologic hospitals. The device is necessary and for perfection of educational process.
На протяжении многих десятков лет, а то и столетий, состояние диска зрительного нерва и сетчатки оценивалось путем офтальмоскопии. В начале ХХ века было внедрено в практику фотографирование глазного дна, а затем и стереофотографирование, что позволило перейти к архивированию объемных изображений. При этом точность измерения размеров отдельных структур по фотографиям оставалась весьма приблизительной.
Для точной и объективной оценки состояния ДЗН возможно использование нескольких приборов: конфокальных сканирующих лазерных офтальмоскопов (КСЛО), сканирующих лазерных поляриметров (СЛП) и оптических когерентных томографов (ОКТ). Принцип их работы различен: КСЛО оценивает поверхность исследуемой структуры, работа СЛП (оценивающих толщину нервных волокон) основана на задержке (двойном лучепреломлении) поляризованного лазерного излучения при прохождении сквозь исследуемые ткани, а ОКТ работает по тому же принципу, что и ультразвуковые В–сканы. Работа СЛП в значительной степени зависит от поляризационных свойств роговой оболочки, что во многих случаях заметно снижает точность исследования. ОКТ, как и КСЛО, лишен этого недостатка, однако в отличие от последнего имеет ограничение – при исследовании оценивается только один оптический срез. КСЛО же позволяет оценивать топографию всего ДЗН.
Гейдельбергский ретинальный томограф (HRT II) создан и производится в Гейдельберге (Германия, фирма Heidelberg Engineering). Он представляет собой конфокальную сканирующую лазерную систему, предназначенную для съемки и анализа трехмерных изображений исследуемых участков глазного дна. Прибор состоит из лазерного излучателя, совмещенного с детектором отраженного света, системного блока, монитора, блока питания и принтера. В качестве источника света используется диодный лазер с длиной волны 675 нм, а размеры изображений, получаемых в ходе исследования – 15х15 градусов или 384х384 пикселя. Таким образом, картина анализируется по 147456 независимым значениям высоты рельефа сетчатки в абсолютных величинах. Программное обеспечение прибора, являющееся неотъемлемой его частью, включает программы оценки ДЗН и макулы.
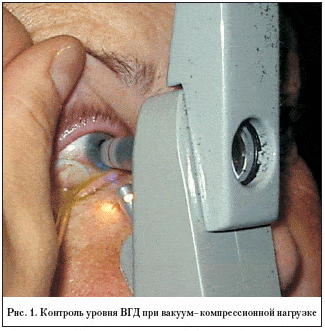
Программа оценки ДЗН предусматривает автоматическое сравнение полученных изображений при наблюдении пациентов в динамике. Эта важнейшая особенность прибора позволила нам провести исследование, целью которого явилась оценка изменений глубины экскавации ДЗН при дозированной вакуум–компрессионной нагрузке при помощи Гейдельбергского ретинального томографа. Дозированное повышение внутриглазного давления (на 10 мм рт.ст.) достигалось при помощи накладываемой на исследуемый глаз (после инстилляции 0,4% раствором оксибупрокаина) чашечки – присоски, соединенной трубочкой с вакуумным насосом. Повышение внутриглазного давления контролировалось аппланационной тонометрией исследуемого глаза по Гольдману при помощи тонометра Перкинса и регулированием уровня вакуума в системе (рис. 1).
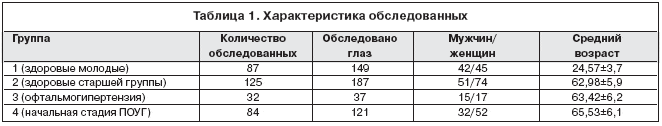
Томография диска зрительного нерва выполнялась до и во время вакуумной нагрузки. В исследование (табл. 1) включены здоровые добровольцы (группа 1 и 2), пациенты с установленным диагнозом офтальмогипертензии (группа 3) и с диагнозом начальной стадии открытоугольной глаукомы (группа 4).
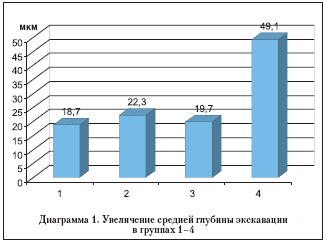
Результаты исследования показали, что повышение ВГД во всех случаях приводило к увеличению средней глубины экскавации. Средняя глубина экскавации ДЗН под действием дозированной вакуум–компрессионной нагрузки в группе 1 в среднем увеличилась на 18,7±1,98 мкм. В группе 2 увеличение составило 22,3±2,59 мкм. В группе 3 – 19,7±4,05 мкм. При сравнении данных величин разница оказалась статистически недостоверной (t=1,39, p>0,05). В группе 4 (начальная ПОУГ) средняя величина увеличения средней глубины экскавации ДЗН при нагрузке составила 49,1±8,13 мкм. При сравнении с данными в группах 2 и 3 разница оказалась статистически достоверна (t=5,38, p<0,05) (см. диаграмму 1). Следует отметить, что величина увеличения средней глубины экскавации в первых трех группах сопоставима с ошибкой метода, а в группе больных ПОУГ превосходит таковую более чем в два раза.
Согласно полученным результатам не удается проследить зависимость между возрастом пациентов и увеличением средней глубины экскавации при дозированной нагрузке: при разнице в возрасте почти в 40 лет разница в среднем увеличении средней глубины экскавации при нагрузке составила менее 4 мкм, при этом статистически данные недостоверны. Напротив, при сравнении среднего увеличения средней глубины экскавации при дозированной вакуум–компрессионной нагрузке у здоровых лиц в возрасте 54–77 лет, у пациентов с диагнозом «офтальмогипертензия» и у больных с начальной глаукомой той же возрастной группы видно, что у последних величина данного параметра в 2 с лишним раза больше.
Полученные результаты позволили сформулировать следующие выводы:
1. Гейдельбергский ретинальный томограф позволяет оценивать изменения диска зрительного нерва при вакуум–компрессионной нагрузке.
2. При увеличении средней глубины экскавации не более чем на 25 мкм можно говорить о нормальной устойчивости ДЗН. Если же средняя глубина экскавации той же степени нагрузки увеличилась более чем на 40 мкм, то устойчивость ДЗН к вакуум–компрессионной нагрузке понижена.
Режим интерактивных измерений программы оценки ДЗН томографа позволяет определять пространственные координаты любой точки полученного в ходе исследования изображения. Данное преимущество прибора позволило нам провести исследование, целью которого являлась разработка способа измерения калибра сосудов сетчатой оболочки глаза по изображениям, полученным в ходе ретинальной томографии, и оценка достоверности полученных результатов. Были проанализированы изображения, полученные при томографии 76 глаз 40 здоровых добровольцев (18 мужчин и 22 женщины) в возрасте от 18 до 35 лет. Измерены диаметры восьми сосудов сетчатки каждого глаза:
– верхне–височная артерия;
– верхне–височная вена;
– нижне–височная артерия;
– нижне–височная вена;
– верхне–носовая артерия;
– верхне–носовая вена;
– нижне–носовая артерия;
– нижне–носовая вена.
Диаметр каждого сосуда был измерен 5 раз, измерения проводились в одних и тех же участках каждого сосуда для исключения влияния на результаты исследования изменения калибра сосуда по его ходу. Все измерения проводились на участках сосудов на расстоянии 0,5–1,0 диаметра диска от края ДЗН. Проблемы при визуализации положения краев стенок сосудов возникали при недостаточно точной фокусировке и несоответствии положения исследуемого глаза и объектива томографа. После проведения повторной съемки с учетом данных факторов трудностей с определением положения края сосуда не возникало.
При вертикальном или горизонтальном расположении измеряемого сосуда диаметр определялся вычитанием показателей y2–y1 или x2–x1 соответственно. Большинство же сосудов имело косой ход. Расчет их диаметра производился по формуле
d = ° (y2–y1)2+(x2–x1)2,
где d – диаметр измеряемого сосуда, y1 и x1 – координаты начальной точки, а y2 и x2 – координаты конечной точки диаметра измеряемого сосуда. В случаях, когда значения координаты z начальной и конечной точек были различны, измерения повторялись в близлежащих участках измеряемого сосуда.
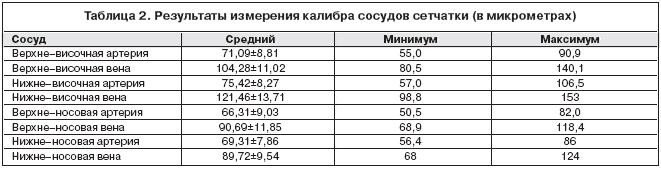
Результаты исследования показали, что стандартное отклонение при измерении диаметра сосудов в «интерактивном режиме измерений» составило от 0,6 до 16 микрон, причем в большинстве случаев величина его была в пределах 6 микрон (табл. 2).
Нельзя не отметить соотношение калибров артерий и вен сетчатки (сравнения проводились для каждого глаза отдельно). Величина его составила от 0,49 до 0,79, в среднем – 0,702±0,039.
Таким образом, измерение диаметра сосудов сетчатки при помощи ретинального томографа HRT II является достаточно информативным и точным. Полученные при таком измерении данные могут быть использованы в динамическом наблюдении за состоянием сосудов как при общей, так и при офтальмологической патологии, и, возможно, при необходимости позволят оценить адекватность проводимой терапии.
Представленный способ является единственным методом, позволяющим проводить измерение калибра сосудов сетчатки в абсолютных величинах.
Программа оценки макулы основана на так называемом профиле конфокальной интенсивности, который представляет собой распределение силы отраженного излучения в каждой точке плоскости XY вдоль оси Z. Следует отметить, что ширина профиля конфокальной интенсивности для здоровой сетчатки составляет около 300 микрон. При утолщении ткани (в частности, за счет отека) профиль конфокальной интенсивности в своей нисходящей части становится еще шире. Таким образом, чем шире профиль, тем более отечна ткань. Кроме обычных пространственных координат x, y и z, вводятся понятия индекса отека E и ширины профиля W. E=W/R, где R – интенсивность отраженного света в данной точке. Интерактивный режим измерений при исследовании макулярной области позволяет определять значения указанных величин в любой точке полученного изображения.
Нами проведено исследование, целью которого явилось сравнение результатов ретинальной конфокальной томографии и стереофотографирования сетчатки с данными клинического осмотра (офтальмобиомикроскопии при помощи асферических линз).
Было обследовано 19 пациентов (30 глаз) с сахарным диабетом 1 типа – основная группа и 30 здоровых добровольцев (52 глаза) – контрольная группа. Средний возраст в основной группе составил 33,4±2,9 лет, в контрольной – 26,9±1,8 лет. У всех пациентов, включенных в основную группу, был выявлен макулярный отек, причем в одной трети случаев отек был фокальным (10 глаз), а в остальных – диффузным (20 глаз). Больные были отобраны методом случайной выборки в рамках программы скрининга диабетической ретинопатии. Длительность диабета в среднем составляла 18,1±2,1 лет. В 52,6% случаев макулярный отек развивался при начальных стадиях непролиферативной диабетической ретинопатии, в 15,8% – при тяжелой непролиферативной диабетической ретинопатии и в 31,6% – при пролиферативной диабетической ретинопатии. В контрольную группу не включались глаза с наличием какой–либо патологии сетчатки или оптических сред.
Всем больным проводилось стандартное офтальмологическое обследование (по алгоритму Санкт–Петербургского территориального диабетологического центра), в обязательном порядке включавшее биомикроскопию сетчатки при помощи асферических линз. Кроме этого, производились 35°–стереофотографирование макулярной зоны и ретинальная томография в режиме оценки макулы.
Стереофотографирование макулярной зоны выполнялось на фундус–камере TRC–50IX фирмы «Topcon» (Япония). Использовалась слайд–пленка Agfachrome–100 фирмы «Agfa–Gevaert AG» (Германия). Исследование проводилось по стандартной методике в рамках семипольного стереофотографирования сетчатки по стандартам Early Treatment Diabetic Retinopathy Study Research Group (ETDRS). Оценивалось поле 2 (макулярная зона). Градация изменений сетчатки проводилась по классификации ETDRS (1991).
Прямым признаком макулярного отека по стереофотографиям являлось утолщение сетчатки в зоне до 1,5 диаметра ДЗН от центра фовеолы. Отложения «твердых» экссудатов, наличие патологических световых рефлексов считались косвенными признаками макулярного отека.
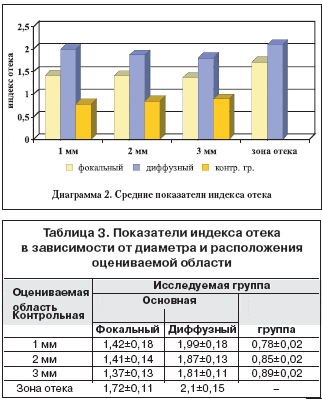
По изображениям, полученным в ходе ретинальной томографии, оценивался средний индекс отека в зоне, очерченной окружностью с центром в фовеоле и диаметром 1, 2 и 3 мм, а также непосредственно в зоне отека (табл. 3).
Как и следовало ожидать, индекс отека был существенно выше при его диффузной форме (см. диаграмму 2).
При фокальных отеках наблюдалась зависимость величины индекса отека от его локализации и диаметра исследуемой зоны. При оценке непосредственно зоны отека индекс отека был наибольшим. Чем дальше от фовеолы располагается отек, тем соответственно меньше был индекс отека при оценке в зонах диаметром 1 и 2 мм. При использовании зоны обследования диаметром 3 мм величина индекса отека не увеличивалась. Возможно, это связано с тем, что при большей площади исследования автоматически обследуется и неизмененная сетчатка, поэтому средний показатель не возрастает.
При томографии утолщение сетчатки в макулярной зоне было выявлено у всех пациентов с клинически диагностированным макулярным отеком. Точное совпадение (по локализации и характеру отека) с данными биомикроскопии обнаружилось в 90,0% случаев (27 глаз). При фокальных отеках такое совпадение наблюдалось в 80,0% случаев, а диффузных – в 95,0%. В остальных случаях макулярный отек также диагностировался по томограммам, но были отличия в локализации и/или степени его распространенности.
Таким образом, по данным ретинальной томографии наблюдаются более выраженные изменения в макулярной зоне, что, возможно, объясняется двумя причинами: либо HRT II может выявлять отеки, которые не обнаруживаются при клиническом осмотре, либо это ложноположительные результаты, связанные с начальными изменениями хрусталика, приводящими к появлению неправильного астигматизма. В контрольной группе (здоровые молодые добровольцы) патологических изменений в макулярной зоне по результатам HRT II не было выявлено. Вполне вероятно, что для оценки состояния макулы требуется определение возрастных норм коэффициента отека.
По стереофотографиям фокальный макулярный отек был выявлен в 11 случаях, из которых в двух по данным биомикроскопии с асферической линзой был диагностирован диффузный отек. Диффузный макулярный отек был обнаружен в 12 случаях, причем в одном при использовании биомикроскопии сетчатки определялся фокальный отек. В остальных случаях наличие макулярного отека было сомнительно.
Таким образом, при сравнении стереофотографирования сетчатки и биомикроскопии с асферической линзой точное совпадение по локализации и распространенности макулярного отека отмечено в 66,7%. При этом чувствительность стереофотографирования для фокальных отеков составила 81,8%, а для диффузных – 60,0%. Меньшее количество совпадений при стереофотографировании объясняется отсутствием косвенных признаков макулярного отека и качеством стереоэффекта.
Все это позволяет утверждать, что обследование больных сахарным диабетом 1 типа с макулярным отеком при помощи Гейдельбергского ретинального томографа (HRT II) показало более высокий уровень совпадений с клиническим осмотром, чем стереофотографирование макулярной зоны.
Следует особо отметить, что при проведении исследования на ретинальном томографе в подавляющем большинстве случаев нет необходимости в расширении зрачка, отсутствует засветка глаза в ходе исследования. Опыт использования Гейдельбергского ретинального томографа на кафедре офтальмологии СПбГМУ им. акад. И.П. Павлова дает возможность рекомендовать данный прибор для оснащения глаукомных кабинетов, диабетологических центров и офтальмологических стационаров. Прибор необходим и для совершенствования учебного процесса. Практикующие врачи, сравнивая свою субъективную оценку состояния оцениваемого структур глазного дна с данными, полученными в ходе ретинальной томографии, смогут значительно усовершенствовать свои навыки в оценке офтальмоскопической картины.
Литература
1. Астахов Ю.С., Джалиашвили О.А. Современные направления в изучении гемодинамики глаза при глаукоме. //Офтальмологический журнал – 1990 –№3– С. 179–183.
2. Волков В.В. Глаукома при псевдонормальном давлении.– М.:Медицина, 2001.– 351с.
3. Гамм Е.Г., Абдулкадырова М.З. «Метод оценки устойчивости зрительногоь нерва к повышению внутриглазного давления».//Вестник офтальмологии. –1989.–№ 1. с.7–9
4. Л.А. Кацнельсон, Т.И. Форофонова, А.Я. Бунин. Сосудистые заболевания глаз. – М.: Медицина, 1990. – 46, 58, 102 с.
5. М.М. Краснов. О внутриглазном кровообращении при глаукоме. // Вестник офтальмологии. – 1998 – №5.– С.5–7.
6. Azuara–Blanco A, Harris A, Cantor LB, Abreu MM, Weinland M. «Effects of short term increase of intraocular pressure on optic disc cupping». // Br J Ophthalmol. Vol. 82. p. 880–883,1998.
7. Azuara–Blanco A., Spaeth G.L. «Methods to objectify reversibility of glaucomatous cupping». // Curr. Opin. Ophthalmol. Vol. 8. p. 50–54,1997.
8. Early Treatment Diabetic Retinopathy Study Research Group. Grading diabetic retinopathy from stereoscopic color fundus photographs – an extension of the modified Airlie House classification. ETDRS report № 10 // Ophthalmology. – 1991. – V.98.– P.786–806.
9. Hudson C, Flanagan JG, McLeod D. A clinical vision science perspective of the management of diabetic macular edema. // Focus Diabetic Retinopathy. – 2001.–V.8.– P.4–9.
10. Iester M., Mikelberg F.S., Courtright P., Burk R.O. Caprioli J., Jonas J.B., Weinreb R.N., Zangwill L. «Interobserver variability of optic disk variables measured by confocal scanning laser tomography». // Am J. Ophthalmol. Vol.132. p.57–62, 2001
11. K. Joos, C. Singleton, J. Shen. Measurement of retinal vessels in images produced by the Heidelberg retinal tomography. // Proc. SPIE. – 1997. –Vol. 2971 – P. 35–39.
12. Klein R, Klein BE, Moss SE, Cruickshanks KJ. The Wisconsin Epidemiologic Study of Diabetic Retinopathy: XVII. The 14–year incidence and progression of diabetic retinopathy and associated risk factors in type 1 diabetes. // Ophthalmology.– 1998.– V.105. – P.1801–1815
13. Kinyoun J, Barton F, Fisher M, Hubbard L, Aiello L, Ferris F. Detection of diabetic macular edema: ophthalmoscopy versus photography–Early Treatment Diabetic Retinopathy Study Report Number 5.The ETDRS Research Group. // Ophthalmology. – 1989. – V.96.– P.746–750
14. F. Mikelberg, K. Wijsman, M. Schulzer. Reproducibility of topographic parameters obtained with the Heidelberg retinal tomography. // Journal of Glaucoma. – 1993. – Vol. 2 – P.101–103.
15. Morgan W.H., Chauhan B.C., Yu D.Y., Cringle S.J., Alder V.A., House P.H. «Optic disc movement with variation in intraocular and cerebrospinal pressure». // Investigative Ophthalmology and Visual Science. Vol. 43. p. 3236–3242, 2002.
16. Shiman J.S., Imaging in Glaucoma. P. 13–17. Slack. Thorofare, 1996
17. Sihota R., Gulani V., Agarwal H.C., Saxena R., Sharma A., Pandey R.M. «Variables affecting test–retest variability of Heidelberg Retina Tomograph II stereometric parameters». // J. Glaucoma. Vol.11, № 4. p. 321–328, 2002.












