V.N. Alexeev, M.A. Levko, Abu Mustafa Sabad Hasan
Authors presented data of efficiency and safety of usage of the new local carboanhydrase inhibitor– 1% brinzolamide suspension.
78 patients with POAG were examined. When IOP was evaluated after one brinzolamide solution instillation, the maximum decrease of IOP was in 3 hours after instillation.
IOP decreased by 5 mm Hg on average. Long–time usage of brinzolamide solution (1,2,3 months) was accompanied by IOP decrease by 5.2, 4.8 and 3.7 mm Hg accordingly. The most frequent complaint was «misting» after drug instillation, the intensity decreased after longer usage. As a whole, the tolerance of the drug was good.
Несмотря на прогресс в методах лечения, глаукома в нашей стране остается одной из главных причин снижения зрения и необратимой слепоты. Ее роль в этом процессе возросла за последнее десятилетие с 12 до 20% (Е.С. Либман, Е.В. Шахова, 2000). По данным H.A. Quigley (1996), число больных первичной глаукомой в мире в 2000 году составило от 66 до 105 миллионов человек, из них с двусторонней слепотой – около 6,6 млн. Пораженность глаукомой в возрасте 40–49 лет составляет 1%, увеличиваясь до 14,3 % в возрастной группе 80 лет и старше (А.П. Нестеров, 1995; W. Leydhecker,1977).
Лечение глаукомы начинают обычно с медикаментозной гипотензивной терапии. Многим больным глаукомой назначают ингибиторы карбоангидразы (ИКА).
Карбоангидраза катализирует реакцию синтеза угольной кислоты (СО2 + H2O = H2CO3). Угольная кислота впоследствии диссоциирует на гидроксильный ион и бикарбонат (H+ + HCO3–).
Ингибиторы карбоангидразы блокируют образование угольной кислоты, таким образом снижая продукцию HCO3–. В отсутствие достаточного количества ионов HCO3– увеличивается позитивный ионный градиент, что вызывает снижение секреции водянистой влаги. Это считается основным эффектом ИКА.
Первый препарат из группы ИКА – ацетазоламид был разработан в 1954 году. Тогда же была выявлена его способность снижать ВГД у больных глаукомой при пероральном приеме.
Степень переносимости гипотензивного препарата – важный показатель качества жизни для больных глаукомой. Применение пероральных ИКА сопровождается серьезными побочными явлениями. Это парестезии, желудочно–кишечные расстройства, потеря веса, депрессия, анорексия и даже потеря либидо. Также отмечаются нарушения кроветворения, включая тромбоцитопению, гемолитическую анемию, лейкопению и агранулоцитоз (А.Е. Егоров, 1996; D.L. Epstein, M.W. Grant, 1977).
Местные ИКА не оказывают значимых системных фармакологических эффектов. В настоящее время для больных доступны два ингибитора карбоангидразы местного применения. Это 2% раствор дорзоламида гидрохлорида (Трусопт) и 1% офтальмологическая суспензия бринзоламида – Азопт (А.Е. Егоров, 1996).
По данным литературы, наиболее частыми побочными эффектами этих препаратов являются жжение, зуд и покалывание в глазу, кратковременное затуманивание зрения или ощущение дискомфорта, появляющееся сразу после введения препарата. Некоторые пациенты отмечают изменение вкуса (горький, кислый или другое). Были отмечены случаи поверхностного точечного кератита, блефарита, ринита.
По данным исследований бринзоламид имеет более хорошую глазную переносимость, чем дорзоламид, что объясняется меньшей его концентрацией, оптимальным составом суспензии и физиологическим рН. Большой процент пациентов вовсе не отмечают какого–либо глазного дискомфорта при применении бринзоламида (L.H. Silver, 1998; L. De Santis, 2000).
Цель работы
Исследование гипотензивного эффекта и переносимости местного ингибитора карбоангидразы – 1% офтальмологической суспензии бринзоламида (Азопт).
Материалы и методы
Обследование проводилось у 78 взрослых пациентов с первичной открытоугольной глаукомой 1–2 стадий. Уровень ВГД до начала применения Азопта у всех больных был в пределах 25–32 мм рт.ст. (по Маклакову).
В группу не включались пациенты:
• с хроническим или рецидивирующим увеитом в анамнезе;
• перенесшие травму глаза в течение последних шести месяцев;
• имеющие дегенеративные изменения сетчатки, диабетическую ретинопатию;
• перенесшие лазерное или традиционное гипотензивное хирургическое вмешательство в течение последних 6 месяцев;
• имеющие гиперчувствительность к сульфаниламидам и ингибиторам карбоангидразы;
• страдающие тяжелой или лабильной формой сердечно–сосудистого заболевания;
• применяющие системные или офтальмологические стероиды.
Перед началом исследования все пациенты прошли стандартную «отмывку» от применявшихся ранее гипотензивных препаратов (3 недели для местных бета–блокаторов; 2 недели для местных симпатомиметиков или альфа–агонистов; 5 дней – для пероральных ингибиторов карбоангидразы).
Всем пациентам до начала лечения проводили визометрию, пробу Ширмера, биомикроскопию глаза (оценка состояния век, конъюнктивы, роговицы), измерение ВГД, офтальмоскопию, электронную тонографию, статическую периметрию (методика Humphrey 30–2). Измерялось артериальное давление (АД) и частота сердечных сокращений (ЧСС).
Затем пациентам назначался Азопт дважды в день в оба глаза в 8 часов утра и 8 часов вечера на весь период исследования (шесть месяцев).
На 1 этапе исследования проводилось исследование краткосрочного эффекта применения 1% офтальмологической суспензии бринзоламида (Азопт).
После первой инстилляции Азопта через 1, 3, 6 и 12 часов производилось измерение ВГД, биомикроскопия переднего отрезка глаз и оценка переносимости препарата (объективная и субъективная). Гипотензивный эффект препарата оценивался по степени снижения ВГД от первоначального уровня. При оценке переносимости препарата учитывались все неприятные ощущения (вкусовые изменения, туман, жжение, чувство инородного тела в глазу, и пр.), зрительные расстройства, возможность гиперергических и аллергических реакций переднего отрезка глаз.
Затем динамика изменения остроты зрения, переднего отрезка глаза и глазного дна отслеживалась еженедельно в течение первого месяца, далее в конце каждого месяца лечения. Одновременно измерялись ВГД, АД и ЧСС. В конце третьего и шестого месяцев исследования проводилась также статическая периметрия и электронная тонография.
Результаты
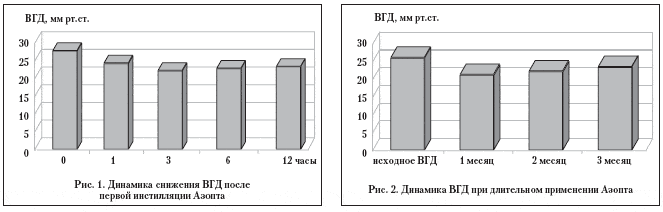
В первый день применения бринзоламида у больных исследуемой группы максимальное снижение ВГД было отмечено через 3 часа после инстилляции препарата. ВГД снизилось в среднем на 5 мм рт.ст. и практически поддерживалось на этом уровне до 12 часов после инстилляции (рис. 1).
При первом применении Азопта 12 пациентов (15 %) отметили затуманивание зрения на 5–10 минут сразу после инстилляции препарата. Чувства жжения или инородного тела не было отмечено ни в одном случае. В первый день не было выявлено каких–либо аллергических или системных реакций на Азопт.
На следующем этапе проводилось изучение эффективности и безопасности длительного применения бринзоламида. У больных исследуемой группы до начала лечения уровень истинного ВГД составлял 26,8±2,3 мм рт. ст. К концу первого месяца лечения ВГД оказалось ниже первоначального на 5,2 мм рт.ст. (21,6±2,2): второго месяца – на 4,8 (22,0±2,1) и третьего – на 3,7 мм рт.ст. (23,1±1,5) (рис. 2).
На этом этапе исследования отмечено уменьшение жалоб на «затуманивание» зрения после инстилляции препарата. Сохранялось это ощущение только у 6 пациентов. У четверых больных к концу первого месяца были отмечены отек и гиперемия конъюнктивы и соответствующие жалобы. Препарат пришлось отменить. Во время исследования не отмечено изменений остроты зрения, состояния поля зрения и глазного дна пациентов. Ни у одного больного не было выявлено отклонений в показателях АД и ЧСС.
Выводы
1% офтальмологическая суспензия бринзоламида – Азопт:
• оказывает достаточный гипотензивный эффект;
• не оказывает системного воздействия и может назначаться больным с системной патологией;
• не вызывает серьезных изменений органа зрения и хорошо переносится больными;
• при длительном (шесть месяцев) применении Азопта не отмечается существенного снижения его эффективности.
Литература
1. Егоров А.Е. Изучение гипотензивного действия и побочных эффектов ингибитора карбоангидразы дорзоламида гидрохлорида. // Вестн. офтальмол. –1996. –№2. –с.3–4.
2. Либман Е.С., Шахова Е.В. Состояние слепоты и динамика слепоты и инвалидности вследствие патологии органа зрения в России. // Тезисы докладов VII съезда офтальмологов России. –Москва, 16 – 20 мая 2000 г. –С.209–215.
3. Нестеров А.П. Глаукома. – М.: Медицина, 1995. – 256 с.
4. De Santis L.: Preclinical Overview of Brinzolamide. // Surv. Ophthalmol. 2000 Jan 1; 44 (4 Suppl. 2): 119 – 129.
5. Epstein D.L., Grant M.W.: Carbonic anhydrase inhibitor side effects // Arch. Ophthalmol. 95: 1378 – 1382, 1977
6. Leydhecker W. Diagnostische und prognostische Bewertung des erhohten i.o. Druckes // Klin. Mbl. Augenheilk. – 1977. – Bd. 170. – ? 5. – S. 679–684.
7. Silver L.H. Clinical efficacy and safety of Brinzolamide (Azopt), a new topical carbonic anhydrase inhibitor for primary open–angle glaucoma and ocular hypertension. // Am. J. Ophthalmol. 1998 Sep; 126 (3): 400–408












