Методы: хирургическое и лазерное лечение было проведено у пациентов с ретиношизисом. У пациентов со II стадией ретиношизиса было применено только лазерное лечение, с III стадией – поэтапная поступательная лазеркоагуляция сетчатки диодным лазером или оперативное лечение. При проведении хирургического лечения стандартное офтальмологическое обследование и контрольная офтальмоскопия выполнялись ежедневно в течение первых 2 нед. после операции, через 2 мес. (в сочетании с УЗИ) и каждые 6 мес. в течение 3–7 лет. Пациенты после лазерного лечения обследовались через 2 мес. и каждые 6 мес. в течение 3–7 лет после операции.
Результаты: хирургическое и лазерное лечение было проведено у 187 пациентов с ретиношизисом (187 глаз). У больных со II стадией ретиношизиса (48 глаз) было применено только лазерное лечение. У пациентов с III стадией (82 глаза) в 25 случаях ограничились несколькими сеансами поэтапной поступательной лазеркоагуляции сетчатки диодным лазером, оперативное лечение проведено у 57 пациентов (57 глаз).
Предложенная поэтапная поступательная методика лазеркоагуляции сетчатки диодным лазером как самостоятельный способ лечения ретиношизиса II стадии оказалась эффективной в 100% случаев. При III стадии процесса эффективность отмечена в 30,48% случаев.
Заключение: применение лазеркоагуляции по отграничению макулярной области до оперативного лечения позволило сохранить максимально возможную остроту зрения, а в послеоперационном периоде способствовало ускорению рассасывания интраретинальной жидкости.
Ключевые слова: ретиношизис, сегмент-овал имплантат, сетчатка.
Abstract
Efficacy of modern extrascleral and laser methods of treatment of retinoschisis
Bagdasarova Т.А.
Scientific Research Institute of Eye Diseases of the Russian Academy of Medical Sciences, Moscow
Purpose: to evaluate the efficacy of new porous segment-oval silicone implants and method of treatment of II and III stages of retinoscihis.
Methods: surgical and laser treatment was carried out in patients with retinoschisis. In patients with II stage of retinoschisis only laser treatment was performed. In III stage of retinoschisis stepped laser coagulation by diod laser or surgical treatment were used.
After surgical treatment standard ophthalmological examination and control ophthalmoscopy were carried out every day during first 2 weeks after the operation, then in 2 months (in combination with ultrasound examination) and in every 6 months during 3-7 years.
After laser treatment patients were examined in 2 months and every 6 months during 3-7 years after the operation.
Results: surgical and laser treatment were performed in 187 patients (187 eyes) with retinoschisis. In patients with II stage of retinoschisis (48 eyes) laser treatment was made, in II stage in 25 patients stepped laser coagulation and in 57 patients – surgical treatment was carried out.
Diod laser coagulation in the II stage of retinoschisis was efficient in 100% and in the III stage – in 30,48%.
Conclusion: laser coagulation prior to the surgery allowed preserving maximum possible visual acuity. Used after the surgery, it allowed faster evacuating of an intraretinal fluid.
Key words: retinoschisis, segment-oval implant, retina
Ретиношизис как самостоятельный и сложный вид витреоретинальной патологии глаза требует внимательного, методичного подхода к его диагностике и лечению. Псевдокисты сетчатки образуются при различных заболеваниях, таких как наследственные дегенерации сетчатки, диабет, травма, глаукома, увеиты, миопия и др., поэтому ретиношизис всегда бывает вторичен. Однако псевдокисты имеют сходство клинической картины и обладают одним общим признаком – расщеплением слоев сетчатки. Известно также, что такая патология, как ретиношизис, имеет многочисленные варианты клинического проявления – от нежных, едва уловимых офтальмоскопически микрокистозных дегенераций до огромных щелевидных пространств, расслаивающих сетчатку на всем ее протяжении, со складками, кровоизлияниями и разрывами. Очень часто эта форма ретиношизиса диагностируется как отслойка сетчатки. При этом может использоваться не совсем адекватная стратегия лечения, что приводит к его неудовлетворительным результатам. Отмечено также, что с каждым годом количество пациентов с кистами сетчатки увеличивается [2, 5, 6]. При этом нет единого мнения о методах лечения этой сложной витреоретинальной патологии [2, 6, 14, 15]. Большинство авторов при прогрессирующих формах ретиношизиса предпочитают применять лазерные и экстрасклеральные хирургические методы лечения [2, 4, 5, 7–10].
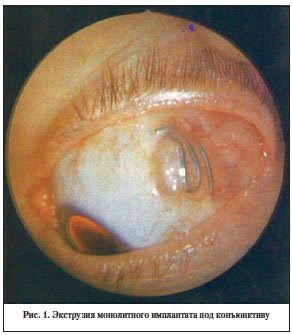
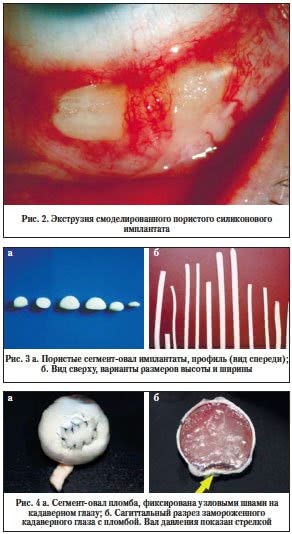
Применяемые до настоящего времени при оперативном лечении ретиношизиса III стадии монолитные силиконовые имплантаты, пористые жгуты и смоделированные имплантаты не отвечают современным требованиям и не вполне удовлетворяют офтальмохирургов. Это связано с трудностями при использовании монолитных имплантатов, поскольку для создания ими вала вдавления необходимо произвести очень значительное натяжение П-образных швов над пломбой. В этом случае материал стремится принять свое первоначальное положение, и швы часто прорезываются (рис. 1). Иногда при истонченной склере имплантат способен погружаться внутрь глаза [1]. Использование для пломбирования целых пористых жгутов, имеющих в поперечном сечении вид круга, также сопряжено с рядом негативных моментов: при фиксации их к склере П-образными швами для создания вала вдавления необходимо растягивать оба конца имплантата и одновременно завязывать швы. В результате этого также возникает излишнее напряжение в области швов, которые со временем, с учетом их дезагрегации, часто прорезываются, и происходит экструзия имплантата. При циркулярном вдавлении целостным жгутом укорочение его осуществляется произвольно, поскольку точные расчеты в каждом конкретном случае провести не представляется возможным. Поэтому даже незначительное передавливание имплантата в послеоперационном периоде может проявиться синдромом сдавления, характеризующимся повышением ВГД, цилиарными болями, отеком роговицы и резким снижением зрительных функций [1]. Моделирование имплантата из пористых жгутов во время операции осложняется наличием шероховатостей по его краям и обнажением большой площади его открытой губчатой структуры, в которую легко проникают кровь, мелкие ворсинки и бактерии. В послеоперационном периоде это может привести к нагноению имплантата, расхождению рубца конъюнктивы и рецидиву ретиношизиса. Подобные осложнения встречаются, по нашим данным, в 13,88% случаев, что требует повторных хирургических вмешательств, а также более длительного лечения (рис. 2) [3, 10, 13].
Кроме того, при разрезании имплантата, т. е. нарушении его целостности теряются такие свойства, как эластичность, прочность и сопротивляемость на разрыв. При этом очень трудно бывает дозировать воспроизведение достаточного и безопасного вала вдавления, блокирующего разрыв сетчатки.
Целью нашего исследования явились поиск и разработка более эффективных материалов и методов хирургического и лазерного лечения ретиношизиса. Для решения поставленной задачи необходимо было разработать универсальную конструкцию пористого силиконового имплантата. В этом случае потребовалось некоторым образом изменить композиционный состав известного материала, затем определить оптимальную конструкцию имплантата и апробировать способы его применения в эксперименте и клинической практике лечения ретиношизиса. Необходимо было также создать новую методику лазерного воздействия на кисты сетчатки с целью сохранения максимально возможной функции центрального зрения и профилактики возникновения вторичных дегенераций сетчатки. Также требовалось разработать клиническую классификацию ретиношизиса с учетом новых технологий лечения.
Методы
В результате многолетних исследований, клинических наблюдений и анализа осложнений при использовании моделированных пористых имплантатов и целостных жгутов нами совместно с ЗАО «Медсил» были разработаны специальные композиции силиконовых резин. Усовершенствованы методы вулканизации с применением соединений платины, обеспечивающих высокий уровень прочности. При этом оптимальная плотность изделия находилась в пределах 0,3–0,5 кг/м3. После нескольких серий испытаний на кадаверных глазах была определена универсальная форма нового поколения пористых имплантатов (патент № 61548 2006.08.14) (рис. 3, 4).
Она соответствовала форме сегмент-овала, имеющего тонкостенный наружный монолитный слой, переходящий в губчатый заполнитель внутреннего объема, с поперечным сечением в виде овала с максимальной высотой в пределах 4–6 мм, отношение высоты к ширине овала – в пределах 0,65–0,75. Эти испытания также показали, что обращенный выпуклой поверхностью к склере и фиксированный к ней узловыми швами имплантат без какого-либо растяжения создает вал вдавления оболочек глаза в 2–3 мм высотой, достаточный для блокирования разрывов сетчатки (рис. 4).
Фиксация имплантата к склере с помощью узловых швов имеет ряд преимуществ перед фиксацией его перекидными П-образными швами. Это возможность прошивания всей толщины имплантата и более поверхностных слоев склеры при наложении от 4 до 10 швов, что очень важно при истонченной склеральной оболочке. При таком способе фиксации имплантата к склере происходит более дозированная аппланация оболочек глаза.
Это связано с тем, что сегмент-овал имплантат имеет внутреннюю губчатую структуру, но покрыт со всех сторон плотной монолитной пленкой, поэтому его свойства остаются неизменными – в отличие от разрезанного жгута, который теряет свои прочностные свойства и эластичность вследствие обнажения значительной части губчатой структуры, заполненной воздухом. Поэтому разрезанный имплантат необходимо фиксировать к склере в состоянии значительного растяжения для создания им вала вдавления, блокирующего разрыв на сетчатке. В результате этого происходят излишнее сдавливание сосудов глаза, оболочек и даже изменение формы глазного яблока. Эти недостатки отсутствуют при использовании губчатых сегмент-овал имплантатов.
После положительных результатов эксперимента были проведены токсикологические и клинические исследования, получены все нормативные документы, сертификат соответствия № РОСС RU. ИМ08. В09763. Орган по сертификации рег. № РОСС RU.0001.11ИМ08. Продукция. Комплект имплантатов офтальмологических губчатых силиконовых ИГ по ТУ 9398-021-18037666-2001 из силиконовой резины МС в составе: ИГЖ-3, ИГЖ-9, ИГЖ-11, ИГТ-6, ИГС-5. Серийный выпуск. Все исследования проводились совместно с ЗАО «Медсил». Затем был налажен промышленный выпуск различных размеров сегмент-овал пористых силиконовых имплантатов.
Для лазерного лечения ретиношизиса применяли собственную методику поэтапной поступательной коагуляции диодным лазером, подробно описанную в журнале «Вестник офтальмологии» (2010, № 6). На предложенную методику получен патент (RU2441631.10.02.2012).
В результате многолетней исследовательской работы с целью создания более эффективных современных способов лечения ретиношизиса была разработана его клиническая классификация с учетом новых технологий лечения этой патологии глазного дна (табл. 1).
Всего под нашим наблюдением находилось 187 пациентов, из них 57 были прооперированы по поводу ретиношизиса III стадии. Возрастной диапазон составлял от 16 до 70 лет. Отмечено наибольшее количество пациентов с миопией – 185, из них 58 – с артифакией и 40 – с глаукомой. В 87 случаях пациенты имели диагнозы миопии и начальной катаракты, в 2 – гиперметропии.
При проведении хирургического лечения стандартное офтальмологическое обследование и контрольная офтальмоскопия выполнялись ежедневно в течение первых 2 нед. после операции, через 2 мес. (в сочетании с УЗИ) и каждые 6 мес. в течение 3–7 лет. Пациенты после лазерного лечения обследовались через 2 мес. и каждые 6 мес. в течение 3–7 лет после операции.
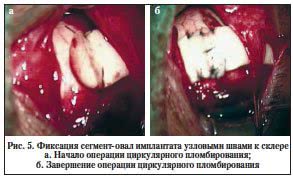
Методика операции: разрез конъюнктивы в 6 мм от лимба проводили в 4 квадрантах при циркулярном аппланационном пломбировании или в 1–2–3 квадрантах. Далее прямые мышцы брали на швы-держалки. Локализацию разрывов, площадь занимаемой кисты и маркировку их на склере осуществляли с помощью бинокулярного офтальмоскопа. Затем в некоторых случаях проводили криопексию на этих участках склеры под контролем бинокулярной офтальмоскопии до появления побеления сетчатки. Выбирали имплантат сегмент-овал по размеру, превышающему размер разрыва (разрывов) на 2 мм. После этого располагали его выпуклой поверхностью на склере и пришивали к ней несколькими узловыми швами с обеих сторон в каждом квадранте без какого-либо растяжения имплантата. Операцию заканчивали при циркулярном аппланационном пломбировании сшиванием концов имплантата двумя-тремя узловыми швами (рис. 5). Эту манипуляцию обычно проводили в нижне-внутреннем квадранте, с предварительной инъекцией в них раствора антибиотика. При сегментарном пломбировании оба конца имплантата плотно пришивали к склере одним или двумя узловыми швами и также без его растяжения. В рану засыпали сухие антибиотики широкого спектра действия, удаляли швы-держалки и зашивали конъюнктиву частым непрерывным швом. Под конъюнктиву вводили раствор антибиотика и кортикостероида.
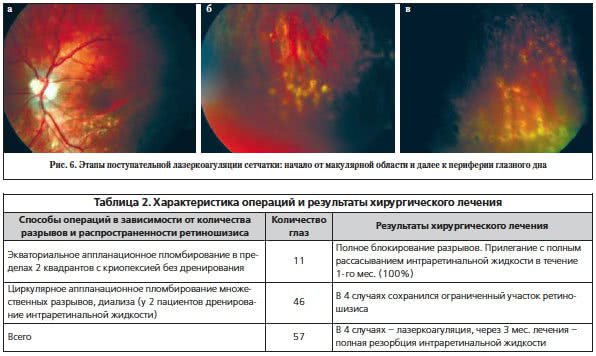
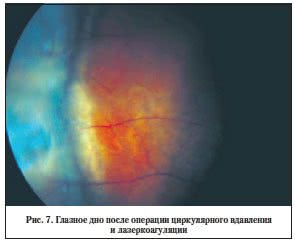
Дренирование интраретинальной жидкости проводили у ограниченного контингента пожилых пациентов при длительном существовании процесса расслоения сетчатки. В остальных случаях обходились без дренирования. Однако почти всем пациентам перед оперативным лечением была проведена лазеркоагуляция с целью отграничения макулярной области сетчатки. Затем в послеоперационном периоде по мере уплощения ретиношизиса некоторым пациентам проводили сеансы поэтапной поступательной лазеркоагуляции для ускорения рассасывания интраретинальной жидкости и восстановления зрительных функций (рис. 6, 7).
Методика поэтапного поступательного лазерного лечения ретиношизиса основана на особенностях воздействия инфракрасного излучения диодного лазера на сетчатку при длине волны от 0,87 мкм, т. е. на его способности коагулировать пигментный эпителий без каких-либо признаков изменений в сосудах и составе крови в них. Известно, что максимальное поглощение энергии при этом приходится на пигментный эпителий со сдвигом теплового эффекта в сторону хориоидеи. Успешное применение метода поэтапной поступательной лазеркоагуляции было зафиксировано у 130 пациентов с ретиношизисом II и III стадий [3].
Результаты и обсуждение
При ретиношизисе II стадии (105 глаз) при сроках наблюдения до 3 лет после использования поэтапной поступательной лазеркоагуляции получили полную резорбцию интраретинальной жидкости (100% случаев). В III стадии ретиношизиса (82 глаза) в 57 глазах (69,5%) после отграничения макулярной зоны проведены операции аппланационного пломбирования с помощью сегмент-овал имплантатов, поскольку появились новые разрывы и увеличение зоны ретиношизиса. Все операции были успешными. При этом у всех 187 пациентов (187 глаз) было проведено 57 операций (30,4%). У 130 пациентов применили только лазерное лечение, что составило 69,5%. В 25 случаях (30,48%) это был ретиношизис III стадии. Никаких осложнений при выполнении лазеркоагуляции и в отдаленные сроки наблюдения отмечено не было. Признаков вторичной дегенерации сетчатки в сроки от 3 до 5 лет также не наблюдалось. Поэтому применение метода поэтапной поступательной лазеркоагуляции начиная с отграничения макулярной области позволило сохранить максимально возможную остроту зрения у данной категории пациентов.
Никаких осложнений во время операций отмечено не было. Это объясняется тем, что имплантаты соответствовали по размерам площади разрывов, гладкая поверхность всего имплантата позволяла легко проводить его под прямыми мышцами и исключала процесс наматывания наружных оболочек на имплантат, что неизбежно происходило при использовании смоделированного имплантата с обнаженной губчатой структурой. При гладкой наружной поверхности всего имплантата не наблюдали и пропитывания его кровью. Кроме того, положение имплантата выпуклой поверхностью на склере с фиксацией его множественными узловыми швами без растяжения не вызывало излишнего сдавливания сосудов и оболочек глаза. Это подтверждалось ультразвуковым допплеровским картированием, согласно которому показатели гемодинамики были в пределах нормы. В сроки наблюдения до 7 лет ни в одном случае не было экструзий имплантатов.
Заключение. Используемая собственная методика поэтапной поступательной лазеркоагуляции в лечении ретиношизиса показала эффективность у больных с II стадией ретиношизиса в 100% случаев, с III стадией – в 30,48% случаев.
Применение силиконовых пористых сегмент-овал имплантатов для хирургического лечения ретиношизиса повысило эффективность результатов операций. Это связано с тем, что при применении имплантатов были исключены моменты моделирования и связанные с этим затруднения и осложнения в процессе выполнения операции, что приводило к отсутствию осложнений в послеоперационном периоде. Положительные результаты хирургического лечения связаны и с применением нескольких сеансов поэтапной поступательной лазеркоагуляции перед хирургическим лечением, что позволило отграничить макулярную зону, перенести зону кисты от центра сетчатки, а также уменьшить ее площадь. Такое комплексное лечение позволило сократить выполнение дренирования интраретинальной жидкости до 4,2% случаев. Следует отметить, что при выполнении циркулярного аппланационного вдавления без всякого растяжения имплантата создается оптимальный вал вдавления, не изменяющий показатели гемодинамики оперированного глаза по сравнению с аналогичными показателями другого глаза. Это также свидетельствует об эффективности предложенного метода лечения ретиношизиса.

Литература
1. Антелава Д.Н., Пивоваров Н.Н., Сафоян А.А. Первичная отслойка сетчатки. Тбилиси, 1986. С. 125–126, 128–129.
2. Астахов Ю.С., Луковская Н.Г. Ретиношизис. Диагностика, классификация, методы обследования // Вестник офтальмологии. 2004. Т. 120. № 1. С. 26.
3. Багдасарова Т.А. Анализ осложнений при использовании пористых имплантатов в лечении отслойки сетчатки // Офтальмология. 2009. Т. 6. № 1. С. 35–37.
4. Багдасарова Т.А., Ильина Т.С. Вариант оптимизации лазерного лечения ретиношизиса // Вестник офтальмологии. 2010. Т. 126. № 6. С. 43–45.
5. Луковская Н.Г., Астахов Ю.С. Ретиношизис. Собственный опыт лечения различных форм ретиношизиса // Вестник офтальмологии. 2004. Т. 120. № 4. С. 29–31.
6. Либман Е.С. Кисты сетчатки и их лечение // Актуальные вопросы офтальмологии. 1971. С. 78–83.
7. Потехин В.К., Курбатов Т.А., Столяренко О.В. Аргоновая лазеркоагуляция у больных с ретиношизисом: Тезисы доклада на VII съезде офтальмологов России. 2000. Ч. 1. С. 474–475.
8. Brokhurst R.J. Photocoagulation in congential rtinoschisis // Brit.J. Ophthalmol. 1973. Vol. 84. № 2. P. 158–165.
9. Ocun E., Cibis P. The role of photocoagulation in management of retinoschisis // Arch. Ophthalmol. 1964. Vol. 72. P. 309–314.
10. Hahn H., Lincoff H., Kreissig I. Infection after sponge implantation for scleral bacling // Am.G. Ophthal. 1979. Vol. 87 (2). P. 180-185.
11. Kreissig I. Traction Retinal Schisis // Minimal surgery Retinal Detachment.2000. Vol. P. 80–83.
12. Regillo C.D. Tasman W.S., Brown G.C. Surgical management of complication associated with х-linked retinoschisis // Arch. Ophthalmol. 1993. Vol. 111. № 8. P. 1080–1086.
13. Russo C. E., Ruiz R.S. Silicone sponge rejection // Arch. Ophthal. 1971. Vol. 85. Р. 647–650.
14. Shea M., Shepens C.L. Retinoschisis senile type A clinical report of one hundred–seven cases // Arch. Ophthalmol. 1960. Vol. 63. № 8. P. 1–9.
15. Shepens C.L. Summation and discussing retinoschisis // Retinal diseases. Philadelphia, 1996. P. 191–194.












