Ключевые слова: эндофтальмит, анти-VEGF, Луцентис, афлиберцепт, конберцепт.
Abstract
Endophthalmitis as a complication of an anti-VEGF treatment
Alpatov S.A., Schuko A.G., Malyshev V.V.
Irkutsk Department of FGU MNTK Eye Microsurgery named after acad. Fedorov S.N.
Optimal Clinic, Podgorica, Montenegro
Review of data of clinical studies and practical usage of anti-VEGF drugs is presented. Authors discuss frequency, methods оf prophylaxis and treatment of endophthalmitis which is developed after the intravitreal injections of anti-VEGF drugs.
Key words: endophthalmitis, anti-VEGF, Lucentis, aflibercept, conbercept.
В последние несколько лет наряду с прогрессом, достигнутым в исследовании патогенеза целого ряда глазных заболеваний, важным шагом явилось открытие и применение в клинике препаратов, блокирующих развитие хориоидальной неоваскуляризации посредством связывания фактора роста эндотелия сосудов. Применение анти-VEGF препаратов (VEGF — фактор роста эндотелия сосудов (vascular endothelial growth factor)) впервые позволило не только остановить развитие таких тяжелых заболеваний, как возрастная макулярная дегенерация (ВМД) (влажная форма) и диабетический макулярный отек, но и в ряде случаев улучшить зрение у больных, ранее обреченных на слепоту. Интравитреальные инъекции стали рутинной практикой, которая выполняется не только по зарегистрированным показаниям, но и off-lable, не только в условиях операционной, но и в качестве офисной процедуры. Понятно, что по мере дальнейшего роста количества инъекций неизбежно будет возрастать и количество осложнений. Поскольку многим пациентам требуются многократные инъекции в течение долгого времени, соответственно, пропорционально увеличивается и их совокупный риск. Хотя серьезные осложнения интравитреальных инъекций отмечаются крайне редко [11, 14, 16], все они, тем не менее, требуют глубокого анализа с целью их профилактики и эффективной коррекции.
Несомненно, эндофтальмит является одним из самых страшных осложнений различных внутриглазных вмешательств. Частота инфицирования полости глаза при интравитреальных инъекциях мала и редко превышает 0,05%, или 1 случай на 2000 инъекций [7, 16]. Хотя риск возникновения эндофтальмита минимален, однако даже и один такой случай может быть страшной трагедией как для пациента, так и для врача.
Первые случаи эндофтальмита после интравитреальных инъекций были описаны задолго до анти-VEGF эры при использовании пневморетинопексии для лечения отслойки сетчетки [20], интравитреальном введении ганцикловира в лечении цитомегаловирусного ретинита и инъекциях триамцинолона ацетонида по самым разным показаниям.
По данным R. Jager et al. (2004) [11], которые проанализировали около 15 тыс. интравитреальных инъекций различных терапевтических агентов, распространенность эндофтальмита составляла на тот момент 0,2%.
Исследования не выявили достоверной разницы в частоте развития эндофтальмита между различными анти-VEGF агентами. Пегаптаниб (Macugen) был первым анти-VEGF препаратом, получившим в 2004 г. разрешение на применение для лечения влажной формы ВМД. Частота возникновения эндофтальмита при его введении во время клинических исследований составила от 0,16 до 0,06% [11, 19]. Сравнимы оказались и данные, полученные в проспективных исследованиях по оценке эффективности применения ранибизумаба (MARINA, PIER, FOCUS, ANCHOR и SAILOR [2, 3, 15], где частота развития эндофтальмита составила 0,05%. При оценке эффективности и безопасности нового китайского аналогичного афлиберцепту анти-VEGF препарата conbercept в исследовании AURORA в течение 1 года лечения 122 пациентов с влажной ВМД отмечен только 1 случай эндофтальмита [12]. Следует отметить, что более поздние исследования дают гораздо меньшую частоту внутриглазного инфицирования. Так, в исследовании HORIZON, которое явилось продолжением 24-месячных исследований MARINA, ANCHOR и FOCUS еще на 2 года до 4 лет, зафиксирован только 1 случай эндофтальмита на 3552 инъекции ранибизумаба [18]. В отчете об исследовании COPERNICUS у 122 пациентов, леченных на протяжении 2 лет инъекциями афлиберцепта, об эндофтальмите не упоминается вообще [10]. Вероятно, причины этого – минимизация процедуры подготовки препарата к инъекции, а также совершенствование технологии введения.
Для лучшего понимания причин развития гнойного воспаления в глазу особый интерес представляют прямые сравнительные исследования анти-VEGF препаратов. Они проводятся примерно в равных условиях и позволяют получить более достоверные данные сравнения эффектов исследуемых препаратов. В большинстве из них не выявлено достоверной зависимости развития эндофтальмита от вида анти-VEGF препарата. Так, при сравнении безопасности применения ранибизумаба и афлиберцепта в 2-годичном исследовании VIEW было отмечено 3 случая (1%) эндофтальмита при использовании ранибизумаба и также 3 случая (1%) при использовании афлиберцепта в дозе 2 мг в течение 1-го года. В течение 2-го года исследования случаев эндофтальмита не было отмечено ни в одной группе [9]. Не наблюдалось ни одного случая эндофтальмита при сравнении ранибизумаба и бевацизумаба в мультицентровом независимом исследовании IVAN, которое проводилось в Великобритании на протяжении 2-х лет. Единичные случаи увеита отмечены в обеих группах применения препаратов [5].
В широко известном независимом исследовании CATT, которое проводилось в США в течение 2-х лет и имело целью прямое сравнение эффективности и безопасности 2-х препаратов, выпускаемых одной фирмой: ранибизумаба и бевацизумаба, эндофтальмит развился у 11 больных (0,06 % от общего числа инъекций), причем в 4-х из этих случаев использовался ранибизумаб и в 7-ми – бевацизумаб (р=0,38). Интересно, что у 10 из этих 11 пациентов инъекции проводились ежемесячно. И это кажется логичным – чем больше пациент получает инъекций, тем больше риск осложнений [13].
Известно, что Авастин (бевацизумаб) выпускается во флаконах, предназначенных для внутривенного введения. В офтальмологической практике обычным является расфасовка препарата из оригинального флакона в несколько шприцев непосредственно для внутриглазного введения. Деление содержимого флакона проводится как в относительно стерильных аптечных условиях, так и, нередко, непосредственно в офисе. Несомненно, в ходе данной процедуры может быть нарушена стерильность лишенного консервантов лекарства, и возникает риск его контаминации, что, в свою очередь, и может стать одной из вероятных причин постинъекционных воспалительных явлений, в частности, экзогенного гнойного эндофтальмита. В США разработаны строгие правила проведения процедуры деления препарата на дозы, включающие жесткие требования прежде всего к аптеке. Этапность процедуры изложена в главе 797 Фармакопеи США и включает целый ряд требований, начиная от идентификации препарата, применения специальных клапанных переходников, проведение контрольных посевов содержимого шприцев уже после деления и т. д. Другой возможный вариант, обеспечивающий безопасность использования бевацизумаба, – применение содержимого одного оригинального флакона только для одного пациента.
Ни для кого не секрет, что деление содержимого стандартного флакона на несколько доз нередко происходит при лечении и ранибизумабом, и афлиберцептом. Соответственно, опасность инфицирования раствора при этом актуальна и для них.
Проведя более 4 тыс. интравитреальных инъекций анти-VEGF препаратов в Иркутском филиале МНТК «Микрохирургия глаза им. С.Н. Федорова» и в клинике «Оптимал» в Подгорице (Черногория), нам во всех случаях удалось избежать этого. Тщательная профилактика любой возможности инфицирования, строгое соответствие существующим стандартам, на наш взгляд, позволяют предотвратить внутриглазное воспаление, связанное с интравитреальной инъекцией.
В настоящее время после интравитреальной инъекции, как правило, в течение нескольких дней применяются инстилляции антибиотиков. Однако многие авторы сообщили, что использование антибиотиков не только не снижает уровень эндофтальмитов, но может даже увеличить их риск. Например, в исследовании, проведенном в Иране, из 5901 пролеченного глаза 68% в постинъекционном периоде получали антибиотики. В ходе наблюдения отмечалось 6 случаев эндофтальмита (0,10%). Причем абсолютно все пациенты с эндофтальмитом получали антибиотики. Среди больных, не получавших антибиотики, эндофтальмитов не было зарегистрировано [8]. В другой серии наблюдений, состоявшй из 15 895 инъекций (как анти-VEGF агентов, так и триамцинолона ацетонида), также сообщили о более высокой частоте развития эндофтальмита именно у пациентов, получавших местно антибиотики, в отличие от больных, их не получавших [6]. В крупном клиническом исследовании DRCRnet в серии 8027 интравитреальных инъекций уровень эндофтальмита был хотя и недостоверно, но выше в группе больных, получавших антибиотики, чем в группе пациентов, которые антибиотики не получали (0,13 против 0,03%, р=0,25) [3]. Более того, является очевидным, что местное использование антибиотиков в ходе неоднократных интравитреальных инъекций может изменить флору конъюнктивы [23] и осложнить дальнейшие лечебные мероприятия. Основываясь на этих и других данных, ряд авторов предлагают отказаться от использования антибиотиков в пользу антисептиков [22].
Из других факторов, которые могли бы влиять на развитие внутриглазной инфекции, представляется существенным рассмотрение вопроса о месте выполнения инъекции – в стационаре или в офисе. Исследования, основанные на анализе 12 249 инъекций, выполненных одним и тем же хирургом в Австралии, показали значительно более низкий уровень эндофтальмита в том случае, когда инъекция была выполнена в условиях стерильной операционной, а не в офисе [1]. Напротив, сравнение 2-х групп больных (одна – в США, другая – в Италии) показало, хотя и недостоверно, но более высокую частоту этого осложнения при выполнении инъекций в операционной стационара по сравнению с условиями медицинского офиса клиники (0,065 против 0,035%) [21].
Проблемы профилактики гнойного воспаления глаза многократно обсуждались. Представлены многочисленные рекомендации, суть которых сводится к одному – строжайшая профилактика возможного инфицирования полости глаза. Многими исследованиями доказано, что этиологическим фактором экзогенного эндофтальмита является, как правило, флора конъюнктивального мешка и реснитчатого края век. Существуют 4 основных пути проникновения микроорганизмов в полость глаза:
1. Затекание инфицированного содержимого конъюнктивальной полости в переднюю камеру через парацентез роговицы.
2. Занос с вводимой в полость глаза контаминированной инъекционной иглой.
3. Рефлюкс содержимого конъюнктивальной полости через инъекционный канал.
4. Инфицирование препарата при набирании лекарства в шприц.
Исходя из этого, меры профилактики, на наш взгляд, должны заключаться в следующем:
• обрабатывать антисептиком (Повидон-Йод) кожу вокруг глаза, краев век, ресниц, промывать конъюнктивальную полость;
• избегать деления препарата на дозы;
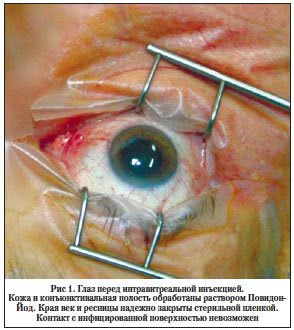
• закрывать реснитчатый край век с помощью стерильных салфеток и блефаростатов (рис. 1);
• отказаться от выполнения парацентеза;
• исключить касание иглой края век и ресниц;
• не выполнять инъекции при наличии острого внутриглазного воспаления;
• не делать инъекции при наличии воспаления периокулярной зоны;
• смещать конъюнктиву перед введением иглы с целью последующего закрытия ею раневого канала;
• выполнять вкол под углом к поверхности глаза для создания клапанного механизма закрытия раны;
• использовать один шприц только для одного пациента;
• проводить контрольный осмотр на следующий день после инъекции;
• информировать больных о возможном риске осложнений.
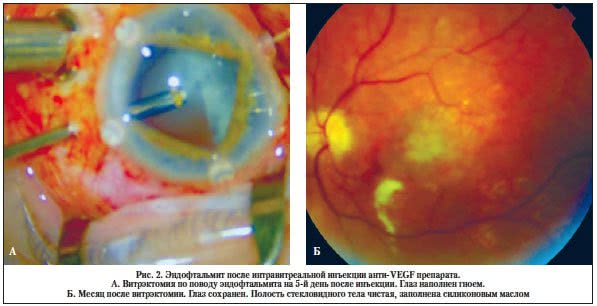
Следует подчеркнуть, что врач, выполняющий интравитреальные инъекции, всегда должен быть готов к тому, чтобы при появлении признаков эндофтальмита немедленно начать его интенсивное лечение, включая интравитреальное введение антибиотиков, а в случае их неэффективности направить пациента для выполнения экстренной витрэктомии с силиконовой тампонадой полости стекловидного тела. Опыт лечения пациентов с постинъекционным эндофтальмитом, направленных из других клиник, в Иркутском филиале МНТК «Микрохирургия глаза» им. акад. С.Н. Федорова» показывает, что чем быстрее направлен пациент на операцию, чем активнее начато лечение, тем больше шансов на сохранения и органа, и его функций (рис. 2).
Теоретически применение лекарств с более длительным сроком действия и, соответственно, уменьшение общего количества инъекций также должны способствовать уменьшению количества случаев внутриглазного инфицирования. В связи с этим введение в клиническую практику препаратов афлиберцепта и конберцепта (сonbercept) внушает некоторый оптимизм. Очень серьезным шагом по обеспечению безопасности лечения является и выпуск ранибизумаба (Луцентис) непосредственно в шприцах для внутриглазных инъекций. Это полностью исключает промежуточную процедуру набирания лекарства из флакона в шприц и значительно повышает безопасность процедуры.
Таким образом, крупномасштабные исследования и клинический опыт показали, что эндофтальмит является достаточно редким осложнением интравитреальных инъекций анти-VEGF препаратов. Строгое соблюдение правил введения лекарств в стекловидное тело позволяет заметно снизить риск развития гнойного воспаления глаза, хотя полностью избежать его, наверное, невозможно.
Литература
1. Abell R., Kerr N., Allen P., Vote B. Intravitreal injections: is there benefit for a theatre setting? // Br. J. Ophthalmol. 2012. Vol. 96. P. 1474–1478.
2. Antoszyk A., Tuomi L., Chung C., Singh A. FOCUS Study Group. Ranibizumab combined with verteporfin photodynamic therapy in neovascular age-related macular degeneration (FOCUS): Year 2 results // Am J Ophthalmol. 2008. Vol. 145. P. 862–874.
3. Bhavsar A.R., Stockdale C.R., Ferris F.L. et al. Update on risk of endophthalmitis after intravitreal drug injections and potential impact of elimination of topical antibiotics // Arch Ophthlamol. 2012. Vol. 130. P. 809–810.
4. Brown D., Michels M., Kaiser P. et al. ANCHOR Study Group. Ranibizumab versus verteporfin photodynamic therapy for neovascular age-related macular degeneration: Two-year results of the ANCHOR study // Ophthalmology. 2009. Vol. 1 (16). Р. 57–65.
5. Chakravarthy U., Harding S., Rogers C. et al. Alternative treatments to inhibit VEGF in age-related choroidal neovascularisation: 2-year fi ndings of the IVAN randomised controlled trial // Lancet. 2013. Vol. 382. P . 1258–1267.
6. Cheung C., Wong A., Lui A. et al. Incidence of endophthalmitis and use of antibiotic prophylaxis after intravitreal injections // Ophthalmology. 2012. Vol. 119. P. 1609–1614.
7. Eifrig C., Flynn H., Scott I.,et al. Acute-onset postoperative endophthalmitis: Review of incidence and visual outcomes (1995-2001) // Ophthalmic Surg Lasers. 2002. Vol. 33. P. 373–378.
8. Falavarjani K., Modarres M., Hashemi M. et al. Incidence of acute endophthalmitis after intravitreal bevacizumab injection in a single clinical center // Retina. 2013.Vol. 33. P. 971–974.
9. Heier, J., Brown D., Chong V. et al. Intravitreal Aflibercept (VEGF Trap-Eye) in Wet Age-related Macular Degeneration // Ophthalmology. 2012. Vol. 119. P. 2537–2548.
10. Heier J., Clark W., Boyer D. Intravitreal Aflibercept Injection for Macular Edema Due to Central Retinal Vein Occlusion: Two-Year Results from the COPERNICUS Study // Ophthalmology. 2014. Vol. 121. P. 1414–1420.
11. Jager R., Aiello L., Patel S., Cunningham E. Risks of intravitreous injection: a comprehensive review // Retina. 2004. Vol. 24. P. 676–698.
12. Li X., Gezhi Xu G., Wang Y. et al. Safety and Efficacy of Conbercept in Neovascular Age-Related Macular Degeneration. Results from a 12-Month Randomized Phase 2 Study: AURORA Study // Ophthalmology. 2014.
13. Martin, D., Maguire М., Fine S. et al. Ranibizumab and Bevacizumab for Treatment of Neovascular Age-related Macular Degeneration Two-Year Results // Ophthalmology. 2012. Vol. 119. P. 1388–1398.
14. Peyman G., Lad E., Moshfeghi D. Intravitreal injection of therapeutic agents // Retina. 2009. Vol. 29. P. 875–912.
15. Rosenfeld P., Brown D., Heier J. et al. Ranibizumab for neovascular age-related macular degeneration // N Engl J Med. 2006. Vol. 355. P. 1419–1431.
16. Sampat K., Garg S. Complications of intravitreal injections // Curr Opin Ophthalmol. 2010. Vol. 21. P. 178–183.
17. Scott I., Flynn H. Reducing the risk of endophthalmitis following intravitreal injections // Retina. 2007. Vol. 27. P. 10–12.
18. Singer M., Awh C., Sadda S. et al. HORIZON: An Open-Label Extension Trial of Ranibizumab for Choroidal Neovascularization Secondary to Age-Related Macular Degeneration // Ophthalmology. 2012. Vol. 119. P. 1175–1183.
19. Singerman L., Masonson H., Patel M. et al. Pegaptanib sodium for neovascular age-related macular degeneration: Third-year safety results of the VEGF Inhibition Study in Ocular Neovascularisation (VISION) trial // Br J Ophthalmol. 2008. Vol. 92. P. 1606–1611.
20. Tornambe P., Hilton G. and the Retinal Detachment Study Group. Pneumatic retinopexy. A multicenter randomized controlled clinical trial comparing pneumatic retinopexy with scleral buckling // Ophthalmology. 1989. Vol. 96. Р. 772–784.
21. Tabandeh H., Boscia F., Sborgia A. et al. Endophthalmitis associated with intravitreal injections: office-based setting and operating room setting // Retina. 2014. Vol. 34. P. 1823.
22. Wykoff C., Flynn H. Jr, Rosenfeld P. Prophylaxis for endophthalmitis following intravitreal injection: antisepsis and antibiotics // Am J Ophthalmol. 2011. Vol.152. P.717–719.
23. Yin V., Wesibrod D., Eng K. et al. Antibiotic resistance of ocular surface flora with repeated use of a topical antibiotic after intravitreal injection // JAMA Ophthalmol. 2013. Vol. 131. P. 456–461.












