Yu.S. Astakhov, A.G. Zalevskaya, I.A. Karpova, Yu.Yu. Sivas, F.E. Shadrichev
St.-Petersburg State Pavlov Medical University, St.-Petersburg Territoral Diabetology Center
Purpose. To estimate the value of several risk factors that could influence diabetic retinopathy progression in type 2 diabetic patients after switching to insulin therapy.
Methods. 238 type 2 diabetic patients were included in the study. Complete ophthalmologic examination was performed before and in 1 year after insulin therapy start. The retinopathy level was established according to ETDRS (1991) classification. Diabetes compensation was estimated by HbA1c level. Statistical analysis was performed using step-wise method of regression analysis.
Results. It was concluded that diabetic retinopathy progression in type 2 diabetic patients after switching to insulin therapy is most strongly influenced by: initial DR level, body weight index, diabetes duration, diabetes compensation (HbA1c level), arterial hypertension (systolic pressure level)
Сахарный диабет (СД) является одной из ведущих причин слепоты в развитых странах, причем на диабетическую ретинопатию (ДР) приходится до 70% случаев [3,13,59]. Считается, что у подавляющего большинства пациентов потерю зрения, связанную с ДР, можно предотвратить [46].
Сахарный диабет 2 типа составляет почти 90% от общего числа больных диабетом. Его распространенность постоянно растет в связи с увеличением продолжительности жизни, распространением «диабетогенного» образа жизни (гиподинамия, высококалорийное питание, ожирение) и совершенствованием методов диагностики диабета.
Часто у больных СД 2 типа ретинопатия обнаруживается в момент установления основного диагноза, а иногда вначале диагностируется поражение сетчатки, а затем и диабет. Имеются данные о наличии ретинопатии даже у лиц с нарушенной толерантностью к глюкозе в 1–8% случаев [6,60]. Примерно у 2/3 больных СД 2 типа признаки ретинопатии выявляются через 15–20 лет после начала заболевания, при этом у пятой части пациентов — уже в пролиферативной стадии [7,55]. По данным И.А. Карповой (2001), при рутинном выявлении СД (по обращаемости) в Санкт–Петербурге диабетические изменения сетчатки определялись у 28,6% больных СД 2 типа [8]. B. Zinman (1997) [61] выявил диабетическую ретинопатию у 25% больных с впервые установленным диагнозом СД 2 типа, а у больных, обследованных в рамках UKPDS1, ее распространенность была еще выше — 37% [57,58]. Поскольку подавляющее большинство больных диабетом — это пациенты с СД 2 типа, именно они определяют количество обращений к офтальмологу, в том числе для выполнения лазеркоагуляции.
Многочисленные исследования выявили прямую зависимость между степенью компенсации СД и сроками возникновения и темпами прогрессирования макро– и микрососудистых осложнений [16,17,19,20,27,38,45]. В связи с этим достижение компенсации нарушений углеводного обмена является важнейшим звеном в комплексе мероприятий, направленных на предотвращение возникновения и прогрессирования поздних осложнений диабета [59].
Лечение больных СД 2 типа включает диетотерапию, применение пероральных сахароснижающих препаратов (ПСП) или инсулина. Инсулинотерапия (ИТ) до сих пор остается противоречивым аспектом лечения больных СД 2 типа, что обусловлено отсутствием единой концепции в понимании этиологии и патогенеза данного типа диабета и продолжающейся дискуссией о том, что является первичным дефектом — снижение секреции инсулина или инсулинорезистентность [2]. В то же время даже при помощи максимальных доз ПСП далеко не всегда удается достичь нормогликемии. По данным различных авторов, вторичная резистентность к пероральным препаратам, связанная со снижением остаточной секреции инсулина, встречается у 5–50% больных, страдающих СД 2 типа [10,11]. C.–C. Chow с соавторами (1995) обнаружили, что через 10 лет лечения ПСП менее чем у 50% больных СД 2 типа контроль гликемии остается удовлетворительным, а следовательно, появляется необходимость в терапии инсулином [23]. По результатам исследования А.М. Мкртумяна с соавторами (2001), 40% больных СД 2 типа нуждаются в инсулинотерапии [11], а по данным Американской диабетической ассоциации (1995) таких пациентов значительно больше [19].
Показаниями для назначения лечения СД 2 типа инсулином являются: отсутствие компенсации сахарного диабета при использовании диетотерапии в сочетании с ПСП, особенно в сочетании с тяжелыми поздними осложнениями диабета или наличие у больного противопоказаний к назначению ПСП [10,19,22].
Существует множество причин (чаще психологических, чем объективных), из–за которых инсулинотерапия при СД 2 типа зачастую назначается слишком поздно и рассматривается, как «последняя возможность» в лечении [10]. Учитывая гетерогенность СД 2 типа, в ряде случаев инсулин должен назначаться достаточно рано [11].
Говоря о патофизиологических аспектах инсулинотерапии больных СД 2 типа, следует отметить, что она в определенной степени воздействует на каждое из трех главных звеньев патогенеза: недостаточность секреции инсулина, избыточную продукцию глюкозы печенью и уменьшение периферической утилизации глюкозы [5,10].
Большая частота сосудистой патологии у больных СД 2 типа, возможно, связана с инсулинорезистентностью. Связь между инсулинорезистентностью и совокупностью нарушений, включающих дислипидемию, артериальную гипертензию, андроидное ожирение, обозначают, как метаболический синдром или «синдром X».
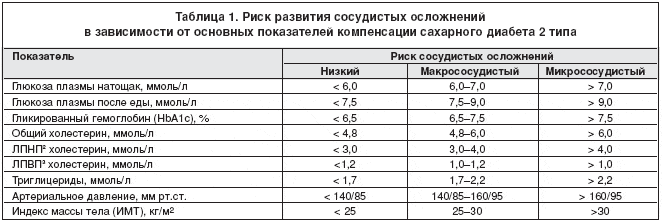
Современная стратегия ведения больных СД 2 типа рекомендует методы лечения, направленные на устранение гипергликемии и артериальной гипертензии, достижение и поддержание массы тела, близкой к идеальной, устранение нарушений липидного обмена, предупреждение возникновения или прогрессирования микро– и макрососудистых осложнений и их лечение. В 1999 году Международная Федерация диабета опубликовала критерии оценки риска развития осложнений в зависимости от степени компенсации СД [5,28] (табл. 1).
Многие авторы сообщают о прогрессировании ДР у пациентов со 2 типом СД после перевода на ИТ, которое встречается, по различным данным, в 26,3–66,7% случаев [30–34,53,54,56]. По мнению исследователей, это может быть объяснено рядом причин: тяжелым поражением сетчатки к моменту перевода, длительно существующим высоким уровнем гипергликемии или его резким снижением, большой длительностью СД, высоким уровнем АД и наличием нефропатии [30,33,51,52,53,56]. В то же время рядом авторов были получены данные о том, что перевод на ИТ не влияет на состояние сетчатки у больных СД 2 типа [18,27,29,47].
Целью данной работы было определение факторов риска прогрессирования ретинопатии у больных СД 2 типа после перевода на ИТ.
Методы обследования и характеристика исследуемых групп. Все больные проходили стандартное офтальмологическое обследование, в обязательном порядке включавшее в себя биомикроскопию сетчатки с применением асферических линз. Части больных выполняли семипольное стереофотографирование стандартных полей сетчатки на ретинальной камере TRC–50IX фирмы TOPCON (пленка Agfachrome–100). Для оценки тяжести поражения сетчатки использовалась итоговая классификация диабетической ретинопатии ETDRS4 (табл. 2).
Для определения состояния сетчатки вычисляли средний уровень ретинопатии по шкале ETDRS (для обоих глаз). Оценка глазного дна производилась до перевода на инсулинотерапию и через год после ее начала. Если при повторном осмотре появлялись признаки ретинопатии или она переходила на следующую стадию, то такое состояние расценивалось, как прогрессирование. Все данные заносились в специально разработанную карту наблюдения.
В исследование было включено 238 больных СД 2 типа, переведенных с ПСП на инсулинотерапию. Подавляющее большинство обследованных (84%) составляли женщины.
Компенсацию нарушений углеводного обмена оценивали по уровню гликированного гемоглобина (HbA1c). Характеристика больных и результаты исследования основных показателей (исходных и через 1 год ИТ) представлены в таблице 3.
Для обработки статистических данных использовался пошаговый метод регрессионного анализа (SPSS 10.1 для Windows, 2000), который позволил построить модель зависимости прогрессирования диабетической ретинопатии от различных факторов. Сравнение средних показателей в группах с наличием прогрессирования и без такового проводили с применением t–критерия Стьюдента (для выборок с неравными дисперсиями по критерию Ливиня вводилась поправка на неравенство дисперсий).
Результаты и их обсуждение. При осмотре больных через год после перевода на инсулинотерапию прогрессирование диабетической ретинопатии было выявлено у 39,9%, причем в 8,8% случаев – на два и более уровней по шкале ETDRS. В течение первого года инсулинотерапии отмечалось двукратное увеличение доли именно тяжелых форм диабетической ретинопатии. Распределение больных по стадиям ДР представлено на рис. 1. Уровни пролиферативной ретинопатии (61–90) объединены (с учетом малого (n=15) количества наблюдений).
Анализ полученных данных
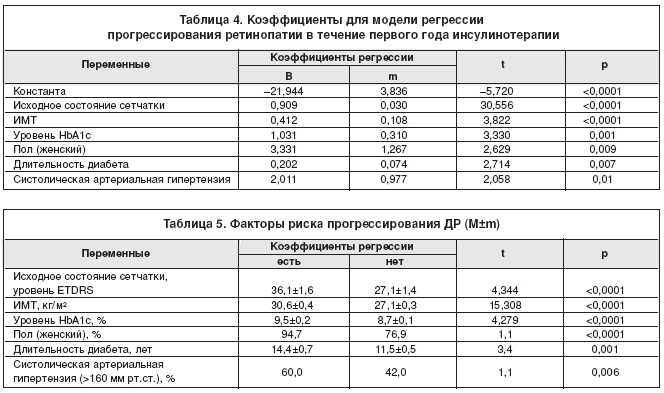
При анализе прогрессирования ДР через год инсулинотерапии модель регрессии (F=327,83; p<0,0001) объясняется на 89,5% (коэффициент детерминации R2=0,845; его статистическая значимость – 0,03). В модель регрессии вошло шесть значимых факторов, с которыми взаимосвязано прогрессирование ДР, коэффициенты для модели регрессии и значимость каждого фактора представлены в табл. 4.
Таким образом, основными факторами, влияющими на прогрессирование ретинопатии, являются исходное состояние сетчатки, ИМТ, уровень HbA1с, длительность СД и наличие систолической артериальной гипертензии. Что касается полученных данных о влиянии пола (при статистическом анализе женский пол оказался значимым фактором прогрессирования ретинопатии, p=0,009) на ухудшение состояния сетчатки у больных с СД 2 типа после перевода на инсулинотерапию – возможно, это связано с абсолютным преобладанием женщин (84,0%) в обследуемой группе.
Через год после перевода на инсулинотерапию больные были разделены на 2 подгруппы – с наличием прогрессирования ДР и без него. Средние данные показателей, значимых для прогрессирования ДР на первом году ИТ и вошедших в регрессионный анализ, представлены в таблице 5.
Исходное состояние сетчатки является самым значимым фактором риска прогрессирования ДР. Многие авторы указывают на то, что прогрессирование диабетической ретинопатии после перевода на ИТ зависит от тяжести ретинопатии до назначения инсулина [33,34,51,53]. Tак, Т.K. Roysarkar с соавторами (1993) обнаружили, что через 6 месяцев после перевода на ИТ появления новых случаев ретинопатии не произошло, а у 66,7% было отмечено прогрессирование непролиферативной и препролиферативной ДР [53]. Это также подтверждают данные, полученные в результате исследования распространенности и прогрессирования ДР, проведенного в Санкт–Петербурге в 1995–1999 гг. В данном исследовании длительностью 30 месяцев в группе больных СД 2 типа с отсутствием изменений на глазном дне вначале наблюдения появление ретинопатии было отмечено в 16,8% случаев, в то время как у пациентов с исходной непролиферативной ДР – в 23,0%, а с препролиферативной – в 42,1% случаев [14]. И в нашем исследовании в группе с наличием прогрессирования исходный средний уровень ретинопатии до перевода на ИТ был выше, чем у пациентов со стабильным состоянием сетчатки (36,1±1,6 и 27,1±1,4 соответственно, p<0,0001). Причем в группе больных (n=21), у которых в течение первого года ДР прогрессировала на два и более уровня, средний уровень ретинопатии до перевода на ИТ составил 42,9±2,9 (p<0,001). Таким образом, ухудшение состояния сетчатки чаще встречается у больных с более тяжелыми стадиями ДР до начала ИТ и реже – при отсутствии изменений на глазном дне либо при минимальных проявлениях ретинопатии. Данные по выраженности прогрессирования ДР в течение первого года ИТ в нашем исследовании в зависимости от состояния сетчатки до изменения терапии представлены на рисунке 2.
Индекс массы тела стал вторым по значимости фактором прогрессирования ДР. Так, прогрессирование ДР отмечено у 15,1% больных с ИМТ<25 кг/м2, у 35,0% – с ИМТ от 25 до 30 кг/м2 и у 62,2% – с ИМТ >30 кг/м2 (p<0,001). В группе пациентов с прогрессированием ретинопатии ИМТ увеличился за первый год ИТ в среднем на 2,5±0,4 кг/м2 (среди больных с прогрессированием ретинопатии на два и более уровня по шкале ETDRS – на 2,7±0,8 кг/м2), а в группе без прогрессирования – на 0,5±0,3 кг/м2 (p<0,001).
Прибавка в весе – одна из главных проблем инсулинотерапии у больных СД 2 типа, поскольку увеличение ИМТ усиливает инсулинорезистентность, ухудшая возможность адекватной компенсации диабета [4,21,25,30,36,43]. Ряд авторов предполагают, что инсулинорезистентность является специфическим маркером прогрессирования диабетической ретинопатии у больных СД 2 типа [44,49].
Уровень гликированного гемоглобина (HbA1c) также является значимым фактором риска по результатам регрессионного анализа. В нашем исследовании уровень HbA1c в группе с наличием прогрессирования ретинопатии оставался высоким до конца года, несмотря на применение инсулина – 9,5±0,2% (при исходном – 11,3±0,2%, p<0,001). У пациентов со стабильным состоянием сетчатки в течение года ИТ уровень HbA1c был ниже – 8,7±0,1% (при исходном – 10,5±0,1%, p<0,001). В группе пациентов, у которых к концу первого года ИТ удалось снизить HbA1c ниже 6,5%, прогрессирование ретинопатии отмечено в 16,7 % случаев, в то время как при уровне HbA1c 6,5–7,5% оно составило 28,6%, а при HbA1c свыше 7,5% – 42,2% (p<0,001).
Интересные данные получены и при оценке прогрессирования ДР за год инсулинотерапии в зависимости от темпов изменения уровня HbA1c и его диапазона. Так, при сохранении исходного повышенного уровня HbA1c либо его дальнейшем увеличении прогрессирование отмечено в 54,6% случаев. Высокий уровень прогрессирования выявлен и в группе больных, где средний уровень гликированного гемоглобина снизился более, чем на 3% – в 44,4% случаев. В остальных же группах прогрессирование ДР произошло приблизительно с одинаковой частотой: в 35,1% случаев – в группе, где уровень HbA1c уменьшился в среднем на 0–1%, при снижении HbA1c на 1–2% и 2–3% – в 37,8% и 37,5% случаев соответственно. Нами получены данные и о том, что быстрое и значительное снижение уровня гликированного гемоглобина за первые 3–6 месяцев после перевода на ИТ приводит к росту прогрессирования ДР, однако, из–за малого числа наблюдений эти данные оказались статистически незначимыми, что требует проведения более детальных исследований в этом направлении.
На сегодняшний день не вызывает сомнений зависимость между уровнем гликированного гемоглобина и риском развития поздних осложнений сахарного диабета. Во многих исследованиях показано, что снижение уровня HbA1c на 1% уменьшает риск микроваскулярных осложнений (в том числе и ретинопатии) более чем на треть [25,26,42,55]. Имеются данные, что у больных с высокими показателями гликированного гемоглобина ДР развивается в 20 раз чаще, чем у больных с хорошей компенсацией углеводного обмена, и что более высокие уровни гликемии являются предиктором быстрого перехода ретинопатии из препролиферативной в пролиферативную стадию [35,55]. По данным M. Henricsson (1996) [34] даже незначительное повышение уровня HbA1c (>6,5%) связано с риском развития и прогрессирования диабетической ретинопатии, а повышение HbA1c на 1% вызывает увеличение риска прогрессирования (на два и более уровня по классификации WESDR5) в 1,7 раза. Этому не противоречат наши данные. Ухудшение состояния сетчатки у больных СД 2 типа при значительном и резком снижении HbA1c требует проведения дополнительных исследований по выяснению причин данного явления.
Женский пол также оказался значимым фактором, влияющим на прогрессирование ретинопатии в течение первого года ИТ. Группу с наличием прогрессирования ДР составляли преимущественно женщины – 94,7% (в подгруппе с прогрессированием на два и более уровня все больные были женского пола), а в группе, где прогрессирования отмечено не было – женщины составили 76,9% (p<0,001). Интересно, что за первый год ИТ прогрессирование ДР произошло у 45,0% женщин и лишь у 13,2% мужчин (p<0,001). Но, как уже было отмечено выше, такие данные, возможно, связаны с абсолютным преобладанием женщин (84,0%) в обследуемой группе. В то же время нельзя не отметить, что ряд авторов указывают на связь риска развития и прогрессирования ДР с женским полом [7,41,50].
Длительность диабета оказывает существенное влияние на риск прогрессирования ретинопатии после перевода на ИТ. Так, средняя длительность СД до перевода на ИТ у пациентов с отсутствием прогрессирования ДР составила 11,5±0,5 лет, в то время как у больных с ухудшением состояния глазного дна – 14,4±0,7 лет, а в группе с прогрессированием на два и более уровня по шкале ETDRS – 17,5±1,4 лет (p<0,001). Наибольший уровень прогрессирования выявлен в группе, где диагноз СД был поставлен более 21 года назад – 60,9% случаев, при длительности СД 11–20 лет прогрессирование отмечалось в 42,5%, при сроке диабета 6–10 лет – в 35,7% и при длительности основного заболевания менее 5 лет – в 25,6% случаев.
Не вызывает сомнений, что длительность СД является одним из основных факторов риска развития и прогрессирования ДР [20,24,37,39,48,56]. При СД 2 типа специфические изменения сетчатки часто обнаруживают уже в момент установления диагноза (в связи с поздней диагностикой основного заболевания) у 15–30% больных, при стаже диабета более 10 лет – в 50–70% случаев, а через 30 лет течения диабета – более чем у 70% больных [12]. По данным WESDR, при сроке СД 2 типа менее 5 лет ДР диагностируют у 17–29% больных, получающих ПСП, и у 40% пациентов на ИТ, а при длительности диабета более 15 лет диабетические изменения сетчатки выявлялись у 50–63% пациентов, принимающих ПСП, и у 85%, получающих инсулин [24,40].
Систолическая артериальная гипертензия также влияет на уровень прогрессирования ДР. В нашем исследовании в группе с наличием прогрессирования ДР у 60,0% больных средний уровень систолического давления на протяжении первого года ИТ превышал 160 мм рт. ст. (микрососудистый риск), а в группе, где состояние сетчатки оставалось стабильным, соответственно у 42%. Прогрессирование ДР выявлено в 48,7% случаев в группе пациентов со средним уровнем систолического давления выше 160 мм рт. ст., в то время как при среднем уровне систолического давления ниже 160 мм рт. ст. – лишь в 31,4% случаев (p=0,006). Другая картина наблюдалась у больных с нормальными цифрами систолического давления за период наблюдения. Среднее систолическое давление ниже 120 мм рт. ст. в группе с наличием прогрессирования ДР выявлено всего в 5,3% случаев, в группе же без прогрессирования – в 16,1%; при этом в группе со средним систолическим давлением ниже 120 мм рт. ст. прогрессирование было отмечено лишь в 17,9% случаев (p=0,01).
Очевидно, что распространенность ретинопатии у больных с артериальной гипертензией (АГ) выше, чем в группе больных с нормальными цифрами артериального давления. Подавляющее большинство авторов признают влияние АГ на возникновение и прогрессирование диабетической ретинопатии [1,15,32,35,40]. Т.В. Лукашина (1984) относит к факторам риска прогрессирования ретинопатии при СД 1 типа повышенное систолическое и диастолическое давление, а при СД 2 типа – только систолическое [9]. Многие работы свидетельствуют о том, что снижение систолического артериального давления на 10 мм рт.ст. при СД 2 типа может привести к значительному уменьшению риска ретинопатии [42,50].
Очень важными являются результаты WESDR и UKPDS, поскольку в них исследовалась взаимосвязь АГ с тяжестью диабетической ретинопатии [12,39,58]. В то же время, если сравнивать результаты WESDR и UKPDS, то они существенно различаются. По данным WESDR, как систолическое, так и диастолическое артериальное давление имеет большое прогностическое значение в плане прогрессирования изменений сетчатки только у пациентов с СД 1 типа, в то время как у больных с СД 2 типа влияние артериального давления несущественно. По WESDR, артериальное давление в большей степени является индикатором риска, чем фактором риска развития и прогрессирования ДР [39,40]. По данным UKPDS, наличие и степень тяжести ретинопатии у пациентов, страдающих СД 2 типа, были четко взаимосвязаны с высоким уровнем артериального давления [57].
Заключение
На развитие и прогрессирование диабетической ретинопатии у больных СД 2 типа после перевода на ИТ основное влияние оказывают: исходное состояние сетчатки, ИМТ, длительность СД, степень компенсации нарушений углеводного обмена (уровень HbA1c), тяжесть систолической артериальной гипертензии. Также возможным фактором риска прогрессирования диабетической ретинопатии является женский пол, хотя такое суждение пока представляется спорным.



Литература:
1. Алешин С.В. Метаболический синдром Х // Гипертония: ответный удар. – М, 2004. – Гл.6. –– С.51–58.
2. Аметов А.С. Ожирение – эпидемия ХХI века // Тер. архив. – 2002. – № 10. – С.5–7.
3. Балаболкин М.И. Диабетология // М.: Медицина, 2001. – 320 с.
4. Бутрова С.А. Метаболический синдром: патогенез, клиника, диагностика, подходы к лечению // РМЖ. – 2001. – Т. 9, № 2. – С.56–62.
5. Дедов И.И., Фадеев В.В. Введение в диабетологию: Руководство для врачей. – М.: Издательство Берег, 1998. – 200 с.
6. Дедов И.И., Чазова Т.Е., Сунцов Ю.И. Эпидемиология сахарного диабета: Пособие для врачей. – М.: Медицина, 2003. – 70 с.
7. Дедов И.И., Шестакова М.В., Миленькая Т.М. Сахарный диабет: ретинопатия, нефропатия. М.: Медицина, 2001. – 176 с.
8. Карпова И.А. Клиническая эффективность и организация программы скрининга сахарного диабета в Санкт–Петербурге: Автореф. дис. Е канд. мед. наук: 14.00.03, 14.00.33 / Санкт–Петерб. воен.–мед. акад. – СПб, 2001. – 20 с.
9. Лукашина Т. В. Факторы риска диабетической ретинопатии у больных инсулинзависимым и инсулиннезависимым типами сахарного диабета: Автореф. дис. Е канд. мед. наук / М., 1984. – 20 с.
10. Майоров А.Ю., Науменкова И.В. Современные сахароснижающие средства в лечении сахарного диабета 2 типа // РМЖ. – 2001. – Т.9, № 24. – С.1105–1112.
11. Мкртумян А.М. Ксеникал в комплексной терапии метаболического синдрома // РМЖ. – 2001. – Т.9, № 2. – С.72–74.
12. Нестеров А.П. Диабетическая ретинопатия // РМЖ. – 2000. – Т.8, № 1. – С.3–9.
13. Сорокин Е.Л. Система ранней диагностики и лечения диабетической ретинопатии в Приамурье. – Автореф. дис. Е доктора мед. наук. – Хабаровск. – 1998. – 52 с.
14. Шадричев Ф.Е. Комплексное обследование и лечение больных с диабетическими поражениями сетчатки: Автореф. дис. Е канд. мед. наук: 14.00.08 / Санкт–Петерб. гос. мед. ун–т – СПб, 2000. – 19 с.
15. Шилов А.М., Мельник М.В., Чубаров М.В., Рыбкина Т.Е. Артериальная гипертензия и сахарный диабет // Рос. мед. вести. – 2004. – № 1. – С.17–22.
16. Abraira C., Colwell J.A., Nuttall F.Q. Veterans Affairs Cooperative Study on Glycemic Control and Complications in Type II Diabetes (VA CSDM): results of the feasibility trial // Diab. Care. – 1995. – № 18. – P.113–1123.
17. Agardh E., Agardh C.D., Hansson–Lundblad C., Cavallin–Sjoberg U. The importance of early diagnosis of treatable diabetic retinopathy for the 4–year visual outcome in older–onset daibetes mellitus // Acta. Ophthalmol. Scand. – 1996. – № 74 (2). – Р.166–70.
18. Allione A., Pomero F., Berardi C. Effects of angiotensin 2 and insulin on TGF–B production by bovine retinal pericytes // Diabetologia. – 2001. – № 44 (1). – A289.
19. American Diabetes Association: Standards of medical care for patients with diabetes mellitus (Position Statement) // Diab. Care. – 2002. – № 25 (1). – S.33–49.
20. Bertram B. Prevalence of patients with diabetes mellitus without and with retinopathy in an ophthalmology practice // Ophthalmologe. – 1997. – № 94 (6). – Р.401–404.
21. Bruce D., Clark E., Campbell L. Insulin therapy in patients with poorly controlled non–insulin–dependent diabetes // Med. J. Australia. – 1987. – №146. – Р.240–242.
22. Burge M.R., Schade D.S. Current therapies for diabetes: insulins // Endocrinol. Metab. Clin. North. Am. – 1997. – № 26. – Р.575–98.
23. Chow C.–C., Tsang L.W.W., Sorensen J.P., Cockram C.S. Comparison of insulin with or without continuation of oral hypoglycemic agents in the treatment of secondary failure in NIDDM patients // Diab. Care. – 1995. – № 18. – Р.307–314.
24. Davis M.D. Diabetic retinopathy. A clinical overview // Diab. Care. – 1992. – № 15. – Р.1844–1874.
25. Diabetes Care: Implications of the Diabetes Control and Complications Trial // Diab. Care. – 2000. – № 23 (1). – P.S24–S26.
26. Early Treatment Diabetic Retinopathy Study Research Group. Early Treatment Diabetic Retinopathy Study design and baseline patient characteristics. ETDRS report № 7 // Ophthalmology. – 1991. – Vol.98. – P.741–756.
27. Emanuele N., Klein R., Abraira C., Colwell J. Evaluations of retinopathy in the VA Cooperative Study on Glycemic Control and Complications in Type 2 Diabetes (VA CSDM). A feasibility study // Diab. Care. – 1996. – № 19 (12). – Р.1375–1381.
28. European Diabetes Policy Group. A desktop guide to diabetes mellitus // Diab. Med. – 1999. – № 16. – Р.716–730.
29. Forjanic–Klapproth J., Home P.D. Progression of retinopathy with insulin Glardine or NPHinsulin – a multi–trial analysis // Diabetologia. – 2001. – № 44 (1). – A287.
30. Frazier L., Mulrow C., Alexander L. Need for insulin therapy in type 2 diabetes mellitus // Arch. Intern. Med. – 1987. – № 147. – Р.1085–1089.
31. Goddijn P.P., Bilo H.J., Feskens E.J., Groeniert K.H., Van der Zee K.I., Meyboom–de Jong B. Longitudinal study on glycaemic control and quality of life in patients with Type 2 diabetes mellitus referred for intensified control // Diab. Med. – 1999. – Vol.1, № 16. – P.23–30.
32. Guillausseau P.J., Massin P., Charles M.A., Allaguy H., Guvenli Z., Virally M., Tielmans D., Assayag M., Warnet A., Lubetzki J. Glycaemic control and development of retinopathy in type 2 diabetes mellitus: a longitudinal study // Diab. Med. –1998. – № 15 (2). – Р.151–155.
33. Henricsson M., Berntorp K , Fernlund P , Sundkvist G. Progression of retinopathy in insulin–treated type 2 diabetic patients // Diab. Care. – 2002. – № 25 (2). – Р.381–385.
34. Henricsson M., Groop L. Progression of retinopathy is related to glycaemic control even in patients with mild diabetes mellitus // Acta. Ophthalmol. Scand. – 1996. – № 74 (6). – Р.528–532.
35. Isomaa B., Henricsson M., Almgren P., Tuomi T., Taskinen M.R., Groop L. The metabolic syndrome influences the risk of chronic complications in patients with type II diabetes // Diabetologia. – 2001. – № 44 (9). – Р.1148–1154.
36. Jarrett R.J. Hyperinsulinaemia and syndrome X // Lancet. – 1993. – № 34 (1). – P.303.
37. Karadeniz S., Yilmas M.T. Age at diabetes onset: Is it one of the determinants for diabetic retinopathy in type 2 diabetes? // Diabetologia. – 2001. – № 44 (1). – A286.
38. Klein R., Klein B.E., Moss S.E. Relation of glycemic control to diabetic microvascular complications in diabetes mellitus // Ann. Intern. Med. – 1996. – № 124 (1 Pt 2). – Р.90–96.
39. Klein R., Klein B.E.K., Moss S.E. The Wisconsin Epidemiological Study of diabetic retinopathy 2. Prevalence and risk of diabetic retinopathy when age a diagnosis is 30 or more years // Arch. Ophthalmol. – 1984. – № 102. – Р.527–532.
40. Klein R., Klein B.E.K., Moss S.E. The Wisconsin Epidemiological Study of diabetic retinopathy (Review) // Diab. Metab. Rev. – 1989. – № 5. – Р.559–570.
41. Kudlacek S., Schernthaner G. The effect of insulin treatment on Hb A1C, body weight and lipids in type 2 diabetic patients with secondary–failure to sulfonilureas. A 5 year follow–up study // Horm. Metab. Res. – 1992. – Vol.10, № 24. – Р.478–83.
42. Mahtab H., Kibriya M.G., Mahtab F.U. Microvascular complications in Bangladeshi type–2 diabetic individuals: Birdem Diabetes Care and Complication Study // Diabetologia. – 2001. – № 44 (1). – A285.
43. Makimattila S., Nikkila K., Yki–Jarvinen H. Causes of weight gain during insulin therapy with and without metformin in patients with type II diabetes mellitus // Diabetologia. – 1999. – № 42. – Р.406–412.
44. Maneschi F., Mashiter K., Kohner E.M. Insulin resistance and insulin deficiency in diabetic retinopathy of non–insulin–dependent diabetes // Diabetes. – 1983. – № 32 (1). – Р.82–87.
45. Nathan D.M. Long–term complications of diabetes mellitus // N. Engl. J. Med. – 1993. – № 328 (23). – Р.1676–1685.
46. National Diabetes Data Group: Diabetes in America // 2nd ed. Bethesda, Md: National Institute of Diabetes and Digestive and Kidney Diseases; National Institutes of Health. – 1995.
47. Ohkubo Y., Kishikawa H., Araki E., Miyata T., Isami S., Motoyoshi S., Kojima Y, Furuyoshi N., Shichiri M. Intensive insulin therapy prevents the progression of diabetic microvascular complications in Japanese patients with non–insulin–dependent diabetes: a randomized prospective 6–year study // Diab. Res. Clin. Pract. – 1995. – № 28. – Р.103–117.
48. Owens D.R., Volund A., Jones D. Retinopathy in newly presenting noninsulin–dependent (type 2) diabetic patients // Diab. Res. – 1988. –№ 9. – Р.59–65.
49. Parvanova A., Iliev I., Ruggenenti P., Dimitrov B.D. Is decreased insulin sensitivity a specific predictor of proliferative retinopathy in type 2 diabetes? // Diabetologia. – 2001. – № 44 (1). – A286.
50. Phenekos C., Ginis A., Goula M. Retinopathy is associated with higher serum free testosterone in women with type 2 DM // Diabetologia. – 2001. – № 44 (1). – A286.
51. Rasmidatta S., Khunsuk–Mengrai K. Risk factors of diabetic retinopathy in non–insulin dependent diabetes mellitus // J. Med. Assoc. Thai. – 1998. – № 81 (3). – Р.169–174.
52. Rema M., Ponnaiya M., Mohan V. Prevalence of retinopathy in non insulin dependent diabetes mellitus at a diabetes centre in southern India // Diab. Res. Clin. Pract. – 1996. – № 34 (1). – Р.29–36.
53. Roysarkar T.K., Gupta A., Dash R.J., Dogra M.R. Effect of insulin therapy on progression of retinopathy in noninsulin–dependent diabetes mellitus // Am. J. Ophthalmol. – 1993. – № 115 (5). – Р.569–574.
54. Savage S., Estacio R.O., Jeffers B., Schrier R.W. Increased complications in non–insulin–dependent diabetic patients treated with insulin versus oral hypoglycemic agents: a population study // Proc. Assoc. Am. Physicians. – 1997. – № 109 (2). – Р.181–189.
55. Stratton I.M., Adler A.I., Neil H.A. Association of glycaemia with macrovascular and microvascular complications of type 2 diabetes (UKPDS 35): prospective observational study // B.M.J. – 2000. – № 321 (7258). – Р.405–412.
56. Tovi J., Ingemansson S.O., Engfeldt P. Insulin treatment of elderly type 2 diabetic patients: effects on retinopathy // Diab. Metab. – 1998. – № 24 (5). – Р.442–447.
57. Turner R.C. The U.K. Prospective Diabetes Study (Review) // Diab. Care. –1998. – № 21 (3). – P.35–38.
58. UK Prospective Diabetes Study: UKPDS VIII. Study design, progress and performance // Diabetologia. – 1991. – № 34 (12). – Р.877–890.
59. WHO. Report of the expert committee on the Diagnosis and Classification of Diabetes Mellitus // Diab. Care. – 1999. – Vol. 23 (1). – P.4–19.
60. Zimmet P. The burden of type 2 diabetes: are we doing enough? // Diab. Metab. – 2003. – № 29. – S.9–18.
61. Zinman B., Tildesley H., Chiasson J.–L. Insulin lispro in CSII: results of a double–blind crossover study // Diabetes. – 1997. – № 46. – Р.440–443.












