–Ъ–ї—О—З–µ–≤—Л–µ —Б–ї–Њ–≤–∞: –≥–Є–∞–ї—Г—А–Њ–љ–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞, —Б–Є–љ–і—А–Њ–Љ «—Б—Г—Е–Њ–≥–Њ –≥–ї–∞–Ј–∞», –Ї–Њ–љ—В–∞–Ї—В–љ—Л–µ –ї–Є–љ–Ј—Л.
Abstract
Hyaluronic acid: it’s usage in ophthalmology and
in treatment of dry eye syndrome
E.A. Egorov
RNIMU named after N.I. Pirogov
Department of Ophthalmology named after acad. A.P. Nesterov
This review describes effectiveness of Hyaluronic acid in treatment of dry eye syndrome and its usage in contact lens and solutions for contact lenses.
Key words: hyaluronic acid, dry eye syndrome, contact lenses.
–У–Є–∞–ї—Г—А–Њ–љ–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞ (–У–Ъ) –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є –њ—А–Є—А–Њ–і–љ—Л–є –њ–Њ–ї–Є—Б–∞—Е–∞—А–Є–і —Б —Г–љ–Є–Ї–∞–ї—М–љ—Л–Љ–Є –≤—П–Ј–Ї–Њ—Н–ї–∞—Б—В–Є—З–µ—Б–Ї–Є–Љ–Є –Є –≥–Є–≥—А–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Є–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є. –≠—В–Є —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞—О—В —Г—З–∞—Б—В–Є–µ –У–Ъ –≤–Њ –Љ–љ–Њ–≥–Є—Е –њ—А–Њ—Ж–µ—Б—Б–∞—Е –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ —З–µ–ї–Њ–≤–µ–Ї–∞ [1–3]. –У–Ъ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –≤ –Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ: –≤ —Е–Є—А—Г—А–≥–Є–Є –Ї–∞—В–∞—А–∞–Ї—В—Л –і–ї—П –Њ–њ—В–Є–Љ–Є–Ј–∞—Ж–Є–Є —Г—Б—В–∞–љ–Њ–≤–Ї–Є –Є–љ—В—А–∞–Њ–Ї—Г–ї—П—А–љ–Њ–є –ї–Є–љ–Ј—Л, –≤ –≤–Є—В—А–µ–Њ—А–µ—В–Є–љ–∞–ї—М–љ–Њ–є —Е–Є—А—Г—А–≥–Є–Є. –У–Ъ –≤—Е–Њ–і–Є—В –≤ —Б–Њ—Б—В–∞–≤ –Љ–∞—В–µ—А–Є–∞–ї–∞ –Ї–Њ–љ—В–∞–Ї—В–љ—Л—Е –ї–Є–љ–Ј –і–ї—П —Г–ї—Г—З—И–µ–љ–Є—П –Ї–Њ–Љ—Д–Њ—А—В–љ–Њ—Б—В–Є –Є—Е –љ–Њ—И–µ–љ–Є—П [4].
–°–Є–љ–і—А–Њ–Љ «—Б—Г—Е–Њ–≥–Њ –≥–ї–∞–Ј–∞»
–Т –њ–Њ—Б–ї–µ–і–љ–Є–µ –і–µ—Б—П—В–Є–ї–µ—В–Є—П –≤–Њ–Ј—А–Њ—Б–ї–∞ –Ј–љ–∞—З–Є–Љ–Њ—Б—В—М –њ—А–Њ–±–ї–µ–Љ—Л «—Б—Г—Е–Њ–≥–Њ –≥–ї–∞–Ј–∞». –≠—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –Є–љ—В–µ–љ—Б–Є–≤–љ—Л–Љ —А–∞–Ј–≤–Є—В–Є–µ–Љ –Ї–∞–Ї —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є –Њ—Д—В–∞–ї—М–Љ–Њ—Е–Є—А—Г—А–≥–Є–Є, —В–∞–Ї –Є —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є–Є –≥–ї–∞–Ј–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є.
–°–Њ–≥–ї–∞—Б–љ–Њ –і–∞–љ–љ—Л–Љ ARVO, –≤ 2012 –≥. —Б–Є–љ–і—А–Њ–Љ «—Б—Г—Е–Њ–≥–Њ –≥–ї–∞–Ј–∞» –њ–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤—Г –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –Ј–∞–љ–Є–Љ–∞–ї —В—А–µ—В—М–µ –Љ–µ—Б—В–Њ, —Г—Б—В—Г–њ–∞—П —В–Њ–ї—М–Ї–Њ –≥–ї–∞—Г–Ї–Њ–Љ–µ –Є –≤–Њ–Ј—А–∞—Б—В–љ–Њ–є –Љ–∞–Ї—Г–ї—П—А–љ–Њ–є –і–µ–≥–µ–љ–µ—А–∞—Ж–Є–Є. –Я–Њ –і–∞–љ–љ—Л–Љ Reddy, —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –і–Њ—Б—В–Є–≥–∞–µ—В 11–17% —Б—А–µ–і–Є –≤—Б–µ–є –њ–Њ–њ—Г–ї—П—Ж–Є–Є [17]. –Ъ–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б–Њ —Б—А–µ–і–љ–µ–є —Б—В–µ–њ–µ–љ—М—О —В—П–ґ–µ—Б—В–Є —Б–Є–љ–і—А–Њ–Љ–∞ «—Б—Г—Е–Њ–≥–Њ –≥–ї–∞–Ј–∞» –њ—А–Є—А–∞–≤–љ–Є–≤–∞–µ—В—Б—П –Ї —В–∞–Ї–Њ–≤–Њ–Љ—Г —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б–Њ —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–µ–є —Б—А–µ–і–љ–µ–є —Б—В–µ–њ–µ–љ–Є —В—П–ґ–µ—Б—В–Є [18].
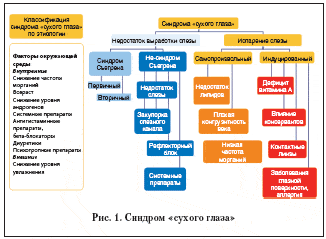
–Э–∞–Є–±–Њ–ї–µ–µ –Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ–∞—П –≥—А—Г–њ–њ–∞ – —Н—В–Њ –њ–∞—Ж–Є–µ–љ—В—Л –Љ–Њ–ї–Њ–і–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ (20–45 –ї–µ—В), —Г –Ї–Њ—В–Њ—А—Л—Е —Б–Є–љ–і—А–Њ–Љ «—Б—Г—Е–Њ–≥–Њ –≥–ї–∞–Ј–∞» —Б–≤—П–Ј–∞–љ —Б –Є–Ј–±—Л—В–Њ—З–љ—Л–Љ –Є—Б–њ–∞—А–µ–љ–Є–µ–Љ —Б–ї–µ–Ј–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є (–Њ—Д–Є—Б–љ—Л–є —Б–Є–љ–і—А–Њ–Љ, –љ–Њ—И–µ–љ–Є–µ –Ї–Њ–љ—В–∞–Ї—В–љ—Л—Е –ї–Є–љ–Ј, —А–µ—Д—А–∞–Ї—Ж–Є–Њ–љ–љ–∞—П —Е–Є—А—Г—А–≥–Є—П, —В—А–∞–љ–Ј–Є—В–Њ—А–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П —Б–ї–µ–Ј–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –њ–Њ—Б–ї–µ –њ–µ—А–µ–љ–µ—Б–µ–љ–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ-–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –Є –і—А.) (—А–Є—Б. 1). –Т –≥—А—Г–њ–њ–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б—В–∞—А—И–µ 55 –ї–µ—В –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ —Н–љ–і–Њ–Ї—А–Є–љ–љ—Л–Љ–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ–Є, –њ—А–Є–≤–Њ–і—П—Й–Є–Љ–Є –Ї –љ–∞—А—Г—И–µ–љ–Є—О —Б–ї–µ–Ј–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П, –Є –љ–Њ—Б–Є—В –љ–∞–Ј–≤–∞–љ–Є–µ —Б–Є–љ–і—А–Њ–Љ–∞ –°—К–µ–≥—А–µ–љ–∞ [19].
–†–µ–Ј—Г–ї—М—В–∞—В–Њ–Љ —Б–ї–µ–Ј–Њ–Ј–∞–Љ–µ—Б—В–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –і–Њ–ї–ґ–љ–Њ –±—Л—В—М —Г—Б—В—А–∞–љ–µ–љ–Є–µ —З—Г–≤—Б—В–≤–∞ –і–Є—Б–Ї–Њ–Љ—Д–Њ—А—В–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Я—А–µ–њ–∞—А–∞—В—Л –і–ї—П –ї–µ—З–µ–љ–Є—П —Б–Є–љ–і—А–Њ–Љ–∞ «—Б—Г—Е–Њ–≥–Њ –≥–ї–∞–Ј–∞» –і–Њ–ї–ґ–љ—Л –Њ–±–ї–∞–і–∞—В—М —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–Љ –і–µ–є—Б—В–≤–Є—П. –Ш–Љ–µ–љ–љ–Њ —В–∞–Ї–Є–µ —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є –њ—А–Є—Б—Г—Й–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ –љ–∞ –Њ—Б–љ–Њ–≤–µ –У–Ъ.
–°–њ–Њ—Б–Њ–± –њ—А–Њ–Є–Ј–≤–Њ–і—Б—В–≤–∞ –У–Ъ –і–ї—П –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П
–≤ —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є–Є —Б–Є–љ–і—А–Њ–Љ–∞ «—Б—Г—Е–Њ–≥–Њ –≥–ї–∞–Ј–∞»
–Т–Њ –Љ–љ–Њ–≥–Њ–Љ –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М —Б–ї–µ–Ј–Њ–Ј–∞–Љ–µ—Б—В–Є—В–µ–ї–µ–є –љ–∞ –Њ—Б–љ–Њ–≤–µ –У–Ъ –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П —Б–њ–Њ—Б–Њ–±–Њ–Љ –њ—А–Њ–Є–Ј–≤–Њ–і—Б—В–≤–∞. –†–∞–љ–µ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є—Б—М –Љ–µ—В–Њ–і—Л –њ–Њ–ї—Г—З–µ–љ–Є—П –У–Ъ –Є–Ј —Б—В–µ–Ї–ї–Њ–≤–Є–і–љ–Њ–≥–Њ —В–µ–ї–∞ –≥–ї–∞–Ј–∞ –Ї–Њ—А–Њ–≤—Л –Є –≥—А–µ–±–µ—И–Ї–∞ –њ–µ—В—Г—Е–∞. –Э–µ–і–Њ—Б—В–∞—В–Ї–∞–Љ–Є –і–∞–љ–љ—Л—Е –Љ–µ—В–Њ–і–Њ–≤ –њ—А–Њ–Є–Ј–≤–Њ–і—Б—В–≤–∞ —П–≤–ї—П–ї–Є—Б—М –Є—Е –і–Њ—А–Њ–≥–Њ–≤–Є–Ј–љ–∞ –Є –љ–∞–ї–Є—З–Є–µ –њ—А–Є–Љ–µ—Б–µ–є –±–µ–ї–Ї–∞ –≤ –Ї–Њ–љ–µ—З–љ–Њ–Љ –њ—А–Њ–і—Г–Ї—В–µ, —З—В–Њ –њ—А–Є–≤–Њ–і–Є–ї–Њ –Ї –±–Њ–ї—М—И–Њ–Љ—Г –Ї–Њ–ї–Є—З–µ—Б—В–≤—Г –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є—Е —А–µ–∞–Ї—Ж–Є–є –љ–∞ –њ—А–µ–њ–∞—А–∞—В [5]. –°–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–µ –њ—А–Њ–Є–Ј–≤–Њ–і—Б—В–≤–Њ –У–Ъ –Њ—Б–љ–Њ–≤–∞–љ–Њ –љ–∞ –њ—А–Њ—Ж–µ—Б—Б–µ —Д–µ—А–Љ–µ–љ—В–∞—Ж–Є–Є —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –±–∞–Ї—В–µ—А–Є–є (Streptococcus equi –Є Streptococcus zooepidemicus). –У–Ъ, –њ–Њ–ї—Г—З–µ–љ–љ–∞—П —В–∞–Ї–Є–Љ –њ—Г—В–µ–Љ, –Є–Љ–µ–µ—В –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї—Г—О —Б—В–µ–њ–µ–љ—М –Њ—З–Є—Б—В–Ї–Є, —З–µ–Љ –Є –Њ–±—К—П—Б–љ—П–µ—В—Б—П –ї—Г—З—И–∞—П –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –У–Ъ –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є [1, 2].
–°–≤–Њ–є—Б—В–≤–∞ –У–Ъ, –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞—О—Й–Є–µ –µ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ
–і–ї—П –ї–µ—З–µ–љ–Є—П —Б–Є–љ–і—А–Њ–Љ–∞ «—Б—Г—Е–Њ–≥–Њ –≥–ї–∞–Ј–∞»
–У–Ъ —П–≤–ї—П–µ—В—Б—П –њ—А–Є—А–Њ–і–љ—Л–Љ –њ–Њ–ї–Є–Љ–µ—А–Њ–Љ –Є –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї –≥—А—Г–њ–њ–µ –њ–Њ–ї–Є—Б–∞—Е–∞—А–Є–і–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ —В–∞–Ї–ґ–µ –љ–∞–Ј—Л–≤–∞—О—В –њ–Њ–ї–Є—Б–∞—Е–∞—А–Є–і–∞–Љ–Є —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є, –Љ—Г–Ї–Њ–њ–Њ–ї–Є—Б–∞—Е–∞—А–Є–і–∞–Љ–Є –Є–ї–Є –≥–ї–Є–Ї–Њ–Ј–∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–∞–љ–∞–Љ–Є [1, 3, 7]. –Ф–∞–љ–љ—Л–µ –њ–Њ–ї–Є—Б–∞—Е–∞—А–Є–і—Л –Њ–Ї–∞–Ј—Л–≤–∞—О—В –≤–ї–Є—П–љ–Є–µ –љ–∞ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–µ –≤–Њ–і—Л –≤ —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є, –≤ —В.—З. –Є —Б—В—А–Њ–Љ–µ —А–Њ–≥–Њ–≤–Є—Ж—Л [6, 8]. –У–Ъ –њ–Њ —Д–Є–Ј–Є–Ї–Њ-—Е–Є–Љ–Є—З–µ—Б–Ї–Є–Љ —Б–≤–Њ–є—Б—В–≤–∞–Љ –Љ–Њ–ґ–µ—В –Є–Ј–Љ–µ–љ—П—В—М —Б—В—А—Г–Ї—В—Г—А—Г –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —А–Э (–Ї–Є—Б–ї–Њ—В–љ–Њ—Б—В–Є –Є–ї–Є —Й–µ–ї–Њ—З–љ–Њ—Б—В–Є), –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є —Б–Њ–ї–Є –Є –≤–ї–Є—П–љ–Є—П –≥—А–∞–і–Є–µ–љ—В–∞ –і–∞–≤–ї–µ–љ–Є—П [9]. –Я–Њ–≤—Л—И–µ–љ–Є–µ –≥—А–∞–і–Є–µ–љ—В–∞ –і–∞–≤–ї–µ–љ–Є—П –Є —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л –њ—А–Є–≤–Њ–і–Є—В –Ї —Б–љ–Є–ґ–µ–љ–Є—О –≤—П–Ј–Ї–Њ—Б—В–Є —А–∞—Б—В–≤–Њ—А–∞. –Р–љ–∞–ї–Њ–≥–Є—З–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ –≤—Б–ї–µ–і—Б—В–≤–Є–µ —Й–µ–ї–Њ—З–љ–Њ–≥–Њ –Ј–љ–∞—З–µ–љ–Є—П —А–Э –Њ–±—А–∞–Ј—Г–µ—В—Б—П –±–Њ–ї–µ–µ –њ–Њ–і–≤–Є–ґ–љ–∞—П –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ–∞—П —Б—В—А—Г–Ї—В—Г—А–∞ [1, 10].
–Я–Њ–Љ–Є–Љ–Њ –≤—П–Ј–Ї–Њ—Н–ї–∞—Б—В–Є—З–µ—Б–Ї–Є—Е —Б–≤–Њ–є—Б—В–≤ –У–Ъ –Њ–±–ї–∞–і–∞–µ—В –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О —Г–і–µ—А–ґ–Є–≤–∞—В—М –≤–Њ–і—Г. –≠—В–Њ —Б–≤–Њ–є—Б—В–≤–Њ –Љ–Њ–ґ–µ—В –±—Л—В—М —Б–≤—П–Ј–∞–љ–Њ —Б –љ–∞–ї–Є—З–Є–µ–Љ –±–Њ–ї—М—И–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –≥–Є–і—А–Њ–Ї—Б–Є–ї—М–љ—Л—Е –≥—А—Г–њ–њ, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—О –≤–Њ–і–Њ—А–Њ–і–љ—Л—Е —Б–≤—П–Ј–µ–є [1, 7, 11–14]. –Ш—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–Є —Г—В–≤–µ—А–ґ–і–∞—О—В, —З—В–Њ –У–Р –Љ–Њ–ґ–µ—В —Г–і–µ—А–ґ–Є–≤–∞—В—М –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –≤–Њ–і—Л, –≤ 1000 —А–∞–Ј –њ—А–µ–≤—Л—И–∞—О—Й–µ–µ —Б–Њ–±—Б—В–≤–µ–љ–љ—Г—О –Љ–∞—Б—Б—Г [7, 24]. –Т –љ–Њ—А–Љ–µ –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ —З–µ–ї–Њ–≤–µ–Ї–∞ –У–Ъ –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞–µ—В—Б—П –≤–Њ –≤–љ–µ–Ї–ї–µ—В–Њ—З–љ–Њ–Љ –Љ–∞—В—А–Є–Ї—Б–µ —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є –≤ –Ї–Њ–ґ–µ –Є —Б–Є–љ–Њ–≤–Є–∞–ї—М–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є [1–3]. –У–Ъ —В–∞–Ї–ґ–µ –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –≤ —Б—В–µ–Ї–ї–Њ–≤–Є–і–љ–Њ–Љ —В–µ–ї–µ, —Б–ї–µ–Ј–љ–Њ–є –ґ–µ–ї–µ–Ј–µ, —Н–њ–Є—В–µ–ї–Є–Є —А–Њ–≥–Њ–≤–Є—Ж—Л –Є –Ї–Њ–љ—К—О–љ–Ї—В–Є–≤–µ –≥–ї–∞–Ј–∞ [1–3, 15, 16].
–Я—А–µ–і–њ–Њ–ї–∞–≥–∞—О—В, —З—В–Њ –У–Ъ –Њ–±–ї–∞–і–∞–µ—В –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є –Є –њ—А–Є–љ–Є–Љ–∞–µ—В —Г—З–∞—Б—В–Є–µ –≤ –њ—А–Њ—Ж–µ—Б—Б–∞—Е —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А–Њ–≤–∞–љ–Є—П –Ї–ї–µ—В–Њ–Ї, —В–∞–Ї–Є—Е –Ї–∞–Ї –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є—П, –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–Ї–∞ –Є –Љ–Є–≥—А–∞—Ж–Є—П [20]. –Ф–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –У–Ъ —Б—В–Є–Љ—Г–ї–Є—А—Г–µ—В –Љ–Є–≥—А–∞—Ж–Є—О —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—Й—Г—О –Ј–∞–ґ–Є–≤–ї–µ–љ–Є—О —А–∞–љ —А–Њ–≥–Њ–≤–Є—Ж—Л [21–23].
–Ь–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –У–Ъ –≤ —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–Љ –ї–µ—З–µ–љ–Є–Є «—Б—Г—Е–Њ–≥–Њ –≥–ї–∞–Ј–∞» [3, 13, 25–29]. –Я—А–Є —Н—В–Њ–Љ –±–Њ–ї—М—И–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ–µ—В —Б–±–∞–ї–∞–љ—Б–Є—А–Њ–≤–∞–љ–љ–∞—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –У–Ъ –≤ —Б–Њ—Б—В–∞–≤–µ —Б–ї–µ–Ј–Њ–Ј–∞–Љ–µ—Б—В–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞.
–Т –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–Љ –і–≤–Њ–є–љ–Њ–Љ —Б–ї–µ–њ–Њ–Љ –њ–µ—А–µ–Ї—А–µ—Б—В–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б —Г—З–∞—Б—В–Є–µ–Љ 20 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —В—П–ґ–µ–ї–Њ–є —Б—В–µ–њ–µ–љ—М—О —Б–Є–љ–і—А–Њ–Љ–∞ «—Б—Г—Е–Њ–≥–Њ –≥–ї–∞–Ј–∞» –љ–∞–Ј–љ–∞—З–∞–ї–Є 0,1% —А–∞—Б—В–≤–Њ—А –У–Ъ, 0,2% —А–∞—Б—В–≤–Њ—А –У–Ъ –Є–ї–Є –њ–ї–∞—Ж–µ–±–Њ 6 —А./–і–µ–љ—М –µ–ґ–µ–і–љ–µ–≤–љ–Њ –≤ —В–µ—З–µ–љ–Є–µ 14 –і–љ–µ–є. –¶–µ–ї—М—О –і–∞–љ–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –±—Л–ї–∞ –љ–µ —В–Њ–ї—М–Ї–Њ –Њ—Ж–µ–љ–Ї–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –У–Ъ –њ—А–Є —В—П–ґ–µ–ї–Њ–є —Б—В–µ–њ–µ–љ–Є «—Б—Г—Е–Њ–≥–Њ –≥–ї–∞–Ј–∞», –љ–Њ –Є –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ –љ–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞. –Т –Њ—В–љ–Њ—И–µ–љ–Є–Є —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ —В–µ—Б—В–∞ –®–Є—А–Љ–µ—А–∞, –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –≤—А–µ–Љ–µ–љ–Є —А–∞–Ј—А—Л–≤–∞ —Б–ї–µ–Ј–љ–Њ–є –њ–ї–µ–љ–Ї–Є (–Т–†–°–Я) –Є —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ —В–µ—Б—В–∞ –Њ–Ї—А–∞—И–Є–≤–∞–љ–Є—П –±–µ–љ–≥–∞–ї—М—Б–Ї–Є–Љ —А–Њ–Ј–Њ–≤—Л–Љ –љ–µ –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є, –њ–Њ–ї—Г—З–∞–≤—И–Є–Љ–Є 0,1% —А–∞—Б—В–≤–Њ—А –У–Ъ –Є –њ–ї–∞—Ж–µ–±–Њ. –Ю–і–љ–∞–Ї–Њ –њ—А–Є —Б—А–∞–≤–љ–µ–љ–Є–Є –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є —А–∞—Б—В–≤–Њ—А–∞ –У–Ъ – 0,2% —Б –њ–ї–∞—Ж–µ–±–Њ –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ –Ј–љ–∞—З–Є–Љ–Њ–µ —А–∞–Ј–ї–Є—З–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Њ–Ї—А–∞—И–Є–≤–∞–љ–Є—П –±–µ–љ–≥–∞–ї—М—Б–Ї–Є–Љ —А–Њ–Ј–Њ–≤—Л–Љ –≤ –≥—А—Г–њ–њ–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –У–Ъ (–†<0,005). –Т –і–∞–љ–љ–Њ–є –≥—А—Г–њ–њ–µ —В–∞–Ї–ґ–µ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Т–†–°–Я –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —В–∞–Ї–Њ–≤—Л–Љ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –њ–ї–∞—Ж–µ–±–Њ (–†<0,005) [29].
–Т —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ–Љ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–Љ —Б–ї–µ–њ–Њ–Љ –њ–ї–∞—Ж–µ–±–Њ-–Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б —Г—З–∞—Б—В–Є–µ–Љ 12 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М –Њ—Ж–µ–љ–Ї–∞ –Т–†–°–Я –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є 0,05%, 0,1% –Є–ї–Є 0,3% —А–∞—Б—В–≤–Њ—А–∞ –У–Ъ. –Ш–Ј–Љ–µ—А–µ–љ–Є—П –Т–†–°–Я –њ—А–Њ–≤–Њ–і–Є–ї–Є—Б—М –і–Њ –Є–љ—Б—В–Є–ї–ї—П—Ж–Є–Є –≥–ї–∞–Ј–љ—Л—Е –Ї–∞–њ–µ–ї—М, –∞ —В–∞–Ї–ґ–µ —З–µ—А–µ–Ј 5, 15, 30, 60, 120 –Є 180 –Љ–Є–љ. –њ–Њ—Б–ї–µ –љ–µ–µ. –С—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Т–†–°–Я –і–ї—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–є –У–Ъ 0,1% –Є 0,3% [25].
–Ф–ї—П –Њ—Ж–µ–љ–Ї–Є —Б—Г–±—К–µ–Ї—В–Є–≤–љ–Њ–є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –Є –Т–†–°–Я —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О –ї–Є–њ–Є–і–љ–Њ–≥–Њ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞ —Б–ї–µ–Ј–љ–Њ–є –њ–ї–µ–љ–Ї–Є 10 –њ–∞—Ж–Є–µ–љ—В–∞–Љ –Є–љ—Б—В–Є–ї–ї–Є—А–Њ–≤–∞–ї–Є 0,18% —А–∞—Б—В–≤–Њ—А –У–Ъ –≤ –Њ–і–Є–љ –≥–ї–∞–Ј –Є 0,3% —А–∞—Б—В–≤–Њ—А –≥–Є–і—А–Њ–Ї—Б–Є–њ—А–Њ–њ–Є–ї–Љ–µ—В–Є–ї—Ж–µ–ї–ї—О–ї–Њ–Ј—Л – –≤ –і—А—Г–≥–Њ–є. –Ю–±–∞ —Б–њ–Њ—Б–Њ–±–∞ –ї–µ—З–µ–љ–Є—П –њ—А–Є–≤–µ–ї–Є –Ї –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ—Г —Г–≤–µ–ї–Є—З–µ–љ–Є—О –Т–†–°–Я —З–µ—А–µ–Ј 15, 30 –Є 60 –Љ–Є–љ. –њ–Њ—Б–ї–µ –Ј–∞–Ї–∞–њ—Л–≤–∞–љ–Є—П –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Є—Б—Е–Њ–і–љ—Л–Љ —Г—А–Њ–≤–љ–µ–Љ (–†<0,05), –Њ–і–љ–∞–Ї–Њ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Т–†–°–Я –≤ –≥—А—Г–њ–њ–µ, –њ–Њ–ї—Г—З–∞–≤—И–µ–є –У–Ъ, –±—Л–ї–Њ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –≤—Л—И–µ –љ–∞ 30 –Є 60 –Љ–Є–љ. –љ–∞–±–ї—О–і–µ–љ–Є—П (–†=0,04 –Є –†=0,005 —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ) [28]. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Г—З–Є—В—Л–≤–∞—П —А–µ–Ј—Г–ї—М—В–∞—В—Л –і–∞–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–µ–є –У–Ъ –Љ–Њ–ґ–љ–Њ —Б—З–Є—В–∞—В—М –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О 0,1–0,3%.
–Т–Њ–Ј–≤—А–∞—Й–∞—П—Б—М –Ї —В–µ–Љ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В–Є —Б–Є–љ–і—А–Њ–Љ–∞ «—Б—Г—Е–Њ–≥–Њ –≥–ї–∞–Ј–∞», –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –Њ–љ –≤—Б—В—А–µ—З–∞–µ—В—Б—П –Ї–∞–Ї —Г –ї–Є—Ж –Љ–Њ–ї–Њ–і–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞, —В–∞–Ї –Є —Г –њ–Њ–ґ–Є–ї—Л—Е –ї—О–і–µ–є. –Я—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є —В–µ—А–∞–њ–Є–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Г—З–Є—В—Л–≤–∞—В—М —Е–∞—А–∞–Ї—В–µ—А —В–µ—З–µ–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –≤ –Ї–∞–ґ–і–Њ–є –Є–Ј —Н—В–Є—Е –≥—А—Г–њ–њ. –Ґ–∞–Ї, –≤ –≥—А—Г–њ–њ–µ –Љ–Њ–ї–Њ–і—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Є–Ј–±—Л—В–Њ—З–љ—Л–Љ –Є—Б–њ–∞—А–µ–љ–Є–µ–Љ —Б–ї–µ–Ј–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є —Б–Є–Љ–њ—В–Њ–Љ—Л –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –љ–Њ—Б—П—В —В—А–∞–љ–Ј–Є—В–Њ—А–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А. –Т —Н—В–Њ–є –≥—А—Г–њ–њ–µ –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –У–Ъ (0,2–0,24%) –і–ї—П –±—Л—Б—В—А–Њ–≥–Њ, –љ–Њ –љ–µ–њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ–≥–Њ –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤. –Т –Љ–µ–ґ–і—Г–љ–∞—А–Њ–і–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –њ—А–µ–Ї—А–∞—Б–љ–Њ –Ј–∞—А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–ї —Б–µ–±—П Artelac Splash (–Ї–Њ–Љ–њ–∞–љ–Є—П Bausch + Lomb, –°–®–Р) – –њ—А–µ–њ–∞—А–∞—В –±–µ–Ј –Ї–Њ–љ—Б–µ—А–≤–∞–љ—В–∞ —Б —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ–Љ 0,2 –Є 0,24% –У–Ъ. –§–Њ—А–Љ–∞ –≤—Л–њ—Г—Б–Ї–∞ –і–∞–љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ —А–∞–Ј–ї–Є—З–љ–∞ – –Ї–∞–Ї –≤ —Б—В–∞–љ–і–∞—А—В–љ–Њ–Љ —Д–ї–∞–Ї–Њ–љ–µ, —В–∞–Ї –Є –≤ –Љ—Г–ї—М—В–Є–і–Њ–Ј–∞—Е.
–Т —Б—В–∞—А—И–µ–є –≤–Њ–Ј—А–∞—Б—В–љ–Њ–є –≥—А—Г–њ–њ–µ (—Б–≤—Л—И–µ 55 –ї–µ—В) —Б —Н–љ–і–Њ–Ї—А–Є–љ–љ–Њ –і–µ—В–µ—А–Љ–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є —Б–µ–Ї—А–µ—Ж–Є–Є —Б–ї–µ–Ј—Л —В–µ—З–µ–љ–Є–µ —Б–Є–љ–і—А–Њ–Љ–∞ «—Б—Г—Е–Њ–≥–Њ –≥–ї–∞–Ј–∞» –љ–Њ—Б–Є—В —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–є —Е–∞—А–∞–Ї—В–µ—А. –Т —Н—В–Њ–є –≥—А—Г–њ–њ–µ –Љ–Њ–ґ–љ–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Б –±–Њ–ї–µ–µ –љ–Є–Ј–Ї–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–µ–є –У–Ъ – –Њ—В 0,15% –Ю–Ї—Б–Є–∞–ї (–Ї–Њ–Љ–њ–∞–љ–Є—П Bausch + Lomb, –°–®–Р).
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–У–Ъ –Є–≥—А–∞–µ—В –≤–∞–ґ–љ—Г—О —А–Њ–ї—М –≤ —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є–Є –≥–ї–∞–Ј–∞. –£–љ–Є–Ї–∞–ї—М–љ—Л–µ —Д–Є–Ј–Є–Ї–Њ-—Е–Є–Љ–Є—З–µ—Б–Ї–Є–µ —Б–≤–Њ–є—Б—В–≤–∞ –У–Ъ –њ–Њ—Б–ї—Г–ґ–Є–ї–Є –Њ—Б–љ–Њ–≤–Њ–є –і–ї—П –µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –≤ —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–Љ –ї–µ—З–µ–љ–Є–Є —Б–Є–љ–і—А–Њ–Љ–∞ «—Б—Г—Е–Њ–≥–Њ –≥–ї–∞–Ј–∞». –° —Г—З–µ—В–Њ–Љ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В–Є —Г–Ї–∞–Ј–∞–љ–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ (–њ–∞—Ж–Є–µ–љ—В—Л –Ї–∞–Ї –Љ–Њ–ї–Њ–і–Њ–≥–Њ, —В–∞–Ї –Є –њ–Њ–ґ–Є–ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞) –Њ–њ—А–µ–і–µ–ї–µ–љ—Л —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—О —А–∞–Ј–ї–Є—З–љ—Л—Е –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–є –У–Ъ –≤ —Б–Њ—Б—В–∞–≤–µ —Б–ї–µ–Ј–Њ–Ј–∞–Љ–µ—Б—В–Є—В–µ–ї–µ–є. –Ґ–∞–Ї, –і–ї—П –±–Њ–ї–µ–µ –±—Л—Б—В—А–Њ–≥–Њ –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П —В—А–∞–љ–Ј–Є—В–Њ—А–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –њ–Њ–Ї–∞–Ј–∞–љ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –У–Ъ –≤ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є 0,2–0,24% Artelac Splash (Bausch + Lomb, –°–®–Р). –Т –≥—А—Г–њ–њ–µ —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ —В–µ—З–µ–љ–Є–µ–Љ —Б–Є–љ–і—А–Њ–Љ–∞ «—Б—Г—Е–Њ–≥–Њ –≥–ї–∞–Ј–∞» (–≤–Њ–Ј—А–∞—Б—В —Б—В–∞—А—И–µ 55 –ї–µ—В) –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –і–ї–Є—В–µ–ї—М–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Б –Љ–µ–љ—М—И–µ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–µ–є –У–Ъ – 0,15% –Ю–Ї—Б–Є–∞–ї, (Bausch + Lomb, –°–®–Р).
–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. Lapcik L. Jr., Lapcik L., DeSmedt S. et al. Hyaluronan: preparation, structure, properties and applications // Chem Rev. 1998. Vol. 98. –†. 2663–2684.
2. Milas M., Rinaudo M. Characterization and properties of hyaluronic acid (hyaluronan). In: Dumitriu S. ed. Polysaccharides Structural Diversity and Functional Versatility. New York, NY: Marcel Dekker, 2005. –†. 535–549.
3. Stuart J.C., Linn J.G. Dilute sodium hyaluronate (Healon) in the treatment of ocular surface disorders // Ann Ophthalmol. 1985. Vol. 17. –†. 190–192.
4. Fonn D. Targeting contact lens induced dryness and discomfort: what properties will make lenses more comfortable // Optom Vis Sci. 2007. Vol. 84. –†. 279–285.
5. Andre P. Evaluation of the safety of a non-animal stabilized hyaluronic acid (NASHAdQ-Medical, Sweden) in European countries: retrospective study from 1997 to 2001 // J Eur Acad Dermatol Venereol. 2004. Vol. 18. –†. 422–425.
6. Duranti F., Salti G., Bovani B. et al. Injectable hyaluronic acid gel for soft tissue augmentation. A clinical and histological study // Dermatol Surg. 1998. Vol. 24. –†. 1317–1325.
7. Hargittai I., Hargittai M. Molecular structure of hyaluronan; an introduction // Struct Chem. 2008. Vol. 19. –†. 697–717.
8. Davies A., Gormally J., Wyn-Jones E. et al. A study of hydration of sodium hyaluronate from compressibility and high precision densitometric measurements // Int J Biol Macromol. 1982. Vol. 4. –†. 436.
9. Scott J.E. Extracellular matrix, supramolecular organisation and shape // J Anat. 1995. Vol. 187 (Pt 2). –†. 259–269.
10. Scott J.E., Cummings C., Brass A. et al. Secondary and tertiary structures of hyaluron in aqueous solution, investigated by rotary shadowingelectron microscopy and computer simulation // Biochem J. 1991. Vol. 274. –†. 699–705.
11. Cantor J.O., Nadkarni P.P. Hyaluronan: the Jekyll and Hyde molecule // Inflamm Allergy Drug Targets. 2006. Vol. 5. –†. 257–260.
12. Polack F.M. Healon (Na Hyaluronate): A review of the literature // Cornea. 1986. Vol. 5. –†. 81–93.
13. Sindt C.W. A new dry eye therapy? Could hyaluronic acid be instrumental in the treatment of dry eye? // Rev Cornea Contact Lenses. 2009. Vol. 1. –†. 12.
14. Szczotka-Flynn L.B. Chemical properties of contact lens rewetter // CL Spectrum. 2006. Vol. 21.
15. Lerner L., Schwartz D., Hwang D. et al. Hyaluronan and CD44 in the human cornea and limbal conjunctiva: letter to the editor // Exp Eye Res. 1998. Vol. 67. –†. 481–484.
16. Yoshida K., Nitatori Y., Uchiyama Y. Localization of glycosaminoglycans and CD44 in the human lacrimal gland // Arch Histol Cytol. 1996. Vol. 59. –†. 505–513.
17. Reddy P. et al. // Cornea. 2004. Vol. 23 (8). –†. 751–761.
18. Brown M.M. // Arch Ophthalmol. 2009. Vol. 127 (2). –†. 146–152.
19. Report of the International Dry Eye WorkShop (DEWS) // Ocul Surf. 2007. Vol. 5 (2). –†. 61–204.
20. Presti D., Scott J.E. Hyaluronan-mediated protective effect against cell damage caused by enzymatically produced hydroxyl (OH.) radicals is dependent on hyaluronan molecular mass // Cell Biochem Funct. 1994. Vol. 12. –†. 281–288.
21. Gomes J.A., Amankwah R., Powell-Richards A. et al. Sodium hyaluronate (hyaluronic acid) promotes migration of human corneal epithelial cells in vitro // Br J Ophthalmol. 2004. Vol. 88. –†. 821–825.
22. Inoue M., Katakami C. The effect of hyaluronic acid on corneal epithelial cell proliferation // Invest Ophthalmol Vis Sci. 1993. Vol. 34. –†. 2313–2315.
23. Nishida T., Nakamura M., Mishima H. et al. Hyaluronan stimulates corneal epithelial migration // Exp Eye Res. 1991. Vol. 53. –†. 753–758.
24. Nakamura M., Hikida M., Nakano T. et al. Characterization of water retentive properties of hyaluronan // Cornea. 1993. Vol. 12. –†. 433–446.
25. Hamano T., Horimoto K., Lee M. et al. Sodium hyaluronate eyedrops enhance tear film stability // Jpn J Ophthalmol. 1996. Vol. 40. –†. 62–65.
26. Johnson M.E., Murphy P.J., Boulton M. Effectiveness of sodium hyaluronate eyedrops in the treatment of dry eye // Graefes Arch Clin Exp Ophthalmol. 2006. Vol. 244. –†. 109–112.
27. Miyauchi S., Sugiyama T., Machida A. et al. A 26-week ophthalmic instillation test of sodium hyaluronate in rabbits // Pharmacometrics. 1993. Vol. 46. –†. 317–328.
28. Prabhasawat P., Tesavibul N., Kasetsuwan N. Performance profile of sodium hyaluronate in patients with lipid tear deficiency: randomised, double-blind, controlled, exploratory study // Br J Ophthalmol. 2007. Vol. 91. –†. 47–50.
29. Sand B.B, Marner K., Norn M.S. Sodium hyaluronate in the treatment of keratoconjunctivitis sicca. A double masked clinical trial // Acta Ophthalmol (Copenh). 1989. Vol. 67. –†. 181–183.












