–Ґ–µ—А–Љ–Є–љ–Њ–Љ ¬Ђ—В—А–Њ–Љ–±–Њ—Д–Є–ї–Є—П¬ї –Њ–±–Њ–Ј–љ–∞—З–∞—О—В —Б–Њ—Б—В–Њ—П–љ–Є–µ, –Њ–±—К–µ–і–Є–љ—П—О—Й–µ–µ –≤—Б–µ –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ—Л–µ (–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л–µ, –њ–Њ—Б—В–Њ—П–љ–љ—Л–µ) –Є –њ—А–Є–Њ–±—А–µ—В–µ–љ–љ—Л–µ (–≤—В–Њ—А–Є—З–љ—Л–µ, —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–µ, –і–µ–є—Б—В–≤—Г—О—Й–Є–µ –≤ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–є –њ—А–Њ–Љ–µ–ґ—Г—В–Њ–Ї –≤—А–µ–Љ–µ–љ–Є) –љ–∞—А—Г—И–µ–љ–Є—П –≤ —Б–Є—Б—В–µ–Љ–µ –≥–µ–Љ–Њ—Б—В–∞–Ј–∞, –Ї–Њ—В–Њ—А—Л–Љ —Б–≤–Њ–є—Б—В–≤–µ–љ–љ–∞ –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ—Б—В—М –Ї —А–∞–љ–љ–µ–Љ—Г –њ–Њ—П–≤–ї–µ–љ–Є—О –Є —А–µ—Ж–Є–і–Є–≤–Є—А–Њ–≤–∞–љ–Є—О —В—А–Њ–Љ–±–Њ–Ј–Њ–≤, —В—А–Њ–Љ–±–Њ—Н–Љ–±–Њ–ї–Є–є, –Є—И–µ–Љ–Є–є –Є –Є–љ—Д–∞—А–Ї—В–Њ–≤ –Њ—А–≥–∞–љ–Њ–≤. –Ю–і–љ–∞ –Є–Ј –њ—А–Є—З–Є–љ —В—А–Њ–Љ–±–Њ—Д–Є–ї–Є–Є вАУ –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ–∞—П —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М –Ї –∞–Ї—В–Є–≤–Є—А–Њ–≤–∞–љ–љ–Њ–Љ—Г –њ—А–Њ—В–µ–Є–љ—Г –° (–†–Р–Я–°) –Ї–∞–Ї –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–є —Д–∞–Ї—В–Њ—А —А–Є—Б–Ї–∞ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –≤–µ–љ–Њ–Ј–љ–Њ–≥–Њ —В—А–Њ–Љ–±–Њ–Ј–∞. –Ф–ї—П –Њ–њ–Є—Б–∞–љ–Є—П —Н—В–Њ–≥–Њ –і–µ—Д–µ–Ї—В–∞ –±—Л–ї –њ—А–µ–і–ї–Њ–ґ–µ–љ —В–µ—А–Љ–Є–љ ¬Ђ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М –Ї –∞–Ї—В–Є–≤–Є—А–Њ–≤–∞–љ–љ–Њ–Љ—Г –њ—А–Њ—В–µ–Є–љ—Г –°¬ї (–Р–†–°-—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М), –Є–ї–Є –Є–љ–і–µ–Ї—Б –†–Р–Я–°. –Ф–µ—Д–µ–Ї—В–љ—Л–є —Д–∞–Ї—В–Њ—А V, –Њ–±–Њ–Ј–љ–∞—З–µ–љ–љ—Л–є –Ї–∞–Ї —Д–∞–Ї—В–Њ—А FV Leiden, –≥–Њ—А–∞–Ј–і–Њ –Љ–µ–і–ї–µ–љ–љ–µ–µ, —З–µ–Љ –≤ –љ–Њ—А–Љ–µ, –њ—А–Њ—В–µ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є —А–∞—Б—Й–µ–њ–ї—П–µ—В—Б—П –∞–Ї—В–Є–≤–Є—А–Њ–≤–∞–љ–љ—Л–Љ –њ—А–Њ—В–µ–Є–љ–Њ–Љ –° (–Р–Я–°). –≠—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О —Б–Ї–Њ—А–Њ—Б—В–Є –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П —В—А–Њ–Љ–±–Є–љ–∞ –њ—А–Є –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е, –Ї –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—О —В—А–Њ–Љ–±–Њ–Ј–∞ –≤ –ї—О–±–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–µ. –†–∞–Ј–≤–Є—В–Є–µ —В—А–Њ–Љ–±–Њ–Ј–∞ –¶–Т–° —Г –Љ–Њ–ї–Њ–і—Л—Е –ї—О–і–µ–є –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ—В —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ—Б—В—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –љ–∞ –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –Љ–∞—А–Ї–µ—А—Л —В—А–Њ–Љ–±–Њ—Д–Є–ї–Є–Є —Б —Г—З–µ—В–Њ–Љ —Н—В–Њ–≥–Њ –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –ї–µ—З–µ–љ–Є—П. –†–Р–Я–° –Љ–Њ–ґ–µ—В –±—Л—В—М –Ї–∞–Ї –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ–Њ–≥–Њ (—Б–≤—П–Ј–∞–љ–љ–Њ–≥–Њ —Б FV Leiden), —В–∞–Ї –Є –њ—А–Є–Њ–±—А–µ—В–µ–љ–љ–Њ–≥–Њ —Е–∞—А–∞–Ї—В–µ—А–∞ вАУ –Ј–∞ —Б—З–µ—В –њ–Њ—П–≤–ї–µ–љ–Є—П –∞–љ—В–Є—Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–љ—Л—Е –∞–љ—В–Є—В–µ–ї, –∞ —В–∞–Ї–ґ–µ –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ –Ї–Њ–љ—В—А–∞—Ж–µ–њ—В–Є–≤–Њ–≤ [2].
–Т –њ–∞—В–Њ–≥–µ–љ–µ–Ј–µ –Ю–Т–° –Љ–Њ–≥—Г—В —Г—З–∞—Б—В–≤–Њ–≤–∞—В—М –Є –∞–љ—В–Є—В–µ–ї–∞ –Ї —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–∞–Љ (–Р–§–Р), –Є–Ј–Љ–µ–љ—П—О—Й–Є–µ –≥–Њ–Љ–µ–Њ—Б—В–∞—В–Є—З–µ—Б–Ї—Г—О —А–µ–≥—Г–ї—П—Ж–Є—О —Б–≤–µ—А—В—Л–≤–∞–љ–Є—П –Ї—А–Њ–≤–Є. –Ґ–Њ—З–љ—Л–є –Љ–µ—Е–∞–љ–Є–Ј–Љ —А–∞–Ј–≤–Є—В–Є—П —В—А–Њ–Љ–±–Њ–Ј–∞ –њ—А–Є —Г—З–∞—Б—В–Є–Є –Р–§–Р, –≤ —В. —З. –≤–Њ–ї—З–∞–љ–Њ—З–љ–Њ–≥–Њ –∞–љ—В–Є–Ї–Њ–∞–≥—Г–ї—П–љ—В–∞ (–Т–Р), –µ—Й–µ –љ–µ –Њ–њ—А–µ–і–µ–ї–µ–љ. –Т—Л–і–≤–Є–≥–∞–µ—В—Б—П –≥–Є–њ–Њ—В–µ–Ј–∞ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —А–Њ–ї–Є –Т–Р –≤ —А–µ–≥—Г–ї—П—Ж–Є–Є —Б–Є—Б—В–µ–Љ—Л –≥–µ–Љ–Њ—Б—В–∞–Ј–∞. –Я–Њ–ї–∞–≥–∞—О—В, —З—В–Њ –њ—А–Њ—В—А–Њ–Љ–±–Њ—В–Є—З–µ—Б–Ї–Є–є –Љ–µ—Е–∞–љ–Є–Ј–Љ –і–µ–є—Б—В–≤–Є—П –Р–§–Р –Ј–∞–Ї–ї—О—З–∞–µ—В—Б—П –≤ –љ–∞—А—Г—И–µ–љ–Є–Є —Н–љ–і–Њ–≥–µ–љ–љ—Л—Е –∞–љ—В–Є–Ї–Њ–∞–≥—Г–ї—П–љ—В–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤: —Б–љ–Є–ґ–µ–љ–Є–Є –∞–љ—В–Є—В—А–Њ–Љ–±–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ—В–µ–љ—Ж–Є–∞–ї–∞ —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є –Є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –µ—Б—В–µ—Б—В–≤–µ–љ–љ—Л—Е –∞–љ—В–Є–Ї–Њ–∞–≥—Г–ї—П–љ—В–Њ–≤, —З—В–Њ –Є –њ—А–Є–≤–Њ–і–Є—В –Ї —А–∞–Ј–≤–Є—В–Є—О –≥–Є–њ–µ—А–Ї–Њ–∞–≥—Г–ї—П—Ж–Є–Є [3вАУ6].
–£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ю–Т–° –љ–∞ —Д–Њ–љ–µ –Љ—Г—В–∞—Ж–Є–Є FV Leiden –Є –Т–Р –Љ–∞–ї–Њ –Є–Ј—Г—З–µ–љ—Л –љ–∞—А—Г—И–µ–љ–Є—П –≤ —Б–Є—Б—В–µ–Љ–µ –≥–µ–Љ–Њ—Б—В–∞–Ј–∞ –Є –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –Ї–ї–Є–љ–Є–Ї–Є.
–¶–µ–ї–Є –і–∞–љ–љ–Њ–є —А–∞–±–Њ—В—Л: –Є–Ј—Г—З–µ–љ–Є–µ –≤–ї–Є—П–љ–Є—П –Љ—Г—В–∞—Ж–Є–Є FV Leiden, —Б–Њ—З–µ—В–∞–љ–Є—П –µ–µ —Б –Т–Р –Є –Є—Е –≤–ї–Є—П–љ–Є–µ –љ–∞ –Ї–ї–Є–љ–Є–Ї–Њ-–ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л–µ –њ–∞—А–∞–Љ–µ—В—А—Л —Б–Є—Б—В–µ–Љ—Л –≥–µ–Љ–Њ—Б—В–∞–Ј–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ю–Т–°; —Б—А–∞–≤–љ–µ–љ–Є–µ –Є—Е —Б –≥—А—Г–њ–њ–Њ–є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±–µ–Ј –Т–Р –Є –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ–Њ–≥–Њ –і–µ—Д–µ–Ї—В–∞ вАУ –Љ—Г—В–∞—Ж–Є–Є FV Leiden; –Є–Ј—Г—З–µ–љ–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є –Ю–Т–° –≤ —Г–Ї–∞–Ј–∞–љ–љ—Л—Е –≥—А—Г–њ–њ–∞—Е.
–Ь–∞—В–µ—А–Є–∞–ї –Є –Љ–µ—В–Њ–і—Л
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Г—З–∞—Б—В–≤–Њ–≤–∞–ї–Є 150 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (150 –≥–ї–∞–Ј) —Б –Ю–Т–°, —Б—А–µ–і–Є –љ–Є—Е –Љ—Г–ґ—З–Є–љ –±—Л–ї–Њ 63, –ґ–µ–љ—Й–Є–љ вАУ 87. –Т–Њ–Ј—А–∞—Б—В –њ–∞—Ж–Є–µ–љ—В–Њ–≤ вАУ 42¬±10 –≥–Њ–і–∞. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –љ–∞—А—Г—И–µ–љ–Є–є –≤ —Б–Є—Б—В–µ–Љ–µ –≥–µ–Љ–Њ—Б—В–∞–Ј–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —А–∞—Б–њ—А–µ–і–µ–ї–Є–ї–Є –њ–Њ 3 –≥—А—Г–њ–њ–∞–Љ: 1-—П –≥—А—Г–њ–њ–∞ вАУ 12 —З–µ–ї–Њ–≤–µ–Ї —Б –Ю–Т–°, –Є–Љ–µ—О—Й–Є—Е FV Leiden –Є –Т–Р; 2-—П –≥—А—Г–њ–њ–∞ вАУ 11 —З–µ–ї–Њ–≤–µ–Ї —Б –Ю–Т–° –Є —В–Њ–ї—М–Ї–Њ –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ—Л–Љ –і–µ—Д–µ–Ї—В–Њ–Љ FV Leiden –±–µ–Ј –Т–Р; 3-—П –≥—А—Г–њ–њ–∞ вАУ 107 —З–µ–ї–Њ–≤–µ–Ї —Б –Ю–Т–° –±–µ–Ј –Р–†–°-R –Є –Т–Р. –Ш–Ј 3-–є –≥—А—Г–њ–њ—Л –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –і–ї—П —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–є –Њ–±—А–∞–±–Њ—В–Ї–Є –≤–Ј—П—В–Њ –≤—Б–µ–≥–Њ 30 —З–µ–ї–Њ–≤–µ–Ї –і–ї—П —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ–Њ—Б—В–Є —З–Є—Б–ї–µ–љ–љ–Њ—Б—В–Є –≥—А—Г–њ–њ. –Ъ–Њ–љ—В—А–Њ–ї—М–љ–∞—П –≥—А—Г–њ–њ–∞ –≤–Ї–ї—О—З–∞–ї–∞ 50 —З–µ–ї–Њ–≤–µ–Ї (20 –Љ—Г–ґ—З–Є–љ –Є 30 –ґ–µ–љ—Й–Є–љ –≤ –≤–Њ–Ј—А–∞—Б—В–µ 35вАУ52 –ї–µ—В) –±–µ–Ј –Ю–Т–° –Є –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ —Б–Є—Б—В–µ–Љ–љ—Л—Е –Є –∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ—Л—Е –њ–Њ—А–∞–ґ–µ–љ–Є–є —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є, –±–µ–Ј –≥–Є–њ–µ—А—В–Њ–љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–µ–Ј–љ–Є, –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–µ–Ј–љ–Є —Б–µ—А–і—Ж–∞, –Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ —В—П–ґ–µ–ї—Л—Е —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е –Є–љ—Д–µ–Ї—Ж–Є–є. –°—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ю–Т–° –њ–Њ —В–Є–њ—Г ¬Ђ—В—А–Њ–Љ–±–Њ–Ј –≤–µ—В–≤–µ–є –¶–Т–°¬ї –±—Л–ї–Њ 78 —З–µ–ї–Њ–≤–µ–Ї (52%); —Б —В—А–Њ–Љ–±–Њ–Ј–Њ–Љ –¶–Т–° вАУ 72 (48%). –С—Л–ї–Є –≤—Л—П–≤–ї–µ–љ—Л —Б–ї–µ–і—Г—О—Й–Є–µ —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П: –≥–Є–њ–µ—А—В–Њ–љ–Є—З–µ—Б–Ї–∞—П –±–Њ–ї–µ–Ј–љ—М вАУ —Г 56 –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Є—И–µ–Љ–Є—З–µ—Б–Ї–∞—П –±–Њ–ї–µ–Ј–љ—М —Б–µ—А–і—Ж–∞ вАУ —Г 30, –≤–∞—А–Є–Ї–Њ–Ј–љ–∞—П –±–Њ–ї–µ–Ј–љ—М –≤–µ–љ –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є вАУ —Г 15. –°—А–Њ–Ї–Є –љ–∞–±–ї—О–і–µ–љ–Є—П —Б–Њ—Б—В–∞–≤–Є–ї–Є –Њ—В 2 –љ–µ–і. –і–Њ 2-—Е –ї–µ—В.–Ы–∞–±–Њ—А–∞—В–Њ—А–љ—Л–µ –Љ–µ—В–Њ–і—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б–Є—Б—В–µ–Љ—Л –≥–µ–Љ–Њ—Б—В–∞–Ј–∞ –њ—А–Њ–≤–Њ–і–Є–ї–Є—Б—М —Б–Ї—А–Є–љ–Є–љ–≥–Њ–≤—Л–Љ–Є –Є —Б–њ–µ—Ж–Є–∞–ї—М–љ—Л–Љ–Є –Љ–µ—В–Њ–і–∞–Љ–Є –∞–≤—В–Њ–Љ–∞—В–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–є –Ї–Њ–∞–≥—Г–ї–Њ–Љ–µ—В—А–Є–Є: –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Д–∞–Ї—В–Њ—А–∞ –Т–Є–ї–ї–µ–±—А–∞–љ–і–∞ (—Д–Т), –∞–љ—В–Є—В—А–Њ–Љ–±–Є–љ–∞ III, –Р–Я–°, VIII—Д, –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ V—Д –≤ –њ–ї–∞–Ј–Љ–µ; –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є —Д–∞–Ї—В–Њ—А–∞ V –Ї –∞–Ї—В–Є–≤–Є—А–Њ–≤–∞–љ–љ–Њ–Љ—Г –њ—А–Њ—В–µ–Є–љ—Г –° вАУ –†–Р–Я–° –Є–ї–Є –Є–љ–і–µ–Ї—Б APC-—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є; –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–µ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ —А–∞—Б—В–≤–Њ—А–Є–Љ—Л—Е —Д–Є–±—А–Є–љ–Љ–Њ–љ–Њ–Љ–µ—А–љ—Л—Е –Ї–Њ–Љ–њ–ї–µ–Ї—Б–Њ–≤ (–†–§–Ь–Ъ); –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ —Д–Є–±—А–Є–љ–Њ–≥–µ–љ–∞ (–њ–Њ –Ъ–ї–∞—Г—Б—Г).
–Т—Л—П–≤–ї–µ–љ–Є–µ –Т–Р –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —П–і–Њ–≤—Л—Е —В–µ—Б—В–Њ–≤, –∞ —В–∞–Ї–ґ–µ –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—Й–Є—Е —В–µ—Б—В–Њ–≤ —Б –њ–ї–∞–Ј–Љ–Њ–є –і–Њ–љ–Њ—А–∞ –Є –Ї–Њ—А—А–Є–≥–Є—А—Г—О—Й–Є–Љ–Є —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–∞–Љ–Є. –І–µ—А–µ–Ј 12 –љ–µ–і. –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –њ–Њ–≤—В–Њ—А–љ–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ.
–Ю–њ—А–µ–і–µ–ї–µ–љ–Є–µ –Љ—Г—В–∞—Ж–Є–Є FV Leiden –Є –і—А—Г–≥–Є—Е –њ–Њ–ї–Є–Љ–Њ—А—Д–Є–Ј–Љ–Њ–≤ –≥–µ–љ–Њ–≤ –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ—Б—В–Є –Ї —В—А–Њ–Љ–±–Њ—Д–Є–ї–Є–Є –њ—А–Њ–≤–Њ–і–Є–ї–Є –Љ–µ—В–Њ–і–Њ–Љ –њ–Њ–ї–Є–Љ–µ—А–∞–Ј–љ–Њ–є —Ж–µ–њ–љ–Њ–є —А–µ–∞–Ї—Ж–Є–Є –≤ —А–µ–∞–ї—М–љ–Њ–Љ –≤—А–µ–Љ–µ–љ–Є (Real-time PCR). –†–∞–±–Њ—В–∞ –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М –љ–∞ –Ї–Њ–∞–≥—Г–ї–Њ–Љ–µ—В—А–µ CL-4 –њ—А–Њ–Є–Ј–≤–Њ–і—Б—В–≤–∞ Benk Elektroni—Б (–У–µ—А–Љ–∞–љ–Є—П), –∞–≥—А–µ–≥–Њ–Љ–µ—В—А–µ ¬Ђ–С–Є–Њ–ї–∞¬ї (–†–Њ—Б—Б–Є—П) –љ–∞ –±–∞–Ј–µ –ї–∞–±–Њ—А–∞—В–Њ—А–Є–Є –≥–µ–Љ–Њ—Б—В–∞–Ј–∞ –Є –ї–∞–±–Њ—А–∞—В–Њ—А–Є–Є –≥–µ–љ–µ—В–Є–Ї–Є –Њ–±–ї–∞—Б—В–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї—М–љ–Є—Ж—Л вДЦ 1 –≥. –Ъ–µ–Љ–µ—А–Њ–≤–Њ.
–С—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ –Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ: –≤–Є–Ј–Њ–Љ–µ—В—А–Є—П, —В–Њ–љ–Њ–Љ–µ—В—А–Є—П, –њ–µ—А–Є–Љ–µ—В—А–Є—П, –њ—А—П–Љ–∞—П –Њ—Д—В–∞–ї—М–Љ–Њ—Б–Ї–Њ–њ–Є—П; —Б–њ–µ—Ж–Є–∞–ї—М–љ—Л–µ –Љ–µ—В–Њ–і—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П: –Њ—Б–Љ–Њ—В—А –≥–ї–∞–Ј–љ–Њ–≥–Њ –і–љ–∞ —Б –ї–Є–љ–Ј–Њ–є –У–Њ–ї—М–і–Љ–∞–љ–∞, –§–Р–У –≥–ї–∞–Ј–љ–Њ–≥–Њ –і–љ–∞, –Њ–њ—В–Є—З–µ—Б–Ї–∞—П –Ї–Њ–≥–µ—А–µ–љ—В–љ–∞—П —В–Њ–Љ–Њ–≥—А–∞—Д–Є—П —Б–µ—В—З–∞—В–Ї–Є (–Ю–°–Ґ), –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–∞—П –њ–µ—А–Є–Љ–µ—В—А–Є—П.
–°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–∞—П –Њ–±—А–∞–±–Њ—В–Ї–∞ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –≤—Л–њ–Њ–ї–љ–µ–љ–∞ –љ–∞ –њ–µ—А—Б–Њ–љ–∞–ї—М–љ–Њ–Љ –Ї–Њ–Љ–њ—М—О—В–µ—А–µ —Б –њ–Њ–Љ–Њ—Й—М—О –њ–∞–Ї–µ—В–∞ –њ—А–Є–Ї–ї–∞–і–љ—Л—Е –њ—А–Њ–≥—А–∞–Љ–Љ Statistica 6.0 (Statsoft) for Windows. –°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ–Є —Б—З–Є—В–∞–ї–Є —А–∞–Ј–ї–Є—З–Є—П –њ—А–Є —Г—А–Њ–≤–љ–µ –Ј–љ–∞—З–Є–Љ–Њ—Б—В–Є p<0,05.
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Є –Њ–±—Б—Г–ґ–і–µ–љ–Є–µ
–Ш–Ј 150 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ю–Т–° –Т–Р –≤—Л—П–≤–Є–ї–Є —Г 32 (21%), –Є–Ј –љ–Є—Е –Т–Р –±–µ–Ј FV Leiden вАУ —Г 20 (13,3%), —Б–Њ—З–µ—В–∞–љ–Є–µ –Т–Р + FV Leiden –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ —Г 12 (8%). –Т—Б–µ–≥–Њ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ю–Т–° —В–Њ–ї—М–Ї–Њ —Б –Љ—Г—В–∞—Ж–Є–µ–є FV Leiden –±—Л–ї–Њ 11 (7,3%).–Р–љ–∞–ї–Є–Ј –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ —Б–Є—Б—В–µ–Љ—Л –≥–µ–Љ–Њ—Б—В–∞–Ј–∞ –±–Њ–ї—М–љ—Л—Е —Б –Ю–Т–° –≤ —В–∞–±–ї–Є—Ж–µ 1 –њ–Њ–Ї–∞–Ј—Л–≤–∞–µ—В, —З—В–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ 2-–є –≥—А—Г–њ–њ—Л –±–µ–Ј –Т–Р –Є —В–Њ–ї—М–Ї–Њ —Б –Љ—Г—В–∞—Ж–Є–µ–є FV Leiden –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –†–§–Ь–Ъ –њ–Њ–≤—Л—И–µ–љ—Л –љ–∞ 20%, –∞ —Д–Є–±—А–Є–љ–Њ–≥–µ–љ вАУ –љ–∞ 15% –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є 3-–є –≥—А—Г–њ–њ—Л. –Т 1-–є –≥—А—Г–њ–њ–µ –Њ—В–Љ–µ—З–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ –њ–Њ–≤—Л—И–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –†–§–Ь–Ъ –љ–∞ 37,5%, —Д–Є–±—А–Є–љ–Њ–≥–µ–љ–∞ вАУ –љ–∞ 20% –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б 3-–є –≥—А—Г–њ–њ–Њ–є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±–µ–Ј –Т–Р –Є –†–Р–Я–°. –Т 1-–є –≥—А—Г–њ–њ–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ—Л–Љ –і–µ—Д–µ–Ї—В–Њ–Љ FV —Б –Т–Р –≤–љ—Г—В—А–Є—Б–Њ—Б—Г–і–Є—Б—В–∞—П –∞–Ї—В–Є–≤–∞—Ж–Є—П —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ –±—Л–ї–∞ –≤—Л—И–µ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –∞–љ–∞–ї–Њ–≥–Є—З–љ—Л–Љ–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ—Л–Љ –і–µ—Д–µ–Ї—В–Њ–Љ, –љ–Њ –±–µ–Ј –Т–Р: —Б—Г–Љ–Љ–∞ –∞–Ї—В–Є–≤–љ—Л—Е —Д–Њ—А–Љ —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ –≤ 1-–є –≥—А—Г–њ–њ–µ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б–Њ 2-–є –≥—А—Г–њ–њ–Њ–є –±—Л–ї–∞ –±–Њ–ї—М—И–µ –љ–∞ 16,2%, –∞ —З–Є—Б–ї–Њ —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤, –≤–Њ–≤–ї–µ—З–µ–љ–љ—Л—Е –≤ –∞–≥—А–µ–≥–∞—В—Л, –≤—Л—И–µ –љ–∞ 26,3%. –Т 3-–є –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е —Б –Ю–Т–° –±–µ–Ј –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ—Д–µ–Ї—В–∞ –Є –Т–Р —В–∞–Ї–ґ–µ –±—Л–ї–Њ –Ј–љ–∞—З–Є–Љ–Њ–µ —Г—Б–Є–ї–µ–љ–Є–µ –≤–љ—Г—В—А–Є—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –∞–Ї—В–Є–≤–∞—Ж–Є–Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤, –љ–Њ –Љ–µ–љ–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ, —З–µ–Љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ—Л–Љ –і–µ—Д–µ–Ї—В–Њ–Љ –Є –±–µ–Ј –Т–Р вАУ –љ–∞ 10,7 –Є 16,4% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ.
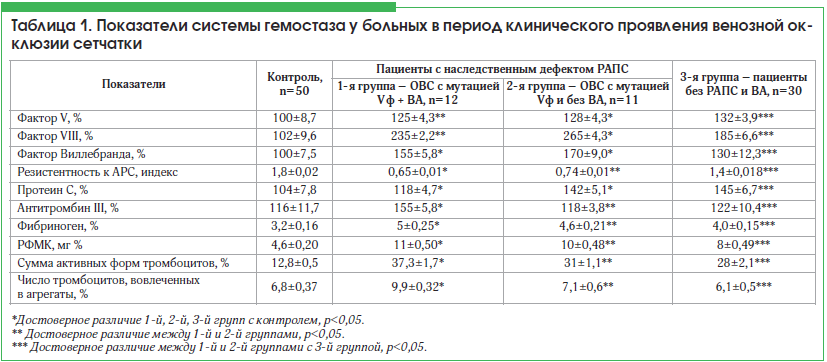
–£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ 1-–є –Є 2-–є –≥—А—Г–њ–њ –Њ—В–Љ–µ—З–∞–ї–Є—Б—М –њ–Њ–≤—Л—И–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є FV –љ–∞ 25% –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ї–Њ–љ—В—А–Њ–ї–µ–Љ, –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ –њ–Њ–≤—Л—И–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є VIII—Д –≤ 1-–є –Є 2-–є –≥—А—Г–њ–њ–∞—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –≤ 2,3 –Є 2,6 —А–∞–Ј–∞ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, –∞ —В–∞–Ї–ґ–µ –µ–µ –њ–Њ–≤—Л—И–µ–љ–Є–µ –љ–∞ 27 –Є 30% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є 3-–є –≥—А—Г–њ–њ—Л —Б –Ю–Т–° –±–µ–Ј –Т–Р –Є –†–Р–Я–°. –Т—Л—П–≤–ї–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Д–Т —Г –±–Њ–ї—М–љ—Л—Е —Б –Ю–Т–° –≤–Њ –≤—Б–µ—Е 3-—Е –≥—А—Г–њ–њ–∞—Е –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ї–Њ–љ—В—А–Њ–ї–µ–Љ вАУ –љ–∞ 55, 70 –Є 30% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ. –≠—В–Њ –і–Њ–Ї–∞–Ј—Л–≤–∞–µ—В, —З—В–Њ —Г –≤—Б–µ—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ю–Т–° –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–µ —Н–љ–і–Њ—В–µ–ї–Є—П –≤–µ–љ–Њ–Ј–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤ –Є–≥—А–∞–µ—В –≤–µ–і—Г—Й—Г—О —А–Њ–ї—М –≤ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–µ –Ю–Т–°. –Ю–і–љ–∞–Ї–Њ –њ–Њ–≤—Л—И–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Д–Т —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ 1-–є –Є 2-–є –≥—А—Г–њ–њ –±—Л–ї–Њ –≤—Л—И–µ, —З–µ–Љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ 3-–є –≥—А—Г–њ–њ—Л, –љ–∞ 16 –Є 23,5% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ.
–£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ю–Т–° 2-–є –Є 3-–є –≥—А—Г–њ–њ, –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л—Е –≤ –Њ—Б—В—А–Њ–є —Д–∞–Ј–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –њ–Њ–≤—Л—И–µ–љ—Л –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –Ї–Њ–љ—В—А–Њ–ї—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Я–°. –Ш–љ–і–µ–Ї—Б –†–Р–Я–° –±—Л–ї –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–љ–Є–ґ–µ–љ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –Ї–Њ–љ—В—А–Њ–ї—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ 1-–є –≥—А—Г–њ–њ—Л –љ–∞ 64%, 2-–є –≥—А—Г–њ–њ—Л вАУ –љ–∞ 58,9%. –Я–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є 3-–є –≥—А—Г–њ–њ—Л, –≥–і–µ –Њ—В—Б—Г—В—Б—В–≤–Њ–≤–∞–ї–Є –Т–Р –Є –†–Р–Я–°, –Є–љ–і–µ–Ї—Б –†–Р–Я–° –±—Л–ї –љ–Є–ґ–µ –≤ 1-–є –Є 2-–є –≥—А—Г–њ–њ–∞—Е –љ–∞ 53,6 –Є 46,4% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ. –°—В–µ–њ–µ–љ—М —Б–љ–Є–ґ–µ–љ–Є—П –Є–љ–і–µ–Ї—Б–∞ –†–Р–Я–° –љ–∞ —Д–Њ–љ–µ –Љ—Г—В–∞—Ж–Є–Є FV Leiden —Г—Б—Г–≥—Г–±–ї—П–µ—В—Б—П –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є –Т–Р.
–£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ю–Т–° –≤ 1-–є, 2-–є –Є 3-–є –≥—А—Г–њ–њ–∞—Е –±—Л–ї–Є –њ–Њ–≤—Л—И–µ–љ—Л –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –Ї–Њ–љ—В—А–Њ–ї—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Я–° вАУ –љ–∞ 13,4, 36,5 –Є 39,4%; —В–∞–Ї–ґ–µ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М –љ–µ–Ї–Њ—В–Њ—А–Њ–µ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ –њ–Њ–≤—Л—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –∞–љ—В–Є—В—А–Њ–Љ–±–Є–љ–∞ III –≤–Њ –≤—Б–µ—Е 3-—Е –≥—А—Г–њ–њ–∞—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О –Ї–Њ–љ—В—А–Њ–ї–µ–Љ вАУ –љ–∞ 33,6, 1,7 –Є 5,18%, —З—В–Њ –Љ–Њ–ґ–љ–Њ –Њ–±—К—П—Б–љ–Є—В—М –Ї–Њ–Љ–њ–µ–љ—Б–∞—В–Њ—А–љ—Л–Љ–Є –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞–Љ–Є.
–£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ю–Т–° –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –Љ—Г—В–∞—Ж–Є–µ–є FV Leiden –Є –Т–Р –≤–Њ –≤—Б–µ—Е 3-—Е –≥—А—Г–њ–њ–∞—Е –њ–Њ–≤—Л—И–µ–љ —Г—А–Њ–≤–µ–љ—М –±–µ–ї–Ї–∞ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П —Д–Є–±—А–Є–љ–Њ–≥–µ–љ–∞ –љ–∞ 56,3, 43,3 –Є 25% –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ї–Њ–љ—В—А–Њ–ї–µ–Љ. –С–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–є —Г—А–Њ–≤–µ–љ—М —Д–Є–±—А–Є–љ–Њ–≥–µ–љ–∞ –≤ 1-–є –Є 2-–є –≥—А—Г–њ–њ–∞—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ю–Т–° –Њ—В–Љ–µ—З–µ–љ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б 3-–є –≥—А—Г–њ–њ–Њ–є вАУ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ –≤ 1,5 –Є 1,2 —А–∞–Ј–∞.
–£–≤–µ–ї–Є—З–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є V—Д –Љ–Њ–ґ–љ–Њ –Њ–±—К—П—Б–љ–Є—В—М –њ—А–Є—Б—Г—В—Б—В–≤–Є–µ–Љ –≤ –Ї—А–Њ–≤–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ 1-–є –Є 2-–є –≥—А—Г–њ–њ FV Leiden; –Њ–љ –±–Њ–ї–µ–µ –Љ–µ–і–ї–µ–љ–љ–Њ –њ–Њ–і–≤–µ—А–≥–∞–µ—В—Б—П –њ—А–Њ—В–µ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Њ–Љ—Г —А–∞—Б—Й–µ–њ–ї–µ–љ–Є—О –∞–Ї—В–Є–≤–Є—А–Њ–≤–∞–љ–љ—Л–Љ –Я–°, –Є –і–µ—Д–µ–Ї—В–љ—Л–є V—Д –љ–∞–Ї–∞–њ–ї–Є–≤–∞–µ—В—Б—П –≤ –Ї—А–Њ–≤–Є. FV Leiden –±—Л—Б—В—А–µ–µ —Б—В–∞–±–Є–ї–Є–Ј–Є—А—Г–µ—В –њ—А–Њ—В—А–Њ–Љ–±–Є–љ–∞–Ј—Г (XIa, VIIIa, —Д–Т), –Є–і–µ—В –њ—А–µ–≤—А–∞—Й–µ–љ–Є–µ –њ—А–Њ—В—А–Њ–Љ–±–Є–љ–∞ –≤ —В—А–Њ–Љ–±–Є–љ. –Ф–µ—Д–µ–Ї—В–љ—Л–є V—Д –Љ–µ–і–ї–µ–љ–љ–Њ –Є–љ–∞–Ї—В–Є–≤–Є—А—Г–µ—В—Б—П –Я–°, –њ–Њ—Н—В–Њ–Љ—Г –і–Њ–ї–≥–Њ —Б–Њ—Е—А–∞–љ—П–µ—В—Б—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М VIII—Д, —З–µ–Љ –Є –Њ–±—К—П—Б–љ—П–µ—В—Б—П –µ–≥–Њ –њ–Њ–≤—Л—И–µ–љ–љ—Л–є —Г—А–Њ–≤–µ–љ—М. –Т–Р —А–µ–∞–≥–Є—А—Г–µ—В —Б –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞–Љ–Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —Н–љ–і–Њ—В–µ–ї–Є—П –Є –≤—Л–Ј—Л–≤–∞–µ—В —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Б–Є–љ—В–µ–Ј–∞ —Д–Т, VIII—Д, –∞ —В–∞–Ї–ґ–µ —Б—В–Є–Љ—Г–ї–Є—А—Г–µ—В —В—А–Њ–Љ–±–Њ—Ж–Є—В—Л —З–µ—А–µ–Ј –Љ–µ–Љ–±—А–∞–љ–љ—Л–µ —А–µ—Ж–µ–њ—В–Њ—А—Л; —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є—О –Є–Ј —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ –≥–Є—Б—В–∞–Љ–Є–љ–∞, —Б–µ—А–Њ—В–Њ–љ–Є–љ–∞ –Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–∞—А–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ 3 –Є 4, –њ–Њ–і–∞–≤–ї—П–µ—В —Б–Є–љ—В–µ–Ј –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–∞ (–Љ–Њ—Й–љ–Њ–≥–Њ –і–µ–Ј–∞–≥—А–µ–≥–∞–љ—В–∞ –Є –і–Є–ї—П—В–∞—В–Њ—А–∞ —Б–Њ—Б—Г–і–Њ–≤), –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —В—А–Њ–Љ–±–Њ–Љ–Њ–і—Г–ї–Є–љ–∞ –Є –њ—А–Њ—В–µ–Є–љ–Њ–≤ –° –Є S, —В–µ–Љ —Б–∞–Љ—Л–Љ –њ—А–Њ–≤–Њ—Ж–Є—А—Г–µ—В —Б–Њ—Б—В–Њ—П–љ–Є–µ –≥–Є–њ–µ—А–Ї–Њ–∞–≥—Г–ї—П—Ж–Є–Є. –Т–Р –љ–∞—А—Г—И–∞–µ—В –љ–Њ—А–Љ–∞–ї—М–љ—Г—О —А–µ–≥—Г–ї—П—Ж–Є—О —Б–Є—Б—В–µ–Љ—Л –≥–µ–Љ–Њ—Б—В–∞–Ј–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В –њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ –њ—А–Њ–Ї–Њ–∞–≥—Г–ї—П–љ—В–Њ–≤ –Є —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –∞–љ—В–Є–Ї–Њ–∞–≥—Г–ї—П–љ—В–Њ–≤, –њ–Њ–і–і–µ—А–ґ–Є–≤–∞–µ—В –∞—Б–µ–њ—В–Є—З–µ—Б–Ї–Њ–µ –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ –≤ –≤–µ–љ–Њ–Ј–љ–Њ–є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–µ, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –∞–Ї—В–Є–≤–∞—Ж–Є–Є —В—А–Њ–Љ–±–Њ–≥–µ–љ–µ–Ј–∞ –≤ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–Љ —А—Г—Б–ї–µ —Б–Њ—Б—Г–і–Њ–≤ —Б–µ—В—З–∞—В–Ї–Є.
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ю–Т–° 1-–є –Є 2-–є –≥—А—Г–њ–њ –≤—Л—П–≤–ї–µ–љ—Л –љ–∞—А—Г—И–µ–љ–Є—П –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є —Б –Љ–Є–Ї—А–Њ–≤–∞–Ј–Њ–Њ–Ї–Ї–ї—О–Ј–Є–≤–љ—Л–Љ–Є –њ—А–Њ—Ж–µ—Б—Б–∞–Љ–Є –≤ —Б–Њ—Б—Г–і–∞—Е —Б–µ—В—З–∞—В–Ї–Є. –§–ї—О–Њ—А–µ—Б—Ж–µ–љ—В–љ–∞—П –∞–љ–≥–Є–Њ–≥—А–∞—Д–Є—П –≥–ї–∞–Ј–љ–Њ–≥–Њ –і–љ–∞ —Г —Н—В–Є—Е –±–Њ–ї—М–љ—Л—Е –і–Њ–Ї–∞–Ј—Л–≤–∞–µ—В –љ–∞–ї–Є—З–Є–µ –ї–Є–Ї–µ–і–ґ-—Б–Є–љ–і—А–Њ–Љ–∞, –Њ—В—Б—Г—В—Б—В–≤–Є–µ –Ї–∞–њ–Є–ї–ї—П—А–љ–Њ–є –њ–µ—А—Д—Г–Ј–Є–Є –Є –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –ї–Њ–Ї–∞–ї—М–љ–Њ–є –Є—И–µ–Љ–Є–Є –≤ —Б–µ—В—З–∞—В–Ї–µ вАУ –Ї–∞–Ї –≤ –µ–µ —Ж–µ–љ—В—А–∞–ї—М–љ—Л—Е –Њ—В–і–µ–ї–∞—Е, —В–∞–Ї –Є –љ–∞ –њ–µ—А–Є—Д–µ—А–Є–Є (—А–Є—Б. 1, 2).
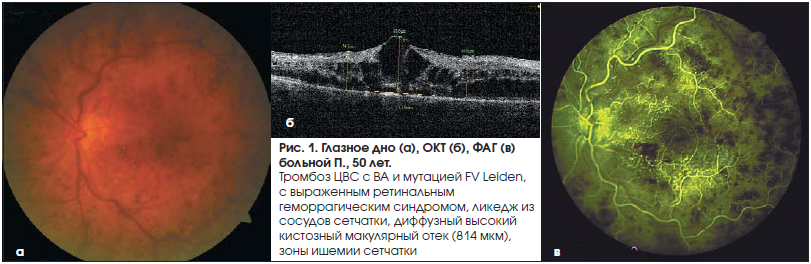
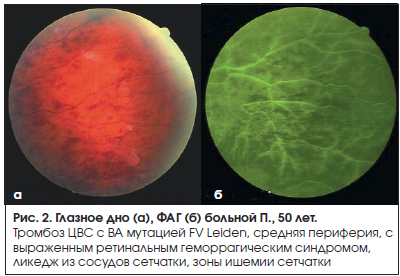
–†–µ—Ж–Є–і–Є–≤—Л –Ю–Т–° –Њ—В–Љ–µ—З–µ–љ—Л –≤ 35% —Б–ї—Г—З–∞–µ–≤, –њ–Њ–≤—В–Њ—А–љ—Л–µ –≥–µ–Љ–Њ—Д—В–∞–ї—М–Љ—Л вАУ –≤ 30%. –£ –≤—Б–µ—Е —Н—В–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ї–∞–Ї –≤ 1-–є, —В–∞–Ї –Є –≤–Њ 2-–є –≥—А—Г–њ–њ–µ –љ–∞–±–ї—О–і–∞–ї—Б—П —В—А–Њ–Љ–±–Њ–Ј –¶–Т–° –Є –µ–µ –≤–µ—В–≤–µ–є —Б –≤—Л—Б–Њ–Ї–Є–Љ –Ї–Є—Б—В–Њ–Ј–љ—Л–Љ –Љ–∞–Ї—Г–ї—П—А–љ—Л–Љ –Њ—В–µ–Ї–Њ–Љ (—Б—А–µ–і–љ—П—П —В–Њ–ї—Й–Є–љ–∞ —Б–µ—В—З–∞—В–Ї–Є –≤ –Љ–∞–Ї—Г–ї–µ –њ–Њ –Ю–°–Ґ вАУ 790¬±20 –Љ–Ї–Љ). –Я–µ—А—Б–Є—Б—В–Є—А—Г—О—Й–Є–є –Ї–Є—Б—В–Њ–Ј–љ—Л–є –Љ–∞–Ї—Г–ї—П—А–љ—Л–є –Њ—В–µ–Ї –Њ—В–Љ–µ—З–∞–ї—Б—П —Г 8% –њ–∞—Ж–Є–µ–љ—В–Њ–≤.
–Т—Л–≤–Њ–і—Л:
1. –Ю–Т–° —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Є–Љ–µ—О—Й–Є—Е –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ—Г—О —В—А–Њ–Љ–±–Њ—Д–Є–ї–Є—О, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Г—О –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–Љ –і–µ—Д–µ–Ї—В–Њ–Љ V—Д –Є –µ–≥–Њ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М—О –Ї –∞–Ї—В–Є–≤–Є—А–Њ–≤–∞–љ–љ–Њ–Љ—Г –Я–° (–†–Р–Я–°), –∞ —В–∞–Ї–ґ–µ –њ–Њ—П–≤–ї–µ–љ–Є–µ–Љ –≤ –Ї—А–Њ–≤–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Т–Р. –°—В–µ–њ–µ–љ—М —Б–љ–Є–ґ–µ–љ–Є—П –Є–љ–і–µ–Ї—Б–∞ –†–Р–Я–° –љ–∞ —Д–Њ–љ–µ –Љ—Г—В–∞—Ж–Є–Є FV Leiden —Г—Б—Г–≥—Г–±–ї—П–µ—В—Б—П –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є –Т–Р.2. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ю–Т–° –љ–∞ —Д–Њ–љ–µ FV Leiden –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –њ–Њ–≤—Л—И–µ–љ–∞ –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Д–∞–Ї—В–Њ—А–Њ–≤ V, VIII, –Т–Є–ї–ї–µ–±—А–∞–љ–і–∞, —Б–љ–Є–ґ–µ–љ –†–Р–Я–°, –∞ –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –Т–Р –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г—Б—Г–≥—Г–±–ї—П—О—В—Б—П —Н–љ–і–Њ—В–µ–ї–Є–Њ–Ј –Є —В—А–Њ–Љ–±–Є–љ–µ–Љ–Є—П, –∞–Ї—В–Є–≤–љ—Л–є —В—А–Њ–Љ–±–Њ–≥–µ–љ–µ–Ј –≤ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–Љ —А—Г—Б–ї–µ —Б–µ—В—З–∞—В–Ї–Є, —З—В–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –њ—А–Њ—П–≤–ї—П–µ—В—Б—П —В—А–Њ–Љ–±–Њ–≥–µ–Љ–Њ—А—А–∞–≥–Є—З–µ—Б–Ї–Є–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ.
3. –Я–Њ–ї—Г—З–µ–љ–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –і–Њ–Ї–∞–Ј—Л–≤–∞—О—В –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ–ї–Є–Љ–Њ—А—Д–Є–Ј–Љ–∞ –≥–µ–Љ–Њ—Б—В–∞–Ј–∞ –Є –Т–Р —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ю–Т–° –і–ї—П —Г—В–Њ—З–љ–µ–љ–Є—П –≥–µ–љ–µ–Ј–∞ —В—А–Њ–Љ–±–Њ–Ј–∞ –≤–µ–љ —Б–µ—В—З–∞—В–Ї–Є, –њ–Њ—Б—В–Њ—П–љ–љ–Њ–≥–Њ –ї–∞–±–Њ—А–∞—В–Њ—А–љ–Њ-–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П –≥–µ–Љ–Њ—Б—В–∞–Ј–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ю–Т–° –і–ї—П –њ—А–Њ–≤–µ–і–µ–љ–Є—П —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –∞–і–µ–Ї–≤–∞—В–љ–Њ–є –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є –∞–љ—В–Є–Ї–Њ–∞–≥—Г–ї—П–љ—В–љ–Њ–є, –і–µ–Ј–∞–≥—А–µ–≥–∞–љ—В–љ–Њ–є, –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ–Њ–є –Є –∞—Д—Д–µ—А–µ–љ—В–љ–Њ–є —В–µ—А–∞–њ–Є–Є.












