L.A. Basinskaya
GOU VPO Amur State Medical Academy, Blagoveschensk
Purpose: to develop method of addressed drug delivery to the retina and evaluate the efficacy of treatment of diabetic retinopathy with Retianalamin in combination with trophic sclerectomy and laser treatment.
Materials and methods: The assessment of Retinalamin treatment efficacy was carried out on 73 patients with diabetic retinopathy. Patients were divided into 2 groups. In the main group the drug was introduced to posterior pole of eyeball under conjunctiva (0.5 ml of solution). Beforehand trophic sclerectomy in upper external segment of eyeball was carried out with further argon laser coagulation of retina in the site of projection of trophic sclerectomy. Patients of the control group received parabulbar Retinalamin injections. The course of treatment lasted 10 days.
Results: After the treatment in the main group visual acuity improved by 0, 25 in comparison with 0, 12 in control group. There was also improvement of rheographic indices and condition of the eye fundus in the both groups. Stabilization of visual function was reached in 71% of patients as a result of complex method of treatment.
Conclusion: Complex method could be recommended for usage in patients with diabetic retinopathy to reach the stabilization of visual functions.
Сложной и не до конца решенной является проблема лечения больных с диабетической ретинопатией. Для устранения патологических явлений на сетчатке при диабетической ретинопатии предложено довольно много медикаментозных и хирургических методик [4–6]. Однако проблема повышения эффективности лечения больных с диабетической ретинопатией остается крайне актуальной, поскольку большинство методик влияют на следствия поражения сетчатки, а не на патогенетические звенья развития ретинопатии.
С учетом многообразия патогенетических факторов заболевания основные методы лечения диабетической ретинопатии направлены на улучшение гемодинамики и обменных процессов в сетчатке и предотвращение дальнейшего прогрессирования заболевания [2].
Существующие методы лечения диабетической ретинопатии наряду с рядом преимуществ (отсутствие травматического фактора, общедоступность и универсальность) имеют свои недостатки, и главный из них – отсутствие возможности воздействовать непосредственно на очаг поражения, что снижает эффективность проводимого лечения.
В связи с этим стоит актуальная задача разработки эффективного метода лечения диабетической ретинопатии, который сочетал бы в себе метод адресной доставки препарата непосредственно к сетчатке, способствовал улучшению зрительных функций и стабилизации процесса в течение длительного времени [1,3].
В этом плане особого внимания заслуживает дальнейший поиск и детальная разработка комплексного подхода для лечения этой тяжелой патологии, в основе которого лежит комбинированный механизм действия.
Цель работы: разработать метод адресной доставки препарата к сетчатке и оценить эффективность лечения диабетической ретинопатии препаратом ретиналамин в сочетании с трофической склерэктомией и лазерным лечением.
Материалы и методы
Под наблюдением находилось 73 пациента (123 глаза) с сахарным диабетом 2 типа в возрасте от 36 до 68 лет. Препролиферативная диабетическая ретинопатия диагностирована у всех пациентов. В 81,2% случаев процесс носил двусторонний характер.
Все пациенты были разделены на две группы, сопоставимые по возрасту, полу, типам и длительности СД и тяжести диабетической ретинопатии.
В 1–ю (основную) группу вошел 31 пациент (60 глаз), здесь проводилось комплексное лечение, включающее хирургическое, лазерное и медикаментозное воздействие. Первым этапом для обеспечения адресной доставки препарата проводили трофическую склерэктомию (ТСЭ) в верхнем наружном квадранте. Вторым этапом – направленную аргонлазеркоагуляцию в проекции ТСЭ. Третьим этапом – под конъюнктиву в верхне–наружный квадрант вводили ретиналамин по 0,5 мл. Курс лечения – 10 дней.
Во 2–ю (контрольную) группу вошли 42 пациента (63 глаза) с диабетической ретинопатией, которым проводилось медикаментозное лечение. Парабульбарные инъекции ретиналамина по 0,5 мл. Курс лечения 10 дней.
Офтальмологическое обследование включало: визометрию, компьютерную статическую периметрию, офтальмоскопию, реоофтальмографию, допплерографию, электрофизиологическое исследование.
Результаты лечения
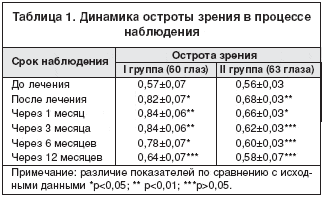
Изменения остроты зрения после лечения представлены в таблице 1. После проведенного курса лечения в основной группе улучшение остроты зрения произошло на 0,25. Повышение остроты зрения наблюдали в 88,9%. К 6–му месяцу отмечали постепенное снижение показателей остроты зрения в среднем на 0,06. Через год средний уровень остроты зрения достоверно не отличался от исходного.
В контрольной группе после проведения курса медикаментозной терапии острота зрения увеличилась на 0,12, что на 0,13 меньше, чем в основной группе. В отдаленном периоде (6–12 месяцев) средний показатель остроты зрения снижался практически до исходного уровня (табл. 1).
Расширение полей зрения в основной группе происходило за счет исчезновения относительных скотом и перехода абсолютных скотом в относительные. Количество нормально воспринимаемых точек возрастало в среднем на 21%. Поля зрения непосредственно после лечения улучшились у 64% больных, в 36% случаев поля зрения не изменились, случаев ухудшения не наблюдалось.
В контрольной группе сразу после лечения количество относительных скотом снизилось до 13,4%. Затем их количество постепенно увеличивалось и к 6–му месяцу наблюдения практически не отличалось от исходных показателей.
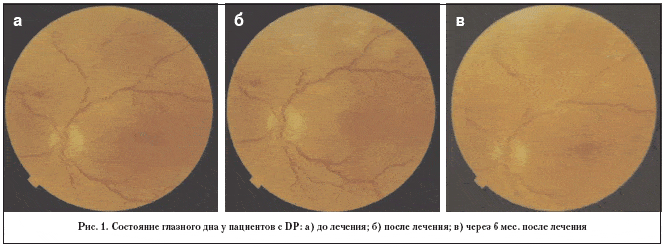
В офтальмоскопической картине глазного дна у пациентов с ДР отмечено улучшение картины глазного дна за счет исчезновения геморрагий, микроаневризм (рис. 1).
Анализ реограмм показал достоверный рост реографического коэффициента в основной группе сразу после курса лечения в среднем на 0,61±0,07д. Более поздние контрольные исследования выявили тенденцию к стабилизации этого показателя в сроки от 3 до 6 месяцев. Через год уровень реографического коэффициента превышал исходные значения на 0,44±0,06д.
В контрольной группе после курса медикаментозной терапии был также отмечен рост реографического коэффициента в среднем по группе на 0,3±0,06д. Дальнейшее наблюдение показало, что такой уровень реографического коэффициента сохранялся от 1 до 6 месяцев, затем мы отмечали тенденцию к его снижению (уже через 12 месяцев после лечения он практически не отличается от исходного).
Значительное снижение линейных скоростей кровотока в глазничной артерии до лечения было выявлено у пациентов в основной группе. После курса лечения в основной группе максимальная скорость кровотока увеличилась на 2,8±0,9 см/с. К 6–му месяцу динамического наблюдения этот показатель стал снижаться, оставаясь, тем не менее, выше исходного уровня. Через год он приближался к показателям, регистрированным до лечения.
В контрольной группе систолическая скорость кровотока в глазничной артерии после лечения увеличилась на 1,8±0,6 см/с. После 3–х месяцев наблюдения систолическая скорость кровотока в глазничной артерии снизилась до исходных цифр – 33,3±0,7 см/с.
При проведении общей электроретинограммы были получены следующие результаты: увеличение амплитуды «а» волны в основной группе сразу после курса лечения в среднем на 11,8±2,1 мкВ. Состояние стабилизации амплитуды «а» волны сохранялось в течение полугода, когда средние значения этого показателя определялись на уровне 37,2±1,3 мкВ. В более поздние сроки (6 месяцев) после лечения амплитуда «а» волны имела тенденцию к некоторому снижению (до 35,4±2,3 мкВ).
В контрольной группе глаз было отмечено повышение среднего уровня амплитуды «а» волны непосредственно после лечения на 9,1±0,8 мкВ. Однако уже через полгода наблюдения выявлено снижение среднего уровня амплитуды «а» волны до 23,3±1,1 мкВ. В более поздние сроки было установлено уменьшение значений амплитуды «а» волны практически до исходного уровня.
После лечения средний показатель амплитуды «b» волны достоверно увеличился на 37,9±11,2 мкВ. Относительно высокий уровень этого показателя был отмечен и при дальнейшем наблюдении. В отдаленные сроки через 12 месяцев наблюдения, несмотря на некоторое снижение уровня амплитуды «b» волны до 233,8±10,1 мкВ, он оставался все же выше исходного.
В контрольной группе было отмечено повышение среднего уровня амплитуды «b» волны непосредственно после лечения на 33,2±10,1 мкВ. Однако уже через полгода наблюдения выявлено снижение амплитуды «b» волны до 198,6±10,1 мкВ. В более поздние сроки было установлено снижение значений амплитуды «b» волны практически до исходного уровня.
Таким образом, применение ретиналамина при лечении диабетической ретинопатии является патогенетически обоснованным. Достигнуто значительное улучшение зрительных функций. По–нашему мнению, это связано с фармакологическим действием лекарственного препарата, а также способом его введения. При введении лекарственного препарата посредством ТСЭ и направленной аргонлазеркоагуляции возникает возможность усилить степень проникновения во внутренние стуктуры глазного яблока и добиться максимального эффекта ретиналамина.
Отдаленные результаты лечения свидетельствуют, что стабилизация диабетического процесса после парабульбарных инъекций наступила в 39% случаев, после комплексного метода у 71% пациентов.
Данный метод лечения позволяет проводить активную медикаментозную терапию, добиваясь улучшения зрительных функций, что дает возможность использовать предложенное лечение, как метод выбора при отсутствии стабилизации процесса у больных с диабетической ретинопатией. Методику подведения лекарственного препарата можно выполнять повторно, в любом квадранте глазного яблока.
Выводы
1. Разработан способ адресной доставки лекарственного препарата к заднему отрезку глаза в лечении диабетической ретинопатии, включающий выполнение трофической склерэктомии, с последующей направленной лазеркоагуляцией и медикаментозной терапией.
2. Комплексный метод лечения диабетической ретинопатии обеспечивает устойчивую стабилизацию зрительных функций у 71% пациентов в течение 12 месяцев после лечения.
Литература
1) Беляев, В. С. О возможности хирургического лечения и профилактике дистрофии сетчатой оболочки, зрительного нерва / В. С. Беляев, Ж. Х. Госсен // Вестн. офтальмологии. – 1983. – № 6. – С. 18 –21.
2) Киселев, Г. А. Лазерное излучение: действие на распределение лекарственных веществ в тканях глаза / Г. А. Киселев, О. И. Лебедев, В. С. Поспелов //Вестн. офтальмологии. – 1988. – № 2. – С. 40–43.
3) Нестеров А.П., Егоров Е.А., Егоров А.Е., Калабухова Л.В. и др //Новый путь введения лекарственных веществ при заболеваниях заднего отрезка глаза и использование его для лечения глаукомной оптической нейропатии..// Клиническая офтальмология.– 2000.– №2.– том 1.– С. 39–41.
4) Tang, S. Expression of intracellular adgesion molecule–1 (ICAM–1) and vascular cell adgesion molecule–1 (VCAM–1) on proliferating vascular endothelial cells in diabetic epiretinal membranes / S. Tang, K. C. Le–Ruppert, V. P. Gabel // Br J Ophthalmol. – 1994. – Vol.78, № 5. – P. 370 – 376.
5) Van der Fiji, J. W. Danaparoid sodium lowers proteinuria in nephropathy / J. W. Van der Fiji, F. J. Van der Woude, P. H. Geelhoed–Duijvestijn // J. Am. Soc. Nephrol. – 1997. – Vol. 8, № 3. – P. 456 – 462.
6) Van der Fiji, J. W. Effect of danaparoid sodium on hard exudates in diabetic retinopathy / J. W. Van der Fiji, F. J. Van der Woude, W. Swart // Lancet. – 1997. – Vol. 350, № 9093. – P. 1743 –1745.
7) Van der Fiji, J. W Danaparoid sodium in diabetic retinopathy / J. W. Van der Fiji, F. J. Van der Woude, P. H. Geelhoed // Lancet. – 1998. – Vol. 351, № 9094. – P. 1743–1744.












