In article indications for radiotherapy of neoplasms of organ of vision and optimal doses of irradiation are based on the authors own long experience and literature data analysis, mostly of the late decade.
Лучевая терапия, как метод лечения, используется практически при опухолях любой локализации, в том числе и при опухолях органа зрения. Она представлена контактным облучением, получившим название брахитерапия, внутритканевым и наружным облучением (облучение электронным, узким медицинским протонным пучком, дистанционная и короткодистанционная рентгенотерапия). В офтальмоонкологии получили распространение брахитерапия и наружное облучение.
Брахитерапия
Внутриглазные опухоли
Угроза лучевых поражений тканей глаза, возникающих при наружном облучении, долгое время ограничивала использование лучевой терапии при внутриглазных опухолях.
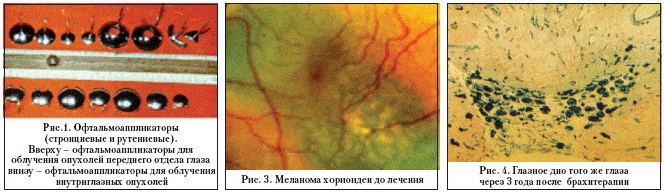
Идея локального разрушения хориоидальной меланомы с помощью контактного радиоактивного облучения появилась в 1930 г., когда Moore Р. [48] впервые ввел в склеру пораженного глаза родон. Позднее Stallard Н. [57], а затем Ellsworth R. [39] предложили использовать пластинки с радиоактивным кобальтом, повторяющие по своей форме наружную кривизну глаза. Seely R. и Buret H. [54] для лечения внутриглазных меланом применяли радиоактивный йод. Однако серьезные осложнения со стороны глаза, которые возникали при облучении, потребовали создания новых, более щадящих и не менее мощных рутениевых и стронциевых офтальмоаппликаторов [2,22,47] (рис. 1).
Особенность поглощения бета–излучения в биологических тканях позволяет создавать в опухоли губительную для ее ткани терапевтическую дозу облучения, почти не воздействуя на окружающие ткани. Энергия излучения изотопов рутения–106 выше, чем изотопов стронция–90, что определяет соответственно большую проникающую способность их бета–частиц. Офтальмоаппликаторы позволяют создавать дозные поля, обеспечивающие эффективное облучение опухолей хориоидеи и сетчатки, располагающихся практически в любом отделе глазного дна (рис. 2). Облучение возможно при непрозрачных средах, любых размерах отслойки сетчатки. Стронциевые офтальмоаппликаторы позволяют облучать новообразования толщиной до 4 мм, рутениевые – до 6 мм [6, 8]. Максимальный диаметр облучаемой опухоли зависит от типа аппликатора, однако следует учитывать, что существующие большие (22 мм) офтальмоаппликаторы имеют максимальный рабочий диаметр 19 мм. Брахитерапия может использоваться, как самостоятельный метод лечения, а также комбинироваться с лазеркоагуляцией, фотодинамической терапией [4, 7, 29, 34, 51]. В зарубежных центрах достаточно широко используют офтальмоаппликаторы с 125–I [45, 53]. Важной составляющей лучевого лечения злокачественных внутриглазных опухолей является индивидуальное планирование. Для него необходимы следующие показатели: толщина опухоли, ее диаметры (радиальный и меридиональный), точная локализация опухоли, переднезадний размер глаза, состояние склеры над опухолью, наличие необходимого офтальмоаппликатора и возможность визуального контроля за его положением [12].
Многолетний опыт мировой практики использования брахитерапии при увеальных меланомах доказал возможность ее применения как альтернативы энуклеации (рис. 3). Однако использование офтальмоаппликаторов ограничивается толщиной опухоли. С целью повышения эффективности лечения используют более мощные источники излучения [45,53] или большие дозы облучения, что, естественно, увеличивает частоту и тяжесть лучевых осложнений.
Фактором, потенцирующим брахитерапию, расширяющим ее возможности, является интракорпоральное облучение опухоли радионуклидом 59–Fe [26,27]. Интракорпоральное облучение меланомы хориоидеи в виде таблеток наведенной активностью 0,8мкКu сопровождается распространением радионуклида током крови с избирательным накоплением его в ткани меланомы (рис. 4). Вполне вероятно, что длительный прием 59–Fe может оказаться превентивным лечением возможных гематогенных метастазов меланомы [12,14].
При ретинобластоме брахитерапия, как составляющая комбинированного лечения, позволяющего сохранить пораженный глаз, находит все большее применение [9,10,24,55].
Главным залогом успешной брахитерапии внутриглазных опухолей является выбор поглощенной дозы. При расчете ее обязательно следует учитывать тип аппликатора, только тогда можно планировать лечение. В противном случае рекомендации для облучения, которые иногда появляются на страницах журналов, могут оказаться абсурдными [28]. Суммарная очаговая доза для меланомы хориоидеи при использовании стронциевых аппликаторов должна составлять от 200 до 270 Гр, при облучении рутениевыми аппликаторами – 120–160 Гр При облучении ретинобластомы рутениевым аппликатором с учетом радиочувствительности опухоли и возраста больных суммарная очаговая доза на вершине опухоли колеблется в пределах 40–80 Гр (с учетом толщины опухоли, площади поражения). Локальное облучение ретинобластомы эффективно только в комбинации с полихимиотерапией, для проведения которой используется несколько протоколов [1, 9, 33, 44, 49, 50 и др].
Многолетние наблюдения за больными, которым в нашем отделе проводилась брахитерапия с индивидуальным планированием, свидетельствуют о том, что можно добиться максимального терапевтического эффекта при минимальных осложнениях [11, 13].
Оценка результатов лечения – задача трудная [42]. Единых критериев такой оценки нет. Для разрешения этого вопроса мы проанализировали чуть менее 1000 историй болезни больных увеальной меланомой, леченных в нашем отделе. Длительность наблюдения за больными в среднем составила 7,8 года. Эффективность брахитерапии оценивали не ранее 6–8 месяцев после начала лечения, когда появлялись признаки уплощения опухоли, вокруг нее формировался четкий хориоретинальный рубец. Сроки оценки эффективности лечения зависели от исходной толщины опухоли, размеров ее максимального диаметра. При маленьких опухолях (толщиной до 1,5 мм и максимальном диаметре до 10 мм) регрессию опухоли можно наблюдать через 6 месяцев. При опухолях больших размеров регрессия наступает в более поздние сроки (спустя 12–18 месяцев). Мы полагаем обоснованным оценивать эффект брахитерапии, как положительный, при уменьшении опухоли на 50% и более от её исходного объема со стабильностью клинической картины в течение 9–12 месяцев [11].
Гемангиомы (отграниченные) хориоидеи длительное время, являясь по сути своей гамартомами, приводили к гибели пораженный глаз в связи с развитием распространенной отслойки сетчатки с последующим формированием вторичной глаукомы. Финал у таких больных заканчивался драматически – энуклеацией. В последние годы появились сведения о возможности регрессии гемангиомы после локального облучения ее офтальмоаппликаторами [15,59].
В литературе имеются ссылки на возможность облучения офтальмоаппликаторами увеальных метастазов [56]. Мы относимся к таким попыткам скептически, так как увеальные метастазы чаще бывают многофокусными и склонны к слиянию. Более эффективным при метастазах оказывается наружное облучение глаза [31,46,52].
Опухоли век и конъюнктивы
Лечение опухолей век и конъюнктивы брахитерапией длительное время находилось вне сферы внимания специалистов, занимающихся этой проблемой. Создание офтальмоаппликаторов уникальных форм, разработка методик облучения, многолетние наблюдения позволяют в настоящее время считать брахитерапию при опухолях век и особенно конъюнктивы адекватным методом лечения, а при меланомах – практически безальтернативным [19, 20, 24]. Однако необходимо подчеркнуть, что брахитерапия противопоказана при меланоме кожи век, распространяющейся на интермаргинальное пространство век или на пальпебральную конъюнктиву, а также при меланоме конъюнктивы, распространяющейся за пределы полулунной складки или слезного мясца.
Разработанная в нашем отделе крупнофракционная методика брахитерапии злокачественных опухолей конъюнктивы (рака и меланомы) повышает эффективность лечения [18, 19]. При злокачественных опухолях конъюнктивы эффективно сочетание брахитерапии с локальной химиотерапией митомицином С [16].
Отмечена высокая эффективность брахитерапии при лимфомах, капиллярных гемангиомах и лимфангиомах бульбарной и пальпебральной конъюнктивы [18, 25].
Брахитерапия показана при злокачественных опухолях кожи век и конъюнктивы, если толщина опухоли не превышает 5 мм. Максимальный диаметр опухоли практически не играет роли, т.к. при необходимости облучение можно проводить несколькими полями. Брахитерапию опухолей придаточного аппарата глаза проводят с помощью стронциевых офтальмоаппликаторов, форма которых разработана специально для этих целей (рис. 1). Показания к лучевому лечению могут быть расширены комбинацией бетатерапии с другими локальными методами воздействия (лазер– или радиоэксцизия, криоразрушение). Брахитерапия может быть использована при облучении послеоперационного рубца в случае опасения или гистологически подтвержденного нерадикального удаления опухоли. Суммарная очаговая доза в наиболее отдаленных от активной поверхности офтальмоаппликатора участках опухоли должна быть в пределах 200–250 Гр при пигментных опухолях, а при раке и эпителиоме Бовена – 150–180 Гр, при лимфангиомах и гемангиомах – 120 Гр
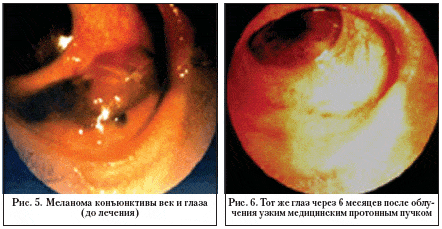
Многолетний опыт лечения таких больных (более 2700 человек) в нашем отделе свидетельствует об эффективности брахитерапии у 75% больных со злокачественными пигментными опухолями и у 94% с опухолями эпителиального генеза. Под эффективностью лечения злокачественной опухоли следует понимать полную регрессию ее при сроках наблюдения от 3 лет и более (рис. 5, 6). Неполная регрессия опухоли требует дополнительного лечения. Наш опыт работы в области офтальмоонкологии позволяет высказаться категорически против оценки «приемлемого» косметического эффекта, который иногда используют в литературе [28]. Злокачественные опухоли кожи век и конъюнктивы опасны не столько косметическим недостатком, сколько склонностью прорастать в ткани орбиты и формировать региональные метастазы.
Наружное облучение
Протонную терапию в клинической практике начали применять в 1954 году на ускорителе университета г. Уппсала (Швеция) и в 1961 году на Гарвардском циклотроне в Бостоне (США), позднее начали облучать на протонном пучке в Швейцарии, во Франции [40, 41, 37, 58]. В нашей стране облучение больных опухолями органа зрения мы проводим на медицинском протонном пучке ИТЭФ с 1975 г. [21, 35, 43].
Пучки протонов энергией 70–100 МэВ в отличие от других видов ионизирующего излучения характеризуются незначительным рассеиванием излучения, возможностью точной локализации пробега в тканях и пиком ионизации (пик Брэга) в заданном конце пробега. Это позволяет формировать дозные поля, полностью соответствующие форме и размерам опухоли, подводить к очагу поражения максимальную дозу облучения при максимальном щажении окружающих здоровых тканей. Указанные особенности создают условия для облучения опухолей различных размеров и многих локализаций.
К настоящему времени облучение с помощью УМПП в нашем отделе получили более 850 больных, имевших злокачественные опухоли придаточного аппарата глаза, цилиохориоидальной локализации и орбиты. По международной классификации опухолей органа зрения в группе леченных преобладали больные с опухолями стадии Т3N0–1 М0. При выявлении метастазов в региональные лимфоузлы облучению подвергались и последние. Это делает протонотерапию практически методом выбора и альтернативой таким калечащим операциям, как экзентерация орбиты или энуклеация.
Как показывает опыт зарубежных исследователей и наш собственный, наиболее эффективным является облучение опухоли крупными фракциями (10–20 Гр за сеанс) с интервалом 1–2 дня. Величина суммарной очаговой дозы зависит от гистологического типа опухоли: при меланоме СОД должна составлять 70–80 Гр, при различных формах рака – 45–50 Гр (3, 5). Полная резорбция опухоли через 6–12 месяцев отмечена у 77% леченных больных, частичная резорбция – у 21%, отсутствие эффекта – у 2% больных. Облучение опухолей придаточного аппарата глаза узким медицинским протонным пучком способствовало сокращению количества экзентераций орбиты, продлению жизни больных при распространенных злокачественных опухолях век и конъюнктивы, улучшению их качества жизни. При рецидиве меланомы в орбиту после энуклеации пораженного глаза облучение рецидивной опухоли узким медицинским протонным пучком оказалось более эффективным, чем дистанционная лучевая терапия: 86% облученных пережили 5–летний период, 73% живут более 15 лет [13]. Для оценки эффективности протонотерапии увеальных меланом играет роль исходная величина новообразования. В наших наблюдениях у 95% больных опухоль превышала в максимальном диаметре 15 мм и по высоте 6,5 мм, иными словами, мы облучали, как правило, больных с большими опухолями, которым до начала облучения узким медицинским протонным пучком врачи могли предложить только энуклеацию. В то же время у 76% облученных больных удалось сохранить глаз, как косметический орган, а у половины из них – и зрительные функции. Из–за отсутствия эффекта от лечения и возникших осложнений в 1/3 случаев облученные глаза были энуклеированы.
Дистанционная гамматерапия
При внутриглазных опухолях, как одна из составляющих комбинированного лечения, дистанционная гамматерапия применима при ретинобластоме. Показанием для наружного облучения орбиты после энуклеации при монолатеральной ретинобластоме являются морфологические признаки прорастания опухоли в зрительный нерв. Существует практика облучения лучшего глаза с нестандартными режимами фракционирования при билатеральной ретинобластоме [30]. Рекомендуемые дозы составляют по 1,5–2 Гр на фракцию при 5-кратном облучении в неделю, суммарные очаговые дозы не превышают 45 Гр [1]. С целью сохранения глаза используются не только клиновидные фильтры и специальные круглые коллиматоры, но и косые поля облучения [23]. Однако при назначении наружного облучения глаза у детей необходимо помнить о существовании таких осложнений, как задержка роста костей орбиты и лицевого скелета, гипоплазия мышц орбиты и лица. Со стороны глаза могут возникать лучевой панофтальмит, гемофтальм, кератит с развитием синдрома «сухого глаза», лучевая катаракта.
При внутриглазных метастазах наружное облучение глаза в настоящее время можно считать безальтернативным методом лечения, значительно улучшающим качество жизни этой категории больных [31].
Увеальная меланома больших размеров все еще является показанием для энуклеации. Проблема наружного облучения глаза до и после энуклеации таких глаз решена в конце прошлого столетия. Кооперированными исследованиями по увеальной меланоме в США показана несостоятельность наружного облучения глаза, как до, так и после энуклеации [36,38].
Опухоли орбиты
Дистанционная гамматерапия более широко используется при первичных и вторичных раках орбиты. Суммарная очаговая доза при монотерапии составляет 60–70 Гр Рекомендации проведения наружного облучения орбиты после ее экзентерации [28], с нашей точки зрения, не обоснованы. При злокачественных орбитальных опухолях показана поднадкостничная экзентерация орбиты – операция достаточно радикальная, после которой в орбите не должны оставаться мягкие ткани. Наружное облучение пораженной орбиты целесообразно в предоперационном периоде суммарной дозой 40–50 Гр, что повышает степень абластичности операции [32]. Дистанционная гамматерапия орбиты эффективна при злокачественных лимфомах и метастатических опухолях. Результативность лечения появляется при суммарной очаговой дозе облучения 30–50 Гр.
Наружное облучение при рабдомиосаркоме орбиты, которая чаще развивается в детском возрасте, более эффективно, если является составляющей комбинированного лечения (полихимиотерапия + наружное облучение + полихимиотерапия). Фракционная доза колеблется в пределах 4–5 Гр через день. Суммарная очаговая доза достигает 45–60 Гр С целью сохранения окружающих здоровых тканей и повышения абластичности лучевой терапии рекомендуют начинать облучение с больших полей, постепенно уменьшая их к концу цикла лечения [17].
При метастатических опухолях, диагноз которых устанавливается цитологически или морфологически (после диагностической орбитотомии) дистанционная терапия достаточно эффективна, хотя длительность ремиссии может быть кратковременной.
Короткодистанционная рентгенотерапия
Используется при лечении опухолей кожи век. В литературе [28] встречается общая оценка эффективности рентгенотерапии опухолей кожи век при довольно монотонном колебании суммарных очаговых доз (50–60 Гр). Это неверно, так как доза облучения определяется с учетом гистологической структуры опухоли. Рак кожи век базально–клеточно типа с успехом лечится суммарной очаговой дозой 45–55 Гр, в то время как чешуйчато–клеточные раки регрессируют при суммарных дозах 65–75 Гр Эффективность лечения при сроках наблюдения 5 лет и более выше при базально–клеточных раках. Проблемным является лучевое лечение аденокарциномы мейбомиевой железы. Рекомендуемая суммарная очаговая доза при этой опухоли достаточно высока – 65–70 Гр. И все же прогноз для жизни при аденокарциноме мейбомиевой железы крайне неблагоприятный: 50–67% больных погибают от дистантных метастазов в течение первых 5 лет. Короткодистанционная рентгенотерапия, как метод лечения метастатических опухолей, паллиативна, суммарная очаговая доза составляет 35 Гр.
Среди доброкачественных опухолей короткодистанционная терапия эффективна при капиллярных гемангиомах у детей. Наиболее эффективна лучевая терапия при облучении гемангиомы век у детей первых 12 месяцев жизни. Опыт лечения большого количества гемангиом век и лица [32] позволил автору рекомендовать разовые дозы 0,75–1,6 Гр с интервалами между первыми 2–3 фракциями облучения 1–4 недели, в последующем интервал увеличивается до 2–6 месяцев. Короткодистанционную рентгенотерапию при гемангиомах век можно расценивать, как метод выбора. Те осложнения, которые могут наблюдаться при короткодистанционной рентгенотерапии (телеангиэктазии, субатрофия кожи, мадароз, заращение слезных канальцев), при облучении гемангиом за счет расщепленности курса лечения отсутствуют.
Таким образом, лучевая терапия в офтальмоонкологии занимает ведущие позиции, но эффективность ее использования, сведение до минимума постлучевых осложнений зависят от следования строгим показаниям для ее проведения, выбора адекватных методик, разовых и суммарных доз облучения.

Литература
1. Белкина Б.М., Дурнов Л.А., Поляков В.Г. и др. Лечебная тактика и результаты комплексной терапии ретинобластомы //Вопросы онкологии.–1997.–Т.43/4.–с.435–439.
2. Бровкина А.Ф., Зарубей Г.Д. О причинах энуклеации после комбинированного лечения меланом хориоидеи //Вестн. Офтальмол.–1982.–№3.–с.48–51.
3. Бровкина А.Ф., Зарубей Г.Д. Лечение цилиохориоидальных меланом узким медицинским протонным пучком //Вестн.Офтальмол.–1986.–№3.–с.30–33.
4. Бровкина А.Ф., Макарская Н.В. Возможности применения лазерного излучения при опухолях органа зрения //В кн.: Лазеры в офтальмологии.–Ташкент.–1987.–с.84–87.
5. Бровкина А.Ф., Зарубей Г.Д. Опыт лечения опухолей органа зрения узким медицинским протонным пучком //Медиц.радиол.–1987.–№8.–с.61–66.
6. Бровкина А.Ф. Современные методы лечения внутриглазных меланом //Ж. Врач.–1991.–№5.–с.13–15.
7. Бровкина А.Ф., Зарубей Г.Д. Обоснованность использования брахитерапии при увеальных меланомах юкстапапиллярной локализации //Вестн. офтальмол.–1991.–№6.–с.41–43.
8. Бровкина А.Ф., Зарубей Г.Д. Об эффективности брахитерапии при увеальных меланомах //Офтальмол. ж.–1993.–№1.–с.1–4.
9. Бровкина А.Ф., Пантелеева О.Г. //Вестн. офтальмол.–1995.–№5.–c.21–23.
10. Бровкина А.Ф., Пантелеева О.Г. Результаты лечения ретинобластомы //Вестн. офтальмол.–1995.–№3.–с.12–14.
11. Бровкина А.Ф., Зарубей Г.Д., Вальский В.В. Критерии оценки эффективности брахитерапии //Вестн. офтальмол.–1997.–№3.–с.14–17.
12. Бровкина А.Ф., Кешелава В.В. // Вестн. офтальмол.–1997.–№2.–с.14–17.
13. Бровкина А.Ф. Современные аспекты лечения увеальных меланом //Вестн. офтальмол.–1998.–№3.–с.3–5.
14. Бровкина А.Ф., Кешелава В.В. Результаты сочетанной лучевой терапии увеальных меланом //Вестн. офтальмол.–2001.–№3.–с.3–5.
15. Бровкина А.Ф. Гемангиомы хориоидеи // в кн.: Современные технологии в диагностике и лечении сосудистой патологии органа зрения.– Краснодар.–2002.– с.52–53.
16. Бровкина А.Ф. Офтальмоонкология. Руководство для врачей.– М.–2002.–с.220–228.
17. Бухны А.Ф., Белкина Б.М., Блинов В.М. и др. Рабдомиосаркома у детей //Вопросы онкологии.–1990.–Т36/11.–с.1312–1316.
18. Вальский В.В., Гришина Е.Е. Сравнение результатов дистанционной рентгенотерапии и брахитерапии лимфопролиферативных заболеваний конъюнктивы // в кн.: Достижения и перспективы офтальмоонкологии.–М.–2001.–с.100–101.
19. Вальский В.В. Крупнофракционная брахитерапия злокачественных опухолей конъюнктивы // в кн.: Достижения и перспективы офтальмоонкологии.–М.–2001.–с.98–100.
20. Волков В.В. Варианты лечебной тактики при опухолях наружного отдела глаза // Вестн. офтальмол.–1991.–№4.–с.34–39.
21. Гольдин Л.Л., Хорошков В.С., Бровкина А.Ф. и др. Физико–технические и экспериментальные подходы к облучению опухолей глаза протонным пучком //В кн.: Использование протонных пучков в лучевой терапии. – Атомиздат.–1979.–с.133–139.
22. Деденков А.Н., Бровкина А.Ф., Зарубей Г.Д. Результаты бетатерапии меланом хориоидеи // Медиц. радиология. – 1980. – №4. – с. 73–75.
23. Дурнов Л.А., Белкина Б.М., Поляков В.Г. и др. Комплексное лечение ретинобластом у детей //Вестн. Рос. АМН.–1996. – №10. – с. 28–33.
24. Зарубей Г.Д., Будкина Г.П., Бровкина А.Ф. и др. Методы контактной бета терапии новообразований глаза // В кн.: Проблемы развития терапевтической радиационной техники. – М. – 1975. – с. 166–158.
25. Зарубей Г.Д., Бровкина А.Ф., Будкина Г.П. Лечение эпибульбарных злокачественных новообразований с помощью радиоактивных стронциевых аппликаторов //Офтальмол.ж. – 1977. – №1. – с. 30–33.
26. Кешелава В.В. Патент 2053776 РФ.–1994.
27. Кешелава В.В. Рак: новые аспекты радионуклидной диагностики и лечения.// в кн.: Рентгенорадиология ХХ1 века.– Челябинск, Москва.–2001.–с.29–30.
28. Корытова Л.И., Алексеев В.Н., Ильин Н.В., Виноградова Ю.Н. Роль лучевой терапии в комбинированном лечении заболеваний органа зрения // Клиническая офтальмология.–2002.–Т3/4.– с.164–168.
29. Линник Л.Ф., Магарамов Д.А., Яровой А.А. и др. Лазерная транспупиллярная термотерапия меланом //Офтальмохирургия.–2002.–№3.–с.45–50.
30. Лобанов Н.В., Голдобенко Г.В. Лучевая терапия двухсторонних ретинобластом // Офтальмол. ж.–1992.–№1.–с.15–17.
31. Михина З.П., Гришина Е.Е. Лучевая терапия хориоидальных метастазов // Медицинская радиология.–2000.–№1.–с.12–14.
32. Шеина А.И. Наружная лучевая терапия // В кн.: Офтальмоонкология. Руководство для врачей.–М.–Медицина. – 2002. – с. 138–172.
33. Bechrakis E., Bornfeld N., Schueler A. et al. Clinicopathologic features of retinoblastoma after primary chemoreduction //Arch. Ophthalmol.–1998.–V.116.–p.887–893.
34. Boniuk N., Cohen J. Combined use of radiation plaques and photocoagulation in the treatment of choroid melanomas // Ocular and adnexal tumors.–Birmingham, ed. Jacobiec I.–1978.–p.80–88.
35. Brovkina A., Zarubej G. Proton beam therapy of ciliochoroidal melanomas // Arch. Ophthalmol.–1986.–V.104.–p.402–404.
36. The Collaborative Ocular Melanoma Stady (COMS) rondomised trial of preenucleation radiation of large choroidal melanoma //Ivest. Ophthalmol.–1994.–V35/4.–p.3994–3998.
37. Dejardins L., Levy C., d?Hermiles F. et al. Results preliminares de la protonotherapie du melanome de la choroide an centre de protontherapie d?Orsay // Сancer radiat. Therapy.–1997.– 3.–2.–333–336.
38. Egan K., Ryan L., Gragoudas E. Survival implications of enucleation after definitive radiotherapy for choroidal melanoma //Arch. Ophthalmol.–1998.–V116/3.–p.366–370.
39. Ellsworth R. Cobalt plaques for melanoma of the choroid // Оcular and adnexal tumors.–ed. Jacobiec I.–Birmingham Aesculapius Publishing Co.–1978.–p.76–79.
40. Gragoudas E., Egan K., Seddon J. Survival of patients with metastases from uveal melanoma // Ophthalmology.–1990.– V.91/4. –p .383–389.
41. Gragoudas E., Egan K., Saornil M. The time course of irradiation changes in proton–beam treated melanomas //Ophthalmology, –1993. – V.100/7.–p.1555–1559.
42. Haye C. Non–surgical treatment of tumours of the choroid // Ophthalmologica (Basel).–1981.–v.182.–p.136–140.
43. Khoroskov V., Goldin L., Minaсhova E. Et al. Itep sybchotron protob beam in radiatiotherapy // Int. J.Radiat. Oncol. Biol. Phys. – 1984. – v10. –p.185–195.
44. Kingston J., Hungerford J., Madreperta S., Plomman P. Results of combined chemotherapy for advanced intraocular retinoblastoma //Arch.Ophthalmol.–1996.–V.114/6.–p.1339–1343.
45. Kreisig I., Rose D., Simadler E. Iod–125 – Brachytherapie des malignen Aderhaut melanoma // Klin. Mnbl. Augenheilk.–1996.– bd.209/1.– s.7–12.
46. McCormick B., Harrison L. Radiatio therapy of choroidal metastases // Radiotherapy of intraocular and orbital tumore ed. Albert W., Sagermay R. – Berlin: Springer –Verlag.–1993.–s.93–97.
47. Lommatsch P. Tratment of choroidal melanomas with Ru–106/Rh–106 betaray applicators //Survay of Ophthalmol.–1974.– V.19.–p.85–100.
48. Moore P. цит. По Haye C.
49. Murphree A., Williblanca I., Deegan W. Chemotherapy plus local treatment in the management of intraocular retinoblastoma //Arh/Ophthalmol.–1996.– V114. – p. 1348–1356.
50. Namouni F., Doz F., Tanguy V. High–dose chemotherapy with carboplatin, etoposide abd cyclophosphamide folloved by a haematopoietic stem cell rescue in patients with high–risk retinoblastoma //Europ. J. cancer. – 1997, – V.33. – p.2368–2375.
51. Oosretrhuis J., Journee de Korver H., Keunen I. Transpupillary thermotherapy // Arch. Ophthalmol. – 1998. – V.116/1.–p.157–162.
52. Rudoller S., Corn B., Shields C. et al. External beam irradiation for choroidal metastases // Int.J. radiat. Oncol. Biol. Phys. – 1997.– v.38/2.–p.251–256.
53. Quivey I., Augsburger J., Snelling L., Brody L. 125–I plaque therapy for uveal melanoma // Cancer. – 1996. – V.77/11. – p.2356–2362.
54. Seedly R., Buret H. Progress in the use of iodine therapy of the eye //Br.J.Ophthalmol.–1980.–V.53.–p.1052–1060.
55. Shields C., Shields J., de Potter P. Plaque radiotherapy in the management of retinoblastoma // Ophthalmology. – 1993. – V.100/3.– p.216–224.
56. Shields C., Shields J., de Potter P. plaque radiotherapy for the management of the uveal metastasis // Arch.ophthalmol.–1997.–V.115/3.–p.203–209.
57. Stallard H. Nalignant melanoma of the choroid in treated with radioactive applicators // Trans. Ophthalmol. Soc. UK. –1960,–V.79.–p.373–392.
58. Zografos L., Perrit E., Egger E. Et al. Proton beam irradoation of uveal melanomas at Paulscheireg.Institute // Strallenther.Oncol.–1990.–V.166/1.–p.114.
59. Zografos L., Bercher R., Chamot L. et al. Cobalt–60–treatment of choroidal hemangiome // Amer.J. Ophthalmol. –1996.–V.121/2.–p.190–199.












