В 85–90% случаев ВМД протекает в виде «сухой» формы, сопровождаясь атрофией пигментного эпителия и образованием друз без проявлений экссудации и неоваскуляризации [3]. В ходе естественного старения сетчатка претерпевает ряд изменений, связанных преимущественно с утратой фотосенсорного слоя [4, 5]. Невозобновляемость пигментного эпителия и его функция поглощения собственных клеток и дисков фоторецепторов обусловливают естественные накопления липофусцина, увеличивающиеся с возрастом [6]. Феномен угасания макулярного рефлекса с возрастом также физиологичен и обоснован увеличением площади бессосудистой области зоны фовеа и измельчением ямки фовеолы [7]. Для диагностики ВМД на основании изменений глазного дна применяют классификацию AREDS, названную по исследованию, в котором она изначально выполняла роль критериев включения и разделения на группы [8]. Первая стадия по AREDS соответствует естественным возрастным изменениям и описывается как единичные друзы размером до 63 мкм. Вторая и третья стадии по AREDS соответствуют классическому пониманию «начальной» и «продвинутой» стадий «сухой» ВМД и описываются как наличие друз размером 63–124 и более 124 мкм с географической атрофией соответственно. Четвертая стадия AREDS описывает терминальную ВМД.
Патогенез заболевания к настоящему моменту полностью не изучен, однако известно о генетической природе болезни, факторах риска и механизмах поражения ткани сетчатки. Помимо образования липофусцина и формирования друз происходит поражение пигментного эпителия, гистологически проявляющееся гипертрофией и миграцией пигментных клеток в субретинальное пространство. Ключевым элементом патогенеза при поражении пигментного эпителия считают оксидативный стресс. Высокое потребление кислорода, постоянная подверженность световому воздействию и участие в перекисном окислении липидов при контакте с фоторецепторами обусловливают анатомическую предрасположенность пигментных клеток к подобному повреждению. При развитии ВМД оксидативный стресс, как правило, сопутствует дисфункции аутофагии – основного лизосомального защитного механизма, отвечающего на возрастные изменения ткани [9]. Разрушение пигментного эпителия ассоциируется с развитием воспалительного иммунологического ответа и ухудшением течения заболевания. В целом изучение патогенеза и разработка лечения ВМД в аспекте локальной иммунологической реакции, связанной с нарушением гематоофтальмического барьера, на текущий момент являются одним из наиболее перспективных направлений [10].
Целью лечения «сухой» формы ВМД является замедление прогрессирования заболевания. Предложено множество вариантов консервативной терапии, основанных на предполагаемых патогенетических механизмах, однако их эффективность является одним из наиболее спорных вопросов современной офтальмологии. Определены модифицируемые факторы риска, однако с высокой достоверностью к ним относят только курение [11]. В ряде исследований выявлена связь между гипертонической болезнью и ВМД [12–14]. В других исследованиях авторы говорят об отсутствии связи между ВМД и заболеваниями сердечно-сосудистой системы [15–17].
К настоящему моменту серия рандомизированных двойных слепых исследований AREDS является основным исследовательским материалом, посвященным терапии «сухой» ВМД. По результатам начальных работ были сделаны рекомендации о применении цинка и антиоксидантов у пациентов с «сухой» ВМД, при этом был обнаружен повышенный риск рака легких у курильщиков при применении бета-каротина [18]. В последующих исследованиях было обнаружено, что применение омега-3 жирных кислот, лютеина и зеаксантина не приводит к дальнейшему улучшению прогноза. Однако было обнаружено, что у пациентов, не принимавших бета-каротин в ходе первого исследования, риск прогрессирования был ниже при приеме лютеина и зеаксантина. Это позволило авторам предположить взаимозаменяемость бета-каротина и лютеина с зеаксантином [19]. Позже в Кохрановских обзорах были подтверждены положительное действие поливитаминов и антиоксидантов и отсутствие эффекта при применении лютеина, зеаксантина и омега-3 жирных кислот [20, 21].
В конце XVIII в. физиологом Броун-Секаром впервые была предпринята попытка использовать эндогенные физиологически активные вещества для лечения различных заболеваний. Он использовал экстракты из семенных желез различных животных в качестве омолаживающего средства. В дальнейшем для лечения различных заболеваний начали применять вещества полипептидной природы, полученные из разных органов и тканей (головного и костного мозга, селезенки, лимфатических узлов, легких, печени, вилочковой железы, сетчатки и др.). Эти вещества получили название пептидных биорегуляторов или цитомединов, они являются щелочными полипептидами, имеющими молекулярную массу от 1 тыс. до 10 тыс. Да. Их получают из различных тканей с помощью метода кислотной экстракции с последующей очисткой от балластных веществ. Данный метод получения исключает возможность переноса вирусов и протоонкогенов, что обеспечивает безопасность применения данных веществ в клинической практике. Независимо от того, из каких органов и тканей они были получены, цитомедины влияют на клеточный и гуморальный иммунитет, состояние системы гомеостаза, перекисное окисление липидов и другие защитные и физиологические реакции организма. Это действие выражено в разной степени и зависит от применяемой дозы. Цитомедины, получаемые из тканей головного мозга и сетчатки, обладают функцией нейропептидов и участвуют в регуляции деятельности нервной ткани. Изучение возможности применения нейропептидов в офтальмологии началось в 1987 г. В настоящее время используются такие нейропептиды, как Ретиналамин и Кортексин производства ООО «Герофарм» (Россия).
Кортексин – комплекс пептидов, выделенных из коры головного мозга крупного рогатого скота и свиней. Согласно инструкции по медицинскому применению он относится к фармакологической группе «ноотропное средство», обладает антиоксидантным, ноотропным, нейропротекторным, тканеспецифическим действием и рекомендуется для применения в неврологии.
Препарат Ретиналамин представляет собой комплекс водорастворимых полипептидных фракций, выделенных из сетчатки крупного рогатого скота, с молекулярной массой не более 10 000 Да. Согласно инструкции по медицинскому применению от 17.02.2016 г. препарат оказывает стимулирующее действие на фоторецепторы и клеточные элементы сетчатки, способствует улучшению функционального взаимодействия пигментного эпителия и наружных сегментов фоторецепторов, глиальных клеток при дистрофических изменениях, ускоряет восстановление световой чувствительности сетчатки, нормализует проницаемость сосудов, уменьшает проявления местной воспалительной реакции, стимулирует репаративные процессы при заболеваниях и травмах сетчатки глаза. Механизм действия Ретиналамина определяется его метаболической активностью: препарат улучшает метаболизм тканей глаза и нормализует функции клеточных мембран, улучшает внутриклеточный синтез белка, регулирует процессы перекисного окисления липидов, способствует оптимизации энергетических процессов [22–25]. Препарат показан при ряде патологий сетчатки, а также при компенсированной первичной открытоугольной глаукоме, парабульбарно или внутримышечно по 5 мг 1 р./сут, курс лечения составляет 10 дней. Препарат растворяют в 1–2 мл воды для инъекций, 0,9% раствора натрия хлорида или 0,5% раствора прокаина (новокаина).
Нами была поставлена цель провести метаанализ отечественных рандомизированных клинических исследований (РКИ) эффективности терапии «сухой» формы ВМД комплексом водорастворимых полипептидных фракций сетчатки.
Материал и методы
Метаанализ можно определить как «количественный систематический обзор литературы». От описательного обзора его отличает количественный анализ результатов исследований. Преимущества метаанализа наиболее очевидны в тех случаях, когда результаты индивидуальных исследований противоречат друг другу или размер каждого исследования слишком мал, а организация широкомасштабного исследования слишком затратна.Поиск литературы проводили по электронной базе ООО «Научная электронная библиотека» (elibrary.ru) после входа в личный кабинет пользователя. Печатные работы для метаанализа отбирали согласно следующим критериям: клиническое исследование, опубликованное на русском языке в периодической научной литературе, в результате которого проводится анализ эффективности применения препарата Ретиналамин, применяемого по способу введения и дозировке согласно последней версии утвержденной инструкции по медицинскому применению у пациентов с «сухой» формой ВМД. Структурная схема результатов стратегии поиска представлена на рисунке 1. Таким образом, всего было отобрано 11 публикаций, соответствующих поставленным критериям [26–36].

Результаты метаанализа
В анализ было включено 11 публикаций за период 2006–2017 гг. [26–36], одно из исследований было выполнено на Украине [28].Число пациентов и глаз. В 9 работах из 11 число пациентов было указано, однако число глаз, вошедших в исследование, отмечено только в 8 статьях [26–28, 31, 33–36]. Средний возраст пациентов приведен в 8 работах [29–36].
Клинические характеристики пациентов. В 6 работах исследователи анализировали эффективность терапии без деления пациентов с ВМД на какие-либо стадии заболевания [26–29, 31, 35]. В работе С.В. Трофимовой пациентов подразделяли на 3 подгруппы по остроте зрения [33]. Н.Х. Хасанова, используя тот же критерий, сформировала уже 6 подгрупп [36]. В работе С.А. Коротких были отобраны пациенты с 2 и 3 стадиями по AREDS [30]. Т.С. Федотова обследовала больных с 2 и 4 стадиями по AREDS [34]. В исследование В.В. Нероева включили пациентов со всеми тремя стадиями по AREDS (2–4) и с клиническими проявлениями ВМД [32].
Как указано выше, были отобраны работы, в которых методика введения Ретиналамина соответствовала или максимально приближалась к заявленной в инструкции. Таким образом, парабульбарный метод применен в 5 исследованиях [27, 28, 33, 35, 36], внутримышечный – в 2-х [29, 32], субконъюнктивальный – в 3-х [26, 30, 31], путем эндоназального электрофореза – в 2-х [26, 31], в 1 работе применяли подкожные инъекции в височную область [34]. Объем вводимого препарата и число инъекций соответствовали рекомендуемым.
Срок наблюдения больных существенно варьировал, что затруднило проведение сравнительного метаанализа (табл. 1). В среднем пациентов обследовали до курса лечения, сразу после (10 дней), спустя 1, 3, 6, 9 и 12 мес.

Методы обследования. Оценка остроты зрения является одним из наиболее объективных методов исследования степени снижения зрительных функций при макулярной дегенерации. Во всех 11 клинических исследованиях проводили оценку остроты зрения по стандартному отечественному алгоритму, что позволило провести наиболее адекватную сравнительную оценку эффективности терапии.
Также во всех исследованиях проводили оценку состояния полей зрения, в большинстве – с помощью статической периметрии [26, 28, 30–35], в 3-х также применяли кинетический алгоритм [27, 29, 36]. К сожалению, не все авторы приводили результаты периметрии, а опубликованные данные сильно варьировали по методам оценки: наличие центральных скотом [30, 34, 35], их площадь [27, 33], средний показатель световой чувствительности [32], оценка контрастной чувствительности [28], определение периферических границ поля зрения [29, 36].
Ряд авторов исследовали электрофизиологические показатели: общую, ритмическую ЭРГ и зрительные вызванные потенциалы [27]; А- и B-волны макулярной ЭРГ [26, 31, 32, 34, 35].
Среди прочих методов следует отметить определение ретинальной остроты зрения [33], генетическое тестирование [34], определение качества жизни [29], тест с помощью сетки Амслера [33], определение линейной скорости кровотока в глазничной артерии [33], комплексную реоофтальмографию и допплерографию [26, 31], оптическую когерентную томографию макулярной зоны [28, 30, 32].
Статистическая обработка данных. В 5 работах авторы рассчитывали средние значения (М), стандартное отклонение (а) и уровень значимости (р) [27, 28, 30, 32, 35]. В работах Н.В. Морозовой и Ю.С. Астахова статистическая обработка представлена только уровнем значимости [26, 31]. Зачастую офтальмологические показатели имеют ненормальное распределение, это требует оценки непараметрическими методами, что не сделано ни в одной работе. В 4–х исследованиях методы статистики не упоминаются [29, 33, 34, 36].
Оценка динамики остроты зрения
Данные визометрии, являясь стандартом любого офтальмологического обследования, приводились авторами всех исследований. Однако в ряде работ указывался только средний процент улучшения остроты зрения в разные сроки после терапии (рис. 2) [27, 33–36]. По данным Т.С. Федотовой, спустя 10 дней комплексной терапии (Ретиналамин, Кортексин, Нормофтал) улучшение остроты зрения было достигнуто в 100% случаев. В исследовании Н.Х. Хасановой тот же результат был получен после 10–дневного курса монотерапии Ретиналамином. При субтеноновом и парабульбарном введении препарата в работе Ц. Гао спустя 10 дней монотерапии были зафиксированы схожие результаты – порядка в 82% случаев. Спустя 3 мес. терапии при парабульбарном введении Ретиналамина положительная динамика несколько снижается – 74,1% и 70,9% по данным С.В. Трофимовой и В.Х. Хавинсона.
Большая часть авторов, описывая динамику остроты зрения, приводит средние величины со стандартным отклонением, что позволило провести классический метаанализ эффективности препарата в различные сроки. Спустя 10 дней терапии при субконъюнктивальном введении Ретиналамина при 2 (ранней) и 3 (промежуточной) стадиях ВМД были получены сопоставимые результаты с некоторым преимуществом 3 стадии (рис. 3).
Анализ динамики остроты зрения спустя 1 мес. после терапии также подтверждает преимущество лечения пациентов с промежуточной стадией ВМД при одинаковых методах введения (рис. 4). Впрочем, выраженность положительного эффекта несколько ниже в сравнении с оценкой на 10 сут терапии.


Трехмесячный срок оценки результатов является своего рода переломным моментом для определения необходимости в проведении повторной терапии: по данным В.В. Нероева, при ранней и поздней стадиях ВМД острота зрения возвращается к исходным значениям, в то время как при промежуточной стадии положительные результаты сохраняются, что также подтверждается данными С.А. Коротких (рис. 5).

Спустя 3 мес. В.В. Нероев провел повторный курс внутримышечного введения Ретиналамина, что позволило зафиксировать положительную динамику остроты зрения спустя 5 мес. от начала первого курса при ранней, промежуточной и поздней стадиях, в сравнении с отсутствием эффекта в соответствующих группах сравнения без повторной терапии (рис. 6).

Согласно ряду исследований спустя 6 мес. после 1 курса терапии (при различных методах введения Ретиналамина) во всех группах отмечали наличие положительной динамики остроты зрения, в т. ч. по данным С.А. Коротких, получившего более выраженный результат при промежуточной стадии в сравнении с ранней (рис. 7). По результатам работы Ю.С. Астахова после субконъюнктивального введения препарата была отмечена более выраженная динамика остроты зрения, чем при его введении методом электрофореза.

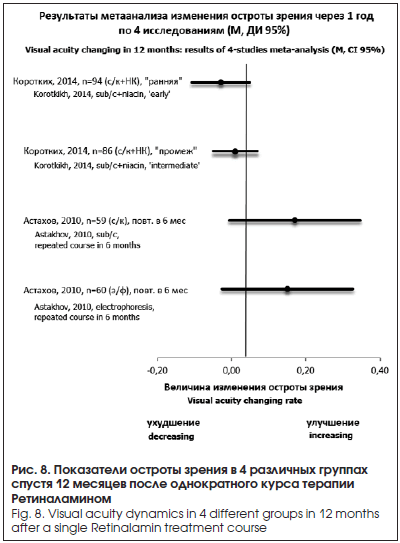
В срок 6 мес. после проведения однократного курса Ретиналамина Ю.С. Астахов проводит повторный курс, в результате которого спустя 1 год наблюдения в обеих группах фиксируют существенный прирост остроты зрения (рис. 8). В эти же сроки результаты своей работы оценивает С.А. Коротких, проведший 1 курс терапии. Исследователь отмечает отрицательную динамику остроты зрения при ранней и промежуточной стадиях ВМД.
Заключение
Из 320 литературных источников, посвященных действию препарата Ретиналамин при «сухой» форме ВМД за период 2006–2017 гг., для метаанализа было отобрано 11 работ, соответствующих следующим критериям: русскоязычное клиническое исследование эффективности Ретиналамина, применяемого по способу введения и дозировке согласно инструкции по медицинскому применению у пациентов с «сухой» формой ВМД.В результате метаанализа было выявлено:
– достоверное увеличение остроты зрения преимущественно в 3 (промежуточной) стадии макулярной дегенерации при различных способах введения в сроки до 6 мес. включительно;
– проведение повторного курса терапии способствует увеличению и пролонгации положительного эффекта при различных стадиях ВМД в сроки до 1 года.
Таким образом, метаанализ РКИ эффективности ретинопротекторной терапии «сухой» формы ВМД с использованием комплекса водорастворимых полипептидных фракций Ретиналамин® выявил доказанную эффективность препарата в терапии «сухой» формы ВМД.
Сведения об авторах: Еричев Валерий Петрович – д.м.н., профессор; Петров Сергей Юрьевич – к.м.н., ведущий научный сотрудник; Волжанин Андрей Вячеславович – аспирант. ФГБНУ «Научно-исследовательский институт глазных болезней». 119021, Российская Федерация, Москва, ул. Россолимо, 11А. Контактная информация: Петров Сергей Юрьевич, e-mail: post@glaucomajournal.ru. Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов отсутствует. Статья поступила 20.11.2017.
About the authors: Valery P. Erichev – professor; Sergey Yu. Petrov – PhD, Research Officer; Andrey V. Volzhanin - postgraduate student. The Scientific Research Institute of Eye Diseases. 11a, Rossolimo str., Moscow, 119021, Russian Federation. Contact information: Sergey Yu. Petrov, e-mail: post@glaucomajournal.ru. Financial Disclosure: no author has a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 20.11.2017.












