V.V. Malyshev
Irkutsk department of FGU “MNTK “Eye Microsurgery” named after Fedorov S.N. of Rosmedbiotechnology”
GOU DPO Irkutsk Medical Refresher Institute of Federal Agency of health and social development.
Purpose: OCT study of vessel and epithelium, vitreal and macular changes in patients with wet AMD .
Materials and methods: 70 patients (140 eyes) with wet type of AMD were examined. Visometry, light sensitivity study, fluorescent angiography and OCT ( on each eye) were performed in all patients.
Results and conclusion: The first stage of wet AMD includes pigment epithelium (PE) detachment. Then neuroepithelial detachment happens. This could be caused by transudation of fluid through choroid capillars of normal PE or exudation from choroid neovascular membrane. Progression of the disease leads to fibrous scar developing, cystoid macular oedema or geographic atrophy. There was no traction from vitreal body. This could be explained by the fact that wet AMD is developed because of pathologic processes based in choroid vessels, Bruch’s membrane and neuroepithelium.
Введение
Возрастная макулярная дегенерация (ВМД) является ведущей причиной снижения зрения у пожилых пациентов в развитых странах [6] и встречается в 58–100% случаев среди лиц старше 70 лет [12]. В клинике традиционно выделяют 2 типа ВМД: сухую и влажную. В большинстве случаев встречается сухая, или неэкссудативная, макулярная дегенерация в виде твердых или мягких друз, когда острота зрения остается достаточно высокой. Лишь в 10–15% развивается влажная, или экссудативная, ВМД, которая характеризуется развитием патологической хориоидальной неоваскуляризации и сопровождается драматическим падением зрения до 0,1 и ниже.
В настоящее время ВМД считается заболеванием, в этиопатогенезе которого участвуют генетические и эпигенетические факторы, а также факторы окружающей среды. Все они взаимодействуют между собой и вносят вклад в риск развития заболевания [7,10,11]. При ВМД происходит накопление продуктов метаболизма в пигментном эпителии сетчатки (ПЭС), плотность его уменьшается, мембрана Бруха становится более плотной и гидрофобной [4]. В дальнейшем в патологический процесс включаются нарушения в системе комплимента, ведущие к экспрессии цитокинов и изменению баланса между протеолитическими ферментами и их ингибиторами. Это потенцирует разрушения в пигментном и нейроэпителии. На фоне заболевания происходит более активная выработка эндотелиального фактора роста сосудов (Vascular Endothelial Grows Factor – VEGF), являющегося мощным стимулятором ангиогенеза. По данным Grossniklaus с соавт. (2007), рост новообразованных сосудов может распространяться вначале под ПЭС и вызывать его отслойку. В дальнейшем происходит перфорация ПЭС и отслойка уже нейроэпителия [8]. По мере прогрессирования процесса формируется хориоидальная неоваскулярная мембрана, увеличивается количество соединительной ткани и, как правило, формируется фиброзный рубец [9].
До недавнего времени эффективное лечение влажной ВМД отсутствовало. Только небольшая часть пациентов могла рассчитывать на замедление прогрессирования заболевания и стабилизацию зрения с помощью лазерного или хирургического лечения. Использование анти–VEGF препаратов в лечении влажной ВМД явилось одним из наиболее значительных успехов офтальмологии в последние годы. Применение интравитреальных инъекций авастина и луцентиса позволило во многих случаях не только сохранить, но даже улучшить зрение у этой тяжелой категории больных. Однако эффективность лечения ВМД анти–VEGF препаратами, как показали наши исследования, во многом зависит от исходного состояния макулы [3]. Возникла необходимость систематизировать макулярные изменения при влажной ВМД для того, чтобы более четко определять показания к вмешательству и прогнозировать результат
Одной из новых методик, которые позволяют с максимальной точностью оценить состояние сетчатки и, что особенно важно, пигментного эпителия и хориокапилляров, является оптическая когерентная томография (Optical Coherence Tomography – OCT) [1]. Это бесконтактная неинвазивная технология, которая позволяет выявить и количественно оценить состояние хориокапилляров, мембраны Бруха, пигментного и нейроэпителия сетчатки и прилежащего стекловидного тела. ОСТ высокого разрешения с точностью до 5 мкм дает срезы исследуемых тканей, а получаемые изображения практически идентичны гистологическим срезам [2,5]. Возможность многократного повторения исследований и сохранение полученных результатов в памяти компьютера позволяет проследить динамику патологического процесса, определить стадию его развития.
Соответственно, основной целью нашего исследования явилось исследование изменений хориокапилляров, мембраны Бруха, пигментного и нейроэпителия, а также витреомакулярного интерфейса у пациентов с влажной ВМД на разных стадиях ее развития, используя для этого возможности оптической когерентной томографии высокого разрешения.
Материал и методы
Обследованы 70 пациентов (140 глаз) с влажной формой возрастной макулярной дегенерации (ВВМД). Учитывая, что патологический процесс, как правило, захватывает оба глаза и протекает в разной степени выраженности, то оценка ОСТ признаков ВМД производилась в каждом глазу отдельно. У 10 пациентов были симметричные изменения на обоих глазах, поэтому они были отнесены к одной группе. Возраст пациентов варьировал от 57 до 88 лет. В представленной группе было 54 женщины (77,2%) и 16 мужчин (22,8 %).
Всем больным было произведено стандартное офтальмологическое обследование, включающее определение остроты зрения, световой чувствительности сетчатки с помощью анализатора LD–400 фирмы Dicon (США), флюоресцентную ангиографию и оптическую когерентную томографию высокого разрешения (ОСТ–HD Cirrus фирмы Zeiss Meditec Inc.).
Результаты
При обследовании пациентов с ВМД были выявлены четыре характерных типа изменений макулы, объединенных в соответствующие группы. Представляем их по мере нарастания тяжести заболевания.
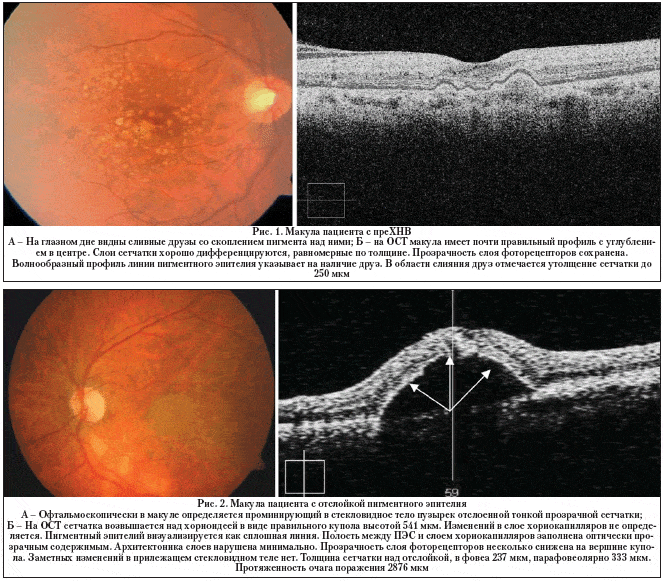
У 27 пациентов (37 глаз) офтальмоскопически на фоне друз определялись участки их слияния, часто сочетающиеся с пигментацией. Зрительные функции оставались высокими, в среднем составляя 0,73±0,09 и в значительной степени зависели от размеров очага и его удаленности от фовеолы. По данным электронной периметрии, явного снижения световой чувствительности в макуле не отмечено. На ОСТ виден пигментный эпителий (ПЭ), который приобретает неравномерную форму и выглядит как волнистая линия за счет появления под ним друз. Толщина сетчатки в области центральной ямки составила 223±10,6 мкм (от 170 до 333 мкм), парафовеолярно 313±8,2 мкм (от 250 до 395 мкм). Было отмечено некоторое снижение прозрачности слоя фоторецепторов, неравномерность толщины слоя пигментного эпителия и единичные его дефекты (рис. 1). Хотя в этой стадии еще нет абсолютных объективных признаков развития хориоидальной неоваскуляризации, однако, по данным Macular Photocoagulation Study (1993), это состояние в течение 5 лет приводит к развитию ХНВ в 60% случаев. Мы предлагаем расценивать крупные сливные друзы в сочетании с гиперпигментацией как преХНВ.
У больных 2–й группы (39 глаз) основным отличительным признаком была отслойка пигментного эпителия. Расстройства зрения при этом были минимальны и заключались в умеренном снижении зрения до 0,52±0,04 (0,95¬¬–0,25), искажении линий при исследовании на сетке Амслера. При выполнении ОСТ у этих пациентов была выявлена отслойка ПЭС в виде проминирующего в стекловидное тело правильного купола с пологими склонами (рис. 2). Толщина сетчатки над зоной отека была изменена незначительно и составила 182±15,7 мкм (от 106 до 280 мкм). Высота серозной отслойки ПЭ варьировала в пределах 359±55 мкм (от 122 до 1200 мкм). В парафовеолярной области также отмечено увеличение толщины сетчатки по сравнению с предыдущей группой исследуемых пациентов до 358±19,2 мкм (246–570 мкм). Протяженность изменений измерялась по меридиану, соответствующему максимальному размеру выявленных патологических изменений, и составила в среднем 2515±288 мкм (от 1087 до 4500 мкм). Нарушения дифференциации слоев сетчатки на данном этапе заболевания были минимальными. Полость между ПЭС и слоем хориокапилляров была заполнена оптически прозрачной жидкостью. Пигментный эпителий сохранен и прослеживается в виде ярко–красной линии относительно одинаковой толщины. Важно подчеркнуть, что ни офтальмоскопически, ни с помощью ФАГ ХНВ явно не определялась.
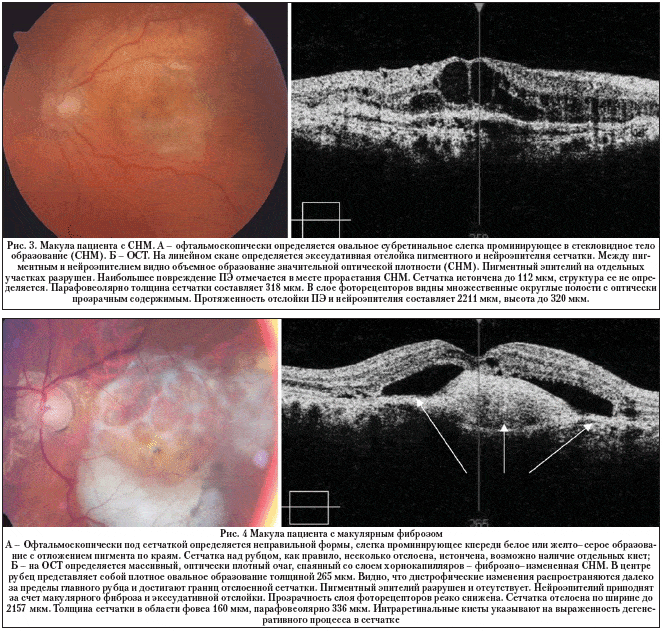
Третью группу составили 22 пациента (28 глаз) с верифицированной ХНВ, которая проявлялась в виде субретинальной неоваскулярной мембраны (СНМ), видимой с помощью офтальмоскопии в виде сероватого образования под сетчаткой в центре макулы, либо на томограмме в виде гиперрефлектирующего образования с четкими границами на поверхности хориокапилляров (рис. 3). Ширина СНМ составила в среднем 2049+234 мкм (от 1220 до 3500 мкм). Пигментный эпителий был поврежден в той или иной степени у всех больных в этой группе. У всех пациентов определялась отслойка нейроэпителия. Толщина сетчатки в центре составляла в среднем 120+29 мкм (от 12 до 400 мкм), слои сетчатки дифференцировались с трудом. В толще сетчатки определяются кисты – округлые полости, заполненные прозрачной жидкостью, размером от 40 до 180 мкм в диаметре. Кистовидные полости располагаются веерообразно, в виде лепестков цветка. Более узкая часть полостей находится в центре, ближе к хориоидее. У этих пациентов отмечалось значительное снижение зрительных функций в виде ухудшения остроты зрения в среднем до 0,11+0,02 (от 0,25 до 0,005) и значительного угнетения световой чувствительности макулы в отдельных случаях до 0.
Еще в 35 глазах основным диагностическим признаком был обширный макулярный фиброз. При этом офтальмоскопически под сетчаткой определяется неправильной формы, слегка проминирующее кпереди белое или желто–серое образование с отложением пигмента по краям. Сетчатка над фиброзным рубцом, как правило, отслоена, истончена, возможно наличие отдельных кист. В более поздних стадиях процесса ретинальная ткань прилежит к рубцу и повторяет неровность его поверхности. Чем больше рубец, тем больше повреждены сетчатка, пигментный эпителий и хориокапилляры и тем значительнее нарушения зрительных функций.
На ОСТ под сетчаткой определяется наличие грубого рубца высокой оптической плотности, интраретинальные кисты (рис. 4). Важно отметить, что наряду с образованием плотных рубцов различной площади и объема на этой стадии происходит выраженная дегенерация как сетчатки, так и подлежащей хориоидеи. Слой пигментного эпителия не определяется, т.к. полностью разрушен. Происходит полная деградация нейроэпителия. За счет наличия субретинального фиброза сетчатка в центре возвышалась до 313±57 мкм (от 110 до 748 мкм) над уровнем слоя ПЭС и хориокапилляров. Протяженность фиброза составляла 2982±387 мкм (от 1379 до 5320 мкм). Все пациенты с макулярным фиброзом отмечали отсутствие центрального зрения со снижением остроты зрения до 0,05±0,05.
Таким образом, проведенные исследования пациентов с ВМД с помощью ОСТ высокого разрешения позволили выявить неизвестные ранее закономерности развития данного заболевания. Выявлено, что на первом этапе происходит образование отслойки ПЭС. При дальнейшем развитии патологического процесса происходит и отслойка нейроэпителия. Причиной этого может быть как просачивание жидкости из хориокапилляров через поврежденный ПЭС, так и экссудация из ХНВ, которую на данном этапе не удается выявить с помощью ОСТ. В дальнейшем на фоне прогрессирования заболевания появляется возможность визуализировать ХНВ с помощью оптической томографии. Последующее развитие процесса приводит к образованию фиброзного рубца, кистовидного макулярного отека или географической атрофии. Следует отметить, что нельзя разграничивать эти понятия, так как они являются разными стадиями одного процесса, а каждая форма лишь может превалировать в каждом индивидуальном случае. Ни в одном случае не было выявлено тракционного воздействия на сетчатку со стороны стекловидного тела. Это может быть еще одним свидетельством того, что в основе формирования ВМД лежат патологические процессы, развивающиеся в хориокапиллярах, мембране Бруха, пигментном эпителии и нейроэпителии сетчатки.
Заключение
Оптическая когерентная томография высокого разрешения является информативной, неинвазивной, доступной технологией исследования морфологии заднего полюса глаза. Она позволяет на более высоком уровне увидеть, количественно оценить изменения макулы при влажной форме возрастной макулярной дегенерации, что может способствовать лучшему пониманию патогенеза этого заболевания, а также своевременному и адекватному лечению.
Литература
1. Аверьянов Д.А., Алпатов С.А., Букина В.В. и др. Оптическая когерентная томография // Под ред. А.Г. Щуко, В.В. Малышева. Иркутск: РИО ГУ НЦ ПВХ ВСНЦ СО РАМН, 2005. 112 с.
2. Алпатов С.А., Щуко А.Г., Малышев В.В. Закономерности формирования идиопатических макулярных разрывов // Вестник офтальмологии. 2001. №5. С. 30–33.
3. Алпатов С.А., Урнева Е.М., Щуко А.Г., Малышев В.В. Оптическая когерентная томография влажной ВМД // Современные технологии лечения витреоретинальной патологии: Сборн. научн. трудов. Москва, 2009. С. 178–180.
4. Кравчук Е.А. Роль свободнорадикального окисления в патогенезе заболеваний глаз // Вестник офтальмологии. 2004. Т. 120. №5. С. 48–51.
5. Шпак А.А., Огородникова С.Н. Трехмерная оптическая когерентная томография высокого разрешения // Офтальмохирургия. 2007. №3. С. 61–65
6. Bird A.C, Bressler N.M., Bressler S.B. et al. An International Classification and Grading System for Age–Related Maculopathy and Age Related Macular Degeneration. Special Article // Survey of Ophthalmology. 1995. Vol. 39. P. 367–374.
7. Gorin M. B., Breitner J. C. S., De Jong P.T. et al. The genetics of age–related macular degeneration // Molecular Vision. 1999. Vol. 5. P. 29.
8. Grossniklaus H. E. Histopathologic and Ultrastructural Findings of Surgically Excised Choroidal Neovascularization // Arch. Ophthalmology. 1998. Vol. 116. P. 745–749.
9. Lafaut B.A., Aisenbrey S., Broecke C.V. et al. Clinicopathological correlation of deep retinal vascular anomalous complex in age–related macular degeneration // Br. J. Ophthalmology. 2000. Vol. 84. P. 1269–1274.
10. Seddom J. M. Familial aggregation of age–related maculopathy // Am. J. Ophthalmology. 1998. Vol. 123. №2. P. 199–206.
11. Tuohy G. Researchers promise personalized blood test to detect risk of AMD // EuroTimes. 2008. Vol. 13. №7–8. P. 50.
12. Williams R.A., Brady B.L., Thomas R.J. The psychosocial impact of macular degeneration // Arch. Ophthalmology. 1998. Vol. 116. №4. P. 514–520.












