–Ь–∞—В–µ—А–Є–∞–ї –Є —А–µ–Ј—Г–ї—М—В–∞—В—Л
–Ш–Ј—Г—З–µ–љ–∞ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –Ї–∞—А—В–Є–љ–∞ —Г 17 –±–Њ–ї—М–љ—Л—Е —Б –Њ—В–µ—З–љ—Л–Љ —Н–Ї–Ј–Њ—Д—В–∞–ї—М–Љ–Њ–Љ –≤ —Б—В–∞–і–Є–Є –і–µ–Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є–Є. –Т–Њ –≤—Б–µ—Е —Б–ї—Г—З–∞—П—Е –Є–Љ–µ–ї–Њ –Љ–µ—Б—В–Њ –±–Є–ї–∞—В–µ—А–∞–ї—М–љ–Њ–µ –њ–Њ—А–∞–ґ–µ–љ–Є–µ. –Ю–њ—В–Є—З–µ—Б–Ї–∞—П –љ–µ–є—А–Њ–њ–∞—В–Є—П –љ–∞–±–ї—О–і–∞–ї–∞—Б—М —Г 12 –±–Њ–ї—М–љ—Л—Е (23 –≥–ї–∞–Ј–∞), —Б—А–µ–і–Є –љ–Є—Е 11 –ґ–µ–љ—Й–Є–љ. –°—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В – 45 –ї–µ—В.
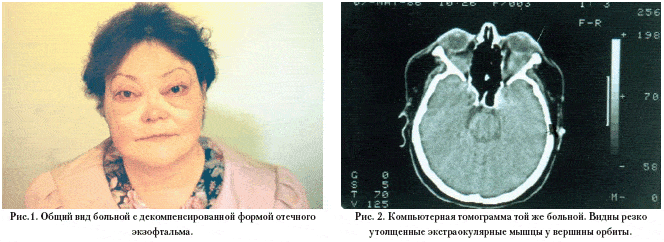
–Ю–±—Й–Є–Љ –і–ї—П –≤—Б–µ—Е –±–Њ–ї—М–љ—Л—Е –Њ–Ї–∞–Ј–∞–ї–Њ—Б—М –±—Л—Б—В—А–Њ–µ —А–∞–Ј–≤–Є—В–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ (–≤ —В–µ—З–µ–љ–Є–µ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –і–љ–µ–є) —Б –њ–∞–і–µ–љ–Є–µ–Љ –Ј—А–Є—В–µ–ї—М–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є –≤ 19 –≥–ї–∞–Ј–∞—Е –Њ—В 0,5 –і–Њ 0,01. –Т–Њ –≤—Б–µ—Е —Б–ї—Г—З–∞—П—Е –њ—А–Є—Б—Г—В—Б—В–≤–Њ–≤–∞–ї–Є –≤–љ–µ—И–љ–Є–µ –њ—А–Є–Ј–љ–∞–Ї–Є –Њ—В–µ—З–љ–Њ–≥–Њ —Н–Ї–Ј–Њ—Д—В–∞–ї—М–Љ–∞ –≤ —Б—В–∞–і–Є–Є –і–µ–Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є–Є: –≤—Л—А–∞–ґ–µ–љ–љ—Л–є —Н–Ї–Ј–Њ—Д—В–∞–ї—М–Љ (–≤—Л—Б—В–Њ—П–љ–Є–µ –≥–ї–∞–Ј–љ—Л—Е —П–±–ї–Њ–Ї —Б–Њ—Б—В–∞–≤–ї—П–ї–Њ 25–30 –Љ–Љ), –љ–µ–њ–Њ–ї–љ–Њ–µ —Б–Љ—Л–Ї–∞–љ–Є–µ –≥–ї–∞–Ј–љ—Л—Е —Й–µ–ї–µ–є, –љ–µ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–є –Њ—В–µ–Ї –њ–µ—А–Є–Њ—А–±–Є—В–∞–ї—М–љ—Л—Е —В–Ї–∞–љ–µ–є, –Ї—А–∞—Б–љ—Л–є —Е–µ–Љ–Њ–Ј, –љ–∞—А—Г—И–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–є –≠–Ь, —А–µ–Ј–Ї–Њ –Ј–∞—В—А—Г–і–љ–µ–љ–љ–∞—П —А–µ–њ–Њ–Ј–Є—Ж–Є—П –≥–ї–∞–Ј–∞ (—А–Є—Б.1).
–Т–љ—Г—В—А–Є–≥–ї–∞–Ј–љ–Њ–µ –і–∞–≤–ї–µ–љ–Є–µ –±—Л–ї–Њ –њ–Њ–≤—Л—И–µ–љ–љ—Л–Љ –≤ 6 –≥–ї–∞–Ј–∞—Е, –њ—А–Є—З–µ–Љ –≤ 5 –Є–Ј –љ–Є—Е —А–∞–Ј–љ–Є—Ж–∞ —Б –њ–∞—А–љ—Л–Љ –≥–ї–∞–Ј–Њ–Љ –њ—А–µ–≤—Л—И–∞–ї–∞ 6 –Љ–Љ —А—В.—Б—В. –Ш–Ј–Љ–µ–љ–µ–љ–Є—П –љ–∞ –≥–ї–∞–Ј–љ–Њ–Љ –і–љ–µ –±—Л–ї–Є –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –Ј–∞—Б—В–Њ–є–љ—Л–Љ –њ–Њ–ї–љ–Њ–Ї—А–Њ–≤–Є–µ–Љ —А–µ—В–Є–љ–∞–ї—М–љ—Л—Е –≤–µ–љ (8 –≥–ї–∞–Ј), –Њ—В–µ–Ї–Њ–Љ –і–Є—Б–Ї–∞ –Ј—А–Є—В–µ–ї—М–љ–Њ–≥–Њ –љ–µ—А–≤–∞ (9) –Є –∞—В—А–Њ—Д–Є–µ–є –µ–≥–Њ (6). –°–љ–Є–ґ–µ–љ–Є–µ –Њ—Б—В—А–Њ—В—Л –Ј—А–µ–љ–Є—П –і–Њ 0,7–0,5 –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ –≤ 5 –≥–ї–∞–Ј–∞—Е —Б –Ј–∞—Б—В–Њ–є–љ—Л–Љ –њ–Њ–ї–љ–Њ–Ї—А–Њ–≤–Є–µ–Љ —А–µ—В–Є–љ–∞–ї—М–љ—Л—Е –≤–µ–љ, –њ—А–Є –Ј–∞—Б—В–Њ–є–љ–Њ–Љ –і–Є—Б–Ї–µ –Њ—Б—В—А–Њ—В–∞ –Ј—А–µ–љ–Є—П –Њ–Ї–∞–Ј–∞–ї–∞—Б—М —Б–љ–Є–ґ–µ–љ–љ–Њ–є –і–Њ 0,5–0,1 –≤ 8 –≥–ї–∞–Ј–∞—Е. –Я—А–Є –∞—В—А–Њ—Д–Є–Є –Ј—А–Є—В–µ–ї—М–љ–Њ–≥–Њ –љ–µ—А–≤–∞ —Б–љ–Є–ґ–µ–љ–Є–µ –Ј—А–µ–љ–Є—П –і–Њ 0,01–0,2 –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ –≤–Њ –≤—Б–µ—Е 6 –≥–ї–∞–Ј–∞—Е. –Я—А–Є –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–Њ–Љ —В–Њ–Љ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Г –≤—Б–µ—Е –±–Њ–ї—М–љ—Л—Е –≤—Л—П–≤–ї–µ–љ—Л —А–µ–Ј–Ї–Њ —Г—В–Њ–ї—Й–µ–љ–љ—Л–µ –≤—Б–µ –њ—А—П–Љ—Л–µ –Љ—Л—И—Ж—Л –≥–ї–∞–Ј–∞. –£—В–Њ–ї—Й–µ–љ–Є–µ –Љ—Л—И—Ж –љ–∞—З–Є–љ–∞–ї–Њ—Б—М –≤ –Њ–±–ї–∞—Б—В–Є –±—А—О—И–Ї–∞ –Є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ—П–ї–Њ—Б—М –і–Њ –≤–µ—А—И–Є–љ—Л –Њ—А–±–Є—В—Л (—А–Є—Б.2).
–£–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–µ —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–µ –Є–ї–ї—О—Б—В—А–Є—А–Њ–≤–∞–ї–Њ —Г—В–Њ–ї—Й–µ–љ–Є–µ –њ—А—П–Љ—Л—Е –Є –Ї–Њ—Б—Л—Е –Љ—Л—И—Ж –≥–ї–∞–Ј–∞ –≤ –Њ–±–ї–∞—Б—В–Є –±—А—О—И–Ї–∞, –Њ—В–µ–Ї —А–µ—В—А–Њ–±—Г–ї—М–±–∞—А–љ–Њ–є –Ї–ї–µ—В—З–∞—В–Ї–Є.
–Т—Б–µ –±–Њ–ї—М–љ—Л–µ –њ–Њ–ї—Г—З–∞–ї–Є –ї–µ—З–µ–љ–Є–µ –≤ —Г—Б–ї–Њ–≤–Є—П—Е —Б—В–∞—Ж–Є–Њ–љ–∞—А–∞. –£ 2 –±–Њ–ї—М–љ—Л—Е –і–Њ –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є—П –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А –њ—А–Њ–≤–Њ–і–Є–ї–Є—Б—М —А–µ—В—А–Њ–±—Г–ї—М–±–∞—А–љ—Л–µ –Є–љ—К–µ–Ї—Ж–Є–Є –Ї–Њ—А—В–Є–Ї–Њ—Б—В–µ—А–Њ–Є–і–Њ–≤ –Є –і–Є—Б—В–∞–љ—Ж–Є–Њ–љ–љ–∞—П —А–µ–љ—В–≥–µ–љ–Њ—В–µ—А–∞–њ–Є—П, –Ї–Њ—В–Њ—А—Л–µ –Њ–Ї–∞–Ј–∞–ї–Є—Б—М –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ–Є. –Ъ–Њ–Љ–њ–ї–µ–Ї—Б–љ–∞—П —В–µ—А–∞–њ–Є—П, –њ—А–Њ–≤–Њ–і–Є–Љ–∞—П –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ, –њ—А–µ–і—Г—Б–Љ–∞—В—А–Є–≤–∞–ї–∞ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –≥–µ–Љ–Њ—Б–Њ—А–±—Ж–Є–Є –Є –њ—Г–ї—М—Б-—В–µ—А–∞–њ–Є–Є. –Я–µ—А—Д—Г–Ј–Є—О –Ї—А–Њ–≤–Є –њ—А–Є –≥–µ–Љ–Њ—Б–Њ—А–±—Ж–Є–Є –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–ї–Є —Б –њ–Њ–Љ–Њ—Й—М—О –∞–њ–њ–∞—А–∞—В–∞ –Р–Ъ–°–Ґ 31-01 –љ–∞ –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ—Л—Е —Г–≥–Њ–ї—М–љ—Л—Е —Б–Њ—А–±–µ–љ—В–∞—Е “–°–Є–Љ–њ–ї–µ–Ї—Б-–§” –њ–Њ –Њ–±—Й–µ–њ—А–Є–љ—П—В–Њ–є –Љ–µ—В–Њ–і–Є–Ї–µ: –і–Њ—Б—В—Г–њ –Ї —Б–Њ—Б—Г–і–∞–Љ “–≤–µ–љ–∞-–≤–µ–љ–∞” —Б –Њ–±—Й–µ–є –≥–µ–њ–∞—А–Є–љ–Є–Ј–∞—Ж–Є–µ–є. –Т –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —В—П–ґ–µ—Б—В–Є –њ—А–Њ—Ж–µ—Б—Б–∞ –Ї—Г—А—Б –ї–µ—З–µ–љ–Є—П —Б–Њ—Б—В–Њ—П–ї –Є–Ј 2–3 —Б–µ–∞–љ—Б–Њ–≤ —Б –љ–µ–і–µ–ї—М–љ—Л–Љ –њ–µ—А–µ—А—Л–≤–Њ–Љ. –Я–Њ—Б–ї–µ –њ–µ—А–≤–Њ–≥–Њ —Б–µ–∞–љ—Б–∞ –≥–µ–Љ–Њ—Б–Њ—А–±—Ж–Є–Є —Б—А–∞–Ј—Г –ґ–µ –љ–∞—З–Є–љ–∞–ї–Є –Ї—Г—А—Б –њ—Г–ї—М—Б-—В–µ—А–∞–њ–Є–Є –њ–Њ –њ—А–Є–љ—П—В–Њ–є —Г –љ–∞—Б –Љ–µ—В–Њ–і–Є–Ї–µ [1]. –Ф–ї—П –Њ—Ж–µ–љ–Ї–Є —В—П–ґ–µ—Б—В–Є –≥–ї–∞–Ј–љ–Њ–≥–Њ —Б—В–∞—В—Г—Б–∞ –Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є —В–µ—А–∞–њ–Є–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є –±–∞–ї–ї—М–љ—Г—О –Њ—Ж–µ–љ–Ї—Г –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ [4]. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –Њ—Б—В—А–Њ—В–∞ –Ј—А–µ–љ–Є—П –≤–Њ –≤—Б–µ—Е –≥–ї–∞–Ј–∞—Е –њ–Њ–≤—Л—Б–Є–ї–∞—Б—М –љ–∞ 0,1–0,6.
–Ю–±—Б—Г–ґ–і–µ–љ–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤
–Ю–њ—В–Є—З–µ—Б–Ї–∞—П –љ–µ–є—А–Њ–њ–∞—В–Є—П, –њ–Њ –љ–∞—И–Є–Љ –і–∞–љ–љ—Л–Љ, –≤—Б—В—А–µ—З–∞–µ—В—Б—П –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –≤ 70% —Б–ї—Г—З–∞–µ–≤ –і–µ–Ї–Њ–Љ–њ–µ–љ—Б–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –Њ—В–µ—З–љ–Њ–≥–Њ —Н–Ї–Ј–Њ—Д—В–∞–ї—М–Љ–∞ —Г –±–Њ–ї—М–љ—Л—Е –њ—А–Њ—Д–µ—Б—Б–Є–Њ–љ–∞–ї—М–љ–Њ –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ –њ—А–Є —Г–≤–µ–ї–Є—З–µ–љ–Є–Є —А–∞–Ј–Љ–µ—А–Њ–≤ –≠–Ь –≤ –Њ–±–ї–∞—Б—В–Є –±—А—О—И–Ї–∞ –Є —Г –≤–µ—А—И–Є–љ—Л –Њ—А–±–Є—В—Л.
–Р–љ–∞–ї–Є–Ј –Њ—Д—В–∞–ї—М–Љ–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –њ—А–Є –Њ—В–µ—З–љ–Њ–Љ —Н–Ї–Ј–Њ—Д—В–∞–ї—М–Љ–µ –њ–Њ–Ј–≤–Њ–ї–Є–ї –≤—Л–і–µ–ї–Є—В—М —В—А–Є —Н—В–∞–њ–∞ –≤ —А–∞–Ј–≤–Є—В–Є–Є –Њ–њ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є–Є. –С—Л—Б—В—А–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –≠–Ь —Г –≤–µ—А—И–Є–љ—Л –Њ—А–±–Є—В—Л –Ј–∞ —Б—З–µ—В –Є—Е –Њ—В–µ–Ї–∞ –Є –ї–Є–Љ—Д–Њ—Ж–Є—В–∞—А–љ–Њ–є –Є–љ—Д–Є–ї—М—В—А–∞—Ж–Є–Є –њ—А–Є–≤–Њ–і–Є—В –љ–∞ –њ–µ—А–≤–Њ–Љ —Н—В–∞–њ–µ –Ї –љ–∞—А—Г—И–µ–љ–Є—О –≤–µ–љ–Њ–Ј–љ–Њ–≥–Њ –Њ—В—В–Њ–Ї–∞, —З—В–Њ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –Ј–∞–Љ–µ–і–ї–µ–љ–Є–µ–Љ –≥–µ–Љ–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є –≤ —Б–Њ—Б—Г–і–∞—Е —Б–µ—В—З–∞—В–Ї–Є –Є –Ј—А–Є—В–µ–ї—М–љ–Њ–≥–Њ –љ–µ—А–≤–∞, –≥–Є–њ–Њ–Ї—Б–Є–Є —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ –љ–∞—А—Г—И–µ–љ–Є–µ–Љ —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞. –Т —Н—В–Њ—В –њ–µ—А–Є–Њ–і –љ–∞ –≥–ї–∞–Ј–љ–Њ–Љ –і–љ–µ –љ–∞–±–ї—О–і–∞–µ—В—Б—П —А–µ–Ј–Ї–Њ–µ –њ–Њ–ї–љ–Њ–Ї—А–Њ–≤–Є–µ —А–µ—В–Є–љ–∞–ї—М–љ—Л—Е –≤–µ–љ —Б–Њ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –Њ—Б—В—А–Њ—В—Л –Ј—А–µ–љ–Є—П –±–Њ–ї–µ–µ —З–µ–Љ —Г –њ–Њ–ї–Њ–≤–Є–љ—Л –±–Њ–ї—М–љ—Л—Е, –≤–µ—А–Њ—П—В–љ–µ–µ –≤—Б–µ–≥–Њ —Б–≤—П–Ј–∞–љ–љ–Њ–µ —Б –≥–Є–њ–Њ–Ї—Б–Є–µ–є –∞–Ї—Б–Є–∞–ї—М–љ–Њ–≥–Њ –њ—Г—З–Ї–∞. –Т–µ–љ–Њ–Ј–љ—Л–є –Ј–∞—Б—В–Њ–є –Є, –Ї–∞–Ї —Б–ї–µ–і—Б—В–≤–Є–µ —Н—В–Њ–≥–Њ, —А–∞—Б—И–Є—А–µ–љ–Є–µ –Ї–∞–њ–Є–ї–ї—П—А–Њ–≤, –њ—А–Є–≤–Њ–і—П—В –Ї —А–µ–Ј–Ї–Њ–Љ—Г –Ј–∞–Љ–µ–і–ї–µ–љ–Є—О —В–Њ–Ї–∞ –Ї—А–Њ–≤–Є. –Т–Њ–Ј–љ–Є–Ї–∞–µ—В –љ–∞—А—Г—И–µ–љ–Є–µ –±–∞—А—М–µ—А–∞ “–Ї—А–Њ–≤—М–—Б–µ—В—З–∞—В–Ї–∞”, “–Ї—А–Њ–≤—М––Ј—А–Є—В–µ–ї—М–љ—Л–є –љ–µ—А–≤”. –°–Њ–Ј–і–∞—О—В—Б—П —Г—Б–ї–Њ–≤–Є—П –і–ї—П –њ—А–Њ–њ–Њ—В–µ–≤–∞–љ–Є—П –Є–Ј –Ї–∞–њ–Є–ї–ї—П—А–Њ–≤ –ґ–Є–і–Ї–Њ—Б—В–Є –Є –Њ—В–µ–Ї–∞ –Ј—А–Є—В–µ–ї—М–љ–Њ–≥–Њ –љ–µ—А–≤–∞, —Б–Њ—Б—В–Њ—П–љ–Є–µ –Ї–Њ—В–Њ—А–Њ–≥–Њ —Г—Б—Г–≥—Г–±–ї—П–µ—В—Б—П –µ—Й–µ –Є –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Є–Љ —Б–і–∞–≤–ї–µ–љ–Є–µ–Љ –µ–≥–Њ —Г –≤–µ—А—И–Є–љ—Л –Њ—А–±–Є—В—Л –Є–Ј–Љ–µ–љ–µ–љ–љ—Л–Љ–Є –≠–Ь. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ—А–Є –Њ–њ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є–Є —Г –±–Њ–ї—М–љ—Л—Е —Б –Њ—В–µ—З–љ—Л–Љ —Н–Ї–Ј–Њ—Д—В–∞–ї—М–Љ–Њ–Љ –≤ –Љ–µ—Е–∞–љ–Є–Ј–Љ–µ —А–∞–Ј–≤–Є—В–Є—П –Ј–∞—Б—В–Њ–є–љ–Њ–≥–Њ –і–Є—Б–Ї–∞ –њ—А–Є–љ–Є–Љ–∞—О—В —Г—З–∞—Б—В–Є–µ –њ–Њ –Љ–µ–љ—М—И–µ–є –Љ–µ—А–µ –і–≤–∞ —Д–∞–Ї—В–Њ—А–∞: –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Њ–µ —Б–і–∞–≤–ї–µ–љ–Є–µ –Ј—А–Є—В–µ–ї—М–љ–Њ–≥–Њ –љ–µ—А–≤–∞ –Є –љ–∞—А—Г—И–µ–љ–Є–µ –≥–µ–Љ–∞—В–Њ–Њ—Д—В–∞–ї—М–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –±–∞—А—М–µ—А–∞, –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ —З–µ–≥–Њ –њ–Њ—П–≤–ї—П–µ—В—Б—П –Њ—В–µ–Ї –Є –≥–Є–њ–Њ–Ї—Б–Є—П —В–Ї–∞–љ–µ–є, –∞ —Н—В–Њ —Б–ї—Г–ґ–Є—В –њ—А–Є—З–Є–љ–Њ–є –±–ї–Њ–Ї–∞–і—Л –∞–Ї—Б–Њ–њ–ї–∞–Ј–Љ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ —В—А–∞–љ—Б–њ–Њ—А—В–∞ –≤ –Ј—А–Є—В–µ–ї—М–љ–Њ–Љ –љ–µ—А–≤–µ –Є –Њ—В–µ–Ї–∞ –µ–≥–Њ —В–Ї–∞–љ–Є. –Я–Њ–ї–∞–≥–∞–µ–Љ, —З—В–Њ –Є–Љ–µ–љ–љ–Њ —Н—В–Є–Љ –Љ–Њ–ґ–љ–Њ –Њ–±—К—П—Б–љ–Є—В—М —А–∞–љ–љ–µ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Њ—Б—В—А–Њ—В—Л –Ј—А–µ–љ–Є—П —Г 89% –±–Њ–ї—М–љ—Л—Е –љ–∞ –≤—В–Њ—А–Њ–Љ —Н—В–∞–њ–µ —А–∞–Ј–≤–Є—В–Є—П –Њ–њ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є–Є –њ—А–Є –Њ—В–µ—З–љ–Њ–Љ —Н–Ї–Ј–Њ—Д—В–∞–ї—М–Љ–µ. –Т –њ–Њ–ї—М–Ј—Г –њ—А–∞–≤–Є–ї—М–љ–Њ—Б—В–Є –њ–Њ–і–Њ–±–љ–Њ–є —В—А–∞–Ї—В–Њ–≤–Ї–Є —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –Є–ї–ї—О—Б—В—А–Є—А—Г—О—Й–Є–µ —А–∞–љ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П, –Њ–њ—А–µ–і–µ–ї—П–µ–Љ—Л–µ —Б –њ–Њ–Љ–Њ—Й—М—О —Н–ї–µ–Ї—В—А–Њ—А–µ—В–Є–љ–Њ–≥—А–∞—Д–Є–Є —Г –±–Њ–ї—М–љ—Л—Е —Б –Њ—В–µ—З–љ—Л–Љ —Н–Ї–Ј–Њ—Д—В–∞–ї—М–Љ–Њ–Љ [3, 5], –∞ —В–∞–Ї–ґ–µ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–є –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ–є –љ–∞ –±—Л—Б—В—А–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Њ—В–µ–Ї–∞ –Є –ї–Є–Љ—Д–Њ—Ж–Є—В–∞—А–љ–Њ–є –Є–љ—Д–Є–ї—М—В—А–∞—Ж–Є–Є.
–Р—В—А–Њ—Д–Є—П –Ј—А–Є—В–µ–ї—М–љ–Њ–≥–Њ –љ–µ—А–≤–∞ —Б —А–µ–Ј–Ї–Є–Љ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –Ј—А–Є—В–µ–ї—М–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є – –µ—Б—В–µ—Б—В–≤–µ–љ–љ—Л–є –Є—Б—Е–Њ–і –љ–µ–ї–µ—З–µ–љ–Њ–є –Њ–њ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є–Є. –£–Љ–µ–љ—М—И–µ–љ–Є–µ –љ–∞–њ—А—П–ґ–µ–љ–Є—П –Љ—П–≥–Ї–Є—Е —В–Ї–∞–љ–µ–є –Њ—А–±–Є—В—Л —Г–і–∞–µ—В—Б—П –і–Њ–±–Є—В—М—Б—П –Є –і–µ–Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Њ–љ–љ—Л–Љ–Є –Њ–њ–µ—А–∞—Ж–Є—П–Љ–Є [6], –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–ґ–љ–Њ –Њ—В–љ–µ—Б—В–Є –Ї —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–Љ—Г –ї–µ—З–µ–љ–Є—О, –Ї —В–Њ–Љ—Г –ґ–µ –Њ–љ–Є –і–∞–ї–µ–Ї–Њ –љ–µ –±–µ–Ј–Њ–њ–∞—Б–љ—Л [7]. –Ь—Л –њ–Њ–ї–∞–≥–∞–µ–Љ, —З—В–Њ –і–µ–Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Њ–љ–љ—Л–µ –Њ–њ–µ—А–∞—Ж–Є–Є –њ—А–Є —В—П–ґ–µ–ї—Л—Е —Д–Њ—А–Љ–∞—Е –Њ—В–µ—З–љ–Њ–≥–Њ —Н–Ї–Ј–Њ—Д—В–∞–ї—М–Љ–∞ –њ–Њ–Ї–∞–Ј–∞–љ—Л —В–Њ–ї—М–Ї–Њ –≤ —Б–ї—Г—З–∞—П—Е –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Ї–Њ—А—В–Є–Ї–Њ—Б—В–µ—А–Њ–Є–і–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ–Њ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–Љ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ.
–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –С—А–Њ–≤–Ї–Є–љ–∞ –Р.–§. –С–Њ–ї–µ–Ј–љ–Є –Њ—А–±–Є—В—Л. –Ь., 1993; 106–21.
2. Tveten S., Mohr C., Esser J. Orbitadekompression in der Behandlung der endokrinen Orbitopathe. Mund-Kiefer-Gesichschir., 1998; 2 (suppl.1): 102–6.
3. Spadea L., Bianco G., Dragani T., Balstrazzi E. Early detection of P-Vep and Perg changes in ophthalmicc Graves disease.- Graefes- Arch-Clin-Exp-Ophthalmol. 1997; bd 235 (8): 501–5.
4. –С—А–Њ–≤–Ї–Є–љ–∞ –§.–§., –Ґ—О—В—О–љ–љ–Є–Ї–Њ–≤–∞ –Р.–Ь. -–Ю –Љ–µ—В–Њ–і–Є–Ї–µ –Њ—Ж–µ–љ–Ї–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —В–µ—З–µ–љ–Є—П –Њ—В–µ—З–љ–Њ–≥–Њ —Н–Ї–Ј–Њ—Д—В–∞–ї—М–Љ–∞ –Є –њ—Б–µ–≤–і–Њ—В—Г–Љ–Њ—А–∞ –Њ—А–±–Є—В—Л. –Т–µ—Б—В–љ. –Њ—Д—В–∞–ї—М–Љ–Њ–ї. 1990; 2: 16–8.
5. Genovesi-Ebert F., Di-Bartolo E., Lepri A., Foggi V., Romani A. Nardi M. -Standardized echography, pattern electroretinography and visual evoked potential and automated perimetry in the early dioagnosis of Graves neuropathy. Ophthalmology 1998; 212 (suppl. 1), 101–3.
6. Ohtsuka K., Nakamura Y. Results of transmedial-canthal etmoidal decompression for severe dysthyroid optic neuropaty.- Jpn-J-Ophthalmol. 1999; 43 (5): 426–32.
7. Partdaens D., Haus K., van-Buitenen S., Mourits M. The incidence of diplopia folloving coronal and transeid orbital decompression in Graves orbitopathy. Eye 1998; 12 (5): 800–5.












