–Т–≤–µ–і–µ–љ–Є–µ
–Я–Њ –і–∞–љ–љ—Л–Љ –Ь–µ–ґ–і—Г–љ–∞—А–Њ–і–љ–Њ–є –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —Д–µ–і–µ—А–∞—Ж–Є–Є [1], –Ї –Ї–Њ–љ—Ж—Г 2014 –≥. –≤ –Љ–Є—А–µ –љ–∞—Б—З–Є—В—Л–≤–∞–ї–Њ—Б—М –±–Њ–ї–µ–µ 400 –Љ–ї–љ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф. –Я—А–Є —Н—В–Њ–Љ —З–Є—Б–ї–Њ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –љ–∞—А—Г—И–µ–љ–Є–µ–Љ —В–Њ–ї–µ—А–∞–љ—В–љ–Њ—Б—В–Є –Ї –≥–ї—О–Ї–Њ–Ј–µ –њ—А–µ–≤—Л—Б–Є–ї–Њ 600 –Љ–ї–љ —З–µ–ї–Њ–≤–µ–Ї. –Т –†–Њ—Б—Б–Є–Є –љ–∞–±–ї—О–і–∞—О—В—Б—П –∞–љ–∞–ї–Њ–≥–Є—З–љ—Л–µ —В–µ–љ–і–µ–љ—Ж–Є–Є [2]. –Я–Њ –і–∞–љ–љ—Л–Љ –Њ—Д–Є—Ж–Є–∞–ї—М–љ–Њ–≥–Њ —А–µ–≥–Є—Б—В—А–∞, –≤ –†–§ –љ–∞ 01.01.2015 –≥. –±—Л–ї–Њ –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ–Њ 4 045 654 –±–Њ–ї—М–љ—Л—Е —Б –°–Ф. –Ю–і–љ–∞–Ї–Њ —А–µ–∞–ї—М–љ–∞—П —З–Є—Б–ї–µ–љ–љ–Њ—Б—В—М —Н—В–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ 2вАУ2,5 —А–∞–Ј–∞ –њ—А–µ–≤—Л—И–∞–µ—В –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ–љ—Г—О –Є –њ—А–Є–±–ї–Є–ґ–∞–µ—В—Б—П –Ї 7% –љ–∞—Б–µ–ї–µ–љ–Є—П —Б—В—А–∞–љ—Л. –Я–Њ—З—В–Є 1/5 —З–∞—Б—В—М –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф (19,85%) –Є–Љ–µ–µ—В –њ—А–Њ–±–ї–µ–Љ—Л —Б–Њ –Ј—А–µ–љ–Є–µ–Љ. –С–Њ–ї—М—И—Г—О —З–∞—Б—В—М –Є–Ј –љ–Є—Е (70вАУ75%) —Б–Њ—Б—В–∞–≤–ї—П—О—В –њ–∞—Ж–Є–µ–љ—В—Л —Б —А–∞–Ј–ї–Є—З–љ–Њ–є —Б—В–µ–њ–µ–љ—М—О –Ф–†, –Љ–µ–љ—М—И—Г—О (20вАУ25%) вАУ —Б –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –Ї–∞—В–∞—А–∞–Ї—В–Њ–є, –≤—В–Њ—А–Є—З–љ–Њ–є –љ–µ–Њ-–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–є –≥–ї–∞—Г–Ї–Њ–Љ–Њ–є (–Э–У), —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –Ї—А–∞–µ–≤ –≤–µ–Ї, —В—А–∞–љ–Ј–Є—В–Њ—А–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є –Ј—А–µ–љ–Є—П –Є –і—А—Г–≥–Є–Љ–Є –њ—А–Њ–±–ї–µ–Љ–∞–Љ–Є [3].
–†–∞–Ј–≤–Є—В–Є–µ –њ—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –≤ –Ј–∞–і–љ–µ–Љ –Њ—В–і–µ–ї–µ –≥–ї–∞–Ј–∞ (—В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ–∞—П –Ј–∞–і–љ—П—П –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є—П) —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П —А–Њ—Б—В–Њ–Љ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е, –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є –љ–µ–њ–Њ–ї–љ–Њ—Ж–µ–љ–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤ –њ–Њ –Ј–∞–і–љ–µ–є –≥–Є–∞–ї–Њ–Є–і–љ–Њ–є –Љ–µ–Љ–±—А–∞–љ–µ (–Ч–У–Ь) —Б—В–µ–Ї–ї–Њ–≤–Є–і–љ–Њ–≥–Њ —В–µ–ї–∞ (–°–Ґ) —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ–Љ –Ї—А–Њ–≤–Њ–Є–Ј–ї–Є—П–љ–Є–є, —Д–Є–±—А–Њ–Ј–∞ –Є –Њ—В—Б–ї–Њ–є–Ї–Є —Б–µ—В—З–∞—В–Ї–Є. –Э–µ–Њ–≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є—П –њ–µ—А–µ–і–љ–µ–≥–Њ –Њ—В—А–µ–Ј–Ї–∞ –≥–ї–∞–Ј–∞ (—В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ–∞—П –њ–µ—А–µ–і–љ—П—П –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є—П) –њ—А–Є–≤–Њ–і–Є—В –Ї –Є–Ј–Љ–µ–љ–µ–љ–Є—О —Б—В—А—Г–Ї—В—Г—А—Л —Г–≥–ї–∞ –њ–µ—А–µ–і–љ–µ–є –Ї–∞–Љ–µ—А—Л (–£–Я–Ъ), –љ–∞—А—Г—И–µ–љ–Є—О –Њ—В—В–Њ–Ї–∞ –≤–љ—Г—В—А–Є–≥–ї–∞–Ј–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є, —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–Љ—Г –њ–Њ–≤—Л—И–µ–љ–Є—О –≤–љ—Г—В—А–Є–≥–ї–∞–Ј–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –Є –≤ –Ї–Њ–љ–µ—З–љ–Њ–Љ –Є—В–Њ–≥–µ вАУ –Ї —А–∞–Ј–≤–Є—В–Є—О –≤—В–Њ—А–Є—З–љ–Њ–є –Э–У, –Ї–Њ—В–Њ—А–∞—П —П–≤–ї—П–µ—В—Б—П –Њ–і–љ–Њ–є –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ —В—П–ґ–µ–ї—Л—Е —Д–Њ—А–Љ –≥–ї–∞—Г–Ї–Њ–Љ—Л –Є –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї –Њ–і–љ–Њ–є –Є–Ј —В–µ—А–Љ–Є–љ–∞–ї—М–љ—Л—Е —Б—В–∞–і–Є–є –њ—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ–Њ–є –Ф–† –њ—А–Є –°–Ф. –Я–Њ –љ–∞—И–Є–Љ –і–∞–љ–љ—Л–Љ, –Њ–љ–∞ –і–Є–∞–≥–љ–Њ—Б—В–Є—А—Г–µ—В—Б—П —Г 0,3% –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Њ–±—А–∞—В–Є–≤—И–Є—Е—Б—П –Ј–∞ –Ї–Њ–љ—Б—Г–ї—М—В–∞—Ж–Є–µ–є –Ї –Њ–Ї—Г–ї–Є—Б—В—Г –њ–Њ –њ–Њ–≤–Њ–і—Г –≥–ї–∞–Ј–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –°–Ф [4].
–§—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ –љ–µ–њ–Њ–ї–љ–Њ—Ж–µ–љ–љ—Л–µ –љ–Њ–≤–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–љ—Л–µ —Б–Њ—Б—Г–і—Л —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—В—Б—П –±—Л—Б—В—А—Л–Љ —А–Њ—Б—В–Њ–Љ, –Љ–∞—Б—Б–Є–≤–љ–Њ–є —В—А–∞–љ—Б—Б—Г–і–∞—Ж–Є–µ–є –њ–ї–∞–Ј–Љ—Л –Є –њ–Њ–≤—Л—И–µ–љ–љ–Њ–є –ї–Њ–Љ–Ї–Њ—Б—В—М—О, –Ї–Њ—В–Њ—А–∞—П –њ—А–Є–≤–Њ–і–Є—В –Ї –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—О –Ї—А–Њ–≤–Њ–Є–Ј–ї–Є—П–љ–Є–є [5]. –Т —А–∞–Ј–≤–Є—В–Є–Є —Б–ї–µ–њ–Њ—В—Л —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ–µ—В –њ—А–Њ—Б–∞—З–Є–≤–∞–љ–Є–µ –Є–Ј –љ–Њ–≤–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤ –±–µ–ї–Ї–Њ–≤—Л—Е —Д—А–∞–Ї—Ж–Є–є –њ–ї–∞–Ј–Љ—Л –Ї—А–Њ–≤–Є, –Ї–Њ—В–Њ—А—Л–µ –Ј–∞–њ—Г—Б–Ї–∞—О—В –њ—А–Њ—Ж–µ—Б—Б—Л —А—Г–±—Ж–µ–≤–∞–љ–Є—П –≤ —В–Ї–∞–љ—П—Е —А–∞–і—Г–ґ–Ї–Є, —Б–µ—В—З–∞—В–Ї–Є –Є –°–Ґ, —З—В–Њ –≤ –Ї–Њ–љ–µ—З–љ–Њ–Љ —Б—З–µ—В–µ –Љ–Њ–ґ–µ—В –±—Л—В—М –њ—А–Є—З–Є–љ–Њ–є –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П —В—А–∞–Ї—Ж–Є–Њ–љ–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞. –Ш–љ–Њ–≥–і–∞ –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є—П –њ—А–Њ—В–µ–Ї–∞–µ—В –љ–µ—В–Є–њ–Є—З–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ вАУ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Б–Њ—Б—Г–і—Л —А–∞—Б—В—Г—В –њ–Њ —Г–њ–ї–Њ—В–љ–µ–љ–љ–Њ–є –њ–µ—А–µ–і–љ–µ–є –≥–Є–∞–ї–Њ–Є–і–љ–Њ–є –Љ–µ–Љ–±—А–∞–љ–µ (–Я–У–Ь) –°–Ґ (—В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ–∞—П —Б—А–µ–і–љ—П—П –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є—П). –Т –Њ–і–љ–Є—Е —Б–ї—Г—З–∞—П—Е –њ—А–Њ—Ж–µ—Б—Б –Љ–Њ–ґ–µ—В –љ–Њ—Б–Є—В—М –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А (—Б–Њ—З–µ—В–∞–љ–Є–µ –љ–µ–Ї–Њ—В–Њ—А—Л—Е –≤–Є–і–Њ–≤ –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –љ–µ–Њ–≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є–Є), –≤ –і—А—Г–≥–Є—Е вАУ –±—Л—В—М —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ—Л–Љ –Є –ї–Њ–Ї–∞–ї—М–љ—Л–Љ —Б–Є–Љ–њ—В–Њ–Љ–Њ–Љ –њ—А–Њ—П–≤–ї–µ–љ–Є—П –њ—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ–Њ–є –Ф–†.
–Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ —Ж–µ–ї—М—О –і–∞–љ–љ–Њ–є —А–∞–±–Њ—В—Л —Б—В–∞–ї–Њ –Њ–±–Њ–±—Й–µ–љ–Є–µ —Б–Њ–±—Б—В–≤–µ–љ–љ—Л—Е –і–∞–љ–љ—Л—Е –Њ —А–∞–Ј–ї–Є—З–љ—Л—Е –≤–∞—А–Є–∞–љ—В–∞—Е —В–µ—З–µ–љ–Є—П –њ—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –њ—А–Є –Ф–† –Є –∞–Ї—В—Г–∞–ї—М–љ—Л—Е —Б–њ–Њ—Б–Њ–±–∞—Е –µ–≥–Њ –ї–µ—З–µ–љ–Є—П.
–Ь–∞—В–µ—А–Є–∞–ї –Є –Љ–µ—В–Њ–і—Л
–С—Л–ї–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ—Л –њ–∞—Ж–Є–µ–љ—В—Л –Є–Ј —А–∞–Ј–ї–Є—З–љ—Л—Е —А–µ–≥–Є–Њ–љ–Њ–≤ –†–Њ—Б—Б–Є–Є —Б –°–Ф 1-–≥–Њ –Є 2-–≥–Њ —В–Є–њ–∞, –Њ–±—А–∞—В–Є–≤—И–Є–µ—Б—П –Ј–∞ –њ–Њ–Љ–Њ—Й—М—О –њ–Њ –њ–Њ–≤–Њ–і—Г –њ—А–Њ–±–ї–µ–Љ —Б–Њ –Ј—А–µ–љ–Є–µ–Љ –≤ –Њ—В–і–µ–ї–µ–љ–Є–µ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —А–µ—В–Є–љ–Њ–њ–∞—В–Є–Є –Є –Њ—Д—В–∞–ї—М–Љ–Њ—Е–Є—А—Г—А–≥–Є–Є –§–У–С–£ –≠–Э–¶ –Ь–Є–љ-–Ј–і—А–∞–≤–∞ –†–Њ—Б—Б–Є–Є –≤ 2011вАУ2015 –≥–≥. –Ч–∞ —Н—В–Њ –≤—А–µ–Љ—П –±—Л–ї–Њ –њ—А–Њ–Ї–Њ–љ—Б—Г–ї—М—В–Є—А–Њ–≤–∞–љ–Њ –±–Њ–ї–µ–µ 31 700 —З–µ–ї–Њ–≤–µ–Ї, –Є–Ј –Ї–Њ—В–Њ—А—Л—Е –Њ–Ї–Њ–ї–Њ 27 —В—Л—Б. –±—Л–ї–Є –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є —Б –°–Ф (85%) –Њ–±–Њ–Є—Е —В–Є–њ–Њ–≤ (–°–Ф 2-–≥–Њ —В–Є–њ–∞ вАУ 92,5%, 1-–≥–Њ —В–Є–њ–∞ вАУ 7,5%), —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є–µ –ґ–µ–љ—Й–Є–љ—Л/–Љ—Г–ґ—З–Є–љ—Л вАУ 68% –Є 32% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, —Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В вАУ –Њ–Ї–Њ–ї–Њ 67 –ї–µ—В.
–£ –≤—Б–µ—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±—Л–ї–Є –≤—Л–њ–Њ–ї–љ–µ–љ—Л –Њ–±—Л—З–љ–Њ–µ —Н–љ–і–Њ–Ї—А–Є–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ (–Ї–Њ–љ—В—А–Њ–ї—М —Г—А–Њ–≤–љ—П —Б–∞—Е–∞—А–∞ –≤ –Ї—А–Њ–≤–Є, –≥–ї–Є–Ї–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –≥–µ–Љ–Њ–≥–ї–Њ–±–Є–љ–∞, —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–Њ–≤, —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞) –Є –Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ (–≤–Є–Ј–Њ–Љ–µ—В—А–Є—П, –Њ—Д—В–∞–ї—М–Љ–Њ—Б–Ї–Њ–њ–Є—П, –≥–Њ–љ–Є–Њ—Б–Ї–Њ–њ–Є—П, –±–µ—Б–Ї–Њ–љ—В–∞–Ї—В–љ–∞—П —В–Њ–љ–Њ–Љ–µ—В—А–Є—П, —В–Њ–љ–Њ–≥—А–∞—Д–Є—П, –њ–µ—А–Є–Љ–µ—В—А–Є—П) –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –Я—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –≤—Л–њ–Њ–ї–љ—П–ї–Є—Б—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л–µ –љ–∞ –≤—Л—П–≤–ї–µ–љ–Є–µ –Є —Г—В–Њ—З–љ–µ–љ–Є–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –°–Ф (–Ї–Њ–љ—Б—Г–ї—М—В–∞—Ж–Є–Є —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є—Е —Б–њ–µ—Ж–Є–∞–ї–Є—Б—В–Њ–≤) –Є –≥–ї–∞–Ј–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є (–Њ–њ—В–Є—З–µ—Б–Ї–∞—П –Ї–Њ–≥–µ—А–µ–љ—В–љ–∞—П —В–Њ–Љ–Њ–≥—А–∞—Д–Є—П, —Д–ї—О–Њ—А–µ—Б—Ж–µ–љ—В–љ–∞—П –∞–љ–≥–Є–Њ–≥—А–∞—Д–Є—П (–§–Р–У), —Д–Њ—В–Њ–≥—А–∞—Д–Є—А–Њ–≤–∞–љ–Є–µ –≥–ї–∞–Ј–љ–Њ–≥–Њ –і–љ–∞ –љ–∞ —Д—Г–љ–і—Г—Б-–Ї–∞–Љ–µ—А–µ).
–Ч–∞ —Г–Ї–∞–Ј–∞–љ–љ—Л–є –њ–µ—А–Є–Њ–і —Г 1035 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (3,8%) –±—Л–ї–Є –њ—А–Њ–≤–µ–і–µ–љ—Л —А–∞–Ј–ї–Є—З–љ—Л–µ –Њ–њ–µ—А–∞—В–Є–≤–љ—Л–µ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞: –≤–Є—В—А—Н–Ї—В–Њ–Љ–Є—П (–Т–≠), —Д–∞–Ї–Њ—Н–Љ—Г–ї—М—Б–Є—Д–Є–Ї–∞—Ж–Є—П –Њ—Б–ї–Њ–ґ–љ–µ–љ–љ–Њ–є –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –Ї–∞—В–∞—А–∞–Ї—В—Л, –і—А–µ–љ–∞–ґ–љ–∞—П —Е–Є—А—Г—А–≥–Є—П –≤—В–Њ—А–Є—З–љ–Њ–є –Э–У, –Є–љ—В—А–∞–≤–Є—В—А–µ–∞–ї—М–љ–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ –∞–љ—В–Є–∞–љ–≥–Є–Њ–≥–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –£ 1844 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (6,8%) –±—Л–ї–∞ –≤—Л–њ–Њ–ї–љ–µ–љ–∞ –ї–∞–Ј–µ—А–љ–∞—П –Ї–Њ–∞–≥—Г–ї—П—Ж–Є—П —Б–µ—В—З–∞—В–Ї–Є (–Ы–Ъ–°).
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Є –Њ–±—Б—Г–ґ–і–µ–љ–Є–µ
–Ъ–ї–∞—Б—Б–Є—З–µ—Б–Ї–Њ–µ —А–∞–Ј–≤–Є—В–Є–µ –њ—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –≤ –≥–ї–∞–Ј–љ–Њ–Љ —П–±–ї–Њ–Ї–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф –Є–і–µ—В –≤ –Ј–∞–і–љ–µ–Љ –Њ—В—А–µ–Ј–Ї–µ –≥–ї–∞–Ј–∞ –Є —Г—Б–ї–Њ–≤–љ–Њ –Љ–Њ–ґ–µ—В –±—Л—В—М –Њ—В–љ–µ—Б–µ–љ–Њ –Ї –Ј–∞–і–љ–µ–є –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є–Є. –Ґ–∞–Ї–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ –Њ–Ї–Њ–ї–Њ 2 —В—Л—Б. —З–µ–ї–Њ–≤–µ–Ї, —З—В–Њ —Б–Њ—Б—В–∞–≤–Є–ї–Њ 6,9% –Њ—В –≤—Б–µ—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф [3].
–Я—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ–∞—П –Ф–† —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –њ–Њ—П–≤–ї–µ–љ–Є–µ–Љ –љ–Њ–≤–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤ –љ–µ —В–Њ–ї—М–Ї–Њ –њ–Њ –≤—Б–µ–Љ—Г –њ–Њ–ї—О —Б–µ—В—З–∞—В–Ї–Є, –љ–Њ –Є –≤ –Њ–±–ї–∞—Б—В–Є –і–Є—Б–Ї–∞ –Ј—А–Є—В–µ–ї—М–љ–Њ–≥–Њ –љ–µ—А–≤–∞ —Б –Є—Е –Є–љ—В–µ–љ—Б–Є–≤–љ—Л–Љ –њ—А–Њ–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ–Љ –≤ –°–Ґ. –Ь–љ–Њ–≥–Є–Љ–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—П–Љ–Є –њ–Њ–Ї–∞–Ј–∞–љ–Њ [6], —З—В–Њ –љ–Њ–≤–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–љ—Л–µ —Б–Њ—Б—Г–і—Л —А–∞—Б—В—Г—В –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –≤–і–Њ–ї—М –Ј–∞–і–љ–µ–є (—А–µ—В–Є–љ–∞–ї—М–љ–Њ–є) –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Ч–У–Ь. –Я—А–Є –љ–∞–ї–Є—З–Є–Є –і–µ—Д–µ–Ї—В–Њ–≤ –≤ –Ч–У–Ь –њ—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ–∞—П —В–Ї–∞–љ—М —А–∞—Б—Б–ї–∞–Є–≤–∞–µ—В –µ–µ –Є–ї–Є –њ—А–Њ—А–∞—Б—В–∞–µ—В –љ–∞ –њ–µ—А–µ–і–љ—О—О –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В—М –Љ–µ–Љ–±—А–∞–љ—Л. –†–Њ—Б—В–∞ –љ–Њ–≤–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤ –≤–љ–µ –Ч–У–Ь –љ–µ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ. –Я—А–Є –Њ—В—Б–ї–Њ–є–Ї–µ –Ч–У–Ь –љ–Њ–≤–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–љ—Л–µ —Б–Њ—Б—Г–і—Л –Њ—Д—В–∞–ї—М–Љ–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Є –Є–Љ–Є—В–Є—А—Г—О—В –њ—А–Њ—А–∞—Б—В–∞–љ–Є–µ –≤ –°–Ґ. –Т —Б–ї—Г—З–∞–µ –Њ—В—Б—Г—В—Б—В–≤–Є—П –Њ—В—Б–ї–Њ–є–Ї–Є –Ч–У–Ь –љ–Њ–≤–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–љ—Л–µ —Б–Њ—Б—Г–і—Л —А–∞—Б—В—Г—В –≤ –њ–ї–Њ—Б–Ї–Њ—Б—В–Є —Б–µ—В—З–∞—В–Ї–Є –Љ–µ–ґ–і—Г –≤–љ—Г—В—А–µ–љ–љ–µ–є –њ–Њ–≥—А–∞–љ–Є—З–љ–Њ–є –Љ–µ–Љ–±—А–∞–љ–Њ–є –Є –Ч–У–Ь, —А–∞—Б–њ–Њ–ї–∞–≥–∞—П—Б—М –љ–∞ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є —Б–µ—В—З–∞—В–Ї–Є. –Т –њ—А–Њ—Ж–µ—Б—Б–µ —А–∞–Ј–≤–Є—В–Є—П –њ—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ–Њ–є –Ф–† –Ч–У–Ь –Є –љ–Њ–≤–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–љ–∞—П —Н–њ–Є—А–µ—В–Є–љ–∞–ї—М–љ–∞—П —В–Ї–∞–љ—М –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –љ–µ –Њ—В–ї–Є—З–∞—О—В—Б—П –і—А—Г–≥ –Њ—В –і—А—Г–≥–∞. –Ф–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ–Њ–ї–љ–∞—П –Њ—В—Б–ї–Њ–є–Ї–∞ –Ч–У–Ь –°–Ґ –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞–µ—В —А–∞–Ј–≤–Є—В–Є–µ –њ—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ–Њ–є –Ф–†. –Я–Њ—Н—В–Њ–Љ—Г –≥–ї–∞–≤–љ–∞—П –Ј–∞–і–∞—З–∞ –≤–Є—В—А–µ–Њ—А–µ—В–Є–љ–∞–ї—М–љ–Њ–є —Е–Є—А—Г—А–≥–Є–Є вАУ –њ–Њ–ї–љ–Њ–µ —Г–і–∞–ї–µ–љ–Є–µ –Ч–У–Ь –Ї–∞–Ї —Б—Г–±—Б—В—А–∞—В–∞ –і–ї—П —А–Њ—Б—В–∞ –љ–Њ–≤–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤.
–Ы–µ—З–µ–љ–Є–µ –њ—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –≤ –ї—О–±–Њ–Љ –Њ—В–і–µ–ї–µ –≥–ї–∞–Ј–љ–Њ–≥–Њ —П–±–ї–Њ–Ї–∞, –Ї–∞–Ї –Є –і—А—Г–≥–Є—Е –њ–Њ–Ј–і–љ–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –°–Ф, –±–∞–Ј–Є—А—Г–µ—В—Б—П –љ–∞ –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–є –Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є–Є –≥–ї–Є–Ї–µ–Љ–Є–Є –і–ї—П –і–∞–љ–љ–Њ–≥–Њ –њ–∞—Ж–Є–µ–љ—В–∞ –љ–∞—А—П–і—Г —Б –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–µ–є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –ґ–Є—А–Њ–≤–Њ–≥–Њ, –±–µ–ї–Ї–Њ–≤–Њ–≥–Њ –Є –≤–Њ–і–љ–Њ-—Б–Њ–ї–µ–≤–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞. –Ю–і–љ–Є–Љ –Є–Ј —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л—Е –Љ–µ—В–Њ–і–Њ–≤ –ї–µ—З–µ–љ–Є—П –Ј–∞–і–љ–µ–є –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є–Є –±—Л–ї–∞ –Є –Њ—Б—В–∞–µ—В—Б—П –Ы–Ъ–°. –Х–µ —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–Њ–µ –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –≤ –∞–і–µ–Ї–≤–∞—В–љ–Њ–Љ –Њ–±—К–µ–Љ–µ –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ —Б—В–∞–±–Є–ї–Є–Ј–Є—А–Њ–≤–∞—В—М –њ—А–Њ—Ж–µ—Б—Б –≤ 70вАУ75% —Б–ї—Г—З–∞–µ–≤ –і–∞–ґ–µ –њ—А–Є –њ—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ–Њ–є —Б—В–∞–і–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П [7].
–Х—Б–ї–Є –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –њ—А–Њ—Ж–µ—Б—Б –±—Л–ї –Њ–≥—А–∞–љ–Є—З–µ–љ –Њ—В–і–µ–ї—М–љ—Л–Љ–Є —Г—З–∞—Б—В–Ї–∞–Љ–Є (—З—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–ї–Њ—Б—М –і–∞–љ–љ—Л–Љ–Є –§–Р–У), —В–Њ –±—Л–ї–∞ –≤—Л–њ–Њ–ї–љ–µ–љ–∞ —Д–Њ–Ї–∞–ї—М–љ–∞—П –Ы–Ъ–° –≤ –њ—А–µ–і–µ–ї–∞—Е –њ–Њ—А–∞–ґ–µ–љ–љ—Л—Е —Г—З–∞—Б—В–Ї–Њ–≤. –Я—А–Є –Њ–±—И–Є—А–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є—П—Е –Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є–Є –Љ—Л –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є –њ–∞–љ—А–µ—В–Є–љ–∞–ї—М–љ—Г—О –Ы–Ъ–°. –Ы–µ—З–µ–љ–Є–µ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –≤ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —Н—В–∞–њ–Њ–≤ (—Б–µ–∞–љ—Б–Њ–≤) –њ–Њ–і –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –§–Р–У. –¶–µ–ї—М –Ы–Ъ–° вАФ –њ—А–µ–Ї—А–∞—Й–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А–Њ–≤–∞–љ–Є—П –љ–µ–њ–Њ–ї–љ–Њ—Ж–µ–љ–љ—Л—Е –љ–Њ–≤–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В —Б–Њ–±–Њ–є –Њ—Б–љ–Њ–≤–љ—Г—О —Г–≥—А–Њ–Ј—Г —А–∞–Ј–≤–Є—В–Є—П —В–∞–Ї–Є—Е —В—П–ґ–µ–ї—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, –Ї–∞–Ї –≥–µ–Љ–Њ—Д—В–∞–ї—М–Љ, –Њ—В—Б–ї–Њ–є–Ї–∞ —Б–µ—В—З–∞—В–Ї–Є, —А—Г–±–µ–Њ–Ј —А–∞–і—Г–ґ–Ї–Є –Є –≤—В–Њ—А–Є—З–љ–∞—П –≥–ї–∞—Г–Ї–Њ–Љ–∞. –Ч–љ–∞—З–Є—В–µ–ї—М–љ—Л–µ –Ї—А–Њ–≤–Њ–Є–Ј–ї–Є—П–љ–Є—П, –љ–∞–ї–Є—З–Є–µ –њ–ї–Њ—В–љ—Л—Е –њ—А–Њ–ї–Є—Д–µ—А–∞—В–Њ–≤ –≤ –°–Ґ, –њ–Њ–Љ—Г—В–љ–µ–љ–Є–µ —Е—А—Г—Б—В–∞–ї–Є–Ї–∞ –Ј–∞—В—А—Г–і–љ—П—О—В, –∞ –Є–љ–Њ–≥–і–∞ –Є –і–µ–ї–∞—О—В –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ—Л–Љ –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –Ы–Ъ–°.
–° —А–Њ—Б—В–Њ–Љ —В–µ—Е–љ–Є—З–µ—Б–Ї–Њ–є –Њ—Б–љ–∞—Й–µ–љ–љ–Њ—Б—В–Є –Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥–Є–Є –≤ —Ж–µ–ї–Њ–Љ –Є —Е–Є—А—Г—А–≥–Є–Є –≤ —З–∞—Б—В–љ–Њ—Б—В–Є –∞–Ї—В–Є–≤–љ–Њ —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –Є –і—А—Г–≥–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–є –Љ–µ—В–Њ–і –ї–µ—З–µ–љ–Є—П –њ—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ–Њ–є —Б—В–∞–і–Є–Є –Ф–† вАУ –Т–≠ вАУ —Г–і–∞–ї–µ–љ–Є–µ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є –Є–Ј–Љ–µ–љ–µ–љ–љ–Њ–≥–Њ –°–Ґ. –Ю–љ–∞ –њ–Њ–Ї–∞–Ј–∞–љ–∞ –њ—А–Є –Љ–∞—Б—Б–Є–≤–љ—Л—Е, –і–ї–Є—В–µ–ї—М–љ–Њ –љ–µ—А–∞—Б—Б–∞—Б—Л–≤–∞—О—Й–Є—Е—Б—П –≥–µ–Љ–Њ—Д—В–∞–ї—М–Љ–∞—Е, —В—А–∞–Ї—Ж–Є–Њ–љ–љ–Њ–Љ —Б–Є–љ–і—А–Њ–Љ–µ, –Њ—В—Б–ї–Њ–є–Ї–µ —Б–µ—В—З–∞—В–Ї–Є. –Ъ—А–Њ–≤–Њ–Є–Ј–ї–Є—П–љ–Є–µ –љ–∞ –µ–і–Є–љ—Б—В–≤–µ–љ–љ–Њ –≤–Є–і—П—Й–µ–Љ –≥–ї–∞–Ј—Г –Є –і–≤—Г—Б—В–Њ—А–Њ–љ–љ–Є–є –≥–µ–Љ–Њ—Д—В–∞–ї—М–Љ —В–∞–Ї–ґ–µ —Б—З–Є—В–∞—О—В –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ–Є –Ї —Б—А–Њ—З–љ–Њ–є –Т–≠. –Ф–ї—П —А–µ—И–µ–љ–Є—П –≤–Њ–њ—А–Њ—Б–∞ –Њ —В–∞–Ї—В–Є–Ї–µ –ї–µ—З–µ–љ–Є—П, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Є –≤—Л–±–Њ—А–µ –∞–љ–µ—Б—В–µ–Ј–Є–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–∞ —Б–Њ–≥–ї–∞—Б–Њ–≤–∞–љ–љ–∞—П —А–∞–±–Њ—В–∞ –Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥–∞, —Н–љ–і–Њ–Ї—А–Є–љ–Њ–ї–Њ–≥–∞ –Є –∞–љ–µ—Б—В–µ–Ј–Є–Њ–ї–Њ–≥–∞.
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –њ–Њ–ї—Г—З–µ–љ —Е–Њ—А–Њ—И–Є–є —Н—Д—Д–µ–Ї—В –ї–µ—З–µ–љ–Є—П –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Љ–∞–Ї—Г–ї—П—А–љ–Њ–≥–Њ –Њ—В–µ–Ї–∞, –Ї–Њ—В–Њ—А—Л–є –≤—Б—В—А–µ—З–∞–µ—В—Б—П –њ—А–Є –ї—О–±–Њ–є —Б—В–∞–і–Є–Є –Ф–†, –Њ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –љ–Њ–≤–Њ–є –≥—А—Г–њ–њ—Л –њ—А–µ–њ–∞—А–∞—В–Њ–≤ вАУ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –∞–љ–≥–Є–Њ–≥–µ–љ–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ (–∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–≤ –≤–∞–Ј–Њ—Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞ —А–Њ—Б—В–∞). –Я–Њ–ї—Г—З–µ–љ–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Е –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –≤–Љ–µ—Б—В–µ —Б –њ–∞–љ—А–µ—В–Є–љ–∞–ї—М–љ–Њ–є –Ы–Ъ–° –≤—Б–µ–ї—П—О—В –љ–∞–і–µ–ґ–і—Г –љ–∞ —Г—Б–њ–µ—И–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ –њ—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ–Њ–є —Б—В–∞–і–Є–Є –Ф–†.
–°–µ–≥–Њ–і–љ—П —Г–ґ–µ —В—А—Г–і–љ–Њ –њ—А–µ–і—Б—В–∞–≤–Є—В—М, —З—В–Њ —А—Г–±–µ–Њ–Ј —А–∞–і—Г–ґ–љ–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є (—А–∞–і—Г–ґ–Ї–Є) –Є–ї–Є –µ–µ –љ–µ–Њ–≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є—П –±—Г–Ї–≤–∞–ї—М–љ–Њ —В—А–Є –і–µ—Б—П—В–Є–ї–µ—В–Є—П —В–Њ–Љ—Г —Б—З–Є—В–∞–ї—Б—П —А–µ–і–Ї–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є –њ–µ—А–µ–і–љ–µ–≥–Њ –Њ—В–і–µ–ї–∞ –≥–ї–∞–Ј–∞. –≠—В–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ –Њ–±—Л—З–љ–Њ —Б–Њ—З–µ—В–∞–ї–Њ—Б—М —Б —Б–Њ—Б—Г–і–Є—Б—В—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є —Б–µ—В—З–∞—В–Ї–Є, –Є –µ–µ –Њ—В–љ–Њ—И–µ–љ–Є–µ –Ї–Њ –≤—В–Њ—А–Є—З–љ–Њ–є –Э–У –±—Л–ї–Њ –љ–µ–њ–Њ–љ—П—В–љ–Њ. –У–µ–Љ–Њ—А—А–∞–≥–Є—З–µ—Б–Ї–∞—П –≥–ї–∞—Г–Ї–Њ–Љ–∞, –љ–∞–±–ї—О–і–∞–µ–Љ–∞—П –њ—А–Є –Њ–Ї–Ї–ї—О–Ј–Є–Є —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є –≤–µ–љ—Л —Б–µ—В—З–∞—В–Ї–Є (–¶–Т–°), —Б—З–Є—В–∞–ї–∞—Б—М –Њ—В–ї–Є—З–љ–Њ–є –Њ—В —А—Г–±–µ–Њ–Ј–љ–Њ–є –≥–ї–∞—Г–Ї–Њ–Љ—Л, –љ–∞–±–ї—О–і–∞–µ–Љ–Њ–є —Г –±–Њ–ї—М–љ—Л—Е –°–Ф. –Т —Б–≤—П–Ј–Є —Б —А–Њ—Б—В–Њ–Љ —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –Њ—А–≥–∞–љ–Є–Ј–Љ–∞, —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –ґ–Є–Ј–љ–Є –љ–∞—Б–µ–ї–µ–љ–Є—П –≤ —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є —А–∞–Ј–≤–Є—В—Л—Е —Б—В—А–∞–љ–∞—Е, –Њ—Б–Њ–±–µ–љ–љ–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф, –Є —Г–ї—Г—З—И–µ–љ–Є–µ–Љ –Ї–∞—З–µ—Б—В–≤–∞ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –љ–µ–Њ-–≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є—П —А–∞–і—Г–ґ–Ї–Є —Б—В–∞–ї–∞ –≤—Л—П–≤–ї—П—В—М—Б—П –≤—Б–µ –±–Њ–ї–µ–µ —З–∞—Б—В–Њ. –° –Њ–њ—А–µ–і–µ–ї–µ–љ–љ–Њ–є –і–Њ–ї–µ–є —Г—Б–ї–Њ–≤–љ–Њ—Б—В–Є –µ–µ –Љ–Њ–ґ–љ–Њ –љ–∞–Ј–≤–∞—В—М –њ–µ—А–µ–і–љ–µ–є –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є–µ–є.
–Т –љ–∞—З–∞–ї—М–љ–Њ–є —Б—В–∞–і–Є–Є —Н—В–Њ–≥–Њ –≤–Є–і–∞ –њ—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –њ—А–Є –±–Є–Њ–Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–Є–Є –≤—Л—П–≤–ї—П—О—В—Б—П —А–∞—Б—И–Є—А–µ–љ–љ—Л–µ –≤–µ—В–≤–Є –Ї–∞–њ–Є–ї–ї—П—А–Њ–≤ –Є —В–Њ–љ–Ї–Є–µ, –±–µ—Б–њ–Њ—А—П–і–Њ—З–љ–Њ –Њ—А–Є–µ–љ—В–Є—А–Њ–≤–∞–љ–љ—Л–µ —Б–Њ—Б—Г–і—Л –љ–∞ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є —А–∞–і—Г–ґ–Ї–Є –њ–Њ –Ј—А–∞—З–Ї–Њ–≤–Њ–Љ—Г –Ї—А–∞—О. –Ъ–∞–Ї –њ–Њ–Ї–∞–Ј–∞–ї–Є –њ–∞—В–Њ–≥–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, —А–Њ—Б—В –љ–Њ–≤–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤ –љ–∞—З–Є–љ–∞–µ—В—Б—П –Є–љ—В—А–∞—Б—В—А–Њ–Љ–∞–ї—М–љ–Њ, –∞ –Ј–∞—В–µ–Љ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ—П–µ—В—Б—П –љ–∞ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В—М —А–∞–і—Г–ґ–Ї–Є.
–Я–Њ –љ–∞—И–Є–Љ –і–∞–љ–љ—Л–Љ, –љ–µ–Њ–≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є—П –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ (80%) —Б–љ–∞—З–∞–ї–∞ –њ–Њ—П–≤–ї—П–µ—В—Б—П –њ–Њ –Ј—А–∞—З–Ї–Њ–≤–Њ–Љ—Г –Ї—А–∞—О —А–∞–і—Г–ґ–Ї–Є. –Т –Њ—Б—В–∞–≤—И–Є—Е—Б—П 20% —Б–ї—Г—З–∞–µ–≤ —А–Њ—Б—В –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—Г–і–Њ–≤ –љ–∞—З–Є–љ–∞–ї—Б—П –Њ—В –£–Я–Ъ –Є —И–µ–ї —Ж–µ–љ—В—А–Њ–±–µ–ґ–љ–Њ –Ї –Ј—А–∞—З–Ї–Њ–≤–Њ–Љ—Г –Ї—А–∞—О. –£ –љ–µ–Ї–Њ—В–Њ—А—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Н—В–Є –Ї—А—Г–њ–љ—Л–µ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Б–Њ—Б—Г–і—Л —П–≤–ї—П–ї–Є—Б—М –Ї–∞–Ї –±—Л –њ—А–Њ–і–Њ–ї–ґ–µ–љ–Є–µ–Љ –Ї—А—Г–њ–љ—Л—Е —Б—В–≤–Њ–ї–Њ–≤ —Б –Ї–Њ–љ—К—О–љ–Ї—В–Є–≤—Л –≥–ї–∞–Ј–љ–Њ–≥–Њ —П–±–ї–Њ–Ї–∞. –•–Њ—В—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –Ї–∞—А—В–Є–љ–∞ —А—Г–±–µ–Њ–Ј–∞ –Њ–і–Є–љ–∞–Ї–Њ–≤–∞ –Ї–∞–Ї –≤ —Б–ї—Г—З–∞–µ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П –≥–ї–∞–Ј, —В–∞–Ї –Є –≤ —Б–ї—Г—З–∞–µ –Њ–Ї–Ї–ї—О–Ј–Є–Є –¶–Т–°, –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞–ї–Њ –љ–∞–ї–Є—З–Є–µ –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–≥–Њ –Є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ–≥–Њ —А—Г–±–µ–Њ–Ј–∞ –≤ –≥–ї–∞–Ј–∞—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф. –Ф–ї—П –љ–Њ–≤–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤ —Е–∞—А–∞–Ї—В–µ—А–љ—Л –љ–∞–ї–Є—З–Є–µ —В–Њ–љ–Ї–Є—Е —Д–µ–љ–µ—Б—В—А–Є—А–Њ–≤–∞–љ–љ—Л—Е —Б—В–µ–љ–Њ–Ї, –≤–∞—А–Є–∞–±–µ–ї—М–љ–Њ—Б—В—М —А–∞–Ј–Љ–µ—А–Њ–≤ –Є –Є–Ј–≤–Є—В–Њ–є —Е–Њ–і. –†–∞—Б–њ—А–Њ—Б—В—А–∞–љ—П—П—Б—М –љ–∞ –њ–µ—А–Є—Д–µ—А–Є—О, –Њ–љ–Є –њ–µ—А–µ—Б–µ–Ї–∞—О—В —Ж–Є–ї–Є–∞—А–љ–Њ–µ —В–µ–ї–Њ –Є —Б–Ї–ї–µ—А–∞–ї—М–љ—Г—О —И–њ–Њ—А—Г, –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В —Б–Њ–±—Б—В–≤–µ–љ–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ —А–∞—Б–њ–Њ–ї–∞–≥–∞—О—В—Б—П –Ї–Ј–∞–і–Є –Њ—В —Б–Ї–ї–µ—А–∞–ї—М–љ–Њ–є —И–њ–Њ—А—Л. –Ъ–Њ–ї–Є—З–µ—Б—В–≤–Њ —В–∞–Ї–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ –љ–∞—И–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б–Њ—Б—В–∞–≤–Є–ї–Њ –Њ–Ї–Њ–ї–Њ 200 —З–µ–ї–Њ–≤–µ–Ї (0,07%), –Є —В–Њ–ї—М–Ї–Њ 81 –Є–Ј –љ–Є—Е (0,03%) –њ–Њ—В—А–µ–±–Њ–≤–∞–ї–Њ—Б—М –≤—Л–њ–Њ–ї–љ–µ–љ–Є–µ –і—А–µ–љ–∞–ґ–љ–Њ–є —Е–Є—А—Г—А–≥–Є–Є.
–Ґ–µ—А–∞–њ–Є—О –Э–У –Љ–Њ–ґ–љ–Њ —Г—Б–ї–Њ–≤–љ–Њ —А–∞–Ј–і–µ–ї–Є—В—М –љ–∞ –Ї–Њ–љ—Б–µ—А–≤–∞—В–Є–≤–љ—Г—О (–Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ—Г—О), –ї–µ—З–µ–љ–Є–µ —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –ї—Г—З–µ–≤–Њ–≥–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –Є —Б–Њ–±—Б—В–≤–µ–љ–љ–Њ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є–µ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ —В–Њ, —З—В–Њ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Є–Љ–µ–µ—В—Б—П –і–Њ—Б—В–∞—В–Њ—З–љ–Њ —И–Є—А–Њ–Ї–Є–є —Б–њ–µ–Ї—В—А –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Љ–µ—Б—В–љ–Њ–≥–Њ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П, –Є—Е —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Є –ї–µ—З–µ–љ–Є–Є –Э–У –љ–µ–≤—Л—Б–Њ–Ї–∞. –Я–Њ–Ї–∞–Ј–∞–љ—Л –≤—Л—Б–Њ–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є –љ–µ—Г—В–µ—И–Є—В–µ–ї—М–љ—Л–є —А–µ–Ј—Г–ї—М—В–∞—В –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–є –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є [4].
–Ф–ї—П –ї–µ—З–µ–љ–Є—П –±–Њ–ї—П—Й–µ–є –Э–У –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –Ї–Њ–љ—В–∞–Ї—В–љ–∞—П —Б –і–Њ–Ј–Є—А–Њ–≤–∞–љ–љ—Л–Љ –≤–і–∞–≤–ї–µ–љ–Є–µ–Љ —Б–Ї–ї–µ—А—Л –Є –±–µ—Б–Ї–Њ–љ—В–∞–Ї—В–љ–∞—П –і–Є–Њ–і–ї–∞–Ј–µ—А–љ–∞—П —В—А–∞–љ—Б—Б–Ї–ї–µ—А–∞–ї—М–љ–∞—П —Ж–Є–Ї–ї–Њ–Ї–Њ–∞–≥—Г–ї—П—Ж–Є—П, –њ—А–Є –Ї–Њ—В–Њ—А–Њ–є, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є–µ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, –∞ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В –љ–µ –≤—Б–µ–≥–і–∞ –њ—А–Њ–≥–љ–Њ–Ј–Є—А—Г–µ–Љ. –Э–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М –Њ–±—Й–µ–њ—А–Є–љ—П—В—Л–Љ —Б–њ–Њ—Б–Њ–±–Њ–Љ –±–ї–Њ–Ї–Є—А–Њ–≤–∞–љ–Є—П –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є—Е –Ј–Њ–љ –Є —Б—В–∞–±–Є–ї–Є–Ј–∞—Ж–Є–Є —Б–Њ—Б—В–Њ—П–љ–Є—П –≥–ї–∞–Ј–∞ –њ—А–Є –Ф–† –≤ —Ж–µ–ї–Њ–Љ –Є –њ—А–Є –Э–У –≤ —З–∞—Б—В–љ–Њ—Б—В–Є –Њ—Б—В–∞–µ—В—Б—П –њ–∞–љ—А–µ—В–Є–љ–∞–ї—М–љ–∞—П –Ы–Ъ–°, –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Ї–Њ—В–Њ—А–Њ–є –±—Л–ї–∞ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–∞ –Ї—А—Г–њ–љ–Њ–Љ–∞—Б—И—В–∞–±–љ—Л–Љ–Є –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Л–Љ–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П–Љ–Є DRS (Diabetic Retinopathy Study, 1972вАУ1976 –≥–≥.) –Є ETDRS (Early Treatment Diabetic Retinopathy Study, 1980вАУ1990 –≥–≥.).
–Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Ї–ї–∞—Б—Б–Є—З–µ—Б–Ї–Є—Е –∞–љ—В–Є–≥–ї–∞—Г–Ї–Њ–Љ–љ—Л—Е –Њ–њ–µ—А–∞—Ж–Є–є (—Б–Є–љ—Г—Б—В—А–∞–±–µ–Ї—Г–ї–Њ—Н–Ї—В–Њ–Љ–Є—П –Є –µ–µ –Љ–Њ–і–Є—Д–Є–Ї–∞—Ж–Є–Є) –њ—А–Є –Э–У –њ–Њ–Ї–∞–Ј–∞–ї–Њ –љ–Є–Ј–Ї—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є–Ј-–Ј–∞ –±—Л—Б—В—А–Њ–є –Њ–±–ї–Є—В–µ—А–∞—Ж–Є–Є –≤–љ–Њ–≤—М —Б–Њ–Ј–і–∞–љ–љ—Л—Е –њ—Г—В–µ–є –Њ—В—В–Њ–Ї–∞ –≤–љ—Г—В—А–Є–≥–ї–∞–Ј–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є. –Ш —В–Њ–ї—М–Ї–Њ –∞–Ї—В–Є–≤–љ–Њ–µ –≤–љ–µ–і—А–µ–љ–Є–µ —Б–Є–ї–Є–Ї–Њ–љ–Њ–≤—Л—Е –і—А–µ–љ–∞–ґ–µ–є –Є –Ї–ї–∞–њ–∞–љ–Њ–≤ (–Р—Е–Љ–µ–і–∞, –Ь–Њ–ї—М—В–µ–љ–Њ –Є –і—А.) –Њ—В–Ї—А—Л–ї–Њ –љ–Њ–≤—Г—О —Б—В—А–∞–љ–Є—Ж—Г –≤ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–Љ –ї–µ—З–µ–љ–Є–Є –≤—В–Њ—А–Є—З–љ–Њ–є –Э–У —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф. –Ю—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –љ–Є–Ј–Ї–Є–є –њ—А–Њ—Ж–µ–љ—В –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, —Г–і–Њ–±–љ–Њ—Б—В—М –њ—А–Є –Є–Љ–њ–ї–∞–љ—В–∞—Ж–Є–Є –Є, —Б–∞–Љ–Њ–µ –≥–ї–∞–≤–љ–Њ–µ, —Б—В–Њ–є–Ї–Є–є –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л–є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В —Б–і–µ–ї–∞–ї–Є –Є—Е –њ—А–Є–≤–ї–µ–Ї–∞—В–µ–ї—М–љ—Л–Љ–Є –і–ї—П —И–Є—А–Њ–Ї–Њ–≥–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –њ—А–Є —Н—В–Њ–є —Б–ї–Њ–ґ–љ–Њ–є –≥–ї–∞–Ј–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є, –њ–ї–Њ—Е–Њ –њ–Њ–і–і–∞—О—Й–µ–є—Б—П –ї–µ—З–µ–љ–Є—О –і—А—Г–≥–Є–Љ–Є –Љ–µ—В–Њ–і–∞–Љ–Є.
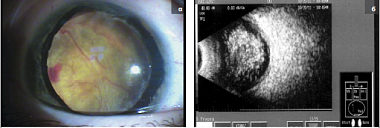
–°–Њ —Б–ї—Г—З–∞–µ–Љ —Б—А–µ–і–љ–µ–є –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є–Є –њ—А–Є –Ф–† [3] –Љ—Л —Б—В–Њ–ї–Ї–љ—Г–ї–Є—Б—М —В–Њ–ї—М–Ї–Њ 2 —А–∞–Ј–∞ (0,007%). –†–Њ—Б—В –љ–Њ–≤–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤ –њ–Њ –Я–У–Ь –°–Ґ, –≤–µ—А–Њ—П—В–љ–Њ, –≤–Њ–Ј–Љ–Њ–ґ–µ–љ –ї–Є—И—М –њ—А–Є —Г—Б–ї–Њ–≤–Є–Є –µ–µ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Є–Ј–Љ–µ–љ–µ–љ–Є—П (—Г–њ–ї–Њ—В–љ–µ–љ–Є—П). –Т –њ–µ—А–≤–Њ–Љ —Б–ї—Г—З–∞–µ –њ—А–Є—З–Є–љ–Њ–є —Д–Є–±—А–Њ–Ј–љ–Њ–є —В—А–∞–љ—Б—Д–Њ—А–Љ–∞—Ж–Є–Є —Б—В–∞–ї —Б—В–∞—А—Л–є, –њ–Њ—З—В–Є —В–Њ—В–∞–ї—М–љ—Л–є –≥–µ–Љ–Њ—Д—В–∞–ї—М–Љ (—А–Є—Б. 1–∞ –Є 1–±), –≤–Њ –≤—В–Њ—А–Њ–Љ вАУ –≤—Л—А–∞–ґ–µ–љ–љ–∞—П –і–Є—Б–ї–Њ–Ї–∞—Ж–Є—П —Б–∞–Љ–Њ–≥–Њ –°–Ґ –≤–њ–µ—А–µ–і –Ї —Е—А—Г—Б—В–∞–ї–Є–Ї—Г, –њ–Њ–ї–љ–∞—П –Њ—В—Б–ї–Њ–є–Ї–∞ –Ч–У–Ь –Є –≥–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ —Г–њ–ї–Њ—В–љ–µ–љ–Є–µ –Њ—Б—В–∞—В–Ї–Њ–≤ —Б—В–µ–Ї–ї–Њ–≤–Є–і–љ—Л—Е –Љ–∞—Б—Б (—А–Є—Б. 2–∞ –Є 2–±).
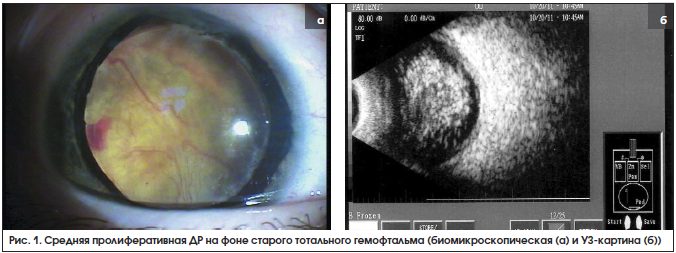

–Я–Њ –≤—Б–µ–є –≤–Є–і–Є–Љ–Њ—Б—В–Є, —В–∞–Ї–Њ–є –њ–ї–Њ—В–љ—Л–є —Б—Г–±—Б—В—А–∞—В, –Ї–∞–Ї –Є–Ј–Љ–µ–љ–µ–љ–љ–∞—П –Я–У–Ь –Љ–Њ–ґ–µ—В —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М—Б—П –Ї–∞–Ї –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–є –Љ–∞—В–µ—А–Є–∞–ї –і–ї—П —А–∞–Ј–≤–Є—В–Є—П —Б—А–µ–і–љ–µ–є –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є–Є. –Я—А–Є —Н—В–Њ–Љ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ —Г –њ–µ—А–≤–Њ–≥–Њ –њ–∞—Ж–Є–µ–љ—В–∞ —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –њ–µ—А–µ–і–љ–µ–є –Є –Ј–∞–і–љ–µ–є –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є–Є –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ –љ–µ –±—Л–ї–Њ, —Г –≤—В–Њ—А–Њ–≥–Њ –±—Л–ї –≤—Л—А–∞–ґ–µ–љ–љ—Л–є —А—Г–±–µ–Њ–Ј —А–∞–і—Г–ґ–Ї–Є –Є –£–Я–Ъ –≥–ї–∞–Ј–∞, –∞ —Б–∞–Љ –њ–∞—Ж–Є–µ–љ—В –±—Л–ї —Г–ґ–µ –њ—А–Њ–Њ–њ–µ—А–Є—А–Њ–≤–∞–љ –њ–Њ –њ–Њ–≤–Њ–і—Г –љ–µ–Ї–Њ–Љ–њ–µ–љ—Б–Є—А–Њ–≤–∞–љ–љ–Њ–є –Э–У —Б –Є–Љ–њ–ї–∞–љ—В–∞—Ж–Є–µ–є –Ї–ї–∞–њ–∞–љ–∞ –Р—Е–Љ–µ–і–∞.
–°—А–µ–і–љ—П—П –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є—П –њ—А–Є –њ—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ–Њ–є –Ф–† –Љ–Њ–ґ–µ—В —Б–Њ—З–µ—В–∞—В—М—Б—П —Б –і—А—Г–≥–Є–Љ–Є –≤–∞—А–Є–∞–љ—В–∞–Љ–Є –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –љ–µ–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –Є–ї–Є –±—Л—В—М —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ—Л–Љ —Б–Є–Љ–њ—В–Њ–Љ–Њ–Љ. –≠—В–Њ –љ–µ –Є—Б–Ї–ї—О—З–∞–µ—В –µ–µ –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є—О –Ї–∞–Ї —В—П–ґ–µ–ї–Њ–µ –њ–Њ—А–∞–ґ–µ–љ–Є–µ –≥–ї–∞–Ј–љ–Њ–≥–Њ —П–±–ї–Њ–Ї–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф –Є —В—А–µ–±—Г–µ—В —Б–Њ–≤–Љ–µ—Б—В–љ—Л—Е —Г—Б–Є–ї–Є–є —Н–љ–і–Њ–Ї—А–Є–љ–Њ–ї–Њ–≥–Њ–≤ –Є –Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥–Њ–≤ –≤ –ї–µ—З–µ–љ–Є–Є. –Р–і–µ–Ї–≤–∞—В–љ–∞—П –Є —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–∞—П –Ї–Њ—А—А–µ–Ї—Ж–Є—П –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—В–∞—В—Г—Б–∞ –≤–Љ–µ—Б—В–µ —Б –њ—А–Њ–≤–µ–і–µ–љ–Є–µ–Љ –≤–Є—В—А–µ–Њ—А–µ—В–Є–љ–∞–ї—М–љ–Њ–є —Е–Є—А—Г—А–≥–Є–Є –Љ–Њ–≥—Г—В —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Г–ї—Г—З—И–Є—В—М –њ—А–Њ–≥–љ–Њ–Ј —Г —Н—В–Њ–є —Б–ї–Њ–ґ–љ–Њ–є –≥—А—Г–њ–њ—Л –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є —Б–љ–Є–Ј–Є—В—М –њ—А–Њ—Ж–µ–љ—В –Є–љ–≤–∞–ї–Є–і–Є–Ј–∞—Ж–Є–Є. –Я—А–Њ–≤–µ–і–µ–љ–Є–µ –Ы–Ъ–° –њ—А–Є —Н—В–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ, –∞ –ї–Њ–Ї–∞–ї—М–љ–Њ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –∞–љ–≥–Є–Њ–≥–µ–љ–µ–Ј–∞ –Њ—Б—В–∞–µ—В—Б—П –њ–Њ–і –≤–Њ–њ—А–Њ—Б–Њ–Љ.
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є—П –њ—А–Є –Ф–† —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф –Љ–Њ–ґ–µ—В –љ–∞–±–ї—О–і–∞—В—М—Б—П –≤–Њ –≤—Б–µ—Е –Њ—В–і–µ–ї–∞—Е –≥–ї–∞–Ј–љ–Њ–≥–Њ —П–±–ї–Њ–Ї–∞. –≠—В–Њ –≥–Њ–≤–Њ—А–Є—В –Њ —В–Њ–Љ, —З—В–Њ –њ—А–Њ—Ж–µ—Б—Б –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –љ–Њ–≤—Л—Е, —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ –љ–µ–њ–Њ–ї–љ–Њ—Ж–µ–љ–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤ –љ–Њ—Б–Є—В –љ–µ –ї–Њ–Ї–∞–ї—М–љ—Л–є, –∞ –≥–µ–љ–µ—А–∞–ї–Є–Ј–Њ–≤–∞–љ–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А, –Є –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –љ–∞ –љ–µ–≥–Њ –і–Њ–ї–ґ–љ–Њ –±—Л—В—М —В–∞–Ї–Є–Љ –ґ–µ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ—Л–Љ. –°–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–Њ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Ы–Ъ–°, –Є–љ—В—А–∞–≤–Є—В—А–µ–∞–ї—М–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –∞–љ–≥–Є–Њ–≥–µ–љ–µ–Ј–∞, –Т–≠, –і—А–µ–љ–∞–ґ–љ–Њ–є —Е–Є—А—Г—А–≥–Є–Є –Є –і—А—Г–≥–Є—Е —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –Љ–µ—В–Њ–і–Њ–≤ –ї–µ—З–µ–љ–Є—П –і–∞–µ—В –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –Є –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Б –Њ–њ—В–Є–Љ–Є–Ј–Љ–Њ–Љ —Б–Љ–Њ—В—А–µ—В—М –≤ –±—Г–і—Г—Й–µ–µ.












