–¶–µ–ї—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П: –Є–Ј—Г—З–µ–љ–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Њ—В–і–∞–ї–µ–љ–љ—Л—Е —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –љ–µ–њ—А–Њ–љ–Є–Ї–∞—О—Й–µ–є —Н–Ї–≤–∞—В–Њ—А–Є–∞–ї—М–љ–Њ–є —Б–Ї–ї–µ—А–Њ—В–Њ–Љ–Є–Є.
–Ь–∞—В–µ—А–Є–∞–ї—Л –Є –Љ–µ—В–Њ–і—Л: –њ–∞—Ж–Є–µ–љ—В—Л —Б —В–µ—А–Љ–Є–љ–∞–ї—М–љ–Њ–є –±–Њ–ї—П—Й–µ–є –≥–ї–∞—Г–Ї–Њ–Љ–Њ–є –±—Л–ї–Є –њ–Њ–і–µ–ї–µ–љ—Л –љ–∞ –і–≤–µ –≥—А—Г–њ–њ—Л. –Т 1––є –≥—А—Г–њ–њ–µ –≤—Л–њ–Њ–ї–љ–µ–љ–∞ –љ–µ–њ—А–Њ–љ–Є–Ї–∞—О—Й–∞—П —Н–Ї–≤–∞—В–Њ—А–Є–∞–ї—М–љ–∞—П —Б–Ї–ї–µ—А–Њ—В–Њ–Љ–Є—П, –≤–Њ 2––є – —В—А–∞–љ—Б—Б–Ї–ї–µ—А–∞–ї—М–љ–∞—П –і–Є–Њ–і–ї–∞–Ј–µ—А–љ–∞—П —Ж–Є–Ї–ї–Њ—Д–Њ—В–Њ–Ї–Њ–∞–≥—Г–ї—П—Ж–Є—П. –Т—Б–µ–Љ –њ–∞—Ж–Є–µ–љ—В–∞–Љ –і–Њ –Є –њ–Њ—Б–ї–µ –Њ–њ–µ—А–∞—Ж–Є–Є –±—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ —Б—В–∞–љ–і–∞—А—В–љ–Њ–µ –Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ. –Я–∞—Ж–Є–µ–љ—В—Л –њ–Њ–ї—Г—З–∞–ї–Є –љ–µ –Љ–µ–љ–µ–µ 1 –≥–Њ–і–∞ –Є–љ—Б—В–Є–ї–ї—П—Ж–Є–Є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л—Е –Ї–∞–њ–µ–ї—М (–≤ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–Љ —А–µ–ґ–Є–Љ–µ) –і–Њ –Є –њ–Њ—Б–ї–µ –Њ–њ–µ—А–∞—Ж–Є–Є: –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ –±–ї–Њ–Ї–∞—В–Њ—А—Л β1–, β2––∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –Є –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Ї–∞—А–±–Њ–∞–љ–≥–Є–і—А–∞–Ј—Л.
–†–µ–Ј—Г–ї—М—В–∞—В—Л: –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±—Л–ї–Є –≤–Ї–ї—О—З–µ–љ—Л 85 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —В–µ—А–Љ–Є–љ–∞–ї—М–љ–Њ–є –±–Њ–ї—П—Й–µ–є –≥–ї–∞—Г–Ї–Њ–Љ–Њ–є, –Ї–Њ—В–Њ—А—Л—Е —А–∞–Ј–і–µ–ї–Є–ї–Є –љ–∞ –і–≤–µ –≥—А—Г–њ–њ—Л: –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є – 61 –њ–∞—Ж–Є–µ–љ—В, —Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В – 64,1±1,6 –≥–Њ–і–∞; –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є – 24 –њ–∞—Ж–Є–µ–љ—В–∞, —Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В – 66,0±1,6 –≥–Њ–і–∞. –Я–Њ—Б–ї–µ –њ—А–Њ–≤–µ–і–µ–љ–Є—П –љ–µ–њ—А–Њ–љ–Є–Ї–∞—О—Й–µ–є —Н–Ї–≤–∞—В–Њ—А–Є–∞–ї—М–љ–Њ–є —Б–Ї–ї–µ—А–Њ—В–Њ–Љ–Є–Є –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л–є –њ–µ—А–Є–Њ–і –њ—А–Њ—В–µ–Ї–∞–ї –ї–µ–≥—З–µ —Б –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ–Љ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е —Б—А–µ–і—Б—В–≤ —В–Њ–ї—М–Ї–Њ –≤ –≤–Є–і–µ –Є–љ—Б—В–Є–ї–ї—П—Ж–Є–є. –Т –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ —В—А–µ–±–Њ–≤–∞–ї–∞—Б—М –Љ–∞—Б—Б–Є–≤–љ–∞—П –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–∞—П —В–µ—А–∞–њ–Є—П –≤ –≤–Є–і–µ –Љ–µ—Б—В–љ—Л—Е –Є –Њ–±—Й–Є—Е –Є–љ—К–µ–Ї—Ж–Є–є. –Т —А–∞–љ–љ–µ–Љ –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ –≤–љ—Г—В—А–Є–≥–ї–∞–Ј–љ–Њ–µ –і–∞–≤–ї–µ–љ–Є–µ —Б–љ–Є–ґ–∞–ї–Њ—Б—М –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –љ–∞ 7–8 –Љ–Љ —А—В. —Б—В. (–љ–µ –±–Њ–ї–µ–µ 15% –Њ—В –Є—Б—Е–Њ–і–љ–Њ–≥–Њ –Ј–љ–∞—З–µ–љ–Є—П).
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ: –љ–µ–њ—А–Њ–љ–Є–Ї–∞—О—Й–∞—П —Н–Ї–≤–∞—В–Њ—А–Є–∞–ї—М–љ–∞—П —Б–Ї–ї–µ—А–Њ—В–Њ–Љ–Є—П —П–≤–ї—П–µ—В—Б—П —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ –ї–µ—З–µ–љ–Є—П —В–µ—А–Љ–Є–љ–∞–ї—М–љ–Њ–є –±–Њ–ї—П—Й–µ–є –≥–ї–∞—Г–Ї–Њ–Љ—Л, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–Є–Љ –Ї—Г–њ–Є—А–Њ–≤–∞—В—М –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ –Є —Б–љ–Є–ґ–∞—В—М –≤–љ—Г—В—А–Є–≥–ї–∞–Ј–љ–Њ–µ –і–∞–≤–ї–µ–љ–Є–µ.
–Ъ–ї—О—З–µ–≤—Л–µ —Б–ї–Њ–≤–∞: –љ–µ–њ—А–Њ–љ–Є–Ї–∞—О—Й–∞—П —Н–Ї–≤–∞—В–Њ—А–Є–∞–ї—М–љ–∞—П —Б–Ї–ї–µ—А–Њ—В–Њ–Љ–Є—П, —В—А–∞–љ—Б—Б–Ї–ї–µ—А–∞–ї—М–љ–∞—П –і–Є–Њ–і–ї–∞–Ј–µ—А–љ–∞—П —Ж–Є–Ї–ї–Њ—Д–Њ—В–Њ–Ї–Њ–∞–≥—Г–ї—П—Ж–Є—П, —В–µ—А–Љ–Є–љ–∞–ї—М–љ–∞—П –±–Њ–ї—П—Й–∞—П –≥–ї–∞—Г–Ї–Њ–Љ–∞.
Abstract
Remote results of nonpenetrating equatorial sclerotomy
A.E. Sineok, A.V. Zolotarev,
E.V. Karlova, E.S. Milyudin
Samara State scientific medical university
Samara clinical ophthlmological hospital named after Eroshevskii T.I., Samara
Purpose: to study remote results of nonpenetrating equatorial sclerotomy.
Materials and methods: patients with terminal aching glaucoma were divided into 2 groups – in first nonpenetrating equatorial sclerectomy (NES) was performed, in second – transscleral diod laser cyclophotocoagulation (TDLC). In all patients standard ophthalmologic examination was carried out before and after surgery. They were prescribed local hypotensive treatment (beta–blockers, carboanhydrase inhibitors) for a year in postoperative surgery.
Results: 85 patients were included, first group consisted of 61, second – of 24 patients, average age 64,1±1,6 and 66,0±1.6 years accordingly. In first group in postoperative period only local anti–inflammatory treatment was needed, in the second – local and systemic drugs were prescribed because of developed postoperative pain syndrome. In both groups IOP reduction was not more than 15% from baseline.
Conclusion: NES is an efficient surgical method allowing reduction of IOP level and minimizing of postoperative pain syndrome and inflammation.
Keywords: nonpenetrating equatorial sclerectomy, transscleral diod laser cyclophotocoagulation, terminal aching glaucoma.
–Р–Ї—В—Г–∞–ї—М–љ–Њ—Б—В—М
–Т –Њ—Б–љ–Њ–≤–µ —А–∞–Ј–≤–Є—В–Є—П –Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –Њ—В–Ї—А—Л—В–Њ—Г–≥–Њ–ї—М–љ–Њ–є –≥–ї–∞—Г–Ї–Њ–Љ—Л –ї–µ–ґ–∞—В –Є–Ј–Љ–µ–љ–µ–љ–Є—П –±–Є–Њ–Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Є—Е —Б–≤–Њ–є—Б—В–≤ –≥–ї–∞–Ј–љ–Њ–≥–Њ —П–±–ї–Њ–Ї–∞, —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—Й–Є–µ—Б—П —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ —А–Є–≥–Є–і–љ–Њ—Б—В–Є –Є–ї–Є –ґ–µ—Б—В–Ї–Њ—Б—В–Є –Њ–±–Њ–ї–Њ—З–µ–Ї –≥–ї–∞–Ј–љ–Њ–≥–Њ —П–±–ї–Њ–Ї–∞ [7–10, 13,14]. –≠—В–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Њ–±—К—П—Б–љ—П—О—В—Б—П –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—П–Љ–Є —Б—В—А–Њ–µ–љ–Є—П —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є —Б–Ї–ї–µ—А—Л –њ—А–Є –≥–ї–∞—Г–Ї–Њ–Љ–µ, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–Ї–∞–Ј–∞–ї–Є –љ–∞—А–∞—Б—В–∞—О—Й—Г—О –і–µ–Ј–Њ—А–≥–∞–љ–Є–Ј–∞—Ж–Є—О –µ–µ –≤–Њ–ї–Њ–Ї–Њ–љ [5]. –Я–Њ–≤—Л—И–µ–љ–Є–µ —А–Є–≥–Є–і–љ–Њ—Б—В–Є –≥–ї–∞–Ј–љ–Њ–≥–Њ —П–±–ї–Њ–Ї–∞ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В –Њ—Д—В–∞–ї—М–Љ–Њ—В–Њ–љ—Г—Б, —Г–Љ–µ–љ—М—И–∞–µ—В –Љ–Є–Ї—А–Њ—Д–ї—Г–Ї—В—Г–∞—Ж–Є–Є –Њ–±—К–µ–Љ–∞ –≥–ї–∞–Ј–љ–Њ–≥–Њ —П–±–ї–Њ–Ї–∞, —З—В–Њ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –љ–∞—А—Г—И–µ–љ–Є—О –Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є–Є –≤–љ—Г—В—А–Є–≥–ї–∞–Ј–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П (–Т–У–Ф) –Є —Б–љ–Є–ґ–∞–µ—В –Њ–±—К–µ–Љ–љ—Л–є –њ—Г–ї—М—Б–Њ–≤–Њ–є –Ї—А–Њ–≤–Њ—В–Њ–Ї –≤ –≥–ї–∞–Ј—Г [9,15]. –¶–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ—Л–Љ –Є –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–љ—Л–Љ –љ–∞–њ—А–∞–≤–ї–µ–љ–Є–µ–Љ –≤ –ї–µ—З–µ–љ–Є–Є –Њ—В–Ї—А—Л—В–Њ—Г–≥–Њ–ї—М–љ–Њ–є –≥–ї–∞—Г–Ї–Њ–Љ—Л —П–≤–ї—П–µ—В—Б—П –Ї–Њ—А—А–µ–Ї—Ж–Є—П –±–Є–Њ–Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Є—Е —Б–≤–Њ–є—Б—В–≤ –≥–ї–∞–Ј–љ–Њ–≥–Њ —П–±–ї–Њ–Ї–∞ [1–3,7,11,14,17]. –Э–∞–Љ–Є –њ—А–µ–і–ї–Њ–ґ–µ–љ–∞ —Н–Ї–≤–∞—В–Њ—А–Є–∞–ї—М–љ–∞—П —Б–Ї–ї–µ—А–Њ—В–Њ–Љ–Є—П, –Ї–Њ—В–Њ—А–∞—П –≤—Л–њ–Њ–ї–љ—П–ї–∞—Б—М —Б —Ж–µ–ї—М—О –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, —Б–љ–Є–ґ–µ–љ–Є—П –Т–У–Ф –Є —Б–Њ—Е—А–∞–љ–µ–љ–Є—П –≥–ї–∞–Ј–љ–Њ–≥–Њ —П–±–ї–Њ–Ї–∞ –њ—А–Є —В–µ—А–Љ–Є–љ–∞–ї—М–љ–Њ–є –±–Њ–ї—П—Й–µ–є –≥–ї–∞—Г–Ї–Њ–Љ–µ [11]. –Я—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П –∞–Ї—В—Г–∞–ї—М–љ—Л–Љ –Њ—Ж–µ–љ–Є—В—М –Њ—В–і–∞–ї–µ–љ–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ—А–µ–і–ї–Њ–ґ–µ–љ–љ–Њ–є –Њ–њ–µ—А–∞—Ж–Є–Є –њ—А–Є —В–µ—А–Љ–Є–љ–∞–ї—М–љ–Њ–є –≥–ї–∞—Г–Ї–Њ–Љ–µ.
–¶–µ–ї—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П: –Є–Ј—Г—З–µ–љ–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Њ—В–і–∞–ї–µ–љ–љ—Л—Е —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –љ–µ–њ—А–Њ–љ–Є–Ї–∞—О—Й–µ–є —Н–Ї–≤–∞—В–Њ—А–Є–∞–ї—М–љ–Њ–є —Б–Ї–ї–µ—А–Њ—В–Њ–Љ–Є–Є.
–Ь–∞—В–µ—А–Є–∞–ї—Л –Є –Љ–µ—В–Њ–і—Л
–Я–Њ–і –љ–∞–±–ї—О–і–µ–љ–Є–µ–Љ –љ–∞—Е–Њ–і–Є–ї–Њ—Б—М 85 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —В–µ—А–Љ–Є–љ–∞–ї—М–љ–Њ–є –±–Њ–ї—П—Й–µ–є –≥–ї–∞—Г–Ї–Њ–Љ–Њ–є. –Я–∞—Ж–Є–µ–љ—В—Л –њ–Њ–і–µ–ї–µ–љ—Л –љ–∞ –і–≤–µ –≥—А—Г–њ–њ—Л, —Г 61 –≤—Л–њ–Њ–ї–љ–µ–љ–∞ –љ–µ–њ—А–Њ–љ–Є–Ї–∞—О—Й–∞—П —Н–Ї–≤–∞—В–Њ—А–Є–∞–ї—М–љ–∞—П —Б–Ї–ї–µ—А–Њ—В–Њ–Љ–Є—П, —Г 24 – —В—А–∞–љ—Б—Б–Ї–ї–µ—А–∞–ї—М–љ–∞—П –і–Є–Њ–і–ї–∞–Ј–µ—А–љ–∞—П —Ж–Є–Ї–ї–Њ—Д–Њ—В–Њ–Ї–Њ–∞–≥—Г–ї—П—Ж–Є—П. –Ъ—А–Є—В–µ—А–Є—П–Љ–Є –Њ—В–±–Њ—А–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б–ї—Г–ґ–Є–ї–∞ –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М —В–µ—З–µ–љ–Є—П –≥–ї–∞—Г–Ї–Њ–Љ—Л –±–Њ–ї–µ–µ 5 –ї–µ—В, –Њ—В—Б—Г—В—Б—В–≤–Є–µ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є —Д–Є–±—А–Њ–Ј–љ–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є, —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤ –љ–∞ —А–Њ–≥–Њ–≤–Є—Ж–µ –Є —Б–Ї–ї–µ—А–µ. –°—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ—Л —Б–Њ—Б—В–∞–≤–Є–ї 64,1±1,6 –≥–Њ–і–∞, –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л – 66,0±1,6 –≥–Њ–і–∞. –Т—Б–µ–Љ –њ–∞—Ж–Є–µ–љ—В–∞–Љ –і–Њ –Є –њ–Њ—Б–ї–µ –Њ–њ–µ—А–∞—Ж–Є–Є –±—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ —Б—В–∞–љ–і–∞—А—В–љ–Њ–µ –Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ. –Я–∞—Ж–Є–µ–љ—В—Л –њ–Њ–ї—Г—З–∞–ї–Є –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л–є —А–µ–ґ–Є–Љ –Є–љ—Б—В–Є–ї–ї—П—Ж–Є–є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л—Е –Ї–∞–њ–µ–ї—М –і–Њ –Є –њ–Њ—Б–ї–µ –Њ–њ–µ—А–∞—Ж–Є–Є –≤ –≤–Є–і–µ –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е –±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤ β1–, β2––∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –Є –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Ї–∞—А–±–Њ–∞–љ–≥–Є–і—А–∞–Ј—Л –љ–µ –Љ–µ–љ–µ–µ 1 –≥–Њ–і–∞.
–Э–µ–њ—А–Њ–љ–Є–Ї–∞—О—Й–∞—П —Н–Ї–≤–∞—В–Њ—А–Є–∞–ї—М–љ–∞—П —Б–Ї–ї–µ—А–Њ—В–Њ–Љ–Є—П –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М –њ–Њ–і —Н–њ–Є–±—Г–ї—М–±–∞—А–љ–Њ–є –∞–љ–µ—Б—В–µ–Ј–Є–µ–є –њ—А–Њ–Ї—Б–Є–Љ–µ—В–∞–Ї–∞–Є–љ–∞ 0,5% –Є –Ј–∞–Ї–ї—О—З–∞–ї–∞—Б—М –≤ –љ–∞–љ–µ—Б–µ–љ–Є–Є —З–µ—В—Л—А–µ—Е –ї–Є–љ–µ–є–љ—Л—Е –љ–∞–і—А–µ–Ј–Њ–≤ –і–ї–Є–љ–Њ–є –і–Њ 7 –Љ–Љ –љ–∞ 2/3 –≥–ї—Г–±–Є–љ—Л —Б–Ї–ї–µ—А—Л, –Љ–µ–ґ–і—Г –њ—А—П–Љ—Л–Љ–Є –Љ—Л—И—Ж–∞–Љ–Є –≤ 10–12 –Љ–Љ –Њ—В –ї–Є–Љ–±–∞, –Њ—А–Є–µ–љ—В–Є—А–Њ–≤–∞–љ–љ—Л—Е —Н–Ї–≤–∞—В–Њ—А–Є–∞–ї—М–љ–Њ. –Э–∞ –і–∞–љ–љ—Л–є —Б–њ–Њ—Б–Њ–± –ї–µ—З–µ–љ–Є—П –≥–ї–∞—Г–Ї–Њ–Љ—Л –њ–Њ–ї—Г—З–µ–љ–∞ –њ—А–Є–Њ—А–Є—В–µ—В–љ–∞—П —Б–њ—А–∞–≤–Ї–∞ вДЦ 2011117279/14(025757) –Њ—В 27.04.2011.
–Я–∞—Ж–Є–µ–љ—В—Л –љ–∞–±–ї—О–і–∞–ї–Є—Б—М –≤ —В–µ—З–µ–љ–Є–µ 12 –Љ–µ—Б. –њ–Њ—Б–ї–µ –Њ–њ–µ—А–∞—Ж–Є–Є. –Р–љ–∞–ї–Є–Ј —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –њ—А–Њ–≤–µ–і–µ–љ –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –і–∞–љ–љ—Л—Е –Њ–њ—А–Њ—Б–∞ –Њ —Б—В–µ–њ–µ–љ–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ (–≤ –±–∞–ї–ї–∞—Е) [4], –≤–љ—Г—В—А–Є–≥–ї–∞–Ј–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П (–њ–Њ –Ь–∞–Ї–ї–∞–Ї–Њ–≤—Г 10 –≥), —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–є –±–Є–Њ–Љ–µ—В—А–Є–Є –≥–ї—Г–±–Є–љ—Л –њ–µ—А–µ–і–љ–µ–є –Ї–∞–Љ–µ—А—Л, –Є–Ј–Љ–µ—А–µ–љ–Є—П –≥–ї—Г–±–Є–љ—Л, –Њ–±—К–µ–Љ–∞ –Є —Г–≥–ї–∞ –њ–µ—А–µ–і–љ–µ–є –Ї–∞–Љ–µ—А—Л —Б –њ–Њ–Љ–Њ—Й—М—О –∞–њ–њ–∞—А–∞—В–∞ Pentacam.
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Є –Њ–±—Б—Г–ґ–і–µ–љ–Є–µ
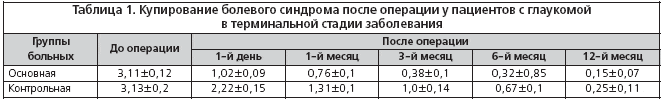
–Я–Њ—Б–ї–µ –њ—А–Њ–≤–µ–і–µ–љ–Є—П –љ–µ–њ—А–Њ–љ–Є–Ї–∞—О—Й–µ–є —Н–Ї–≤–∞—В–Њ—А–Є–∞–ї—М–љ–Њ–є —Б–Ї–ї–µ—А–Њ—В–Њ–Љ–Є–Є –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л–є –њ–µ—А–Є–Њ–і –њ—А–Њ—В–µ–Ї–∞–ї –ї–µ–≥—З–µ —Б –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ–Љ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е —Б—А–µ–і—Б—В–≤ (—В–Њ–ї—М–Ї–Њ –≤ –≤–Є–і–µ –Є–љ—Б—В–Є–ї–ї—П—Ж–Є–є). –Т –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ —В—А–µ–±–Њ–≤–∞–ї–∞—Б—М –Љ–∞—Б—Б–Є–≤–љ–∞—П –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–∞—П —В–µ—А–∞–њ–Є—П –≤ –≤–Є–і–µ –Љ–µ—Б—В–љ—Л—Е –Є –Њ–±—Й–Є—Е –Є–љ—К–µ–Ї—Ж–Є–є. –Т —В–∞–±–ї–Є—Ж–µ 1 –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л —А–µ–Ј—Г–ї—М—В–∞—В—Л –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞.
–Я–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Б—В–µ–њ–µ–љ—М –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –њ–Њ—Б–ї–µ –љ–µ–њ—А–Њ–љ–Є–Ї–∞—О—Й–µ–є —Н–Ї–≤–∞—В–Њ—А–Є–∞–ї—М–љ–Њ–є —Б–Ї–ї–µ—А–Њ—В–Њ–Љ–Є–Є –љ–Є–ґ–µ, —З–µ–Љ –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ. –Э–∞ —Б–ї–µ–і—Г—О—Й–Є–є –і–µ–љ—М –њ–Њ—Б–ї–µ –Њ–њ–µ—А–∞—Ж–Є–Є –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ —Б–љ–Є–Ј–Є–ї—Б—П —Г 93,4% –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б 76,6% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ. –Я–Њ–ї–љ–Њ–µ –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є–µ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –≤ –Ї–Њ–љ—Ж–µ —Б—А–Њ–Ї–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П –њ—А–Є –≤—Л–њ–Њ–ї–љ–µ–љ–Є–Є –љ–µ–њ—А–Њ–љ–Є–Ї–∞—О—Й–µ–є —Н–Ї–≤–∞—В–Њ—А–Є–∞–ї—М–љ–Њ–є —Б–Ї–ї–µ—А–Њ—В–Њ–Љ–Є–Є –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М –≤ 62,1% —Б–ї—Г—З–∞–µ–≤ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б 33,3% –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ. –Т —В–∞–±–ї–Є—Ж–µ 2 –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –і–∞–љ–љ—Л–µ –Є–Ј–Љ–µ—А–µ–љ–Є—П –Т–У–Ф.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –≤ —А–∞–љ–љ–µ–Љ –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ –Т–У–Ф —Б–љ–Є–ґ–∞–ї–Њ—Б—М –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –љ–∞ 7–8 –Љ–Љ —А—В. —Б—В. (–љ–µ –±–Њ–ї–µ–µ 15% –Њ—В –Є—Б—Е–Њ–і–љ–Њ–≥–Њ –Ј–љ–∞—З–µ–љ–Є—П). –°–љ–Є–ґ–µ–љ–Є–µ –Т–У–Ф –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –Ї –Ї–Њ–љ—Ж—Г —Б—А–Њ–Ї–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П –±—Л–ї–Њ –≤ 79,3% —Б–ї—Г—З–∞–µ–≤ –љ–∞ 4,9±1,8 –Љ–Љ —А—В. —Б—В. (–љ–µ –±–Њ–ї–µ–µ 10% –Њ—В –Є—Б—Е–Њ–і–љ–Њ–є –≤–µ–ї–Є—З–Є–љ—Л), –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ – –≤ 73,3% —Б–ї—Г—З–∞–µ–≤ –љ–∞ 13,5±2,4 –Љ–Љ —А—В. —Б—В. (–љ–µ –±–Њ–ї–µ–µ 15–31% –Њ—В –Є—Б—Е–Њ–і–љ–Њ–є –≤–µ–ї–Є—З–Є–љ—Л). –Т —В–∞–±–ї–Є—Ж–µ 3 –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л —А–µ–Ј—Г–ї—М—В–∞—В—Л –Є–Ј–Љ–µ—А–µ–љ–Є—П –≥–ї—Г–±–Є–љ—Л –њ–µ—А–µ–і–љ–µ–є –Ї–∞–Љ–µ—А—Л —Б –њ–Њ–Љ–Њ—Й—М—О —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–є –±–Є–Њ–Љ–µ—В—А–Є–Є.
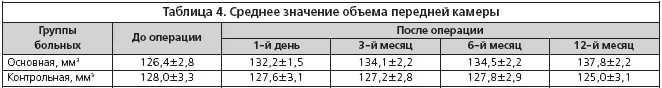
–£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ—Л –≥–ї—Г–±–Є–љ–∞ –њ–µ—А–µ–і–љ–µ–є –Ї–∞–Љ–µ—А—Л –Ї –Ї–Њ–љ—Ж—Г —Б—А–Њ–Ї–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П –±—Л–ї–∞ –±–Њ–ї—М—И–µ, —З–µ–Љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л (t=2,9; p<0,05). –Т —В–∞–±–ї–Є—Ж–µ 4 –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –і–∞–љ–љ—Л–µ –Є–Ј–Љ–µ—А–µ–љ–Є—П –Њ–±—К–µ–Љ–∞ –њ–µ—А–µ–і–љ–µ–є –Ї–∞–Љ–µ—А—Л, –≤—Л–њ–Њ–ї–љ–µ–љ–љ—Л–µ —Б –њ–Њ–Љ–Њ—Й—М—О –∞–њ–њ–∞—А–∞—В–∞ Pentacam (Allegro Oculyser).
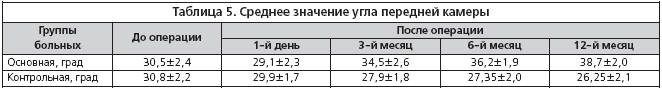
–Ю–±—К–µ–Љ –њ–µ—А–µ–і–љ–µ–є –Ї–∞–Љ–µ—А—Л –Ї –Ї–Њ–љ—Ж—Г —Б—А–Њ–Ї–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ –±—Л–ї –±–Њ–ї—М—И–µ, —З–µ–Љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є (t=2,3; p<0,05). –Т —В–∞–±–ї–Є—Ж–µ 5 –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –і–∞–љ–љ—Л–µ –Є–Ј–Љ–µ—А–µ–љ–Є—П —Г–≥–ї–∞ –њ–µ—А–µ–і–љ–µ–є –Ї–∞–Љ–µ—А—Л, –≤—Л–њ–Њ–ї–љ–µ–љ–љ—Л–µ —Б –њ–Њ–Љ–Њ—Й—М—О –∞–њ–њ–∞—А–∞—В–∞ Pentacam (Allegro Oculyser).
–Т–µ–ї–Є—З–Є–љ–∞ —Г–≥–ї–∞ –њ–µ—А–µ–і–љ–µ–є –Ї–∞–Љ–µ—А—Л –Ї –Ї–Њ–љ—Ж—Г —Б—А–Њ–Ї–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –±—Л–ї–∞ –±–Њ–ї—М—И–µ, —З–µ–Љ –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є (t=3,4; p<0,05).
–Т—Л–≤–Њ–і—Л
–У–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В –Њ–њ–µ—А–∞—Ж–Є–Є –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —А–Є–≥–Є–і–љ–Њ—Б—В–Є –≥–ї–∞–Ј–љ–Њ–≥–Њ —П–±–ї–Њ–Ї–∞, –Ї–Њ—В–Њ—А–Њ–µ –≤–ї–µ—З–µ—В –Ј–∞ —Б–Њ–±–Њ–є —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –≥–ї—Г–±–Є–љ—Л, –Њ–±—К–µ–Љ–∞ –Є —Г–≥–ї–∞ –њ–µ—А–µ–і–љ–µ–є –Ї–∞–Љ–µ—А—Л.
–Э–µ–њ—А–Њ–љ–Є–Ї–∞—О—Й–∞—П —Н–Ї–≤–∞—В–Њ—А–Є–∞–ї—М–љ–∞—П —Б–Ї–ї–µ—А–Њ—В–Њ–Љ–Є—П —П–≤–ї—П–µ—В—Б—П –±–Њ–ї–µ–µ —Й–∞–і—П—Й–Є–Љ —Б–њ–Њ—Б–Њ–±–Њ–Љ –ї–µ—З–µ–љ–Є—П –і–∞–љ–љ–Њ–є –Ї–∞—В–µ–≥–Њ—А–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —В–∞–Ї –Ї–∞–Ї –љ–µ —В—А–µ–±—Г–µ—В –њ—А–Њ–≤–µ–і–µ–љ–Є—П —А–µ—В—А–Њ–±—Г–ї—М–±–∞—А–љ–Њ–є –∞–љ–µ—Б—В–µ–Ј–Є–Є –Є –Њ–±—Й–µ–є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –≤ –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ –ї–µ—З–µ–љ–Є—П —В–µ—А–Љ–Є–љ–∞–ї—М–љ–Њ–є –±–Њ–ї—П—Й–µ–є –≥–ї–∞—Г–Ї–Њ–Љ—Л —П–≤–ї—П–µ—В—Б—П –љ–µ–њ—А–Њ–љ–Є–Ї–∞—О—Й–∞—П —Н–Ї–≤–∞—В–Њ—А–Є–∞–ї—М–љ–∞—П —Б–Ї–ї–µ—А–Њ—В–Њ–Љ–Є—П, –Ї–Њ—В–Њ—А–∞—П –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Ї—Г–њ–Є—А–Њ–≤–∞—В—М –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ –Є —Б–љ–Є–ґ–∞—В—М –Т–У–Ф.


–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –С–Њ—А–Є—Б–Њ–≤–∞ –Э.–Р. –°—Г–±–Љ—Г—Б–Ї—Г–ї—П—А–љ–∞—П –і–µ–Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Њ–љ–љ–∞—П –Љ—Г–ї—М—В–Є—Б–Ї–ї–µ—А—Н–Ї—В–Њ–Љ–Є—П –Ї–∞–Ї –Љ–µ—В–Њ–і –ї–µ—З–µ–љ–Є—П –љ–µ–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л—Е –≥–ї–∞—Г–Ї–Њ–Љ: –Р–≤—В–Њ—А–µ—Д. –і–Є—Б. ... –Ї–∞–љ–і. –Љ–µ–і. –љ–∞—Г–Ї. –Ь., 1999. 20 —Б.
2. –У–Њ–љ—З–∞—А –Я.–Р., –Ф—Г—И–Є–љ –Э.–Т., –§—А–Њ–ї–Њ–≤ –Ь.–Р. –Є –і—А. –Т–ї–Є—П–љ–Є–µ —Б—Г–њ—А–∞—Ж–Є–ї–Є–∞—А–љ—Л—Е –љ–∞–і—А–µ–Ј–Њ–≤ –љ–∞ –≥–Є–і—А–Њ–і–Є–љ–∞–Љ–Є–Ї—Г –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е –≥–ї–∞–Ј // 4–—П –Т—Б–µ—А–Њ—Б—Б. —И–Ї–Њ–ї–∞ –Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥–Њ–≤: –°–±. –љ–∞—Г—З. —В—А—Г–і. –Ь., 2005. –°. 75–82.
3. –У—Г–ї—П–µ–≤ –Ь.–Т., –Ш–≤–∞—И–Є–љ–∞ –Р.–Ш., –Ъ–Њ—А—И—Г–љ–Њ–≤–∞ –Э.–Ъ. –Ь–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ–∞—П –Ј–∞–і–љ—П—П —В—А–µ–њ–∞–љ–∞—Ж–Є—П —Б–Ї–ї–µ—А—Л –≤ –ї–µ—З–µ–љ–Є–Є —В–µ—А–Љ–Є–љ–∞–ї—М–љ–Њ–є –±–Њ–ї—П—Й–µ–є –≥–ї–∞—Г–Ї–Њ–Љ—Л // –°–±. –Љ–∞—В–µ—А–Є–∞–ї–Њ–≤ –Ї–Њ–љ—Д–µ—А–µ–љ—Ж–Є–є. –Ь., 2010. –°. 260–263.
4. –Х–≥–Њ—А–Њ–≤ –Т.–Т., –°–Њ—А–Њ–Ї–Є–љ –Х.–Ы., –Ь–∞—А—З–µ–љ–Ї–Њ –Р.–Э., –С–∞—З–∞–ї–і–Є–љ –Ш.–Ы. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —В—А–∞–љ—Б—Б–Ї–ї–µ—А–∞–ї—М–љ–Њ–є –і–Є–Њ–і–ї–∞–Ј–µ—А–Ї–Њ–∞–≥—Г–ї—П—Ж–Є–Є —Ж–Є–ї–Є–∞—А–љ–Њ–≥–Њ —В–µ–ї–∞ –≤ –ї–µ—З–µ–љ–Є–Є —В–µ—А–Љ–Є–љ–∞–ї—М–љ–Њ–є –±–Њ–ї—П—Й–µ–є –≥–ї–∞—Г–Ї–Њ–Љ—Л // –У–ї–∞—Г–Ї–Њ–Љ–∞. 2009. вДЦ 2. –°. 33–36.
5. –Ч–∞—В—Г–ї–Є–љ–∞ –Э.–Ш., –Я–∞–љ–Њ—А–Љ–Њ–≤–∞ –Э.–Т., –°–µ–љ–љ–Њ–≤–∞ –Ы.–У. –Ъ–Њ–љ—Ж–µ–њ—Ж–Є—П –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ –њ–µ—А–≤–Є—З–љ–Њ–є –Њ—В–Ї—А—Л—В–Њ—Г–≥–Њ–ї—М–љ–Њ–є –≥–ї–∞—Г–Ї–Њ–Љ—Л // 7––є –°—К–µ–Ј–і –Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥–Њ–≤ –†–Њ—Б—Б–Є–Є: –Ґ–µ–Ј. –і–Њ–Ї–ї. –Ь., 2000. –C. 131.
6. –Ч–Њ–ї–Њ—В–∞—А–µ–≤ –Р.–Т. –Ь–Є–Ї—А–Њ—Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–∞—П –∞–љ–∞—В–Њ–Љ–Є—П –і—А–µ–љ–∞–ґ–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л –≥–ї–∞–Ј–∞. –°–∞–Љ–∞—А–∞, 2009. 73 —Б.
7. –Ш–Њ–Љ–і–Є–љ–∞ –Х.–Э. –С–Є–Њ–Љ–µ—Е–∞–љ–Є–Ї–∞ —Б–Ї–ї–µ—А–∞–ї—М–љ–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –≥–ї–∞–Ј–∞ –њ—А–Є –Љ–Є–Њ–њ–Є–Є: –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –љ–∞—А—Г—И–µ–љ–Є–є –Є –Є—Е —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ–∞—П –Ї–Њ—А—А–µ–Ї—Ж–Є—П: –Р–≤—В–Њ—А–µ—Д. –і–Є—Б. … –і–Њ–Ї—В. –±–Є–Њ–ї. –љ–∞—Г–Ї. –Ь., 2000. 48 —Б.
8. –Ъ–Њ–Ј–ї–Њ–≤ –Т.–Ш. –Э–Њ–≤—Л–є –Љ–µ—В–Њ–і –Є–Ј—Г—З–µ–љ–Є—П —А–∞—Б—В—П–ґ–Є–Љ–Њ—Б—В–Є –Є —Н–ї–∞—Б—В–Є—З–љ–Њ—Б—В–Є –Њ–±–Њ–ї–Њ—З–µ–Ї –≥–ї–∞–Ј–∞ –њ—А–Є –Є–Ј–Љ–µ–љ–µ–љ–Є–Є –Њ—Д—В–∞–ї—М–Љ–Њ—В–Њ–љ—Г—Б–∞ // –Т–µ—Б—В–љ. –Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥–Є–Є. 1967. вДЦ 2. –°. 5–9.
9. –Ъ–Њ—И–Є—Ж –Ш.–Э., –°–≤–µ—В–ї–Њ–≤–∞ –Ю.–Т., –Ъ–Њ—В–ї—П—А –Ъ.–Х. –Є –і—А. –С–Є–Њ–Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј —В—А–∞–і–Є—Ж–Є–Њ–љ–љ—Л—Е –Є —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є–є –Њ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–µ –њ–µ—А–≤–Є—З–љ–Њ–є –Њ—В–Ї—А—Л—В–Њ—Г–≥–Њ–ї—М–љ–Њ–є –≥–ї–∞—Г–Ї–Њ–Љ—Л // –У–ї–∞—Г–Ї–Њ–Љ–∞. 2005. вДЦ 1. –°. 41–62.
10. –°–≤–µ—В–ї–Њ–≤–∞ –Ю.–Т. –§—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П —Б–Ї–ї–µ—А—Л, –∞–Ї–Ї–Њ–Љ–Њ–і–∞—Ж–Є–Њ–љ–љ–Њ–є –Є –і—А–µ–љ–∞–ґ–љ–Њ–є —Б–Є—Б—В–µ–Љ –≥–ї–∞–Ј–∞ –њ—А–Є –≥–ї–∞—Г–Ї–Њ–Љ–љ–Њ–є –Є –Љ–Є–Њ–њ–Є—З–µ—Б–Ї–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є: –Р–≤—В–Њ—А–µ—Д. –і–Є—Б. … –і–Њ–Ї—В. –Љ–µ–і. –љ–∞—Г–Ї. –Ь., 2009. 40 —Б.
11. –°–Є–љ–µ–Њ–Ї –Р.–Х., –Ч–Њ–ї–Њ—В–∞—А–µ–≤ –Р.–Т., –Ъ–∞—А–ї–Њ–≤–∞ –Х.–Т. –Ю—Ж–µ–љ–Ї–∞ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –љ–µ–њ—А–Њ–љ–Є–Ї–∞—О—Й–µ–є —Б–Ї–ї–µ—А–Њ—В–Њ–Љ–Є–Є –њ—А–Є —В–µ—А–Љ–Є–љ–∞–ї—М–љ–Њ–є –≥–ї–∞—Г–Ї–Њ–Љ–µ // –У–ї–∞—Г–Ї–Њ–Љ–∞: —В–µ–Њ—А–Є–Є, —В–µ–љ–і–µ–љ—Ж–Є–Є, —В–µ—Е–љ–Њ–ї–Њ–≥–Є–Є. HRT –Ъ–ї—Г–± –†–Њ—Б—Б–Є—П–2010: –°–±. –љ–∞—Г—З. —Б—В. –Ь., 2010. –°. 352–356.
12. –°—В–µ–±–љ–µ–≤–∞ –Ш.–У. –Я–Њ–≤—Л—И–µ–љ–Є–µ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ —Д–∞–Ї–Њ—Н–Љ—Г–ї—М—Б–Є—Д–Є–Ї–∞—Ж–Є–Є –Ї–∞—В–∞—А–∞–Ї—В—Л —Г –±–Њ–ї—М–љ—Л—Е –њ–µ—А–≤–Є—З–љ–Њ–є –Њ—В–Ї—А—Л—В–Њ—Г–≥–Њ–ї—М–љ–Њ–є –≥–ї–∞—Г–Ї–Њ–Љ–Њ–є –љ–∞ –Њ—Б–љ–Њ–≤–µ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П –∞–Ї–Ї–Њ–Љ–Њ–і–∞—Ж–Є–Є –Є –≥–Є–і—А–Њ–і–Є–љ–∞–Љ–Є–Ї–Є –≥–ї–∞–Ј–∞: –Р–≤—В–Њ—А–µ—Д. –і–Є—Б. … –Ї–∞–љ–і. –Љ–µ–і. –љ–∞—Г–Ї. –°–∞–Љ–∞—А–∞, 2009. –°. 141.
13. –°—В—А–∞—Е–Њ–≤ –Т.–Т., –Р–ї–µ–Ї—Б–µ–µ–≤ –Т.–Т. –°—Д–Є–≥–Љ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є–є –Љ–µ—В–Њ–і –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —А–Є–≥–Є–і–љ–Њ—Б—В–Є –≥–ї–∞–Ј–∞ // –°–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –Љ–µ—В–Њ–і—Л –Є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є –ї–µ—З–µ–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —А–Њ–≥–Њ–≤–Є—Ж—Л –Є —Б–Ї–ї–µ—А—Л: –°–±. –љ–∞—Г—З. —Б—В. –Ь., 2007. –°. 293–299.
14. –®–Љ—Л—А–µ–≤–∞ –Т.–§., –Ъ—А–∞—Б–љ–Њ–≤ –Ь.–Ь., –Ь–Њ—Б—В–Њ–≤–Њ–є –Х.–Э. –Ф–µ–Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Њ–љ–љ—Л–µ –Њ–њ–µ—А–∞—Ж–Є–Є –љ–∞ –Ј—А–Є—В–µ–ї—М–љ–Њ–Љ –љ–µ—А–≤–µ –њ—А–Є –≥–ї–∞—Г–Ї–Њ–Љ–µ // –Т–µ—Б—В–љ. –Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥–Є–Є. 1989. вДЦ 5. –°. 8–12.
15. Dastiridou A.I., Ginis H.S, Brouwere D.D. et al. Ocular rigidity, ocu–lar pulse amplitude, and pulsatile ocular blood flow: the effect of in–traocular pressure // Invest. Ophthalmol. Vis. Sci. 2009. N 50. P. 5718–5722.
16. Fukusaku H., Marron J. Anterior ciliary’s sclerotomy with silicone expansion plug implantation: effect on presbyopia and intraocular pressure // Int. Ophtalmol Clin.– 2001. Vol. 41. N 2. P. 133–141.
17. Schachar R.A. Scleral epansion band procedure: therapy for ocular hypertension and primary open–angle glauocoma // Ann. Ophthalmol. 2000. Vol. 32. N 2. P. 87–89.












