hemorrhages and postoperative fibrinoid syndrome
Zh.Yu. Alyabyeva, E.A. Egorov
Intraocular hemorrhages and fibrinoid syndrome are frequent complications of various types of ophthalmopathology. Thrombolytic drugs are widely used in the treatment of these complications. Results of clinical trials of Hemasa showed it’s high thrombolytic and fibrinolytic activity.
Внутриглазные кровоизлияния и фибриноидный синдром являются достаточно частым осложнением различной офтальмопатологии, нередко усугубляя течение и послеоперационный период наиболее распространенных плановых глазных операций, в частности, экстракции катаракты, антиглаукоматозных операций, витрэктомии. Известно, что фибрин в полости глаза стимулирует миграцию клеток пигментного эпителия и глиальных клеток. Это может приводить к формированию эпиретинальных, трансвитреальных и циклитических контрактильных мембран с последующей отслойкой сетчатки, цилиарного тела и развитием субатрофии.
В настоящее время следует считать доказанным тот факт, что внутриглазные кровоизлияния, особенно гемофтальм, способствуют развитию неоваскуляризации. Это, вероятно, обусловлено интенсификацией перекисного окисления липидов, вторичными изменения локального гемостаза и фибринолиза, а также реакцией иммунной системы организма – изменениями, установленными на примере травматического гемофтальма [7].
Для стекловидного тела характерны низкие параметры массопереноса, что обусловливает особенности рассасывания интравитреального кровоизлияния. Как известно, в этом процессе можно выделить 3 основные звена:
• Гемолиз
• Фибринолиз
• Фагоцитоз.
Очищение стекловидного тела от дериватов крови обеспечивается 3–м звеном вышеуказанного комплекса и происходит следующими путями:
1. Макрофаги мигрируют к эпителию цилиарного тела, а также к зрительному нерву и наружу через периваскулярные пространства.
2. Макрофаги мигрируют к внутренним слоям сетчатки, проникают в ретинальные сосуды и удаляются кровотоком.
3. Гемосидерин диффундирует к цилиарному телу и строме радужки [10].
Все применяющиеся в офтальмологии фибринолитики воздействуют на первые два звена (гемолиз и фибринолиз), из которых, по мнению большинства авторов, ведущая роль принадлежит гемолизу. Однако бурный гемолиз, происходящий на фоне эффективного медикаментозного лечения, еще не является гарантией благополучного исхода гемофтальма: фибринолитики лишь усиливают гемолиз и лизируют выпавший в ходе патологического процесса фибрин.
Низкие параметры массопереноса и токсическое действие продуктов гемолиза на сетчатку, их ангиогенный эффект вынуждают офтальмологов искать пути хирургического решения проблемы (такие как закрытая витрэктомия) и более щадящие методы – ферментный витреолиз [7], криопексия [5] и др. К сожалению, данные методы не всегда применимы. Тяжелое общее состояние, выраженная пролиферация на глазном дне, остаточное зрение на единственном зрячем глазу, рецидивирующий гемофтальм – затрудняют или делают невозможным проведение обширных операций на стекловидном теле. При закрытой витрэктомии общее число осложнений составляет 25–40%. Это отек роговицы, повторные кровоизлияния, ятрогенные разрывы и отслойка сетчатки, развитие рубеоза радужки и неоваскулярной глаукомы [3]. Поэтому продолжается разработка методов консервативного лечения интравитреальных кровоизлияний. Известно, что стекловидное тело практически не обладает фибринолитической активностью и рассасывание крови в случае гемофтальма протекает медленно [9], поэтому патогенетически обоснованным в лечении кровоизлияний в стекловидное тело является применение ферментов. Использовались различные протео– и фибринолитические ферменты: коллализин, урокиназа, стрептокиназа [4, 8]. Однако нативные ферменты имеют целый ряд существенных недостатков. Так, при местном введении не достигается оптимальная концентрация фермента, необходимая для лизиса крови, увеличение разовой вводимой дозы препарата приводит к рецидивам геморрагий, токсическому воздействию на оболочки глаза. Ферменты нестабильны, быстро выводятся из организма, инактивируются ингибиторами. Многократное их применение ведет к возникновению аллергических реакций. Идет поиск новых ферментов и проферментов, в частности, тромболитиков.
Тромболитики – это активаторы плазминогена, которые переводят плазминоген, неактивный фермент системы фибринолиза крови в протеолитический фермент плазмин. Плазмин разлагает фибрин сгустка крови, но может также разрушать нормальные компоненты системы гемостаза, способствуя кровотечению. В настоящее время 5 тромболитических ферментов либо приняты к клиническому применению, либо находятся в стадии клинических испытаний. Это стрептокиназа, урокиназа, рекомбинантный активатор плазминогена тканевого типа, анизолированный комплекс плазминоген–стрептокиназа и активатор плазминогена типа урокиназы с одной цепью – проурокиназа. Тромболитические агенты первого поколения – стрептокиназа и урокиназа – обладают лишь средней эффективностью, и их применение чревато распространенным нарушением системы свертывания, т. к. они не обладают специфичностью по отношению к фибрину (разрушают также фибриноген). По сравнению с ними рекомбинантный тканевой активатор плазминогена в клинических испытаниях у больных острым инфарктом миокарда показал большую специфичность и фибринспецифичность. Эти же преимущества свойственны и проурокиназе. Этот профермент относится к группе тромболитиков 2–го поколения, обладает повышенным сродством к фибрину, резистентен к ингибиторам активаторов плазминогена и превращается в активную урокиназу на фибрине под действием малых доз плазмина. Функционирование урокиназы в организме проявляется в двух аспектах: в кровеносной системе урокиназа служит для рассасывания кровеносных сгустков, а на уровне тканей и отдельных клеток она инициирует протеолиз внеклеточного матрикса и облегчает клеточную миграцию. В крови урокиназа находится в основном в состоянии малоактивного фермента, связанного вдобавок с ингибиторами. При появлении тромба урокиназа адсорбируется на нем и начинает свою работу. По–видимому, ее активация на тромбе происходит с участием тканевого активатора плазминогена, для которого характерна значительная стимуляция собственно фибрином [6]. Tripathi R. C. et al. (1990) сообщают о наличии активатора плазминогена урокиназного типа в тканях глаза человека и животных [12]. Имеется опыт применения проурокиназы и тканевого активатора плазминогена для лечения кровоизлияний в офтальмологии (в клинике и в эксперименте) [2, 1, 11].
С учетом вышеизложенного для применения в офтальмологии был разработан препарат рекомбинантной проурокиназы – гемаза. Препарат гемаза создан сотрудниками научно–производственного объединения «Техноген» совместно с Российским кардиологическим научно–производственным комплексом Минздравмедпрома России (РКНПК МЗМП). Гемаза представляет собой лиофилизированный ферментный препарат, содержащий смесь рекомбинантной проурокиназы (РПУ) с декстраном и хлоридом натрия. Действующей субстанцией препарата является РПУ, декстран и хлорид натрия создают инертную матрицу фермента. Гемаза катализирует превращение плазминогена в плазмин – сериновую протеазу, способную лизировать фибриновые сгустки. Специфическая активность гемазы – 80 000–100 000 МЕ на 1 мг белка. Гемаза хорошо растворима в воде и физиологическом растворе, обладает низкой токсичностью и хорошей переносимостью. Фармакологическое изучение препарата показало его высокую тромболитическую и фибринолитическую активность.
Клинические исследования гемазы в группе больных с заболеваниями и травмами глаза, сопровождающимися внутриглазными кровоизлияниями и фибринообразованием, показали, что гемаза обладает выраженным лечебным эффектом и отсутствием побочных явлений при различных способах введения: подконъюнктивально, в переднюю камеру глаза и парабульбарно в дозе 5000 МЕ.
Средний срок полного рассасывания тотальной гифемы составил около 4,5±1,5 дня, фибринозного экссудата в передней камере после оперативных вмешательств – 3,0±0,5 дня. Гифема до 5 мм рассасывалась в течение 2–3 суток во всех случаях. Для полного рассасывания гифемы высотой 5–9 мм требовалось 3–5 суток. Тотальная гифема рассасывалась за 5–7 суток.
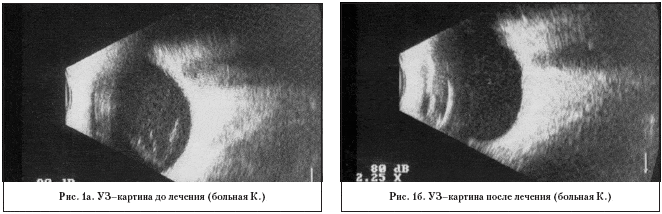
Препарат был наиболее эффективен при рассасывании частичных гемофтальмов. Выраженный эффект появлялся к 7–10 дню. Отсроченное действие препарата продолжалось после окончания курса инъекций (до 10–14 на курс), и к 1 месяцу после начала лечения острота зрения повышалась в среднем в два раза, у большинства пациентов с частичным гемофтальмом к 3–му месяцу восстанавливалась полная прозрачность стекловидного тела. Данные ультразвука до и после курса лечения частичного гемофтальма (осложнения диабетической ретинопатии) гемазой (5000 парабульбарно №10) представлены на рис. 1а. и 1б. При рецидивирующих гемофтальмах (гипертоническая болезнь, тромбозы ЦВС, пролиферативная диабетическая ретинопатия) эффективность курса лечения была максимальной при первом кровоизлиянии и снижалась при последующих рецидивах. Отмечается снижение эффективности препарата при развитии процессов швартообразования в стекловидном теле. При тяжелых пролиферативных изменениях с рубеозом сетчатки и рецидивирующими геморрагическими осложнениями применение гемазы может быть сопряжено с увеличением риска рецидива кровоизлияния.
Применение гемазы при реактивном фибриноидном синдроме показало, что рассасывание даже выраженного фибринозного выпота в передней камере глаза происходило в сроки до 17 суток (в среднем за 5,8±1,6 дня) и было особенно эффективным на ранних стадиях (при длительно наблюдаемой опалесценции влаги передней камеры – в течение 3–4 дней) и в сочетании с применением дексаметазона (с интервалом между инъекциями дексаметазона и гемазы не менее 3–4 часов). Это позволяло не только достаточно быстро купировать реактивный фибриноидный синдром, но и предотвратить развитие задних синехий радужки и деформацию зрачка.
Гемазу рекомендуется применять для повышения эффективности лечения гемофтальмов различного генеза, гифемы, реактивного фибриноидного синдрома после экстракции катаракты и ленсвитрэктомии, инволюционной центральной хориоретинальной дистрофии с геморрагическим компонентом, тромбоза центральной вены сетчатки и ее ветвей, преретинальных и субретинальных кровоизлияний различного генеза, при фибринозно–пластических иридоциклитах. Также возможно применение гемазы для профилактики заращения фистулы при антиглаукоматозных операциях фистулизирующего типа.
Литература
1. Алябьева Ж. Ю., Матвеев М. Ю., Евграфов В. Ю., Домогатский С. П. Фармакокинетика глазной формы рекомбинантной проурокиназы. / Вестн. офтальмол. – 1998 – N 1 – c. 38–41.1.
2. Бойко Э. В., Даниличев В. Ф., Кольцова С. В. Оптимизация дозы нативной и иммобилизованной проурокиназы для интравитреального введения и рассасывания экспериментального кровоизлияния в стекловидную камеру глаза // Боевые повреждения органа зрения: Тез. докл. – СПб.: ВмедА,1993 – с. 79.
3. Витрэктомия при диабетической ретинопатии. Метод. рекомендации. Сост. С. Н. Федоров. – М.1988.– 15 с.
4. Егоров Е. А. Тромболитическая терапия укиданом в офтальмологии // Международная конференция офтальмологов городов–побратимов Одессы, тезисы докладов. – Одесса, 1981 – с. 96–98.
5. Кацнельсон Л. А., Форофонова Т. И., Елисеева Р. Ф. Транссклеральная криопексия при гемофтальмах диабетического генеза//Вестн.офтальмол.– 1990.– N 2. – с.19–21.
6. Панченко В. М. Тромбозы и эмболии. Вопросы патогенеза, диагностики и лечения. – М., 1993. – 68 с.
7. Ромащенко A. Д. Диагностика и патогенетически ориентированное лечение травматического гемофтальма // Дисc. ... докт. мед. наук. – М.,1989. – 355 с.
8. Чазов Е. Н., Гундорова Р. А., Ромащенко А. Д. Иммобилизованная стрептокиназа (стрептодеказа) в лечении внутриглазных кровоизлияний // Вестн.офтальмол. – 1982. – N 4. – с.61–64.
9. Forrester J. V., Prentice C. R., Williamson J. et al. Fibrinolytic activity of the vitreous body // Nature. – 1974. – V.2542(83). – p.875–879.
10. Maberly A. L., Chisgilm L. D. The effect of a fibrinolytic agents in vitreal haemorrage in rabbits // Canad. J. Ophth. – 1970. – V. 5(1). – p.55–64.
11. Oncel M., Peyman G. A., Khoobehi B. Tissue plasminogen activator in the treatment of experimental retinal occlusion //Retina. – 1989. – N 1. – p.1–7.
12. Tripathy R. C., Tripathy B. J., Park J. K. Localization of urokinase–type plasminogen activator in human eyes: an immunocytochemical study// Exp. Eye Res. – 1990. – V. 51(5). – p.545–552.












