of pigment epithelium areas of hyperpermeability
(experimental study)
A.E. Egorov, D.V. Katz, N.N. Tovstenko
Russian State Medical University
Institute of bioorganic chemistry named after M.M. Shemyakin and Yu. A. Ovchinnikov, Moscow
Purpose: Development and experimental evaluation of efficacy of the method of drug depositing by using of the subtenon’s space introduction for addressed delivery inside the eye globe.
Materials and methods:
We took for experiment 30 sexually mature chinchilla rabbits. On the 3rd day after performing of trophic laser coagulation, on the background of local vasoconstriction, we introduced Р32 subconjunctivally, combined with methylcellulose to the rabbits of experimental group and Р32 alone in the control group.
After removing of rabbits from experiment by introduction of the air to the ear vein, we enucleated eyes in 30 minutes, 1 hour, 2, 4, 6 hours. Vitreous body, retina with choroid and optic nerve were extracted. Spicemens were placed into the gamma counter and radioactivity counting was performed.
Results and conclusion:
In the experimental group we observed more fluent deposition of Р32 and higher values of tissue radioactivity and also more prolonged preservation of concentration of introduced tracer in comparison with control group. It indicates efficacy of methylcellulose, used as depositing agent for prolongation of drug effect which was introduced into the subtenon’s space at the areas of hyper permeability.
Широкая распространенность таких тяжелых заболеваний, как глаукомная оптическая нейропатия, диабетическая ретинопатия, передняя ишемическая нейропатия, макулодистрофия, обусловливает необходимость разработки новых методов лечения с целью доставки лекарственных препаратов в задний отдел глазного яблока и создания высоких терапевтических концентраций лекарственных средств в сетчатке и зрительном нерве. Обычно для лечения различных патологий заднего отрезка глазного яблока используют внутривенное и внутримышечное, пара– и ретробульбарное введение сосудорасширяющих препаратов и других лекарственных средств. Также используется субтеноновая имплантация коллагеновой инфузионной системы в различных модификациях [1,5,7]. Однако эти способы введения лекарственных препаратов не являются оптимальными, так как существует повышенный риск травматизации глаза, развития орбитальных гематом после пара– и ретробульбарных инъекций, повышенный риск проникновения инфекции по ходу силиконовой трубочки коллагеновой инфузионной системы. Кроме того, препятствием для проникновения лекарственных веществ внутрь глаза служит гематоофтальмический барьер, важнейшей составляющей которого является пигментный эпителий сетчатки [6].
На кафедре глазных болезней РГМУ была разработана и апробирована методика создания зон повышенной проницаемости гематоофтальмического барьера в области плоской части цилиарного тела с помощью диодного лазера [3]. На сегодняшний день это эффективный и малотравматичный способ доставки лекарственных средств в область заднего сегмента. Эффективность его была доказана экспериментально и клинически [2,4]. Суть метода заключается в том, что после создания «окон» в пигментном эпителии на фоне применения местной вазоконстрикции и субтенонового введения лекарственных препаратов удается получить терапевтически значимые концентрации их в депо стекловидного тела. В клинической практике это позволяет достичь улучшения зрительных функций у больных глаукомной оптической нейропатией. Недостатком приведенного метода является необходимость выполнения ежедневных субконъюнктивальных инъекций в течение 10 дней, что снижает качество жизни пациентов и приводит к дополнительной травматизации структур глазного яблока.
Для повышения качества жизни пациента оптимальным решением было бы снижение количества введения препаратов до 1–2 раз, что также существенно облегчило бы проведение консервативной терапии в амбулаторных условиях. В связи с этим нами было проведено экспериментальное исследование эффективности депонирования пролонгированных форм лекарственных препаратов при субтеноновом введении для адресной доставки внутрь глазного яблока с использованием зон повышенной проницаемости.
Целью нашей работы являлась разработка и экспериментальная оценка эффективности методики депонирования лекарственных препаратов при субтеноновом введении для адресной доставки внутрь глазного яблока.
Материал и методы
В исследовании использовалось 30 половозрелых кроликов породы шиншилла.
Всем животным была произведена трофическая транссклеральная лазерциклокоагуляция диодным лазером «Алком».
Техника операции. После премедикации 1% раствором димедрола, инстилляционной анестезии 0,25% раствором дикаина и фиксации животного в станке, с помощью контактного лазерного зонда, с умеренным вдавлением склеры, в 3 мм от лимба, в зоне между верхней и наружной прямой мышцами (на 10–11 часах для правого глаза), в шахматном порядке в 3–4 ряда наносились 8–12 лазерных коагулятов. Режим работы лазера: мощность 1,0 Вт, экспозиция 3 с.
На третий день после вмешательства животные помещались в радиоизотопный блок, где на фоне местной вазоконстрикции в зону нанесения лазерных коагулятов под конъюнктиву вводилась радиоактивная метка. В качестве радиофармпрепарата использовался радиоактивный Р32. Молекула этого вещества определялась с помощью гамма–счетчика.
В каждый глаз кролика производилась инъекция, содержащая 800 мкг KH2PO4, с радиоактивностью 1млн. g импульсов в мин. В правый глаз (опыт) после инстилляции дикаином вводился радиоактивный фосфат, разведенный в 2% р–ре метилцеллюлозы до 0,2 мл (30 мкл соли радиоактивного Р32 + 30 мкл соли «холодного» Р31 + 80 мкл NaCl + 60 мкл вискоэластика). Перед введением раствор вискоэластика перемешивался для достижения более равномерного распределения метки. В левый глаз (контрольный) вводился радиоактивный фосфат, разведенный в физ. р–ре до 0,2 мл (30 мкл соли радиоактивного Р32 + 30 мкл соли «холодного» Р31 + 140 мкл NaCl). Все инъекции проводились на фоне вазоспазма, вызванного закапыванием 10% ирифрина за 30 мин до введения радиоактивной метки, и после введения инстилляция проводилась каждые полчаса до конца опыта.
Затем животных выводили из опыта путем введения в ушную вену воздуха и производилась энуклеация глаз. Выведение из опыта происходило по 2 особи по следующей схеме: через 30 мин, 1 час после инъекции, через 2, 4 и 6 часов.
Энуклеированные глаза препарировались, выделялись стекловидное тело, зрительный нерв, сетчатка с хориоидеей, которые помещались в пробные пробирки, затем производилось измерение радиоактивности g–счетчиком.
Результаты
В результате произведенных измерений были полученны следующие данные, которые обсчитывались по стандартной формуле расчета радиоизотопных разбавлений радиоактивного Р32.
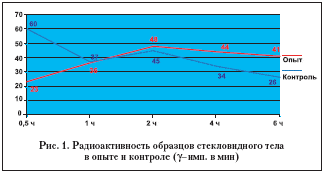
Из графика радиоактивности образцов стекловидного тела в опыте и контроле (рис. 1) видно, что после ведения Р32 в область плоской части цилиарного тела в зоне коагулятов, через 30 минут в контрольной группе отмечается пик накопления радиоактивности в среднем до 60±7 g–имп./мин (р<0,05), что свидетельствует о более быстром проникновении маркерного вещества и начале относительно быстрой элиминации метки, тогда как в опытной группе еще происходит нарастание радиоактивности в среднем от 23±5 имп. мин (р<0,05), пик накопления смещается во времени – максимум радиоактивности приходится на 2 часа и составляет в среднем до 48±9 g–имп./мин (р<0,05). Также в опытной группе отмечается более медленное снижение концентрации фосфора, что, по–видимому, свидетельствует о пролонгирующем действии вискоэластика на поступление маркерной субстанции в витреальное депо.
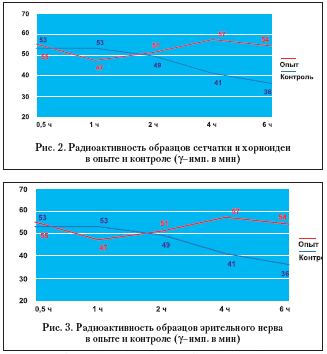
Исследование образцов сетчатки и хориоидеи (рис. 2) позволило получить сходные результаты. Так, в опытной группе максимальное накопление радиоактивной метки происходит через 4 часа после субтенонового введения маркерного вещества (1 час в контрольной группе) и достигает более высоких значений по сравнению с группой, где не использовалась пролонгированная форма раствора радиоактивной метки (в среднем 57±7 g–имп./мин, р< 0,05 и 41±9 g–имп./мин, р<0,05 соответственно).
При оценке средних значений радиоактивности образцов внутриглазной части зрительного нерва (рис. 3) также отмечается значительно более активное накопление метки в опытной группе на протяжении всего эксперимента по сравнению с контролем. Так, в исследованных тканях максимальное значение сцинтилляций приходится на 6 часов и в среднем достигает 26±10 g–имп./мин (р<0,05), тогда как в контрольной группе 16±10 g–имп./мин (р< 0,05).
Таким образом, максимальные значения радиоактивности в контрольной группе достигаются через 30 минут после введения радиоактивной метки в область коагулятов, исключение составляет зрительный нерв, где происходит нарастание маркерного вещества в течение всего периода наблюдения. В опытной группе отмечается постепенное нарастание концентрации метки, более высокие значения сцинтилляций на протяжении всего опыта, начиная с 1 часа. В зависимости от времени забора материала количество Р32 в опытной группе превышает контроль: в стекловидном теле – в 1,0–1,57 раза (р< 0,05); в сетчатке и хориоидее – в 1,1–1,5 раза (р< 0,05) и в зрительном нерве – в 1,4–1,7 раза (р< 0,05).
Выводы
В опытной группе наблюдается более плавное накопление Р32 и более высокие значения радиоактивности тканей, а также более длительное сохранение концентрации введенной метки по сравнению с контролем, что свидетельствует об эффективности гидроксипропилметилцеллюлозы, использованной в качестве депонирующего агента для пролонгации действия лекарственных препаратов, вводимых в субтеноново пространство в области зон повышенной проницаемости.
Возможность клинического применения предлагаемой методики является целью наших дальнейших исследований.
Литература
1. Басинский С.Н.. Способ адресной доставки лекарственных препаратов в лечении дистрофических состояний глаз // Клиническая офтальмология. – 2004 – Том 5 – № 1 – с. 5–8.
2. Егоров А.Е. Управляемое локальное воспаление как новый подход к лечению глаукомной оптической нейропатии. // Дисс. Ена соискание степени д.м.н., Москва, 2003, 165 с.
3. Егоров А.Е., Касимов Э.М., Шрамко Ю.Г. Временное локальное нарушение проницаемости гематоофтальмического барьера как способ введения лекарственных средств для лечения глаукомной оптической нейропатии. // Рефракционная хирургия и офтальмология, т.3, №1, 2003, с. 43–46.
4. Егоров А.Е., Нестеров А.П., Егоров Е.А., Гришин Е.В., Шрамко Ю.Г., Касимов Э.М. Экспериментальное обоснование эффективности зон повышенной проницаемости в плоской части цилиарного тела, создаваемых с помощью диод–лазерных аппликаций // Клиническая офтальмология. – 2001 – Том 2 – № 2 – с. 44
5. Егоров Е.А. «Рациональная фармакология в офтальмологии» // Москва, «Литтера», 2004
6. Нестеров А.П. Глаукома – дискуссионные проблемы. Доклад на конференции «Актуальные проблемы глаукомы». // Клиническая офтальмология. – 2004 – Том 5 – № 2 – с. 49–51.
7. Нестеров А.П., Басинский С.Н. Новый метод введения лекарственных препаратов в задний отдел тенонова пространства // Вестн.офтальмол. – 1991. – №5. – С.11–14.












