Ae.M. Kasimov, D.V. Gasanov
National Center of Ophthalmology named after acad. Zarifa Alieva, Azerbaijan, Baku
Purpose: to evaluate the efficiency and safety of canal plastics in patients with POAG.
Materials and methods: IOP level was measured before and in 1 and 3 months after surgery. Also OCT and gonioscopy were performed in all patients.
Results: 9 operations were carried out, in 6 subjects – single canal plastics and in 3 – canal plastics and phacoemulsification with IOL implantation. 3-months observation period was settled. Average decrease of IOP level was 15.2 mm Hg. No serious complications were registered in postoperative period. The most frequent complication was transient hyphema.
Conclusion: Method of canal plastics is safe and efficient but still needs longer observation and further research.
Введение
Во всем мире глаукома является второй ведущей причиной слепоты, от этой болезни страдает около 66 млн человек. Глаукома поражает каждого из 200 человек в возрасте 50 лет и одного из 10 старше 80 лет [1–4].
Основным фактором риска для большинства видов глаукомы является повышенное внутриглазное давление (ВГД), которое возникает в результате продукции водянистой влаги цилиарными отростками глаза и ее дренажа через трабекулярную сеть (ТС) и Шлеммов канал (ШК) в склеральное сплетение. Открытоугольная глаукома (ОГ) является следствием снижения оттока водянистой влаги через TС и ШК. При закрытоугольной глаукоме (ЗУ) радужка выталкивается вперед по отношению к ТС, блокируя отток водянистой влаги.
На ранней стадии медикаментозное или хирургическое вмешательство способно остановить или замедлить прогрессирование глаукомы. Доказано, что первичное хирургическое вмешательство эффективнее первичной медицинской помощи пациентам с ОГ [5].
С начала 1970-х гг. трабекулэктомия, описанная Сугаром, Кэрнсом и позже Фронипоулосом, стала «золотым стандартом» в лечении ОГ [6–8]. Это процедура предназначена для снижения ВГД и включает в себя хирургическое формирование пути для оттока водянистой влаги из передней камеры глаза в субконъюнктивальное пространство, основной целью является формирование фильтрационной подушки (ФП). Этот относительно нефизиологический подход и образование рубцов склеры, а также конъюнктивы привели к введению антиметаболитов.
Информация о многочисленных интра- и послеоперационных осложнениях была опубликована [9–12], среди них указывались гипотония, макулопатия, инфицирование ФП/эндофтальмит, гифема, супрахориоидальное кровоизлияние, инкапсуляция ФП, приводящая к повышению ВГД, потеря остроты зрения и повышенный риск формирования катаракты. Все это привело к поиску более физиологического (непроникающего в переднюю камеру глаза) и независимого от ФП хирургического вмешательства, способствующего понижению ВГД [13,14].
На основе синусотомии Краснова были описаны несколько непроникающих фильтрационных методов хирургии для ОГ [15,16]. В 1984 г. Федоров описал технику глубокой склерэктомии (с внешней фильтрацией), основной целью которой является удаление роговично-склеральной стромы над десцеметовой мембраной и передней ТС. Оставшаяся трабекуло-десцеметова мембрана (TДM) обеспечивала некоторую устойчивость к оттоку водянистой влаги [17,18].
В 1995 г. Стигман описал технику вискоканалостомии (без внешней фильтрации), основной целью которой является расширение коллапсированного ШК с помощь вискоэластика (OVD; Healon GV, AMO (Santa Ana, Calif)) [19]. Водянистая влага, оттекая через ТДМ, попадает в интрасклеральное озеро, как при глубокой склерэктомии, через микротрещины расширенного ШК и далее следует по физиологическому пути без внешней фильтрации. Тем не менее, основной причиной неудачи вискоканалостомии является реколлапс ШК [20,21]. Кроме того, большое количество коллекторных каналов расположено в нижне-носовой части [22–24].
Последние технологические достижения позволили хирургам использовать гибкие микрокатетеры (iTrack, iScience Interventional, USA, Glaucolight, DORC, Netherlands) для более атравматического доступа по всей длине ШК. Эта техника называется каналопластикой [25,26]. Каналопластика – это новая непенетрирующая, не зависящая от ФП антиглаукоматозная операция, основной целью которой является восстановление физиологического оттока водянистой влаги путем воздействия на юкстаканаликулярную ТС и внутреннюю стенку ШК. Полипропилен помещается с помощью микрокатетера в ШК, чтобы растянуть внутреннюю стенку.
Цель
Оценить безопасность и эффективность каналопластики у пациентов с ОГ.
Методы
С 14 июля 2011 г. в Национальном центре офтальмологии им. академика Зарифы Алиевой мы начали выполнять каналопластику у пациентов с ОГ. Девять успешных процедур были выполнены одним хирургом. У 6 пациентов (6 глаз) была проведена только каналопластика, у 3 пациентов (3 глаза) – каналопластика в сочетании с факоэмульсификацией и имплантацией интраокулярной линзы. Наблюдения проводились в течение 3 мес. Средний возраст пациентов составил 60,3±8,2 года. Среднее значение предоперационного ВГД было 30,6±4,7 мм рт. ст. Среднее значение используемых противоглаукомных капель до операции составило 2,3±0,5. ВГД измерялось через 1 и 3 мес. после операции. Всем пациентам через 2 нед. проводились оптическая когерентная томография переднего сегмента (ПС-ОКТ-Visante, Carl Zeiss Meditec) и гониоскопия.
Хирургическая техника
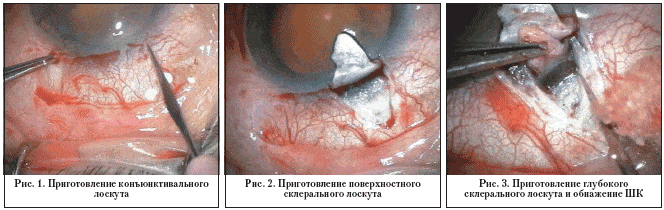
Конъюнктива и Тенонова капсула иссекаются по лимбу. Для сохранения эписклеральных коллекторных каналов коагуляция не проводится (рис. 1).
Приготовление поверхностного склерального лоскута параболической формы размером около 5,0x5,0 мм и толщиной от 200 до 300 нм, что составляет примерно половину толщины склеры (рис. 2).
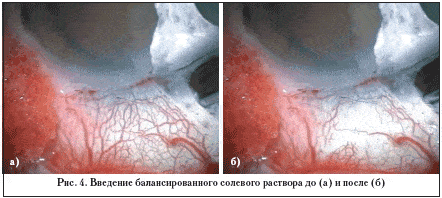
1. Приготовление глубокого склерального лоскута и обнажение ШК. Глубокий склеральный лоскут меньше, чем поверхностный, его размер – около 4,0x4,0 мм (рис. 3). После обнажения ШК для оценки расположения его отверстия вводится сбалансированный солевой раствор (рис. 4а, б).
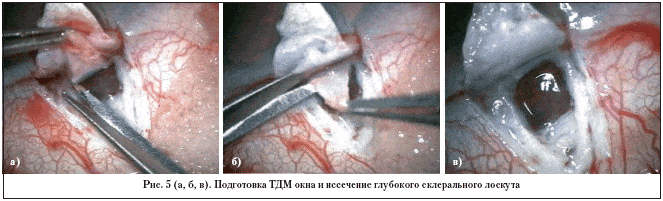
Подготовка TДM окна и иссечение глубокого склерального лоскута (рис. 5а, б, в). Чтобы минимизировать риск перфорации и пролапса радужки, понижаем ВГД. Аккуратным надавливанием на линию Швальбе отделяем TДM от роговично-склерального соединения. Для увеличения оттока водянистой влаги удаляем юкстаканаликулярную ТС (рис. 6).
2. Катетеризация ШК. С помощью микрокатетера Glaucolight (рис. 7) проводится полное (360°) механическое расширение ШК. Красное свечение обеспечивает визуальный контроль при продвижении катетера вдоль ШК (рис. 7–9).
Размещение шва. После полной круговой дилатации ШК (рис. 10) на дистальный конец Glaucolight-волокна привязывается нитка из 10,0 полипропилена (Prolene, Ethicon Inc.). Далее вытягиваем катетер обратно.
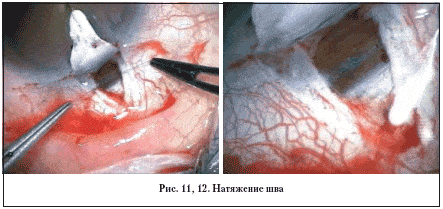
3. Натяжение шва. Степень натяжения шва оценивается по степени прогибания ТДМ (рис. 11, 12).
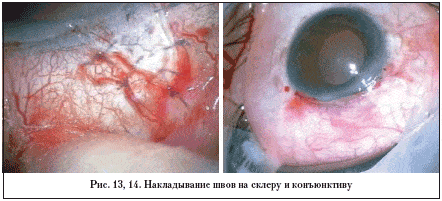
4. Плотное наложение швов на склеру и конъюнктиву. На склеру накладывается 5–7 8,0 рассасывающихся швов (рис. 13). Закрытие конъюнктивы проводится 8,0 рассасывающимися швами (рис. 14).
Результаты
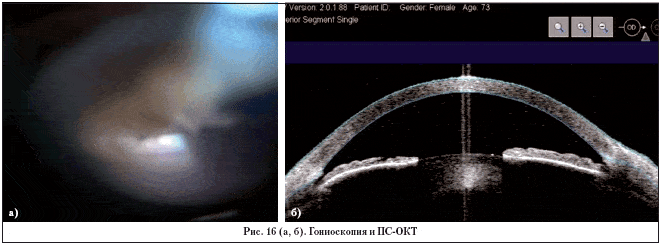
Среднее ВГД составило 12,4±2,0 мм рт. ст. через 1 мес., 14,4±2,5 мм рт. ст. – через 3 мес. после операции. Все послеоперационные данные ВГД были значительно снижены (p <0,001). Рутинно всем пациентам через 2 нед. после операции были проведены гониоскопия и ПС-ОКТ, которая показала натяжение и расширение ШК (рис. 16 а, б).
Среднее количество антиглаукоматозных капель до каналопластики составляло 2,3±0,5 и существенно уменьшилось после операции (до 0,11±0,33, p <0,01). Самым частым послеоперационным осложнением была транзиторная гифема (44,4%), которая проходила в течение недели. После хирургической операции не было отмечено острого подъема ВГД. Средний хирургически индуцированный астигматизм уменьшился с 1,27±0,8 дo 0,22±0,4 в течение 2 мес. Мелкой передней камеры, связанной с гипотонией, макулопатии и отслойки хориоидеи отмечено не было. В случае перфорации ТДМ операция была конвертирована в трабекулэктомию, и пациенты исключались из исследования.
Обсуждение
Основным преимуществом каналопластики перед трабекулэктомией является мизерный процент осложнений. Результаты многолетних исследований показывают, что трабекулэктомия не является лучшей хирургической альтернативой [27]. Клинические исследования доказали безопасность и эффективность каналопластики в снижении ВГД. Grieshaber и др. опубликовали долгосрочные результаты каналопластики при ОГ у темнокожих африканцев. Среднее ВГД через 12 мес. после операции у них было 15,4±5,2 мм рт. ст.
Наше исследование показало, что среднее ВГД на 3-й мес. после операции составляло 14,4±2,5 мм рт. ст. Никаких серьезных интра- и послеоперационных осложнений не возникало, транзиторная гифема была самым частым послеоперационным осложнением (44,4%). Также уменьшилось количество используемых антиглаукоматозных капель.
Следует отметить, что технически это трудновыполнимая операция, которая требует времени для обучения и навыков у хирурга. Главным недостатком нашего исследования является короткое время наблюдения.
Выводы
Каналопластика – это эффективная, но требующая навыков операция, которая помогает восстановить естественный отток внутриглазной жидкости с помощью интраканаликулярного натяжного шва. Она приводит к значительному снижению ВГД у взрослых пациентов с ОГ и имеет малое количество послеоперационных осложнений. Необходимо длительное наблюдение больных, чтобы оценить эффект каналопластики при ОГ.


Литература
1. Quigley H.A. The number of persons with glaucoma worldwide // Br. J. Ophthalmol. – 1996. – Vol. 80. – P. 389–393.
2. Pizzarello L., Abiose A., Ffytche T. Vision 2020: The Rightto Sight a global initiative to eliminate avoidable blindness // Arch. Ophthalmol. – 2004. – Vol. 122. – № 4. – P. 615–620.
3. Congdon N., O'Colmain B., Klaver C.C. Cause and prevalence of visual impairment among adults in the United States // Arch. Ophthalmol. – 2004. – Vol. 122. – № 4. – P. 477–485.
4. Friedman D.S., Wolfs R.C., O'Colmain B.J. Prevalence of open-angle glaucoma among adults in the United States // Arch. Ophthalmol. – 2004. – Vol. 122. – № 4. – P. 532–538.
5. Migdal C., Gregory W., Hitchings R. Long-term functional outcome after early surgery compared with laser and medicine in open-angle glaucoma // Ophthalmology. – 1994. – Vol. 101. – № 10. – P. 1651–1656.
6. Sugar H.S. Experimental trabeculectomy in glaucoma //Am. J. Ophthalmol. – 1961. – Vol. 51. – P. 623.
7. Cairns J.E. Trabeculectomy. Prelimanary report of e new method // Am. J. Ophthalmol. – Vol. 66. – № 4. – P. 673–679.
8. Fronimopoulus J., Lambrou N., Pelekis N., Christakis C. Elliot’s trepanation with scleral cover (procedure for protecting the fistula in Elliot’s trepanation with lamellar sclera cover) // Klin. Monbl. Aungenheilkd. – 1970. – Vol. 156. – № 1. – P. 1–8.
9. Jones E., Clarke J., Khaw P.T. Recent advances in trabeculectomy technique // Curr. Opin. Ophthalmol. – 2005. – Vol. 16. – P. 107–113.
10. Mac I., Soltau J.B. Glaucoma-filtering bleb infection // Curr. Opin. Ophthalmol. – 2003. – Vol. 14. – P. 91–94.
11. Borisuth N.S.C., Phillips B., Krupin T. The risk of glaucoma surgery // Curr. Opin. Ophthalmol. – 1999. – Vol. 10. – P. 112–116.
12. Ophir A., Encapsulated filtering bleb; selective review-new deducations // Eye. – 1992. – Vol. 6. – P. 348–352.
13. Gedde S.J., Herndon L.W., Brandt J.D. et al. Surgical complication in the tube versus trabeculectomy study during the first year of follow-up // Am. J. Ophthalmol. – 2007. – Vol. 143. – P. 23–31.
14. Ellingsen B.A., Grant W.M. Trabeculotomy and sinusotomy in enuculated human eyes // Invest. Ophthalmol. – 1972. – Vol. 11. – P. 21–28.
15. Zimmerman T.J., Kooner K.S., Ford V.J. et al. Trabeculectomy vs. nonpenetrating trabeculectomy: retrospective study of two procedures in phakic patients with glaucoma // Ophthalmic. Surg. – 1984. – Vol. 15. – P. 734–740.
16. Arenas E. Trabeculectomy ab externo // Highlights Ophthalmol. – 1991. – Vol. 19. – P. 59–66.
17. Fyodorov S.N., Ioffe D.I., Ronkina T.I. Deep sclerectomy: technique and mechanism of a new antiglaucomatous procedure // Glaucoma. – 1984. – Vol. 6. – P. 181–183.
18. Kozlov V., Bagrov S.N., Anisimova S.Y. Nonpenetrating deep sclerectomy with collagen // Eye Microsurgery. – 1990. – Vol. 3. – P. 157–162.
19. Stegmann R. Visco-canalostomy: a new surgical technique for open angle glaucoma // An. Inst. Barraquer. Spain. – 1995. – Vol. 25. – P. 229–232.
20. Stegmann R., Pienaar A., Grieshaber M.C. Schlemm’s canal surgery: restoring physiological aqueous outflow. In: Grieshaber M.C., Orgul S., Flammer J., eds. Glaucoma TherapyVState of the Art. Basel: Association for Continuing Education in Ophthalmology, 2009.
21. Grieshaber M.C., Pienaar A., Olivier J. et al. Canaloplasty for primary open-angle glaucoma: long-term outcome // Br. J. Ophthalmol. – 2010. – Vol. 94. – № 11. – P. 1478–1482.
22. Ashton N. Anatomical study of Schlemm’s canal and aqueous veins by means of neoprene casts. Part I. Aqueous veins // Br. J. Ophthalmol. - 1951. - Vol. 35. - № 5. - P. 291–303.
23. Kleinert H. The visible flow of aqueous humor in glaucoma after instillation of fluorescein into the anterior chamber; pathology of the intraocular humoral circulation // Klin. Monatsblatter Augenheilkd Augenarztl Fortbild. – 1953. – Vol. 123. – № 6. – P. 653–680.
24. Kleinert H. Vital staining of aqueous humor and its epibulbar outflow pathways following fluorescein injection into anterior chamber // Klin. Monatsblatter Augenheilkd Augenarztl Fortbild. – 1953. – Vol. 122. – № 6. – P. 665–682.
25. Bull H., von Wolff K., Korber N., Tetz M.Three-year canaloplasty outcomes for the treatment of open-angle glaucoma: European study results // Graef.Arch. Clin. Exp. Ophthalmol. – 2011. – Vol. 249. – № 10. – P. 1537–1545.
26. Lewis R.A., von Wolff K., Tetz M. et al. Canaloplasty: Three-year results of circumferential viscodilation and tensioning of Schlemm canal using a microcatheter to treat open-angle glaucoma // J. Cataract Refract. Surg. – 2011. – Vol. 37. – № 4. – P. 682–690.
27. Wishart P.K. Trabeculectomy is not the best surgical option for glaucoma. // Eye. – 2008. – Vol. 22. – P. 603–606.
28. Grieshaber M.C., Pienaar A., Olivier J., Stegmann R. Clinical evaluation of the aqueous outflow system in primary open-angle glaucoma for canaloplasty // Invest. Ophthalmol. Vis. Sci. – 2010. – Vol. 51. – № 3.– P. 1498–1504.












