T.N. Kiseleva, G.S. Polunin, M.V. Budzinskaya,
Yu. M. Lagutina, M.V. Vorobyeva
GU NII of Eye Diseases RAMN
Authors give detailed review of modern conceptions of etiology, classification, pathogenesis and methods of treatment of age–related macular degeneration.
Эпидемиология, классификация
Возрастная макулярная дегенерация (ВМД) – одно из самых распространенных заболеваний глаз, угрожающих значительным снижением зрения и инвалидностью во второй половине жизни. По официальным материалам Центра ВОЗ по профилактике устранимой слепоты (2003), распространенность этой патологии по обращаемости составляет 300 на 100 тыс. населения [6,23,25]. По данным R. Klein, B. Klein [36] заболевание встречается в 40% случаев среди лиц старше 40 лет, по данным R.A. Williams [55] – в 58–100% среди лиц старше 60 лет. В экономически развитых странах мира ВМД как причина слабовидения занимает третье место в структуре глазной патологии после глаукомы и диабетической ретинопатии; оба глаза оказываются пораженными в 60% случаев [37,38]. В США 10% лиц в возрасте от 65 до 75 лет и 30% старше 75 лет имеют потерю центрального зрения вследствие ВМД [39]. Терминальная стадия ВМД (слепота) встречается у 1,7% всего населения старше 50 лет и около 18% населения старше 85 лет.
В России заболеваемость ВМД составляет 15 на 1000 населения [6].
В связи с тем, что клиническая картина заболевания очень разнообразна, в отечественной и зарубежной литературе возникло множество различных терминов: центральная хориоретинальная дистрофия, дистрофия типа Кунта–Юниуса, сенильная макулярная дистрофия, центральная инволюционная дистрофия, возрастная макулярная дистрофия и т.д. В настоящее время большинство офтальмологов считают, что этими многочисленными терминами определяется проявление одного заболевания. В зарубежной офтальмологической практике применяют классификации AREDS (Age–related Eye Disease Study) и Wisconsin Age–related Maculopathy Grading System, которые являются удобными для клинической практики и отражают основные стадии заболевания [34].
1. Ранняя стадия ВМД или возрастная макулопатия (ВМП) – «нормальный» возрастной процесс, характеризующийся появлением друз и/или зон дегенерации ретинального пигментного эпителия (РПЭ). Острота зрения у данной категории пациентов остается в пределах возрастной нормы.
2. Поздняя, или далекозашедшая, угрожающая зрению стадия ВМД характеризуется следующими клиническими симптомами:
– географическая атрофия РПЭ с визуализацией подлежащих сосудов хориоидеи;
– мягкие сливные друзы;
– отслойка пигментного эпителия (ОПЭ) с отслойкой нейроэпителия или без нее;
– субретинальная или суб–РПЭ хориоидальная неоваскуляризация;
– фиброглиальная рубцовая ткань, кровоизлияния или экссудация.
Наиболее распространенной клинической формой заболевания является неэкссудативная или «сухая» форма, встречающаяся в 90% случаев и характеризующаяся медленным прогрессирующим снижением зрения. Более редкая, экссудативная или «влажная» форма ВМД, встречающаяся примерно в 10% случаев, приводит к развитию хориоидальной неоваскуляризации и потере зрения.
Этиология и патогенез возрастной
макулярной дегенерации
Патогенез ВМД до сих пор остается неизвестным, что является причиной поиска возможности лечения заболевания на самых ранних стадиях. Помимо главного фактора риска – возраста, существуют дополнительные факторы. К ним относятся генетическая предрасположенность, атеросклероз, артериальная гипертензия, а также курение, воздействие ультрафиолетового излучения, несбалансированное питание [7,8,12,16].
В настоящее время рассматривают четыре основополагающих теории патогенеза ВМД: первичное старение ретинального пигментного эпителия и мембраны Бруха; повреждение продуктами перекисного окисления липидов (ПОЛ); первичные генетические дефекты; патологические изменения кровоснабжения глазного яблока [5,13,24,28,33].
Вне всякого сомнения, существует определенная генетическая предрасположенность: дети родителей, страдающих ВМД, впоследствии имеют высокий риск развития заболевания. Многочисленные исследования последних лет показали семейный, наследственный характер ВМД с аутосомно–доминантным типом наследования [19,35]. Имеются сведения о клинических проявлениях ВМД в больших семьях, которые отмечаются у нескольких поколений. Ученые определили, что за развитие ВМД могут отвечать 50 генов [41,43,44,48,54].
Лица, имеющие светлую кожу и повышенную чувствительность к воздействию яркого света, также страдают ВМД значительно чаще. Женщины болеют чаще мужчин [47,49].
Доказано, что ряд изменений в макулярной области относится к процессам нормального старения: скопление продуктов обмена в клетках пигментного эпителия, изменения коллагеновых соединительнотканных волокон и утолщение мембраны Бруха, возрастные изменения сосудов хориоидеи [42,46]. Однако по данным R.Klein и соавт. [38], только у 30% лиц старше 60 лет развивается ВМД. Остаются невыясненными процессы физиологического старения, способствующие развитию ВМД, а также вопрос о том, является ли заболевание самостоятельной патологией или сопутствующей процессам старения.
Кроме того, уровень макулярной пигментации также имеет огромное значение в развитии ВМД. Имеются данные о том, что макулярный пигмент является единственным антиоксидантом сетчатой оболочки, который работает как активно (нейтрализует действие свободных радикалов), так и пассивно (ограничивает голубой свет, вызывающий фотооксидантное повреждение, активируя фильтр для голубого света на дорецепторном уровне) [11,22,50].
В патогенезе большинства заболеваний, связанных с возрастом (в том числе при ВМД) существенную роль играет окислительный стресс. Что означает термин «окислительный стресс»? Если вам приходилось когда–либо видеть бурое яблоко или ржавый металл, тогда вы встретились с результатом окислительного стресса. В прямом смысле с точки зрения химии процесс окисления означает удаление электронов из атома или молекулы. В связи с тем, что кислород довольно легко получает дополнительные электроны от атомов и молекул, окисление относится к процессу связывания молекул с кислородом. Кислород присутствует всюду, но, к счастью, в инертном состоянии. Именно этим можно объяснить тот факт, что воспламеняющиеся материалы, например, дерево, не загораются самопроизвольно. Однако в том случае, если кислород получит дополнительный электрон или дополнительную энергию (так называемый «синглетный кислород»), он становится агрессивным и атакует другие молекулы. В таком случае это явление и называется окислительным стрессом. Данное понятие характеризует окислительное повреждение, протекающее в клетке, в тканях или органах. Поскольку процесс образования энергии происходит непрерывно в клетках нашего организма, то и кислород постоянно взаимодействует с нашими клетками и тканями. По иронии судьбы, кислород является той субстанцией, без которой мы не можем жить, но и которая в большинстве случаев может вызвать повреждение. Процесс метаболизма кислорода способствует образованию его активных, повреждающих форм, получивших название свободных радикалов, которые при взаимодействии с другими молекулами в клетках являются причиной повреждения белков, мембран и генов. В нормальных условиях клетки организма имеют большое число защитных механизмов в форме антиоксидантов и восстанавливающих ферментов, которые успешно защищают клетки от окислительного повреждения, вызванного свободными радикалами. И хотя окислительный стресс действует в течение всей жизни, его результаты особенно ощутимы с возрастом. Полагают, что по мере старения организма происходит истощение его защитных резервов, что проявляется ухудшением физического и интеллектуального здоровья. Сетчатка особенно чувствительна к окислительному стрессу, поскольку она нуждается в большом количестве кислорода, подвергаясь чрезвычайно высокому уровню воздействия света, способного инициировать выработку свободных радикалов, а мембраны клеток содержат большое количество легко окисляемых полиненасыщенных жирных кислот [3,5,14,40].
Активация свободнорадикального окисления вызывает повреждение белков, нуклеиновых кислот, но прежде всего – липидов биологических мембран, которые чрезвычайно легко вовлекаются в цепные свободнорадикальные реакции. Окислительный стресс рассматривается как универсальное звено гибели клеток, которое имеет место при некрозе, апоптозе, токсических повреждениях клетки. В результате нарушения баланса между окислительными и антиоксидантными системами нарушается целостность комплекса фоторецепторов и РПЭ, происходит накопление продуктов распада клеток, липофусциновых гранул и образование друз [26,31].
Снижение центрального зрения при ВМД является результатом перемещения в мембрану Бруха патологического материала, который происходит из РПЭ и накапливается вследствие недостатка устранения его обломков, высвобождающихся в эту область. Друзы состоят из отдельных отложений патологического материала, расположенных между базальной мембраной РПЭ и внутренним коллагеновым слоем мембраны Бруха. Основным компонентом друз является липофусцин [30,36,43]. Утолщение мембраны Бруха дополняется избыточной продукцией основного мембраноподобного материала из РПЭ. Установлено, что липидное содержимое друзы может определять ее последующее клиническое течение.
Другим фактором риска возникновения ВМД является атеросклероз и причины его развития: курение и повышенный уровень артериального давления. В связи с этим значительную роль в развитии ВМД имеют общие и местные сосудистые заболевания, приводящие к ухудшению кровоснабжения и трофических процессов в глазу [1,15,16,51].
Развитие ВМД связано с атеросклеротическими изменениями сосудов хориокапиллярного слоя глазного яблока. Изменения мембраны Бруха и сосудистой оболочки, сопровождающие развитие этого заболевания, выявлены у 75% больных атеросклерозом. Нарушение микроциркуляции в хориокапиллярах, являющихся единственным источником кровоснабжения макулярной зоны, на фоне возрастных изменений в ретинальном пигментном эпителии (РПЭ) и мембране Бруха могут послужить толчком к началу развития дистрофического процесса, а затем влиять и на тяжесть его проявления. При проведении ультразвукового исследования сосудов глаза и орбиты у пациентов с «сухими» формами ВМД обнаружен дефицит кровотока в артериях, осуществляющих кровоснабжение сетчатки. В наших исследованиях у 88,2% пациентов с «сухими» формами ВМД при помощи современных ультразвуковых методов выявлено наличие С– и S–образной патологической извитости брахиоцефальных артерий в сочетании с умеренно выраженными признаками атеросклероза [4].
Кроме того, дефицит витаминов в организме (в особенности витаминов Е и С) также ускоряет развитие ВМД. Основные правила, установленные для профилактики развития атеросклероза, соответствуют профилактике ВМД: отказ от курения, пища, богатая витаминами, снижение веса, физические упражнения и т.д. В связи с тем, что влияние света играет значительную роль в патогенезе ВМД, рекомендуют ношение солнцезащитных очков высокого качества, которые абсорбируют голубой свет, в особенности при нахождении на море, вблизи воды, снега и в горах [10,46,52].
Лечение возрастной макулярной дегенерации
Специфического лечения «сухих» форм ВМД не существует. Среди соединений, способных защитить сетчатку от окислительного стресса и развития ВМД, особую роль в последнее время отводят каротиноидам – лютеину и зеаксантину, которые являются широко распространенными природными пигментами [41,52].
Каротиноиды
Около 50 каротиноидов обнаружены в желто–оранжевых фруктах и темно–зеленых овощах. Человек не способен синтезировать каротиноиды, поэтому их поступление в организм напрямую связано с питанием. Плазма человека в значительных количествах содержит 6 каротиноидов: a– и b–каротин (из моркови), b–криптоксантин (из цитрусов), ликопен (из томатов), лютеин (из шпината) и зеаксантин (из кукурузы). Только лютеин и зеаксантин транспортируются в сетчатку, где они формируют желтый макулярный пигмент или макулярный ксантофилл.
Распределение в сетчатке
Желтый пигмент макулы находится в центре сетчатки, по окружности радиусом 2–3 мм от так называемого желтого пятна макулы. Наибольшее его содержание определяется в самой макуле, где желтый пигмент виден при офтальмоскопии. Концентрация желтого пигмента уменьшается по мере удаления от центра сетчатки. Несмотря на то, что на расстоянии 1,5 мм от центра макулы желтый пигмент практически неразличим, методы тонкого химического анализа позволяют обнаруживать каротиноиды даже на крайней периферии сетчатки. Качественный состав желтого пигмента также меняется по мере удаления от центра макулы. В центре содержится больше зеаксантина, чем лютеина. По мере удаления от центральной зоны концентрация зеаксантина снижается быстрее по сравнению с лютеином, и на периферии основным каротиноидом является лютеин, а зеаксантин доминирует в центре. По данным гистологического исследования макулярные пигменты расположены в слое волокон Генле или аксонов фоторецепторов. В результате свет, прежде чем попадает на светочувствительный наружный сегмент фоторецепторов, сначала проходит через желтый пигмент. Таким образом, макулярный пигмент осуществляет функцию внутриглазного и пререцепторного ультрафиолетового фильтра. Лютеин и зеаксантин располагаются не только перед фоторецепторами в качестве пассивного оптического фильтра. Они обнаружены, хотя и в меньших концентрациях, в наружном сегменте фоторецепторов.
Влияние лютеина на зрительные функции
у пациентов, страдающих ВМД
Известно, что лютеинсодержащие препараты являются средством для повышения плотности макулярного пигмента, и соответственно, возможности предупредить развитие патологических изменений в центральной зоне сетчатки [9,33]. Увеличение плотности макулярного пигмента в зависимости от приема лютеинсодержащих витаминно–минеральных комплексов было подтверждено несколькими исследованиями. Лютеин осуществляет антиоксидантную защиту, выполняет функцию светофильтра, поглощая до 40% коротковолнового синего излучения, таким образом предохраняя пигментный эпителий от светового повреждения. Значительное повышение плотности макулярного пигмента (приблизительно на 5% в течение четырех недель) может быть достигнуто посредством приема лютеина в виде добавок или с пищей.
В клинической практике проводились исследования, доказывающие положительное влияние лютеина на остроту зрения, улучшение показателей световой чувствительности и ахроматической пространственной on/off колбочковой чувствительности, положительную динамику показателей биоэлектрической активности нейронов макулярной зоны сетчатки по данным макулярной электроретинографии, а также стабилизацию и улучшение биоморфометрических показателей центральной зоны сетчатки по результатам оптической когерентной томографии и компьютерной ретинальной томографии.
Огромное значение имеет применение лютеина с целью профилактики развития ВМД. Прием 6 мг лютеина ежедневно уменьшает риск дегенерации макулы на 43%.
Влияние антоцианозидов на зрительные функции
и глазной кровоток у пациентов с ВМД
Одним из направлений лечения дистрофических заболеваний сетчатки является применение лекарственных препаратов, получаемых из растительного сырья, которые содержат различные биофлаваноиды и антоцианозиды. Довольно длительное время с этой целью использовали препараты из плодов черники. В 80–е годы прошлого столетия ученые после множества экспериментов установили, что основными действующими веществами черники являются антоцианозиды. Антоцианозиды и флавоноиды обладают противовоспалительным и антиоксидантным действием, укрепляют стенку сосудов, снижают проницаемость биологических барьеров, положительно влияют на репаративные процессы, регулируют биосинтез коллагена, способствуют восстановлению окисленного родопсина и улучшению трофики сетчатки за счет коррекции микроциркуляции, транскапиллярного обмена и восстановления тканевых механизмов защиты [2,5,45].
Клинические исследования показали, что использование препаратов черники способствует улучшению зрительных функций у больных с поражением сетчатки различного генеза. В последние годы в офтальмологической практике успешно используют препарат Стрикс® внутрь по 1 капсуле 2 раза в сутки в течение 1–2 месяцев. Шульга И.В. и Калинина О.В. (2003) после курса медикаментозной терапии с использованием препарата Стрикс® наблюдали статистически достоверное повышение остроты зрения (в среднем на 0,1 или 18,8 % от исходного уровня) у 50% пациентов с ВМД. В исследовании J. Lee и соавт. (1995) было показано, что применение высоких доз очищенных олигомеров антоцианозидов способствует повышению контрастной чувствительности зрительного анализатора. В нашем клиническом исследовании с применением препарата Стрикс® у пациентов с ранними проявлениями ВМД через 2 месяца после лечения наблюдалось достоверное улучшение остроты зрения, увеличение амплитуды а– и b–волн макулярной электроретинографии, увеличение показателей скорости кровотока в глазной артерии, центральной артерии сетчатки, задних коротких цилиарных артериях. Положительная динамика показателей скорости кровотока в глазных артериях при применении препарата Стрикс® свидетельствует об улучшении кровоснабжения оболочек глаза, что является благоприятным признаком для прогноза заболевания. Таким образом, в нашем исследовании была показана необходимость включения в схему патогенетической терапии ранних проявлений ВМД препаратов, содержащих антоцианозиды, которые улучшают кровоток в сосудах глаза.
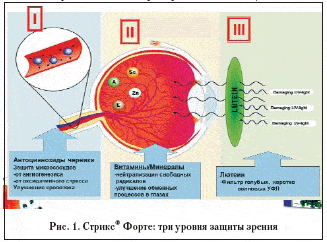
Применение лютеин– и антоцианозидсодержащих препаратов способствует уменьшению риска возникновения возрастной макулярной дегенерации и препятствует прогрессированию этого заболевания. В настоящее время доказана эффективность препаратов лютеина и антоцианозидов в лечении ВМД. Назначение этих препаратов при начальных проявлениях ВМД или возрастной макулопатии способствует положительной динамике зрительных функций, улучшению гемодинамики глаза, длительной стабилизации дистрофического процесса макулярной области, что позволяет рекомендовать их для широкого применения в офтальмологической практике. В настоящее время в клинической практике успешно используют антиоксидантные комплексы, включающие каротиноиды и антоцианозиды. К таким антиоксидантным комплексам относится Стрикс® Форте (рис. 1), в состав которого входят:
– Экстракт черники – 102,6 мг, что соответствует 20 мг антоцианозидов;
– Лютеин – 3 мг;
– Витамин Е – 5 мг;
– Витамин А – 400 мкг;
– Цинк – 7,5 мг;
– Селен – 25 мкг.
Медикаментозное лечение, включающее каротиноиды и антоцианозиды, рекомендуют проводить пациентам, страдающим возрастной макулярной дегенерацией в течение всего периода жизни.
Методы лечения «влажных» форм
возрастной макулярной дегенерации
При «влажных» формах ВМД осуществляют попытку деструкции новообразованных сосудов с помощью лазера. Эти сосуды действительно исчезают после лазерного воздействия [27].
Однако не следует расценивать данный метод, как самый лучший, поскольку: a) при любом лазерном воздействии здоровые ткани также подвергаются разрушению и б) отсутствует влияние на основную причину ВМД.
В последние годы лазерное лечение достигло значительного прогресса с появлением фотодинамической терапии. Выполнение этой лечебной манипуляции связано с внутривенным введением фотосенсибилизатора, который первично адгезируется на стенках новообразованных и патологических сосудов и, в минимальной степени, на стенках здоровых сосудов. Активация фотосенсибилизатора с помощью нетермального лазерного воздействия приводит к биохимической реакции, вследствие которой происходит закрытие и, в конце концов, разрушение «маркированных» новообразованных сосудов. В дальнейшем в большинстве случаев необходимо частое проведение детального обследования пациента и повторное лечение, потому что причины заболевания не устранены. Фотодинамическая терапия повысила шансы и, в действительности, остается способом лечения, который оказывает существенную пользу и благоприятное воздействие на длительное время.
К другим методам лечения новообразованных сосудов относится их хирургическое удаление или полное отслоение сетчатки, ее ротация и фиксация в позиции, которая создает контакт макулы с неповрежденным сегментом пигментного эпителия. Однако такой вид лечения возможен лишь в очень небольшом числе случаев, к тому же исход операции пока предсказать невозможно.
При исследовании влажной формы ВМД в нашем организме было обнаружено химическое вещество, критический уровень которого является причиной роста аномальных кровеносных сосудов под сетчаткой. Это вещество назвали фактором роста сосудистого эндотелия, или vascular endothelial growth factor (VEGF). Недавно ученым удалось синтезировать новые лекарственные препараты, способные блокировать образование VEGF (так называемые анти–VEGF). Эти препараты позволяют уменьшить рост аномальных кровеносных сосудов, снижают их проницаемость и способствуют замедлению потери зрения. В связи с этим анти–VEGF особенно полезны при лечении экссудативной формы ВМД. Эти препараты являются шагом вперед в лечении «влажной» ВМД, потому что они действуют на основную причину роста патологических сосудов. К анти–VEGF отнесятся ранибизумаб (Ranibizumab), пегаптаниб (Pegaptanib), и анекортав (Anecortave). Ранибизумаб и пегаптаниб блокируют специфические VEGF– рецепторы и препятствуют активации VEGF.
Офтальмологи часто используют инъекции кортикостероидов в сочетании с фотодинамической терапией с целью уменьшения персистенции или роста патологических сосудов. Один из главных побочных эффектов стероидов – возможность повышения внутриглазного давления. В данном случае пациентам, получающим стероидную терапию, рекомендуют проводить мониторинг внутриглазного давления. Для внутриглазных инъекций анти–VEGF используют тонкую инъекционную иглу. Процедура осуществляется с соблюдением мер асептики под местной анестезией. Обычно курс лечения требует проведения неоднократных инъекций и длится много месяцев. Как и при других методах лечения, существует определенный риск возникновения осложнений. Большинство осложнений связаны непосредственно с инъекцией и угрозой повреждения глазного яблока или инфицирования.
Для многих пациентов с ВМД наиболее сложной проблемой является адаптация к условиям жизни с пониженным зрением. Однако путем тренировки сохраненного периферического зрения и адаптации к окружающей среде, а также благодаря использованию вспомогательных средств (специальных очков) пациенты с ВМД имеют возможность продолжать их привычный образ жизни. Необходимо также участие специализированного медперсонала и экспертов по реабилитации зрения, которые непосредственно работают со слабовидящими пациентами. Эти специалисты могут помочь пациентам научиться использовать остаточное зрение и выполнять ежедневные задачи. Специальные очки для слабовидящих помогают частично восстановить возможность чтения пациентам с развитой стадией ВМД (по крайней мере, некоторые документы и тексты).
Реабилитацией низкого зрения занимаются такие специалисты, как оптометристы или офтальмологи, имеющие навыки обследования и лечения пациентов с нарушением зрения, которые обучают больных двигаться и ориентироваться в пространстве в условиях низкого зрения.
Таким образом, поиск эффективных способов лечения ВМД продолжается. Огромное внимание в последние годы уделяется разработке новых методов генной терапии.
Статья принята в печать 10 мая 2007 г.
Литература
1. Абдулаева Э.А. Патогенетичкое лечение центральной инволюционной хориоретинальной дистрофии: Автореф. Дис.... канд. мед. наук. – Уфа,2002, 21с.
2. Гваришвили Е.П. Применение метода фармакофизического воздействия при лечении хориоретинальных дистрофий: Автореф. Дис....канд.мед.наук. – Москва, 1999, 25с.
3. Зенков Н.К., Ланкин В.З., Меньщикова Е.Б. Окислительный стресс. – М., 2001. – 315c.
4. Киселева Т.Н., Лагутина Ю.М., Кравчук Е.А. Роль вазоактивных препаратов в терапии неэкссудативной возрастной макулярной дегенерации// Рефракционная хирургия и офтальмология. – 2006. – Т. 6, №2. – C.41–45.
5. Кравчук Е.А. Роль свободнорадикального окисления в патогенезе заболеваний глаз// Вестник офтальмологии. – 2004. –Т. 120,№5. – С.48–51.
6. Либман Е.С., Шахова Е.В. Состояние и динамика слепоты и инвалидности вследствие патологии органа зрения в России.–Материалы VII съезда офтальмологов России. – М., 2000. – С.209–214.
7. Миронова Э.М. Роль пигментного эпителия и взаимодействующих с ним структур в патогенезе глазных заболеваний: Автореф. дис. ... докт. биол. наук. – Москва, 1990. – 32с.
8. Можайцев Б.С., Таратухина И.К., Овечкина О.П. О взаимосвязи активности некоторых ферментов с содержанием микроэлементов и липидов с дистрофией желтого пятна // Вестник офтальмологии. – 1978 – № 2– С. 31–34.
9. Морозов В.И., Яковлев А.А. Фармакотерапия глазных болезней: справочник.–М.: Медицина, 2001. – С.239–241.
10. Мухина М.А., Сотникова Е.В., Кутенова О.М. Социальная значимость и актуальность проблемы лечения макулодистрофии.–Материалы VII съезда офтальмологов России .– М., 2000. – С.220.
11. Островский М.А.,Федорович И.Б. Ретиналь как сенсибилизатор фотоповреждения ретинальсодержащих белков сетчатки глаза // Биофизика. – 1994. – Т.39. – С. 13–25.
12. Пономарева Н.В. Хориоидальное микроциркуляторное русло при общей сосудистой патологии. Морфологические аспекты офтальмологии. – М., 1983. – С.83–85.
13. Cелицкая Т.И. Центральная атеросклеротическая хориоретинопатия. Изд. Томского ун–та, Томск., 1985. – 230с.
14. Старостин А.В., Островский М.А., Федорович И.Б., Львов К.М. ЭПР исследование светоиндуцированной агрегации родопсина в фоторецепторной мембране // Биофизика. – 1987. – Т. 32. – С. 624–627.
15. Тартаковская А.И., Александрова Л.М., Степанянц Е.Р. Состояние свертывающей системы крови и антикоагулянтные препараты в комплексном лечении хориоретинальных дистрофий. – Вестник офтальмологии. – 1977. – №1. – с. 74.
16. Шамшинова А.М. Наследственные и врожденные заболевания сетчатки и зрительного нерва.–М.:Медицина, 2001. – С.229–261.
17. Шилкина С.В. Изучение связи дистрофических изменений в сетчатке и некоторых показателей общего состояния организма// Офтальмологич. Журнал. – 1979. Т. 7. – С. 430–433
18. Шлопак Т.В. Особенности липидного обмена у больных атеросклеротической макулодистрофией.– Материалы 5–го Всеросс. съезд офтальмологов. – М.,1982. – с.475–477.
19. Allikmets R., Shroyer N.F., Singh N., et al. Mutation of the Stargardt disease gene (ABCR) in age–related macular degeneration// Science 1997. – Vol. 277. –P. 1805–1807.
20. Barondes M.J., Pagliarini S., Chisholm I.H. et al. Controlled trial of laser photocoagulation of pigment epithelial detachments in the elderly: 4 year review// Br.J.Opthalmol. – 1992. Vol. 76. – P. 5–7.
21. Berkow J.W., Orth D.H., Kelley J.S. Fluorescein Angiography: Techniques and Interrelation (Monograph N5).– 1991. – P.65–93.
22. Brown R. L.,Snow S.D.,Haley T.L. Movement of gating machinery during the activation of rod cyclic nucleotice–gated channels// Biophis.J. – 1998. Vol. 75. – Vol. 825–833.
23. Cherney E.F. Патогенез сосудистой макулодистрофии// Тез.докл. офтальмологического конгресса «Белые ночи», 28–31 мая 2001г. – С.3–5.
24. Dobreanu M., Mody E. Influence of natural antioxidants on in vitro lipoprotein oxidation. // Rom. J. Intern. Med. – 1997. – Jan–Dec. – 35(1–4). – P. 55–62.
25. Evans J., Wormald K. Is the incident of registrable age–related macular degeneration in increasing?// Br. J. Ophthalmol.– 1996. – Vol. 80,№1. – P.9–14.
26. Floyd R.A., Carney J.M. Free radical damage to protein and DNA: mechanisms involved and relevant observations on brain undergoing oxidative stress // Ann. Neurol. – 1992. – Vol.32 Suppl. – P. 22–27.
27. Gass J.D. Choroidal neovascular membranes their visualization and treatment// Trans.Am.Acad. Ophthal. Otolaryng. – 1973. Vol. 77– P. 310–320.
28. Gorin M.B., Sarneso O.C., Paul T.O., et al. The genetics of age–related maculopathy.–Retina Degeneration: Clinical and Laboratory Applications/ Eds. J.G. Hollifild, R.E. Anderson, M.M. Lavial.– New York:Premium Press, 1993.
29. Hanutsaha P., Guyer D. R., Yannuzzi L.A., et al. Indocyanine–green videoangiography of drusen as a possible predictive of exudative maculopathy//Ophthalmology. – 1998. Vol. 105. – Vol. 1632–1636.
30. Holz F.G., Wolfensberger T.J., Piguet B., et al. Bilateral macular druzen in age–related macular degeneration. Prognosis and risk factors// Ophthalmology. – 1994. Vol. 101. – P. 1522–1528.
31. Housset B. Free radicals and respiratory pathology// C.R. Seances Soc.Biol. Fill.– 1994. Vol. 188. – P. 321–333.
32. Hruby K. Die pehandlung seniler degenerativer maculopathien mit etaretinerfolgsassichten und wirtschaftliche gesishtspunkte// Klin. Mbl. Augenheilk.– 1974. – Vol. 165,№1. – P.68–71.
33. Klaver C.C., Wolts R.S., Vingerling J.R., et al.//Arch. Ophthalmol. 1998. – Vol. 116. – Vol. 653–658.
34. Klein R., Davis M.D., Magli V.L., et al. Wisconsin Age–Related Maculopathy Grading System. Madison: Department of Ophthalmology University of Wisconsin School of Medicine, 1991// Ophthalmology. – 1991. – Vol. 98. – P. 1128–1134.
35. Klein R., Rowland M.L. Radial/ethnic differences in age–related maculopathy//Ophthalmology. – 1995. – Vol. 102. – P. 371–381.
36. Klein R., Klein B.E.K., Jensen S.C., Meuer S.M. The five–year incidence and progression of age–related maculopathy. The Beaver Dam Eye Study// Ophthalmology. – 1997. – Vol. 104. – P.7–21.
37. Klein R., Klein B.E.K., Lee K.E., et al. Changes in visual acuity in a population over a 10–year period. The Beaver Dam Study// Ophthalmology.– 2001. – Vol. 108. – Vol. 1757–1766.
38. Klein R., Klein B.E.K., et al. The association of Cataract and Cataract Surgery with the long–term incidence of age–related maculopathy//Arch.Ophthalmol. – 2002. – Vol. 102. – P. 1551–1557.
39. Klein R., Klein B.E.K., Tomany S.C., et al. Ten–year incidence and progression of age–related maculopathy// Ophthalmology. – 2002– Vol.109. –P. 1767–1778.
40. Liles M.R., Newsome D.A., Oliver P.D. Antioxidant enzymes in the aging human retinal pigment epithelium // Archives of Ophthalmology. – 1991. – Vol. 109,№ 9. – P. 503–512.
41. Meyers S.M., Greene T., Gutman F.A. A twin study on age–related macular degeneration// Am. J. Ophthalmol. – 1995. –Vol. 120. – P.757–766.
42. Milam A.H., Curcio C.A., Cidaciyan A.V. et al. Dominant late–outset retinal degeneration with regional variation of sub–retinal pigment epithelium deposits, retinal function and photoreceptor degeneration// Ophthalmology. – 2002. Vol. 107. – P. 2256–2266.
43. Mitcheel P., Swith W., Attebo K., Wang J.J. Prevalence of age–related maculopathy in Australia. The Blue Mountains Eye Study// Ophthalmology.– 1995. Vol. 102. – P.1450–1460.
44. Mylan R., Van–NewKirk J. The prevalence of age–related maculopathy//Arch.Ophthalmol.–1988. Vol. 106– P.192–198.
45. Newsome D.A., Swarts M., Leone N.C. et al. Oral Zinc in macular degeneration// Arch. Ophthalmol.– 1988. Vol.106. –P. 192–198.
46. Perry W.Y., Christine A.C. Perypapillary chorioretinal atrophy: Bruch membrane changes and photoreceptor loss. Ophthalmology. 2002; 107: 334–343.
47. Sarks S.H. Ageing and degeneration in the macular region//Brit.J.Ophthalmol.– 1976. – Vol. 60. – P.324–330.
48. Seddom J.M., Ajani U.A., Mitchel B.D. Familial aggregation of age–related maculapathy// Am. J.Ophthalmol. – 1997. Vol.123.– P.199–204.
49. Sies H. Oxidative stress – from basic research to clinical application // Amer. J. Med. – 1991. – Vol. 91, Suppl.3. – P. 31–38.
50. Smith W., Assin K.J., Klein R., et al. Risk factors for age–related macular degeneration. Pooled findings from three continents//Ophthalmology.– 2001. – Vol. 108. – P. 697–704.
51. Snow K.K., Seddom J.M. Do age–related macular degeneration and cardiovascular disease share common antecedents//Ophthal. Epidemiol. 1999. –Vol. 6. – P 125–143.
52. Sommerburg O., Keunen J. E., Bird A. C. et al. Fruits and vegetables that are sourses for lutein and zeaxanthin: the macular pigment in human eyes. // Brit. J. Ophthalmol. – 1998. – Vol. 82. – P. 907–910.
53. Tso O.M., Shin C.V. Experimental macular edema after lens extraction// Invest.Ophthalmol. – 1977. Vol. 16,№5.– P. 381–392.
54. Vingerling J.R., Dielemans I., Hofman A., et al. The prevalence of age–related maculopathy in the Rotterdam Study// Ophthalmology. – 1995.– Vol. 102. – P. 205–210.
55. Williams R.A., Brady B.L., Thomas R.J. The psychosocial impact of macular degeneration. Arch. Ophthalmol. 1998; 116 (4): 514–520.












