Ключевые слова: нормотензивная глаукома, головка зрительного нерва, классификация нормотензивной глаукомы.
Abstract
Modern approach to the problem of normotensive
glaucoma. Literal review
Egorov E.A., Alyabyeva J.G.
RNIMU named after Pirogov N.I.
Classification of normotensive glaucoma according to optic nerve head condition is discussed in the article. Some modern approaches for the normotensive glaucoma pathogenesis, diagnostics and treatment tactics arehighlighted.
Key words: normotensive glaucoma, optic nerve head, classification of normotensive glaucoma.
Последние 10–15 лет проблеме нормотензивной глаукомы (НГ) уделялось огромное внимание, результатом чего явилось достижение консенсуса по многим спорным вопросам ее патогенеза, диагностики и тактики лечения.
Частота НГ среди пациентов с первичной открытоугольной глаукомой (ПОУГ) составляет, по различным данным, от 10 до 50% и более. Например, в Японии у пациентов в возрасте после 40 лет число случаев НГ в 4 раза превышает число случаев глаукомы высокого давления, составляя 2% населения страны [21, 41]. Также надо отметить, что число случаев глаукомы с внутриглазным давлением (ВГД) в пределах статистически нормального (истинное ВГД до 21–22 мм рт. ст. при измерении стандартными методами) растет с каждым годом в связи с нарастающей миопизацией населения планеты и увеличивающимся числом кераторефракционных операций.
В клинике применяют классификацию НГ по состоянию головки зрительного нерва (ЗН). Клинические формы НГ могут быть подразделены на:
– миопическую (с наиболее высоким риском прогрессии (рис. 1));
– сенильную склеротическую (у лиц старшего возраста с сердечно-сосудистой патологией; отмечается блюдцеобразная экскавация (рис. 2));
– фокальную ишемическую (у пациентов молодого возраста, склонных к вазоспазму (рис. 3));
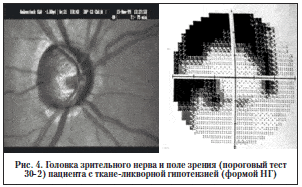
– иные формы (рис. 4).
Также выделяют группу пациентов с подозрением на НГ [21].
Все эти группы различаются по этиологии и прогнозу. Развитие глаукомы в миопических глазах при статистически нормальном ВГД ранее отмечалось отечественными исследователями [3]. Для сенильной склеротической НГ характерны блюдцеобразная экскавация, умеренные изменения полей зрения и медленное прогрессирование нейропатии на раннем этапе. При медленном прогрессировании, отсутствии дефектов поля зрения, близких к точке фиксации, и преклонном возрасте больного возможно наблюдение без назначения гипотензивного режима.
При умеренно выраженной миопии для миопической НГ характерна заметная потеря нейроглиального кольца, при миопии высоких степеней форма головки ЗН резко изменена, отмечается ее бледность. Наблюдаются асимметрия ЗН, характерные глаукоматозные изменения поля зрения: скотомы в носовой части, формирование дугообразной скотомы.
Основная отличительная анамнестическая особенность фокальной ишемической НГ – склонность к вазоспазмам, мигрень. Характерны локальный прорыв нейроглиального кольца, наличие кровоизлияния на головке ЗН (рис. 3). Данная форма НГ чаще встречается у женщин. Различие изменений головки ЗН при НГ и гипертензивной глаукоме – вопрос спорный.
J. Caprioli и G. Spaeth (1985) обнаружили, что при НГ по сравнению с гипертензивной глаукомой наблюдаются более пологие края экскавации и более узкое нейроглиальное кольцо в височной и нижневисочной частях головки ЗН [13]. G. Tezel и соавт. (1996) обследовали большое количество пациентов с НГ, ПОУГ и глазной гипертензией, чтобы определить, существуют ли различия в морфологии головки ЗН между этими группами [45]. Авторы обнаружили в группе НГ более выраженную потерю ткани нейроглиального кольца и обширную зону перипапиллярной атрофии хориоидеи. По их мнению, это может быть связано с относительно поздней диагностикой данного вида глаукомы. Они также отметили высокую частоту кровоизлияний на головке ЗН при НГ по сравнению с остальными группами, эти данные подтверждаются другими авторами. Установлено прогностическое значение кровоизлияний в пользу прогрессирования НГ [29, 42]. Приобретенные ямки головки ЗН, которые, по мнению ряда авторов, являются результатом фокальной атрофии нейроглиального кольца и выглядят как локальные экскавации решетчатой пластинки, наиболее часто встречаются при НГ [25, 39]. В отличие от врожденных ямок ЗН, локализующихся, как правило, в центре или височно, они располагаются в местах наименьшей устойчивости решетчатой пластинки – нижне-височном или верхне-височном секторе (рис. 3). Целесообразно выделить еще глаукоматозные изменения, сочетающиеся с нейроофтальмологической патологией (оптохиазмальный арахноидит в анамнезе; возможно, патология ликвородинамики в сочетании со слабостью решетчатой пластинки) – НГ с ткане-ликворной гипотензией (рис. 4) [6] или НГ на фоне компартмент-синдрома [28]. Улучшение диагностики НГ может быть достигнуто улучшением техники обследования головки ЗН в процессе скрининга, в т.ч. использованием стереофото и гейдельбергской ретинальной томографии.
При НГ имеется несоответствие ВГД, находящегося в пределах статистически нормального, толерантному для данного ЗН. Четкой грани между НГ и глаукомой с повышением давления не существует, вопрос лишь в разном уровне толерантного ВГД.
Условно грань проведена по уровню P0=21 мм рт. ст. Чем ниже толерантное ВГД, тем больше факторов риска, снижающих этот уровень либо степень выраженности этих факторов. Патогенез НГ до конца не изучен. Полагают, что глаукома в своем развитии связана с сосудистыми факторами, в частности ишемией и сосудистым спазмом.
Примечательно, что в одной семье можно наблюдать больных как НГ, так и гипертензивной глаукомой [50]. Наличие НГ у ближайших родственников отмечается в 5–40% случаев НГ [21, 34].
В последние десятилетия получены сведения, утверждающие, что ПОУГ связана с 6 хромосомными областями. Из них мутации генов, кодирующих миоциллин (MYOC gene) и оптиневрин (OPTN gene), обусловливают тип глаукомы. Глаукома, вызванная (disease causing variant (DCV)) мутацией МYОС, относится к так называемой «миоциллиновой глаукоме». В свою очередь, DCV мутация гена MYOC может проявляться и в виде типичной ПОУГ, и как НГ или доброкачественная офтальмогипертензия [22]. Высказаны суждения о том, что геном, ответственным за развитие НГ (преимущественно у лиц европеоидной расы), является оптиневрин (OPTN) [12, 44]. Есть данные об участии в развитии НГ аллели гена, кодирующего аполипопротеин Е, АПОE-e4 – изоформу аполипротеина Е эпсилон 4 (также ассоциированного с большей частотой болезни Альцгеймера). Он отвечает за реакцию нейронов на повреждение формированием b-амилоидных бляшек в ткани головного мозга [48].
Важным является понятие толерантного ВГД: А.М. Водовозов (1991) предложил выделять понятие толерантного ВГД, на которое оказывает влияние состояние сердечно-сосудистой системы [4]. Было показано, что индивидуальный уровень ВГД в здоровой популяции не имеет нормального распределения, а изучаемая выборка состоит из 2 групп лиц: 1-й, для которой характерны низкие цифры ВГД, и 2-й, которая имеет тенденцию к высокой норме ВГД. Доля группы со склонностью к низким значениям ВГД составила 30,8% [1], что близко к частоте НГ по данным европейских и американских авторов.
Совершенно по-новому подошел к изучению роли толерантного давления В.В. Волков (1970), одним из первых обративший внимание на роль нейроофтальмологического фактора при глаукоме, в частности на соотношение внутриглазного, артериального и ликворного давления, им показано значение ткане-ликворной гипотензии в патогенезе НГ [5–7]. Эти данные нашли подтверждение у западных офтальмологов [36].
В настоящее время доминируют взгляды на первичную глаукому как на полиэтиологичное заболевание. По-видимому, в патогенезе НГ и развитии глаукоматозной оптической нейропатии играет роль сочетанное действие различных факторов, которые могут быть подразделены на факторы, не зависящие от ВГД, и факторы, связанные с ВГД. К 1–й группе относятся факторы, влияющие на перфузию головки ЗН [30]: нарушение кровотока, системная гипотензия (в т.ч. ятрогенная), нарушения свертываемости, венозная дисциркуляция и некоторые другие. Особое внимание при НГ уделяется нарушению кровотока в сосудах, питающих ЗН. Развитию НГ могут способствовать наследственные особенности архитектоники решетчатой пластинки [35].
S.M. Drance и соавт. (1973) описывали 2 формы НГ:
– непрогрессирующую, которая обычно связана с преходящим сосудистым нарушением;
– прогрессирующую, являющуюся, как считают, результатом хронической недостаточности кровообращения в головке ЗН.
В настоящее время к НГ относят только прогрессирующую глаукомную оптическую нейропатию [18].
Ганглиозные клетки при глаукоме гибнут из-за повреждения аксонов на уровне ЗН. По-видимому, в патогенезе глаукоматозной нейропатии (как гипертензивной глаукомы, так и НГ) большую роль играет апоптоз – программированная гибель клеток и дефицит, или отсутствие нейротрофинов (в частности, фактора роста, выделенного из головного мозга) и цитокинов (цилиарного нейротрофического фактора). Наиболее важным фактором выживания ганглиозных клеток сетчатки считается BDNF (brain derived nerve factor), выработка которого происходит в верхнем двухолмии (крыша среднего мозга). BDNF поступает к ганглиозным клеткам сетчатки преимущественно с аксональным током, но частично, возможно, с кровотоком и по межоболочечным пространствам ЗН [49].
Известно, что гибель одной ганглиозной клетки, вызванная ишемией и/или блокадой ретроградного аксонального тока (превышение уровня ВГД, толерантного для данного ЗН), приводит к высвобождению возбуждающих нейротрансмиттерных аминокислот, обусловливая вторичную дегенерацию здоровых нейронов, находящихся в непосредственной близости от уже погибших (нейротоксический эффект глутамата). Этим также объясняется прогрессирование глаукомы вне зависимости от достигнутого снижения ВГД. Имеется все больше свидетельств о развитии НГ у пациентов с аутоиммунными заболеваниями. Так, у части пациентов с НГ повышен уровень антифосфатидилсериновых антител, отмечается высокая частота прогрессирующей нейросенсорной тугоухости [31]. Сообщают о нарушении у пациентов с НГ циркадианных ритмов вегетативной нервной системы [27]. К факторам риска НГ относится отягощенная наследственность по глаукоме (особенно родственники первой степени родства, из них более всего – сиблинги) [43]. Кроме того, необходима настороженность при высокой миопии и кераторефракционных операциях [8], а также гемодинамических кризах (эпизоды массивной кровопотери или гипотензивного шока в анамнезе) [17]. Сообщают о более высоком уровне гиперхолестеринемии у пациентов с НГ [51].
С учетом общего кровоснабжения мозга и ЗН был проведен ряд исследований, направленных на уточнение корреляции между ишемией и сосудистой патологией головного мозга и НГ. K. Ong и соавт. (1995) [38] обнаружили более высокую частоту инфарктов головного мозга по данным магнитно-резонансной томографии в группе НГ по сравнению с контрольной группой пациентов соответствующего возраста, в то время как достоверного увеличения частоты патологии сонных артерий в аналогичном исследовании выявлено не было [16, 32]. В то же время есть наблюдения об отсутствии глаукомных изменений головки ЗН или выпадений поля зрения у пациентов с глазной гипертензией и различными билатеральными заболеваниями сонных артерий в сроки наблюдения от 3 до 12 лет [24]. Получены данные о снижении церебрального перфузионного резерва при НГ [10] и наличии церебральной венозной дисциркуляции у преобладающего числа пациентов в группе НГ в отличие от группы гипертензивной глаукомы [11], что подтверждается клинической картиной (наличие кровоизлияний на головке ЗН, как полосчатых, характерных для глаукомы, так и более выраженных). Роль венозной дисциркуляции в развитии НГ широко исследуется в последние годы и находит подтверждение как у западных [20], так и у отечественных офтальмологов [9].
Глубокие дефекты близко к точке фиксации при НГ в поле зрения, учитывая характер изменений порога яркостной чувствительности и времени сенсомоторной реакции при цветовой компьютерной камипиметрии, по-видимому, связаны с феноменом «нищей перфузии» и являются следствием микроинфарктов ткани ЗН на всем протяжении до хиазмы [2]. Таким образом, нарушения глазного и церебрального кровотока играют важную роль в развитии глаукоматозной нейропатии при НГ [37].
Несмотря на то, что НГ, по определению, отличается от гипертензивной глаукомы тем, что у этих пациентов истинное ВГД не регистрировалось выше 21 мм рт. ст., имеется тенденция к повышению и к большим, по сравнению с нормальной популяцией, дневным колебаниям ВГД. При наличии асимметрии ВГД более выраженное нарушение поля зрения характерно для глаза с более высоким давлением. Асимметрия давления между глазами колеблется от 1 до 5 мм рт. ст. [14]. Необходимо снижение ВГД на 30% от исходного, что может быть достигнуто с помощью хирургического лечения, а также назначения гипотензивных капель, комбинации капель с лазерной трабекулопластикой или даже только с применением лазерного метода лечения [40]. Медикаментозным лечением можно ограничиться лишь в том случае, если оно позволяет достигнуть 25–30% снижения ВГД [21, 40].
Критериями диагноза НГ являются истинное ВГД в пределах статистически нормального (до 21 мм рт. ст.), прогрессирующая глаукоматозная экскавация, изменения поля зрения по типу дефекта пучка нервных волокон, открытый угол при гониоскопии, отсутствие в анамнезе глазных заболеваний, сопровождающихся подъемом ВГД [23].
В то же время необходимость наличия прогрессирования заболевания для диагностики спорна, т.к. хотя НГ обычно прогрессирует, изменения могут быть минимальными в течение нескольких лет. Поэтому, учитывая неэтичность ожидания прогрессии, возможна постановка диагноза на основании данных дневной тонометрии и характерных изменений головки ЗН и поля зрения, если исключены другие заболевания, вызывающие аналогичные изменения [26, 33].
При оценке полученных цифр ВГД крайне важен учет рефракции глаза и толщины роговицы. Известно, что у миопов и гиперметропов измерение ВГД по Гольдману не вполне отражает реальные цифры истинного ВГД. Миопия и правильный астигматизм приводят к занижению получаемых цифр. Согласно рекомендациям Европейского глаукомного общества [19], на каждые 3 диоптрии рефракции у миопов необходимо прибавлять 1 мм рт. ст. к данным, полученным при тонометрии по Гольдману. Поправка на правильный астигматизм составляет плюс 1 мм рт. ст. на каждые 4 диоптрии. Показано, что у пациентов с НГ толщина центральной зоны роговицы значительно меньше, а у пациентов с доброкачественной офтальмогипертензией – значительно больше, чем в группе контроля. В связи с этим рекомендуется делать поправку полученных цифр ВГД на толщину роговицы, а также исследовать толщину роговицы у больных глаукомой (наряду с измерением ВГД и оценкой поля зрения) для определения уровня целевого давления [15].
В настоящее время отмечается, что при наличии тонкой роговицы данные, получаемые с помощью стандартных методов тонометрии, занижаются, однако четкая зависимость отсутствует, кроме того, важны биомеханические свойства оболочек глаза. Поэтому при нестандартных роговицах, высокой миопии и кераторефракционных операциях в анамнезе в дополнение к тонометрии по Гольдману показано исследование на контурном динамическом тонометре (Паскаля) и анализаторе биомеханических свойств роговицы.
Неврологическое обследование пациентов с ГНД
При статистически нормальном ВГД необходимо исключить неврологические причины изменения зрительного нерва, любую патологию зрительного анализатора выше глазного яблока. Компьютерная томография и магнитно-резонансная томография являются дорогими исследованиями, поэтому, по мнению части офтальмологов, нет необходимости использовать их в качестве рутинных.
В группе НГ чаще отмечается лишь диффузная ишемическая патология на уровне мелких сосудов головного мозга [16]. D. Kamal и R. Hitchings (1998) рекомендуют направлять пациентов к неврологу для дальнейшего обследования только при отсутствии корреляции между состоянием головки ЗН и изменениями поля зрения [26]. Показанием для направления к неврологу является и наличие бледных ЗН без типичной экскавации или изменения поля зрения, подозрительные на наличие неврологической патологии (например, гомонимные дефекты поля зрения, с четкой границей по срединной линии, с вовлечением центра (точки фиксации), но не парацентральные и/или аркуатные), а также если жалобы пациента не объясняются потерей зрения. Хотя наличие экскавации нехарактерно для патологии зрительного нерва, обусловленной его сдавлением, однако сообщения об этом имеются в литературе [46, 47]. При глаукоме имеется выраженное соответствие объема экскавации и дефекта поля зрения. Если атрофия головки ЗН более выражена, чем изменения поля зрения, то можно предполагать наличие передней ишемической нейропатии в анамнезе.
Целями лечения НГ являются:
• снижение ВГД на 30% от исходного с контролем поля зрения пороговой статической компьютерной периметрией для уточнения уровня толерантного ВГД и предотвращения его излишнего снижения;
• достижение стабилизации поля зрения и состояния ЗН;
• выявление и коррекция всех факторов риска прогрессирования глаукомной оптической нейропатии;
• предотвращение инвалидизации (при характерном выпадении поля зрения близко к точке фиксации с выраженным снижением качества жизни в трудоспособном возрасте);
• предотвращение острой сердечно-сосудистой патологии и нарушений мозгового кровообращения у лиц молодого возраста (группа риска) – консультации смежных специалистов [8].
В заключение надо отметить, что прогноз при НГ является благоприятным при раннем выявлении, достижении и поддержании толерантного уровня ВГД, постоянных поддерживающих курсах нейропротекторной терапии, коррекции факторов риска прогрессии глаукомной оптической нейропатии и должной приверженности пациента к лечению.


Литература
1. Алексеев В.Н., Егоров Е.А., Мартынова Е.Б. О распределении уровней внутриглазного давления в нормальной популяции // Клиническая офтальмология. 2001. № 2. С. 38–40.
2. Алябьева Ж.Ю, Серова Н.К., Мусин Р.С, Лаврентьев А.В., Шнайдер Я.Э. Проблема дифференциальной диагностики глаукомы с нормальным давлением с позиции нейроофтальмологии: Материалы V Московской науч.-практ. нейроофтальмол. конф., 26 января 2001 г. М., 2001. С. 59–60.
3. Бару Е. Ф. Клиника и лечение глаукомы, сочетающейся с миопией: Дис. ... канд. мед. наук. М., 1986. 172 с.
4. Водовозов A.M. Толерантное и интолерантное внутриглазное давление при глаукоме. Волгоград, 1991. 160 с.
5. Волков В.В. О так называемой псевдоглаукоме и ее отношении к первичной глаукоме: Тез. докл. на 2-й зональной науч.-практич. конф. офтальмологов Дальнего Востока. Владивосток, 1970. С. 129–130.
6. Волков В.В. Глаукома при псевдонормальном давлении. М.: Медицина, 2001. 352 с.
7. Волков В.В., Сухинина Л.Б., Устинова Е.Н. Глаукома, преглаукома, офтальмогипертензия. Л.: Медицина, 1985. 215 с.
8. Егоров Е.А., Алябьева Ж.Ю. Глаукома нормального давления / Глаукома. Национальное руководство. М.: ГЭОТАР-Медиа, 2012. С. 292–321.
9. Курышева Н.И., Киселева Т.Н., Иртегова Е.Ю. Сравнительная характеристика показателей глазного кровотока при глаукоме нормального давления и первичной глаукоме с повышенным офтальмотонусом: Сб. науч. тр. 11-й Всерос. школы офтальмолога.– М., 2012. С. 89–92.
10. Нестеров А.П., Алябьева Ж.Ю., Лаврентьев А.В. Глаукома нормального давления: гипотеза патогенеза // Вестник офтальмологии. 2003. Т. 119. № 1. C. 3–6.
11. Нестеров А.П., Алябьева Ж.Ю., Шумилина М.В., Бузиашвили Ю.И. Значение венозной патологии в генезе глаукомной оптической нейропатии при нормотензивной глаукоме у лиц пожилого возраста // Клиническая геронтология. 2005. Т. 11 (12). С. 77–80.
12. Alward W.L., Kwon Y.H., Kawase K. et al. Evaluation of optineurin sequence variations in 1,048 patients with open-angle glaucoma // Am. J. Ophthalmol. 2003. Vol. 136. No. 5. P. 904–910.
13. Caprioli J., Spaeth G.L. Comparison of visual fields defects in the low-tension glaucoma with those in high-tension glaucomas // Am. J. Ophthalmol. 1984. Vol. 97. P. 730–737.
14. Cartwright M.J., Anderson D.R. Correlation of asymmetric damage with asymmetric intraocular pressure in normal-tension glaucoma (low-tension glaucoma) // Arch. Ophthalmol. 1988. Vol. 106. P. 898–900.
15. Dave H., Kutschan A., Pauer A., Wiegand W. Measurement of corneal thickness in glaucoma patients // Ophthalmologe. 2004. Vol. 101. No. 9. Р. 919–924.
16. Demailly P., Cambert F., Plouin F. Do patients with low tension glaucoma have particular cardiovascular characteristics? // Surv. Ophthalmol. 1994. Vol. 38. P. 65–75.
17. Drance S.M., Sweeney V.P, Morgan R.W., Feldman F. Studies of factors involved in the production of low-tension glaucoma // Arch. Ophthalmol. 1973. Vol. 89. P. 457–465.
18. Drance S.M., Sweeney V.P, Morgan R.W. Shock-induced optic neuropathy: a cause of nonprogressive glaucoma // N. Engl. J. Med. 1973. Vol. 288 (8). P. 392–395.
19. European Glaucoma Society // Terminology and Guidelines for Glaucoma. Savona: Dogma, 1998. 120 p.
20. Flammer J., Konieczka K., A. Flammer J. The role of ocular blood flow in the pathogenesis of glaucomatous damage // US Ophthalmic Review. Vol. 4 (2). P. 84–87.
21. Geijssen H.C. Studies on normal pressure glaucoma. Amsterdam: Kugler, 1991. 240 p.
22. Gong G., Kosoko-Lasaki O., Haynatzki G.R., Wilson M.R. Genetic dissection of myocilin glaucoma // Hum. Mol. Genet. 2004. Suppl. 1. Р. 91–102.
23. Hitchings R. http://medtextfree.wordpress.com/2011/04/05/chapter-221-normal-tension-glaucoma.
24. Jampol L.M., Miller N.R. Carotid artery disease and glaucoma // Brit. J. Ophthalmol. 1978. Vol. 62. P. 324–326.
25. Javit J.C., Spaeth G.L., Katz L.J. et al. Acquired pits of the optic nerve: increased prevalence in patients with low tension glaucoma // Ophthalmology. 1990. Vol. 97. P. 1038–1043.
26. Kamal D., Hitchings R. Normal tension glaucoma- a practical approach // Br. J. Ophthalmol. 1998. Vol. 82. No. 7. P. 835–840.
27. Kashiwagi K., Tsumura T., Ishii H. et al. Circadian rhythm of autonomic nervous function in patients with normal-tension glaucoma compared with normal subjects using ambulatory electrocardiography // J. Glaucoma. 2000. Vol. 9. No. 3. P. 239–246.
28. Killer H.E., Jaggi G.P., Flammer J., Miller N.R. Is open-angle glaucoma caused by impaired cerebrospinal fluid circulation: around the optic nerve? // Clin. Exp. Ophthalmol. 2008. Vol. 36. P. 308–311.
29. Kitazawa Y., Shirato S., Yamamoto T. Optic disc hemorrhage in low-tension glaucoma // Ophthalmology. 1986. Vol. 93 (6). P. 853–837.
30. Klaver J.H.J., Greve E.L., Goslinga H. et al. Blood and plasma viscosity measurements in patients with glaucoma // Br. J. Ophthalmol. 1985. Vol. 69. P. 765.
31. Kremmer S., Kreuzfelder E., Bachor E. et al. Coincidence of normal tension glaucoma, progressive sensorineural hearing loss, and elevated antiphosphatidylserine antibodies // Br. J. Ophthalmol. 2004. Vol. 88. No.10. P. 1259–1262.
32. Levene R. Low tension glaucoma: a critical review and new material // Surv. Ophthalmol. 1980. Vol. 61. P. 621–624.
33. Meier-Gibbons F., Sturmer J., Gloor B. Normal pressure glaucoma: a diagnostic challenge // Klin. Mbl. Augenheilkl. 1995. Vol. 206. No. 3. P. 157–160.
34. Miglior M. Low critical tension glaucoma: present problems // Glaucoma. 1987. No. 9. P. 77.
35. Miller K.M., Quigley H.A. Comparison of optic disc features in low tension and typical open angle glaucoma // Ophthalmic. Surg. 1987. Vol. 18. P. 882–889.
36. Morgan W.H. et al. The influence of cerebrospinal fluid pressure on the lamina cribrosa tissue pressure gradient // Invest. Ophthalmol. Vis. Sci. 1995. Vol. 36. No. 6. P. 1163–1172.
37. Mozaffarieh M., Flammer J. Ocular Blood Flow and Glaucomatous Optic Neuropathy. Springer-Verlag Berlin Heidelberg, 2009. P. 117.
38. Ong K., Farinelli A., Billson F. et al. Comparative study of brain magnetic resonance findings in patients with low tension glaucoma and control subjects // Ophthalmology. 1995. Vol. 102. P. 1632–1638.
39. Radius R.L., Maumenee A.E., Green W.R. Pit-like changes of the optic nerve head in open angle glaucoma // Br. J. Ophthalmol. 1978. Vol. 62. P. 389–393.
40. Schulzer M. The Normal Tension Glaucoma Study Group. Intraocular pressure reduction in normal tension glaucoma // Ophthalmology. 1992. Vol. 99. P. 1468–1470.
41. Shiose Y., Kitazawa Y., Tsukahara S. et al. Epidemiology of glaucoma in Japan - a nationwide glaucoma survey // Jpn. J. Ophthalmol. 1991. Vol. 35. P. 135–155.
42. Siegner S.W., Netland P.A. Optic disc haemorrhages and progression of glaucoma // Ophthalmology. 1996. Vol. 103. P. 1014–1024.
43. Sung V.C.T., Koppens J.M., Vernon S.A. et al. Longitudinal glaucoma screening for siblings of patients with primary open angle glaucoma: the Nottingham Family Glaucoma Screening Study // Br J Ophthalmol. 2006. Vol. 90 (1). P. 59–63.
44. Tang S., Toda Y., Kashiwagi K. et al. The association between Japanese primary open-angle glaucoma and normal tension glaucoma patients and the optineurin gene // Hum. Genet. 2003. Vol. 113. No. 3. P. 276–279.
45. Tezel G., Kass M.A., Kolker A.E. et al. Comparative optic disc analysis in normal pressure glaucoma, primary open angle glaucoma, and ocular hypertension // Ophthalmology. 1996. Vol. 103. P. 2105–2113.
46. Trobe J.D., Glaser J.S., Cassidy J.C. Optic atrophy, differential diagnosis by fundus examination alone // Arch. Ophthalmol. 1980. Vol. 98. P. 1040–1045.
47. Trobe J.D., Glaser J.S., Cassidy J. et al. Non-glaucomatous excavation of the optic disc // Arch. Ophthalmol. 1980. Vol. 98. P. 1046.
48. Vickers J.C., Craig J.E., Stankovich J. еt al. The apolipoprotein epsilon4 gene is associated with elevated risk of normal tension glaucoma // Mol Vis. 2002. Oct 14. Vol. 8. P. 389–393.
49. Wax M.B., Tezel G., Edward P.D. Clinical and ocular histopathological findings in a patient with normal-pressure glaucoma // Arch. Ophthalmol. 1998. Vol. 116. No. 8. P. 993–1001.
50. Werner E.B. Normal tension glaucoma // In The Glaucomas (R. Ritch, M. B. Shields, Th. Krupin eds). Mosby, St. Louis, 1996. P. 769–797.
51. Winder A.F. Circulating lipoprotein and blood glucose levels in association with low-tension and chronic simple glaucoma // Br. J. Ophthalmol. 1977. Vol. 61. P. 641.












