A.V. Svirin, Yu.I. Kiiko*,
B.V. Obruch, A.V. Bogomolov
Russian State Medical University of Roszdrav,
*FGU VCGPH of Roszdrav, Moscow
Authors discuss principles, diagnostic possibilities and types of new examination method – spectral optic coherent tomography which information value exceeds the OCT’s.
Оптическая когерентная томография (ОКТ) широко используется в современной медицине. Это неинвазивный и высокоточный метод исследования, с помощью которого стало возможным получать изображение поперечного среза исследуемых тканей in vivo. ОКТ была разработана в Массачусетском технологическом университете в конце 80–х годов ХХ века.
ОКТ нашла применение во многих отраслях медицины – в гастроэнтерологии, кардиологии, урологии, дерматологии, стоматологии. Однако наибольшую популярность новая методика завоевала в диагностике заболеваний глаза. Самый известный прибор, реализующий технологию ОКТ в офтальмологии – Stratus OCT (Carl Zeiss Meditec) на данный момент был продан в количестве, превышающем 6 тыс. экземпляров. В мире насчитывается более тысячи статей и научных трудов, посвященных применению ОКТ в диагностике заболеваний глаза.
Принципы метода
Суть ОКТ заключается в измерении времени задержки светового луча, отраженного от исследуемой ткани. Поскольку современное оборудование не позволяет непосредственно измерять этот параметр на столь малых пространственных отрезках, работа ОКТ построена на принципах световой интерферометрии.
До недавнего времени основой всех когерентных томографов был интерферометр Михельсона (time–domain OCT). Источником света в нем является суперлюминесцентный диод, позволяющий получать луч низкой когерентности. С помощью делителя световой пучок расщепляется на две равные части, одна из которых направляется на исследуемую структуру, вторая – на подвижное зеркало (опорное плечо). Исследователь путем смещения рабочей части прибора добивается того, чтобы расстояние до обоих объектов было одинаковым. После этого отраженные лучи суммируются, что вызывает эффект интерференции, регистрируемый фотодетектором. Полученная амплитуда интерферировавшей световой волны характеризует отражающую способность конкретной точки исследуемого объекта. Затем опорное плечо смещается и выполняется исследование следующей точки. В итоге формируется одномерный А–скан (axial scan). Получаемое путем суммирования нескольких А–сканов двухмерное изображение, по аналогии с ультразвуковым исследованием, называется В–сканом. Расстояние между точками А–скана определяет продольное (аксиальное) разрешение, между соседними А–сканами – поперечное.
Основным фактором, ограничивающим возможности Time–domain OCT, является наличие механического элемента системы – подвижного зеркала опорного плеча. От точности и скорости его смещения напрямую зависят аксиальное разрешение и время сканирования. Максимальная продольная разрешающая способность ОКТ, полученная в лабораторных условиях, составляет 2–3 мкм. Этот результат достигнут на неподвижных объектах с использованием в качестве источника света фемтосекундного лазера. Однако коммерческий вариант данной системы не был реализован ввиду ее высокой стоимости.
Максимальная разрешающая способность Time–domain ОКТ в клинике представлена в последней модификации Stratus OCT и составляет 8–10 мкм при скорости сканирования 400 А–сканов в секунду. Стандартное исследование, состоящее из 512 А–сканов, занимает, таким образом, более 1 секунды.
Спектральная ОКТ
Коренной перелом в технологии оптической когерентной томографии произошел с внедрением в практику спектральных интерферометров, использующих преобразование Фурье (spectral/Fourier domain). Их отличием от интерферометра Михельсона является наличие спектрометра и высокоскоростной CCD – камеры (CCD – charge–coupled device, русскоязычный аналог термина – ПЗС (прибор зарядовой связи). Источником света является широкополосный суперлюминесцентный диод, позволяющий получить низкокогерентный луч, содержащий несколько длин волн.
Как и в time–domain OCT, световой импульс делится на две равные части, одна из которых отражается от фиксированного опорного плеча (зеркала), вторая – от исследуемого объекта. Затем сигналы суммируются, а проинтерферировавший луч света раскладывается на составные части спектра, которые одномоментно фиксируются CCD–камерой. Полученный спектр интерференции состоит из совокупности световых волн, отраженных от различных по глубине участков исследуемого объекта. Затем из полученного массива данных путем математического преобразования Фурье выделяются частотные составляющие, из которых формируется А–скан.
Таким образом, получение линейного скана происходит не путем последовательного измерения отражающих свойств каждой отдельной точки пространства, а одномоментно. Глубина сканирования при этом равна зоне когерентности. Подобный принцип исследования позволяет преодолеть ограничивающие факторы, связанные со скоростью и точностью движения механических частей интерферометра, поскольку опорное плечо остается во время исследования неподвижным.
Скорость сканирования спектральных ОКТ зависит от быстроты работы CCD–камеры и математического преобразователя, а аксиальная разрешающая способность – от чувствительности спектрометра. Поперечное разрешение всех типов ОКТ ограничивается аберрациями оптической системы глаза.
Благодаря принципу своей работы, спектральные ОКТ позволяют выполнять более 25 тыс. линейных сканов в секунду, превосходя по этому параметру оптические томографы предыдущего поколения более чем в 60 раз (некоторые модели – в 120 раз). Аксиальная разрешающая способность находится в пределах 3–8 мкм, поперечная – 10–15 мкм.
К моменту написания статьи на мировом рынке было представлено 5 моделей спектральных оптических когерентных томографов c возможностью исследования заднего отрезка глаза:
1) RTVue–100 фирмы Optovue (США) – позволил совместить в одном приборе возможности исследования как переднего, так и заднего отрезка глазного яблока;
2) 3D OCT–1000 (Topcon) – обладает функциями фундус–камеры и сопоставления фотоснимка глазного дна с ОКТ изображением;
3) CIRRUS HD OCT (Carl Zeiss);
4) Soct Copernicus и Soct Copernicus HR совместного производства Reichert (США) – Optopol (Польша). Soct Copernicus HR обладает на сегодняшний день максимальной заявленной скоростью сканирования (55000 А–сканов в секунду) и аксиальным разрешением (3 мкм). Также под маркой Soct разработан спектральный ОКТ для исследования переднего отрезка глаза;
5) Spectralis HRA+OCT (Heidelberg Engineering) – ОКТ–приставка к лазерному сканирующему ангиографу HRA.
Первым коммерческим прибором, в котором были реализованы возможности спектральной ОКТ глаза, стал RTVu–100 фирмы Optovue (США). Компания объявила о начале его производства в конце 2006 г. Именно этот прибор мы используем в работе нашей клиники, поэтому в дальнейшем основные технические характеристики и протоколы обследования приводятся исходя из возможностей RTVu–100.
Улучшенные диагностические возможности
Значительный прирост скорости и точности метода качественно изменил роль оптической когерентной томографии в диагностике заболеваний глаза. Чтобы понять всю значимость этих изменений, рассмотрим спектральную ОКТ с точки зрения ее клинического применения.
Одной из самых главных проблем, возникающих при использовании томографов предыдущего поколения, является чувствительность метода к микродвижениям глазного яблока. Наибольшие погрешности вызывают так называемые микросаккады – непроизвольные быстрые движения с амплитудой 2–10 угловых мин и интервалом от 100 мс. Одно стандартное исследование на Stratus OCT (512 А–сканов) длится 1,28 сек. – за это время глазное яблоко 10–14 раз меняет свое положение. Подобный эффект негативно сказывается на конечной томограмме. Для нейтрализации появляющихся артефактов применяются методы графического сглаживания. Они эффективно выравнивают изображение, но могут скрывать локальные изменения, что вносит дополнительные затруднения в интерпретацию результатов.
Спектральные когерентные томографы в отличие от time–domain OCT позволяют получить стандартный линейный профиль (1024 А–сканов) в среднем за 0,04 сек. За этот промежуток времени глазное яблоко не успевает совершить значимых движений, а значит, конечный В–скан максимально соответствует истинной структуре изучаемого объекта.
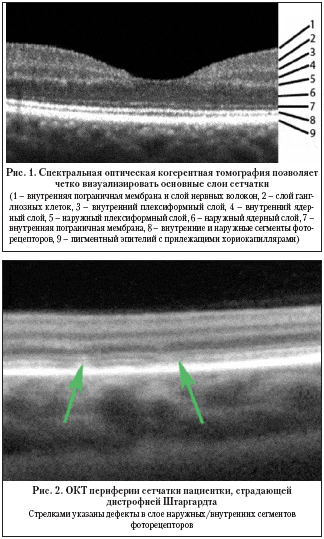
Высокое разрешение позволяет четко идентифицировать все слои сетчатки и внутренние слои сосудистой оболочки. Диагностический поиск производится на уровне отдельных структур и групп клеток (рис. 1). Четкая визуализация комплекса «пигментный эпителий – слой фоторецепторов – наружная пограничная мембрана» способствует раннему выявлению ретино–хориоидальной патологии. В качестве примера на рисунке 2 представлена ОКТ периферической зоны сетчатки пациента, страдающего дистрофией Штаргардта. Высокая разрешающая способность метода позволяет выявить патологические изменения в слое наружных сегментов фоторецепторов.
Трехмерная визуализация
Однако главным отличием спектральных ОКТ стала возможность трехмерной визуализации объекта (участок сетчатки, головка зрительного нерва, роговица и проч.). Высокая скорость сканирования позволяет выполнить большое количество А–сканов (более 50 000) участка ткани фиксированной площади за 1–2 с. На основе этих данных программное обеспечение восстанавливает трехмерную структуру объекта.
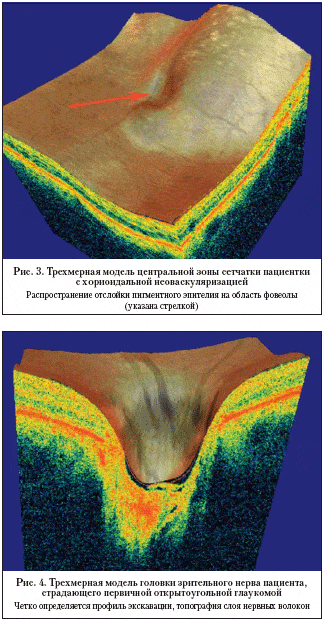
Полученное 3D–изображение позволяет оценить профиль поверхности изучаемой структуры, ее внутреннюю топографию. Возможна четкая визуализация границ патологических образований, наблюдение за их динамикой. Также эта функция незаменима в поиске небольших по размерам изменений, вероятность попадания которых в одиночный линейный скан мала. На рисунке 3 продемонстрирована трехмерная структура центральной зоны сетчатки пациентки с хориоидальной неоваскуляризацией. 3D–томограмма позволяет оценить вовлеченность фовеолы в патологический процесс и проследить динамику изменений.
Трехмерная модель головки зрительного нерва (ГЗН) открывает новые возможности в оценке профиля экскавации при глаукоме (рис. 4). RTVu–100 позволяет выполнять морфометрию ГЗН, сходную по структуре получаемых данных с HRT. При этом определение границ диска зрительного нерва производится на основе 3D–изображения, что позволяет наносить его контур, основываясь на структурных особенностях ГЗН.
Функции картирования
Возможность исследования толщины сетчатки и ее слоев на определенном участке впервые была реализована в Stratus OCT. Итогом выполнения стандартного протокола является карта, представляющая полученные результаты графически и в абсолютных значениях. Методы картирования нашли широкое применение как в практической, так и в научно–исследовательской работе.
Спектральная оптическая томография предоставляет новые возможности построения карт глазных структур. Прежде всего высокая скорость сканирования повышает их точность, поскольку на единицу площади приходится большее количество А–сканов. Кроме того, выполнение стандартного протокола исследования занимает не более 1 с, следовательно, движения глазного яблока оказывают минимальное воздействие на конечный результат.
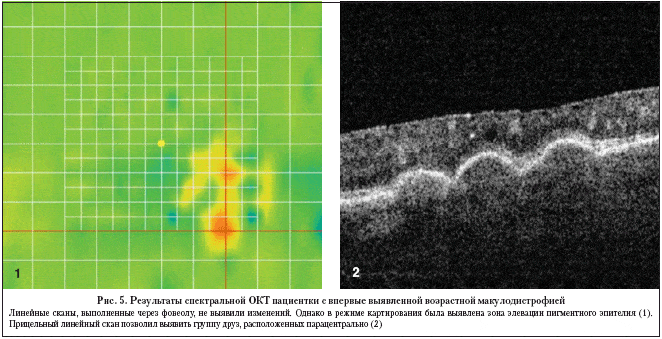
Высокая разрешающая способность позволяет четко идентифицировать границы между слоями сетчатки в автоматическом режиме. В результате становится возможным получать не только карту толщины сетчатки, но и ее отдельных слоев (слой ганглиозных клеток и нервных волокон, фоторецепторных клеток, пигментного эпителия). На рисунке 5–1 представлена карта элевации пигментного эпителия сетчатки пациентки с впервые диагностированной ВМД. Линейные сканы центральной зоны сетчатки не выявили патологических изменений. Однако методом картирования парацентрально были обнаружены участки локальной элевации пигментнго эпителия. Линейный скан, выполненный прицельно, позволил выявить расположенные на периферии друзы (рис. 5–2).
Карта толщины слоя нервных волокон и ганглиозных клеток сетчатки расширяет возможности прибора в диагностике атрофий зрительного нерва, в том числе глаукомного генеза. Можно провести параллель в структуре получаемых результатов с поляриметрическими методами (хотя в последних определяется только толщина слоя нервных волокон без учета слоя ганглиозных клеток).
Заключение
К сожалению, в рамках одной статьи невозможно описать все новые возможности, которые предоставляет исследователю спектральная оптическая когерентная томография. Еще предстоит выработать комплекс диагностических критериев для основных групп заболеваний заднего отрезка глаза, оценить точность получаемых результатов относительно приборов, использующих другие физические принципы (сканирующие лазерные офтальмоскопы, лазерные поляриметры и т.п.).
Однако уже сейчас можно утверждать, что спектральная оптическая когерентная томография является качественно новым методом диагностики заболеваний глаз. Ее информативность значительно превосходит ОКТ предыдущего поколения за счет возросшей разрешающей способности и высокой скорости исследования. Метод позволяет получить исчерпывающее представление об ультраструктуре произвольного участка сетчатки и головки зрительного нерва. Разнонаправленность получаемых результатов, широкие возможности диагностики и динамического наблюдения различных глазных заболеваний делают спектральную оптическую когерентную томографию одним из наиболее точных и универсальных методов морфологического исследования в офтальмологии.