В последнее десятилетие ОКТ играет все более важную роль в ведении пациентов с глаукомой. Измерение толщины внутреннего слоя сетчатки в области макулы (ганглионарных клеток сетчатки (ГКС)) и толщины перипапиллярного СНВС с помощью приборов ОКТ, работа которых основана на принципах преобразования Фурье, в настоящее время признано высокоточным методом, способным выявлять начальные признаки глаукомы или ее прогрессирование [1–12]. Однако наличие у пациента катаракты может снизить точность измерений, поскольку при этом уменьшается соотношение сигнал/шум [13–17] и возрастает вероятность ошибок сегментации изображения, что, в свою очередь, может привести к ошибочной оценке глаукомного процесса. Установлено, что после неосложненной операции экстракции катаракты с имплантацией интраокулярной линзы (ИОЛ) сила ОКТ-сигнала и соотношение сигнал/шум увеличивались в сравнении с предоперационными величинами. Это может привести к получению более высоких значений толщины сетчатки после операции [14, 16, 17], хотя при неосложненной факоэмульсификации и так в первые несколько недель происходит увеличение толщины сетчатки в макуле из-за клинически незначимого транзиторного макулярного отека [18–21].
RTVue-100 OКT (RTVue OКT) – это один из оптических когерентных томографов, основанных на принципах преобразования Фурье [3, 11, 22]. В наше распоряжение разработчики предоставили новую версию ПО – 6.12, в настоящее время недоступную для коммерческого использования. В сравнении с предыдущей (6.3) в данной версии улучшилось качество сегментации изображений, а также особое внимание уделяется протоколу оценки глаукомных поражений. В недавно проведенном нами исследовании было убедительно доказано, что новое ПО позволяет значительно повысить качество исследования ГКС на примере пациентов с макулярными друзами и субретинальной неоваскулярной мембраной при сравнении с версией 6.3 [24]. Целью нашего нового исследования является определение преимуществ новой версии ПО в ситуациях, когда снижается соотношение сигнал/шум из-за наличия у пациента катаракты. Сканы толщины СНВС и комплекса ГКС были получены с помощью версии 6.3 непосредственно перед операцией и через 1 мес. после неосложненной факоэмульсификации с имплантацией ИОЛ и затем проанализированы с участием обеих версий ПО (6.3 и 6.12). Нашей основной задачей было установить, будут ли различия в значениях параметров, чувствительных к ошибкам сегментации (параметры толщины комплекса ГКС), в до- и послеоперационном периодах, а также разницу в значениях, получаемых при обработке изображений 2-мя версиями ПО.
Материал и методы
Участники исследования
Протокол исследования был одобрен этической комиссией по клиническим испытаниям Университета Земмельвейс (Будапешт, Венгрия). Перед включением в наш эксперимент все пациенты подписали информированное согласие. В ходе этой работы были соблюдены все действующие институциональные и правительственные нормативные акты, касающиеся этического использования добровольцев. В исследовании приняли участие белые европеоиды, которые поступили в офтальмологическое отделение Университета Земмельвейс для проведения факоэмульсификации начальной катаракты. У каждого пациента обследовался только один глаз – тот, что планировалось прооперировать. Для включения пациента в исследование необходимо было иметь рефракцию в пределах от –6,0 до +6,0 диоптрий; остроту зрения, обеспечивающую фиксацию на метке; качество ОКТ изображения, позволяющее проводить клиническую оценку; внутриглазное давление (ВГД) менее 22 мм рт. ст., должны отсутствовать глаукома, патология зрительного нерва, макулярной области и др. в истории болезни и при обследовании на щелевой лампе и стереоскопической оценке; факоэмульсификация катаракты должна быть неосложненной; на визите в 1-й мес. после операции исследуемый глаз должен иметь прозрачные преломляющие среды, нормальное послеоперационное состояние и отсутствие изменений в сетчатке, макуле и зрительном нерве. Сбор данных проводился в период с января по июнь 2014 г. Все сканы ОКТ RTVue были сделаны одним и тем же специалистом. Плотность ядра хрусталика измерялась с помощью системы Pentacam nucleus staging (Pentacam, Oculus Optikgeräte GmbH, Wetzlar, Germany). Предоперационные измерения на RTVue ОКТ (версия 6.3) были сделаны за 1 день до операции через расширенный зрачок, послеоперационные измерения проводились спустя 4 нед. после неосложненной факоэмульсификации с имплантацией заднекамерной ИОЛ без мидриаза. Данные о демографической принадлежности, уровне ВГД и длине переднезадней оси глаза были получены на первом визите. Рефрактометрия и определение остроты зрения с наилучшей коррекцией проводились на обоих визитах.
Оптический когерентный томограф
Исследование пациентов проводилось на оптическом когерентном томографе RTVue-100 (Optovue Inc., Fremont, CA, USA), версия 6.3. О принципах работы данного прибора подробно рассказано в литературе [3, 22, 23]. Для получения изображений RTVue-100 использует сканирование в ближней части инфракрасного диапазона (840 нм) с шириной спектра излучения 50 нм. Для получения параметров толщины СНВС и ГКС использовался стандартный глаукомный протокол [3, 22, 23]. Он включает в себя 3-мерное сканирование зрительного нерва с автоматизированным распознаванием границ зрительного нерва, определяемых на границе слоя пигментного эпителия сетчатки, сканирование головки зрительного нерва с определением параметров диска зрительного нерва (ДЗН) и толщины СНВС в радиусе 4 мм, а также стандартный скан ГКС. Каждый скан головки зрительного нерва состоит из 12 радиальных линий и 6 концентрических окружностей, на основании которых строится карта толщины СНВС.
Измерительный круг диаметром 3,5 мм (920 точек) получают после того, как контурная окружность будет расположена по центру ДЗН. Границы головки зрительного нерва определяются при первом визите пациента, а в дальнейшем автоматически переносятся на все последующие измерения. Исследуемые в данной работе параметры СНВС рассчитываются для всей окружности, верхнего и нижнего секторов. Сканирование ГКС проводится в зоне размером 7×7 мм, центрированной на расстоянии 1 мм темпоральнее фовеолы (т. е. в области максимальной концентрации ганглиозных клеток). Свое внимание мы сосредоточили на оценке толщины ГКС, объема глобальных потерь ГКС (Global Loss Volume, GLV) и объема фокальных потерь комплекса ГКС (Focal Loss Volume, FLV). Толщина комплекса ГКС, т. е. расстояние между внутренней пограничной мембраной и наружной границей внутреннего плексиформного слоя, и ее усредненное значение, а также значение для верхнего и нижнего сегментов рассчитываются автоматически. Параметр FLV рассчитывается как процентное соотношение суммы статистически значимых потерь объема комплекса ГКС к площади карты ГКС. Параметр GLV определяется как сумма всех относительных дефектов, нормализованная к общей площади карты измерений (в %). После каждого сканирования оценивалось качество полученного изображения, и при выявлении низкого качества или артефактов съемка проводилась повторно. Удовлетворительными считались снимки с индексом силы сигнала (ИСС) для протокола исследования СНВС >30, для ГКС >35 до экстракции катаракты. Следует подчеркнуть, что ИСС не зависит от ПО и является идентичным для версий 6.3 и 6.12. Расчет по каждому изображению проводился на 2-х версиях ПО, параметры средней толщины СНВС и ГКС автоматически были классифицированы следующим образом: «в пределах нормы» (вероятность того, что нет обусловленных глаукомой поражений ≥5%), «пограничное состояние» (p<5%, но ≥1%) и «за пределами нормы» (p<1%). Один и тот же исследователь оценивал сегментацию изображений для параметров СНВС и ГКС и фиксировал наличие или отсутствие ошибок сегментации при использовании версий 6.3 и 6.12.
Методы статистической обработки
Для статистической обработки данных нами использовалась программа SPSS 22. Нормальность распределения оценивалась с помощью критерия Шапиро – Уилка. Для сравнения 2-х версий ПО и данных на разных временных отрезках использовались тесты ANOVA, апостериорный тест Сидака или, при необходимости, критерий Фридмана для апостериорных множественных сравнений. Тест МакНемара применялся для оценки частоты ошибок сегментации изображения и автоматического классифицирования результатов («в пределах нормы» и «пограничное состояние» или «за пределами нормы»), определяемых старой и новой версиями ПО и сравнения данных до и после операции по экстракции катаракты. Критерий знаковых рангов Уилкоксона использовался при сравнении данных наилучшей корригированной остроты зрения до и после операции. Статистически достоверным считалось значение р≤0,01.
Результаты
Мы обследовали 22 глаза у 22 пациентов с катарактой без сопутствующей глазной патологии, их демографические данные представлены в таблице 1. При определении плотности ядра хрусталика на аппарате Pentacam nucleus staging получены следующие значения: 1 – у 5 глаз, 0 – у 15 глаз; данные 2-х глаз были утеряны вследствие ошибки ПО. ИСС (медиана и интерквартильный размах) до и после факоэмульсификации составил для сканов толщины СНВС 39,4 (от 35,9 до 44,9) и 49,9 (от 45,6 до 57,0; критерий знаковых рангов Уилкоксона, p<0,0015), для сканов комплекса ГКС – 43,1 (от 40,7 дo 47,1) и 56,25 (от 50,8 дo 58,0; p<0,0002). Никаких существенных различий для любого параметра толщины СНВС между версиями ПО до или после операции не наблюдалось, также не было выявлено достоверных изменений толщины СНВС в послеоперационном периоде при оценке обеими версиями ПО (табл. 2). Хотя при оценке толщины комплекса ГКС разными версиями ПО достоверных различий в до- и послеоперационном периодах не было найдено, отмечается значимое увеличение параметров толщины ГКС при оценке ПО версии 6.12 после операции по удалению катаракты (табл. 2). Меньшее и статистически недостоверное увеличение наблюдалось для тех же параметров толщины ГКС с версией 6.3. Обе версии ПО отметили снижение (улучшение) показателя GLV статистически значимым образом после факоэмульсификации (табл. 3). Снижение было меньше и не достигло уровня статистической значимости для FLV. Различий в показателях GLV и FLV до и после операции не выявила ни одна версия ПО.

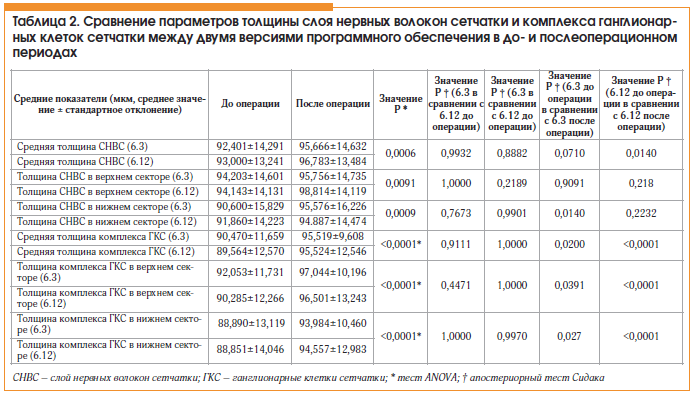
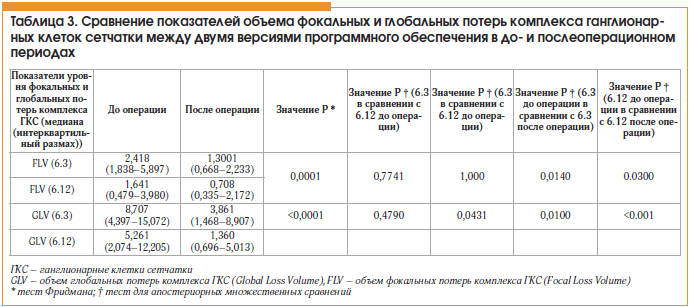
Число глаз с по крайней мере 1 ошибкой сегментации для среднего значения толщины СНВС было 1; 1 (версия 6.3) и 1; 0 (версия 6.12) до и после операции соответственно (тест МакНемара, p≥0,8752 для всех сравнений). При проведении сканирования комплекса ГКС перед факоэмульсификацией 9 глаз (ПО 6.3) и 7 глаз (ПО 6.12) имели 1 ошибку сегментации или более (p=0,3753). Соответствующие показатели составили 2 и 0 после операции (р=1,0000). Уменьшение числа глаз с не менее 1 ошибкой сегментации было значительным с использованием версии 6.3 (р=0,0080), но не достигло уровня статистической значимости с версией 6.12 (р=0,0701). При автоматическом классифицировании параметров средней толщины СНВС выходящими «за пределы нормы» признаны 4; 5 глаз (версия 6.3) и 3; 2 глаза (версия 6.12), а для средней толщины ГКС – 1; 3 (версия 6.3) и 1; 2 глаза (версия 6.12) до и после операции, соответственно (р≥0,3750 для всех сравнений).
Обсуждение
В данном исследовании мы проводили сканирование СНВС и комплекса ГКС до и через 1 мес. после несложной операции по удалению катаракты с использованием имеющейся в настоящее время версии ПО (6.3) RTVue-100 ОКТ. Затем нами был проведен анализ полученных данных 2-мя версиями ПО: 6.3 и 6.12. Недавно разработанная и пока недоступная для коммерческого использования версия 6.12 содержит протокол для оценки глаукомных поражений. По словам производителей, версия 6.12 позволяет значительно улучшить сегментацию изображений с помощью нового алгоритма постобработки получаемых сканов, а также за счет увеличения разделения измерительного сигнала и шума. Хотя детали этого алгоритма не разглашаются, в более раннем исследовании нами было показано, что версия ПО 6.12 обеспечивает значительное улучшение сегментации изображения при сканировании ГКС у пациентов с макулярными друзами и субретинальной неоваскулярной мембраной по сравнению с имеющейся на данный момент версией ПО [24].
Наличие катаракты подавляет мощность сигнала при проведении ОКТ [13–17] и, как следствие, снижает воспроизводимость измерений [13] и уменьшает соотношение сигнал/шум [13–17]. Эти негативные эффекты устраняются после хирургического вмешательства по поводу катаракты [14, 16, 17]. Представленные в этом исследовании результаты также показали значительное возрастание значений мощности сигнала после операции. Мы предположили, что проведение ОКТ у здоровых пациентов с катарактой с использованием RTVue (версии 6.3) до и после факоэмульсификации и анализирование результатов обеими версиями ПО даст нам возможность установить, распространяются ли заявленные производителями преимущества версии 6.12 перед текущей версией на пациентов, у которых из-за начальной катаракты снижено соотношение сигнал/шум.
Вопреки нашим ожиданиям, мы не обнаружили никаких существенных различий между версиями ПО для параметров толщины СНВС (перипапиллярно 360о, в верхнем и нижнем секторах) и комплекса ГКС (средняя толщина, в верхнем и нижнем сегментах, FLV и GLV) ни до, ни после операции. Это можно объяснить тем фактом, что плотность ядра хрусталика была невысокой, а перед операцией измерения ОКТ на RTVue были сделаны с широким зрачком, что способствовало увеличению соотношения сигнал/шум по сравнению с изображениями, полученными через узкий зрачок. В отличие от этого все средние значения толщины ГКС существенно увеличены при оценке версией ПО 6.12 после операции по сравнению с предоперационным значением. Увеличение тех же параметров не было статистически достоверным при оценке ПО версии 6.3. Поскольку наличие легкого транзиторного макулярного отека после неосложненной факоэмульсификации является установленным фактом [18–21], эта разница версий ПО свидетельствует о том, что новая версия имеет преимущества в обнаружении незначительных изменений толщины ГКС, чем имеющаяся версия. Более высокие результаты версии 6.12 можно объяснить ее улучшенной способностью сегментации изображения: хотя обе версии показали снижение (улучшение) GLV после операции по сравнению с предоперационными значениями, уровня статистической достоверности достигли лишь данные, полученные при обработке изображений версией 6.12.
При оценке параметров средней толщины СНВС обеими версиями ПО каких-либо изменений в послеоперационном периоде не обнаружено. Это вполне логично, поскольку транзиторный макулярный отек в раннем послеоперационном периоде не распространяется на перипапиллярную область. В нашей работе число глаз с по крайней мере 1 ошибкой сегментации и неправильно классифицированных как «вне пределов нормы» было небольшим, поэтому вполне ожидаемым оказалось отсутствие различий в этом отношении между 2-мя ПО.
Наше исследование имеет некоторые ограничения. Мы оценивали изображения, полученные с помощью ПО версии 6.3, таким образом, наши результаты не дают информации о возможностях съемки с использованием версии 6.12. Поскольку плотность ядра хрусталика у наших пациентов была невысокой, мы не беремся делать выводы о клинической значимости этого метода для людей с незрелой катарактой. Все наши пациенты были европеоидами и имели рефракцию от -6,0 до +6,0 диоптрий до операции, поэтому некорректно было бы экстраполировать полученные результаты на другие этнические группы или лиц с высокими аномалиями рефракции. И наконец, все участники исследования имели лишь катаракту без какой-либо иной глазной патологии, вследствие чего никаких заключений относительно пациентов с катарактой и сопутствующей глаукомой из наших данных сделано быть не может.
Заключение
Наши результаты свидетельствуют о том, что готовящаяся к выпуску новая версия ПО 6.12 RTVue ОКТ улучшает сегментацию изображения в области сканирования комплекса ГКС и по этим параметрам превосходит ныне доступную версию 6.3. В клинической практике это может оказать существенную помощь в ситуациях, когда необходимо оценить глаукомное поражение у пациентов с начальной катарактой. Однако необходимы дальнейшие детальные исследования, чтобы выяснить, способны ли указанные выше преимущества повысить точность выявления первых признаков глаукомы и ее прогрессирование в рутинной клинической практике.
Благодарность
Авторы выражают благодарность Péter Vargha за помощь в обработке статистических данных и Miklós Resch за помощь в наборе участников исследования.
Перевод с английского языка выполнен И.А. Королевой (ГБУЗ «ГКБ №15 им. О.М. Филатова» ДЗ г. Москвы).












