GOU VPO Kuban State Medical University of Roszdrav,
Krasnodar
Purpose: to study clinical efficacy of lymphotropic drugs in complex treatment of dry eye syndrome and chronic eye ischemic syndrome (CEIS).
Materials and methods: 103 patients with medium stage of dry eye syndrome and CEIS of average age of 66,2±2,1 years old were included into the study. Besides standard ophthalmologic examination in all patients Shirmer and Norn tests, evaluation of hemodynamic indices of ophthalmic and lachrymal arteries, microcirculation of bulbar conjunctiva were performed. Examinations were carried out before treatment,in 9 and 30 days. 3 groups of patients were formed according to the type of treatment:1st group received tear replacing drugs, 2nd – tear replacing drugs and standard CEIS treatment, 3rd – tear replacing drugs and lymphotropic treatment (lidocain+trental).
Results: In patients of the 3rd group there was reliably more evident decrease of subjective discomfort index by 9th day after beginning of treatment then in patients of 1st and 2nd groups. Lymphotropic drugs allowed decreasing the quantity of instillations of artificial tear drops (by 2.5±0,1 per day). Summary tear production increased more in the 3rd then in the 2nd group. It correlated with rising of maximal systolic blood flow in the lachrymal artery in the 3rd group.
Xerotic changes reduced more evidently in the 3rd group by 9 day of treatment in comparison with both other groups.
Conclusion: Results of the study allows including of lymphotropic drugs into the complex treatment of dry eye syndrome and CEIS.
Дальнейшая оптимизация терапии синдрома «сухого глаза» (ССГ) является актуальной научно–практической задачей (Бржеский В.В., Сомов Е.Е., 2003; Майчук Д.Ю., 2008; Behrens A. et al., 2006; Baudouin C., 2007; The Management and Therapy Subcommittee of the International Dry Eye WS, 2007). Это определяется увеличением распространенности и заболеваемости ССГ в течение последних десятилетий во всех странах мира (Майчук Ю.Ф., 2009; Полунин Г.С. и соавт., 2009; Marquardt R. et al., 1980; Moss S.E., 2000; Lee A.J. et al., 2002; Schaumberg D.A. et al., 2009). С другой стороны, эффективность лечебного воздействия далеко не всегда бывает достаточной, поскольку основным направлением терапии «сухого глаза» продолжает оставаться заместительная терапия препаратами искусственной слезы (Бржеский В.В. и соавт., 2004; Майчук Д.Ю., 2007; Brewitt H. et al., 1997; Liu Z., 1999; Kaercher K., 2003).
Вместе с тем новые возможности терапии ССГ могут быть связаны со стимуляцией слезопродукции путем местного или системного использования препаратов, улучшающих микроциркуляцию бульбарной конъюнктивы и (или) большой слезной железы (Ерёменко А.И., Янченко С.В., 2006, 2008, 2009; Луцевич Е.Э. и соавт., 2007; Gobbels M. et al., 1991; Kaercher K., 2003; Schaumberg D.A., 2008).
Цель: изучить клиническую эффективность лимфотропной терапии (ЛТТ) в комплексном лечебном воздействии при ССГ в условиях хронического глазного ишемического синдрома (ХГИС).
Пациенты и методы. Объект исследования: 103 человека (49 мужчин, 54 женщины) пожилого возраста (мужчины от 61 до 75 лет, женщины от 56 до 75 лет). Средний возраст обследованных составил 66,2±2,1 года. Кроме этого было обследовано 25 офтальмологически здоровых человек той же возрастной группы. Критерии включения: впервые выявленный ССГ средней степени тяжести (в соответствии с клинической классификацией Бржеского В.В. и Сомова Е.Е., 2003); наличие атеросклероза и артериальной гипертензии, наличие ХГИС в форме хронической сосудистой оптической нейропатии (в соответствии с классификацией Ерёменко А.И., 2001). Критерии исключения: системные заболевания соединительной ткани, наличие острых или хронических воспалительных заболеваний переднего отрезка глаза, наличие аллергических заболеваний глаз, первичные и вторичные дегенеративные поражения глазной поверхности, состояние после офтальмохирургии, длительная инстилляционная терапия препаратами с наличием эпителиотоксичных консервантов.
Помимо традиционного офтальмологического обследования всем наблюдавшимся проводили: определение показателя субъективного дискомфорта (по Бржескому В.В., 2003; в баллах, 3–балльная шкала); учет необходимого количества инстилляций препаратов искусственной слезы для купирования субъективных проявлений ССГ (n инстилляций/сут.); определение суммарной слезопродукции (тест Ширмера–1, мм); оценку состояния слезной пленки (тест Норна, с; индекс нижнего слезного мениска); оценку гемодинамических показателей глазничной и слезной артерий (цветовое и энергетическое картирование; цифровой ультразвуковой сканер Philips); описательную и компьютерную морфометрическую оценку состояния микроциркуляции бульбарной конъюнктивы с использованием авторской программы для ЭВМ (Янченко С.В., Ерёменко А.И. и соавт., 2009; свидетельство о госрегистрации №2009616529); описательную и компьютерную морфометрическую оценку показателя ксероза конъюнктивы и роговицы при окрашивании лиссаминовым зеленым (по Bijsterveld, 1969; в баллах, 9–балльная шкала); классическую (Singh R. et al., 2005) и модифицированную (Ерёменко А.И., Янченко С.В., 2008) импрессионную цитологию бульбарной конъюнктивы с компьютерной морфометрической оценкой показателя тканевой энтропии (по Автандилову, 1990; усл. ед.), определением коэффициента муцинпродуцирующей активности эпителиальной выстилки (усл. ед.), и использованием инструмента для дозированного забора клеточного материала (Янченко С.В., Ерёменко А.И. и соавт., 2009; патент на изобретение №237905). Средние арифметические вышеуказанных показателей у офтальмологически здоровых добровольцев и больных ССГ в условиях ХГИС, а также их стандартные отклонения (М±s) приведены в таблице 1.
Таким образом, у всех больных ССГ и ХГИС, включенных в исследование, было зафиксировано достоверное снижение функциональных тестов слезопродукции, гемодинамических показателей большой слезной железы и бульбарной конъюнктивы, интегрального коэффициента муцинпродуцирующей активности эпителиальной выстилки конъюнктивы, а также достоверное повышение показателя тканевой энтропии конъюнктивы, сравнительно с показателями здоровых добровольцев той же возрастной группы. Хронический глазной ишемический синдром у всех больных ССГ протекал в форме хронической ишемической нейропатии зрительного нерва, сочетающейся с хронической ишемической ретинопатией (по Тарасовой Л.Н. и соавт., 2003). Ультразвуковое цветовое и доплеровское картирование позволило выявить у 67 человек (65%) стенозирующее поражение внутренней сонной артерии (ВСА). При этом лишь у 1/3 из них стенозирующее поражение было гемодинамически значимым (стеноз более 75%). У остальных 36 больных ССГ и ХГИС атеросклеротическое поражение было нестенозирующим. Кроме указанного, у 47 пациентов (45,6%) определялась патологическая извитость ВСА, у 33 (32%) – патологическая извитость позвоночной артерии (ПА), а у остальных 23 (22,3%) – сочетание патологической извитости ВСА и ПА. У всех пациентов было зафиксировано атеросклеротическое поражение глазничной артерии, что проявлялось снижением скоростных характеристик, повышением индекса вазорезистентности, изменением доплеровского спектра (паттерна) кровотока и «обеднением» цветовой карты кровотока. Как было отмечено выше (табл. 1.), у всех больных ССГ в условиях ХГИС отмечалось достоверное ухудшение гемодинамики слезопродуцирующих органов (большой слезной железы и добавочных слезных железок, располагающихся в конъюнктиве глазной поверхности).
Необходимо отметить, что из 103 человек с идентичной исходной тяжестью ССГ и ХГИС 27 человек отказались от какой–либо терапии хронического глазного ишемического синдрома. Указанные лица были включены в 1–ю группу (контроль). Всем им проводилась изолированная слезозаместительная терапия. Больные 2–й группы (36 человек; 72 глаза) помимо слезозамещения получали традиционную терапию ХГИС. Пациентам 3–й группы (40 человек; 80 глаз) проводили слезозамещение и лимфотропную терапию. Для проведения слезозаместительной терапии нами был выбран препарат 0,15%–ной гиалуроновой кислоты c минимальным количеством консерванта, подверженного биологическому распаду (Oxial, Santen). Помимо отсутствия эпителиотоксичного побочного действия выбор данного препарата был обусловлен данными научной литературы о способности гиалуроновой кислоты восстанавливать морфофункциональное состояние эпителия глазной поверхности (Aragona P. et al., 2002). Традиционная терапия ХГИС включала парабульбарное введение трентала – 0,5 мл, №8, внутримышечное введение никотиновой кислоты 1% – 1,0 мл №8, пероральный прием кавинтона, антиоксидантов и витаминов группы В).
Лимфотропное введение лекарственных препаратов проводили в соответствии с авторской модификацией (Ерёменко А.И., Янченко С.В., 2006) классической техники «субмастоидальной блокады» (Братко В.И. и соавт., 2007; Шурупова Н.Б., 2004), – в точке, расположенной на 1,0 см ниже и 1,0 см медиальнее вершины сосцевидного отростка, в зоне, богатой регионарными лимфоузлами (Краснов М.Л., 1952). Глубина введения лекарственной смеси 1,0 см. Смесь лекарственных препаратов включала 1,0 мл трентала и 1,0 мл 2%–ного раствора лидокаина (в качестве лимфостимулятора). Учитывая двухсторонний характер поражения, лимфотропную терапию у больных ССГ и ХГИС проводили одновременно с обеих сторон. Лимфотропное введение смеси лекарственных препаратов проводили в течение 8 дней. Оптимальная продолжительность курса была определена нами в ходе предварительных поисковых исследований (Ерёменко А.И., Янченко С.В., 2008). Лечебный эффект способа основан на купировании хронической ишемии слезопродуцирующих органов в условиях хронического глазного синдрома и проявляется увеличением основной и стимулированной слезопродукции (Янченко С.В., Ерёменко А.И. и соавт., 2009; патент на изобретение №2371080).
Все результаты, полученные в ходе исследования, подвергали статистической обработке с помощью стандартных методов параметрической статистики и их непараметрических аналогов, путем использования прикладного пакета программы SPSS (русифицированная версия SPSS 12.0.2 для Windows). Различия считали достоверными при р<0,05.
Результаты и обсуждение. Сравнительная оценка эффективности изолированной слезозаместительной терапии (1–я группа), слезозамещения в сочетании с традиционной терапией ХГИС (2–я группа) и слезозамещения в сочетании с лимфотропной терапией (3–я группа) у больных ССГ и ХГИС представлена на рисунках 1–4.
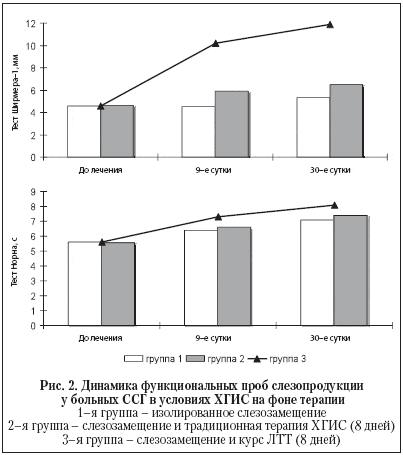
Как следует из приведенных данных (рис. 1), у пациентов, получавших слезозамещение и лимфотропную терапию, на 9–е сутки наблюдения отмечалось достоверно более выраженное уменьшение показателя субъективного дискомфорта, чем у больных 1–й группы (р<0,01) и пациентов 2–й группы (р<0,05). Кроме этого, использование лимфотропной терапии позволило оптимизировать инстилляционный режим у пациентов 3–й группы, путем сокращения количества инстилляций препарата искусственной слезы (до 2,5±0,1 инстилляций в течение суток).
Также у пациентов 3–й группы отмечалась более выраженное, чем во 2–й группе, повышение суммарной слезопродукции (рис. 2). По нашему мнению, вышеуказанный эффект был связан с достоверно более выраженным влиянием лимфотропной терапии на гемодинамические показатели слезопродуцирующих органов (большой слезной железы и добавочных слезных железок конъюнктивы глазной поверхности).
Как показано на рисунке 3, гемодинамические показатели у пациентов 1–й группы (изолированная слезозаместительная терапия) закономерно не изменились. Необходимо отметить, что более выраженное увеличение максимальной систолической скорости кровотока в слезной артерии (р<0,05), а также более выраженное увеличение калибра артериол бульбарной конъюнктивы (р<0,01) у больных 3–й группы сравнительно с пациентами 2–й группы коррелировало с более выраженным приростом объема суммарной слезопродукции (r = 0,78; р<0,05).
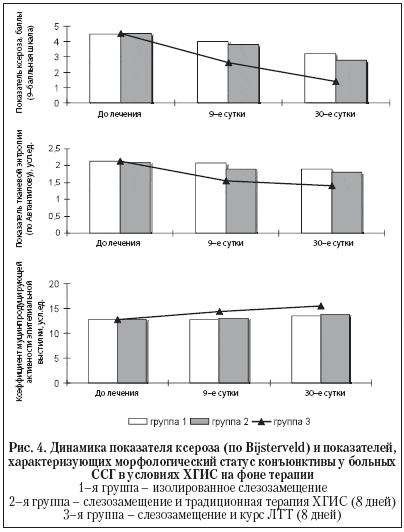
Как представлено на рисунке 4, в 3–й группе (слезозамещение + лимфотропная терапия) на 9–е сутки наблюдения отмечалось более выраженное уменьшение ксеротических изменений конъюнктивы глазной поверхности и роговицы сравнительно с пациентами 2–й группы (слезозамещение + традиционная консервативная терапия ХГИС; р<0,05), и больными 1–й группы (изолированная слезозаместительная терапия; р<0,01).
Изменение вышеуказанных показателей, косвенно отражающих состояние морфологии тканей глазной поверхности, коррелировали с положительной динамикой данных, полученных в ходе модифицированной импрессионной цитологии (снижение коэффициента тканевой энтропии и повышение коэффициента муцинпродуцирующей активности эпителиальной выстилки).
Заключение. Проведенное нами исследование позволило установить, что включение лимфотропного введения лекарственных препаратов (трентал + лидокаин) в комплексную терапию ССГ в условиях хронического глазного ишемического синдрома, дополнительно к слезозамещению, позволяет в короткие сроки достигнуть достоверно более выраженного уменьшения субъективных и объективных проявлений «сухого глаза» и ХГИС. Немаловажным является тот факт, что использование разработанной комплексной терапии ССГ и ХГИС позволяет нормализовать режим инстилляционной терапии путем сокращения количества закапываний препарата искусственной слезы, что уменьшает потенциальный риск развития медикаментозной аллергии и повышает качество жизни пациентов.
Необходимо отметить, что достоверно более выраженная динамика теста Ширмера–1 у пациентов, получавших слезозамещение и лимфотропную терапию, коррелировала с более выраженным улучшением гемодинамических показателей слезопродуцирующих органов. Таким образом, можно считать, что увеличение объема слезопродукции было в значительной степени связано с эффективным купированием ХГИС и хронической ишемии слезопродуцирующих органов. В свою очередь, восстановление объема слезопродукции позволило в короткие сроки достигнуть достоверно более выраженного уменьшения показателя ксероза конъюнктивы и роговицы и улучшения морфологического статуса тканей глазной поверхности, сравнительно с традиционным лечебным воздействием.
Приведенные факты позволяют рекомендовать включение лимфотропного введения смеси лекарственных препаратов (лидокаин + трентал) в комплексную терапию ССГ у больных с наличием хронического глазного ишемического синдрома дополнительно к слезозамещению препаратами искусственной слезы.