Введение
Птеригиум является дегенеративным заболеванием конъюнктивы глазного яблока. Его выраженные изменения (III и IV степени по З. Д. Татаренко, 1993) расценивают как вазопролиферативную патологию, которая в 60—70% случаев способна сформировать грубые косметические дефекты, индуцированный роговичный астигматизм, помутнение центральной зоны роговицы со снижением остроты зрения [1, 2].Единственным методом его лечения остается хирургическая резекция. Несмотря на множество различных хирургических методик, частота его рецидивирования высока и составляет от 40 до 70% [3–5]. Наиболее высок риск рецидивирования при птеригиуме II–III степеней (мясистая консистенция, выраженная сосудистая сеть). Основой рецидивирующего роста птеригиума является обильная васкуляризация полулунной складки внутреннего угла глаза и теноновой капсулы. Наиболее часто рецидив птеригиума возникает в течение 1-го года после хирургического вмешательства [3, 5].
Для профилактики рецидивирования птеригиума после его резекции в настоящее время используют искусственный тканевой барьер у лимба. В качестве трансплантатов применяют различные ауто- и гетероткани: слизистую с губы, твердую мозговую оболочку, капсулу почек [5–9].
Среди барьерных биологических трансплантационных материалов в последние годы все чаще применяется амниотическая мембрана. Это обусловлено тем, что ткань амниона способна снижать активность фиброобразования и неоваскуляризации, стимулировать рост и дифференцировку поверхностного эпителия роговицы [6, 10, 11]. Но поскольку зона лимба является иммунокомпетентной, ее амниопластика после хирургии птеригиума способна, напротив, сопровождаться неадекватной воспалительной реакцией на хирургическое вмешательство, замедляя тем самым репаративные процессы в конъюнктиве и роговице. Все это может привести к грубому рубцеванию конъюнктивы внутреннего угла глаза и даже к стойкому помутнению роговицы [6]. Учитывая это, при хирургии птеригиума нами была разработана и внедрена в клиническую практику методика создания барьера, не затрагивающего лимбальную зону [12].
Цель исследования: оценить клиническую эффективность разработанного нами способа профилактики рецидивирования птеригиума II и III степеней после его резекции.
Материал и методы
Был проведен отбор 46 пациентов (46 глаз) с первичным птеригиумом II и III степеней. Возраст пациентов составил от 52 до 73 лет (в среднем 65±2 года). Среди них было 25 женщин и 21 мужчина.Во всех случаях птеригиум локализовался с внутренней стороны глаза, имел мясистую консистенцию, выступающую на 0,8–1,5 мм над поверхностью роговицы, характеризовался наличием выраженной сосудистой сети. В 29 глазах он широко распространялся по поверхности роговицы, достигая 1/2 проекции радужки, а в 17 глазах доходил до проекции зрачкового края (рис. 1).
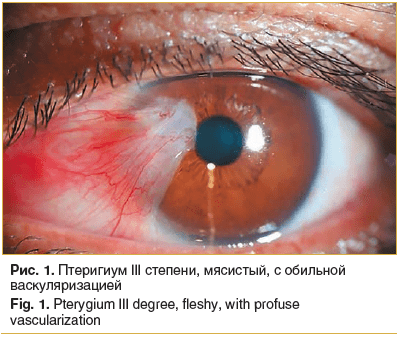
Для оценки эффективности разработанного способа хирургического лечения птеригиума все пациенты были разделены на 2 группы, сопоставимые по полу, возрасту, степени выраженности птеригиума и его сосудистой сети. Основную группу составили 22 пациента (22 глаза), которым выполнялась амниопластика по разработанному нами способу [12–15].
Суть методики заключается в следующем. После проведения резекции головки птеригиума и очищения роговичного ложа тенонова капсула внутренней части глазного яблока тщательно отсепаровывается от конъюнктивы и резецируется до полулунной складки; конъюнктивальный лоскут перемещается и покрывает обнаженную зону склеры вплоть до лимба; в зоне полулунной складки поперечно росту птеригиума к склере подшивается полоска амниона шириной 2–3 мм (4 узловых шва, шелк 8/0).
Важным в данной методике является то, что лоскут амниона располагается не в зоне лимба, а в отдалении от него. Кроме того, важно то, что покрытие склеры в зоне лимба осуществляется собственной конъюнктивой с неповрежденной собственной сосудистой сетью (не обладающей антигенными свойствами), что улучшает процессы эпителизации роговицы.
Группу сравнения составили 24 пациента (24 глаза), которым после иссечения птеригиума, поверхностной кератэктомии удалялась конъюнктива с подлежащей субконъюнктивальной тканью. Замещение склерального дефекта выполняли полоской амниотической мембраны шириной 3–5 мм, подшиваемой в зоне лимба к склеральной капсуле глаза 5–6 узловыми швами (шелк 8/0) [11].
В обеих группах использовалась единая методика хирургической резекции головки птеригиума.
Все операции прошли без осложнений. В постоперационном периоде пациентам обеих групп исследования назначались местные 4-кратные инстилляции растворов антибиотиков и антисептиков (0,3% ципрофлоксацин, 0,01% окомистин), за веки 3 р./сут закладывался 5% декспантенол.
После завершения процессов эпителизации роговичного ложа (7–10-е сут) антисептические растворы отменялись, назначались 3-кратные инстилляции 0,1% р-ра дексаметазона в течение 10 дней. Снятие швов с конъюнктивы выполняли на 10-е сут после операции.
В процессе динамического наблюдения проводили биомикроскопический мониторинг течения регенеративно-репаративного процесса в зоне резекции птеригиума. Оценивали следующие показатели: длительность эпителизации ложа птеригиума на роговице (при инстилляции 1% р-ра флюоресцеина); изучали показатели витализации трансплантатов (цвет, наличие отека, гиперемии); выясняли наличие и степень сосудистой реакции конъюнктивального покрытия (отсутствует, умеренно выраженная, выраженная).
Среди дополнительных методов исследования проводилось изучение осмолярности слезной жидкости (ОСЖ), являющейся интегральным объективным показателем оценки наличия и степени воспалительной реакции роговицы и конъюнктивы. Чем выше ее значение, тем, соответственно, выше степень реакции [16, 17]. Данный показатель мы оценивали как исходно, так и спустя 1–2 мес. после операции методом биоимпедансометрии (ТearLab Oamolarity system, США) [16].
Срок наблюдения составил 10–12 мес. Критериями сравнения в обеих группах являлись наличие и частота рецидивов птеригиума к окончанию срока наблюдения.
Результаты и обсуждение
Результаты постоперационного мониторинга обеих групп пациентов представлены в таблице 1.
Исходно показатели ОСЖ основной группы и группы сравнения имели умеренно повышенные значения (норма не более 316 мОсм/л) [16]. Это указывало на наличие умеренной воспалительной реакции на передней поверхности глаза, обусловленной агрессивным ростом массивного птеригиума.
На 4–6-сут постоперационного периода во всех глазах пациентов группы сравнения амниотический трансплантат был отечным, бледного цвета, с умеренным количеством слизистого отделяемого, зона лимба обильно васкуляризирована, роговичное ложе эпителизируется (рис. 2). Конъюнктивальное покрытие в 8 глазах характеризовалось выраженной сосудистой активностью, отеком и гиперемией, более выраженной в зоне слезного мясца, а также на границе с трансплантатом.
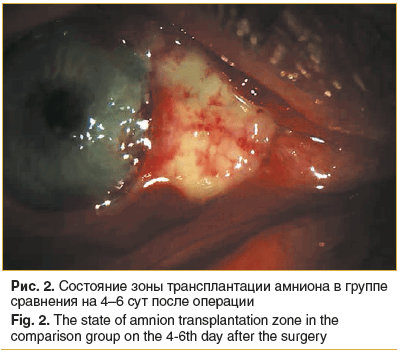
Во всех глазах пациентов основной группы амниотический трансплантат имел бледно-розовый цвет без признаков экссудативной реакции, что свидетельствовало о его адекватной витализации. Зона лимба прикрыта собственной конъюнктивой, васкуляризации лимба нет, роговичное ложе полностью эпителизировано (рис. 3). Конъюнктивальное покрытие характеризовалось умеренной сосудистой реакцией и отеком.
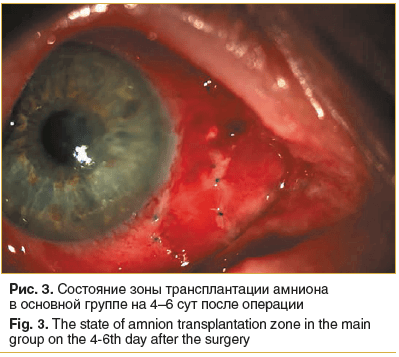
В группе сравнения завершение полной эпителизации роговичного ложа произошло к 6–7 сут, в то время как у пациентов основной группы — к 4–5 сут (p<0,01). Купирование воспалительной реакции конъюнктивы также оказалось более продолжительным, чем в основной группе пациентов (p<0,01).
Отмечены существенные различия в витализации амниотических трансплантатов у пациентов обеих групп исследования. Так, к 10–14 сут во всех 24 глазах пациентов группы сравнения трансплантат у лимба оставался бледным, по его границам выявлялись единичные петехиальные кровоизлияния (рис. 4). Это свидетельствовало о его неудовлетворительной витализации. Зона лимба обильно васкуляризирована, роговичное ложе полностью эпителизировано. На 8 глазах имелась тенденция к сокращению амниотического трансплантата с соответствующим натяжением слезного мясца.
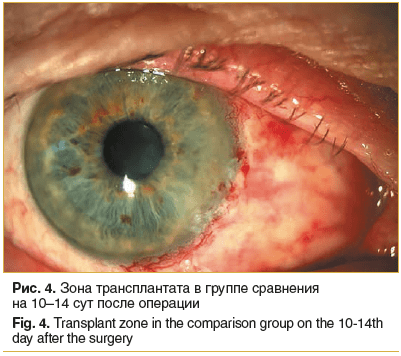
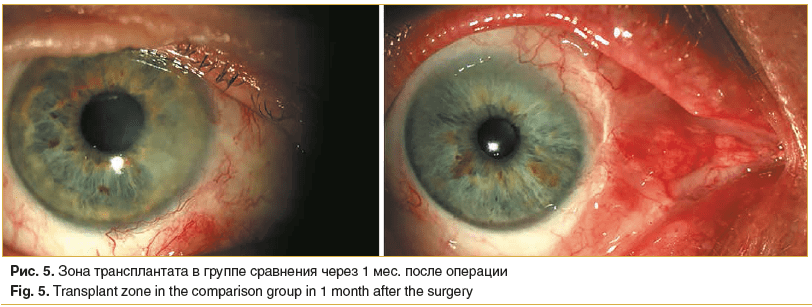
Через 1 мес. в 19 глазах пациентов группы сравнения амниотический трансплантат постепенно приобрел розовый оттенок, однако в 5 глазах сформировалась избыточная васкуляризация лимба, и сохранялось натяжение слезного мясца. Это было расценено нами как дебют рецидивирующего роста птеригиума. Данным пациентам были назначены ежедневные 5-кратные инстилляции 0,1% раствора дексаметазона. Но несмотря на усиление противовоспалительного лечения, в 3 глазах все же произошло прогрессирующее нарастание на 1,5–2 мм рубцово-измененной васкуляризированной ткани на роговичное ложе по зоне лимба, с сопутствующим натяжением и деформацией полулунной складки, что было расценено нами как рецидивирующий рост птеригиума (рис. 5).
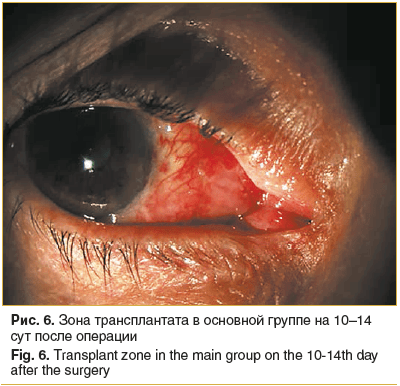
В основной группе пациентов к 10–14 сут во всех 22 глазах отмечено адекватное приживление амниотического трансплантата. Он имел розовый оттенок, в зоне полулунной складки полностью витализирован, роговичное ложе полностью эпителизировано, прозрачное, ни в одном глазу не было отмечено деформаций и натяжения слезного мясца (рис. 6).
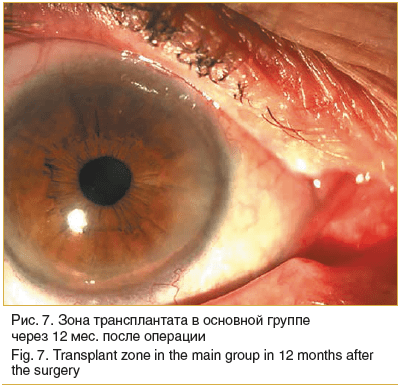
Спустя 1 мес. после операции в 18 глазах пациентов основной группы трансплантаты были витализированы и имели розовый оттенок. В 4 глазах определялась умеренная васкуляризация лимба внутреннего угла глаза. Проведение ежедневных 4-кратных инстилляций 0,1% р-ра дексаметазона позволило купировать формирование васкуляризации во всех глазах в течение 10–15 дней. Ни в одном случае не возник рецидив птеригиума (рис. 7).
Показатели ОСЖ в группе сравнения спустя 1–1,5 мес. значимо снизились по сравнению с исходными значениями (р<0,05), но все же превышали показатели нормы. Это свидетельствовало о вялотекущей умеренной воспалительной реакции конъюнктивы и роговицы, вероятно, поддерживаемой дополнительным раздражением лимбальной зоны [16, 17].
В основной группе пациентов спустя 1–1,5 мес. после операции произошло значимое снижение показателей ОСЖ до значений, сопоставимых с нормальными (p<0,01). Это свидетельствовало о постепенном купировании вялотекущего воспалительного процесса, обусловленного наличием массивного птеригиума, а также, вероятно, об отсутствии дополнительного фактора, раздражающего область лимба. Сравнительный анализ показателей ОСЖ в основной группе и группе сравнения к этому сроку выявил их статистически значимую разницу (p<0,01).
В связи с рецидивирующим ростом птеригиума 3 пациентам группы сравнения были выполнены повторные операции по технологии, примененной в основной группе пациентов. При сроках наблюдения до 12 мес. ни у одного из них не произошло повторного рецидива птеригиума.
Таким образом, преимуществами разработанной нами методики хирургического лечения птеригиума является то, что трансплантат напрямую не соприкасается с иммунокомпетентной зоной лимба. Располагаясь непосредственно в ростковой зоне птеригиума, он более эффективно выполняет свою барьерную функцию, препятствуя росту сосудов в зоне лимба. Его адекватная витализация достигается за счет хорошей васкуляризации области внутреннего угла глаза. Это, соответственно, минимизирует риск его отторжения, некроза и сморщивания.












