for evaluation of effect of combined treatment of patients with uveal melanoma
Institute of eye diseases and tissue therapy
named after V.P. Filatov
V.I. Vit, L.S. Terent’eva , E.I. Dragomiretskaya, S.I. Polyakova, V.K. Spirko
Purpose: To study connection between clinical features of uveal melanoma and effect of organosafe treatment from the viewpoint of preservation of eye and evaluate the possibility of “failures” depending on combination of revealed risk factors.
Materials and methods: Case histories of 520 patients with uveal melanoma after photocoagulation and beta application therapy were looked through.
Tumor localization, its primary size (protrusion) by ultrasound scanning, summary dose of radiation, quantity of beta-therapy and photocoagulation courses in combined treatment and also complications that are observed during the treatment were evaluated.
Results: We created the model which allows calculating the possibility of «failures» of eye preservation depending on four risk factors. It will let to take into consideration chances of saving the eye when choosing treatment tactics.
Conclusion:
The most important clinical factors that influence the effect of organosafe treatment are primary tumor size, its localization, glaucoma onset during the treatment.
В последние годы в результате внедрения в практику современных информационных технологий и развитию понятия «доказательная медицина», широкое распространение получили методы количественной оценки риска или эффекта воздействия в сравнительном анализе получаемых результатов, позволяющих также давать строгую оценку разрабатываемых прогностических и диагностических тестов [1,2,3,5].
Как правило, прогноз результата лечения для конкретного больного однозначно не определен и поэтому должен быть выражен через вероятность.
Эта вероятность может быть оценена на основе предыдущего опыта, накопленного в отношении подобных больных [1,4]. Особенно ценным является возможность качественного прогноза различных клинических состояний при анализе альтернативных подходов к ведению больных, когда в результате таких прогнозов принимается решение об адекватной тактике лечения (хирургическое или консервативное).
Увеальная меланома – наиболее частая внутриглазная злокачественная опухоль. В течение многих лет энуклеация пораженного глаза была единственным методом для пациента с меланомой заднего отдела глаза [5]. В 1979 году Zimmerman и McLean оспорили эффективность энуклеации для предотвращения метастазирования и предположили, что энуклеация может способствовать ускорению метастазирования [6]. Эта дискуссия способствовала развитию органосохранных лечебных методов.
В зависимости от размера и выстояния опухоли имеются приверженцы фотокоагуляции, радиотерапии, локальной резекции, энуклеации либо периодического наблюдения. В настоящее время в США проводятся крупномасштабные рандомизированные клинические исследования, объединившие многие медицинские центры, по оценке эффективности (выживаемости) больных увеальной меланомой при энуклеации проведении радиотерапии и локальной резекции. К настоящему времени эти исследования не закончены, но по данным отчетов многочисленных разрозненных исследований пятилетняя выживаемость больных увеальной меланомой составляет от 65 до 95% [7-12]. В выводах большинства из этих работ говорится о том, что в настоящее время из всех существующих методов лечения ни один не имеет преимуществ в отношении выживаемости пациентов.
Сегодня важная роль отводится методам, сохраняющим качество жизни пациентов, т.е. органосохранным методам. В этой связи актуальной задачей офтальмоонкологии является анализ факторов, которые определяют возможность успешного проведения органосохранного лечения.
Целью данного исследования являются: изучение взаимосвязи между клиническими признаками увеальной меланомы и эффективностью органосохранного лечения, с точки зрения сохранения органа зрения и оценка вероятности «неудач» в зависимости от сочетания выявленных факторов риска.
Материал и методы исследования. Нами проанализированы истории болезни пациентов с увеальной меланомой, которым проводилось органосохранное лечение в виде сочетания фотокоагуляции и бета-аппликационной терапии. Всего таких больных в базе данных в настоящее время 594, из них 520 с полным набором изучаемых признаков. Из этих пациентов случайным образом (путем генерации случайных чисел) были сформированы две выборки: обучающая – 250 человек (у 166 глаз был сохранен и у 84 (33,6%) после комбинированного лечения была энуклеация) и проверочная – 270 человек (у 179 глаз был сохранен, а у 91 (33,7%) была проведена энуклеация после лечения).
Были проанализированы такие клинические признаки, как локализация опухоли, ее первоначальный размер (выстояние) по данным ультразвукового сканирования, суммарная доза облучения, количество курсов бета-терапии и фотокоагуляции при комбинированном воздействии, а также наблюдаемые в процессе лечения осложнения.
Для определения степени сопряженности каждого из перечисленных клинических признаков с различным результатом лечения (глаз сохранен – код признака «0», энуклеация – код «1») использовали c2 – критерий Пирсона. Для численной оценки факторов риска «неудач» нами был применен аппарат логистической регрессии. При этом в качестве оценки относительного риска, связанного с действием фактора, используется экспоненциальный коэффициент уравнения регрессии [14,15]. В общем виде уравнение логистической регрессии записывается так:
оdds (yjґ0)=exp (xjbj + b0) (1)
Pслучая = odds (2),
odds+1
где odds – шанс, связанный с вероятностью формулой (2), xj– значения неизвестных переменных (факторов),
bj – коэффициенты, которые необходимо определить[16].
Расчеты проводились с использованием статистического пакета SPSS 11 (http://www.SPSS.com).
Результаты и их обсуждение
На первом этапе мы проанализировали зависимость результата лечения (успех, неудача) от каждого изучаемого клинического показателя, т.е. определили относительный риск развития «неудачи» по результатам одновариантной логистической регрессии. Изучаемые клинические показатели и их условное обозначение представлены следующим списком:
1. Локализация опухоли:
а) радужка (L1);
б) радужка + цилиарное тело (L2);
в) цилиарное тело + хориоидея, хориоидея в области экватора (L3);
г) только хориоидея (L4).
2. Начальный размер опухоли (НВС), кодировки в данном исследовании: 1- если выстояние >6 мм, 0 – если выстояние 6 мм.
3. Помутнение хрусталика, возникшее при проведении терапии (CA).
4. Глаукома, развившаяся при проведении лечения (GL).
5. Суммарная доза бета-облучения (DOZA).
6. Число курсов фотокоагуляции (NFOTO).
7. Число курсов бета облучения (NBETA).
Перечисленные признаки, кроме 5-7, являются бинарными, принимающими значение 1, если фактор присутствует и 0, если фактор отсутствует. Переменные 5-7 – численные.
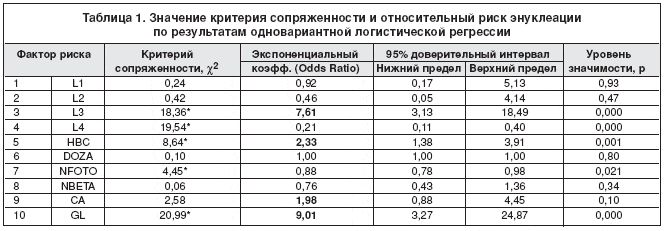
В таблице 1 представлена степень сопряженности каждого изучаемого признака с клиническим результатом (c2) и его уровень значимости (р), а также оценка относительного риска, выраженная через экспоненциальный коэффициент уравнения регрессии (оdds Ratio) и 95% доверительный интервал для его оценки.
В таблице 1 звездочкой отмечены значения c2 имеющие достоверную связь с эффективностью лечения на 5% уровне значимости. Наличие глаукомы, локализация L3 и L4, начальный размер опухоли >6 мм и число курсов фотокоагуляций демонстрируют высокую связь с результатом органосохранного лечения.
Как следует из данных таблицы 1, четыре показателя имеют значение относительного риска, выраженного через экспоненциальный коэффициент уравнения регрессии (оdds Ratio) больше единицы и могут рассматриваться как степени риска. Так, риск «неудач» органосохранного лечения у больных с начальным размером опухоли >6 мм (НВС) в 2,33 раза выше, чем у больных с меньшими опухолями. Наличие глаукомы, возникшей в результате проведения комбинированной терапии, в 9 раз увеличивает риск «неудач». Локализация опухоли L3 повышает риск энуклеации в 7,6 раза. А для больных с локализацией L4 риск энуклеации достоверно ниже, чем при любой другой локализации.
Однако все эти оценки, представленные в таблице 1 демонстрируют знание каждого фактора риска в отдельности.
Для выявления комплексного влияния изучаемых признаков на вероятность «неудачи» органосохранного лечения мы использовали уравнение многовариантной логической регрессии. Для поиска лучших предикторов была запущена процедура FORWARD, которая позволяет включать переменные последовательно одну за другой, начиная с наиболее значимой для прогноза сохранения глаза. На первом этапе была включена – GL, на втором – L3, на третьем – НВС и на четвертом – СА.
В результате была получена математическая модель, позволяющая оценить факторы риска и рассчитать вероятность наступления «неудач» органосохранного лечения при различных значениях четырех признаков.
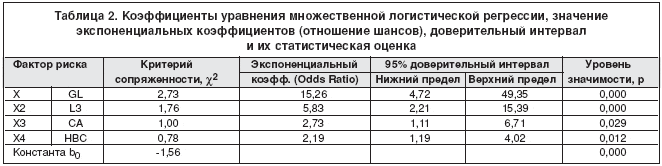
В таблице 2 представлены параметры уравнения множественной логистической регрессии и их оценки.
Как следует из данных таблицы 2, из четырех представленных в таблице факторов риска наибольшую роль в «неудаче» органосохранного лечения играет такой признак, как возникновение глаукомы. Риск потери глаза при ее возникновении в 15,26 раз выше, чем при отсутствии этого осложнения. Вероятность сохранения глаза при локализации опухоли в области цилиарного тела с вовлечением хориоидеи или хориоидеи в области экватора (L3) в 5,8 раз ниже, чем при других локализациях опухоли. Выстояние опухоли более 6 мм. (НВС) также увеличивает риск энуклеации более чем в два раза по сравнению с меньшими опухолями. Для всех представленных в таблице 2 предикторов значения относительного риска энуклеации (отношения шансов) имеют высокую статистическую оценку, их доверительные интервалы не превышают значения менее единицы. Наименьшее значение в прогнозе имеет наличие помутнения хрусталика (р=0,029).
С учетом полученных коэффициентов уравнение логистической регрессии имеет следующий вид:
оdds=exp(-56+2,73xХ1+1,76xХ2+1,00xХ3+0,78xХ4) (1)
Полученная нами регрессионная модель имеет высокую статистическую оценку c2=50,68; ч.с.с=4; р=0,00001.
Используя уравнение (1) мы рассчитали вероятности поведения энуклеации после комбинированного лечения для обучающей и для проверочной выборки. Пациента относили к группе «неудачи», если расчетная вероятность энуклеации была >0,50.
Технологию расчета демонстрирует следующий пример.
Пример: Пациент имеет следующие значения переменных (их обозначения представлены в таблице 2):
Х1 = 1, Х3 = 0
Х2 = 1, Х4 = 0
Подставляя их значение в уравнение (3), получаем следующее выражение:
оdds=exp(-56+2,73X1+1,76X1+1,00X0+0,78X0)
оdds=exp (2,93)=18,73
Рслучая = 0,95, т.е. вероятность неудачного органосохранного лечения у пациента с такими значениями факторов риска = 0,95 (развитие глаукомы при локализации опухоли в цилиарном теле и хориоидеи или хориоидеи в области экватора).
Поскольку все вошедшие в модель показатели принимают только два значения, то легко рассчитать вероятность «неудачи» при любом сочетании факторов риска. В случае присутствия у больного только одного фактора риска – размера опухоли >6 мм, вероятность неудачи составляет 0,32. Т.о. вероятность сохранения глаза при опухолях более 6 мм при любой локализации отличной от L3, в случае отсутствия изученных осложнений, превышает 0,5 и составляет соответственно 1-0,32=0,68. Однако при сочетании размера >6 мм и локализации L3 вероятность неудачи возрастает до р=0,73 даже при отсутствии осложнений.
Сравнивая наблюдательные значения результата лечения с прогнозируемыми, при помощи модели мы получили корректный прогноз у 191 пациента (153+38) из 250 в обучающей выборке (76,4%). В проверочной выборке этот процент равняется 74,8. Таким образом, в проверочной выборке мы получили результат прогноза по выборке из 270 больных.
Заключение. Проведенное исследование показало, что наиболее важными клиническими факторами, определяющими эффективность органосохранного лечения, является начальный размер опухоли, ее локализация, возникновение глаукомы в процессе лечения. Создана модель, позволяющая рассчитать вероятности «неудач» сохранения глаза в зависимости от сочетания четырех факторов риска, что позволит при выборе тактики лечения учитывать шансы больного на сохранение глаза.
Литература
1. Реброва О.Ю. Статистический анализ медичинских данных. М. 2002, 305 с.
2. Драгомицкая Е.И. Количественная оценка клинических характеристик в рамках понятия «доказательная медицина». Тези доповiдей конференцi? “Бiофiзичнi стандарти та iнформацiйнi технологi? в медицинi”, Одеса, 2002 р. с.14
3. Флетчер Р., Флетчер С., Вагнер Э. Клиническая эпидемология. Основы доказательств медицины. Москва, 1998 г.; с. 352
4. Власов В.В. Введение в доказательную медицину. М.2001, 392 с.
5. Davidorf FH, McAdoo JF, Chambers RB. Enucleations for choroidal melanomas. In: Ryan SJ, ed. Retina. Vol 1. 2nd ed St Louis: CV Mosby? 1994:776-71.
6. Zimmerman LE? McLean IW. An evaluation of enucleation in the management of uveal melanomas. Am J Ophthalmol 1992;110:245-50
7. Diener-West M? Hawkins BS? Markowitz JA. Et al. A review of mortality of from chorodial melanoma: a meta-analysis of 5-year mortality rates following enucleation, 1966 through 1988. Arch Ophthalmol 1992;110:245-50.
8. Jensen OA. Malignant melanomas of the human uvea: 25-year follow-up of cases in Denmark, 1943-1952. Acta Ophthalmol 1982;60:161-82.
9. Davidorf FH, McAdoo JF, Chambers RB. Enucleation for choroidal melanomas. In: Ryan SJ, ed. Retina Vol 1 . 2nd ed St Louis: CV Mosby? 1994:776-71.
10. Kindy-Degnan NA, Char DH, Castro JR, et al. Evect of various doses of radiation for uveal melanoma on regression, visual acuity, complications, and survival. Am J Ophthalmol 1989;107:114-20.
11. Gragoudas ES, Seddon JM, Egan K, et al. Longs-term results of proton beam irradiated uveal melanomas. Ophthalmology 1989;97:349-53.
12. Shields JA, Shields CL, Shah P, et al. Patial lamellar sclerouvectomy for ciliary body and chorodial tumors. Ophthalmology 1991;98:971-83.
13. Bland JM. The odds ratio. BMJ. 2000; 320:1486
14. Боровиков В.П., Боровиков И.П. STATISTIKA. Статистический анализ и обработка данных в среде Windows. Москва, 1997, с405-419
15. Ахим Блюм, Петер Цефель. SPSS 10.: Искусство обработки информации. Diasoft. Москва. С-Петербург, Киев, 2002,с.287.
16. Stata Technical Bulletin. (53) January 2000, p.22












