Ключевые слова: ВМД, антиоксиданты, лютеин, зеаксантин.
Abstract
Age-related macular degeneration. Treatment of the dry form of AMD
A.S. Izmailov
FGBU MNTK Eye Microsurgery of Rosmedtechnology
named after acad. Fedorov S.N., S.-Petersburg
In the article mechanisms and risk factors of dry form of AMD are discussed. Author carries out a comparative analysis of clinical research results of effectiveness of antioxidants for treatment and prophylaxis of dry form of AMD.
Key words: AMD, antioxidants, lutein, zeaxanthin.
Эпидемиологические исследования последних десятилетий выявили основные факторы риска возникновения возрастной макулярной дегенерации (ВМД). Установлено, что это заболевание в значительной степени генетически детерминировано. Так, при отсутствии дефектных генов (аллели CFH, ARMS2) среди людей в возрасте 85 лет и старше частота развития поздней ВМД не превышает 5% [22].
Однако факторы внешней среды также способны влиять на развитие возрастных изменений центральных отделов сетчатки. Например, курение увеличивает частоту возникновения поздних стадий ВМД в 2,5–4 раза, причем неблагоприятное воздействие этого фактора обладает выраженным дозозависимым эффектом [23]. При наличии генетических факторов риска CFH вероятность развития ВМД среди некурящих людей возрастает в 12,5 раза, тогда как у курильщиков – в 35 раз [22].
Таким образом, имеются основания полагать, что модификация неблагоприятных факторов внешней среды (рациональное питание, отказ от курения, солнцезащитные очки), в т. ч. и адекватное медикаментозное лечение способны уменьшить вероятность развития ВМД.
Однако следует признать, что консервативная терапия при сухой (неэкссудативной) форме ВМД – один из наиболее противоречивых разделов современной офтальмологии. С одной стороны, отечественными офтальмологами накоплен большой опыт успешного применения патогенетически ориентированной так называемой «антидистрофической» терапии в виде различного рода препаратов, периокулярные инъекции которых нашли широчайшее распространение в лечебных учреждениях страны. С другой стороны, подавляющее большинство проведенных исследований пользы подобного рода терапии не соответствует требованиям доказательной медицины, ее клиническая эффективность не подтверждена, поэтому в клиниках Америки и Европы такая терапия не применяется.
Термин «доказательная медицина» предполагает использование в клинической практике диагностических, профилактических и лечебных мероприятий, эффективность и безопасность применения которых подтверждена. В современной медицинской науке принято выделять следующие категории убедительности доказательности исследований [9]:
I – основывающиеся на результатах тщательно спланированных, рандомизированных контролируемых исследований, мета-анализах или систематизированных обзорах (наиболее высокий уровень доказательности);
II – основанные на результатах когортных исследований или исследований по типу «случай – контроль»;
III – нерандомизированные клинические исследования на ограниченном количестве пациентов или выработка экспертами соглашения по конкретной проблеме.
Категории убедительности доказательств являются хорошим подспорьем практическому врачу в оценке терапевтических возможностей традиционных и новых методов лечения, поэтому дальнейшее рассмотрение материала будет основываться на исследованиях I и II уровней убедительности доказательств.
Минералы и антиоксиданты
В течение многих лет антиоксиданты назначались при ВМД исходя из теоретических представлений о том, что под воздействием активного синего света в фоторецепторах сетчатки возникает оксидативный стресс и накапливаются свободные радикалы, оказывающие разрушительное действие на структуры глазного дна. В соответствии с этим предполагалось, что назначение антиоксидантов (витамины С и Е, бета-каротин, минералы цинк, селен и марганец) может оказывать защитное действие на сетчатку. Позднее был опубликован ряд сообщений о том, что диета, богатая антиоксидантами, предупреждает развитие признаков ранней ВМД, однако роль пищевых антиоксидантов в первичной профилактике возрастных изменений сетчатки длительное время оставалась неясной.
В начале 1990-х гг. результаты плацебо-контролируемых исследований Eye Disease Case-Control Study (1993)1 и Baltimore Longitudinal Study (1994)2 подтвердили защитное действие высоких уровней витаминов А, С и Е, бета-каротина, цинка и селена в плазме крови на прогрессирование ВМД [2, 21]. В 1998 г. исследование Beaver Dam Eye Study3 (1700 пациентов, срок наблюдения 5 лет) продемонстрировало уменьшение риска возникновения крупных друз при употреблении высоких доз витамина Е, высокое содержание цинка в пище приводило к уменьшению частоты возникновения аномалий пигментного эпителия [20].
Исследование Age Related Eye Disease Study (AREDS, 1992–2001)4 – одно из наиболее крупных исследований эффективности профилактического лечения ВМД и катаракты, заслуживающее более детального рассмотрения. В исследование были вовлечены 11 клинических центров США, 4757 пациентов в возрасте 55–88 лет (в среднем – 69 лет), срок наблюдения составил 5 лет. Участники исследования были разделены на 4 группы: получавшие антиоксиданты, минералы, антиоксиданты + минералы и плацебо (табл. 1) [3].
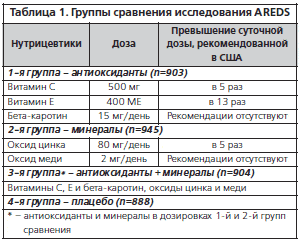
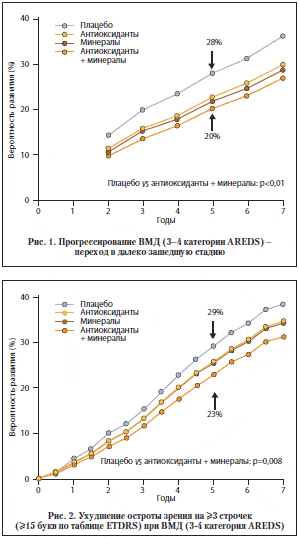
Применительно к ВМД целью исследования AREDS явилось изучение влияния высоких доз антиоксидантов и минералов на остроту зрения и течение ВМД. Полученные результаты подтвердили защитное действие высоких доз антиоксидантов и минералов при 3 и 4 уровнях тяжести ВМД по классификации AREDS5 (рис. 1, 2).
В течение 5-летнего срока наблюдения отмечено уменьшение риска развития далеко зашедшей стадии ВМД: на 17% в группе пациентов, получавших лечение антиоксидантами, на 21% – у получавших преимущественно препараты на основе минералов, на 25% – в группе получавших антиоксиданты и минералы по сравнению с плацебо-контролем. Применение комбинированной терапии на 19% сократило количество случаев снижения остроты зрения на 3 строчки (15 букв) по таблице ETDRS. На основании результатов исследования комбинированная схема лечения AREDS (3-я группа) была рекомендована к широкому клиническому применению при промежуточной стадии ВМД или любой стадии заболевания на лучшем глазу при наличии далеко зашедшей ВМД на парном глазу.
Несколько позднее популяционное исследование Rotterdam Study (2005)6 с участием 4170 пациентов с наличием крупных друз в макуле также подтвердило эффективность комбинированной схемы лечения AREDS в предупреждении прогрессирования ВМД, снижение риска развития поздней стадии заболевания составило 35% [19].
В протоколе AREDS № 13 [7] проанализированы побочные эффекты лечения. В 12% случаев отмечено уменьшение смертности по сравнению с контролем среди лиц, получавших высокие дозы цинка в сочетании с антиоксидантами или без них. Хотя уровни смертности в группах контроля и лечения существенно не отличались, и у пациентов наблюдалась хорошая переносимость исследуемых препаратов, был зарегистрирован ряд нежелательных явлений при назначении высоких доз антиоксидантов и минералов. Назначение бета-каротина увеличивало риск развития рака легких у курильщиков, в связи с чем комбинированная схема лечения AREDS не была рекомендована для данной категории больных. Кроме того, существуют данные, что назначение высоких доз бета-каротина не только не уменьшает, но даже увеличивает риск развития неоваскулярной ВМД. Причем данная зависимость прослеживается не только у курильщиков, но и у никогда не куривших людей [16]. Прием витамина Е приводил к учащению сердечных приступов у больных сахарным диабетом, а цинка в высоких дозах – к росту случаев госпитализации у пациентов с болезнями мочеполовой системы [7].
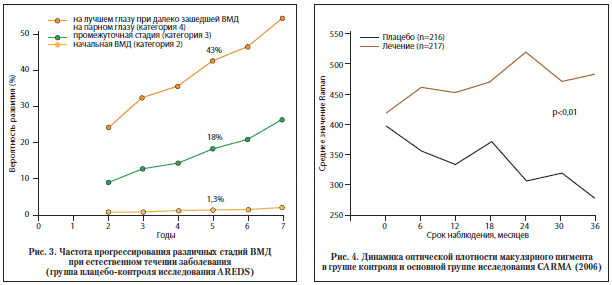
Вследствие низкой вероятности прогрессирования изменений сетчатки (рис. 3) и потенциального риска возникновения побочных эффектов исследователи AREDS не рекомендовали применение лекарственной терапии, содержащей бета-каротин, витамин Е и цинк в высоких дозах при начальной ВМД или отсутствии возрастных изменений сетчатки [3].
При анализе данных систематического обзора и метаанализе 9 проспективных когортных исследований и 3 крупных рандомизированных исследований E.W.Chong et al. (2007) установили невыраженный эффект лечения либо его отсутствие от применения витаминов А, С и Е, цинка, альфа-, бета-каротина, бета-криптоксантина и ликопена при начальной стадии ВМД.
Каротиноиды – природные органические пигменты, синтезируемые бактериями, грибами, водорослями, кораллами и растениями. Эти вещества придают окраску большинству оранжевых или красных овощей и фруктов. В природе обнаружено более 600 каротиноидов, 34 из них выделены в сыворотке крови человека и оказывают ряд благоприятных эффектов на организм. Только два из них – лютеин и зеаксантин определяются в сетчатке. Эти желтые пигменты макулы выполняют функции «солнцезащитных очков» сетчатки, предотвращают окисление триглицеридов и холестерина и являются протекторами перекисного окисления липидов клеточных мембран. Зеаксантин может образовываться в сетчатке из лютеина, но лютеин не синтезируется в организме человека. Оба вещества поступают в него с пищей, в основном при употреблении овощей и фруктов.
К настоящему времени накоплено большое количество данных, свидетельствующих об увеличении частоты развития ВМД при снижении содержания лютеина и зеаксантина в плазме крови человека. Например, исследование Eye Disease Control Study (1993)7 подтвердило высокодостоверную (p=0,0001) взаимосвязь между распространенностью ВМД и уровнем лютеина и зеаксантина в плазме крови. При их низких концентрациях риск развития неоваскулярных поражений возрастал на 70% и выше [2]. Та же исследовательская группа доказала, что риск развития тяжелых стадий ВМД достоверно снижается на 43% у лиц, в большом количестве потребляющих овощи и фрукты (6 мг лютеина и зеаксантина в день) [15]. Крупное популяционное исследование POLA study (2006)8, выполненное на 899 испытуемых, выявило высокодостоверную взаимосвязь между высоким содержанием лютеина и зеаксантина в плазме крови и снижением частоты ВМД [8]. Аналогичные данные (женщины моложе 75 лет, промежуточная стадия ВМД) были получены в исследовании CAREDS (2006)9 [10]. Высокое содержание лютеина и зеаксантина в пище (3–6 мг/сут.) по сравнению с группой низкого потребления каротиноидов (0,5–0,8 мг/сут.) снижало риск развития ВМД на 43–57% [10, 15].
В работе P. Bernstein et al. (2002) по результатам рамановской спектроскопии зарегистрировано уменьшение средней концентрации лютеина и зеаксантина на 32% в макулярной области у лиц с проявлениями ВМД по сравнению с контролем (пожилые люди, употребляющие мало овощей и фруктов). Назначение пациентам с проявлениями ВМД и снижением концентрации макулярных пигментов пищевых добавок с лютеином (>4 мг в день) позволило нормализовать содержание лютеина в макуле [5]. Возможность увеличения оптической плотности макулярных пигментов на фоне приема высоких доз лютеина (12 мг) и зеаксантина (0,6 мг) подтверждена в 3-летнем рандомизированном плацебо-контролируемом исследовании с двойным слепым контролем CARMA (2006)10 (рис. 4) [11].
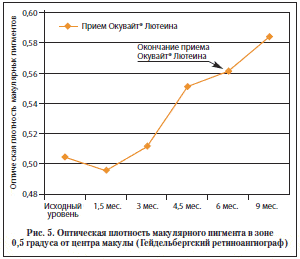
Аналогичные результаты представила исследовательская группа LUNA (2007)11 [18]. Помимо постепенного увеличения оптической плотности макулярных пигментов на фоне приема 12 мг лютеина и 1 мг зеаксантина (Окувайт Лютеин производства компании Bausch & Lomb) сохранялась положительная динамика в отношении оптической плотности пигмента в ближайшие сроки после прекращения приема исследуемого препарата (рис. 5).
Наиболее крупное исследование терапевтического потенциала каротиноидов при сухой форме ВМД – недавно завершенное рандомизированное клиническое исследование AREDS 2 (2006–2012), основанное на 5-летнем наблюдении 4203 пациентов с сухой формой ВМД (билатеральные крупные друзы в макуле или крупные друзы на исследуемом глазу в сочетании с поздней ВМД на парном глазу). В отличие от других ранее выполненных рандомизированных исследований AREDS 2 подтвердило эффективность лютеина (10 мг) и зеаксантина (2 мг) в профилактике прогрессирования ВМД, а также допустимость замещения каротиноидами небезопасного для курильщиков бета-каротина в стандартной рецептуре AREDS. При этом риск развития поздних стадий ВМД несколько снизился (с 34% до 30%, p=0,02). Предполагается, что 25 мг цинка в сутки – максимально возможный уровень абсорбции, поэтому AREDS 2 изучило возможность сокращения дозы цинка с 80 до 25 мг в сутки. Это не привело к увеличению частоты возникновения поздних стадий ВМД и позволило уменьшить риск появления побочных эффектов лечения [4].
Полиненасыщенные жирные кислоты (ПНЖК)
Известно, что атеросклероз и сердечно-сосудистые заболевания в значительной степени связаны с избыточным потреблением жирной пищи, богатой насыщенными жирными кислотами животного происхождения. Наличие ВМД у пациента сопряжено с повышенным риском развития инфаркта миокарда. С учетом сходного патогенеза ВМД и сердечно-сосудистых заболеваний есть основания предполагать, что рациональное питание может предупредить развитие возрастных изменений сетчатки.
Полиненасыщенные омега-3 жирные кислоты (омега-3 ПНЖК) – альфа-линоевая кислота (короткоцепочечные омега-3 жирные кислоты), а также докозагексаеновая и эйкозапентаеновая жирные кислоты (длинноцепочечные омега-3 ПНЖК) обнаруживаются в наружных сегментах палочек и колбочек, обладают противовоспалительными свойствами, препятствуют апоптозу клеток и патологическому ангиогенезу, участвуют в конформационных изменениях родопсина, уменьшают накопление липофусцина в пигментном эпителии сетчатки и липидных депозитов в мембране Бруха. Ряд эпидемиологических исследований подтвердил, что высокое потребление жиров животного происхождения сопряжено с риском развития далеко зашедших стадий ВМД. В свою очередь потребление рыбы один-два раза в неделю приводит к сокращению риска развития неоваскулярной ВМД, а также перехода билатеральных друз в географическую атрофию пигментного эпителия и хориокапиллярного слоя [13, 14].
Недавно завершенное крупное рандомизированное клиническое исследование AREDS 2 (2006–2012) продемонстрировало отсутствие профилактического эффекта при ВМД от назначения пищевых добавок, содержащих омега-3 жирные кислоты [4]. Возможным объяснением данного результата могут быть как действительное отсутствие терапевтического эффекта, так и неучтенное исследователями влияние прочих факторов (особенности диеты, соотношение насыщенных и ненасыщенных жирных кислот в рационе, биологическая доступность пищевых добавок и т. д.). С учетом приведенных выше результатов эпидемиологических исследований имеются основания рекомендовать пациентам старшей возрастной группы дополнить недельный пищевой рацион 1–2-кратным приемом рыбы.
Перспективы лечения сухой ВМД
Перспективы консервативного лечения сухой ВМД не исчерпываются применением минералов и антиоксидантов, клиническая эффективность применения которых подтверждена многоцентровыми исследованиями. Наблюдательные эпидемиологические исследования, сообщения отдельных авторов и групп исследователей свидетельствуют о большом потенциале самых разных биологических добавок в профилактике возрастных изменений сетчатки.
Эпидемиологические данные подтверждают дефицит витамина D в плазме крови среди пациентов с неоваскулярной ВМД. Согласно результатам лабораторных исследований, наблюдаются снижение уровня провоспалительного цитокина TNF-альфа, восстановление нормальной структуры фоторецепторов глаз мышей на фоне приема повышенных доз витамина D. Для нормальной функции сетчатки имеют большое значение ряд других витаминов (А, B6 и В12), оптимальные концентрации и терапевтические возможности которых продолжают изучаться. Выраженные антиоксидантные свойства присущи антоцианозидам и биофлавоноидам, которые уменьшают ломкость капилляров и улучшают состояние соединительной ткани. Большие надежды связываются с применением при ВМД системной энзимотерапии (вобензим) и пептидных биорегуляторов (ретиналамин, кортексин), однако налицо дефицит плацебо-контролируемых клинических исследований эффективности подобных препаратов. Также противоречивы сообщения о профилактическом действии аспирина в профилактике ВМД.
На последнем конгрессе EURETINA (2013) были представлены положительные результаты многоцентрового плацебо-контролируемого исследования II фазы MAHALO Study (2013)12 по ежемесячному применению интравитреальных инъекций лампализумаба (моноклональное тело – ингибитор фактора D системы комплемента) производства фирмы Genentech (США) при сухой ВМД. Препарат зарекомендовал себя как безопасный. Лечебный эффект лампализумаба определялся с 6 мес. от начала лечения, к 18 мес. уменьшение частоты прогрессирования географической атрофии составило 20,4% (p<0,005) [1]. Планируется III фаза исследования препарата.
Таким образом, на сегодняшний день в профилактике возникновения и развития ВМД подтверждена эффективность приема каротиноидов (лютеина (10–12 мг), зеаксантина (1–2 мг)), витаминов С и Е, оксида цинка (10–20 мг) и селена (40 мг).
1 Eye Disease Case-Control Study – глазные заболевания, исследование по типу «случай – контроль» (США)
2 Baltimore Longitudinal Study – продольное исследование (Baltimore, Maryland, США)
3 Beaver Dam Eye Study – исследование глаза (Beaver Dam, Wisconsin, США)
4 Age Related Eye Disease Study (AREDS) – исследование возрастного заболевания глаза. Спонсировано Национальным глазным институтом США. Препараты сравнения были произведены и представлены в рамках исследовательского соглашения компанией Bausch & Lomb
5 Age Related Eye Disease Study (AREDS) – исследование возрастного заболевания глаза. Спонсировано Национальным глазным институтом США. Препараты сравнения были произведены и представлены в рамках исследовательского соглашения компанией Bausch & Lomb
6 Rotterdam Study – исследование Rotterdam (Нидерланды)
7 Eye Disease Control Study – контрольное исследование заболеваний глаза (США)
8 Pathologies Oculaires Liées á l'Age (POLA) – исследование патологии глаз, связанной с возрастом (Франция)
9 Carotenoids in Age-Related Eye Disease Study (CAREDS) – каротиноиды в исследовании глазного заболевания, связанного с возрастом (США)
10 Carotenoids and co-antioxidants in Age-Related Maculopathy (CARMA) – каротиноиды и ко-антиоксиданты при связанной с возрастом макулопатии (Ирландия)
11 LUtein Nutrition effects measured by Auto-fluorescence (LUNA) – эффект добавления в питание лютеина, измеряемый аутофлюоресценцией (Германия)
12 MAHALO Study – исследование 2 фазы эффективности лампанизумаба при сухой форме ВМД.
Литература
1. McNamara D. Lampalizumab Appears Safe for Dry Macular Degeneration. - 2013. - URL: http://www.medscape.com/viewarticle/811878 (дата обра-щения: 02/11/2013).
2. Antioxidant status and neovascular age-related macular degeneration. Eye Disease Case-Control Study Group // Arch Ophthalmol. 1993. Vol. 111. № 1. P. 104–109.
3. A randomized, placebo-controlled, clinical trial of high-dose supplementation with vitamins C and E, beta carotene, and zinc for age-related macular degeneration and vision loss: AREDS report no. 8 // Arch Ophthalmol. 2001. Vol. 119. № 10. P. 1417–1436.
4. Lutein + zeaxanthin and omega-3 fatty acids for age-related macular degeneration: the Age-Related Eye Disease Study 2 (AREDS2) randomized clinical trial // JAMA. 2013. Vol. 309. № 19. P. 2005–2015.
5. Bernstein P.S., Zhao D. Y., Wintch S. W. et al. Resonance Raman measurement of macular carotenoids in normal subjects and in age-related macular degeneration patients // Ophthalmology. 2002. Vol. 109. № 10. P. 1780–1787.
6. Chong E.W., Robman L. D., Simpson J. A. et al. Fat consumption and its association with age-related macular degeneration // Arch Ophthalmol. 2009. Vol. 127. № 5. P. 674–680.
7. Clemons T.E., Kurinij N., Sperduto R. D. Associations of mortality with ocular disorders and an intervention of high-dose antioxidants and zinc in the Age-Related Eye Disease Study: AREDS Report No. 13 // Arch Ophthalmol. 2004. Vol. 122. № 5. P. 716–726.
8. Delcourt C., Carriere I., Delage M. et al. Plasma lutein and zeaxanthin and other carotenoids as modifiable risk factors for age-related maculopathy and cataract: the POLA Study // Invest Ophthalmol Vis Sci. 2006. Vol. 47. № 6. P. 2329–2335.
9. Eccles M., Clapp Z., Grimshaw J. et al. North of England evidence based guidelines development project: methods of guideline development // BMJ. 1996. Vol. 312. № 7033. P. 760–762.
10. Moeller S.M., Parekh N., Tinker L. et al. Associations between intermediate age-related macular degeneration and lutein and zeaxanthin in the Carotenoids in Age-related Eye Disease Study (CAREDS): ancillary study of the Women's Health Initiative // Arch Ophthalmol. 2006. Vol. 124. № 8. P. 1151–1162.
11. Neelam K., Hogg R. E., Stevenson M. R. et al. Carotenoids and co-antioxidants in age-related maculopathy: design and methods // Ophthalmic Epidemiol. 2008. Vol. 15. № 6. P. 389–401.
12. SanGiovanni J.P., Agron E., Clemons T.E. et al. Omega-3 long-chain polyunsaturated fatty acid intake inversely associated with 12-year progression to advanced age-related macular degeneration // Arch Ophthalmol. 2009. Vol. 127. № 1. P. 110–112.
13. SanGiovanni J.P., Chew E. Y., Agron E. et al. The relationship of dietary omega-3 long-chain polyunsaturated fatty acid intake with incident age-related macular degeneration: AREDS report no. 23 // Arch Ophthalmol. 2008. Vol. 126. № 9. P. 1274–1279.
14. SanGiovanni J.P., Chew E.Y., Clemons T.E., Davis M.D. et al. The relation-ship of dietary lipid intake and age-related macular degeneration in a case-control study: AREDS Report No. 20 // Arch Ophthalmol. 2007. Vol 125. № 5. P. 671–679.
15. Seddon J.M., Ajani U. A., Sperduto R. D. et al. Dietary carotenoids, vitamins A, C, and E, and advanced age-related macular degeneration. Eye Disease Case-Control Study Group // JAMA. 1994. Vol. 272. № 18. P. 1413–1420.
16. Tan J.S., Wang J. J., Flood V. et al. Dietary antioxidants and the long-term incidence of age-related macular degeneration: the Blue Mountains Eye Study // Ophthalmology. 2008. Vol. 115. № 2. P. 334–341.
17. Tan J.S., Wang J. J., Flood V. et al. Dietary fatty acids and the 10-year incidence of age-related macular degeneration: the Blue Mountains Eye Study // Arch Ophthalmol. 2009. Vol. 127. № 5. P. 656–665.
18. Trieschmann M., Beatty S., Nolan J. M. et al. Changes in macular pigment optical density and serum concentrations of its constituent carotenoids following supplemental lutein and zeaxanthin: the LUNA study // Exp Eye Res. 2007. Vol. 84. № 4. P. 718–728.
19. van Leeuwen R., Boekhoorn S., Vingerling J. R. et al. Dietary intake of antioxidants and risk of age-related macular degeneration // JAMA. 2005. Vol. 294. № 24. P. 3101–3107.
20. Van den Langenberg G.M., Mares-Perlman J.A., Klein R., Klein B.E. et al. Associations between antioxidant and zinc intake and the 5-year incidence of early age-related maculopathy in the Beaver Dam Eye Study // Am J Epidemiol. 1998. Vol. 148. № 2. P. 204–214.
21. West S., Vitale S., Hallfrisch J., Munoz B. et al. Are antioxidants or supplements protective for age-related macular degeneration? // Arch Ophthalmol. 1994. Vol. 112. № 2. P. 222–227.
22. Claver C. AMD Genetics. Effects of AMD-causing genes worst in smokers and those with poor diets // Eurotimes. 2012. Vol. 17. № 3. P. 28.
23. Delcourt C. Age-related macular degeneration // Modifiable risk factors for AMD./ Ed. by F. B. Loures: "Thea Portugal", 2010. P. 21–29.












