В настоящее время лечение злокачественных новообразований в печени представляет собой сложную многофакторную терапию, включающую, помимо резекции печени, применение современных противоопухолевых химиопрепаратов, использование рентгенохирургических технологий, локальных методов опухолевой деструкции, таких как крио– или термоаблация. Использование всех вышеперечисленных методик в комплексе позволяет существенно увеличить продолжительность жизни и улучшить ее качество у больных с данной опухолевой патологией.
Основной целью данной публикации является освещение принципов диагностики и лечения пациентов с метастатическим колоректальным раком печени на основании 19–летнего опыта работы хирургического отделения опухолей печени и поджелудочной железы РОНЦ им. Н.Н. Блохина РАМН.
Диагностика колоректального
метастатического поражения печени
Печень является органом–мишенью для метастазирования большинства опухолей различных локализаций. Первичная опухоль в зоне, дренируемой воротной веной, дает метастазы в 50% случаев [Curtiss, 1995]. У большинства пациентов с колоректальным раком развивается вторичное поражение печени. Диагностика метастатических опухолей у данной категории больных основана на периодическом лабораторном и инструментальном мониторинге, включающем определение уровня опухолевых маркеров, ультразвуковую или рентгеновскую компьютерную томографию и морфологическую верификацию диагноза в случае выявления опухолевого поражения печени.
Опухолевые маркеры – это определенные белки крови, уровень которых коррелирует в определенной степени с наличием злокачественной опухоли. При метастатическом колоректальном раке наиболее информативным маркером является раково–эмбриональный антиген (РЭА), открытый в 1965 г. Gold and Freedman. Специфичность данного показателя составляет порядка 60%. Регулярное определение РЭА после радикальных операций позволяет выявить рецидивы (в том числе бессимптомные) у 47% больных [3].
Помимо определения опухолевых маркеров диагностический алгоритм, направленный на выявление опухолевых очагов в печени, включает в себя различные методы лучевой диагностики. Наиболее универсальным и простым методом является ультразвуковое исследование. В подавляющем большинстве случаев данная методика способна дать ответы на все вопросы, необходимые для определения дальнейшей тактики лечения, т.е. определить количество и размеры опухолевых очагов, их локализацию. Под ультразвуковым контролем производится и тонкоигольная пункционная биопсия очагов в печени. Цитологическое исследование полученного данным путем материала является завершающим для постановки окончательного диагноза. Нами произведено несколько тысяч подобных манипуляций, причем большинство из них – амбулаторно, и мы не имели ни одного серьезного осложнения.
Рентгеновская компьютерная томография, магнитно–резонансная томография и ангиография применяются на дооперационном этапе для уточнения ряда параметров, необходимых для выработки тактики лечения, определения точной зоны поражения, соотношения с важными анатомическими структурами (особенно магастральными сосудами).
К другим факторам, необходимым для предоперационного обследования, относятся определение состояния кардио–респираторной и мочевыделительной систем, свертывающей системы крови, а также функционального состояния не пораженной опухолью паренхимы печени. Все это способствует оптимальному планированию предстоящего хирургического вмешательства.
Материалы и методы
Работа основана на анализе клинических наблюдений 415 больных, находившихся на лечении в хирургическом отделении опухолей печени и поджелудочной железы ГУ РОНЦ им. Н.Н. Блохина РАМН и перенесших радикальное хирургическое лечение по поводу колоректального метастатического поражения печени. Во всех случаях диагноз был морфологически верифицирован.
Всего нами выполнено 454 оперативных вмешательства по поводу метастазов рака толстой кишки в печень, из них экономные резекции печени составили 36,8% (n=167).
Наиболее часто метастатическое поражение печени определялось при локализации опухоли в ободочной кишке – 306 пациентов, что составило 67,4% от общего количества наблюдений. Второе место по частоте составили больные раком прямой кишки – 128 человек (28,2%). Мультицентричный рост опухоли определялся у 18 больных – 4,0%. Метастатическое поражение печени при опухолях перианальной зоны было выявлено у двух больных, что составило 0,4%.
У 180 пациентов метастатическое поражение печени было диагностировано одномоментно с первичным очагом, что составило 39,6% от общего числа больных.
Наиболее часто опухолевые очаги при колоректальном метастатическом поражении печени определялись в правой доле – 218 случаев (48,1%). Левая доля была поражена у 81 пациента, что составило 17,8% от общего числа наблюдений. Билобарное поражение печени присутствовало у 155 больных – 34,1%.
Мы дифференцировали пациентов также в зависимости от количества опухолевых очагов в печени. Солитарные метастазы были резецированы у 50% больных (n=227); единичные опухолевые очаги (не более трех) были подвергнуты оперативному лечению в 25,6% случаев (n=116); операции по поводу множественного метастатического поражения составили 24,2% от общего числа наблюдений (n=111).
Гемигепатэктомии или операции, при которых объем удаляемой паренхимы печени превышал правую или левую доли, перенесли 287 пациентов, что составило 63,2%.
У 62 больных с билобарным колоректальным метастатическим поражением печени гемигепатэктомия сочеталась с воздействием на очаги контралатеральной доли. Из них у 31 пациента резекция печени сочеталась с локальным циторедуктивным воздействием на опухолевые очаги в печени – криодеструкцией или радиочастотной термоаблацией.
Повторным резекциям печени по поводу рецидивов колоректальных метастазов в печени подверглись 39 пациентов.
Правосторонняя гемигепатэктомия по поводу колоректального метастатического поражения печени была выполнена у 220 пациентов, что составило 79% от общего числа наблюдений. Левосторонняя гемигепатэктомия выполнялась у 60 больных (21%).
Из 454 резекций печени, выполненных в нашем отделении по поводу метастатического рака толстой кишки, изолированное поражение печени отмечалось лишь в 329 случаях (72,5%). У 34 больных (7,5%) было выявлено распространение опухоли на соседние органы и структуры. У 91 пациента (20%) определялись внепеченочные метастазы
При распространении опухолевого очага на соседние органы и структуры наиболее предпочтительной тактикой, на наш взгляд, являлась резекция пораженных органов и тканей. Наиболее часто мы выполняли резекцию диафрагмы – 28 случаев – и паранефральной клетчатки – 12 случаев. При врастании опухоли в магистральные сосуды в 7 случаях нами выполнена резекция нижней полой вены и в двух случаях – воротной.
При внепеченочном метастатическом поражении, наиболее часто поражались лимфатические узлы ворот печени и чревного ствола – 73 пациента. Среди других внепеченочных проявлений основного заболевания у пациентов, перенесших резекции печени, следует отметить метастатическое поражение забрюшинных лимфатических узлов, метастазы в яичники, легкое, почку.
У 51 пациента с синхронным колоректальным метастатическим поражением печени выполнены симультанные операции. Основной объем операций на печени при симультанных операциях по поводу распространенного колоректального рака составили стандартные гемигепатэктомии.
С 1997 г. в рамках научной работы нашего отделения стала применяться адьювантная химиотерапия после резекции печени по поводу колоректальных метастазов. Всего дополнительное лекарственное лечение получили 293 пациента. Из них у 136 пациентов использовалась комбинация препаратов 5–фторурацил и кальция фолинат. С 2004 г. мы стали применять схему с включением Оксалиплатина – данную терапию получили 127 больных. Остальные пациенты в силу различных обстоятельств получали терапию с включением таких препаратов, как ралтитрексид, капецитабин, иринотекан и бевацизумаб. Применение комбинации 5–фторурацила и кальция фолината заключалось во введении 5–фторурацила 600 мг/м2 в сутки в виде 96–часовой инфузии, кальция фолината – 100 мг/м2 в сутки – струйно 1–4–й дни. Схема с включением оксалиплатина (FOLFOX 6) также подразумевает использование длительных инфузий и представляет собой применение препарата оксалиплатин в дозировке 100 мг/м2 в виде 2–часовой инфузии, кальция фолината 200 мг/м2 – 2–часовая инфузия, 5–фторурацила 400 мг/м2 – болюсное введение с последующим введением 5–фторурацила 2400–3000 мг/м2 путем 46–часовой инфузии.
Первый курс при обеих схемах проводился регионарно, в печеночную артерию, последующие – системно. Каждому больному планировалось проведение 6 курсов (при наличии внепеченочных метастазов – 8 курсов) химиотерапии. Среднее число полученных больными курсов составило 4,7. Уменьшение продолжительности терапии было обусловлено развившейся в ряде случаев токсичностью, а также прогрессированием основного заболевания на фоне проводимой химиотерапии или самостоятельным отказом больного от дальнейшего лечения.
Результаты
Средняя операционная кровопотеря у всех больных, перенесших резекции печени по поводу колоректального метастатического поражения (n=454), составила 1395,9 мл. Имеется прямая корреляция между объемом оперативного пособия и объемом кровопотери. При операциях наибольшего объема (трисекционэктомии) кровопотеря составила 1750 мл. У пациентов, перенесших трисекционэктомию с резекцией нижней полой вены (n=6), средний объем кровопотери составил 3860 мл, однако следует отметить, что у одного из шести пациентов данной группы кровопотеря составила 10 тыс. мл, что и привело к существенному увеличению среднего показателя в сравнении с общей группой. При стандартных гемигепатэктомиях объем кровопотери был несколько ниже и составил 1445,6 мл. Наименьшая кровопотеря получена нами при экономных резекциях печени – 950 мл.
При оценке среднего объема кровопотери у пациентов, перенесших резекции печени по поводу метастазов рака толстой кишки за последний год, отмечается снижение данного показателя до 1000,3 мл. Данный факт объясняется как совершенствованием технических аспектов выполнения оперативных вмешательств (максимальная сосудистая изоляция печени путем предварительной перевязки магистральных сосудов кавальных и портальных ворот, выполнение сегментоориентированных вмешательств), так и применением специальных технических средств, обеспечивающих гемостаз при рассечении паренхимы и обработке резецированной поверхности печени. К таким средствам следует отнести аппараты для радиочастотной аблации (RITA) с насадками для резекции печени (HABIB SEALER), аргоновые коагуляторы и гемостатические губки.
Снижению интраоперационной кровопотери также способствовал такой этап оперативного вмешательства, как пережатие гепатодуоденальной связки, выполняемый в момент резекции печени. Данная процедура, при продолжительности менее 25 мин. не приводила к увеличению риска развития печеночной недостаточности.
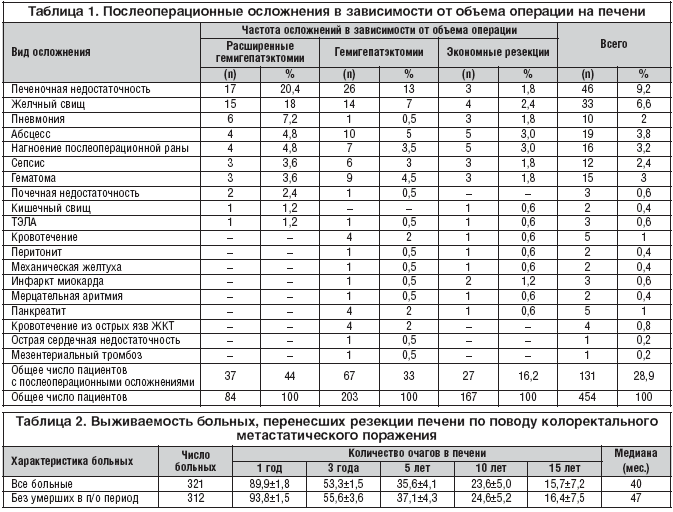
Послеоперационная летальность во всей исследуемой группе больных составила 3,5% (n=16), наиболее частая ее причина – острая печеночная недостаточность: данное осложнение стало фатальным для 6 больных, что составило 1,3% от общего числа наблюдений. Другой наиболее частой причиной послеоперационной летальности стало кровотечение в области операции – 2 пациента (0,4%). Такие осложнения, как пневмония, кровотечение из острых язв желудочно–кишечного тракта, перитонит, почечная недостаточность, тромбоэмболия легочной артерии, инфаркт миокарда, острая сердечная недостаточность и мезентериальный тромбоз, стали фатальными для остальных умерших больных данной группы. Летальность от данных осложнений составила по 0,2% от общего числа наблюдений. Учитывая то, что уровень послеоперационных осложнений напрямую зависит от объема оперативного вмешательства на печени, частота возникновения отдельных осложнений оценивалась нами как у всей исследуемой группы в целом, так и в отдельных группах пациентов, дифференцированных в зависимости от объема оперативного лечения. Осложнения после оперативного вмешательства на печени по поводу колоректальных метастазов выявлены у 28,9% больных (n=131).
Наибольшее число осложнений возникло у пациентов с предельно обширными резекциями печени (44%). Среди лиц, перенесших стандартные гемигепатэктомии, и у пациентов, перенесших экономные резекции печени, число послеоперационных осложнений было несколько меньше и составило 33 и 16,2% соответственно. На первом месте среди осложнений выступает печеночная недостаточность, возникшая вследствие недостаточного объема оставшейся части печени. Проявления печеночной недостаточности заключались в энцефалопатии, адинамии, желтушности кожных покровов, треморе кистей рук, а также в повышении печеночных ферментов (трансаминаз, щелочной фосфатазы), повышении свободного или связанного билирубина, гипоальбуминемии на 7–е сутки после хирургического вмешательства, асците. Следует отметить, что у подавляющего большинства пациентов печеночная недостаточность носила невыраженный характер и после адекватной терапии купировалась в 7–14–е сутки после оперативного лечения. Во всей исследуемой группе больных печеночная недостаточность возникла у 46 (9,2%) пациентов. У перенесших трисекционэктомии частота развития печеночной недостаточности составила 20,4% (n=17). У больных, подвергнутых операциям в объеме удаления доли печени или экономным резекциям, частота развития данного осложнения была достоверно ниже и составила 13 и 1,8% соответственно. На 2–м месте среди послеоперационных осложнений стоит желчеистечение (если оно носит продолжительный характер, то можно говорить о формировании желчного свища). Частота возникновения данного осложнения составила 6,6% (n=33). У пациентов с расширенными резекциями печени желчные свищи формировались в 18% случаев. У пациентов, перенесших стандартные гемигепатэктомии, – в 7%. После экономных резекций печени данное осложнение развивалось в 2,4% случаев. Третьим по частоте возникновения осложнением в исследуемой группе пациентов стало развитие послеоперационных абсцессов – 3,8% (n=19). Наиболее часто данное осложнение встретилось у пациентов, перенесших стандартную гемигепатэктомию – 5% (n=10). У пациентов с обширными резекциями печени частота послеоперационных абсцессов не превышала 4,8%, с экономными резекциями – 3,0%. Следующее часто возникающее после операций на печени осложнение – нагноение послеоперационной раны. Данное состояние развивалось у 3,2% больных (n=16) и наиболее часто встречалось у перенесших предельно обширные резекции печени – в 4,8%. Гематома в зоне резекции печени, сепсис и послеоперационная пневмония также относятся к достаточно частым осложнениям в исследуемой группе больных. Частота их развития составила 3,2, 3 и 2,4% соответственно. К остальным послеоперационным осложнениям следует отнести такие патологические состояния, как почечная недостаточность, кишечный свищ, тромбоэмболия легочной артерии, кровотечение в области операции, перитонит, механическая желтуха, инфаркт миокарда, мерцательная аритмия, панкреатит, кровотечение из острых язв желудочно–кишечного тракта, острая сердечная недостаточность и мезентериальный тромбоз. Частота развития данных осложнений в исследуемой группе варьировала от 0,2 до 1,0%. Приведенные данные представлены в таблице 1.
Отдаленные результаты прослежены у 312 пациентов, перенесших радикальные резекции печени по поводу колоректального метастатического поражения. Однолетняя выживаемость в данной группе больных составила 89,9±1,8%, 3–летняя – 53,3±1,5%, 5–летняя – 35,6±4,1%, 10–летняя – 23,6±5,0% и 15–летняя – 15,7±7,2%. Медиана – 40 мес. При исключении из данной группы пациентов, умерших в раннем послеоперационном периоде от хирургических осложнений, 5–летняя выживаемость составила 37,1±4,3%, 10–летняя – 24,6±5,2 % и 15–летняя – 16,4±7,5%. Медиана – 47 мес. Полученные данные отражены в таблице 2.
Мы оценили отдаленные результаты лечения больных с колоректальным метастатическим поражением печени, перенесших радикальные резекции, в зависимости от количества опухолевых очагов. Наилучшие результаты получены при солитарном метастатическом поражении печени. Пятилетняя выживаемость в данной группе составила 42,9±5,1%, 10–летняя – 28,8±6,4%. Медиана выживаемости – 50 мес. При единичных метастазах (не более трех) показатели выживаемости были несколько хуже – 5–летняя выживаемость составила 36,5±8,2%, 10–летняя – 25,5±8,8%. Медиана – 48 мес. Наиболее прогностически неблагоприятной оказалась группа пациентов со множественным опухолевым поражением печени. Десятилетней выживаемости у данной категории больных не получено, 5–летняя составила 18,7±14,6%. Медиана – 27 мес.
При оценке результатов лечения больных с различной распространенностью опухолевого процесса в печени в зависимости от объема оперативного лечения, мы не получили статистически достоверного различия между показателями выживаемости больных с солитарными и единичными опухолевыми очагами в печени, перенесших экономные либо обширные резекции печени. Так, 5–летняя выживаемость у пациентов, прооперированных в объеме стандартной или расширенной гемигепатэктомии при солитарном опухолевом поражении, составила 42,2±8,0%, при единичном – 46,6±11,0%. Медиана выживаемости составила 53 и 50 мес. соответственно. После экономных резекций печени 5–летняя выживаемость у больных с солитарными очагами составила 49,7±6,9%, с единичными – 36,8±11,6%. Медиана выживаемости – 48 и 50 мес. соответственно. Наихудшие результаты получены у больных с множественным метастатическим поражением печени, перенесших экономные резекции. Пятилетней выживаемости в данной группе не получено, 3–летняя составила 34,3±16,0. Медиана – 30 мес. После расширенных операций на печени при множественных метастазах колоректального рака результаты лечения были несколько лучше. Так, 5–летняя выживаемость составила 19,9±15,6% при медиане в 48 мес. Полученные результаты выживаемости в зависимости от объема оперативного лечения отражены в таблице 3.
Мы дифференцировали всех 65 пациентов с множественным очаговым поражением печени в зависимости от моно– или билобарной распространенности опухолевого процесса. При оценке отдаленных результатов лечения у этих групп пациентов достоверно лучшие результаты получены у больных с билобарными метастазами (n=49) – 5–летняя выживаемость составила 19,6±15,5% при медиане в 48 мес. При монолобарных множественных метастазах в печени 5–летней выживаемости не получено, а 3–летняя составила 40,7±15,6%. Медиана – 27 мес.
При обширной билобарной распространенности опухолевого процесса, не позволяющей произвести радикальную резекцию, у 20 пациентов мы выполняли гемигепатэктомию на стороне наибольшего опухолевого поражения печени, а очаги в оставшейся доле печени подвергали локальному аблативному противоопухолевому воздействию. К таким методам относятся прежде всего радиочастотная термоаблация или криодеструкция. Применение данных методик в сочетании с традиционным хирургическим подходом позволяло существенно увеличить радикализм оперативного вмешательства и удалить все определяемые опухолевые очаги у пациентов, ранее считавшихся неоперабельными. Пятилетняя выживаемость у данной категории больных составила 20,8±16,2% при медиане 26 мес.
Важнейшим моментом при определении объема оперативного вмешательства при колоректальном метастатическом поражении печени является удаление всех определяемых опухолевых очагов. У ряда пациентов мы выполнили паллиативные вмешательства на печени с циторедуктивной целью, удалив наибольший опухолевый массив. У других больных нерадикальность выполненной операции была определена только при гистологическом исследовании удаленного препарата, выявившем опухолевую ткань в крае резекции печени. Отдаленные результаты в данной группе пациентов крайне неудовлетворительны – 3–летней выживаемости не получено, а 2–летняя составила 21,1±8,6%. Медиана – 16 мес.
Также оставляют желать лучшего показатели выживаемости пациентов, перенесших резекции печени по поводу колоректального метастатического поражения при наличии доказанных внепеченочных метастазов. Пятилетняя выживаемость в данной группе составляет 8,6±5,1% при медиане 19 мес. Тем не менее в ряде случаев с циторедуктивной целью мы выполняем операции при подобной распространенности опухолевого процесса. Все больные с оставленными метастазами в печени либо с внепеченочными опухолевыми очагами в послеоперационный период нуждаются в проведении химиотерапии.
Большинство пациентов, перенесших радикальные резекции печени по поводу метастатического поражения при колоректальном раке, получали адьювантную химиотерапию по одной из принятых в отделении методик. Отдаленные результаты выживаемости 212 пациентов данной группы, получивших не менее трех курсов лекарственного лечения в послеоперационный период по схеме FOLFOX либо препаратами 5–фторурацил и кальция фолинат, мы сопоставили с показателями выживаемости 86 пациентов со сходной распространенностью опухолевого процесса, получивших только хирургическое лечение. В обеих группах были исключены из анализа пациенты, перенесшие повторные операции на печени или нерадикальные резекции, а также больные с внепеченочными метастазами. При комбинированном подходе 5–летняя выживаемость составила 42,6±5,7%, 10–летняя – 26,7±7,9. Медиана выживаемости – 53 мес. Данные показатели достоверно лучше результатов лечения больных, не получавших дополнительного лекарственного лечения, где 5–летняя выживаемость составила 25,5±6,1%, 10–летняя – 18,6±6,1% при медиане в 26 мес. Результаты отражены в таблице 4.
Обсуждение
Ежегодно в мире регистрируется более 600 тыс. новых случаев заболевания раком толстой кишки. В России показатель заболеваемости превышает 50 тыс. в год. Уровень выявления данной патологии на поздних стадиях достигает 70%, что обусловливает высокую летальность, достигающую 40% в течение первого года с момента выявления заболевания.
По данным зарубежной медицинской литературы, 5–летняя выживаемость у пациентов с колоректальным метастатическим поражением печени, не получавших специфического лечения, не превышает 2%, а медиана выживаемости колеблется от 6,6 до 10 мес. [13].
В настоящее время смертность после резекций печени по поводу метастазов колоректального рака составляет менее 6%, а в крупных специализированных клиниках – менее 3% [8,12,14]. Есть публикации, в которых приведен показатель послеоперационной летальности не более 0,8% [5]. Даже при резекциях печени с удалением более чем 80% печени летальность не превышает 5% в специализированных клиниках. По данным хирургического отделения опухолей печени и поджелудочной железы ГУ РОНЦ им. Н.Н. Блохина РАМН, послеоперационная летальность во всей исследуемой группе больных составила 3,5%. Наиболее частая причина послеоперационной летальности – острая печеночная недостаточность.
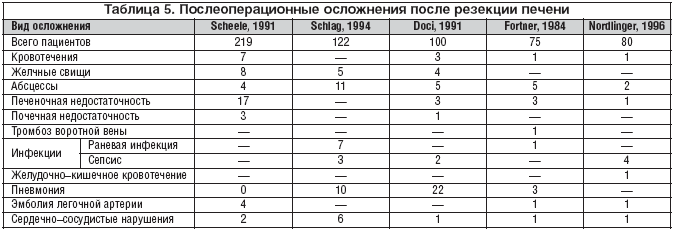
Самыми грозными осложнениями после резекции являются печеночная недостаточность и кровотечения. Всего послеоперационные осложнения встречаются у приблизительно 20–30% больных [6,7,9,10]. В таблице 5 представлены наиболее часто встречающиеся послеоперационные осложнения.
В нашей клинике осложнения после оперативного вмешательства на печени по поводу колоректальных метастазов выявлены у 28,9% больных. На первом месте среди осложнений выступает печеночная недостаточность. Во всей исследуемой группе больных, печеночная недостаточность возникла у 46 (9,2%) пациентов. Уровень данного осложнения напрямую коррелирует с объемом перенесенной резекции печени. Так, у больных с обширными резекциями печени частота печеночной недостаточности в послеоперационном периоде составила 20,4%. У больных, подвергнутых операциям в объеме удаления доли печени или экономным резекциям, частота развития данного осложнения была достоверно ниже и составила 13 и 1,8% соответственно.
Другими наиболее грозными послеоперационными осложнениями, по нашим данным, явились формирование желчных свищей и развитие послеоперационных абсцессов. Данные патологические состояния не стали причиной послеоперационной летальности и развивались в 6,6 и 3,8% случаев соответственно.
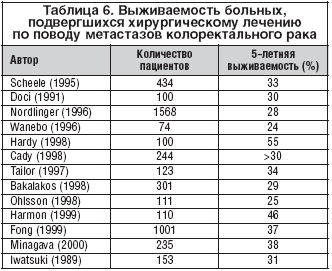
В случае выполнения радикальной резекции печени, по данным ряда авторов, 5–летняя выживаемость по поводу метастазов колоректального рака колеблется от 24 до 55%. Разброс в показателях обусловлен в значительной мере различными критериями при отборе больных для резекции печени, а также тем, что авторы пользуются различными методиками при подсчете выживаемости. Литературные данные, касающиеся выживаемости после хирургического лечения, представлены в таблице 6.
По нашим данным, 5–летняя выживаемость у всех радикально оперированных больных с колоректальным метастатическим поражением печени составила 37,1±4,3%, что значительно превышает среднемировой показатель.
Данные показатели получены у больных, единственным проявлением заболевания которых являлось очаговое поражение печени. При большей распространенности опухолевого процесса отдаленные результаты лечения были значительно хуже. Так, при наличии доказанных внепеченочных метастазов 5–летняя выживаемость составила 8,6±5,1% при медиане 19 мес. При нерадикально выполненной операции отдаленные результаты также крайне неудовлетворительны – 3–летней выживаемости не получено, а 2–летняя составила 21,1±8,6%. Медиана – 16 мес.
Наилучшие результаты лечения получены нами при применении комбинированного подхода – сочетания резекции печени с адьювантной химиотерапией. Пятилетняя выживаемость пациентов, получивших в послеоперационном периоде не менее 3 курсов лекарственного лечения по схеме FOLFOX либо препаратами 5–фторурацил и кальция фолинат, составила 42,6±5,7% при медиане в 53 мес. У больных, перенесших только оперативное лечение, 5–летняя выживаемость составила 25,5±6,1% при медиане в 26 мес. Полученные данные подтверждает исследование, проведенное Nordlinger c соавт. (2008), показавшее на примере 151 пациента с метастатическим колоректальным раком печени, что 3–летняя безрецидивная выживаемости после применения адьювантной химиотерапии по схеме FOLFOX достоверно выше, чем в группе только хирургического лечения (35,4% против 28,1%) [11].
Отдельного внимания заслуживают комбинированные вмешательства при колоректальном очаговом поражении печени, заключающиеся в сочетании оперативного удаления наибольшего опухолевого массива с локальными аблативными методами – такими как крио– или термодеструкция. Подобным вмешательствам в нашем отделении было подвергнуто 20 пациентов с обширной билобарной распространенностью опухолевого процесса. Пятилетняя выживаемость у данной категории больных составила 20,8±16,2% при медиане 26 мес., что позволяет считать данный подход целесообразным. Применение подобных методик позволяет выполнить радикальное вмешательство пациентам с обширным метастатическим поражением печени.
Заключение
Все приведенные выше данные, невысокий уровень летальности и допустимый уровень послеоперационных осложнений у оперированных пациентов с колоректальным метастатическим поражением печени, а также высокие показатели отдаленной выживаемости подтверждают тезис о необходимости применения комплексного подхода при лечении этого тяжелого контингента больных. Применение и комбинирование всех вышеперечисленных методик и схем лечения позволяет достичь наилучших результатов лечения.

Литература
1. Патютко Ю.И., Сагайдак И.В., Котельников А.Г., Бадалян Х.В., Подлужный Д.В. Хирургическое и комбинированное лечение метастазов колоректального рака в печень. Вестник московского онкологического общества, 2004, 2 (505), 4–5.
2. Патютко Ю.И., Сагайдак И.В., Котельников А.Г. Стратегия лечения метастазов колоректального рака в печень. Тезисы II съезда онкологов стран СНГ, Украина– Киев, 2000, 683.
3. Патютко Ю.И. Хирургическое лечение злокачественных опухолей печени. М. 2005.
4. Патютко Ю.И., Поляков А.Н., Сагайдак И.В., Котельников А.Г. Комбинированное лечение больных колоректальным раком с метастатическим поражением печени. Хирургия. Журнал им. Н.И.Пирогова. 2008;(7):20–3.
5. Adam R., Bismuth H., Castaing D., et al. Repeat hepatectomy for colorectal cancer liver metastases. Ann Surg 1997; 225:51–62.
6. Cole D., Ferguson C.M. Complication of hepatic resection for colorectal carcinoma metastasis. American Surgeon. 1992.V. 58. P. 88–91.
7. Hubert C, Gigot JF. Surgical management of colorectal liver metastases. Bull Cancer. 2008 Mar 1;95(3):365–8.
8. Hughes K.S., SimonR., Songhorabodi S. et al.: Resection of the liver for colorectal carcinoma metastases: a multi–institutional study of patterns of recurrence. Surgery 100:278–284,1986.
9. Leong S, Coffey JC, Hill AD. Hepatic resection for colorectal metastases. Value for risk scoring systems. Ann Surg. 2007 Aug;246(2):183–91
10. Minagawa M., Makuuchi M., Torzilli G., et al. Extension of the frontiers of surgical indications in the treatment of liver metastases from colorectal cancer. Ann. Surg. 2000, 231(4), 487–499.
11. Nordlinger B. et al. Perioperative chemotherapy with FOLFOX and surgey versus surgery alone for resectable liver metastases from colorectal cancer: a randomized controlled trial. Lancet. 2008 Mar 22; 371(9617): 1007 – 16.
12. Schlag P.Hohenberger P.,Herfath C.: Resection of liver metastases in colorectal cancer–competitive analysis of treatment results in synchronous versus metachronous metastases. Eur J. Surg. Oncol 16:360–365,1990.
13. Vigano L, Ferrero A, Lo Tesoriere R, Capussotti L. Liver surgery for colorectal metastases: results after 10 years of follow–up. Long–term survivors, late recurrences, and prognostic role of morbidity. Ann Surg Oncol. 2008 Sep;15(9):2458–64. Epub 2008 May 8.
14. Wang X, Hershman DL, Abrams JA, Feingold D, Grann VR, Jacobson JS, Neugut AI. Predictors of survival after hepatic resection among patients with colorectal liver metastasis. Br J Cancer. 2007 Dec 17;97(12):1606–12. Epub 2007 Dec 11.












