–ù–Β―¹–Φ–Ψ―²―Ä―è –Ϋ–Α ―¹―²–Ψ–Ι–Κ–Ψ–Β ―¹–Ϋ–Η–Ε–Β–Ϋ–Η–Β –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Β–Φ–Ψ―¹―²–Η ―Ä–Α–Κ–Ψ–Φ –Ε–Β–Μ―É–¥–Κ–Α, –Ψ―²–Φ–Β―΅–Β–Ϋ–Ϋ–Ψ–Β –≤ –±–Ψ–Μ―¨―à–Η–Ϋ―¹―²–≤–Β ―¹―²―Ä–Α–Ϋ –Φ–Η―Ä–Α, –≤ –Ω–Ψ―¹–Μ–Β–¥–Ϋ–Η–Β –≥–Ψ–¥―΄ –Ϋ–Α–±–Μ―é–¥–Α–Β―²―¹―è ―Ä–Ψ―¹―² ―΅–Α―¹―²–Ψ―²―΄ –Α–¥–Β–Ϋ–Ψ–Κ–Α―Ä―Ü–Η–Ϋ–Ψ–Φ―΄ –Ζ–Ψ–Ϋ―΄ –Κ–Α―Ä–¥–Η–Η –Η –Ω–Η―â–Β–≤–Ψ–¥–Ϋ–Ψ––Ε–Β–Μ―É–¥–Ψ―΅–Ϋ–Ψ–≥–Ψ –Ω–Β―Ä–Β―Ö–Ψ–¥–Α. –†–Ψ―¹―² –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Β–Φ–Ψ―¹―²–Η –≤ ―ç―²–Ψ–Ι –≥―Ä―É–Ω–Ω–Β –Ζ–Α –Ω–Ψ―¹–Μ–Β–¥–Ϋ–Η–Β –¥–≤–Α –¥–Β―¹―è―²–Η–Μ–Β―²–Η―è XX –≤–Β–Κ–Α –Ω―Ä–Β–≤―΄―à–Α–Β―² ―Ä–Ψ―¹―² ―΅–Α―¹―²–Ψ―²―΄ –¥―Ä―É–≥–Η―Ö –Ψ–Ϋ–Κ–Ψ–Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η–Ι – –±–Ψ–Μ–Β–Β 350% [1–5].
–£ –Γ–®–ê ―΅–Α―¹―²–Ψ―²–Α –Α–¥–Β–Ϋ–Ψ–Κ–Α―Ä―Ü–Η–Ϋ–Ψ–Φ―΄ –Ω―Ä–Ψ–Κ―¹–Η–Φ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ–Α –Ε–Β–Μ―É–¥–Κ–Α –Η –Ζ–Ψ–Ϋ―΄ –Ω–Η―â–Β–≤–Ψ–¥–Ϋ–Ψ––Ε–Β–Μ―É–¥–Ψ―΅–Ϋ–Ψ–≥–Ψ –Ω–Β―Ä–Β―Ö–Ψ–¥–Α ―É–≤–Β–Μ–Η―΅–Η–≤–Α–Β―²―¹―è ―²–Α–Κ –Η–Ϋ―²–Β–Ϋ―¹–Η–≤–Ϋ–Ψ, –Κ–Α–Κ –Ϋ–Η –Ψ–¥–Ϋ–Α –¥―Ä―É–≥–Α―è ―³–Ψ―Ä–Φ–Α –Ψ–Ω―É―Ö–Ψ–Μ–Η: –Β―¹–Μ–Η –≤ 1960 –≥–Ψ–¥―É –±–Ψ–Μ―¨–Ϋ―΄–Β ―Ä–Α–Κ–Ψ–Φ –Ω―Ä–Ψ–Κ―¹–Η–Φ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ–Α –Ε–Β–Μ―É–¥–Κ–Α ―¹–Ψ―¹―²–Α–≤–Μ―è–Μ–Η –Μ–Η―à―¨ 16%, ―²–Ψ –Κ –Ϋ–Α―΅–Α–Μ―É 80–―Ö – ―É–Ε–Β 44%, –Α –Κ –Κ–Ψ–Ϋ―Ü―É 90–―Ö – –±–Ψ–Μ–Β–Β 60% –Ψ―² –≤―¹–Β―Ö –Ζ–Α–±–Ψ–Μ–Β–≤―à–Η―Ö ―Ä–Α–Κ–Ψ–Φ –Ε–Β–Μ―É–¥–Κ–Α [6–12].
–î–Ψ―¹―²–Ψ–≤–Β―Ä–Ϋ–Ψ–≥–Ψ –Ψ–±―ä―è―¹–Ϋ–Β–Ϋ–Η―è –Ω―Ä–Η―΅–Η–Ϋ ―Ä–Ψ―¹―²–Α –Ψ–Ω―É―Ö–Ψ–Μ–Β–Ι –¥–Α–Ϋ–Ϋ–Ψ–Ι –Μ–Ψ–Κ–Α–Μ–Η–Ζ–Α―Ü–Η–Η –≤ –Ϋ–Α―¹―²–Ψ―è―â–Β–Β –≤―Ä–Β–Φ―è –Ω–Ψ––Ω―Ä–Β–Ε–Ϋ–Β–Φ―É –Ϋ–Β―².–™–Α―¹―²―Ä–Ψ―ç–Ζ–Ψ―³–Α–≥–Β–Α–Μ―¨–Ϋ―΄–Ι ―Ä–Β―³–Μ―é–Κ―¹, –Κ–Α–Κ –Ω―Ä–Η―΅–Η–Ϋ–Ϋ―΄–Ι ―³–Α–Κ―²–Ψ―Ä, –Ϋ–Β –Ψ―Ö–≤–Α―²―΄–≤–Α–Β―² –≤―¹–Β –Φ–Ϋ–Ψ–≥–Ψ–Ψ–±―Ä–Α–Ζ–Η–Β –Ψ–Ω―É―Ö–Ψ–Μ–Β–Ι –Ω–Η―â–Β–≤–Ψ–¥–Ϋ–Ψ––Ε–Β–Μ―É–¥–Ψ―΅–Ϋ–Ψ–≥–Ψ –Ω–Β―Ä–Β―Ö–Ψ–¥–Α – –Ζ–Ϋ–Α―΅–Β–Ϋ–Η–Β ―Ä–Β―³–Μ―é–Κ―¹–Α –¥–Ψ–Κ–Α–Ζ–Α–Ϋ–Ψ –¥–Μ―è –Ω–Η―â–Β–≤–Ψ–¥–Α –ë–Α―Ä―Ä–Β―²―²–Α, –Ϋ–Ψ –Ϋ–Β –¥–Μ―è ―Ä–Α–Κ–Α –Κ–Α―Ä–¥–Η–Η –Η ―¹―É–±–Κ–Α―Ä–¥–Η–Η.
–‰–Ζ––Ζ–Α ―¹–Ω–Β―Ü–Η―³–Η―΅–Ϋ–Ψ―¹―²–Η –Μ–Ψ–Κ–Α–Μ–Η–Ζ–Α―Ü–Η–Η –Ω―Ä–Β–¥―¹―²–Α–≤–Μ―è–Β–Φ―΄–Β –≤ –Μ–Η―²–Β―Ä–Α―²―É―Ä–Β –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η ―ç―²–Η―Ö –Ψ–Ω―É―Ö–Ψ–Μ–Β–Ι –Ω―Ä–Ψ―²–Η–≤–Ψ―Ä–Β―΅–Η–≤―΄. –î–Ψ –Ϋ–Α―¹―²–Ψ―è―â–Β–≥–Ψ –≤―Ä–Β–Φ–Β–Ϋ–Η ―¹―Ä–Β–¥–Η ―¹–Ω–Β―Ü–Η–Α–Μ–Η―¹―²–Ψ–≤ –Ϋ–Β―² –Β–¥–Η–Ϋ–Ψ–≥–Ψ –Φ–Ϋ–Β–Ϋ–Η―è –Ψ―²–Ϋ–Ψ―¹–Η―²–Β–Μ―¨–Ϋ–Ψ ―²–Β―Ä–Φ–Η–Ϋ–Α «–Κ–Α―Ä–¥–Η–Ψ―ç–Ζ–Ψ―³–Α–≥–Β–Α–Μ―¨–Ϋ―΄–Ι ―Ä–Α–Κ». –≠―²–Ψ –Ψ―²―Ä–Α–Ε–Α–Β―²―¹―è –≤ –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ –Ψ―²–Μ–Η―΅–Α―é―â–Η―Ö―¹―è ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Η―Ö –Ω–Ψ–¥―Ö–Ψ–¥–Α―Ö –Κ –Μ–Β―΅–Β–Ϋ–Η―é –Η –Ω–Ψ–Κ–Α–Ζ–Α―²–Β–Μ―è―Ö –≤―΄–Ε–Η–≤–Α–Β–Φ–Ψ―¹―²–Η –Ω–Ψ―¹–Μ–Β ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Μ–Β―΅–Β–Ϋ–Η―è. –€–Β–Ε–¥―É ―²–Β–Φ –Ω–Ψ―²―Ä–Β–±–Ϋ–Ψ―¹―²–Η –Κ–Μ–Η–Ϋ–Η―Ü–Η―¹―²–Ψ–≤ –Ψ–Ω―Ä–Β–¥–Β–Μ―è―é―² –Ϋ–Β–Ψ–±―Ö–Ψ–¥–Η–Φ–Ψ―¹―²―¨ –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η, –Ψ―²―Ä–Α–Ε–Α―é―â–Β–Ι –¥–Ψ―¹―²–Η–Ε–Β–Ϋ–Η―è –Η –Ω–Β―Ä―¹–Ω–Β–Κ―²–Η–≤―΄ –Μ–Β―΅–Β–Ϋ–Η―è ―ç―²–Ψ–≥–Ψ –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è.
–û–Ω―΄―² –Φ–Ϋ–Ψ–≥–Η―Ö –Κ―Ä―É–Ω–Ϋ―΄―Ö –Κ–Μ–Η–Ϋ–Η–Κ ―¹–≤–Η–¥–Β―²–Β–Μ―¨―¹―²–≤―É–Β―², ―΅―²–Ψ ―Ä–Α–Κ –Κ–Α―Ä–¥–Η–Ψ―ç–Ζ–Ψ―³–Α–≥–Β–Α–Μ―¨–Ϋ–Ψ–Ι –Ζ–Ψ–Ϋ―΄ –Η ―Ä–Α–Κ –¥―Ä―É–≥–Η―Ö –Ψ―²–¥–Β–Μ–Ψ–≤ –Ε–Β–Μ―É–¥–Κ–Α – ―ç―²–Ψ ―Ä–Α–Ζ–Μ–Η―΅–Ϋ―΄–Β –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è [Papa V. Et al., 2001; Doglietto GB et al., 2003; Kattan M. Et al., 2005]. –ü–Ψ―΅–Β–Φ―É –Κ–Α―Ä–¥–Η–Ψ―ç–Ζ–Ψ―³–Α–≥–Β–Α–Μ―¨–Ϋ―΄–Ι ―Ä–Α–Κ ―¹–Μ–Β–¥―É–Β―² ―¹―΅–Η―²–Α―²―¨ –Ψ―²–¥–Β–Μ―¨–Ϋ―΄–Φ –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η–Β–Φ? –ö–Α–Κ –Φ–Η–Ϋ–Η–Φ―É–Φ, ―²―Ä–Η ―¹–Μ–Β–¥―É―é―â–Η–Β –Ω―Ä–Η―΅–Η–Ϋ―΄ –Ψ–±–Ψ―¹–Ϋ–Ψ–≤―΄–≤–Α―é―² ―²–Α–Κ―É―é –Ϋ–Β–Ψ–±―Ö–Ψ–¥–Η–Φ–Ψ―¹―²―¨:
1) –Ψ–Ω―É―Ö–Ψ–Μ–Η, –Η―¹―Ö–Ψ–¥―è―â–Η–Β –Η–Ζ –Κ–Α―Ä–¥–Η–Α–Μ―¨–Ϋ–Ψ–Ι ―¹–Μ–Η–Ζ–Η―¹―²–Ψ–Ι –≤ –Ψ―²–Μ–Η―΅–Η–Β –Ψ―² ―Ä–Α–Κ–Α –¥―Ä―É–≥–Η―Ö –Ψ―²–¥–Β–Μ–Ψ–≤ –Ε–Β–Μ―É–¥–Κ–Α ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Η–Ζ―É―é―²―¹―è –±–Ψ–Μ–Β–Β –≤―΄―¹–Ψ–Κ–Η–Φ ―É―Ä–Ψ–≤–Ϋ–Β–Φ –Η–Ϋ―³–Η–Μ―¨―²―Ä–Α―Ü–Η–Η –Ω–Η―â–Β–≤–Ψ–¥–Α;
2) –Ψ–Ω―É―Ö–Ψ–Μ–Η –Κ–Α―Ä–¥–Η–Ψ―ç–Ζ–Ψ―³–Α–≥–Β–Α–Μ―¨–Ϋ–Ψ–Ι –Ζ–Ψ–Ϋ―΄ –Φ–Β―²–Α―¹―²–Α–Ζ–Η―Ä―É―é―² –Ϋ–Β ―²–Ψ–Μ―¨–Κ–Ψ –≤ –Α–±–¥–Ψ–Φ–Η–Ϋ–Α–Μ―¨–Ϋ―΄–Β, –Ϋ–Ψ –Η –≤ –Φ–Β–¥–Η–Α―¹―²–Η–Ϋ–Α–Μ―¨–Ϋ―΄–Β –Μ–Η–Φ―³–Ψ―É–Ζ–Μ―΄, ―΅―²–Ψ –Ω–Ψ–Ζ–≤–Ψ–Μ―è–Β―² ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Η–Ζ–Ψ–≤–Α―²―¨ –Ψ–Ω―É―Ö–Ψ–Μ–Η –¥–Α–Ϋ–Ϋ–Ψ–Ι –Μ–Ψ–Κ–Α–Μ–Η–Ζ–Α―Ü–Η–Η –Η –Κ–Α–Κ ―Ä–Α–Κ –Ε–Β–Μ―É–¥–Κ–Α, –Η –Κ–Α–Κ ―Ä–Α–Κ –Ω–Η―â–Β–≤–Ψ–¥–Α;
3) –≤–Α–Ε–Ϋ–Β–Ι―à–Β–Ι ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Η―¹―²–Η–Κ–Ψ–Ι –Κ–Α―Ä–¥–Η–Ψ―ç–Ζ–Ψ―³–Α–≥–Β–Α–Μ―¨–Ϋ–Ψ–≥–Ψ ―Ä–Α–Κ–Α, –Ω–Ψ–¥―²–≤–Β―Ä–Ε–¥–Α―é―â–Β–Ι –Β–≥–Ψ «–Η–Ϋ–¥–Η–≤–Η–¥―É–Α–Μ―¨–Ϋ–Ψ―¹―²―¨», ―è–≤–Μ―è–Β―²―¹―è –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ –±–Ψ–Μ–Β–Β –Ϋ–Β–±–Μ–Α–≥–Ψ–Ω―Ä–Η―è―²–Ϋ―΄–Ι –Ω―Ä–Ψ–≥–Ϋ–Ψ–Ζ, ―΅–Β–Φ –Ω―Ä–Η –Η–Ζ–Ψ–Μ–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ―΄―Ö –Ψ–Ω―É―Ö–Ψ–Μ–Β–≤―΄―Ö –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η―è―Ö –Ω–Η―â–Β–≤–Ψ–¥–Α –Η–Μ–Η –Ε–Β–Μ―É–¥–Κ–Α.
–ê–Ϋ–Α―²–Ψ–Φ–Η―è –Η ―²–Β―Ä–Φ–Η–Ϋ–Ψ–Μ–Ψ–≥–Η―è
–ü–Ψ –≤–Ψ–Ω―Ä–Ψ―¹―É –Ψ–Ω―Ä–Β–¥–Β–Μ–Β–Ϋ–Η―è –Η –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η ―Ä–Α–Κ–Α –Ω―Ä–Ψ–Κ―¹–Η–Φ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ–Α –Ε–Β–Μ―É–¥–Κ–Α –≤ –Μ–Η―²–Β―Ä–Α―²―É―Ä–Β ―¹―É―â–Β―¹―²–≤―É–Β―² –±–Ψ–Μ―¨―à–Ψ–Β –Κ–Ψ–Μ–Η―΅–Β―¹―²–≤–Ψ –Ω–Ψ―Ä–Ψ–Ι –≤–Β―¹―¨–Φ–Α –Ω―Ä–Ψ―²–Η–≤–Ψ―Ä–Β―΅–Η–≤―΄―Ö –Ψ–Ω―Ä–Β–¥–Β–Μ–Β–Ϋ–Η–Ι: «–Ψ–±–Μ–Α―¹―²―¨ –Ε–Β–Μ―É–¥–Κ–Α ―²–Ψ―²―΅–Α―¹ –Ϋ–Η–Ε–Β ―¹–Ψ–Β–¥–Η–Ϋ–Β–Ϋ–Η―è ―¹ –Ω–Η―â–Β–≤–Ψ–¥–Ψ–Φ, –Ω―Ä–Ψ–¥–Ψ–Μ–Ε–Α―é―â–Α―è―¹―è –Ϋ–Α –±–Ψ–Μ―¨―à―É―é –Κ―Ä–Η–≤–Η–Ζ–Ϋ―É, –≤–Κ–Μ―é―΅–Α―è –≤–Β―Ä―Ö–Ϋ―é―é ―΅–Α―¹―²―¨ –¥–Ϋ–Α –Ε–Β–Μ―É–¥–Κ–Α» [J. Garlock, 1942], «–Ψ–±–Μ–Α―¹―²―¨ –Ε–Β–Μ―É–¥–Κ–Α –Ω–Ψ –Φ–Α–Μ–Ψ–Ι –Κ―Ä–Η–≤–Η–Ζ–Ϋ–Β, ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤―É―é―â–Α―è –≤–Ψ―¹―Ö–Ψ–¥―è―â–Β–Ι –≤–Β―²–≤–Η –Μ–Β–≤–Ψ–Ι –Ε–Β–Μ―É–¥–Ψ―΅–Ϋ–Ψ–Ι –Α―Ä―²–Β―Ä–Η–Η» [–ë.–ï. –ü–Β―²–Β―Ä―¹–Ψ–Ϋ, 1972], «–Ω―Ä–Ψ–Κ―¹–Η–Φ–Α–Μ―¨–Ϋ–Α―è ―΅–Α―¹―²―¨ –Ε–Β–Μ―É–¥–Κ–Α –Ψ―² –Ω–Η―â–Β–≤–Ψ–¥–Ϋ–Ψ––Ε–Β–Μ―É–¥–Ψ―΅–Ϋ–Ψ–≥–Ψ –Ω–Β―Ä–Β―Ö–Ψ–¥–Α –¥–Ψ –Μ–Η–Ϋ–Η–Η, –Ω―Ä–Ψ―Ö–Ψ–¥―è―â–Β–Ι –Ϋ–Α ―É―Ä–Ψ–≤–Ϋ–Β –≤–Ψ―Ä–Ψ―² ―¹–Β–Μ–Β–Ζ–Β–Ϋ–Κ–Η» [–°.–ï. –ë–Β―Ä–Β–Ζ–Ψ–≤, 1976], «―΅–Α―¹―²―¨ –Ε–Β–Μ―É–¥–Κ–Α, ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤―É―é―â–Α―è ―Ä–Α–Ι–Ψ–Ϋ―É –≤–Β―²–≤–Μ–Β–Ϋ–Η―è –≤–Ψ―¹―Ö–Ψ–¥―è―â–Β–Ι –≤–Β―²–≤–Η –Μ–Β–≤–Ψ–Ι –Ε–Β–Μ―É–¥–Ψ―΅–Ϋ–Ψ–Ι –Α―Ä―²–Β―Ä–Η–Η, –Ψ―² –Κ–Ψ―²–Ψ―Ä–Ψ–Ι –Μ–Η–Φ―³–Α –Ψ―²―²–Β–Κ–Α–Β―² –Κ –Ω–Α―Ä–Α–Κ–Α―Ä–¥–Η–Α–Μ―¨–Ϋ―΄–Φ –Μ–Η–Φ―³–Α―²–Η―΅–Β―¹–Κ–Η–Φ ―É–Ζ–Μ–Α–Φ, –Ζ–Α–Ϋ–Η–Φ–Α―é―â–Α―è –Ω–Ψ–¥–Κ–Ψ–≤–Ψ–Ψ–±―Ä–Α–Ζ–Ϋ–Ψ–Β –Ω―Ä–Ψ―¹―²―Ä–Α–Ϋ―¹―²–≤–Ψ ―à–Η―Ä–Η–Ϋ–Ψ–Ι 5 ―¹–Φ ―É –≤―Ö–Ψ–¥–Α –≤ –Ε–Β–Μ―É–¥–Ψ–Κ» [–ê.–ê. –†―É―¹–Α–Ϋ–Ψ–≤, 1978], «―΅–Α―¹―²―¨ –Ε–Β–Μ―É–¥–Κ–Α –Ψ―² –≤―Ö–Ψ–¥–Α –¥–Ψ –Φ–Β―¹―²–Α –Ω–Β―Ä–Β―Ö–Ψ–¥–Α –Μ–Β–≤–Ψ–Ι –Ε–Β–Μ―É–¥–Ψ―΅–Ϋ–Ψ–Ι –Α―Ä―²–Β―Ä–Η–Η –Η–Ζ –Ε–Β–Μ―É–¥–Ψ―΅–Ϋ–Ψ––Ω–Ψ–¥–Ε–Β–Μ―É–¥–Ψ―΅–Ϋ–Ψ–Ι ―¹–≤―è–Ζ–Κ–Η –Ϋ–Α ―¹―²–Β–Ϋ–Κ―É –Ε–Β–Μ―É–¥–Κ–Α» [–ï.–ê. –£–Α–≥–Ϋ–Β―Ä, 1981]. –Δ–Α–Κ–Ψ–Β –Φ–Ϋ–Ψ–≥–Ψ–Ψ–±―Ä–Α–Ζ–Η–Β –≤–Ζ–≥–Μ―è–¥–Ψ–≤ –Ϋ–Β –Ω–Ψ–Ζ–≤–Ψ–Μ―è–Β―² ―¹–Η―¹―²–Β–Φ–Α―²–Η–Ζ–Η―Ä–Ψ–≤–Α―²―¨ –Ϋ–Α–Κ–Ψ–Ω–Μ–Β–Ϋ–Ϋ―΄–Ι –Ψ–Ω―΄―² –Η –Ψ–Ω―Ä–Β–¥–Β–Μ–Η―²―¨ –Α–¥–Β–Κ–≤–Α―²–Ϋ―É―é ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ―É―é ―²–Α–Κ―²–Η–Κ―É –≤ ―Ä–Α–Ζ–Μ–Η―΅–Ϋ―΄―Ö –Κ–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Η―Ö ―¹–Η―²―É–Α―Ü–Η―è―Ö.
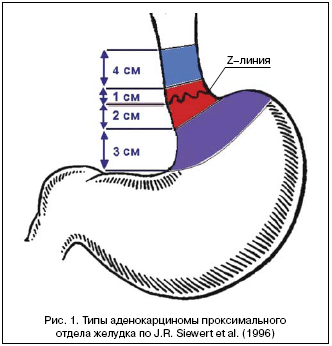
–ö–Α―Ä–¥–Η―è – ―¹–Ω–Β―Ü–Η―³–Η―΅–Β―¹–Κ–Η–Ι –Ψ―²–¥–Β–Μ –Ε–Β–Μ―É–¥–Κ–Α. –Γ ―³–Η–Ζ–Η–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Ψ–Ι ―²–Ψ―΅–Κ–Η –Ζ―Ä–Β–Ϋ–Η―è ―ç―²–Ψ ―¹―³–Η–Ϋ–Κ―²–Β―Ä, –Ω―Ä–Β–Ω―è―²―¹―²–≤―É―é―â–Η–Ι ―Ä–Β―³–Μ―é–Κ―¹―É –Ε–Β–Μ―É–¥–Ψ―΅–Ϋ–Ψ–≥–Ψ ―¹–Ψ–¥–Β―Ä–Ε–Η–Φ–Ψ–≥–Ψ –≤ –Ω–Η―â–Β–≤–Ψ–¥. –£–Ϋ–Β―à–Ϋ–Η–Φ –Ψ―Ä–Η–Β–Ϋ―²–Η―Ä–Ψ–Φ –Ω–Η―â–Β–≤–Ψ–¥–Ϋ–Ψ––Ε–Β–Μ―É–¥–Ψ―΅–Ϋ–Ψ–≥–Ψ –Ω–Β―Ä–Β―Ö–Ψ–¥–Α (–≤–Β―Ä―Ö–Ϋ―è―è –≥―Ä–Α–Ϋ–Η―Ü–Α –Κ–Α―Ä–¥–Η–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ε–Ψ–Φ–Α –Η–Μ–Η –Κ–Α―Ä–¥–Η–Α–Μ―¨–Ϋ–Ψ–Β –Ψ―²–≤–Β―Ä―¹―²–Η–Β) ―è–≤–Μ―è–Β―²―¹―è ―É―¹–Μ–Ψ–≤–Ϋ–Α―è –Μ–Η–Ϋ–Η―è, ―Ä–Α―¹–Ω–Ψ–Μ–Ψ–Ε–Β–Ϋ–Ϋ–Α―è –Ϋ–Α 0,5 ―¹–Φ –≤―΄―à–Β –Κ–Α―Ä–¥–Η–Α–Μ―¨–Ϋ–Ψ–Ι –≤―΄―Ä–Β–Ζ–Κ–Η (incisura cardialis) (―Ä–Η―¹. 1). –Γ–Ψ ―¹―²–Ψ―Ä–Ψ–Ϋ―΄ ―¹–Μ–Η–Ζ–Η―¹―²–Ψ–Ι –Κ–Α―Ä–¥–Η–Α–Μ―¨–Ϋ–Ψ–Φ―É –Ψ―²–≤–Β―Ä―¹―²–Η―é ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤―É–Β―² Z––Μ–Η–Ϋ–Η―è, ―è–≤–Μ―è―é―â–Α―è―¹―è –≥―Ä–Α–Ϋ–Η―Ü–Β–Ι –Φ–Β–Ε–¥―É –Ω–Μ–Ψ―¹–Κ–Η–Φ –Φ–Ϋ–Ψ–≥–Ψ―¹–Μ–Ψ–Ι–Ϋ―΄–Φ ―ç–Ω–Η―²–Β–Μ–Η–Β–Φ –Ω–Η―â–Β–≤–Ψ–¥–Α –Η –Ε–Β–Μ–Β–Ζ–Η―¹―²―΄–Φ –Ψ–¥–Ϋ–Ψ―Ä―è–¥–Ϋ―΄–Φ ―ç–Ω–Η―²–Β–Μ–Η–Β–Φ –Ε–Β–Μ―É–¥–Κ–Α.
–ö–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η―è
–Κ–Α―Ä–¥–Η–Ψ―ç–Ζ–Ψ―³–Α–≥–Β–Α–Μ―¨–Ϋ–Ψ–≥–Ψ ―Ä–Α–Κ–Α
–ö–Α–Κ ―É–Ε–Β –Ψ―²–Φ–Β―΅–Α–Μ–Ψ―¹―¨ –≤―΄―à–Β, ―Ä–Α–Κ –Ω―Ä–Ψ–Κ―¹–Η–Φ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ–Α –Ε–Β–Μ―É–¥–Κ–Α ―¹ –Ω–Β―Ä–Β―Ö–Ψ–¥–Ψ–Φ –Ϋ–Α –Ω–Η―â–Β–≤–Ψ–¥ (–Η–Μ–Η –Κ–Α―Ä–¥–Η–Ψ―ç–Ζ–Ψ―³–Α–≥–Β–Α–Μ―¨–Ϋ―΄–Ι ―Ä–Α–Κ) –Ϋ–Β –≤―΄–¥–Β–Μ–Β–Ϋ –≤ –Ψ―²–¥–Β–Μ―¨–Ϋ―É―é –Ϋ–Ψ–Ζ–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ―É―é –≥―Ä―É–Ω–Ω―É, –Ϋ–Β―¹–Φ–Ψ―²―Ä―è –Ϋ–Α –Β–≥–Ψ ―¹–≤–Ψ–Β–Ψ–±―Ä–Α–Ζ–Η–Β, ―²―Ä–Β–±―É―é―â–Β–Β ―¹–Α–Φ–Ψ―¹―²–Ψ―è―²–Β–Μ―¨–Ϋ–Ψ–Ι ―²–Α–Κ―²–Η–Κ–Η ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Μ–Β―΅–Β–Ϋ–Η―è. –≠―²–Ψ―² –Ω―Ä–Ψ–±–Β–Μ –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η, –Ψ–±―É―¹–Μ–Ψ–≤–Μ–Β–Ϋ–Ϋ―΄–Ι –Ψ―¹–Ψ–±–Β–Ϋ–Ϋ–Ψ―¹―²―è–Φ–Η –Κ–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Ψ–≥–Ψ ―²–Β―΅–Β–Ϋ–Η―è –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è, –Κ–Α―Ä–¥–Η–Ϋ–Α–Μ―¨–Ϋ–Ψ –Ψ―²–Μ–Η―΅–Α―é―â–Η–Φ–Η –Β–≥–Ψ –Η –Ψ―² ―Ä–Α–Κ–Α –Ε–Β–Μ―É–¥–Κ–Α –Η –Ψ―² ―Ä–Α–Κ–Α –Ω–Η―â–Β–≤–Ψ–¥–Α, –Φ–Ϋ–Ψ–≥–Η–Β ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Η–Β ―à–Κ–Ψ–Μ―΄ –Ω―΄―²–Α―é―²―¹―è –Ϋ–Η–≤–Β–Μ–Η―Ä–Ψ–≤–Α―²―¨ –Ω―Ä–Η–Φ–Β–Ϋ–Β–Ϋ–Η–Β–Φ ―¹–Ψ–±―¹―²–≤–Β–Ϋ–Ϋ―΄―Ö –≤–Α―Ä–Η–Α–Ϋ―²–Ψ–≤ –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η –Μ–Η–±–Ψ –Η―¹–Ω–Ψ–Μ―¨–Ζ–Ψ–≤–Α–Ϋ–Η–Β–Φ ―É–¥–Ψ–±–Ϋ–Ψ–≥–Ψ, –Ψ―²–≤–Β―΅–Α―é―â–Β–≥–Ψ –≤–Ζ–≥–Μ―è–¥–Α–Φ –Α–≤―²–Ψ―Ä–Ψ–≤ –Ω–Ψ–¥―Ö–Ψ–¥–Α. –ü―Ä–Η―΅–Β–Φ –Ζ–Α―΅–Α―¹―²―É―é ―²–Α–Κ–Η–Β –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η, –Ω―Ä–Β―²–Β–Ϋ–¥―É―é―â–Η–Β –Ϋ–Α ―Ä–Ψ–Μ―¨ ―É–Ϋ–Η–≤–Β―Ä―¹–Α–Μ―¨–Ϋ―΄―Ö, –Ψ―²―Ä–Α–Ε–Α―é―² –Μ–Η―à―¨ –¥–Ψ–Κ―²―Ä–Η–Ϋ―É –Ψ―²–¥–Β–Μ―¨–Ϋ―΄―Ö ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Η―Ö ―à–Κ–Ψ–Μ –Η –Ϋ–Β –Φ–Ψ–≥―É―² –≤ –Ω–Ψ–Μ–Ϋ–Ψ–Ι –Φ–Β―Ä–Β ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤–Ψ–≤–Α―²―¨ ―²–Β–Φ –¥–Ψ―¹―²–Η–Ε–Β–Ϋ–Η―è–Φ ―ç–≤–Ψ–Μ―é―Ü–Η–Η ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Φ–Β―²–Ψ–¥–Α, –Κ–Ψ―²–Ψ―Ä―΄–Β –Ϋ–Α ―¹–Β–≥–Ψ–¥–Ϋ―è―à–Ϋ–Η–Ι –¥–Β–Ϋ―¨ –≤–Ψ –Φ–Ϋ–Ψ–≥–Η―Ö –Κ–Μ–Η–Ϋ–Η–Κ–Α―Ö ―è–≤–Μ―è―é―²―¹―è ―¹―²–Α–Ϋ–¥–Α―Ä―²–Ψ–Φ.
–ü―Ä–Α–Κ―²–Η―΅–Β―¹–Κ–Η –Ζ–Ϋ–Α―΅–Η–Φ―΄–Φ –Ω―Ä–Η–Φ–Β―Ä–Ψ–Φ –Ω–Ψ–Ω―΄―²–Κ–Η ―¹–Ψ–Ζ–¥–Α–Ϋ–Η―è ―É–Ϋ–Η–≤–Β―Ä―¹–Α–Μ―¨–Ϋ–Ψ–Ι –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η –¥–Μ―è –Α–¥–Β–Ϋ–Ψ–Κ–Α―Ä―Ü–Η–Ϋ–Ψ–Φ―΄ –Ζ–Ψ–Ϋ―΄ –Ω–Η―â–Β–≤–Ψ–¥–Ϋ–Ψ––Ε–Β–Μ―É–¥–Ψ―΅–Ϋ–Ψ–≥–Ψ –Ω–Β―Ä–Β―Ö–Ψ–¥–Α ―è–≤–Μ―è–Β―²―¹―è –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η―è, –Ω―Ä–Β–¥–Μ–Ψ–Ε–Β–Ϋ–Ϋ–Α―è J.R. Siewert, A.H. Holscher –Η ―¹–Ψ–Α–≤―². –≤ 1996 –≥–Ψ–¥―É [13]. –£ –Ψ―¹–Ϋ–Ψ–≤―É –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η –Ω–Ψ–Μ–Ψ–Ε–Β–Ϋ―΄ –¥–≤–Α –Ω―Ä–Η–Ϋ―Ü–Η–Ω–Α, –Ψ–±―ä–Β–¥–Η–Ϋ–Β–Ϋ–Ϋ―΄–Β –≤–Φ–Β―¹―²–Β: –≥–Η―¹―²–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Α―è ―¹―²―Ä―É–Κ―²―É―Ä–Α –Ψ–Ω―É―Ö–Ψ–Μ–Η – –Α–¥–Β–Ϋ–Ψ–Κ–Α―Ä―Ü–Η–Ϋ–Ψ–Φ–Α –Η –Β–Β –Μ–Ψ–Κ–Α–Μ–Η–Ζ–Α―Ü–Η―è –≤ –Ζ–Ψ–Ϋ–Β –Ω–Η―â–Β–≤–Ψ–¥–Ϋ–Ψ––Ε–Β–Μ―É–¥–Ψ―΅–Ϋ–Ψ–≥–Ψ –Ω–Β―Ä–Β―Ö–Ψ–¥–Α. –û–Ω―Ä–Β–¥–Β–Μ―è―é―â–Η–Φ ―³–Α–Κ―²–Ψ―Ä–Ψ–Φ ―è–≤–Μ―è–Β―²―¹―è –Μ–Ψ–Κ–Α–Μ–Η–Ζ–Α―Ü–Η―è ―ç–Ω–Η―Ü–Β–Ϋ―²―Ä–Α –Ψ–Ω―É―Ö–Ψ–Μ–Η –Ψ―²–Ϋ–Ψ―¹–Η―²–Β–Μ―¨–Ϋ–Ψ –Ω–Η―â–Β–≤–Ψ–¥–Ϋ–Ψ––Ε–Β–Μ―É–¥–Ψ―΅–Ϋ–Ψ–≥–Ψ –Ω–Β―Ä–Β―Ö–Ψ–¥–Α –Η –Ζ–Ψ–Ϋ―΄ –Α–Ϋ–Α―²–Ψ–Φ–Η―΅–Β―¹–Κ–Ψ–Ι –Κ–Α―Ä–¥–Η–Η. –ê–Ϋ–Α―²–Ψ–Φ–Η―΅–Β―¹–Κ–Η–Ι ―Ü–Β–Ϋ―²―Ä –Ψ–Ω―É―Ö–Ψ–Μ–Η –Η–¥–Β–Ϋ―²–Η―³–Η―Ü–Η―Ä―É–Β―²―¹―è –Ϋ–Α –Ψ―¹–Ϋ–Ψ–≤–Α–Ϋ–Η–Η ―Ä–Β–Ϋ―²–≥–Β–Ϋ–Ψ–Κ–Ψ–Ϋ―²―Ä–Α―¹―²–Ϋ–Ψ–≥–Ψ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è, ―³–Η–±―Ä–Ψ–≥–Α―¹―²―Ä–Ψ―¹–Κ–Ψ–Ω–Η–Η –Η –¥–Α–Ϋ–Ϋ―΄―Ö –Η–Ϋ―²―Ä–Α–Ψ–Ω–Β―Ä–Α―Ü–Η–Ψ–Ϋ–Ϋ–Ψ–Ι ―Ä–Β–≤–Η–Ζ–Η–Η.
–ê–≤―²–Ψ―Ä―΄ –≤―΄–¥–Β–Μ―è―é―² 3 ―²–Η–Ω–Α –Ψ–Ω―É―Ö–Ψ–Μ–Η ―¹ ―É―΅–Β―²–Ψ–Φ –Μ–Ψ–Κ–Α–Μ–Η–Ζ–Α―Ü–Η–Η ―Ü–Β–Ϋ―²―Ä–Α –Ϋ–Ψ–≤–Ψ–Ψ–±―Ä–Α–Ζ–Ψ–≤–Α–Ϋ–Η―è (―Ä–Η―¹. 1):
- I ―²–Η–Ω – –Α–¥–Β–Ϋ–Ψ–Κ–Α―Ä―Ü–Η–Ϋ–Ψ–Φ–Α –¥–Η―¹―²–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ–Α –Ω–Η―â–Β–≤–Ψ–¥–Α, ―ç–Ω–Η―Ü–Β–Ϋ―²―Ä –Κ–Ψ―²–Ψ―Ä–Ψ–Ι ―Ä–Α―¹–Ω–Ψ–Μ–Ψ–Ε–Β–Ϋ –≤ –Ω―Ä–Β–¥–Β–Μ–Α―Ö –Ψ―² 1 –¥–Ψ 5 ―¹–Φ –≤―΄―à–Β –Ζ–Ψ–Ϋ―΄ –Ω–Η―â–Β–≤–Ψ–¥–Ϋ–Ψ––Ε–Β–Μ―É–¥–Ψ―΅–Ϋ–Ψ–≥–Ψ –Ω–Β―Ä–Β―Ö–Ψ–¥–Α (Z––Μ–Η–Ϋ–Η–Η) ―¹ –≤–Ψ–Ζ–Φ–Ψ–Ε–Ϋ–Ψ―¹―²―¨―é ―Ä–Α―¹–Ω―Ä–Ψ―¹―²―Ä–Α–Ϋ–Β–Ϋ–Η―è ―΅–Β―Ä–Β–Ζ –Ω–Ψ―¹–Μ–Β–¥–Ϋ―é―é –≤ ―¹―²–Ψ―Ä–Ψ–Ϋ―É –Ε–Β–Μ―É–¥–Κ–Α.
- II ―²–Η–Ω – –Η―¹―²–Η–Ϋ–Ϋ–Α―è –Α–¥–Β–Ϋ–Ψ–Κ–Α―Ä―Ü–Η–Ϋ–Ψ–Φ–Α –Ζ–Ψ–Ϋ―΄ –Ω–Η―â–Β–≤–Ψ–¥–Ϋ–Ψ––Ε–Β–Μ―É–¥–Ψ―΅–Ϋ–Ψ–≥–Ψ –Ω–Β―Ä–Β―Ö–Ψ–¥–Α (–Η―¹―²–Η–Ϋ–Ϋ―΄–Ι ―Ä–Α–Κ –Κ–Α―Ä–¥–Η–Η), ―ç–Ω–Η―Ü–Β–Ϋ―²―Ä ―Ä–Α―¹–Ω–Ψ–Μ–Ψ–Ε–Β–Ϋ –≤ –Ω―Ä–Β–¥–Β–Μ–Α―Ö 1 ―¹–Φ –Ω―Ä–Ψ–Κ―¹–Η–Φ–Α–Μ―¨–Ϋ–Ψ (–Ψ―Ä–Α–Μ―¨–Ϋ–Ψ) –Η 2 ―¹–Φ –¥–Η―¹―²–Α–Μ―¨–Ϋ–Ψ (–Α–±–Ψ―Ä–Α–Μ―¨–Ϋ–Ψ) –Ψ―² Z––Μ–Η–Ϋ–Η–Η.
- III ―²–Η–Ω – ―Ä–Α–Κ ―¹ –Μ–Ψ–Κ–Α–Μ–Η–Ζ–Α―Ü–Η–Β–Ι –Ψ―¹–Ϋ–Ψ–≤–Ϋ–Ψ–≥–Ψ –Φ–Α―¹―¹–Η–≤–Α –Ψ–Ω―É―Ö–Ψ–Μ–Η –≤ ―¹―É–±–Κ–Α―Ä–¥–Η–Α–Μ―¨–Ϋ–Ψ–Φ –Ψ―²–¥–Β–Μ–Β –Ε–Β–Μ―É–¥–Κ–Α (–Ψ―² 2 –¥–Ψ 5 ―¹–Φ –Α–±–Ψ―Ä–Α–Μ―¨–Ϋ–Ψ –Ψ―² Z––Μ–Η–Ϋ–Η–Η) –Η –≤–Ψ–Ζ–Φ–Ψ–Ε–Ϋ―΄–Φ –≤–Ψ–≤–Μ–Β―΅–Β–Ϋ–Η–Β–Φ –¥–Η―¹―²–Α–Μ―¨–Ϋ―΄―Ö –Ψ―²–¥–Β–Μ–Ψ–≤ –Ω–Η―â–Β–≤–Ψ–¥–Α.
–£–Α–Ε–Ϋ–Ψ―¹―²―¨ –¥–Ψ–Ψ–Ω–Β―Ä–Α―Ü–Η–Ψ–Ϋ–Ϋ–Ψ–Ι –Η–¥–Β–Ϋ―²–Η―³–Η–Κ–Α―Ü–Η–Η ―²–Η–Ω–Α –Ψ–Ω―É―Ö–Ψ–Μ–Η –Ζ–Α–Κ–Μ―é―΅–Α–Β―²―¹―è –≤ –≤–Ψ–Ζ–Φ–Ψ–Ε–Ϋ–Ψ―¹―²–Η –Ω–Μ–Α–Ϋ–Η―Ä–Ψ–≤–Α―²―¨ –Ψ–±―ä–Β–Φ –Ψ–Ω–Β―Ä–Α―Ü–Η–Η –Η –Ψ–Ω―Ä–Β–¥–Β–Μ–Η―²―¨―¹―è ―¹ –≤―΄–±–Ψ―Ä–Ψ–Φ ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –¥–Ψ―¹―²―É–Ω–Α.
–ö–Μ–Η–Ϋ–Η–Κ–Ψ––Φ–Ψ―Ä―³–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Η–Β
–Ψ―¹–Ψ–±–Β–Ϋ–Ϋ–Ψ―¹―²–Η –Κ–Α―Ä–¥–Η–Ψ―ç–Ζ–Ψ―³–Α–≥–Β–Α–Μ―¨–Ϋ–Ψ–≥–Ψ ―Ä–Α–Κ–Α
–Γ―Ä–Α–≤–Ϋ–Η―²–Β–Μ―¨–Ϋ–Α―è ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Η―¹―²–Η–Κ–Α ―²―Ä–Β―Ö ―²–Η–Ω–Ψ–≤ –Κ–Α―Ä–¥–Η–Ψ―ç–Ζ–Ψ―³–Α–≥–Β–Α–Μ―¨–Ϋ–Ψ–≥–Ψ ―Ä–Α–Κ–Α, –Ω―Ä–Ψ–≤–Β–¥–Β–Ϋ–Ϋ–Α―è –≥―Ä―É–Ω–Ω–Ψ–Ι J.R. Siewert (Technische Universita–Βt Mu–Βnchen, Germany) –Η –±–Α–Ζ–Η―Ä―É―é―â–Α―è―¹―è –Ϋ–Α ―Ä–Β–Ζ―É–Μ―¨―²–Α―²–Α―Ö –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è 1002 –±–Ψ–Μ―¨–Ϋ―΄―Ö, –Ω–Ψ–Ζ–≤–Ψ–Μ―è–Β―² –Ψ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Η–Ζ–Ψ–≤–Α―²―¨ –Κ–Α–Ε–¥―΄–Ι ―²–Η–Ω –Ψ–Ω―É―Ö–Ψ–Μ–Η:
–Δ–Η–Ω I AEG: –Κ–Α–Κ –Ω―Ä–Α–≤–Η–Μ–Ψ (80–100%, –Ω–Ψ –¥–Α–Ϋ–Ϋ―΄–Φ ―Ä–Α–Ζ–Ϋ―΄―Ö –Α–≤―²–Ψ―Ä–Ψ–≤), ―Ä–Α–Ζ–≤–Η–≤–Α–Β―²―¹―è –Η–Ζ –Φ–Β―²–Α–Ω–Μ–Α–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ–Ψ–≥–Ψ ―ç–Ω–Η―²–Β–Μ–Η―è –Ω–Η―â–Β–≤–Ψ–¥–Α (–Ω–Η―â–Β–≤–Ψ–¥ –ë–Α―Ä―Ä–Β―²―²–Α). –½–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ –Ω―Ä–Β–Ψ–±–Μ–Α–¥–Α–Β―² –Κ–Η―à–Β―΅–Ϋ–Α―è ―³–Ψ―Ä–Φ–Α –Ψ–Ω―É―Ö–Ψ–Μ–Η –Ω–Ψ –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η Lauren. –û―²–Ϋ–Ψ―¹–Η―²–Β–Μ―¨–Ϋ–Ψ –Ϋ–Β–≤―΄―¹–Ψ–Κ–Η–Ι ―É–¥–Β–Μ―¨–Ϋ―΄–Ι –≤–Β―¹ –Ψ–Ω―É―Ö–Ψ–Μ–Β–Ι ―¹ –≤―΄―Ö–Ψ–¥–Ψ–Φ –Ϋ–Α ―¹–Β―Ä–Ψ–Ζ―É.
–Δ–Η–Ω II AEG: ―΅–Α―â–Β ―Ä–Α–Ζ–≤–Η–≤–Α–Β―²―¹―è –Η–Ζ ―ç–Ω–Η―²–Β–Μ–Η―è –Κ–Α―Ä–¥–Η–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ–Α –Ε–Β–Μ―É–¥–Κ–Α, –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ ―Ä–Β–Ε–Β –Η–Ζ –Φ–Β―²–Α–Ω–Μ–Α–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ–Ψ–≥–Ψ ―ç–Ω–Η―²–Β–Μ–Η―è –Ω–Η―â–Β–≤–Ψ–¥–Α (―΅–Α―¹―²–Ψ―²–Α –Ω–Η―â–Β–≤–Ψ–¥–Α –ë–Α―Ä―Ä–Β―²―²–Α –Ω―Ä–Η II ―²–Η–Ω–Β ―¹–Ψ―¹―²–Α–≤–Μ―è–Β―² 10%). –ü―Ä–Β–Ψ–±–Μ–Α–¥–Α–Β―² –¥–Η―³―³―É–Ζ–Ϋ–Α―è ―³–Ψ―Ä–Φ–Α –Ψ–Ω―É―Ö–Ψ–Μ–Η –Ω–Ψ –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η Lauren. –Γ–Α–Φ―΄–Ι –Ϋ–Η–Ζ–Κ–Η–Ι ―¹―Ä–Β–¥–Η –≤―¹–Β―Ö ―²―Ä–Β―Ö ―²–Η–Ω–Ψ–≤ ―É–¥–Β–Μ―¨–Ϋ―΄–Ι –≤–Β―¹ –Ψ–Ω―É―Ö–Ψ–Μ–Β–Ι ―¹ –Η–Ϋ–≤–Α–Ζ–Η–Β–Ι ―¹–Β―Ä–Ψ–Ζ―΄ (29%).
–Δ–Η–Ω III AEG: –Ω―Ä–Β–¥―¹―²–Α–≤–Μ―è–Β―² ―¹–Ψ–±–Ψ–Ι –Ψ–¥–Ϋ―É –Η–Ζ ―³–Ψ―Ä–Φ –Ω―Ä–Ψ–Κ―¹–Η–Φ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ ―Ä–Α–Κ–Α –Ε–Β–Μ―É–¥–Κ–Α. –ö–Η―à–Β―΅–Ϋ–Α―è –Φ–Β―²–Α–Ω–Μ–Α–Ζ–Η―è ―ç–Ω–Η―²–Β–Μ–Η―è –Ω–Η―â–Β–≤–Ψ–¥–Α –¥–Μ―è ―ç―²–Ψ–≥–Ψ ―²–Η–Ω–Α –Ϋ–Β ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Ϋ–Α (―΅–Α―¹―²–Ψ―²–Α –Ω–Η―â–Β–≤–Ψ–¥–Α –ë–Α―Ä―Ä–Β―²―²–Α –Μ–Η―à―¨ 2%). –ù–Α–Η–±–Ψ–Μ–Β–Β –Ϋ–Β–±–Μ–Α–≥–Ψ–Ω―Ä–Η―è―²–Ϋ–Α―è –Φ–Ψ―Ä―³–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Α―è ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Η―¹―²–Η–Κ–Α ―¹―Ä–Β–¥–Η –≤―¹–Β―Ö ―²―Ä–Β―Ö ―²–Η–Ω–Ψ–≤: ―¹–Α–Φ―΄–Ι –≤―΄―¹–Ψ–Κ–Η–Ι ―É–¥–Β–Μ―¨–Ϋ―΄–Ι –≤–Β―¹ –Ϋ–Β–¥–Η―³―³–Β―Ä–Β–Ϋ―Ü–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ―΄―Ö –Η –¥–Η―³―³―É–Ζ–Ϋ―΄―Ö ―³–Ψ―Ä–Φ, –Η–Ϋ–≤–Α–Ζ–Η–Η ―¹–Β―Ä–Ψ–Ζ–Ϋ–Ψ–Ι –Ψ–±–Ψ–Μ–Ψ―΅–Κ–Η, –Μ–Η–Φ―³–Ψ–≥–Β–Ϋ–Ϋ―΄―Ö –Η –Ψ―²–¥–Α–Μ–Β–Ϋ–Ϋ―΄―Ö –Φ–Β―²–Α―¹―²–Α–Ζ–Ψ–≤. –Γ―É―â–Β―¹―²–≤―É–Β―² –≥–Η–Ω–Ψ―²–Β–Ζ–Α, ―΅―²–Ψ –Ψ–¥–Ϋ–Ψ–Ι –Η–Ζ –Ω―Ä–Η―΅–Η–Ϋ –Ω―Ä–Β–Ψ–±–Μ–Α–¥–Α–Ϋ–Η―è –Ζ–Α–Ω―É―â–Β–Ϋ–Ϋ―΄―Ö ―¹―²–Α–¥–Η–Ι –Ω―Ä–Η –Κ–Α―Ä–¥–Η–Ψ―ç–Ζ–Ψ―³–Α–≥–Β–Α–Μ―¨–Ϋ–Ψ–Φ ―Ä–Α–Κ–Β III ―²–Η–Ω–Α (–Ψ–Κ–Ψ–Μ–Ψ 70%) ―è–≤–Μ―è–Β―²―¹―è –Ω–Ψ–Ζ–¥–Ϋ–Β–Β –Ω–Ψ―è–≤–Μ–Β–Ϋ–Η–Β –¥–Η―¹―³–Α–≥–Η–Η.
–ü–Ψ –Φ–Ϋ–Β–Ϋ–Η―é –Α–≤―²–Ψ―Ä–Ψ–≤ –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η, –Α ―²–Α–Κ–Ε–Β ―¹–Ω–Β―Ü–Η–Α–Μ–Η―¹―²–Ψ–≤, –Η–Φ–Β―é―â–Η―Ö –Ψ–Ω―΄―² ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Μ–Β―΅–Β–Ϋ–Η―è –Α–¥–Β–Ϋ–Ψ–Κ–Α―Ä―Ü–Η–Ϋ–Ψ–Φ –Κ–Α―Ä–¥–Η–Ψ―ç–Ζ–Ψ―³–Α–≥–Β–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ω–Β―Ä–Β―Ö–Ψ–¥–Α [Lerut T. et al., 1997; Siewert J.R. et al., 1998; Feith M., 2006], ―Ä–Α–Ζ–Μ–Η―΅–Η―è –Φ–Β–Ε–¥―É I –Η III ―²–Η–Ω–Α–Φ–Η, –Κ–Α–Κ –≤ –Ψ―²–Ϋ–Ψ―à–Β–Ϋ–Η–Η –Κ–Μ–Η–Ϋ–Η–Κ–Ψ––Φ–Ψ―Ä―³–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Η―Ö ―¹–≤–Ψ–Ι―¹―²–≤, ―²–Α–Κ –Η –Ω–Ψ ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Ψ–Ι ―²–Α–Κ―²–Η–Κ–Β, ―è–≤–Μ―è―é―²―¹―è –Ω―Ä–Η–Ϋ―Ü–Η–Ω–Η–Α–Μ―¨–Ϋ―΄–Φ–Η, ―²–Ψ–≥–¥–Α –Κ–Α–Κ II ―²–Η–Ω –Η–Φ–Β–Β―² –±–Ψ–Μ–Β–Β ―¹―Ö–Ψ–¥–Ϋ―΄–Β ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Η―¹―²–Η–Κ–Η ―¹ ―²–Η–Ω–Ψ–Φ III, –Ϋ–Β–Ε–Β–Μ–Η ―¹ ―²–Η–Ω–Ψ–Φ I.
–û―¹–Ψ–±–Β–Ϋ–Ϋ–Ψ―¹―²–Η –Μ–Η–Φ―³–Ψ–≥–Β–Ϋ–Ϋ–Ψ–≥–Ψ –Φ–Β―²–Α―¹―²–Α–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Η―è –Α–¥–Β–Ϋ–Ψ–Κ–Α―Ä―Ü–Η–Ϋ–Ψ–Φ―΄ –Ζ–Ψ–Ϋ―΄
–Ω–Η―â–Β–≤–Ψ–¥–Ϋ–Ψ––Ε–Β–Μ―É–¥–Ψ―΅–Ϋ–Ψ–≥–Ψ –Ω–Β―Ä–Β―Ö–Ψ–¥–Α
–Ω–Ψ –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η Siewert J.R.
–‰–Φ–Β―é―²―¹―è –≤―΄―Ä–Α–Ε–Β–Ϋ–Ϋ―΄–Β ―Ä–Α–Ζ–Μ–Η―΅–Η―è –≤ –Μ–Η–Φ―³–Ψ–Ψ―²―²–Ψ–Κ–Β –≤ –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²–Η –Ψ―² –Μ–Ψ–Κ–Α–Μ–Η–Ζ–Α―Ü–Η–Η –Ψ–Ω―É―Ö–Ψ–Μ–Η –Ψ―²–Ϋ–Ψ―¹–Η―²–Β–Μ―¨–Ϋ–Ψ –Ω–Η―â–Β–≤–Ψ–¥–Ϋ–Ψ––Ε–Β–Μ―É–¥–Ψ―΅–Ϋ–Ψ–≥–Ψ –Ω–Β―Ä–Β―Ö–Ψ–¥–Α, ―΅―²–Ψ ―è–≤–Μ―è–Β―²―¹―è –Κ–Μ―é―΅–Β–≤―΄–Φ ―³–Α–Κ―²–Ψ―Ä–Ψ–Φ, –Ψ–Ω―Ä–Β–¥–Β–Μ―è―é―â–Η–Φ –≤ –¥–Α–Ϋ–Ϋ–Ψ–Ι –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η –Α–Μ–≥–Ψ―Ä–Η―²–Φ ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Μ–Β―΅–Β–Ϋ–Η―è [Siewert J.R. et al., 1998; Holscher A.H., 2002] [14]. –Δ–Α–Κ, –Ω―Ä–Η ―Ä–Α–Κ–Β –Ϋ–Η–Ε–Ϋ–Β–≥―Ä―É–¥–Ϋ–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ–Α –Ω–Η―â–Β–≤–Ψ–¥–Α –Μ–Η–Φ―³–Ψ–Ψ―²―²–Ψ–Κ –Ϋ–Α–Ω―Ä–Α–≤–Μ–Β–Ϋ –≤ –Ψ–±–Β ―¹―²–Ψ―Ä–Ψ–Ϋ―΄: –Κ–Α–Κ –≤ –Ψ―Ä–Α–Μ―¨–Ϋ–Ψ–Φ –Ϋ–Α–Ω―Ä–Α–≤–Μ–Β–Ϋ–Η–Η, –≤ ―¹―²–Ψ―Ä–Ψ–Ϋ―É –Μ–Η–Φ―³–Ψ–Κ–Ψ–Μ–Μ–Β–Κ―²–Ψ―Ä–Ψ–≤ ―¹―Ä–Β–¥–Ψ―¹―²–Β–Ϋ–Η―è, ―²–Α–Κ –Η –≤ –Κ–Α―É–¥–Α–Μ―¨–Ϋ–Ψ–Φ –Ϋ–Α–Ω―Ä–Α–≤–Μ–Β–Ϋ–Η–Η, –≤ ―¹―²–Ψ―Ä–Ψ–Ϋ―É –Μ–Η–Φ―³–Ψ–Κ–Ψ–Μ–Μ–Β–Κ―²–Ψ―Ä–Ψ–≤ –±―Ä―é―à–Ϋ–Ψ–Ι –Ω–Ψ–Μ–Ψ―¹―²–Η –Η –Ζ–Α–±―Ä―é―à–Η–Ϋ–Ϋ–Ψ–≥–Ψ –Ω―Ä–Ψ―¹―²―Ä–Α–Ϋ―¹―²–≤–Α. –£ ―²–Ψ –Ε–Β –≤―Ä–Β–Φ―è –Ω―Ä–Η ―Ä–Α–Κ–Β –Κ–Α―Ä–¥–Η–Η –Η ―¹―É–±–Κ–Α―Ä–¥–Η–Η –Ψ―¹–Ϋ–Ψ–≤–Ϋ–Ψ–Ι –≤–Β–Κ―²–Ψ―Ä –Μ–Η–Φ―³–Ψ–Ψ―²―²–Ψ–Κ–Α –Ϋ–Α–Ω―Ä–Α–≤–Μ–Β–Ϋ –≤ ―¹―²–Ψ―Ä–Ψ–Ϋ―É ―É–Ζ–Μ–Ψ–≤ –Ζ–Α–±―Ä―é―à–Η–Ϋ–Ϋ–Ψ–≥–Ψ –Ω―Ä–Ψ―¹―²―Ä–Α–Ϋ―¹―²–≤–Α –Η –≤–Β―Ä―Ö–Ϋ–Β–Ι –Ω–Α―Ä–Α–Α–Ψ―Ä―²–Α–Μ―¨–Ϋ–Ψ–Ι –Ψ–±–Μ–Α―¹―²–Η. –≠―²–Η –Ω―Ä–Η–Ϋ―Ü–Η–Ω–Η–Α–Μ―¨–Ϋ―΄–Β ―Ä–Α–Ζ–Μ–Η―΅–Η―è –≤ ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Β –Μ–Η–Φ―³–Ψ–Ψ―²―²–Ψ–Κ–Α –Η ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤–Β–Ϋ–Ϋ–Ψ –Ψ―¹–Ϋ–Ψ–≤–Ϋ―΄―Ö –Ϋ–Α–Ω―Ä–Α–≤–Μ–Β–Ϋ–Η―è―Ö –Μ–Η–Φ―³–Ψ–≥–Β–Ϋ–Ϋ–Ψ–≥–Ψ –Φ–Β―²–Α―¹―²–Α–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Η―è ―Ä–Α–Κ–Α –¥–Η―¹―²–Α–Μ―¨–Ϋ–Ψ–Ι ―²―Ä–Β―²–Η –Ω–Η―â–Β–≤–Ψ–¥–Α –Η ―Ä–Α–Κ–Α –Κ–Α―Ä–¥–Η–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ–Α –Ε–Β–Μ―É–¥–Κ–Α –Ω–Ψ–Ζ–≤–Ψ–Μ–Η–Μ–Η Korst R.J. –Η ―¹–Ψ–Α–≤―². (1998) [15] –Ω–Β―Ä–Β―¹–Φ–Ψ―²―Ä–Β―²―¨ –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η―é ―¹–Η–Φ–≤–Ψ–Μ–Α “N” –Α–¥–Β–Ϋ–Ψ–Κ–Α―Ä―Ü–Η–Ϋ–Ψ–Φ –¥–Α–Ϋ–Ϋ―΄―Ö –Μ–Ψ–Κ–Α–Μ–Η–Ζ–Α―Ü–Η–Ι. –ü–Ψ –Φ–Ϋ–Β–Ϋ–Η―é –Α–≤―²–Ψ―Ä–Ψ–≤, –Ω―Ä–Η –Α–¥–Β–Ϋ–Ψ–Κ–Α―Ä―Ü–Η–Ϋ–Ψ–Φ–Β –¥–Η―¹―²–Α–Μ―¨–Ϋ–Ψ–Ι ―²―Ä–Β―²–Η –Ω–Η―â–Β–≤–Ψ–¥–Α ―Ä–Β–≥–Η–Ψ–Ϋ–Α―Ä–Ϋ―΄–Φ–Η ―è–≤–Μ―è―é―²―¹―è: –±–Η―³―É―Ä–Κ–Α―Ü–Η–Ψ–Ϋ–Ϋ―΄–Β, –Ζ–Α–¥–Ϋ–Β–Φ–Β–¥–Η–Α―¹―²–Η–Ϋ–Α–Μ―¨–Ϋ―΄–Β, –Ω–Α―Ä–Α–Κ–Α―Ä–¥–Η–Α–Μ―¨–Ϋ―΄–Β –Η –Μ–Η–Φ―³–Α―²–Η―΅–Β―¹–Κ–Η–Β ―É–Ζ–Μ―΄ –Ω–Ψ ―Ö–Ψ–¥―É –Μ–Β–≤–Ψ–Ι –Ε–Β–Μ―É–¥–Ψ―΅–Ϋ–Ψ–Ι –Α―Ä―²–Β―Ä–Η–Η. –ü―Ä–Η –Α–¥–Β–Ϋ–Ψ–Κ–Α―Ä―Ü–Η–Ϋ–Ψ–Φ–Β –Κ–Α―Ä–¥–Η–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ–Α –Ε–Β–Μ―É–¥–Κ–Α ―Ä–Β–≥–Η–Ψ–Ϋ–Α―Ä–Ϋ―΄–Φ–Η ―è–≤–Μ―è―é―²―¹―è –Ω–Β―Ä–Η–≥–Α―¹―²―Ä–Α–Μ―¨–Ϋ―΄–Β –Η –Ζ–Α–±―Ä―é―à–Η–Ϋ–Ϋ―΄–Β –Μ–Η–Φ―³–Α―²–Η―΅–Β―¹–Κ–Η–Β ―É–Ζ–Μ―΄ ―΅―Ä–Β–≤–Ϋ–Ψ–≥–Ψ ―¹―²–≤–Ψ–Μ–Α –Η –Β–≥–Ψ –≤–Β―²–≤–Β–Ι, –Α ―²–Α–Κ–Ε–Β –Ϋ–Η–Ε–Ϋ–Η–Β –Ω–Α―Ä–Α―ç–Ζ–Ψ―³–Α–≥–Β–Α–Μ―¨–Ϋ―΄–Β –Μ–Η–Φ―³–Α―²–Η―΅–Β―¹–Κ–Η–Β ―É–Ζ–Μ―΄.
–Δ–Α–Κ–Ε–Β –Ψ―²–Φ–Β―΅–Α―é―²―¹―è ―¹―É―â–Β―¹―²–≤–Β–Ϋ–Ϋ―΄–Β ―Ä–Α–Ζ–Μ–Η―΅–Η―è –≤ ―΅–Α―¹―²–Ψ―²–Β –≤―΄―è–≤–Μ–Β–Ϋ–Η―è –Φ–Η–Κ―Ä–Ψ–Φ–Β―²–Α―¹―²–Α–Ζ–Ψ–≤ –≤ –Μ–Η–Φ―³–Α―²–Η―΅–Β―¹–Κ–Η―Ö ―É–Ζ–Μ–Α―Ö –Ω―Ä–Η ―Ä–Α–Ϋ–Ϋ–Η―Ö ―³–Ψ―Ä–Φ–Α―Ö –Ψ–Ω―É―Ö–Ψ–Μ–Η [16–19]. –ü―Ä–Η I ―²–Η–Ω–Β –Α–¥–Β–Ϋ–Ψ–Κ–Α―Ä―Ü–Η–Ϋ–Ψ–Φ―΄ ―΅–Α―¹―²–Ψ―²–Α –≤―΄―è–≤–Μ–Β–Ϋ–Η―è –Φ–Η–Κ―Ä–Ψ–Φ–Β―²–Α―¹―²–Α–Ζ–Ψ–≤ (–¥–Α–Ε–Β –Ω―Ä–Η –Ω―Ä–Η–Φ–Β–Ϋ–Β–Ϋ–Η–Η –Η–Φ–Φ―É–Ϋ–Ψ–≥–Η―¹―²–Ψ―Ö–Η–Φ–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è) –Ϋ–Β –Ω―Ä–Β–≤―΄―à–Α–Β―² 7%, ―²–Ψ–≥–¥–Α –Κ–Α–Κ –Ω―Ä–Η II –Η III ―²–Η–Ω–Α―Ö –≤–Ψ–Ζ―Ä–Α―¹―²–Α–Β―² –¥–Ψ 24%. –ü―Ä–Η―΅–Β–Φ –Φ–Η–Κ―Ä–Ψ–Φ–Β―²–Α―¹―²–Α–Ζ―΄ ―¹–Μ–Β–¥―É–Β―² ―Ä–Α―¹―¹–Φ–Α―²―Ä–Η–≤–Α―²―¨, –Κ–Α–Κ –Η―¹―²–Η–Ϋ–Ϋ―΄–Β –Φ–Β―²–Α―¹―²–Α–Ζ―΄ ―Ä–Α–Κ–Α –Ε–Β–Μ―É–¥–Κ–Α, ―΅―²–Ψ –Ψ–Ω―Ä–Β–¥–Β–Μ―è–Β―² –Ω―Ä–Ψ–≥–Ϋ–Ψ–Ζ –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è [20]. –ü–Ψ –¥–Α–Ϋ–Ϋ―΄–Φ Peracchia A. –Η ―¹–Ψ–Α–≤―². (1999), –Φ–Η–Κ―Ä–Ψ–Φ–Β―²–Α―¹―²–Α–Ζ―΄ –≤ ―É–¥–Α–Μ–Β–Ϋ–Ϋ―΄―Ö –Μ–Η–Φ―³–Α―²–Η―΅–Β―¹–Κ–Η―Ö ―É–Ζ–Μ–Α―Ö –≤―΄―è–≤–Μ―è―é―²―¹―è ―É 33% –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤, ―É –Κ–Ψ―²–Ψ―Ä―΄―Ö –Ω―Ä–Η ―¹―²–Α–Ϋ–¥–Α―Ä―²–Ϋ–Ψ–Φ –Φ–Η–Κ―Ä–Ψ―¹–Κ–Ψ–Ω–Η―΅–Β―¹–Κ–Ψ–Φ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Η –Φ–Β―²–Α―¹―²–Α–Ζ―΄ –Ϋ–Β –Ψ–Ω―Ä–Β–¥–Β–Μ―è–Μ–Η―¹―¨. –ü―Ä–Ψ–≥–Ϋ–Ψ–Ζ –Ω―Ä–Η –Ϋ–Α–Μ–Η―΅–Η–Η –Φ–Η–Κ―Ä–Ψ–Φ–Β―²–Α―¹―²–Α–Ζ–Ψ–≤ –±―΄–Μ –Α–Ϋ–Α–Μ–Ψ–≥–Η―΅–Β–Ϋ –Ϋ–Α–Μ–Η―΅–Η―é –Μ–Η–Φ―³–Ψ–≥–Β–Ϋ–Ϋ―΄―Ö –Φ–Β―²–Α―¹―²–Α–Ζ–Ψ–≤ – ―É –Ω–Ψ–Μ–Ψ–≤–Η–Ϋ―΄ –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –≤ ―ç―²–Ψ–Ι –≥―Ä―É–Ω–Ω–Β –≤ ―²–Β―΅–Β–Ϋ–Η–Β –Ω–Β―Ä–≤–Ψ–≥–Ψ –≥–Ψ–¥–Α –Ϋ–Α–±–Μ―é–¥–Β–Ϋ–Η―è –≤―΄―è–≤–Μ–Β–Ϋ–Ψ –Ω―Ä–Ψ–≥―Ä–Β―¹―¹–Η―Ä–Ψ–≤–Α–Ϋ–Η–Β –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è.
–£―¹–Β –≤―΄―à–Β–Ω―Ä–Η–≤–Β–¥–Β–Ϋ–Ϋ―΄–Β –Ψ―²–Μ–Η―΅–Η―è –Ω–Ψ–Ζ–≤–Ψ–Μ―è―é―² –Ω–Ψ–Ϋ―è―²―¨ –¥–Ψ―¹―²–Α―²–Ψ―΅–Ϋ―É―é –≥–Β―²–Β―Ä–Ψ–≥–Β–Ϋ–Ϋ–Ψ―¹―²―¨ –Ψ–Ω–Η―¹―΄–≤–Α–Β–Φ―΄―Ö –Ψ–Ω―É―Ö–Ψ–Μ–Β–Ι, –Κ–Α–Κ ―¹ ―²–Ψ―΅–Κ–Η –Ζ―Ä–Β–Ϋ–Η―è ―²–Α–Κ―²–Η–Κ–Η –Μ–Β―΅–Β–Ϋ–Η―è, ―²–Α–Κ –Η ―¹ –Ω―Ä–Ψ–≥–Ϋ–Ψ―¹―²–Η―΅–Β―¹–Κ–Η―Ö –Ω–Ψ–Ζ–Η―Ü–Η–Ι.
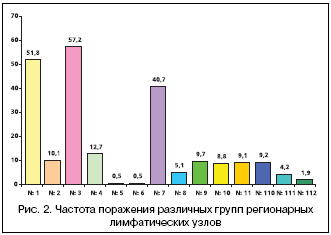
–ù–Α–Φ–Η –±―΄–Μ–Α –Η–Ζ―É―΅–Β–Ϋ–Α ―΅–Α―¹―²–Ψ―²–Α –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η―è ―Ä–Α–Ζ–Μ–Η―΅–Ϋ―΄―Ö –≥―Ä―É–Ω–Ω ―Ä–Β–≥–Η–Ψ–Ϋ–Α―Ä–Ϋ―΄―Ö –Μ–Η–Φ―³–Α―²–Η―΅–Β―¹–Κ–Η―Ö ―É–Ζ–Μ–Ψ–≤ (―Ä–Η―¹. 2) [–Δ–Β―Ä– –û–≤–Α–Ϋ–Β―¹–Ψ–≤ –€.–î., 2007]. –ù–Α –Ψ―¹–Ϋ–Ψ–≤–Α–Ϋ–Η–Η –Α–Ϋ–Α–Μ–Η–Ζ–Α ―Ä–Β–Ω―Ä–Β–Ζ–Β–Ϋ―²–Α―²–Η–≤–Ϋ–Ψ–≥–Ψ –Φ–Α―²–Β―Ä–Η–Α–Μ–Α –±–Ψ–Μ–Β–Β ―΅–Β–Φ 400 –≤–Φ–Β―à–Α―²–Β–Μ―¨―¹―²–≤ –Φ―΄ –Ω–Ψ–Κ–Α–Ζ–Α–Μ–Η, ―΅―²–Ψ –Ω―Ä–Η ―Ä–Α–Κ–Β –Ω―Ä–Ψ–Κ―¹–Η–Φ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ–Α –Ε–Β–Μ―É–¥–Κ–Α –Ϋ–Α–Η–±–Ψ–Μ–Β–Β ―΅–Α―¹―²–Ψ –Ω–Ψ―Ä–Α–Ε–Α―é―²―¹―è ―É–Ζ–Μ―΄ –Φ–Α–Μ–Ψ–Ι –Κ―Ä–Η–≤–Η–Ζ–Ϋ―΄ (ⳕ 3 – 57,2%), –Ω―Ä–Α–≤–Ψ–Ι –Ω–Α―Ä–Α–Κ–Α―Ä–¥–Η–Α–Μ―¨–Ϋ–Ψ–Ι –Ψ–±–Μ–Α―¹―²–Η (ⳕ 1 – 51,8%), –Α ―²–Α–Κ–Ε–Β –Ω–Ψ ―Ö–Ψ–¥―É –Μ–Β–≤–Ψ–Ι –Ε–Β–Μ―É–¥–Ψ―΅–Ϋ–Ψ–Ι –Α―Ä―²–Β―Ä–Η–Η (ⳕ 7 – 40,7%). –‰–Ζ –Φ–Β–¥–Η–Α―¹―²–Η–Ϋ–Α–Μ―¨–Ϋ―΄―Ö –Μ–Η–Φ―³–Α―²–Η―΅–Β―¹–Κ–Η―Ö –Κ–Ψ–Μ–Μ–Β–Κ―²–Ψ―Ä–Ψ–≤ –Ϋ–Α–Η–±–Ψ–Μ–Β–Β ―΅–Α―¹―²–Ψ –Ψ―²–Φ–Β―΅–Α–Β―²―¹―è –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η–Β –Ϋ–Η–Ε–Ϋ–Η―Ö –Ω–Α―Ä–Α―ç–Ζ–Ψ―³–Α–≥–Β–Α–Μ―¨–Ϋ―΄―Ö –Μ–Η–Φ―³–Α―²–Η―΅–Β―¹–Κ–Η―Ö ―É–Ζ–Μ–Ψ–≤ (ⳕ 110 – 9,2%).
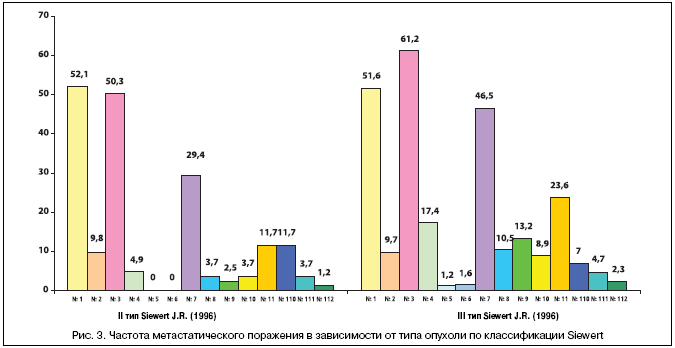
–Δ–Α–Κ–Ε–Β –±―΄–Μ–Α –Η–Ζ―É―΅–Β–Ϋ–Α ―΅–Α―¹―²–Ψ―²–Α –Φ–Β―²–Α―¹―²–Α―²–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η―è –≤ –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²–Η –Ψ―² ―²–Η–Ω–Α –Ψ–Ω―É―Ö–Ψ–Μ–Η –Ω–Ψ –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η Siewert (―Ä–Η―¹. 3) [21]. –ü―Ä–Η ―¹―Ä–Α–≤–Ϋ–Η―²–Β–Μ―¨–Ϋ–Ψ–Φ –Α–Ϋ–Α–Μ–Η–Ζ–Β –Ψ―²–Φ–Β―΅–Α–Β―²―¹―è ―¹―²–Α―²–Η―¹―²–Η―΅–Β―¹–Κ–Η –Ζ–Ϋ–Α―΅–Η–Φ–Ψ–Β ―É–≤–Β–Μ–Η―΅–Β–Ϋ–Η–Β ―΅–Α―¹―²–Ψ―²―΄ –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η―è –Μ–Η–Φ―³–Α―²–Η―΅–Β―¹–Κ–Η―Ö ―É–Ζ–Μ–Ψ–≤ –≤―²–Ψ―Ä–Ψ–≥–Ψ ―ç―²–Α–Ω–Α –Φ–Β―²–Α―¹―²–Α–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Η―è, –Ψ―¹–Ψ–±–Β–Ϋ–Ϋ–Ψ –≤ –Ψ–±–Μ–Α―¹―²–Η ―΅―Ä–Β–≤–Ϋ–Ψ–≥–Ψ ―¹―²–≤–Ψ–Μ–Α (ⳕ 9) – 2,5% –Ω―Ä–Ψ―²–Η–≤ 13,2%, –Α ―²–Α–Κ–Ε–Β –Ω–Ψ ―Ö–Ψ–¥―É ―¹–Β–Μ–Β–Ζ–Β–Ϋ–Ψ―΅–Ϋ–Ψ–Ι –Α―Ä―²–Β―Ä–Η–Η (ⳕ 11) – 11,7% –Ω―Ä–Ψ―²–Η–≤ 23,6% –≤ –≥―Ä―É–Ω–Ω–Β III ―²–Η–Ω–Α –Ω–Ψ –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η Siewert J.R., ―΅―²–Ψ –Ψ–Ω―Ä–Β–¥–Β–Μ―è–Β―² –Ϋ–Β–±–Μ–Α–≥–Ψ–Ω―Ä–Η―è―²–Ϋ―΄–Ι –Ω―Ä–Ψ–≥–Ϋ–Ψ–Ζ (―Ä–Α–Ζ–Ϋ–Η―Ü–Α –Φ–Β–Ε–¥―É –≥―Ä―É–Ω–Ω–Α–Φ–Η ―¹―²–Α―²–Η―¹―²–Η―΅–Β―¹–Κ–Η –¥–Ψ―¹―²–Ψ–≤–Β―Ä–Ϋ–Α, p<0,001).
–û–±―â–Η–Ι –Ω–Ψ–Κ–Α–Ζ–Α―²–Β–Μ―¨ ―΅–Α―¹―²–Ψ―²―΄ –Μ–Η–Φ―³–Ψ–≥–Β–Ϋ–Ϋ–Ψ–≥–Ψ –Φ–Β―²–Α―¹―²–Α–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Η―è ―¹–Ψ―¹―²–Α–≤–Η–Μ 65,5%, ―΅―²–Ψ ―¹–≤–Η–¥–Β―²–Β–Μ―¨―¹―²–≤―É–Β―² –Ψ –Ζ–Μ–Ψ–Κ–Α―΅–Β―¹―²–≤–Β–Ϋ–Ϋ–Ψ–Φ –Ω–Ψ―²–Β–Ϋ―Ü–Η–Α–Μ–Β ―Ä–Α–Κ–Α –Ω―Ä–Ψ–Κ―¹–Η–Φ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ–Α –Ε–Β–Μ―É–¥–Κ–Α. –ü―Ä–Ψ―¹–Μ–Β–Ε–Η–≤–Α–Β―²―¹―è ―²–Β–Ϋ–¥–Β–Ϋ―Ü–Η―è ―É–≤–Β–Μ–Η―΅–Β–Ϋ–Η―è ―΅–Α―¹―²–Ψ―²―΄ –Μ–Η–Φ―³–Ψ–≥–Β–Ϋ–Ϋ–Ψ–≥–Ψ –Φ–Β―²–Α―¹―²–Α–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Η―è –≤ –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²–Η –Ψ―² –≤–Ψ–≤–Μ–Β―΅–Β–Ϋ–Η―è –≤ –Ω―Ä–Ψ―Ü–Β―¹―¹ –Ω–Η―â–Β–≤–Ψ–¥–Α. –ü―Ä–Η –Μ–Ψ–Κ–Α–Μ–Η–Ζ–Α―Ü–Η–Η –Ψ–Ω―É―Ö–Ψ–Μ–Η –Μ–Η―à―¨ –≤ –Ω―Ä–Ψ–Κ―¹–Η–Φ–Α–Μ―¨–Ϋ–Ψ–Φ –Ψ―²–¥–Β–Μ–Β –±–Β–Ζ –Ω–Β―Ä–Β―Ö–Ψ–¥–Α –Ϋ–Α –Ω–Η―â–Β–≤–Ψ–¥ ―΅–Α―¹―²–Ψ―²–Α –Μ–Η–Φ―³–Ψ–≥–Β–Ϋ–Ϋ–Ψ–≥–Ψ –Φ–Β―²–Α―¹―²–Α–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Η―è ―¹–Ψ―¹―²–Α–≤–Μ―è–Β―² 41,4%, ―²–Ψ–≥–¥–Α –Κ–Α–Κ –Ω―Ä–Η –Η–Ϋ―³–Η–Μ―¨―²―Ä–Α―Ü–Η–Η ―Ä–Ψ–Ζ–Β―²–Κ–Η –Κ–Α―Ä–¥–Η–Η ―΅–Α―¹―²–Ψ―²–Α –≤–Ψ–Ζ―Ä–Α―¹―²–Α–Β―² –¥–Ψ 56,7%, –Α –Ω―Ä–Η –Ω–Β―Ä–Β―Ö–Ψ–¥–Β –Ϋ–Α –Ω–Η―â–Β–≤–Ψ–¥ ―¹–Ψ―¹―²–Α–≤–Μ―è–Β―² 68,0% (―Ä–Α–Ζ–Ϋ–Η―Ü–Α ―¹ –Ω–Β―Ä–≤–Ψ–Ι –≥―Ä―É–Ω–Ω–Ψ–Ι ―¹―²–Α―²–Η―¹―²–Η―΅–Β―¹–Κ–Η –¥–Ψ―¹―²–Ψ–≤–Β―Ä–Ϋ–Α –≤ –Ψ–±–Β–Η―Ö –≥―Ä―É–Ω–Ω–Α―Ö).
–†–Α―¹―¹–Φ–Ψ―²―Ä–Β–Ϋ–Ϋ―΄–Β –≤―΄―à–Β –Ψ―¹–Ψ–±–Β–Ϋ–Ϋ–Ψ―¹―²–Η –Μ–Η–Φ―³–Ψ–≥–Β–Ϋ–Ϋ–Ψ–≥–Ψ –Φ–Β―²–Α―¹―²–Α–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Η―è –Κ–Α―Ä–¥–Η–Ψ―ç–Ζ–Ψ―³–Α–≥–Β–Α–Μ―¨–Ϋ–Ψ–≥–Ψ ―Ä–Α–Κ–Α –≤ –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ–Ι ―¹―²–Β–Ω–Β–Ϋ–Η –Ψ–Ω―Ä–Β–¥–Β–Μ―è―é―² ―¹–Ω–Β―Ü–Η―³–Η–Κ―É ―ç―²–Ψ–≥–Ψ –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è –Η –Ω–Ψ–¥―Ö–Ψ–¥―΄ –Κ ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Ψ–Φ―É –Μ–Β―΅–Β–Ϋ–Η―é.
–Ξ–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Α―è ―²–Α–Κ―²–Η–Κ–Α
–Ω―Ä–Η –Α–¥–Β–Ϋ–Ψ–Κ–Α―Ä―Ü–Η–Ϋ–Ψ–Φ–Β –Ζ–Ψ–Ϋ―΄
–Ω–Η―â–Β–≤–Ψ–¥–Ϋ–Ψ––Ε–Β–Μ―É–¥–Ψ―΅–Ϋ–Ψ–≥–Ψ –Ω–Β―Ä–Β―Ö–Ψ–¥–Α
–Ω–Ψ –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η J.R. Siewert
–ü―Ä–Η–≤–Β–¥–Β–Ϋ–Ϋ―΄–Ι –≤―΄―à–Β –Α–Ϋ–Α–Μ–Η–Ζ –¥–Α–Ϋ–Ϋ―΄―Ö –Ω–Ψ–Ζ–≤–Ψ–Μ―è–Β―² –Ω–Ψ–Ϋ―è―²―¨, ―΅―²–Ψ –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η―è Siewert J.R. –Ψ–±―ä–Β–¥–Η–Ϋ―è–Β―² –≥–Β―²–Β―Ä–Ψ–≥–Β–Ϋ–Ϋ―΄–Β –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è – ―Ä–Α–Κ –¥–Η―¹―²–Α–Μ―¨–Ϋ–Ψ–Ι ―²―Ä–Β―²–Η –Ω–Η―â–Β–≤–Ψ–¥–Α, ―Ä–Α–Κ –Ω―Ä–Ψ–Κ―¹–Η–Φ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ–Α –Ε–Β–Μ―É–¥–Κ–Α ―¹ –Ω–Β―Ä–Β―Ö–Ψ–¥–Ψ–Φ –Ϋ–Α –Ω–Η―â–Β–≤–Ψ–¥ (–Η―¹―²–Η–Ϋ–Ϋ―΄–Ι –Κ–Α―Ä–¥–Η–Ψ―ç–Ζ–Ψ―³–Α–≥–Β–Α–Μ―¨–Ϋ―΄–Ι ―Ä–Α–Κ) –Η ―Ä–Α–Κ ―¹―É–±–Κ–Α―Ä–¥–Η–Η, –Κ–Ψ―²–Ψ―Ä―΄–Ι –Ω–Ψ –±–Η–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Η–Φ ―¹–≤–Ψ–Ι―¹―²–≤–Α–Φ ―¹–Ψ–Ψ―²–≤–Β―²―¹―²―É–Β―² ―Ä–Α–Κ―É –Ε–Β–Μ―É–¥–Κ–Α, ―¹ –Μ–Ψ–Κ–Α–Μ–Η–Ζ–Α―Ü–Η–Β–Ι –≤ –Ζ–Ψ–Ϋ–Β –Ω―Ä–Ψ–Κ―¹–Η–Φ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ–Α.
–£ –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²–Η –Ψ―² ―²–Η–Ω–Α –Ψ–Ω―É―Ö–Ψ–Μ–Η Siewert J.R. –Η ―¹–Ψ–Α–≤―². (2007) –Ω―Ä–Β–¥–Μ–Α–≥–Α―é―² –¥–Η―³―³–Β―Ä–Β–Ϋ―Ü–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ―É―é ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ―É―é ―²–Α–Κ―²–Η–Κ―É. –£ ―¹–Μ―É―΅–Α–Β –Α–¥–Β–Ϋ–Ψ–Κ–Α―Ä―Ü–Η–Ϋ–Ψ–Φ―΄ –¥–Η―¹―²–Α–Μ―¨–Ϋ–Ψ–Ι ―²―Ä–Β―²–Η –Ω–Η―â–Β–≤–Ψ–¥–Α –Ω―Ä–Β–¥–Μ–Α–≥–Α–Β―²―¹―è –≤―΄–Ω–Ψ–Μ–Ϋ―è―²―¨ ―¹―É–±―²–Ψ―²–Α–Μ―¨–Ϋ―É―é ―Ä–Β–Ζ–Β–Κ―Ü–Η―é –Ω–Η―â–Β–≤–Ψ–¥–Α ―¹ –Ω―Ä–Ψ–Κ―¹–Η–Φ–Α–Μ―¨–Ϋ–Ψ–Ι ―Ä–Β–Ζ–Β–Κ―Ü–Η–Β–Ι –Ε–Β–Μ―É–¥–Κ–Α –Η ―³–Ψ―Ä–Φ–Η―Ä–Ψ–≤–Α–Ϋ–Η–Β–Φ –Ω–Η―â–Β–≤–Ψ–¥–Ϋ–Ψ––Ε–Β–Μ―É–¥–Ψ―΅–Ϋ–Ψ–≥–Ψ ―¹–Ψ―É―¹―²―¨―è –≤ –Κ―É–Ω–Ψ–Μ–Β –Ω―Ä–Α–≤–Ψ–Ι –Ω–Μ–Β–≤―Ä–Α–Μ―¨–Ϋ–Ψ–Ι –Ω–Ψ–Μ–Ψ―¹―²–Η –Η–Ζ –Ω―Ä–Α–≤–Ψ―¹―²–Ψ―Ä–Ψ–Ϋ–Ϋ–Β–≥–Ψ ―²―Ä–Α–Ϋ―¹―²–Ψ―Ä–Α–Κ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –¥–Ψ―¹―²―É–Ω–Α. –Γ–Μ–Β–¥―É–Β―² –Ψ―¹–Ψ–±–Ψ –Ψ―²–Φ–Β―²–Η―²―¨, ―΅―²–Ψ –Ϋ–Α –Ψ―¹–Ϋ–Ψ–≤–Α–Ϋ–Η–Η –±–Ψ–Μ–Β–Β ―΅–Β–Φ 20––Μ–Β―²–Ϋ–Β–≥–Ψ –Ψ–Ω―΄―²–Α ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Μ–Β―΅–Β–Ϋ–Η―è ―Ä–Α–Κ–Α –Ω–Η―â–Β–≤–Ψ–¥–Α, –Κ–Α–Κ –Ω–Μ–Ψ―¹–Κ–Ψ–Κ–Μ–Β―²–Ψ―΅–Ϋ–Ψ–≥–Ψ, ―²–Α–Κ –Η –Α–¥–Β–Ϋ–Ψ–Κ–Α―Ä―Ü–Η–Ϋ–Ψ–Φ―΄, Siewert J.R. –Ψ–±–Ψ―¹–Ϋ–Ψ–≤–Α–Μ –Η –¥–Ψ–Κ–Α–Ζ–Α–Μ –Ω―Ä–Β–Η–Φ―É―â–Β―¹―²–≤–Α ―²―Ä–Α–Ϋ―¹―²–Ψ―Ä–Α–Κ–Α–Μ―¨–Ϋ–Ψ–Ι ―Ä–Β–Ζ–Β–Κ―Ü–Η–Η –Ω–Η―â–Β–≤–Ψ–¥–Α ―¹ ―³–Ψ―Ä–Φ–Η―Ä–Ψ–≤–Α–Ϋ–Η–Β–Φ –≤–Ϋ―É―²―Ä–Η–≥―Ä―É–¥–Ϋ–Ψ–≥–Ψ ―¹–Ψ―É―¹―²―¨―è –Ϋ–Α–¥ ―²―Ä–Α–Ϋ―¹―Ö–Η–Α―²–Α–Μ―¨–Ϋ–Ψ–Ι ―²―Ä–Α–Ϋ―¹–Φ–Β–¥–Η–Α―¹―²–Η–Ϋ–Α–Μ―¨–Ϋ–Ψ–Ι ―¹―É–±―²–Ψ―²–Α–Μ―¨–Ϋ–Ψ–Ι ―Ä–Β–Ζ–Β–Κ―Ü–Η–Β–Ι ―¹ –Α–Ϋ–Α―¹―²–Ψ–Φ–Ψ–Ζ–Ψ–Φ –Ϋ–Α ―à–Β–Β. –Γ–Ψ–≥–Μ–Α―¹–Ϋ–Ψ –Β–≥–Ψ –¥–Α–Ϋ–Ϋ―΄–Φ, ―ç―²–Ψ –Ψ–Ω―Ä–Β–¥–Β–Μ―è–Β―²―¹―è ―¹–Ψ–≤–Ψ–Κ―É–Ω–Ϋ–Ψ―¹―²―¨―é ―³–Α–Κ―²–Ψ―Ä–Ψ–≤: ―¹―²–Α―²–Η―¹―²–Η―΅–Β―¹–Κ–Η –±–Ψ–Μ―¨―à–Β–Ι ―΅–Α―¹―²–Ψ―²–Ψ–Ι –Μ–Ψ–Κ–Ψ–―Ä–Β–≥–Η–Ψ–Ϋ–Α―Ä–Ϋ–Ψ–≥–Ψ ―Ä–Β―Ü–Η–¥–Η–≤–Α –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è –≤ ―¹―Ä–Β–¥–Ψ―¹―²–Β–Ϋ–Η–Η –≤ ―¹–Ψ―΅–Β―²–Α–Ϋ–Η–Η ―¹ –Ϋ–Η–Ζ–Κ–Η–Φ –Κ–Α―΅–Β―¹―²–≤–Ψ–Φ –Ε–Η–Ζ–Ϋ–Η –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –Ω―Ä–Η ―²―Ä–Α–Ϋ―¹―Ö–Η–Α―²–Α–Μ―¨–Ϋ―΄―Ö –≤–Φ–Β―à–Α―²–Β–Μ―¨―¹―²–≤–Α―Ö. –Γ–Μ–Β–¥―¹―²–≤–Η–Β–Φ ―ç―²–Ψ–≥–Ψ ―è–≤–Μ―è―é―²―¹―è –±–Ψ–Μ–Β–Β –Ϋ–Η–Ζ–Κ–Η–Β –Ω–Ψ–Κ–Α–Ζ–Α―²–Β–Μ–Η –≤―΄–Ε–Η–≤–Α–Β–Φ–Ψ―¹―²–Η.
–ü―Ä–Η II –Η III ―²–Η–Ω–Α―Ö –Ψ–Ω―É―Ö–Ψ–Μ–Η –Ϋ–Β–Ψ–±―Ö–Ψ–¥–Η–Φ―΄–Φ –Ψ–±―ä–Β–Φ–Ψ–Φ –≤–Φ–Β―à–Α―²–Β–Μ―¨―¹―²–≤–Α, –Ω–Ψ –¥–Α–Ϋ–Ϋ―΄–Φ –Α–≤―²–Ψ―Ä–Α, ―è–≤–Μ―è–Β―²―¹―è ―΅―Ä–Β–Ζ–±―Ä―é―à–Η–Ϋ–Ϋ–Α―è –≥–Α―¹―²―Ä–Ψ―ç–Κ―²–Ψ–Φ–Η―è ―¹ –Μ–Η–Φ―³–Ψ–¥–Η―¹―¹–Β–Κ―Ü–Η–Β–Ι (–¦–î) D2 –Η ―²―Ä–Α–Ϋ―¹―Ö–Η–Α―²–Α–Μ―¨–Ϋ–Ψ–Ι ―Ä–Β–Ζ–Β–Κ―Ü–Η–Β–Ι –≤–Ψ–≤–Μ–Β―΅–Β–Ϋ–Ϋ―΄―Ö –Ψ―²–¥–Β–Μ–Ψ–≤ –Ω–Η―â–Β–≤–Ψ–¥–Α ―¹ –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η–Β–Φ –Μ–Η–Φ―³–Ψ–¥–Η―¹―¹–Β–Κ―Ü–Η–Η –Ζ–Α–¥–Ϋ–Β–≥–Ψ ―¹―Ä–Β–¥–Ψ―¹―²–Β–Ϋ–Η―è. –Δ–Α–Κ–Ψ–Ι –Ω–Ψ–¥―Ö–Ψ–¥ –Κ ―²–Α–Κ―²–Η–Κ–Β ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Μ–Β―΅–Β–Ϋ–Η―è –Ω–Ψ–Ζ–≤–Ψ–Μ―è–Β―² –≤―΄–¥–Β–Μ–Η―²―¨ ―¹–Ω–Ψ―Ä–Ϋ―΄–Β, –Ω–Ψ –Ϋ–Α―à–Β–Φ―É –Φ–Ϋ–Β–Ϋ–Η―é, –Ω–Ψ–Μ–Ψ–Ε–Β–Ϋ–Η―è, –Κ–Ψ―²–Ψ―Ä―΄–Β –Ω–Ψ–¥–Μ–Β–Ε–Α―² –Ψ–±―¹―É–Ε–¥–Β–Ϋ–Η―é.
–Γ–Ω–Ψ―Ä–Ϋ―΄–Φ –Ω–Ψ–Μ–Ψ–Ε–Β–Ϋ–Η–Β–Φ, –Ω–Ψ –Ϋ–Α―à–Β–Φ―É –Φ–Ϋ–Β–Ϋ–Η―é, ―è–≤–Μ―è–Β―²―¹―è ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Η–Ι –¥–Ψ―¹―²―É–Ω –Η –Ψ–±―ä–Β–Φ –≤–Φ–Β―à–Α―²–Β–Μ―¨―¹―²–≤–Α –Ω―Ä–Η II ―²–Η–Ω–Β – –Η―¹―²–Η–Ϋ–Ϋ–Ψ–Φ ―Ä–Α–Κ–Β –Κ–Α―Ä–¥–Η–Η. –Δ–Α–Κ―²–Η–Κ–Α –Μ–Β―΅–Β–Ϋ–Η―è –Ω―Ä–Η ―ç―²–Ψ–Φ –¥–Ψ–Μ–Ε–Ϋ–Α –Ψ–Ω―Ä–Β–¥–Β–Μ―è―²―¨―¹―è, –Κ–Α–Κ –¥–Μ―è ―Ä–Α–Κ–Α –Ε–Β–Μ―É–¥–Κ–Α ―¹ –≤–Ψ–≤–Μ–Β―΅–Β–Ϋ–Η–Β–Φ –¥–Η―¹―²–Α–Μ―¨–Ϋ―΄―Ö –Ψ―²–¥–Β–Μ–Ψ–≤ –Ω–Η―â–Β–≤–Ψ–¥–Α. –≠―²–Ψ –Ω–Ψ–Μ–Ψ–Ε–Β–Ϋ–Η–Β ―²―Ä–Β–±―É–Β―² –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η―è ―¹–Η―¹―²–Β–Φ–Α―²–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Α–Ϋ–Α–Μ–Η–Ζ–Α ―¹ –¥–≤―É―Ö –Ω―Ä–Η–Ϋ―Ü–Η–Ω–Η–Α–Μ―¨–Ϋ―΄―Ö –Ω–Ψ–Ζ–Η―Ü–Η–Ι: –≤–Ψ––Ω–Β―Ä–≤―΄―Ö, ―¹ ―²–Ψ―΅–Κ–Η –Ζ―Ä–Β–Ϋ–Η―è –≤–Φ–Β―à–Α―²–Β–Μ―¨―¹―²–≤–Α –Ϋ–Α –Ω–Η―â–Β–≤–Ψ–¥–Β ―¹ ―É―΅–Β―²–Ψ–Φ –±–Β–Ζ–Ψ–Ω–Α―¹–Ϋ–Ψ–≥–Ψ ―É―Ä–Ψ–≤–Ϋ―è –Β–≥–Ψ ―Ä–Β–Ζ–Β–Κ―Ü–Η–Η –Η –Α–¥–Β–Κ–≤–Α―²–Ϋ–Ψ―¹―²–Η –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η―è –Φ–Β–¥–Η–Α―¹―²–Η–Ϋ–Α–Μ―¨–Ϋ–Ψ–Ι –Μ–Η–Φ―³–Ψ–¥–Η―¹―¹–Β–Κ―Ü–Η–Η, –Α –≤–Ψ––≤―²–Ψ―Ä―΄―Ö, ―¹ ―É―΅–Β―²–Ψ–Φ –Α–¥–Β–Κ–≤–Α―²–Ϋ–Ψ―¹―²–Η –Η ―³―É–Ϋ–Κ―Ü–Η–Ψ–Ϋ–Α–Μ―¨–Ϋ–Ψ―¹―²–Η –≤–Φ–Β―à–Α―²–Β–Μ―¨―¹―²–≤–Α –Ϋ–Α –Ε–Β–Μ―É–¥–Κ–Β ―¹ –≤–Ψ–Ζ–Φ–Ψ–Ε–Ϋ–Ψ―¹―²―¨―é –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η―è ―Ä–Α–¥–Η–Κ–Α–Μ―¨–Ϋ–Ψ–Ι –Ω―Ä–Ψ–Κ―¹–Η–Φ–Α–Μ―¨–Ϋ–Ψ–Ι ―¹―É–±―²–Ψ―²–Α–Μ―¨–Ϋ–Ψ–Ι –Β–≥–Ψ ―Ä–Β–Ζ–Β–Κ―Ü–Η–Η. –ü–Β―Ä–≤–Ψ–Β –Ω–Ψ–Μ–Ψ–Ε–Β–Ϋ–Η–Β –≤–Κ–Μ―é―΅–Α–Β―² –Ϋ–Α–Η–±–Ψ–Μ–Β–Β –Α–Κ―²―É–Α–Μ―¨–Ϋ―΄–Ι –≤–Ψ–Ω―Ä–Ψ―¹ – ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Η–Ι –¥–Ψ―¹―²―É–Ω –¥–Μ―è –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η―è –≤–Φ–Β―à–Α―²–Β–Μ―¨―¹―²–≤–Α –Κ–Α–Κ –≤ –±―Ä―é―à–Ϋ–Ψ–Ι, ―²–Α–Κ –Η –≤ –Ω–Μ–Β–≤―Ä–Α–Μ―¨–Ϋ–Ψ–Ι –Ω–Ψ–Μ–Ψ―¹―²―è―Ö. –£―²–Ψ―Ä–Ψ–Β –Ω–Ψ–Μ–Ψ–Ε–Β–Ϋ–Η–Β –Ψ–Ω―Ä–Β–¥–Β–Μ―è–Β―² –Ω―Ä–Η–Ϋ―Ü–Η–Ω–Η–Α–Μ―¨–Ϋ―É―é –≤–Ψ–Ζ–Φ–Ψ–Ε–Ϋ–Ψ―¹―²―¨ –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η―è –±–Ψ–Μ–Β–Β ―³―É–Ϋ–Κ―Ü–Η–Ψ–Ϋ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –≤–Φ–Β―à–Α―²–Β–Μ―¨―¹―²–≤–Α – –Ω―Ä–Ψ–Κ―¹–Η–Φ–Α–Μ―¨–Ϋ–Ψ–Ι ―¹―É–±―²–Ψ―²–Α–Μ―¨–Ϋ–Ψ–Ι ―Ä–Β–Ζ–Β–Κ―Ü–Η–Η –Ε–Β–Μ―É–¥–Κ–Α –±–Β–Ζ ―É―â–Β―Ä–±–Α –¥–Μ―è ―Ä–Α–¥–Η–Κ–Α–Μ―¨–Ϋ–Ψ―¹―²–Η.
–ü―Ä–Η ―¹―Ä–Α–≤–Ϋ–Η―²–Β–Μ―¨–Ϋ–Ψ–Φ –Α–Ϋ–Α–Μ–Η–Ζ–Β ―Ä–Β–Ζ―É–Μ―¨―²–Α―²–Ψ–≤ ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Μ–Β―΅–Β–Ϋ–Η―è II ―²–Η–Ω–Α –Ψ–Ω―É―Ö–Ψ–Μ–Η –Ω―Ä–Η –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η–Η –≥–Α―¹―²―Ä―ç–Κ―²–Ψ–Φ–Η–Η ―¹ –¦–î D2 –Η ―¹―É–±―²–Ψ―²–Α–Μ―¨–Ϋ–Ψ–Ι ―Ä–Β–Ζ–Β–Κ―Ü–Η–Β–Ι –Ω–Η―â–Β–≤–Ψ–¥–Α ―¹ –Ω―Ä–Ψ–Κ―¹–Η–Φ–Α–Μ―¨–Ϋ–Ψ–Ι ―Ä–Β–Ζ–Β–Κ―Ü–Η–Β–Ι –Ε–Β–Μ―É–¥–Κ–Α (–Ψ–Ω–Β―Ä–Α―Ü–Η―è ―²–Η–Ω–Α –¦―¨―é–Η―¹–Α) –Α–≤―²–Ψ―Ä―΄ –Ψ―²–Φ–Β―²–Η–Μ–Η ―É–Μ―É―΅―à–Β–Ϋ–Η–Β –≤―΄–Ε–Η–≤–Α–Β–Φ–Ψ―¹―²–Η –Ω–Ψ―¹–Μ–Β –Ω–Β―Ä–≤–Ψ–≥–Ψ ―²–Η–Ω–Α –≤–Φ–Β―à–Α―²–Β–Μ―¨―¹―²–≤–Α, ―΅―²–Ψ ―²–Α–Κ–Ε–Β –Ψ–Ω―Ä–Β–¥–Β–Μ―è–Β―²―¹―è –Ω―Ä–Η–Ϋ–Α–¥–Μ–Β–Ε–Ϋ–Ψ―¹―²―¨―é –¥–Α–Ϋ–Ϋ–Ψ–≥–Ψ ―²–Η–Ω–Α –Ψ–Ω―É―Ö–Ψ–Μ–Β–Ι –Κ ―Ä–Α–Κ―É –Ε–Β–Μ―É–¥–Κ–Α.
–û―²–Ϋ–Ψ―¹–Η―²–Β–Μ―¨–Ϋ–Ψ III ―²–Η–Ω–Α –Ψ–Ω―É―Ö–Ψ–Μ–Β–Ι –Ϋ–Β–Ψ–±―Ö–Ψ–¥–Η–Φ–Ψ –Ψ―²–Φ–Β―²–Η―²―¨, ―΅―²–Ψ ―¹ ―É―΅–Β―²–Ψ–Φ –Η–Ϋ―²―Ä–Α–Φ―É―Ä–Α–Μ―¨–Ϋ–Ψ–Ι ―Ä–Α―¹–Ω―Ä–Ψ―¹―²―Ä–Α–Ϋ–Β–Ϋ–Ϋ–Ψ―¹―²–Η –Ω–Ψ –Ε–Β–Μ―É–¥–Κ―É, –≤―΄―¹–Ψ–Κ–Ψ–Ι –Ζ–Μ–Ψ–Κ–Α―΅–Β―¹―²–≤–Β–Ϋ–Ϋ–Ψ―¹―²–Η –¥–Α–Ϋ–Ϋ–Ψ–≥–Ψ ―²–Η–Ω–Α –Ψ–Ω―É―Ö–Ψ–Μ–Β–Ι –¥–Α–Ε–Β –Ω―Ä–Η –≤–Ψ–≤–Μ–Β―΅–Β–Ϋ–Η–Η –¥–Η―¹―²–Α–Μ―¨–Ϋ―΄―Ö –Ψ―²–¥–Β–Μ–Ψ–≤ –Ω–Η―â–Β–≤–Ψ–¥–Α –Ψ–Ω–Β―Ä–Α―Ü–Η–Β–Ι –≤―΄–±–Ψ―Ä–Α ―è–≤–Μ―è–Β―²―¹―è –≥–Α―¹―²―Ä―ç–Κ―²–Ψ–Φ–Η―è ―¹ ―²―Ä–Α–Ϋ―¹―Ö–Η–Α―²–Α–Μ―¨–Ϋ–Ψ–Ι ―Ä–Β–Ζ–Β–Κ―Ü–Η–Β–Ι –Ω–Η―â–Β–≤–Ψ–¥–Α [22].
–£―΄–¥–Β–Μ–Β–Ϋ–Ϋ―΄–Β ―²―Ä–Η ―²–Η–Ω–Α –Ψ–Ω―É―Ö–Ψ–Μ–Β–Ι ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Η–Ζ―É―é―²―¹―è ―Ä–Α–Ζ–Μ–Η―΅–Ϋ―΄–Φ –Ω―Ä–Ψ–≥–Ϋ–Ψ–Ζ–Ψ–Φ, ―΅―²–Ψ –Ψ–Ω―Ä–Β–¥–Β–Μ―è–Β―²―¹―è ―¹–Ψ–≤–Ψ–Κ―É–Ω–Ϋ–Ψ―¹―²―¨―é –Φ–Ϋ–Ψ–Ε–Β―¹―²–≤–Α ―³–Α–Κ―²–Ψ―Ä–Ψ–≤, –≤ –Ω–Β―Ä–≤―É―é –Ψ―΅–Β―Ä–Β–¥―¨ – ―Ä–Α―¹–Ω―Ä–Ψ―¹―²―Ä–Α–Ϋ–Β–Ϋ–Ϋ–Ψ―¹―²―¨―é –Ϋ–Α –Φ–Ψ–Φ–Β–Ϋ―² –Μ–Β―΅–Β–Ϋ–Η―è, –Α ―²–Α–Κ–Ε–Β ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Η―¹―²–Η–Κ–Α–Φ–Η –Ψ–Ω―É―Ö–Ψ–Μ–Β–Ι. –ù–Α –Ψ―¹–Ϋ–Ψ–≤–Α–Ϋ–Η–Η ―Ä–Β–Ζ―É–Μ―¨―²–Α―²–Ψ–≤ –Μ–Β―΅–Β–Ϋ–Η―è –±–Ψ–Μ–Β–Β ―΅–Β–Φ 1600 –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –Ζ–Α –Ω–Β―Ä–Η–Ψ–¥ ―¹ 1982 –Ω–Ψ 2003 –≥–Ψ–¥ Siewert J.R. –Η ―¹–Ψ–Α–≤―². (2006) ―É―¹―²–Α–Ϋ–Ψ–≤–Η–Μ–Η, ―΅―²–Ψ –Ϋ–Α–Η–Μ―É―΅―à–Η–Φ –Ω―Ä–Ψ–≥–Ϋ–Ψ–Ζ–Ψ–Φ ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Η–Ζ―É–Β―²―¹―è I ―²–Η–Ω, –≤–Ψ–Ζ–Ϋ–Η–Κ―à–Η–Ι –Ϋ–Α ―³–Ψ–Ϋ–Β –Ω–Η―â–Β–≤–Ψ–¥–Α –ë–Α―Ä―Ä–Β―²―²–Α. –ë–Ψ–Μ–Β–Β –Ω–Μ–Ψ―Ö–Η–Φ –Ω―Ä–Ψ–≥–Ϋ–Ψ–Ζ–Ψ–Φ ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Η–Ζ―É–Β―²―¹―è II ―²–Η–Ω, ―²–Ψ–≥–¥–Α –Κ–Α–Κ –Ω―Ä–Η III ―²–Η–Ω–Β –Ψ―²–Φ–Β―΅–Α―é―²―¹―è –Ϋ–Α–Η―Ö―É–¥―à–Η–Β ―Ä–Β–Ζ―É–Μ―¨―²–Α―²―΄ – ―ç―²–Ψ –Ψ–±―É―¹–Μ–Ψ–≤–Μ–Β–Ϋ–Ψ –Ω―Ä–Β–Ψ–±–Μ–Α–¥–Α–Ϋ–Η–Β–Φ –Ψ–Ω―É―Ö–Ψ–Μ–Β–Ι –¥–Η―³―³―É–Ζ–Ϋ–Ψ–≥–Ψ ―²–Η–Ω–Α ―¹ –±–Ψ–Μ–Β–Β –≤―΄―¹–Ψ–Κ–Ψ–Ι ―΅–Α―¹―²–Ψ―²–Ψ–Ι –≤–Ψ–≤–Μ–Β―΅–Β–Ϋ–Η―è ―¹–Β―Ä–Ψ–Ζ–Ϋ–Ψ–Ι –Ψ–±–Ψ–Μ–Ψ―΅–Κ–Η –Η –Ϋ–Α–Μ–Η―΅–Η–Β–Φ –Μ–Η–Φ―³–Ψ–≥–Β–Ϋ–Ϋ―΄―Ö –Φ–Β―²–Α―¹―²–Α–Ζ–Ψ–≤ [23–26].
–ù–Α –Ψ―¹–Ϋ–Ψ–≤–Α–Ϋ–Η–Η –Ω―Ä–Ψ–≤–Β–¥–Β–Ϋ–Ϋ–Ψ–≥–Ψ –Α–Ϋ–Α–Μ–Η–Ζ–Α –Α–≤―²–Ψ―Ä―΄ –¥–Β–Μ–Α―é―² –≤―΄–≤–Ψ–¥ –Ψ –≤―΄―¹–Ψ–Κ–Ψ–Ι –Ω―Ä–Ψ–≥–Ϋ–Ψ―¹―²–Η―΅–Β―¹–Κ–Ψ–Ι –Ζ–Ϋ–Α―΅–Η–Φ–Ψ―¹―²–Η –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η –Α–¥–Β–Ϋ–Ψ–Κ–Α―Ä―Ü–Η–Ϋ–Ψ–Φ –Κ–Α―Ä–¥–Η–Ψ―ç–Ζ–Ψ―³–Α–≥–Β–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ω–Β―Ä–Β―Ö–Ψ–¥–Α –¥–Μ―è –Ψ–Ω―Ä–Β–¥–Β–Μ–Β–Ϋ–Η―è ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Α –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è –Η ―¹―²–Α–Ϋ–¥–Α―Ä―²–Η–Ζ–Α―Ü–Η–Η ―²–Α–Κ―²–Η–Κ–Η ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Μ–Β―΅–Β–Ϋ–Η―è. –ù–Α ―¹–Β–≥–Ψ–¥–Ϋ―è―à–Ϋ–Η–Ι –¥–Β–Ϋ―¨ –≤―¹–Β –±–Ψ–Μ―¨―à–Β –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α―²–Β–Μ–Β–Ι –Ψ―²–Φ–Β―΅–Α―é―² –Ω―Ä–Ψ―¹―²–Ψ―²―É –Η –Ω―Ä–Α–Κ―²–Η―΅–Β―¹–Κ―É―é ―Ü–Β–Μ–Β―¹–Ψ–Ψ–±―Ä–Α–Ζ–Ϋ–Ψ―¹―²―¨ –Ω―Ä–Η–Φ–Β–Ϋ–Β–Ϋ–Η―è –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η Siewert J.R. –Ω―Ä–Η ―Ä–Α–Κ–Β –Ω―Ä–Ψ–Κ―¹–Η–Φ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ–Α –Ε–Β–Μ―É–¥–Κ–Α. –ù–Α –Κ–Ψ–Ϋ―¹–Β–Ϋ―¹―É―¹–Ϋ–Ψ–Ι –Κ–Ψ–Ϋ―³–Β―Ä–Β–Ϋ―Ü–Η–Η, –Ω―Ä–Ψ–≤–Β–¥–Β–Ϋ–Ϋ–Ψ–Ι ―¹–Ψ–≤–Φ–Β―¹―²–Ϋ–Ψ –€–Β–Ε–¥―É–Ϋ–Α―Ä–Ψ–¥–Ϋ―΄–Φ –û–±―â–Β―¹―²–≤–Ψ–Φ –Ω–Ψ –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è–Φ –Ω–Η―â–Β–≤–Ψ–¥–Α (International Society for Diseases of the Esophagus – ISDE) –Η –€–Β–Ε–¥―É–Ϋ–Α―Ä–Ψ–¥–Ϋ–Ψ–Ι –ê―¹―¹–Ψ―Ü–Η–Α―Ü–Η–Β–Ι –Ω–Ψ ―Ä–Α–Κ―É –Ε–Β–Μ―É–¥–Κ–Α (International Gastric Cancer Association – IGCA) –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η―è Siewert J.R. –±―΄–Μ–Α –Ω―Ä–Η–Ϋ―è―²–Α –Ζ–Α –Ψ―¹–Ϋ–Ψ–≤―É –≤ –Ψ–Ω–Η―¹–Α–Ϋ–Η–Η, –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η –Η –Ω–Ψ–¥―Ö–Ψ–¥–Α–Φ –Κ –Μ–Β―΅–Β–Ϋ–Η―é –¥–Α–Ϋ–Ϋ–Ψ–Ι –Ω–Α―²–Ψ–Μ–Ψ–≥–Η–Η [27].
–û–±―ä–Β–Φ –Α–±–¥–Ψ–Φ–Η–Ϋ–Α–Μ―¨–Ϋ–Ψ–Ι
–Η –Φ–Β–¥–Η–Α―¹―²–Η–Ϋ–Α–Μ―¨–Ϋ–Ψ–Ι –Μ–Η–Φ―³–Ψ–¥–Η―¹―¹–Β–Κ―Ü–Η–Η
D2 –¦–î – –Φ–Η–Ϋ–Η–Φ–Α–Μ―¨–Ϋ–Ψ –Ϋ–Β–Ψ–±―Ö–Ψ–¥–Η–Φ―΄–Ι –Ψ–±―ä–Β–Φ –≤–Φ–Β―à–Α―²–Β–Μ―¨―¹―²–≤–Α –Ϋ–Α –Μ–Η–Φ―³–Ψ–Κ–Ψ–Μ–Μ–Β–Κ―²–Ψ―Ä–Α―Ö –±―Ä―é―à–Ϋ–Ψ–Ι –Ω–Ψ–Μ–Ψ―¹―²–Η, –Ϋ–Β–Ζ–Α–≤–Η―¹–Η–Φ–Ψ –Ψ―² ―²–Η–Ω–Α –Κ–Α―Ä–¥–Η–Ψ―ç–Ζ–Ψ―³–Α–≥–Β–Α–Μ―¨–Ϋ–Ψ–≥–Ψ ―Ä–Α–Κ–Α. –≠―²–Ψ―² –Ψ–±―ä–Β–Φ –Ω―Ä–Η–Ϋ―è―² –Α–±―¹–Ψ–Μ―é―²–Ϋ―΄–Φ –±–Ψ–Μ―¨―à–Η–Ϋ―¹―²–≤–Ψ–Φ ―¹–Ω–Β―Ü–Η–Α–Μ–Η–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ―΄―Ö –Κ–Μ–Η–Ϋ–Η–Κ, –Η –≤ –Ϋ–Α―¹―²–Ψ―è―â–Β–Β –≤―Ä–Β–Φ―è –Ψ―¹―²―Ä–Ψ―²–Α –¥–Η―¹–Κ―É―¹―¹–Η–Η «D1 –Η–Μ–Η D2?» –Ω–Ψ―²–Β―Ä―è–Μ–Α –Α–Κ―²―É–Α–Μ―¨–Ϋ–Ψ―¹―²―¨.
–û–±―ä–Β–Φ –Φ–Β–¥–Η–Α―¹―²–Η–Ϋ–Α–Μ―¨–Ϋ–Ψ–Ι –¦–î –Ψ–Ω―Ä–Β–¥–Β–Μ―è–Β―²―¹―è –≤ –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ–Ι ―¹―²–Β–Ω–Β–Ϋ–Η ―²–Η–Ω–Ψ–Φ –Ψ–Ω―É―Ö–Ψ–Μ–Η –Η, ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤–Β–Ϋ–Ϋ–Ψ, –≤–Ψ–Ζ–Φ–Ψ–Ε–Ϋ–Ψ―¹―²―è–Φ–Η –≤―΄–±―Ä–Α–Ϋ–Ϋ–Ψ–≥–Ψ ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –¥–Ψ―¹―²―É–Ω–Α. –ü―Ä–Η ―²–Η–Ω–Β I, ―¹ ―É―΅–Β―²–Ψ–Φ –≤―΄―¹–Ψ–Κ–Ψ–Ι ―΅–Α―¹―²–Ψ―²―΄ –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η―è –Μ–Η–Φ―³–Ψ―É–Ζ–Μ–Ψ–≤ –Ϋ–Β ―²–Ψ–Μ―¨–Κ–Ψ –Ϋ–Η–Ε–Ϋ–Β–≥–Ψ, –Ϋ–Ψ –Η –≤–Β―Ä―Ö–Ϋ–Β–≥–Ψ ―¹―Ä–Β–¥–Ψ―¹―²–Β–Ϋ–Η―è, ―²―Ä–Β–±―É–Β―²―¹―è –±–Η–Μ–Α―²–Β―Ä–Α–Μ―¨–Ϋ–Α―è –Φ–Β–¥–Η–Α―¹―²–Η–Ϋ–Α–Μ―¨–Ϋ–Α―è –¦–î – ―Ä–Α―¹―à–Η―Ä–Β–Ϋ–Ϋ–Α―è –¥–≤―É―Ö–Ζ–Ψ–Ϋ–Α–Μ―¨–Ϋ–Α―è –¦–î [Siewert J.R. et al., 2006] [28]. –ü―Ä–Η –Κ–Α―Ä–¥–Η–Ψ―ç–Ζ–Ψ―³–Α–≥–Β–Α–Μ―¨–Ϋ–Ψ–Φ ―Ä–Α–Κ–Β II –Η III ―²–Η–Ω–Ψ–≤ –Φ–Β―²–Α―¹―²–Α–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Η–Β –≤ –Μ–Η–Φ―³–Ψ―É–Ζ–Μ―΄ –≤–Β―Ä―Ö–Ϋ–Β–≥–Ψ ―¹―Ä–Β–¥–Ψ―¹―²–Β–Ϋ–Η―è –Ϋ–Β ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Ϋ–Ψ –Η –Ψ–±―ä–Β–Φ –Φ–Β–¥–Η–Α―¹―²–Η–Ϋ–Α–Μ―¨–Ϋ–Ψ–Ι –¦–î, –Κ–Α–Κ –Ω―Ä–Α–≤–Η–Μ–Ψ, –Ψ–≥―Ä–Α–Ϋ–Η―΅–Η–≤–Α–Β―²―¹―è –Η―¹―¹–Β―΅–Β–Ϋ–Η–Β–Φ –Ϋ–Α–¥–¥–Η–Α―³―Ä–Α–≥–Φ–Α–Μ―¨–Ϋ―΄―Ö, –Ϋ–Η–Ε–Ϋ–Η―Ö –Ω–Α―Ä–Α―ç–Ζ–Ψ―³–Α–≥–Β–Α–Μ―¨–Ϋ―΄―Ö –Η –±–Η―³―É―Ä–Κ–Α―Ü–Η–Ψ–Ϋ–Ϋ―΄―Ö –Μ–Η–Φ―³–Ψ―É–Ζ–Μ–Ψ–≤.
–ê–±–¥–Ψ–Φ–Η–Ϋ–Α–Μ―¨–Ϋ–Α―è –Η –Φ–Β–¥–Η–Α―¹―²–Η–Ϋ–Α–Μ―¨–Ϋ–Α―è –¦–î –Ω―Ä–Η –Ψ–Ω–Β―Ä–Α―Ü–Η―è―Ö –Ω–Ψ –Ω–Ψ–≤–Ψ–¥―É –Κ–Α―Ä–¥–Η–Ψ―ç–Ζ–Ψ―³–Α–≥–Β–Α–Μ―¨–Ϋ–Ψ–≥–Ψ ―Ä–Α–Κ–Α, –Ϋ–Α―Ä―è–¥―É ―¹ –Η―¹―¹–Β―΅–Β–Ϋ–Η–Β–Φ –Φ–Α–Κ―Ä–Ψ– –Η –Φ–Η–Κ―Ä–Ψ–Φ–Β―²–Α―¹―²–Α–Ζ–Ψ–≤ –≤ –Μ–Η–Φ―³–Ψ―É–Ζ–Μ–Α―Ö, –Ω–Ψ–≤―΄―à–Α―é―â–Η–Φ ―Ä–Α–¥–Η–Κ–Α–Μ–Η–Ζ–Φ ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –≤–Φ–Β―à–Α―²–Β–Μ―¨―¹―²–≤–Α, –¥–Α–Β―² –Β―â–Β –Η –≤–Ψ–Ζ–Φ–Ψ–Ε–Ϋ–Ψ―¹―²―¨ –Ψ―Ü–Β–Ϋ–Η―²―¨ ―¹―²–Β–Ω–Β–Ϋ―¨ –Η –Ϋ–Α–Ω―Ä–Α–≤–Μ–Β–Ϋ–Ϋ–Ψ―¹―²―¨ –Μ–Η–Φ―³–Ψ–≥–Β–Ϋ–Ϋ–Ψ–≥–Ψ –Φ–Β―²–Α―¹―²–Α–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Η―è, –Α –Ζ–Ϋ–Α―΅–Η―², –Ω–Ψ–Ζ–≤–Ψ–Μ―è–Β―² –±–Ψ–Μ–Β–Β ―²–Ψ―΅–Ϋ–Ψ –Ψ–Ω―Ä–Β–¥–Β–Μ–Η―²―¨ ―¹―²–Α–¥–Η―é –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è.
–û―²–¥–Α–Μ–Β–Ϋ–Ϋ―΄–Β ―Ä–Β–Ζ―É–Μ―¨―²–Α―²―΄
–ü–Ψ –¥–Α–Ϋ–Ϋ―΄–Φ –†–û–ù–Π –†–ê–€–ù, ―¹―É–Φ–Φ–Α―Ä–Ϋ–Α―è 5––Μ–Β―²–Ϋ―è―è –≤―΄–Ε–Η–≤–Α–Β–Φ–Ψ―¹―²―¨ –±–Ψ–Μ―¨–Ϋ―΄―Ö, –Ψ–Ω–Β―Ä–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ―΄―Ö –Ω–Ψ –Ω–Ψ–≤–Ψ–¥―É –Κ–Α―Ä–¥–Η–Ψ―ç–Ζ–Ψ―³–Α–≥–Β–Α–Μ―¨–Ϋ–Ψ–≥–Ψ ―Ä–Α–Κ–Α, ―¹–Ψ―¹―²–Α–≤–Η–Μ–Α 36,2%.
–Δ–Α–Κ, –Ω―Ä–Η –Η―¹―²–Η–Ϋ–Ϋ–Ψ–Φ ―Ä–Α–Κ–Β –Κ–Α―Ä–¥–Η–Ψ―ç–Ζ–Ψ―³–Α–≥–Β–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ω–Β―Ä–Β―Ö–Ψ–¥–Α (AEG II type) ―¹―Ä–Β–¥–Ϋ―è―è –Ω―Ä–Ψ–¥–Ψ–Μ–Ε–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²―¨ –Ε–Η–Ζ–Ϋ–Η ―¹–Ψ―¹―²–Α–≤–Η–Μ–Α 72,3±6,1 –Φ–Β―¹―è―Ü–Β–≤. –≠―²–Η –Ω–Ψ–Κ–Α–Ζ–Α―²–Β–Μ–Η –±―΄–Μ–Η ―¹―²–Α―²–Η―¹―²–Η―΅–Β―¹–Κ–Η –¥–Ψ―¹―²–Ψ–≤–Β―Ä–Ϋ–Ψ –Μ―É―΅―à–Β, ―΅–Β–Φ –≤ –≥―Ä―É–Ω–Ω–Β ―Ä–Α–Κ–Α ―¹―É–±–Κ–Α―Ä–¥–Η–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ–Α –Ε–Β–Μ―É–¥–Κ–Α (AEG III type) ―¹ ―Ä–Α―¹–Ω―Ä–Ψ―¹―²―Ä–Α–Ϋ–Β–Ϋ–Η–Β–Φ –Ϋ–Α –Ω–Η―â–Β–≤–Ψ–¥, –≥–¥–Β –Α–Ϋ–Α–Μ–Ψ–≥–Η―΅–Ϋ―΄–Β –Ω–Ψ–Κ–Α–Ζ–Α―²–Β–Μ–Η ―¹–Ψ―¹―²–Α–≤–Μ―è―é―² 36,5±3,2 –Φ–Β―¹―è―Ü–Β–≤. –Γ―²–Α―²–Η―¹―²–Η―΅–Β―¹–Κ–Η –Ζ–Ϋ–Α―΅–Η–Φ–Ψ–Β –Ω―Ä–Β–Η–Φ―É―â–Β―¹―²–≤–Ψ –Ψ–Ω―É―Ö–Ψ–Μ–Β–Ι –≤―²–Ψ―Ä–Ψ–≥–Ψ ―²–Η–Ω–Α ―²–Α–Κ–Ε–Β ―¹ –¥–Ψ―¹―²–Α―²–Ψ―΅–Ϋ–Ψ–Ι –Ψ―΅–Β–≤–Η–¥–Ϋ–Ψ―¹―²―¨―é –Ψ–Ω―Ä–Β–¥–Β–Μ―è–Β―²―¹―è –Φ–Β–¥–Η–Α–Ϋ–Ψ–Ι –≤―΄–Ε–Η–≤–Α–Β–Φ–Ψ―¹―²–Η, –Κ–Ψ―²–Ψ―Ä–Α―è ―¹–Ψ―¹―²–Α–≤–Μ―è–Β―² 38,0±8,4 –Η 15,0±1,2 –Φ–Β―¹―è―Ü–Β–≤ ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤–Β–Ϋ–Ϋ–Ψ.
–ü―Ä–Β–¥―¹―²–Α–≤–Μ–Β–Ϋ–Ϋ―΄–Β –¥–Α–Ϋ–Ϋ―΄–Β –Ϋ–Α–≥–Μ―è–¥–Ϋ–Ψ –¥–Β–Φ–Ψ–Ϋ―¹―²―Ä–Η―Ä―É―é―² –Ω―Ä–Ψ–≥–Ϋ–Ψ―¹―²–Η―΅–Β―¹–Κ–Ψ–Β –Ζ–Ϋ–Α―΅–Β–Ϋ–Η–Β –Μ–Ψ–Κ–Α–Μ–Η–Ζ–Α―Ü–Η–Η –Ψ–Ω―É―Ö–Ψ–Μ–Η, ―΅―²–Ψ –Ψ–Ω―Ä–Β–¥–Β–Μ―è–Β―²―¹―è ―¹–Ψ–≤–Ψ–Κ―É–Ω–Ϋ–Ψ―¹―²―¨―é ―³–Α–Κ―²–Ψ―Ä–Ψ–≤. –†–Α–Ζ–Ϋ–Η―Ü–Α –Φ–Β–Ε–¥―É –≥―Ä―É–Ω–Ω–Α–Φ–Η ―¹ –Ψ–Ω―É―Ö–Ψ–Μ―è–Φ–Η II –Η III ―²–Η–Ω–Α ―¹―²–Α―²–Η―¹―²–Η―΅–Β―¹–Κ–Η –¥–Ψ―¹―²–Ψ–≤–Β―Ä–Ϋ–Α (?2 = 34,99 –Ω―Ä–Η ―Ä=0,0001).
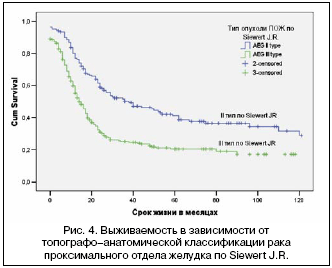
–£ ―Ü–Β–Μ–Ψ–Φ –Ω―Ä–Η II ―²–Η–Ω–Β –Α–¥–Β–Ϋ–Ψ–Κ–Α―Ä―Ü–Η–Ϋ–Ψ–Φ―΄ –Ω―Ä–Ψ–Κ―¹–Η–Φ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ–Α –Ε–Β–Μ―É–¥–Κ–Α (–ü–û–•) –Ω–Ψ–Κ–Α–Ζ–Α―²–Β–Μ–Η 5– –Η 10––Μ–Β―²–Ϋ–Β–Ι –≤―΄–Ε–Η–≤–Α–Β–Φ–Ψ―¹―²–Η ―¹–Ψ―¹―²–Α–≤–Μ―è―é―² ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤–Β–Ϋ–Ϋ–Ψ 47±4,1% –Η 38±4,7%, ―²–Ψ–≥–¥–Α –Κ–Α–Κ –¥–Μ―è –Α–¥–Β–Ϋ–Ψ–Κ–Α―Ä―Ü–Η–Ϋ–Ψ–Φ 3 ―²–Η–Ω–Α ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤―É―é―â–Η–Β –Ω–Ψ–Κ–Α–Ζ–Α―²–Β–Μ–Η –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ ―Ö―É–Ε–Β – ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤–Β–Ϋ–Ϋ–Ψ 23±3,0% –Η 21±3,4% (―Ä–Η―¹. 4).
–ù–Α–Η–±–Ψ–Μ–Β–Β –Ϋ–Η–Ζ–Κ–Η–Β –Ω–Ψ–Κ–Α–Ζ–Α―²–Β–Μ–Η –≤―΄–Ε–Η–≤–Α–Β–Φ–Ψ―¹―²–Η –Ω―Ä–Η III ―²–Η–Ω–Β –Ψ–Ω―É―Ö–Ψ–Μ–Β–Ι –Ω–Ψ–¥―²–≤–Β―Ä–Ε–¥–Β–Ϋ―΄ ―²–Α–Κ–Ε–Β –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è–Φ–Η Harrison L.E. (1997), Fern –€. (1998), Siewert J.R. (2000).
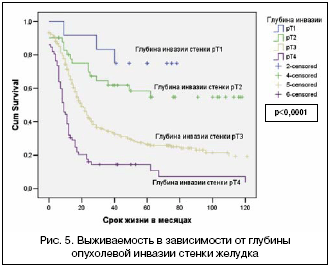
–Γ―Ä–Β–¥–Η ―³–Α–Κ―²–Ψ―Ä–Ψ–≤, ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Η–Ζ―É―é―â–Η―Ö ―Ä–Α―¹–Ω―Ä–Ψ―¹―²―Ä–Α–Ϋ–Β–Ϋ–Ϋ–Ψ―¹―²―¨ –Ψ–Ω―É―Ö–Ψ–Μ–Η, –Ψ–¥–Ϋ–Η–Φ –Η–Ζ –Ϋ–Α–Η–±–Ψ–Μ–Β–Β –Ζ–Ϋ–Α―΅–Η–Φ―΄―Ö ―è–≤–Μ―è–Β―²―¹―è –≥–Μ―É–±–Η–Ϋ–Α –Ψ–Ω―É―Ö–Ψ–Μ–Β–≤–Ψ–Ι –Η–Ϋ–≤–Α–Ζ–Η–Η.
–ù–Α–Η–±–Ψ–Μ–Β–Β ―Ö–Ψ―Ä–Ψ―à–Η–Β –Ψ―²–¥–Α–Μ–Β–Ϋ–Ϋ―΄–Β ―Ä–Β–Ζ―É–Μ―¨―²–Α―²―΄ –Ω–Ψ–Μ―É―΅–Β–Ϋ―΄ –≤ –≥―Ä―É–Ω–Ω–Α―Ö ―¹ ―É―Ä–Ψ–≤–Ϋ–Β–Φ –Η–Ϋ–≤–Α–Ζ–Η–Η –≤ –Ω―Ä–Β–¥–Β–Μ–Α―Ö ―¹―²–Β–Ϋ–Κ–Η –Ε–Β–Μ―É–¥–Κ–Α –±–Β–Ζ –Ω―Ä–Ψ―Ä–Α―¹―²–Α–Ϋ–Η―è ―¹–Β―Ä–Ψ–Ζ–Ϋ–Ψ–Ι –Ψ–±–Ψ–Μ–Ψ―΅–Κ–Η. –£ ―ç―²–Η―Ö –≥―Ä―É–Ω–Ω–Α―Ö –Ϋ–Β –¥–Ψ―¹―²–Η–≥–Ϋ―É―²–Α –Φ–Β–¥–Η–Α–Ϋ–Α –≤―΄–Ε–Η–≤–Α–Β–Φ–Ψ―¹―²–Η, ―΅―²–Ψ ―¹–≤–Η–¥–Β―²–Β–Μ―¨―¹―²–≤―É–Β―² –Ψ–± ―É–¥–Ψ–≤–Μ–Β―²–≤–Ψ―Ä–Η―²–Β–Μ―¨–Ϋ―΄―Ö –Ψ―²–¥–Α–Μ–Β–Ϋ–Ϋ―΄―Ö ―Ä–Β–Ζ―É–Μ―¨―²–Α―²–Α―Ö.
–ë–Ψ–Μ–Β–Β –Ϋ–Β–±–Μ–Α–≥–Ψ–Ω―Ä–Η―è―²–Ϋ―΄–Β –Ψ―²–¥–Α–Μ–Β–Ϋ–Ϋ―΄–Β ―Ä–Β–Ζ―É–Μ―¨―²–Α―²―΄ –Ω–Ψ–Μ―É―΅–Β–Ϋ―΄ –≤ –≥―Ä―É–Ω–Ω–Β –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –Ω―Ä–Η –Ω―Ä–Ψ―Ä–Α―¹―²–Α–Ϋ–Η–Η ―¹–Β―Ä–Ψ–Ζ–Ϋ–Ψ–Ι –Ψ–±–Ψ–Μ–Ψ―΅–Κ–Η –Η, –Ψ―¹–Ψ–±–Β–Ϋ–Ϋ–Ψ, –Ω―Ä–Η –≤―Ä–Α―¹―²–Α–Ϋ–Η–Η –≤ –Ψ–Κ―Ä―É–Ε–Α―é―â–Η–Β ―¹―²―Ä―É–Κ―²―É―Ä―΄. –ü―Ä–Η –Ω―Ä–Ψ―Ä–Α―¹―²–Α–Ϋ–Η–Η ―¹–Β―Ä–Ψ–Ζ–Ϋ–Ψ–Ι –Ψ–±–Ψ–Μ–Ψ―΅–Κ–Η (―Ä–Δ3) ―¹―Ä–Β–¥–Ϋ―è―è –Ω―Ä–Ψ–¥–Ψ–Μ–Ε–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²―¨ –Ε–Η–Ζ–Ϋ–Η ―¹–Ψ―¹―²–Α–≤–Μ―è–Β―² 48,0±3,6 –Φ–Β―¹―è―Ü–Β–≤ –Ω―Ä–Η –Φ–Β–¥–Η–Α–Ϋ–Β –≤―΄–Ε–Η–≤–Α–Β–Φ–Ψ―¹―²–Η 20,0±1,4 –Φ–Β―¹―è―Ü–Β–≤.
–ü―Ä–Η –≤―Ä–Α―¹―²–Α–Ϋ–Η–Η –≤ –Ψ–Κ―Ä―É–Ε–Α―é―â–Η–Β ―¹―²―Ä―É–Κ―²―É―Ä―΄ (―Ä–Δ4) –Ω–Ψ–Κ–Α–Ζ–Α―²–Β–Μ–Η –≤―΄–Ε–Η–≤–Α–Β–Φ–Ψ―¹―²–Η –Ϋ–Α–Η–±–Ψ–Μ–Β–Β –Ϋ–Η–Ζ–Κ–Η–Β – ―¹―Ä–Β–¥–Ϋ―è―è –Ω―Ä–Ψ–¥–Ψ–Μ–Ε–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²―¨ –Ε–Η–Ζ–Ϋ–Η ―¹–Ψ―¹―²–Α–≤–Η–Μ–Α –Μ–Η―à―¨ 22,5±5,3 –Φ–Β―¹―è―Ü–Β–≤, –Α –Φ–Β–¥–Η–Α–Ϋ–Α –≤―΄–Ε–Η–≤–Α–Β–Φ–Ψ―¹―²–Η –Μ–Η―à―¨ 9 –Φ–Β―¹―è―Ü–Β–≤, ―².–Β. –±–Ψ–Μ–Β–Β –Ω–Ψ–Μ–Ψ–≤–Η–Ϋ―΄ –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―É–Φ―Ä–Β―² –≤ ―²–Β―΅–Β–Ϋ–Η–Η –Ω–Β―Ä–≤–Ψ–≥–Ψ –≥–Ψ–¥–Α –Ϋ–Α–±–Μ―é–¥–Β–Ϋ–Η―è (―Ä–Η―¹. 5).
–£ –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²–Η –Ψ―² ―É―Ä–Ψ–≤–Ϋ―è –Η–Ϋ–≤–Α–Ζ–Η–Η 5– –Η 10––Μ–Β―²–Ϋ―è―è –≤―΄–Ε–Η–≤–Α–Β–Φ–Ψ―¹―²―¨ ―¹–Ψ―¹―²–Α–≤–Η–Μ–Α –¥–Μ―è –Ψ–Ω―É―Ö–Ψ–Μ–Β–Ι –Δ1, –Δ2, –Δ3 –Η –Δ4 ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤–Β–Ϋ–Ϋ–Ψ 76±12,1% –Η 76±12,1%; 54±7,6% –Η 54±7,6%; 31±5,3% –Η 21±5,8%; 17±5,3% –Η 11±5,6%.
–î―Ä―É–≥–Η–Φ –≤–Α–Ε–Ϋ―΄–Φ –Ω―Ä–Ψ–≥–Ϋ–Ψ―¹―²–Η―΅–Β―¹–Κ–Η–Φ ―³–Α–Κ―²–Ψ―Ä–Ψ–Φ ―è–≤–Μ―è–Β―²―¹―è –Μ–Η–Φ―³–Ψ–≥–Β–Ϋ–Ϋ–Α―è ―Ä–Α―¹–Ω―Ä–Ψ―¹―²―Ä–Α–Ϋ–Β–Ϋ–Ϋ–Ψ―¹―²―¨ –Ω―Ä–Ψ―Ü–Β―¹―¹–Α.
–ù–Α–Η–±–Ψ–Μ―¨―à–Β–Β –Ω―Ä–Η–Φ–Β–Ϋ–Β–Ϋ–Η–Β –Ϋ–Α ―¹–Β–≥–Ψ–¥–Ϋ―è―à–Ϋ–Η–Ι –¥–Β–Ϋ―¨ –Η–Φ–Β―é―² 2 –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η – –·–Ω–Ψ–Ϋ―¹–Κ–Ψ–Ι –ê―¹―¹–Ψ―Ü–Η–Α―Ü–Η–Η –Ω–Ψ ―Ä–Α–Κ―É –Ε–Β–Μ―É–¥–Κ–Α (JGCA, 1998 –≥–Ψ–¥–Α) –Η –€–Β–Ε–¥―É–Ϋ–Α―Ä–Ψ–¥–Ϋ–Ψ–≥–Ψ –Ω―Ä–Ψ―²–Η–≤–Ψ―Ä–Α–Κ–Ψ–≤–Ψ–≥–Ψ –Γ–Ψ―é–Ζ–Α (UICC, 2002). –£ –Ψ―¹–Ϋ–Ψ–≤–Β ―ç―²–Η―Ö –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Ι –Μ–Β–Ε–Η―² ―Ä–Α–Ζ–Μ–Η―΅–Ϋ―΄–Ι –Ω―Ä–Η–Ϋ―Ü–Η–Ω ―¹―²–Α–¥–Η―Ä–Ψ–≤–Α–Ϋ–Η―è –Μ–Η–Φ―³–Ψ–≥–Β–Ϋ–Ϋ–Ψ–Ι ―Ä–Α―¹–Ω―Ä–Ψ―¹―²―Ä–Α–Ϋ–Β–Ϋ–Ϋ–Ψ―¹―²–Η. –£ –Ψ―¹–Ϋ–Ψ–≤–Β –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η JGCA (1998) –Μ–Β–Ε–Η―² –Α–Ϋ–Α―²–Ψ–Φ–Η―΅–Β―¹–Κ–Η–Ι –Ω―Ä–Η–Ϋ―Ü–Η–Ω. –£ –Ψ―²–Μ–Η―΅–Η–Β –Ψ―² –Ω―Ä–Η–Ϋ―Ü–Η–Ω–Ψ–≤ JGCA –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η―è UICC (2002) ―Ä–Α―¹―¹–Φ–Α―²―Ä–Η–≤–Α–Β―² –Μ–Η―à―¨ –Κ–Ψ–Μ–Η―΅–Β―¹―²–≤–Β–Ϋ–Ϋ–Ψ–Β –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η–Β ―Ä–Β–≥–Η–Ψ–Ϋ–Α―Ä–Ϋ―΄―Ö –Μ–Η–Φ―³–Α―²–Η―΅–Β―¹–Κ–Η―Ö ―É–Ζ–Μ–Ψ–≤ –≤–Ϋ–Β –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²–Η –Ψ―² –Η―Ö –Μ–Ψ–Κ–Α–Μ–Η–Ζ–Α―Ü–Η–Η.
–ü―Ä–Η–Ϋ―Ü–Η–Ω–Η–Α–Μ―¨–Ϋ―΄–Φ ―Ä–Α–Ζ–Μ–Η―΅–Η–Β–Φ –¥–≤―É―Ö –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Ι, ―¹ –Ψ–¥–Ϋ–Ψ–Ι ―¹―²–Ψ―Ä–Ψ–Ϋ―΄, ―è–≤–Μ―è–Β―²―¹―è –Ψ–±―ä–Β–¥–Η–Ϋ–Β–Ϋ–Η–Β ―Ä–Α–Ζ–Μ–Η―΅–Ϋ―΄―Ö –≥―Ä―É–Ω–Ω –Μ–Η–Φ―³–Ψ–Κ–Ψ–Μ–Μ–Β–Κ―²–Ψ―Ä–Ψ–≤ –≤ ―Ä–Β–≥–Η–Ψ–Ϋ–Α―Ä–Ϋ―΄–Β, –≤–Ϋ–Β –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²–Η –Ψ―² –Μ–Ψ–Κ–Α–Μ–Η–Ζ–Α―Ü–Η–Η –Ω–Β―Ä–≤–Η―΅–Ϋ–Ψ–Ι –Ψ–Ω―É―Ö–Ψ–Μ–Η –≤ –Ε–Β–Μ―É–¥–Κ–Β –Η –Ψ―²–¥–Α–Μ–Β–Ϋ–Ϋ–Ψ―¹―²–Η –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Ϋ―΄―Ö ―É–Ζ–Μ–Ψ–≤, ―¹ ―É―΅–Β―²–Ψ–Φ ―ç―²–Α–Ω–Ϋ–Ψ―¹―²–Η –Φ–Β―²–Α―¹―²–Α–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Η―è, –Α ―¹ –¥―Ä―É–≥–Ψ–Ι – –Φ–Β―Ö–Α–Ϋ–Η―¹―²–Η―΅–Β―¹–Κ–Η–Ι –Ω–Ψ–¥―Ö–Ψ–¥ –Κ –Ψ―Ü–Β–Ϋ–Κ–Β ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Α –Μ–Η–Φ―³–Ψ–≥–Β–Ϋ–Ϋ–Ψ–Ι ―Ä–Α―¹–Ω―Ä–Ψ―¹―²―Ä–Α–Ϋ–Β–Ϋ–Ϋ–Ψ―¹―²–Η.
–†–Β–Ζ―é–Φ–Η―Ä―É―è –Ϋ–Α―à–Η –¥–Α–Ϋ–Ϋ―΄–Β –Ω–Ψ –Α–Ϋ–Α–Μ–Η–Ζ―É –Ψ–±–Β–Η―Ö –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Ι, –Φ–Ψ–Ε–Ϋ–Ψ ―¹–¥–Β–Μ–Α―²―¨ –Ϋ–Β―¹–Κ–Ψ–Μ―¨–Κ–Ψ –≤―΄–≤–Ψ–¥–Ψ–≤. –û―¹–Ϋ–Ψ–≤–Ϋ―΄–Φ –≤―΄–≤–Ψ–¥–Ψ–Φ ―è–≤–Μ―è–Β―²―¹―è ―²–Ψ, ―΅―²–Ψ –Ψ–±–Β –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η –¥–Ψ―¹―²–Α―²–Ψ―΅–Ϋ–Ψ ―΅–Β―²–Κ–Ψ, ―¹―²–Α―²–Η―¹―²–Η―΅–Β―¹–Κ–Η –Ζ–Ϋ–Α―΅–Η–Φ–Ψ, ―¹―²―Ä–Α―²–Η―³–Η―Ü–Η―Ä―É―é―² –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –Ω–Ψ –Ω–Ψ–¥–≥―Ä―É–Ω–Ω–Α–Φ ―¹ ―É―΅–Β―²–Ψ–Φ –Ω–Ψ–Κ–Α–Ζ–Α―²–Β–Μ–Β–Ι –≤―΄–Ε–Η–≤–Α–Β–Φ–Ψ―¹―²–Η. –û–¥–Ϋ–Α–Κ–Ψ, –Ω–Ψ–Φ–Η–Φ–Ψ ―¹–Α–Φ–Ψ–Ι –Ζ–Ϋ–Α―΅–Η–Φ–Ψ―¹―²–Η, –Κ–Α–Ε–¥–Α―è –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η―è –¥–Ψ–Μ–Ε–Ϋ–Α ―Ä–Β―à–Α―²―¨ –Η ―¹–Ω–Β–Κ―²―Ä –Ω―Ä–Α–Κ―²–Η―΅–Β―¹–Κ–Η―Ö –Ζ–Α–¥–Α―΅. –Δ–Α–Κ, –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η―è JGCA (1998) ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Η–Ζ―É–Β―²―¹―è –Ω–Ψ–Μ–Η–≤–Α–Μ–Β–Ϋ―²–Ϋ–Ψ―¹―²―¨―é:
• –Ω–Ψ–Ζ–≤–Ψ–Μ―è–Β―² –¥–Ψ–Ψ–Ω–Β―Ä–Α―Ü–Η–Ψ–Ϋ–Ϋ–Ψ ―¹―²–Α–¥–Η―Ä–Ψ–≤–Α―²―¨ –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ ―É―΅–Β―²–Ψ–Φ –Μ–Η–Φ―³–Ψ–≥–Β–Ϋ–Ϋ–Ψ–Ι ―Ä–Α―¹–Ω―Ä–Ψ―¹―²―Ä–Α–Ϋ–Β–Ϋ–Ϋ–Ψ―¹―²–Η, ―΅―²–Ψ –Ϋ–Β –Ω–Ψ–Ζ–≤–Ψ–Μ―è–Β―² –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η―è UICC (2002);
• ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Η–Ζ―É–Β―² –Ϋ–Β–Ψ–±―Ö–Ψ–¥–Η–Φ―΄–Ι –Η –¥–Ψ―¹―²–Α―²–Ψ―΅–Ϋ―΄–Ι –Ψ–±―ä–Β–Φ –Μ–Η–Φ―³–Ψ–¥–Η―¹―¹–Β–Κ―Ü–Η–Η, –Ϋ–Α –Ψ―¹–Ϋ–Ψ–≤–Α–Ϋ–Η–Η –Κ–Ψ―²–Ψ―Ä–Ψ–≥–Ψ –Ψ–Ω―Ä–Β–¥–Β–Μ―è–Β―²―¹―è ―Ö–Α―Ä–Α–Κ―²–Β―Ä –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Ϋ–Ψ–≥–Ψ –≤–Φ–Β―à–Α―²–Β–Μ―¨―¹―²–≤–Α (―¹―²–Α–Ϋ–¥–Α―Ä―²–Ϋ―΄–Ι, ―Ä–Α―¹―à–Η―Ä–Β–Ϋ–Ϋ―΄–Ι);
• –Ω–Ψ–Ζ–≤–Ψ–Μ―è–Β―² –≤―΄–¥–Β–Μ–Η―²―¨ –Μ–Η–Φ―³–Α―²–Η―΅–Β―¹–Κ–Η–Β –Κ–Ψ–Μ–Μ–Β–Κ―²–Ψ―Ä―΄ –Ω–Ψ –≥―Ä―É–Ω–Ω–Α–Φ.
–Δ–Α–Κ–Η–Φ –Ψ–±―Ä–Α–Ζ–Ψ–Φ, –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η―è –·–Ω–Ψ–Ϋ―¹–Κ–Ψ–Ι –ê―¹―¹–Ψ―Ü–Η–Α―Ü–Η–Η –Ω–Ψ ―Ä–Α–Κ―É –Ε–Β–Μ―É–¥–Κ–Α ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Η–Ζ―É–Β―²―¹―è ―à–Η―Ä–Ψ–Κ–Η–Φ–Η –≤–Ψ–Ζ–Φ–Ψ–Ε–Ϋ–Ψ―¹―²―è–Φ–Η –Ω―Ä–Η –Ψ–Ω―Ä–Β–¥–Β–Μ–Β–Ϋ–Η–Η ―¹―²–Α–¥–Η–Η –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è –Η ―²–Α–Κ―²–Η–Κ–Η –Μ–Β―΅–Β–Ϋ–Η―è. –Λ–Α–Κ―²–Ψ―Ä ―¹―²–Α―²–Η―¹―²–Η―΅–Β―¹–Κ–Ψ–Ι –¥–Ψ―¹―²–Ψ–≤–Β―Ä–Ϋ–Ψ―¹―²–Η –¥–Η–≤–Β―Ä–≥–Β–Ϋ―Ü–Η–Η –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –Ω–Ψ –≥―Ä―É–Ω–Ω–Α–Φ –Ψ–Ω―Ä–Β–¥–Β–Μ―è–Β―² –≤―΄―¹–Ψ–Κ―É―é –Ω―Ä–Α–Κ―²–Η―΅–Β―¹–Κ―É―é –Ζ–Ϋ–Α―΅–Η–Φ–Ψ―¹―²―¨ –¥–Α–Ϋ–Ϋ–Ψ–Ι –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η. –ü–Ψ ―¹–≤–Ψ–Β–Φ―É –Ζ–Ϋ–Α―΅–Β–Ϋ–Η―é –¥–Μ―è ―³–Ψ―Ä–Φ–Η―Ä–Ψ–≤–Α–Ϋ–Η―è –Ω―Ä–Ψ–≥–Ϋ–Ψ–Ζ–Α –Ψ–Ϋ–Α –Ϋ–Β ―É―¹―²―É–Ω–Α–Β―² –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η UICC (2002), ―΅―²–Ψ –≤–Α–Ε–Ϋ–Ψ ―É―΅–Η―²―΄–≤–Α―²―¨ –≤ –Ω―Ä–Α–Κ―²–Η―΅–Β―¹–Κ–Ψ–Ι ―Ä–Α–±–Ψ―²–Β.
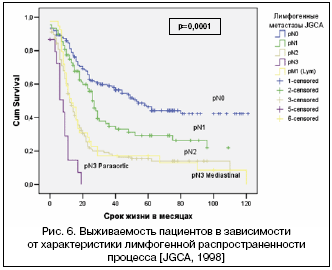
–ü―è―²–Η–Μ–Β―²–Ϋ―è―è –≤―΄–Ε–Η–≤–Α–Β–Φ–Ψ―¹―²―¨ –≤ –≥―Ä―É–Ω–Ω–Β pN0 ―¹–Ψ―¹―²–Α–≤–Μ―è–Β―² 53,5±4,4%, ―²–Ψ–≥–¥–Α –Κ–Α–Κ –Ω―Ä–Η pN1 ―¹–Ϋ–Η–Ε–Α–Β―²―¹―è –¥–Ψ 31±5,6%, –Α –Ω―Ä–Η pN2 ―¹–Ψ―¹―²–Α–≤–Μ―è–Β―² –Μ–Η―à―¨ 20,6±3,9%. –ü―Ä–Η –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η–Η –Μ–Η–Φ―³–Α―²–Η―΅–Β―¹–Κ–Η―Ö –Κ–Ψ–Μ–Μ–Β–Κ―²–Ψ―Ä–Ψ–≤ ―²―Ä–Β―²―¨–Β–≥–Ψ ―ç―²–Α–Ω–Α –Φ–Β―²–Α―¹―²–Α–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Η―è –Ψ―²–Φ–Β―΅–Α–Β―²―¹―è –¥–Η–≤–Β―Ä–≥–Β–Ϋ―Ü–Η―è –Κ―Ä–Η–≤―΄―Ö – –Ω―Ä–Η –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η–Η –Ω–Α―Ä–Α–Α–Ψ―Ä―²–Α–Μ―¨–Ϋ―΄―Ö ―É–Ζ–Μ–Ψ–≤ (pN3 Paraaortic) –Ϋ–Η–Κ―²–Ψ –Η–Ζ –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –Ϋ–Β –Ω–Β―Ä–Β–Ε–Η–≤–Α–Β―² 2 –Μ–Β―² –Ϋ–Α–±–Μ―é–¥–Β–Ϋ–Η―è, ―²–Ψ–≥–¥–Α –Κ–Α–Κ –Ω―Ä–Η –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η–Η –Φ–Β–¥–Η–Α―¹―²–Η–Ϋ–Α–Μ―¨–Ϋ―΄―Ö –Μ–Η–Φ―³–Ψ–Κ–Ψ–Μ–Μ–Β–Κ―²–Ψ―Ä–Ψ–≤ (pN3 Mediastinal) ―ç―²–Ψ―² –Ω–Ψ–Κ–Α–Ζ–Α―²–Β–Μ―¨ ―¹–Ψ―¹―²–Α–≤–Μ―è–Β―² 19,3±7,1% (―Ä–Η―¹. 6).
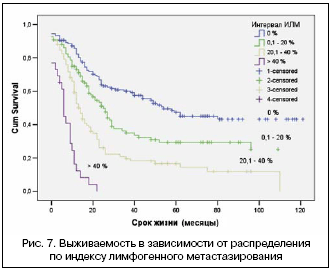
–ù–Α –Ψ―¹–Ϋ–Ψ–≤–Α–Ϋ–Η–Η –Ω―Ä–Η–≤–Β–¥–Β–Ϋ–Ϋ―΄―Ö –≤―΄―à–Β –¥–Α–Ϋ–Ϋ―΄―Ö –Ϋ–Α–Φ–Η –±―΄–Μ ―Ä–Α–Ζ―Ä–Α–±–Ψ―²–Α–Ϋ –Η–Ϋ–¥–Β–Κ―¹ –Μ–Η–Φ―³–Ψ–≥–Β–Ϋ–Ϋ–Ψ–≥–Ψ –Φ–Β―²–Α―¹―²–Α–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Η―è («–‰–¦–€») [29]. –≠―²–Ψ―² –Η–Ϋ–¥–Β–Κ―¹ ―è–≤–Μ―è–Β―²―¹―è –Η–Ϋ―²–Β–≥―Ä–Α–Μ―¨–Ϋ―΄–Φ –Ω–Ψ–Κ–Α–Ζ–Α―²–Β–Μ–Β–Φ ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Α –Η ―Ä–Α―¹–Ω―Ä–Ψ―¹―²―Ä–Α–Ϋ–Β–Ϋ–Ϋ–Ψ―¹―²–Η –Μ–Η–Φ―³–Ψ–≥–Β–Ϋ–Ϋ–Ψ–≥–Ψ –Φ–Β―²–Α―¹―²–Α–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Η―è, –Α ―²–Α–Κ–Ε–Β –Ψ–±―ä–Β–Φ–Α –Η ―²―â–Α―²–Β–Μ―¨–Ϋ–Ψ―¹―²–Η –≤―΄–Ω–Ψ–Μ–Ϋ―è–Β–Φ–Ψ–Ι –Μ–Η–Φ―³–Ψ–¥–Η―¹―¹–Β–Κ―Ü–Η–Η. –Γ ―É―΅–Β―²–Ψ–Φ –Η–Ϋ―²–Β–≥―Ä–Α–Μ―¨–Ϋ–Ψ―¹―²–Η ―¹–≤–Ψ–Β–≥–Ψ –Ζ–Ϋ–Α―΅–Β–Ϋ–Η―è –‰–¦–€ –Ψ―²―Ä–Α–Ε–Α–Β―² ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Η―¹―²–Η–Κ–Η –¥–≤―É―Ö –Κ–Ψ–Φ–Ω–Ψ–Ϋ–Β–Ϋ―²–Ψ–≤ ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Μ–Β―΅–Β–Ϋ–Η―è. –Γ –Ψ–¥–Ϋ–Ψ–Ι ―¹―²–Ψ―Ä–Ψ–Ϋ―΄, –Ψ–Ϋ –Ψ―²―Ä–Α–Ε–Α–Β―² ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Η―¹―²–Η–Κ―É –Μ–Η–Φ―³–Ψ–≥–Β–Ϋ–Ϋ–Ψ–≥–Ψ –Φ–Β―²–Α―¹―²–Α–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Η―è ―Ä–Α–Κ–Α –Ε–Β–Μ―É–¥–Κ–Α, –Α ―¹ –¥―Ä―É–≥–Ψ–Ι ―¹―²–Ψ―Ä–Ψ–Ϋ―΄, –Ψ–Ϋ ―É―΅–Η―²―΄–≤–Α–Β―² ―Ö–Α―Ä–Α–Κ―²–Β―Ä –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Ϋ–Ψ–Ι –Μ–Η–Φ―³–Ψ–¥–Η―¹―¹–Β–Κ―Ü–Η–Η. –ß–Β–Φ –Φ–Β–Ϋ―¨―à–Β –Ψ–±―ä–Β–Φ –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Ϋ–Ψ–Ι –Μ–Η–Φ―³–Ψ–¥–Η―¹―¹–Β–Κ―Ü–Η–Η, ―²–Β–Φ –≤―΄―à–Β –Ω–Ψ–Κ–Α–Ζ–Α―²–Β–Μ―¨ –Η–Ϋ–¥–Β–Κ―¹–Α –Η ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤–Β–Ϋ–Ϋ–Ψ ―Ö―É–Ε–Β –Ω―Ä–Ψ–≥–Ϋ–Ψ–Ζ –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è – –≤–Ψ–Ζ–Φ–Ψ–Ε–Ϋ–Ψ―¹―²―¨ –Ϋ–Η–≤–Β–Μ–Η―Ä–Ψ–≤–Α―²―¨ ―³–Β–Ϋ–Ψ–Φ–Β–Ϋ «–Φ–Η–≥―Ä–Α―Ü–Η–Η ―¹―²–Α–¥–Η–Η – Will Rogers» (―Ä–Η―¹. 7).
–ù–Α –Ψ―¹–Ϋ–Ψ–≤–Α–Ϋ–Η–Η –Ω―Ä–Β–¥–Μ–Ψ–Ε–Β–Ϋ–Ϋ–Ψ–≥–Ψ –‰–¦–€ –±―΄–Μ–Η ―Ä–Α―¹―¹―΅–Η―²–Α–Ϋ―΄ –Ω–Ψ–Κ–Α–Ζ–Α―²–Β–Μ–Η –≤―΄–Ε–Η–≤–Α–Β–Φ–Ψ―¹―²–Η. –ü―è―²–Η– –Η –¥–Β―¹―è―²–Η–Μ–Β―²–Ϋ―è―è –≤―΄–Ε–Η–≤–Α–Β–Φ–Ψ―¹―²―¨ –≤ –≥―Ä―É–Ω–Ω–Β pN0 ―¹–Ψ―¹―²–Α–≤–Μ―è–Β―² 52,8±4,4% –Η 49,0±4,6%, ―²–Ψ–≥–¥–Α –Κ–Α–Κ –Ω―Ä–Η pN1 ―¹–Ϋ–Η–Ε–Α–Β―²―¹―è –¥–Ψ 37,6±5,1% –Η 35,3±5,4% ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤–Β–Ϋ–Ϋ–Ψ, ―΅―²–Ψ –±–Μ–Η–Ζ–Κ–Ψ –Κ –Ω–Ψ–Κ–Α–Ζ–Α―²–Β–Μ―è–Φ –≤―΄–Ε–Η–≤–Α–Β–Φ–Ψ―¹―²–Η –Ω―Ä–Η ―¹―²―Ä–Α―²–Η―³–Η–Κ–Α―Ü–Η–Η –Ϋ–Α –Ψ―¹–Ϋ–Ψ–≤–Α–Ϋ–Η–Η ―è–Ω–Ψ–Ϋ―¹–Κ–Ψ–Ι –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η. –ü―Ä–Η pN2 –≤―΄–Ε–Η–≤–Α–Β–Φ–Ψ―¹―²―¨ –¥–Ψ―¹―²–Ψ–≤–Β―Ä–Ϋ–Ψ ―Ö―É–Ε–Β – –Μ–Η―à―¨ 25,2±4,8% –Η 18,8±4,8%, ―΅―²–Ψ ―²–Α–Κ–Ε–Β ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤―É–Β―² ―Ä–Β–Ζ―É–Μ―¨―²–Α―²–Α–Φ –≤―΄–Ε–Η–≤–Α–Β–Φ–Ψ―¹―²–Η –Ω―Ä–Η ―Ä–Α–Ζ–¥–Β–Μ–Β–Ϋ–Η–Η –Ϋ–Α –Ψ―¹–Ϋ–Ψ–≤–Α–Ϋ–Η–Η –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η JGCA (1998). –ü―Ä–Η –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η–Η pN3 – –Ϋ–Η–Κ―²–Ψ –Η–Ζ –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –Ϋ–Β –Ω–Β―Ä–Β–Ε–Η–≤–Α–Β―² 2 –≥–Ψ–¥–Α –Ϋ–Α–±–Μ―é–¥–Β–Ϋ–Η―è, ―΅―²–Ψ –Ψ―²―Ä–Α–Ε–Α–Β―² –Ω―Ä–Ψ–≥–Ϋ–Ψ–Ζ ―²–Β―΅–Β–Ϋ–Η―è –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è. –†–Α–Ζ–Ϋ–Η―Ü–Α –Φ–Β–Ε–¥―É –≤―¹–Β–Φ–Η –Ω–Ψ–¥–≥―Ä―É–Ω–Ω–Α–Φ–Η ―¹―²–Α―²–Η―¹―²–Η―΅–Β―¹–Κ–Η –¥–Ψ―¹―²–Ψ–≤–Β―Ä–Ϋ–Α (?2=114,6, ―Ä<0,0001).
–£–Μ–Η―è–Ϋ–Η–Β –Μ–Η–Φ―³–Ψ–¥–Η―¹―¹–Β–Κ―Ü–Η–Η –Ϋ–Α ―Ä–Β–Ζ―É–Μ―¨―²–Α―²―΄
―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Μ–Β―΅–Β–Ϋ–Η―è ―Ä–Α–Κ–Α
–Ω―Ä–Ψ–Κ―¹–Η–Φ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ–Α –Ε–Β–Μ―É–¥–Κ–Α
–ü―Ä–Η –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Η ―Ä–Β–Ζ―É–Μ―¨―²–Α―²–Ψ–≤ –Μ–Β―΅–Β–Ϋ–Η―è ―Ä–Α–Κ–Α –Ω―Ä–Ψ–Κ―¹–Η–Φ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ–Α –Ε–Β–Μ―É–¥–Κ–Α –Ϋ–Α –Ψ―¹–Ϋ–Ψ–≤–Α–Ϋ–Η–Η –Ψ–±―ä–Β–Φ–Α –Η ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Α –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Ϋ–Ψ–Ι –Μ–Η–Φ―³–Ψ–¥–Η―¹―¹–Β–Κ―Ü–Η–Η –±―΄–Μ–Η –Ω–Ψ–Μ―É―΅–Β–Ϋ―΄ –¥–Α–Ϋ–Ϋ―΄–Β, –Ω–Ψ–¥―²–≤–Β―Ä–Ε–¥–Α―é―â–Η–Β ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ –Κ–Ψ–Ϋ―Ü–Β–Ω―Ü–Η–Η ―¹―²–Α–Ϋ–¥–Α―Ä―²–Ϋ–Ψ–≥–Ψ –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η―è –¦–î D2 –Ω―Ä–Η ―Ä–Α–Κ–Β –Ε–Β–Μ―É–¥–Κ–Α.
–£ –Ψ–±―â–Β–Ι –≥―Ä―É–Ω–Ω–Β –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η–Β–Φ –¦–î D2 ―¹―Ä–Β–¥–Ϋ―è―è –Ω―Ä–Ψ–¥–Ψ–Μ–Ε–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²―¨ –Ε–Η–Ζ–Ϋ–Η ―¹–Ψ―¹―²–Α–≤–Η–Μ–Α 57,2±4,1 –Φ–Β―¹―è―Ü–Β–≤ –Ω―Ä–Η –Φ–Β–¥–Η–Α–Ϋ–Β –≤―΄–Ε–Η–≤–Α–Β–Φ–Ψ―¹―²–Η 22,0±2,0 –Φ–Β―¹―è―Ü–Β–≤. –ë–Ψ–Μ–Β–Β ―¹–Κ―Ä–Ψ–Φ–Ϋ―΄–Β ―Ä–Β–Ζ―É–Μ―¨―²–Α―²―΄ –±―΄–Μ–Η –Ω–Ψ–Μ―É―΅–Β–Ϋ―΄ –≤ –≥―Ä―É–Ω–Ω–Β ―¹ –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η–Β–Φ ―Ä–Α―¹―à–Η―Ä–Β–Ϋ–Ϋ–Ψ–Ι D3 –Μ–Η–Φ―³–Ψ–¥–Η―¹―¹–Β–Κ―Ü–Η–Η ―¹ ―É–¥–Α–Μ–Β–Ϋ–Η–Β–Φ –Μ–Η–Φ―³–Α―²–Η―΅–Β―¹–Κ–Η―Ö ―É–Ζ–Μ–Ψ–≤ ―²―Ä–Β―²―¨–Β–≥–Ψ ―ç―²–Α–Ω–Α –Φ–Β―²–Α―¹―²–Α–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Η―è – ―¹―Ä–Β–¥–Ϋ―è―è –Ω―Ä–Ψ–¥–Ψ–Μ–Ε–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²―¨ –Ε–Η–Ζ–Ϋ–Η 35,1±7,6 –Φ–Β―¹―è―Ü–Β–≤ (–Φ–Β–¥–Η–Α–Ϋ–Α –≤―΄–Ε–Η–≤–Α–Β–Φ–Ψ―¹―²–Η 16,0±2,8 –Φ–Β―¹―è―Ü–Β–≤). –≠―²–Η –¥–Α–Ϋ–Ϋ―΄–Β ―è–≤–Μ―è―é―²―¹―è –Ζ–Α–Κ–Ψ–Ϋ–Ψ–Φ–Β―Ä–Ϋ―΄–Φ ―¹–Μ–Β–¥―¹―²–≤–Η–Β–Φ –±–Ψ–Μ―¨―à–Β–Ι –Η―¹―Ö–Ψ–¥–Ϋ–Ψ–Ι ―Ä–Α―¹–Ω―Ä–Ψ―¹―²―Ä–Α–Ϋ–Β–Ϋ–Ϋ–Ψ―¹―²–Η –Ω―Ä–Ψ―Ü–Β―¹―¹–Α, ―¹ ―É―΅–Β―²–Ψ–Φ –≤–Ψ–Ζ–Φ–Ψ–Ε–Ϋ–Ψ―¹―²–Η –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η―è –¥–Β―²–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Φ–Ψ―Ä―³–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è ―É–¥–Α–Μ–Β–Ϋ–Ϋ–Ψ–≥–Ψ –Ω―Ä–Β–Ω–Α―Ä–Α―²–Α, –Α –Ζ–Ϋ–Α―΅–Η―², –¥–Ψ―¹―²–Ψ–≤–Β―Ä–Ϋ–Ψ–≥–Ψ ―¹―²–Α–¥–Η―Ä–Ψ–≤–Α–Ϋ–Η―è –Η―¹―²–Η–Ϋ–Ϋ–Ψ–Ι ―Ä–Α―¹–Ω―Ä–Ψ―¹―²―Ä–Α–Ϋ–Β–Ϋ–Ϋ–Ψ―¹―²–Η –Ϋ–Α –Φ–Ψ–Φ–Β–Ϋ―² ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Μ–Β―΅–Β–Ϋ–Η―è.
–ù–Α–Η–±–Ψ–Μ–Β–Β –Ϋ–Η–Ζ–Κ–Η–Β –Ω–Ψ–Κ–Α–Ζ–Α―²–Β–Μ–Η –Ψ―²–¥–Α–Μ–Β–Ϋ–Ϋ―΄―Ö ―Ä–Β–Ζ―É–Μ―¨―²–Α―²–Ψ–≤ –Μ–Β―΅–Β–Ϋ–Η―è –±―΄–Μ–Η –Ω–Ψ–Μ―É―΅–Β–Ϋ―΄ –≤ –≥―Ä―É–Ω–Ω–Β ―¹ –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η–Β–Φ –Ϋ–Β―Ä–Α–¥–Η–Κ–Α–Μ―¨–Ϋ–Ψ–Ι –¦–î D1: ―¹―Ä–Β–¥–Ϋ―è―è –Ω―Ä–Ψ–¥–Ψ–Μ–Ε–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²―¨ –Ε–Η–Ζ–Ϋ–Η ―¹–Ψ―¹―²–Α–≤–Η–Μ–Α 29,6±5,7 –Φ–Β―¹―è―Ü–Β–≤ (–Φ–Β–¥–Η–Α–Ϋ–Α –≤―΄–Ε–Η–≤–Α–Β–Φ–Ψ―¹―²–Η 12,0±2,3 –Φ–Β―¹―è―Ü–Β–≤). –≠―²–Η –Ω–Ψ–Κ–Α–Ζ–Α―²–Β–Μ–Η –Ψ―²―Ä–Α–Ε–Α―é―² –≤ –Ω–Β―Ä–≤―É―é –Ψ―΅–Β―Ä–Β–¥―¨ –Ϋ–Β–Α–¥–Β–Κ–≤–Α―²–Ϋ―΄–Ι –Ψ–±―ä–Β–Φ, –Α ―¹–Μ–Β–¥–Ψ–≤–Α―²–Β–Μ―¨–Ϋ–Ψ, –Η ―Ä–Α–¥–Η–Κ–Α–Μ―¨–Ϋ–Ψ―¹―²―¨ –Μ–Η–Φ―³–Ψ–¥–Η―¹―¹–Β–Κ―Ü–Η–Η –≤ –¥–Α–Ϋ–Ϋ–Ψ–Ι –≥―Ä―É–Ω–Ω–Β, –Ϋ–Β –Ω–Ψ–Ζ–≤–Ψ–Μ―è―é―â–Β–Ι –¥–Ψ―¹―²–Ψ–≤–Β―Ä–Ϋ–Ψ –Ψ–Ω―Ä–Β–¥–Β–Μ–Η―²―¨ ―¹―²–Α–¥–Η―é, ―¹ –≤–Ψ–Ζ–Φ–Ψ–Ε–Ϋ–Ψ―¹―²―¨―é –Β–Β –Φ–Η–≥―Ä–Α―Ü–Η–Η.
–†–Α–Ζ–Ϋ–Η―Ü–Α –Φ–Β–Ε–¥―É –≥―Ä―É–Ω–Ω–Α–Φ–Η ―¹ –¦–î D2 –Η D3 ―¹―²–Α―²–Η―¹―²–Η―΅–Β―¹–Κ–Η –Ϋ–Β–¥–Ψ―¹―²–Ψ–≤–Β―Ä–Ϋ–Α (?2 = 2,7 –Ω―Ä–Η ―Ä=0,099), ―²–Ψ–≥–¥–Α –Κ–Α–Κ ―Ä–Α–Ζ–Ϋ–Η―Ü–Α –Φ–Β–Ε–¥―É –≥―Ä―É–Ω–Ω–Ψ–Ι ―¹ –¦–î D2 –Η D1 ―¹―²–Α―²–Η―¹―²–Η―΅–Β―¹–Κ–Η –¥–Ψ―¹―²–Ψ–≤–Β―Ä–Ϋ–Α (?2=9,9 –Ω―Ä–Η ―Ä=0,02), ―΅―²–Ψ –Ψ―²―Ä–Α–Ε–Α–Β―² –≤―΄―¹–Ψ–Κ―É―é –Ζ–Ϋ–Α―΅–Η–Φ–Ψ―¹―²―¨ ―¹―²–Α–Ϋ–¥–Α―Ä―²–Ϋ–Ψ–≥–Ψ –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η―è –¦–î D2 ―¹ ―É–¥–Α–Μ–Β–Ϋ–Η–Β–Φ ―Ä–Β–≥–Η–Ψ–Ϋ–Α―Ä–Ϋ–Ψ–≥–Ψ –Μ–Η–Φ―³–Α―²–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Α–Ω–Ω–Α―Ä–Α―²–Α –Ε–Β–Μ―É–¥–Κ–Α –Ω―Ä–Η –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η–Η ―Ä–Α–¥–Η–Κ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Μ–Β―΅–Β–Ϋ–Η―è.
–Δ–Α–Κ–Η–Φ –Ψ–±―Ä–Α–Ζ–Ψ–Φ, –¥–Α–Ϋ–Ϋ―΄–Β –Α–Ϋ–Α–Μ–Η–Ζ–Α –Φ–Α―²–Β―Ä–Η–Α–Μ–Α –Ω–Ψ–Ζ–≤–Ψ–Μ―è―é―² –Ψ–±–Ψ―¹–Ϋ–Ψ–≤–Α―²―¨ –Ω―Ä–Β–Η–Φ―É―â–Β―¹―²–≤–Ψ ―¹―²–Α–Ϋ–¥–Α―Ä―²–Ϋ–Ψ–≥–Ψ –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η―è ―Ä–Α–¥–Η–Κ–Α–Μ―¨–Ϋ–Ψ–Ι –¦–î D2 ―É –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –Φ–Β―¹―²–Ϋ–Ψ―Ä–Α―¹–Ω―Ä–Ψ―¹―²―Ä–Α–Ϋ–Β–Ϋ–Ϋ―΄–Φ ―Ä–Α–Κ–Ψ–Φ –Ε–Β–Μ―É–¥–Κ–Α. –î–Α–Ϋ–Ϋ―΄–Ι –Ψ–±―ä–Β–Φ –≤–Φ–Β―à–Α―²–Β–Μ―¨―¹―²–≤–Α, ―¹ ―É―΅–Β―²–Ψ–Φ –Ψ―²―¹―É―²―¹―²–≤–Η―è ―É–≤–Β–Μ–Η―΅–Β–Ϋ–Η―è ―΅–Α―¹―²–Ψ―²―΄ –Ψ―¹–Μ–Ψ–Ε–Ϋ–Β–Ϋ–Η–Ι –Η –Μ–Β―²–Α–Μ―¨–Ϋ–Ψ―¹―²–Η, –¥–Ψ–Μ–Ε–Β–Ϋ ―Ä–Α―¹―¹–Φ–Α―²―Ä–Η–≤–Α―²―¨―¹―è –Κ–Α–Κ ―¹―²–Α–Ϋ–¥–Α―Ä―² ―Ä–Α–¥–Η–Κ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –≤–Φ–Β―à–Α―²–Β–Μ―¨―¹―²–≤–Α –Ω―Ä–Η ―Ä–Α–Κ–Β –Ε–Β–Μ―É–¥–Κ–Α, –Ϋ–Α―΅–Η–Ϋ–Α―è ―¹ –Ϋ–Α―΅–Α–Μ―¨–Ϋ―΄―Ö ―É―Ä–Ψ–≤–Ϋ–Β–Ι –Η–Ϋ–≤–Α–Ζ–Η–Η –Ψ–Ω―É―Ö–Ψ–Μ–Η –Η, –Κ–Ψ–Ϋ–Β―΅–Ϋ–Ψ –Ε–Β, –≤ –≥―Ä―É–Ω–Ω–Α―Ö ―¹ –Φ–Β―¹―²–Ϋ–Ψ―Ä–Α―¹–Ω―Ä–Ψ―¹―²―Ä–Α–Ϋ–Β–Ϋ–Ϋ―΄–Φ ―Ä–Α–Κ–Ψ–Φ –Ε–Β–Μ―É–¥–Κ–Α, –Ω―Ä–Η –≥–Μ―É–±–Η–Ϋ–Β –Η–Ϋ–≤–Α–Ζ–Η–Η –±–Ψ–Μ–Β–Β ―Ä–Δ2–Α.
–≠―²–Η –Ω–Ψ–Κ–Α–Ζ–Α―²–Β–Μ–Η –Ϋ–Α–≥–Μ―è–¥–Ϋ–Ψ –Ω–Ψ–Ζ–≤–Ψ–Μ―è―é―² –Ψ―Ü–Β–Ϋ–Η―²―¨ –Ϋ–Β–Α–¥–Β–Κ–≤–Α―²–Ϋ–Ψ―¹―²―¨ –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η―è –¦–î D1 –Ω―Ä–Η ―Ä–Α–Κ–Β –Ε–Β–Μ―É–¥–Κ–Α –≤–Ϋ–Β –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²–Η –Ψ―² –Μ–Η–Φ―³–Ψ–≥–Β–Ϋ–Ϋ–Ψ–Ι ―Ä–Α―¹–Ω―Ä–Ψ―¹―²―Ä–Α–Ϋ–Β–Ϋ–Ϋ–Ψ―¹―²–Η, ―¹ ―É―΅–Β―²–Ψ–Φ –Κ―Ä–Α–Ι–Ϋ–Β –Ϋ–Η–Ζ–Κ–Ψ–Ι –¥–Ψ―¹―²–Ψ–≤–Β―Ä–Ϋ–Ψ―¹―²–Η –Η–Ϋ―²―Ä–Α–Ψ–Ω–Β―Ä–Α―Ü–Η–Ψ–Ϋ–Ϋ–Ψ–Ι –Ψ―Ü–Β–Ϋ–Κ–Η ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Α –Η ―Ä–Α―¹–Ω―Ä–Ψ―¹―²―Ä–Α–Ϋ–Β–Ϋ–Ϋ–Ψ―¹―²–Η –Μ–Η–Φ―³–Ψ–≥–Β–Ϋ–Ϋ–Ψ–≥–Ψ –Φ–Β―²–Α―¹―²–Α–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Η―è.
–Δ–Α–Κ–Ε–Β –¥–Ψ―¹―²–Α―²–Ψ―΅–Ϋ–Ψ –¥–Η―¹–Κ―É―²–Α–±–Β–Μ―¨–Ϋ–Ψ–Ι –Ψ―¹―²–Α–Β―²―¹―è –Ω―Ä–Ψ–±–Μ–Β–Φ–Α –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η―è ―Ä–Α―¹―à–Η―Ä–Β–Ϋ–Ϋ–Ψ–Ι –¦–î D3 –Ω―Ä–Η ―Ä–Α–Κ–Β –Ω―Ä–Ψ–Κ―¹–Η–Φ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ–Α –Ε–Β–Μ―É–¥–Κ–Α. –Δ–Α–Κ, –Β―¹–Μ–Η ―¹―Ä–Α–≤–Ϋ–Η―²–Β–Μ―¨–Ϋ―΄–Ι –Α–Ϋ–Α–Μ–Η–Ζ ―Ä–Β–Ζ―É–Μ―¨―²–Α―²–Ψ–≤ –≤―΄–Ε–Η–≤–Α–Β–Φ–Ψ―¹―²–Η ―¹ –≥―Ä―É–Ω–Ω–Ψ–Ι –¦–î D1 –¥–Ψ―¹―²–Α―²–Ψ―΅–Ϋ–Ψ –Ψ―΅–Β–≤–Η–¥–Β–Ϋ –≤ –Ω–Ψ–Μ―¨–Ζ―É ―Ä–Α―¹―à–Η―Ä–Β–Ϋ–Ϋ–Ψ–Ι ―Ä–Α–¥–Η–Κ–Α–Μ―¨–Ϋ–Ψ–Ι –¦–î D3, ―²–Ψ –Ω―Ä–Η ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η–Η ―¹–Ψ ―¹―²–Α–Ϋ–¥–Α―Ä―²–Ϋ–Ψ–Ι –¦–î D2 ―Ä–Α–Ζ–Ϋ–Η―Ü–Α –≤―΄–Ε–Η–≤–Α–Β–Φ–Ψ―¹―²–Η, –¥–Α–Ε–Β –Ω―Ä–Η –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η–Η –Μ–Η–Φ―³–Α―²–Η―΅–Β―¹–Κ–Η―Ö –Κ–Ψ–Μ–Μ–Β–Κ―²–Ψ―Ä–Ψ–≤ –≤―²–Ψ―Ä–Ψ–≥–Ψ ―ç―²–Α–Ω–Α –Φ–Β―²–Α―¹―²–Α–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Η―è, –Ϋ–Β ―¹―²–Ψ–Μ―¨ –Ψ―΅–Β–≤–Η–¥–Ϋ–Α. –Δ–Α–Κ–Η–Φ –Ψ–±―Ä–Α–Ζ–Ψ–Φ, –¥–Α–Ϋ–Ϋ―΄–Β –Α–Ϋ–Α–Μ–Η–Ζ–Α –Ϋ–Β –Ω–Ψ–Ζ–≤–Ψ–Μ―è―é―² –≤―΄―¹–Κ–Α–Ζ–Α―²―¨―¹―è –≤ –Ω–Ψ–Μ―¨–Ζ―É –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η―è ―Ä–Α―¹―à–Η―Ä–Β–Ϋ–Ϋ–Ψ–≥–Ψ –Ψ–±―ä–Β–Φ–Α –Μ–Η–Φ―³–Ψ–¥–Η―¹―¹–Β–Κ―Ü–Η–Η –¥–Α–Ε–Β –≤ –≥―Ä―É–Ω–Ω–Β, –≥–¥–Β ―²–Β–Ψ―Ä–Β―²–Η―΅–Β―¹–Κ–Η ―ç―²–Ψ –Φ–Ψ–Ε–Β―² –Ω―Ä–Η–Ϋ–Β―¹―²–Η –Ϋ–Α–Η–±–Ψ–Μ―¨―à–Η–Β –Ω―Ä–Β–Η–Φ―É―â–Β―¹―²–≤–Α. –ö–Ψ–Ϋ–Β―΅–Ϋ–Ψ –Ε–Β, –Ϋ–Β ―¹–Μ–Β–¥―É–Β―² –Ζ–Α–±―΄–≤–Α―²―¨, ―΅―²–Ψ ―¹ ―É―΅–Β―²–Ψ–Φ –≤–Ψ–Ζ–Φ–Ψ–Ε–Ϋ–Ψ―¹―²–Η –Ω–Ψ―¹–Μ–Β–¥―É―é―â–Β–Ι –Φ–Η–≥―Ä–Α―Ü–Η–Η –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –Η–Ζ –≥―Ä―É–Ω–Ω―΄ ―¹ ―ÄN2 –≤ –≥―Ä―É–Ω–Ω―É ―¹ ―ÄN3, –Ω―Ä–Η –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η–Η ―Ä–Α―¹―à–Η―Ä–Β–Ϋ–Ϋ–Ψ–≥–Ψ –Ψ–±―ä–Β–Φ–Α –≤–Φ–Β―à–Α―²–Β–Μ―¨―¹―²–≤–Α, ―Ä–Β–Ζ―É–Μ―¨―²–Α―²―΄ –≤ ―¹–Ψ–±―¹―²–≤–Β–Ϋ–Ϋ–Ψ –≥―Ä―É–Ω–Ω–Β ―ÄN2 –Φ–Ψ–≥―É―² –Φ–Β–Ϋ―è―²―¨―¹―è –≤ ―¹―²–Ψ―Ä–Ψ–Ϋ―É ―É–≤–Β–Μ–Η―΅–Β–Ϋ–Η―è –≤―΄–Ε–Η–≤–Α–Β–Φ–Ψ―¹―²–Η, ―΅―²–Ψ –Ψ―²―Ä–Α–Ζ–Η―²―¹―è –Ϋ–Α ―Ä–Β–Ζ―É–Μ―¨―²–Α―²–Α―Ö –≤ ―Ü–Β–Μ–Ψ–Φ.
–€–Ψ–Ε–Ϋ–Ψ –Ψ―²–Φ–Β―²–Η―²―¨, ―΅―²–Ψ –¥–Μ―è –Ψ–±–Ψ―¹–Ϋ–Ψ–≤–Α–Ϋ–Η―è –≤–Ψ–Ζ–Φ–Ψ–Ε–Ϋ–Ψ–≥–Ψ –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η―è ―Ä–Α―¹―à–Η―Ä–Β–Ϋ–Ϋ–Ψ–Ι –Μ–Η–Φ―³–Ψ–¥–Η―¹―¹–Β–Κ―Ü–Η–Η ―²―Ä–Β–±―É–Β―²―¹―è –Ω―Ä–Ψ–≤–Β–¥–Β–Ϋ–Η–Β –Ω―Ä–Ψ―¹–Ω–Β–Κ―²–Η–≤–Ϋ―΄―Ö ―Ä–Α–Ϋ–¥–Ψ–Φ–Η–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ―΄―Ö –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Ι –≤ ―¹―Ä–Α–≤–Ϋ–Η–Φ―΄―Ö –≥―Ä―É–Ω–Ω–Α―Ö –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ ―Ü–Β–Μ―¨―é –≤―΄―Ä–Α–±–Ψ―²–Κ–Η –Ω–Ψ–Κ–Α–Ζ–Α–Ϋ–Η–Ι –Κ –Β–Β –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η―é. –ù–Α ―¹–Β–≥–Ψ–¥–Ϋ―è―à–Ϋ–Η–Ι –¥–Β–Ϋ―¨ ―¹―²–Α–Ϋ–¥–Α―Ä―²–Ψ–Φ –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η―è ―Ä–Α–¥–Η–Κ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –≤–Φ–Β―à–Α―²–Β–Μ―¨―¹―²–≤–Α ―è–≤–Μ―è–Β―²―¹―è –¦–î D2, –Κ–Ψ―²–Ψ―Ä–Α―è ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Η–Ζ―É–Β―²―¹―è –¥–Ψ―¹―²–Ψ–≤–Β―Ä–Ϋ―΄–Φ ―É–≤–Β–Μ–Η―΅–Β–Ϋ–Η–Β–Φ –≤―΄–Ε–Η–≤–Α–Β–Φ–Ψ―¹―²–Η –Ω–Ψ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η―é ―¹ –Ϋ–Β―Ä–Α–¥–Η–Κ–Α–Μ―¨–Ϋ―΄–Φ –Ψ–±―ä–Β–Φ–Ψ–Φ –¦–î D1.
–€–Ϋ–Ψ–≥–Ψ―³–Α–Κ―²–Ψ―Ä–Ϋ―΄–Ι –Α–Ϋ–Α–Μ–Η–Ζ ―³–Α–Κ―²–Ψ―Ä–Ψ–≤ –Ω―Ä–Ψ–≥–Ϋ–Ψ–Ζ–Α ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Μ–Β―΅–Β–Ϋ–Η―è ―Ä–Α–Κ–Α –Ω―Ä–Ψ–Κ―¹–Η–Φ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ–Α –Ε–Β–Μ―É–¥–Κ–Α
–ù–Α –Ψ―¹–Ϋ–Ψ–≤–Α–Ϋ–Η–Η –Ω―Ä–Ψ–≤–Β–¥–Β–Ϋ–Ϋ–Ψ–≥–Ψ –Α–Ϋ–Α–Μ–Η–Ζ–Α –±―΄–Μ–Η –≤―΄–¥–Β–Μ–Β–Ϋ―΄ «–Ψ–Ω―É―Ö–Ψ–Μ―¨––Ζ–Α–≤–Η―¹–Η–Φ―΄–Β» –Η «–Μ–Β―΅–Β–Ϋ–Η–Β––Ζ–Α–≤–Η―¹–Η–Φ―΄–Β» ―³–Α–Κ―²–Ψ―Ä―΄, –Ω–Ψ–Κ–Α–Ζ–Α–≤―à–Η–Β ―¹―²–Α―²–Η―¹―²–Η―΅–Β―¹–Κ–Η –Ζ–Ϋ–Α―΅–Η–Φ–Ψ–Β –≤–Μ–Η―è–Ϋ–Η–Β –Ϋ–Α –Ψ―²–¥–Α–Μ–Β–Ϋ–Ϋ―΄–Β ―Ä–Β–Ζ―É–Μ―¨―²–Α―²―΄. –î–Μ―è –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –Ψ–Ω―Ä–Β–¥–Β–Μ―è–Μ–Η―¹―¨ –Ζ–Ϋ–Α―΅–Β–Ϋ–Η―è 50 ―³–Α–Κ―²–Ψ―Ä–Ψ–≤, ―Ä–Α–Ζ–¥–Β–Μ–Β–Ϋ–Ϋ―΄―Ö –Ϋ–Α 3 –≥―Ä―É–Ω–Ω―΄.
–Γ―²–Α―²–Η―¹―²–Η―΅–Β―¹–Κ–Η–Ι –Α–Ϋ–Α–Μ–Η–Ζ –Ω―Ä–Ψ–≤–Ψ–¥–Η–Μ―¹―è –Ω–Ψ –Φ–Β―²–Ψ–¥―É –ë–Α–Ι–Β―¹–Α ―¹ –Ψ–Ω―Ä–Β–¥–Β–Μ–Β–Ϋ–Η–Β–Φ ―Ä–Β―à–Α―é―â–Η―Ö –Ω―Ä–Α–≤–Η–Μ. –î–Μ―è –Ω―Ä–Ψ–≤–Β―Ä–Κ–Η –¥–Ψ―¹―²–Ψ–≤–Β―Ä–Ϋ–Ψ―¹―²–Η ―Ä–Α–Ζ–Μ–Η―΅–Η–Ι –Ζ–Ϋ–Α―΅–Β–Ϋ–Η–Ι –Ω―Ä–Η–Ζ–Ϋ–Α–Κ–Ψ–≤ –≤ –≥―Ä―É–Ω–Ω–Α―Ö –Η―¹–Ω–Ψ–Μ―¨–Ζ–Ψ–≤–Α–Μ–Η―¹―¨ ―²–Β―¹―²―΄ ?2 –ü–Η―Ä―¹–Ψ–Ϋ–Α –Η ―²–Ψ―΅–Ϋ―΄–Ι –Κ―Ä–Η―²–Β―Ä–Η–Ι –Λ–Η―à–Β―Ä–Α. –ë―΄–Μ–Ψ –≤―΄–¥–Β–Μ–Β–Ϋ–Ψ 8 ―Ä–Β―à–Α―é―â–Η―Ö –Ω―Ä–Α–≤–Η–Μ, –Η―¹–Ω–Ψ–Μ―¨–Ζ―É―é―â–Η―Ö ―Ä–Α–Ζ–Μ–Η―΅–Ϋ―΄–Β –Ϋ–Α–±–Ψ―Ä―΄ –Ω―Ä–Η–Ζ–Ϋ–Α–Κ–Ψ–≤. –¦―É―΅―à–Η–Φ –Ψ–Κ–Α–Ζ–Α–Μ–Ψ―¹―¨ –Ω―Ä–Α–≤–Η–Μ–Ψ, –Ψ―¹–Ϋ–Ψ–≤–Α–Ϋ–Ϋ–Ψ–Β –Ϋ–Α 13 –Ω―Ä–Η–Ζ–Ϋ–Α–Κ–Α―Ö –Η –Η–Φ–Β―é―â–Β–Β ―²–Ψ―΅–Ϋ–Ψ―¹―²―¨ 78,2% (95%––Ι –¥–Ψ–≤–Β―Ä–Η―²–Β–Μ―¨–Ϋ―΄–Ι –Η–Ϋ―²–Β―Ä–≤–Α–Μ: 64,8% – 83,8%).
–ù–Α –Ψ―¹–Ϋ–Ψ–≤–Α–Ϋ–Η–Η –Ω–Ψ–Μ―É―΅–Β–Ϋ–Ϋ―΄―Ö ―Ä–Β–Ζ―É–Μ―¨―²–Α―²–Ψ–≤ –±―΄–Μ–Ψ –≤―΄–¥–Β–Μ–Β–Ϋ–Ψ 13 ―¹―²–Α―²–Η―¹―²–Η―΅–Β―¹–Κ–Η –Ζ–Ϋ–Α―΅–Η–Φ―΄―Ö ―³–Α–Κ―²–Ψ―Ä–Ψ–≤, –Ψ–Ω―Ä–Β–¥–Β–Μ―è―é―â–Η―Ö –Ω―Ä–Ψ–≥–Ϋ–Ψ–Ζ ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Μ–Β―΅–Β–Ϋ–Η―è ―Ä–Α–Κ–Α –Ω―Ä–Ψ–Κ―¹–Η–Φ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ–Α –Ε–Β–Μ―É–¥–Κ–Α. –ë―΄–Μ–Η ―Ä–Α―¹―¹―΅–Η―²–Α–Ϋ―΄ –Κ–Ψ―ç―³―³–Η―Ü–Η–Β–Ϋ―²―΄ –Η–Ϋ―³–Ψ―Ä–Φ–Α―²–Η–≤–Ϋ–Ψ―¹―²–Η, –Ω–Ψ–Ζ–≤–Ψ–Μ–Η–≤―à–Η–Β –Ψ–Ω―Ä–Β–¥–Β–Μ–Η―²―¨ ―Ä–Α–Ϋ–≥–Ψ–≤–Ψ–Β –Φ–Β―¹―²–Ψ –¥–Μ―è –Κ–Α–Ε–¥–Ψ–≥–Ψ –Η–Ζ –Ζ–Ϋ–Α―΅–Η–Φ―΄―Ö ―³–Α–Κ―²–Ψ―Ä–Ψ–≤. –†–Α–Ϋ–≥–Ψ–≤–Ψ–Β –Φ–Β―¹―²–Ψ –Ψ–Ω―Ä–Β–¥–Β–Μ―è–Β―² –≤–Μ–Η―è–Ϋ–Η–Β –Κ–Α–Ε–¥–Ψ–≥–Ψ –Η–Ζ ―³–Α–Κ―²–Ψ―Ä–Ψ–≤ –Ϋ–Α –Ω―Ä–Ψ–≥–Ϋ–Ψ–Ζ –Ψ―²–¥–Α–Μ–Β–Ϋ–Ϋ―΄―Ö ―Ä–Β–Ζ―É–Μ―¨―²–Α―²–Ψ–≤ ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Μ–Β―΅–Β–Ϋ–Η―è ―Ä–Α–Κ–Α –Ω―Ä–Ψ–Κ―¹–Η–Φ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ–Α –Ε–Β–Μ―É–¥–Κ–Α.
–ù–Α –Ψ―¹–Ϋ–Ψ–≤–Α–Ϋ–Η–Η –Ψ–Ω―Ä–Β–¥–Β–Μ–Β–Ϋ–Η―è –Κ–Ψ―ç―³―³–Η―Ü–Η–Β–Ϋ―²–Ψ–≤ –Κ–Α–Ε–¥–Ψ–≥–Ψ –Η–Ζ –¥–Ψ―¹―²–Ψ–≤–Β―Ä–Ϋ–Ψ –Ζ–Ϋ–Α―΅–Η–Φ―΄―Ö –Ω―Ä–Ψ–≥–Ϋ–Ψ―¹―²–Η―΅–Β―¹–Κ–Η―Ö ―³–Α–Κ―²–Ψ―Ä–Ψ–≤ –±―΄–Μ–Η –≤―΄–¥–Β–Μ–Β–Ϋ―΄ ―³–Α–Κ―²–Ψ―Ä―΄ –±–Μ–Α–≥–Ψ–Ω―Ä–Η―è―²–Ϋ–Ψ–≥–Ψ –Ω―Ä–Ψ–≥–Ϋ–Ψ–Ζ–Α. –ö –¥–Α–Ϋ–Ϋ―΄–Φ ―³–Α–Κ―²–Ψ―Ä–Α–Φ –Ψ―²–Ϋ–Ψ―¹―è―²―¹―è:
- –≤―²–Ψ―Ä–Ψ–Ι ―²–Η–Ω –Α–¥–Β–Ϋ–Ψ–Κ–Α―Ä―Ü–Η–Ϋ–Ψ–Φ―΄ –Ζ–Ψ–Ϋ―΄ –Ω–Η―â–Β–≤–Ψ–¥–Ϋ–Ψ––Ε–Β–Μ―É–¥–Ψ―΅–Ϋ–Ψ–≥–Ψ –Ω–Β―Ä–Β―Ö–Ψ–¥–Α –Ω–Ψ –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η Siewert J.R.;
- 1 –Η 2 ―²–Η–Ω ―Ä–Ψ―¹―²–Α –Ψ–Ω―É―Ö–Ψ–Μ–Η –Ω–Ψ Borrmann R.;
- –≥–Μ―É–±–Η–Ϋ–Α –Ψ–Ω―É―Ö–Ψ–Μ–Β–≤–Ψ–Ι –Η–Ϋ–≤–Α–Ζ–Η–Η –Ϋ–Α ―É―Ä–Ψ–≤–Ϋ–Β ―¹–Μ–Η–Ζ–Η―¹―²–Ψ––Ω–Ψ–¥―¹–Μ–Η–Ζ–Η―¹―²–Ψ–≥–Ψ ―¹–Μ–Ψ―è (pT1);
- ―Ä–Α–¥–Η–Κ–Α–Μ―¨–Ϋ―΄–Ι –Η–Μ–Η ―É―¹–Μ–Ψ–≤–Ϋ–Ψ–―Ä–Α–¥–Η–Κ–Α–Μ―¨–Ϋ―΄–Ι ―Ö–Α―Ä–Α–Κ―²–Β―Ä –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Ϋ–Ψ–≥–Ψ –≤–Φ–Β―à–Α―²–Β–Μ―¨―¹―²–≤–Α (Curability type A, B);
- –Ψ―²―¹―É―²―¹―²–≤–Η–Β ―Ä–Β–Ζ–Η–¥―É–Α–Μ―¨–Ϋ–Ψ–Ι –Ψ–Ω―É―Ö–Ψ–Μ–Η (R0);
- –Η–Ϋ–¥–Β–Κ―¹ –Μ–Η–Φ―³–Ψ–≥–Β–Ϋ–Ϋ–Ψ–≥–Ψ –Φ–Β―²–Α―¹―²–Α–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Η―è N0 –Η–Μ–Η N1;
- –Ψ―²―¹―É―²―¹―²–≤–Η–Β –Μ–Η–Φ―³–Ψ–≥–Β–Ϋ–Ϋ―΄―Ö –Φ–Β―²–Α―¹―²–Α–Ζ–Ψ–≤ –Μ–Η–±–Ψ –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η–Β –Μ–Η–Φ―³–Α―²–Η―΅–Β―¹–Κ–Η―Ö ―É–Ζ–Μ–Ψ–≤ –Ω–Β―Ä–≤–Ψ–≥–Ψ ―ç―²–Α–Ω–Α –Φ–Β―²–Α―¹―²–Α–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Η―è –Ω–Ψ –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η JGCA (1998);
- –Ψ―²―¹―É―²―¹―²–≤–Η–Β –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η―è –Μ–Η–±–Ψ –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η–Β –¥–Ψ 6 –Μ–Η–Φ―³–Α―²–Η―΅–Β―¹–Κ–Η―Ö ―É–Ζ–Μ–Ψ–≤ –Ω–Ψ –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η UICC (2002);
- –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η–Β –Φ–Β–¥–Η–Α―¹―²–Η–Ϋ–Α–Μ―¨–Ϋ―΄―Ö –Μ–Η–Φ―³–Ψ–Κ–Ψ–Μ–Μ–Β–Κ―²–Ψ―Ä–Ψ–≤, –Κ–Α–Κ ―³–Α–Κ―²–Ψ―Ä –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η―è –Ψ―²–¥–Α–Μ–Β–Ϋ–Ϋ―΄―Ö –Μ–Η–Φ―³–Ψ–Κ–Ψ–Μ–Μ–Β–Κ―²–Ψ―Ä–Ψ–≤, ―΅―²–Ψ –±–Ψ–Μ―¨―à–Β ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤―É–Β―² –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η―é –Μ–Η–Φ―³–Α―²–Η―΅–Β―¹–Κ–Η―Ö ―É–Ζ–Μ–Ψ–≤ –≤―²–Ψ―Ä–Ψ–≥–Ψ ―ç―²–Α–Ω–Α –Φ–Β―²–Α―¹―²–Α–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Η―è;
- –Ψ―²―¹―É―²―¹―²–≤–Η–Β –Ω–Β―Ä–Η–Ϋ–Ψ–¥–Α–Μ―¨–Ϋ–Ψ–Ι –Ψ–Ω―É―Ö–Ψ–Μ–Β–≤–Ψ–Ι –Η–Ϋ–≤–Α–Ζ–Η–Η;
- –Ψ―²―¹―É―²―¹―²–≤–Η–Β –Η–Ϋ–≤–Α–Ζ–Η–Η –Μ–Η–Φ―³–Α―²–Η―΅–Β―¹–Κ–Η―Ö ―¹–Ψ―¹―É–¥–Ψ–≤;
- –Ψ―²―¹―É―²―¹―²–≤–Η–Β –Ψ―²–¥–Α–Μ–Β–Ϋ–Ϋ―΄―Ö –Φ–Β―²–Α―¹―²–Α–Ζ–Ψ–≤;
- ―¹―²–Α–¥–Η―è –†–• I–IIIa –Ω–Ψ –Κ–Μ–Α―¹―¹–Η―³–Η–Κ–Α―Ü–Η–Η JGCA (1998).
–£ ―Ü–Β–Μ–Ψ–Φ –Ω–Ψ–Κ–Α–Ζ–Α―²–Β–Μ–Η –¥–Α–Ϋ–Ϋ―΄―Ö –Φ–Ϋ–Ψ–≥–Ψ―³–Α–Κ―²–Ψ―Ä–Ϋ–Ψ–≥–Ψ –Α–Ϋ–Α–Μ–Η–Ζ–Α –Ω–Ψ–Ζ–≤–Ψ–Μ―è―é―² –Ω―Ä–Ψ–≥–Ϋ–Ψ–Ζ–Η―Ä–Ψ–≤–Α―²―¨ –Ψ―²–¥–Α–Μ–Β–Ϋ–Ϋ―΄–Β ―Ä–Β–Ζ―É–Μ―¨―²–Α―²―΄ –Μ–Β―΅–Β–Ϋ–Η―è:
- ―΅―É–≤―¹―²–≤–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²―¨ – 76,0% (65,7–88,5%);
- ―¹–Ω–Β―Ü–Η―³–Η―΅–Ϋ–Ψ―¹―²―¨ – 77,9% (66,8–89,2%);
- –Ψ–±―â–Α―è ―²–Ψ―΅–Ϋ–Ψ―¹―²―¨ – 82,2% (64,6–87,2%).
–ù–Α –Ψ―¹–Ϋ–Ψ–≤–Α–Ϋ–Η–Η –Ω―Ä–Ψ–≤–Β–¥–Β–Ϋ–Ϋ–Ψ–≥–Ψ –Φ–Ϋ–Ψ–≥–Ψ―³–Α–Κ―²–Ψ―Ä–Ϋ–Ψ–≥–Ψ –Α–Ϋ–Α–Μ–Η–Ζ–Α –Η –Ω–Ψ–Μ―É―΅–Β–Ϋ–Ϋ―΄―Ö ―Ä–Α–Ϋ–≥–Ψ–≤―΄―Ö –≤–Β–Μ–Η―΅–Η–Ϋ –¥–Μ―è ―¹―²–Α―²–Η―¹―²–Η―΅–Β―¹–Κ–Η –Ζ–Ϋ–Α―΅–Η–Φ―΄―Ö ―³–Α–Κ―²–Ψ―Ä–Ψ–≤ –Ω―Ä–Ψ–≥–Ϋ–Ψ–Ζ–Α –Φ–Ψ–Ε–Β―² –±―΄―²―¨ –Ω–Ψ―¹―²―Ä–Ψ–Β–Ϋ –Η–Ϋ–¥–Η–≤–Η–¥―É–Α–Μ―¨–Ϋ―΄–Ι –Ω―Ä–Ψ–≥–Ϋ–Ψ–Ζ ―Ä–Β–Ζ―É–Μ―¨―²–Α―²–Ψ–≤ ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Μ–Β―΅–Β–Ϋ–Η―è ―Ä–Α–Κ–Α –Ω―Ä–Ψ–Κ―¹–Η–Φ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ–Α –Ε–Β–Μ―É–¥–Κ–Α, –Ω–Ψ–Ζ–≤–Ψ–Μ―è―é―â–Η–Ι –≤―΄–¥–Β–Μ–Η―²―¨ –≥―Ä―É–Ω–Ω―É ―Ä–Η―¹–Κ–Α –¥–Α–Μ―¨–Ϋ–Β–Ι―à–Β–≥–Ψ –Ω―Ä–Ψ–≥―Ä–Β―¹―¹–Η―Ä–Ψ–≤–Α–Ϋ–Η―è –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è. –£ ―ç―²–Ψ–Ι –≥―Ä―É–Ω–Ω–Β ―¹ ―É―΅–Β―²–Ψ–Φ –Ψ–Ω―΄―²–Α –Κ–Ψ–Φ–±–Η–Ϋ–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ–Ψ–≥–Ψ –Μ–Β―΅–Β–Ϋ–Η―è –Φ–Ψ–Ε–Β―² –Ω―Ä–Ψ–≤–Ψ–¥–Η―²―¨―¹―è –¥–Α–Μ―¨–Ϋ–Β–Ι―à–Α―è ―¹–Ω–Β―Ü–Η―³–Η―΅–Β―¹–Κ–Α―è ―²–Β―Ä–Α–Ω–Η―è, –Ϋ–Α–Ω―Ä–Α–≤–Μ–Β–Ϋ–Ϋ–Α―è –Ϋ–Α ―É–Μ―É―΅―à–Β–Ϋ–Η–Β ―Ä–Β–Ζ―É–Μ―¨―²–Α―²–Ψ–≤ –Μ–Β―΅–Β–Ϋ–Η―è. –≠―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ ―²–Α–Κ–Ψ–≥–Ψ –Μ–Β―΅–Β–Ϋ–Η―è –±―É–¥–Β―² –Ψ–Ω―Ä–Β–¥–Β–Μ―è―²―¨―¹―è ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Ψ–Φ –Ω―Ä–Η–Φ–Β–Ϋ―è–Β–Φ―΄―Ö –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤, –Α ―²–Α–Κ–Ε–Β –Φ–Β―²–Ψ–¥–Η–Κ –Β–≥–Ψ –Ω―Ä–Ψ–≤–Β–¥–Β–Ϋ–Η―è.
–¦–Η―²–Β―Ä–Α―²―É―Ä–Α
1. Stein HJ, Siewert JR. Barrett’s esophagus: pathogenesis, epidemiology, functional abnormalities, malignant degeneration and surgical management. Dysphagia 1993;8:276–288.
2. Devesa SS, Blot WJ, Fraumeni JF Jr. “Changing patterns in the incidence of esophageal and gastric carcinoma in the United States.” Cancer. 1998 Nov 15; 83(10):2049–53.
3. Blot W.J., Devesa S.S., Kneller R.W., Fraumeni J.F. “Rising incidence of Adenocarcinoma of the esophagus and gastric cardia.” JAMA 1991; 265: 1287–1289.
4. Vizcaino A.P., Moreno V., Lambert R. Et al. “Time trends incidence of both major histologoc types of esophageal carcinomas in selected countries, 1975–1995.” Int J Cancer 99: 860–868, 2002.
5. Souza Rh.F., Spechler St.J. “Concepts in the prevention of Adenocarcinoma of the distal Esophagus and Proximal Stomach.” CA Cancer J Clin 2005; 55: 334–351.
6. Nomura A, Stemmermann GN, Chyou PH, Kato I, Perez GIP, Blazer MJ. Helicobacter pylori infection and gastric carcinoma among Japanese American in Hawaii. N Engl J Med 1991;325:1132–6.
7. Blot W.J., Devesa S.S., Kneller R.W., Fraumeni J.F. “Rising incidence of Adenocarcinoma of the esophagus and gastric cardia.” JAMA 1991; 265: 1287–1289.
8. Pera M., Cameron A.J., Trastek V.F., Carpenter H.A., Zinsmeister A.R. “Increasing incidence of adenocarcinoma of the esophagus and esophagogastric junction.” Gastroenterology 1993; 104: 510–513.
9. Blot WJ, McLaughlin JK “The changing epidemiology of EG–J cancer” Semin Oncol 26: 2–8; 1999.
10. Ekstrom AM, Signorello LB, Hansson LE, Bergstrom A, Lindgren A, Nyren O. Evaluating gastric cancer misclassification: a potential explanation for the rise in cardia cancer incidence. J Natl Cancer Inst 1999;91:786–90.
11. Engel L.S., Vaughan Th.L., Gammon M.D., Chow W.–H., Risch H.A. et al. “Occupation and risk of Esophageal and Gastric Cardia Adenocarcinoma.” Americal Journal of Industrial Medicine 42: 11–22, 2002.
12. Hundahl S.A., Wanebo H.J. «Changing gastric cancer treatment in the United States and the pursuit of quality.” European Journal of Surgical Oncology Vol 31, #6: 605–615, 2005.
13. Siewert JR, Holscher AH, Becker K, et al.: «Kardiakarzinom: Versuch einer therapeutisch relevanten Klassifikation.» Chirurg 1996;58:25–34.
14. JR Siewert, HJ Stein. Classification of the adenocarcinoma of the oesophagogastric junction. British Journal Surgery 1998, 85, 1457–1459.
15. Korst RJ, Rusch VW, Venkatraman E. et al. ”Proposed revision of the staging clasification for esophageal and gastric cancer.” J Thoracic Cardiovascular Surg 1998; 115: 660–669.
16. JR Siewert, M Feith, M Werner and HJ Stein. Adenocarcinoma of the esophagogastric junction. Annals of Surgery, vol 232, n°3 , 353–361; 2000.
17. SM Dresner, PJ Lamb, MK Bennett, N Hayes,SM Griffin. The pattern of metastatic lymph node dissemination from adenocarcioma of the esophagogastric junction. Surgery 2001; 129: 103–9.
18. Fukagawa T., Sasako M., Nunobe S., Saka M., Katai H., Sano T. “Isolated tumour cells in lymph nodes in proximal gastric cancer.” The proceedings of the 6th International Gastric Cancer Congress, Tokyo, Japan, 2005: Workshop 3 (Micrometastasis), p. 63.
19. Lymph node micrometastasis and lymphatic Mapping Determined by reverse Transcriptase–polymerase chain reaction in N0 gastric carcinoma.” The proceedings of the 6th International Gastric Cancer Congress, Tokyo, Japan, 2005: Workshop 3 (Micrometastasis), p. 64.
20. J Mueller, H Stein, T Oyang, S Natsugoe, M Feith, M Werner, JR Siewert. Frequency and clinical impact of lymph node micrometastasis and tumor cell microinvolvement in patients with adenocarcinoma of the esophagogastric junction. Cancer 2000; 89: 1874–82.
21. –Δ–Β―Ä––û–≤–Α–Ϋ–Β―¹–Ψ–≤ –€.–î. «–Λ–Α–Κ―²–Ψ―Ä―΄ –Ω―Ä–Ψ–≥–Ϋ–Ψ–Ζ–Α ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Μ–Β―΅–Β–Ϋ–Η―è ―Ä–Α–Κ–Α –Ω―Ä–Ψ–Κ―¹–Η–Φ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ–Α –Ε–Β–Μ―É–¥–Κ–Α» –î–Η―¹―¹ –Ϋ–Α ―¹–Ψ–Η―¹–Κ. …–¥–―Ä–Α –Φ–Β–¥.–Ϋ–Α―É–Κ, –€–Ψ―¹–Κ–≤–Α, 2007.
22. Shen K.R., Cassiva St.D., Deschamps C., Allen M.S., Nichols Fr.S., Harmsen W.S., Pairolero P.C. “Surgical treatment of tumours of the proximal stomach with involvement of the distal esophagus: A 26–years experience with Siewert type III tumours.” The Journal of Thoracic and Cardiovascular Surgery 2006; 132: 755–762.
23. Dresner SM, Wayman J., Bennett MK, Hayes N, Griffin SM “Pattern of lymph node dissemination from adenocarcinoma of the esophagogastric junction.” British Journal of Surgery 1999, 86: 417 – 419.
24. Peracchia A., Bonavina L., Incarbone R., Floridi A. “Results of surgical therapy in patients with adenocarcinoma of the esophagus and cardia.” Gastric cancer 1999; 2: 89–94.
25. Siewert J.R., Feith M., Werner M., Stein H.J. “Adenocarcinoma of the esophagogastric junction. Results of surgical therapy based on anatomical /topographic classification in 1002 consecutive patients.” Annals of Surgery 2000; 232: 353–361.
26. Kurita A., Nozaki I., Kubo Y., Tanada M., Takashima Sh. “Strategy of the treatment of the carcinoma of the gastric cardia.” The proceedings of the 6th International Gastric Cancer Congress, Tokyo, Japan, 2005: Oral Presentation (Surgery of EG–Junction Cancer, P 14–6), p. 147.
27. Stein H.J. “Epidemiology, classification, pathology and surveillance for adenocarcinoma of the esophagogastric junction: results of Consensus Conference of the International Society for Diseases of the Esophagus and International Gastric Cancer Association.” Dis Esophagus 2000 (suppl).
28. –Δ–Β―Ä––û–≤–Α–Ϋ–Β―¹–Ψ–≤ –€.–î. «–†–Α―¹―à–Η―Ä–Β–Ϋ–Ϋ–Α―è –¥–≤―É―Ö– –Η ―²―Ä–Β―Ö––Ζ–Ψ–Ϋ–Α–Μ―¨–Ϋ–Α―è –Μ–Η–Φ―³–Ψ–¥–Η―¹―¹–Β–Κ―Ü–Η―è –≤ ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Ψ–Φ –Μ–Β―΅–Β–Ϋ–Η–Η ―Ä–Α–Κ–Α –≥―Ä―É–¥–Ϋ–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ–Α –Ω–Η―â–Β–≤–Ψ–¥–Α» –î–Η―¹―¹. –Ϋ–Α ―¹–Ψ–Η―¹–Κ… –Κ–Α–Ϋ–¥–Η–¥–Α―²–Α –Φ–Β–¥. –ù–Α―É–Κ, –€–Ψ―¹–Κ–≤–Α. 1998.
29. –Δ–Β―Ä––û–≤–Α–Ϋ–Β―¹–Ψ–≤ –€.–î., –î–Α–≤―΄–¥–Ψ–≤ –€.–‰., –¦–Β―¹–Ϋ–Η–¥–Ζ–Β –≠.–≠. ««–‰–Ϋ–¥–Β–Κ―¹ –¦–Η–Φ―³–Ψ–≥–Β–Ϋ–Ϋ–Ψ–≥–Ψ –€–Β―²–Α―¹―²–Α–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Η―è» (–‰–¦–€) –Κ–Α–Κ –Ω―Ä–Ψ–≥–Ϋ–Ψ―¹―²–Η―΅–Β―¹–Κ–Η–Ι ―³–Α–Κ―²–Ψ―Ä ―Ö–Η―Ä―É―Ä–≥–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Μ–Β―΅–Β–Ϋ–Η―è ―Ä–Α–Κ–Α –Ε–Β–Μ―É–¥–Κ–Α, ―¹–Ω–Ψ―¹–Ψ–±–Ϋ―΄–Ι –Ϋ–Η–≤–Β–Μ–Η―Ä–Ψ–≤–Α―²―¨ ―³–Β–Ϋ–Ψ–Φ–Β–Ϋ –Φ–Η–≥―Ä–Α―Ü–Η–Η ―¹―²–Α–¥–Η–Η.» 5 –Γ―ä–Β–Ζ–¥ –Ψ–Ϋ–Κ–Ψ–Μ–Ψ–≥–Ψ–≤ ―¹―²―Ä–Α–Ϋ –Γ–ù–™, –Δ–Α―à–Κ–Β–Ϋ―², –€–Α–Ι 2008, ―¹. 323.












