

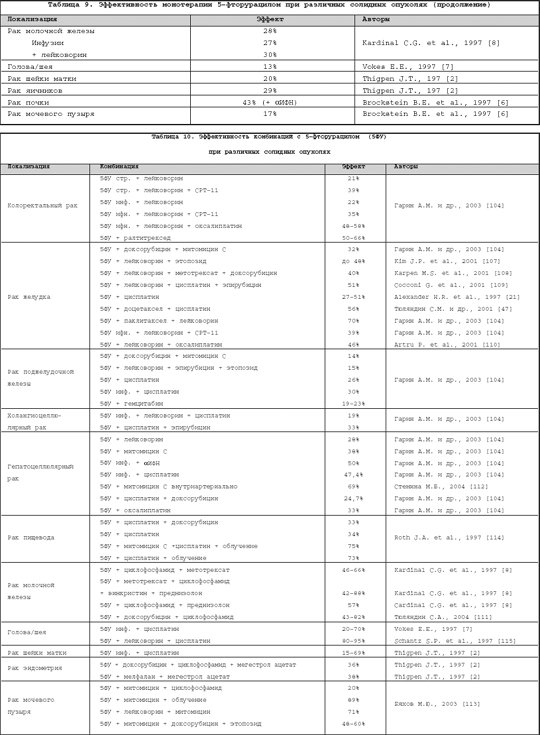
Литература
1. Gutheil J., Kearns Christina. Antimetabolites. In: The chemotherapy source
book. Ed. M.C. Perry, 1997, 317–343.
2. Thigpen J.T. Chemotherapy of Gynecologic Cancer. In: The chemotherapy source book. Ed. M.C. Perry, 1997, 1253–1288.
3. Muss H., Blessing J., Hatch K., et al. Methotrexate in advanced endometrial carcinoma: a phase II trial of the Gynecologic Oncology Group. Am. J. Clin. Oncol., 1990; 13:61–63.
4. Thigpen J.T. Single agent chemotherapy in the management of ovarian carcinoma. In: Alberts D.S., Surwit E.A. eds. Ovarian carcinoma. Boston, 1985; 115–146.
5. Cavins J., Geisler H. Treatment of advanced unresectable cervical carcinoma alredy subjected to complete irradiation therapy. Gynecol. Oncol., 1978; 6:256–260.
6. Brockstein B.E., Vogelzang N.J. Chemotherapy of Genitourinary Cancers. In: The chemotherapy source book. Ed. M.C. Perry, 1997, 1215–1251.7. Vokes E.E. Head and neck cancer. In: The chemotherapy source book. Ed. M.C. Perry, 1997, 1083–1101.
8. Kardinal C.G., Cole J.T. Chemotherapy of breast cancer. In: The chemotherapy source book. Ed. M.C. Perry, 1997, 1125–1183.
9. Rathopoulos H., Antman K.H. Chemotherapy of sarcomas of bone and soft tissue. In: The chemotherapy source book. Ed. M.C. Perry, 1997, 1289–1315.
10. Ihde D.C., Pass H.I., Glatstein E. Small cell lung cancer. In: Cancer
Principles and Practice of Oncology. Ed. V.T. DeVita, 1997, 911–949.
11. Curry S.L., Blessing J.A., Di Saia P.J., et al. A prospective randomized comparison of methotrexate, dactinomycin and chlorambucil versus methotrexate, dactonomycin, cyclophosphamide, doxorubicin, melphalan, hydroxyurea and vincristine in poor prognosis metastatic gestaational trophoblastic disease: a Gynecologic Oncology Group study. Obstet. Gynecol., 1989; 73: 357–362.
12. Горбунова В.А. Лекарственное лечение рака яичников: стандарты и перспективы. Совр. онкол., 2000, т. 2, №4, 108–112.
13. Ермакова Н.А. Роль химиотерапии на различных этапах лечения рака шейки матки. Практическая онкология, 2002, т. 3, №3, 211–219.
14. Ilson D., Bains M., Karpeh M., et al. Phase I trial of weekly cisplatin, irinotecan and radiation in esophagial cancer: A well tolerated regimen. Ann. Oncol., 2002, v.
13 (suppl. 5), 188, N696PD.
15. Бычков М.Б., Орел Н.Ф., Денчик С.А. и др. Химиолучевое лечение при распростра- ненном мелкоклеточном раке легкого. Сов. Мед., 1989, 89–91.
16. Hansen H.H., Dombernowsky P., Hansen M., et al. Chemotherapy of advanced small cell anaplastic carcinoma. Ann. Intern. Med., 1978; 89: 177.
17. Kelsen D., Atiq O.T., Saltz L., et al. FAMTX versus etoposide, doxorubicin and cisplatin: a random assignment trial in gastric cancer. J. Clin. Oncol., 1992; 10 (4):541–548.
18. Bunn P.A. The expanding role of cisplatin in the treatment of non–small cell
lung cancer. Semin. Oncol., 1989; 16:10–21.
19. Thigpen T., Shingleton H., Homesley H., et al. Cis–platinum in treatment of
advanced or recurrent squamous cell carcinoma of the cervix. Cancer, 1981;
48:899–903.
20. Roth J.A., Putman J.B., Rich T.A., et al. Cancer of the esophagus. In: Cancer principles and practice of oncology. Ed. V.T. DeVita, 1997; v. 1, 980–1021.
21. Alexander H.R., Kelsen D.G., Tepper J.C. Cancer of the stomach. In: Cancer principles and practice of oncology. Ed. V.T. DeVita, 1997; v. 1, 1021–1054.
22. Brennan M.F., Casper E.S., Harrison L.B. Soft tissue sarcoma. In: Cancer principles and practice of oncology. Ed. V.T. DeVita, 1997; v. 2, 1738–1788.
23. Antman K.H., Pass J.I., Schiff P.B. Benign and malignant mesothelioma. In: Cancer principles and practice of oncology. Ed. V.T. DeVita, 1997; v. 2, 1853–1878.
24. Balch C.M., Reitgen D.S., Kirwood J.M., et al. Cutaneous melanoma. In: Cancer principles and practice of oncology. Ed. V.T. DeVita, 1997; v. 2, 1947–1994.
25. Omura G.A., Bundy B.A., Berek J.S., et al. Randomized trial; of cyclophosphamide plus cisplatin with or without doxorubicin in ovarian carcinoma: a Gynecologic Oncology Group study. J. Clin. Oncol., 1989; 7: 457–465.
26. Горбунова В.А. Современные возможности лекарственной терапии рака яичников. В сб. «Современные экспериментальные и клинические подходы к диагностике и рациональному лечению рака яичников» под ред. В.А. Горбуновой, Москва, 2001, 92–115.
27. Ginsberg R.J., Vokes E.E., Raben A.A. Non–small cell lung cancer. In: Cancer principles and practice of oncology. Ed. V.T. DeVita, 1997; v. 1, 858–911.
28. Маренич А.Ф. Паклитаксел в лечении немелкоклеточного рака легкого. В сб. «Паклитаксел в клинической практике» под ред. Н.И. Переводчиковой, Москва, 2001, 107–154.
29. Горбунова В.А., Маренич А.Ф. Современные противоопухолевые препараты в лечении немелкоклеточного рака легкого. В сб. « Новое в терапии рака легкого» под ред. Н.И. Переводчиковой, Москва, 2003, 81–117.
30. Переводчикова Н.И., Бычков М.Б. Современная терапевтическая тактика при мелкоклеточном раке легкого. В сб. «Новое в терапии рака легкого», Москва, 2003, 54–68.
31. Бычков М.Б. Таксаны при мелкоклеточном раке легкого. В сб. «Паклитаксел в клинической практике» под ред. Н.И. Переводчиковой, Москва, 2001, 155–167.
32. Bezwoda W.R., Nissenbaum M., Derman D.P. Treatment of metastatic and recurrent cervix cancer with chemotherapy – a randomized trial comparing hydroxyurea with cis–diamminedichloroplatinum plus methotrexate. Med. Pediat. Oncol., 1986; 14: 17–19.
33. Chauvergue J., Heron J., Mayer F., et al. Chemotherapy of cancers of the uterine cervix with a combination of bleomycin, mitomycin, cisplatin and etoposide. Bull. Cancer, 1993; 80:70–79.
34. Brenner D. Combination chemotherapy of advanced cervix cancer. In: Cervix cancer. Ed. Surwit E., Akberts D., Boston, 1987; 137–160.
35. Thigpen T., Blessing J., Homesley H., et al. Phase III trial of doxorubicin
+/– cisplatin in advanced or recurrent endometrial carcinoma. Proc. ASCO, 1993; 12:261.
36. Moore T.D., Phillips P.H., Nerenstone R., et al. Systemic treatment of advanced and recurrent endometrial carcinoma: current status and future directions. J. Clin. Oncol., 1991; 9: 1071–1088.
37. Ogothefis C.J., Dexens F.H., Finn L., et al. A prospective randomized trial
comparing MVAC and CISCA chemotherapy for patients with metastatic urothelial tumors. J. Clin. Oncol., 1990; 8: 1050–1055.
38. Болотина Л.В., Русаков И.Г. Гемцитабин в лечении рака мочевого пузыря. В сб. «Гемцитабин в клинической практике» под ред. М.Б. Бычкова, АРТИНФО Паблишинг, 2002, 149–170.
39. Гарин А.М. Потенциал расширения противоопухолевой активности паклитаксела. В сб. «Паклитаксел в клинической практике» под ред. Н.И. Переводчиковой, Москва, 2001, 202–231.
40. Горбунова В.А., Орел Н.Ф., Бесова Н.С. Современные достижения в клинической химиотерапии злокачественных опухолей. Российский биотерапевтический журнал, 2003, т. 1, №2, 15–27.
41. Подвязников С.О., Бяхов М.Ю. Паклитаксел в химиотерапии плоскоклеточного рака головы и шеи. В сб. «Паклитаксел в клинической практике» под ред. Н.И. Переводчиковой, Москва, 2001, 185–201.
42. Sledge G.W., Roth B.J. Cisplatin in the management of breast cancer. Semin. Oncol., 1989: 14 (suppl. 6): 110–115.
43. Cox E.B., Burton C.V., Olsen G.A., et al. Cisplatin and etoposide: an effective treatment for refractory brerast carcinoma. Ann. J. Clin. Oncol., 1989; 12 (1): 53–56.
44. Hurley J., Doliny P., Gomez C., et al. High complete pathologic response rate of locally advanced breast cancer to neoadjuvant docetaxel and cisplatin
chemotherapy. Proc. ASCO, 2000; 19:127a, N494.
45. Переводчикова Н.И., Тюляндин С.А. Паклитаксел в терапии больных метастатическим (диссеминированным) раком молочной железы. В сб. «Паклитаксел в клинической практике» под ред. Н.И. Переводчиковой, Москва, 2001, 55–78.
46. Viret F., Ychou M., Lepille D., et al. Gemcitabine in combination with cisplatin (GP) versus gemcitabine alone in the treatment of locally advanced or metastatic pancreatic cancer: Final results of a multicenter randomized phase II study. Proc. ASCO, 2004, v. 23, p. 341, N4118.
47. Тюляндин С.А. Химиотерапия рака желудка. Практическая онкология, 2001, №3, 44–52.
48. Blossom G.B., Steiger Z., Stophenson L.W. Neoplasms of the mediastinum. In: Cancer principles and practice of oncology. Ed. V.T. DeVita, 1997; v. 1, 951–969.
49. Носов Д.А. Лекарственное лечение диссеминированной меланомы. Практическая онкология, 2001, №4, 50–57.
50. Pedersen A.G., Hansen H.H. Etoposide (VP–16) in the treatment of the lung cancer. Cancer Treat. Res., 1983; 10: 245–264.
51. Jahanzeb M., Ihde D.C. Chemotherapy of lung cancer. In: The chemotherapy source book. Ed. M.C. Perry, 1997, 1103–1123.
52. Rose P., Blessing J., Mayer A., et al. Prolonged oral etoposide as second line therapy for platinum resistant and platinum sensitive ovarian carcinoma: a
Gynecologic Oncology Group study. Proc. ASCO, 1996; 15:282.
53. Vogelzang N.J., Kennedy B.J. «Salvage» chemotherapy for refractory germ cell tumors. Proc. ASCO, 1981; 22:471.
54. Ajani J.A., Ota D.M., Jackson D.E. Current strategies in management of locoregional and metaatatic gastric carcinoma. Cancer, 1991; 67: 260–265.
55. Laubenstein L.J., Krigel R.L., Odajnyk C.M., et al. Treatment of epidemic
Kaposi’s sarcoma with etoposide or a combination of doxorubicin, bleomycin and vinblastine. J. Clin. Oncol., 1984; 2: 1115.
56. Базин И.С., Гарин А.М. Рак желудка: значение проблемы и современные возможности лечения. Русск.мед.журнал, 2002, т. 10, №14, 588–593.
57. Ihde D.C., Mulshine J.L., Kramer B.S., et al. Prostective randomized comparison of high–dose and standard–dose etoposide and cisplatin chemotherapy in patients with extensive stage small cell lung cancer. J. Clin. Oncol., 1994; 12:2022.
58. Bosl G.L., Geller N.L., Bajorin D., et al. A randomized trial of etoposide and cisplatin versus vinblastine + bleomycin + cisplatin + cyclophosphamide + dactinomycin in patients with good–prognosis germ cell tumors. J. Clin. Oncol., 1988; 6:1231–1238.
59. Bajorin D.F., Sarosdy M.F., Pfister D.G., et al. Randomized trial of etoposide and cisplatin versus etoposide and carboplatin in patients with good–risk germ cell tumors: a multi institutional study. J. Clin. Oncol., 1993; 11:598–606.
60. Muggia F.M., Eifel P.J., Burke T.W. Gestational trophoblastic disease. In:
Cancer principles and practice of oncology. Ed. V.T. DeVita, 1997; v. 1, 1499–1502.
61. Oesterling J., Fuks Zvi, Lee C.T., et al. Cancer of the prostate. In: Cancer
principles and practice of oncology. Ed. V.T. DeVita, 1997; v. 1, 1322–1386.
62. Norton J.A. Adrenal tumors. In: Cancer principles and practice of oncology.
Ed. V.T. DeVita, 1997; v. 2, 1659–1677.
63. Moertel C.G., Kvols L.K., O’Connell M.J., et al. Treatment of neuroendocrine carcinomas with combined etoposide and cisplatin. Cancer, 1991; 68:227.
64. Doz F., Neuenschwander S., Plantaz D., et al. Etoposide and carboplatin in extaocular retinoblastoma: a study by the Societe Francaise d’Oncologie
Pediatrique. J. Clin. Oncol., 1995; 13:902.
65. Nabholtz J.M., Gelmon K., Bontenbal M., et al. Multicenter randomized comparative study of two doses of paclitaxel in patients with metastatic breast cancer. J. Clin. Oncol., 1996, 14: 1558–1567.
66. Thigpen T., Vance R., Khausur T. The platinum compounds and paclitaxel in the management of carcinoma of the endometrium and uterine cervix. Semin. Oncol., 1995; 22: 67–75.
67. Маренич А.Ф. Паклитаксел в лечении немелкоклеточного рака легкого. В сб. «Паклитаксел в клинической практике» под ред. Н.И. Переводчиковой, Москва, 2001,107–154.
68. Kudelka A.P., Winn R., Edwaeds C.L., et al. Advanced squamous cell cancer of the cervix: an update of a multicenter phase II study of paclitaxel 250 mg/m2 administered intravenously over three hours every 21 days with G–CSF support. Proc. ASCO, 1997, N1327.
69. Ball H.G., Blessing J.A., Lentz S.S., et al. A phase II trial of taxol in
advanced and recurrent adenocarcinoma of the endometrium: A Gynecologic Oncology Group study. Gyn. Oncol., 1996; 62:278–281.
70. Legha S.S., Ring S., Papadopoulos M., et al. A phase II trial of taxol in
metastatic melanoma. Cancer, 1990; 65:2478–2481.
71. Hutter H., Motzer R., Schwarz L., et al. Phase II trial of taxol in cisplatin
resistant germ cell tumor patients. Proc. ASCO, 1994, N712.
72. Sparano J.A., Neuberg D., Glick J.H., et al. Phase II trial of biweekly paclitaxel and cisplatin in advanced breast carcinoma: an Eastern Cooperative Oncology Group study. J. Clin. Oncol., 1997; 15: 1880–1884.
73. Gelmon K.A., O’Keilly S.E., Talcher A.W., et al. Phase I/II trial of biweekly
paclitaxel and cisplatin in the metastatic breast cancer. J. Clin. Oncol., 1996;












