Введение
Боль в горле — одна из наиболее частых жалоб пациентов при обращении к врачу первичного звена. Причины формирования данного симптома достаточно разнообразны, наиболее часто болевые ощущения в глотке являются проявлением острого тонзиллофарингита. Острый тонзиллофарингит — собирательный термин, которым обозначается любое острое воспаление слизистой оболочки и лимфоидных образований ротоглотки, развивающееся сочетанно или, гораздо реже, в форме изолированного локального поражения вышеуказанных структур. В большинстве клинических случаев наблюдается инфекционный генез воспалительного процесса. Наиболее часто возбудителями острого тонзиллофарингита являются респираторные вирусы — аденовирус, риновирус, коронавирус, вирусы гриппа, простого герпеса, парагриппа, респираторно-синцитиальный вирус, энтеровирусы (Коксаки В), вирус Эпштейна – Барри др. [1, 2]. Бактериальная этиология отмечается у 5–15% взрослых пациентов и примерно у 40% детей с острыми заболеваниями глотки. Самый распространенный и клинически значимый бактериальный возбудитель острого тонзиллофарингита — β-гемолитические стрептококки группы А (БГСА), а именно наиболее частый представитель этой группы Streptococcus pyogenes. Также в качестве этиотропного фактора данной патологии могут выступать стрептококки групп C и G, Streptococcus pneumoniae, Haemophilus influenzae, Arcanobacterium haemolyticum, Mycoplasma pneumoniae, Chlamydia pneumoniae, Leptotrix buccalis, Neisseria gonorrhoeae, Corynebacterium diphtheriae, Corynebacterium ulcerans, симбиоз спирохеты и фузобактерий (язвенно-некротическая ангина Симановского — Плаута — Венсана) и некоторые иные бактериальные агенты [3, 4]. Кроме того, причиной острых воспалительных изменений в глотке могут быть грибы, к примеру Candida albicans. Не стоит забывать, что ряд микроорганизмов входят в состав нормальной микрофлоры ротоглотки и способны вызвать заболевание только при определенных условиях, например при иммунодефиците.
Тактика лечения острого тонзиллофарингита
Для врача крайне важно знать различия в клинической картине острого тонзиллофарингита, вызванного разными типами микроорганизмов — бактериями, вирусами или грибами, т. к. это будет определять дальнейшую тактику лечения. При остром воспалении в глотке на первое место выступает жалоба на боль в горле, чаще при глотании, с возможностью иррадиации в рядом расположенные структуры. Важным дифференциально-диагностическим признаком является причина усиления боли: на фоне бактериальной инфекции усиление боли отмечается при проглатывании пищи, на фоне вирусной инфекции при «пустом» глотке отмечаются ощущение инородного тела в горле, сухость. Для больных стрептококковым тонзиллофарингитом характерны проявления общей интоксикации, такие как фебрильная температура тела, слабость, лихорадка, головная боль. Общие жалобы у пациентов с вирусными процессами в глотке могут быть выражены незначительно или отсутствовать. Очень важно оценить характерную фарингоскопическую картину: гиперемия и отек небных миндалин, небных дужек, задней стенки глотки, белые налеты или гнойные фолликулы на небных миндалинах, регионарный лимфаденит, у детей иногда наблюдается петехиальная энантема. Все эти проявления носят симметричный характер. При вирусной инфекции кроме изменений в глотке, как правило, имеют место и другие респираторные симптомы: затруднение носового дыхания, отделяемое из носа, конъюнктивит, стоматит, кашель, осиплость, диарея. При грибковой природе острого тонзиллофарингита на первое место выступают симптомы общей интоксикации. Боль в горле выражена не так сильно, а налеты часто выходят за пределы небных миндалин и локализуются также на мягком небе и язычке, имеют творожистый характер. Грибковый тонзиллофарингит, как упоминалось ранее, чаще всего встречается у лиц с иммунодефицитом (онкологические заболевания, СПИД и др.), у детей, а также после длительного приема определенных групп лекарственных препаратов (ингаляционные глюкокортикоиды, системные антибиотики).Основной задачей при назначении лечения пациентам с заболеваниями глотки является решение вопроса о необходимости системной антибактериальной терапии, которая абсолютно показана только при БГСА-процессах. Для выявления заболевания в глотке стрептококковой этиологии используются клинические шкалы Centor (в детском возрасте) и McIsaaс, данные микробиологического исследования и экспресс-тестов. Микробиологическая диагностика является высокочувствительным методом, однако при этом имеет место достаточно длительное ожидание результатов. При подозрении на БГСА-этиологию заболевания важное значение имеет экспресс-тест на поверхностный антиген возбудителя, который можно провести в условиях первичного обращения и получить результат в течение нескольких минут. Забор материала проводится из устьев крипт небных миндалин и задней стенки глотки, избегая контакта с зубами и языком, до начала антибиотикотерапии. При подтверждении бактериальной природы острого тонзиллофарингита назначается системная антибактериальная терапия. Препаратами первой линии являются феноксиметилпенициллин и амоксициллин. В качестве альтернативных лекарственных средств выступают амоксициллин/клавуланат и цефалоспорины II–III поколений. При аллергии на β-лактамы назначаются макролиды. По показаниям могут быть использованы антибиотики глубокого резерва — линкозамиды.
Основным методом лечения большинства пациентов с воспалительной патологией глотки и важной составляющей терапии больных стрептококковым тонзиллофарингитом является использование топических препаратов — полосканий, спреев, таблеток для рассасывания. Чаще всего местные лекарственные формы представлены комбинацией различных препаратов, что помогает быстро и эффективно воздействовать на основные проявления заболевания. Другими плюсами средств для топического использования являются их низкая системная биодоступность, обусловливающая минимизацию побочных эффектов, в сочетании с высокой концентрацией вещества в очаге воспаления и меньшим риском селекции резистентных штаммов нормальной микрофлоры [4].
Трудности терапии больных острым тонзиллофарингитом в ряде случаев могут быть связаны с формированием микробных биопленок. Нахождение в составе биопленки — одна из двух форм существования бактерий. Предполагается, что 90% известных бактерий способны формировать биопленки. Биопленкой называется высокоорганизованное сообщество клеток микроорганизмов (5–35% от ее состава), адгезированных на биотической или абиотической поверхности, окруженное полимерным матриксом (65–95% состава биопленки) и обладающее сложной системой регуляции физиологических процессов, основанной на межклеточной коммуникации [5–7].
Микроорганизмы, находясь в составе биопленок, приобретают устойчивость к факторам воздействия, способны изменять свои свойства, в основном за счет наличия матрикса — он обеспечивает снижение диффузии антибиотиков и накапливает ферменты, разрушающие лекарственные средства. Бактерии в биопленках обмениваются генами резистентности к различным лекарственным субстанциям, что сужает возможности системной антибиотикотерапии. Благодаря агрегации поверхности клеток возбудителей уменьшается площадь их контакта с внешней средой, что также осложняет воздействие на них антимикробного препарата. Из-за снижения активности метаболизма бактерий снижается их восприимчивость к факторам внешней среды — развивается антибиотикотолерантность. Однако, даже находясь в составе биопленок, микроорганизмы способны высвобождать эндотоксины, тем самым способствуя развитию воспаления в ткани [6–9]. Считается, что образование биопленок является основой развития хронического инфекционного воспаления.
Впервые биопленки на миндалинах у больных хроническим тонзиллитом были обнаружены в 2003 г. Бактериальные пленки формируются на элементах эпителиальной выстилки крипт, что может быть одним из факторов быстрой хронизации и рецидивирования тонзиллита. До настоящего времени нет окончательного ответа на вопрос: биопленка является причиной или следствием обострения хронического тонзиллита? В литературе имеется указание, что в составе биопленки небных миндалин могут находиться до 48 видов микроорганизмов из разных групп, таких как стрептококки, стафилококки, энтеробактерии, грибы и др. [6–14]. В среднем у 85% пациентов с острым тонзиллофарингитом отмечается биопленкообразование [6].
Таким образом, для этиотропного местного лечения важно подобрать препарат, который дополнял бы системную противомикробную терапию, был удобен в применении, плохо абсорбировался со слизистой оболочкой, не вызывал раздражающего эффекта, а также имел способность проникать в толщу биопленки, что крайне необходимо для эрадикации возбудителя.
Вышеуказанным требованиям отвечает препарат Граммидин® производства российской инновационной фармацевтической компании АО «Валента Фарм». В состав препарата Граммидин® входят антибиотик грамицидин С и антисептик цетилпиридиния хлорид. Данные компоненты обладают синергизмом, усиливая действие друг друга.
Грамицидин C и цетилпиридиния хлорид
Грамицидин C — антибиотик широкого спектра действия, был выделен в 1942 г. учеными Г.Ф. Гаузе и М.Г. Бражниковой, широко применялся в годы Великой Отечественной войны. Данный антибиотик представляет собой циклическую белковую молекулу, состоящую из двух пентапептидов. Каждый пентапептид содержит 5 аминокислот: L-валин, L-орнитин, L-лейцин, D-фенилаланин и L-пролин, концы двух пентапептидов замыкаются в кольцо. Грамицидин C проявляет активность в отношении всех актуальных с точки зрения инфекционно-воспалительной патологии глотки патогенов бактериальной природы, эффективно действуя против грамположительных и грамотрицательных аэробов и анаэробов, особенно стрептококков и стафилококков, часто выступающих возбудителями острого тонзиллофарингита. Механизм действия грамицидина С — бактерицидный. Данный антибиотик вызывает необратимые нарушения в цитоплазматической мембране микробной клетки, неминуемо приводя к ее гибели. К преимуществам препарата относится крайне низкий риск развития к нему резистентности у бактерий [15, 16].Цетилпиридиния хлорид — вещество из группы антисептиков, широко применяющееся в лечении острых воспалительных заболеваний полости рта и глотки более 70 лет. Основными его достоинствами являются активность в отношении бактерий, грибов и вирусов, наличие поверхностно-активных свойств, способность проникать и разрушать бактериальные и грибковые биопленки [17, 18]. Цетилпиридиния хлорид препятствует адгезии бактерий и обладает бактерицидным эффектом в отношении бактерий в составе биопленки. В 2011 г. было проведено исследование по сравнению эффективности воздействия 0,075% раствора цетилпиридиния хлорида и стерильного солевого раствора на биопленку, содержащую различные виды микроорганизмов. Результаты эксперимента показали, что 72,7% бактерий в составе биопленки, обработанной цетилпиридиния хлоридом, были повреждены. После воздействия стерильным солевым раствором этот показатель составил 25,7% [7, 10, 13].
В другом исследовании была показана способность цетилпиридиния хлорида влиять на толщину биопленки — в среднем после воздействия отмечалось ее сокращение на 34–43% [7, 14]. В научной литературе имеются указания на то, что в реальных условиях цетилпиридиния хлорид более эффективно воздействует на биопленки, чем хлоргексидин, не уступает другим антисептикам по воздействию на грибковые биопленки и при этом эффективнее других препаратов в отношении планктонных грибов рода Candida.
Комбинация грамицидина C и цетилпиридиния хлорида, эффективно элиминируя причинный фактор инфекционного процесса, способствует быстрому купированию болевого синдрома и оказывает выраженный противовоспалительный эффект. Таким образом, Граммидин® у больных с инфекционно-воспалительными процессами в глотке оказывает противомикробное действие, уменьшает воспаление, смягчает неприятные ощущения в горле, облегчает глотание, в т. ч. прием пищи.
Граммидин® выпускается в виде таблеток для рассасывания и дозированного спрея. Граммидин® — единственный в РФ препарат в форме спрея, содержащий комбинацию местного антибиотика и антисептика для лечения пациентов с инфекционно-воспалительными заболеваниями глотки. Данная лекарственная форма удобна в применении, при орошении ротоглотки препарат равномерно распределяется по поверхности слизистой оболочки. Таблетки для рассасывания Граммидин® используются у взрослых и детей с 4 лет, спрей Граммидин® детский разрешен к применению с 6-летнего возраста [16–18].
Граммидин® имеет достаточную доказательную базу. Эффективность и безопасность таблеток в лечении детей с острым тонзиллофарингитом нестрептококковой этиологии продемонстрированы результатами нескольких клинических исследований: показано, что использование препарата Граммидин® у таких пациентов курсом 6 дней позволило быстро купировать болевой синдром и фарингоскопические признаки острого тонзиллофарингита. Нежелательных эффектов при применении препарата Граммидин® не было отмечено ни в одном случае [10, 18].
Возможности использования дозированного спрея
Граммидин® были показаны в открытом многоцентровом исследовании при лечении пациентов с инфекционно-воспалительными заболеваниями глотки, такими как острый фарингит, острый назофарингит, хронический фарингит в стадии обострения. Всего наблюдались 73 пациента в возрасте от 18 до 67 лет, которые использовали дозированный спрей Граммидин® 3 р./день после еды, по 4 впрыска, курс лечения составил 7 дней. Эффективность терапии оценивалась по динамике боли в глотке, катаральных явлений и интоксикационного синдрома. Безопасность оценивалась путем регистрации и отслеживания исходов всех нежелательных явлений. Результаты исследования продемонстрировали высокую клиническую эффективность: у всех наблюдаемых пациентов, получавших препарат Граммидин® спрей, отмечались положительная динамика и полное купирование симптомов по окончании лечения. На фоне использования спрея Граммидин® у 4 пациентов отмечались непродолжительные нежелательные явления легкой степени тяжести, не потребовавшие отмены препарата. По результатам оценки витальных функций, биохимического и клинического анализа крови, клинического анализа мочи отрицательной динамики не выявлено [19].
На базе Первого МГМУ им. И.М. Сеченова было проведено открытое неинтервенционное исследование нового препарата Граммидин® спрей дозированный для симптоматического лечения боли в горле у пациентов с хронической патологией ЛОР-органов. Всего в исследование было включено 120 пациентов с симптомом «боль в горле» и диагностированными клинически острыми или в стадии обострения хроническими инфекционно-воспалительными заболеваниями глотки. Препарат Граммидин® спрей дозированный назначался врачом исходя из наличия показаний у пациента и применялся в соответствии с инструкцией 3 р./день по 4 впрыска после еды, курс лечения составил 7 дней. Методология программы включала 4 запланированных визита: 1-й визит (начало лечения), 2-й визит (через сутки от начала лечения, допускался телефонный звонок), 3-й визит (через 4 сут от начала лечения), 4-й визит (на 7–8-й день, завершение лечения). В ходе данных визитов оценивались клинические проявления симптома «боль в горле» по 4-балльной шкале, степень выраженности местных признаков острого воспаления при фарингоскопии (во время очных визитов), а также переносимость терапии.
Все 120 пациентов завершили исследование согласно протоколу и были включены в анализ эффективности и безопасности. У всех пациентов было выявлено наличие сопутствующей хронической патологии одного или нескольких ЛОР-органов. Наиболее распространенными были хронические заболевания глотки: изолированный хронический фарингит — 53,3%; хронический фарингит + хронический тонзиллит — 10,8%; хронический фарингит + хронический синусит — 7,5%; хронический фарингит + хронический бронхит — 5,8%; хронический фарингит + хронический ларингит — 5%. Всего изолированные или сочетанные хронические заболевания глотки зафиксированы у 110 пациентов. В связи с этим представляло интерес изучить возможность применения препарата Граммидин® спрей дозированный в данной группе пациентов.
При количественной оценке симптомов фарингеальной парестезии при включении в исследование в группе пациентов с хронической патологией глотки и миндалин першение и саднение в горле проявлялись со средним баллом 1,136±0,439 и 1,036±0,557 соответственно, тогда как средний балл проявления сухости в горле составил 0,891±0,655. К 3-му визиту отмечено существенное снижение выраженности всех симптомов: першение — 0,364±0,502 балла, саднение — 0,255±0,478 балла, сухость — 0,146±0,425 балла. На 4-м визите все симптомы фарингеальной парестезии отсутствовали (рис. 1).
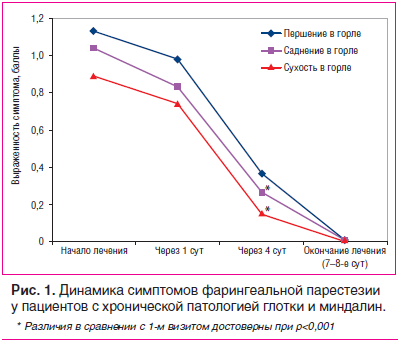
При количественной оценке болевых ощущений при включении в исследование в группе пациентов с хронической патологией глотки и миндалин наиболее выраженной была боль при глотании — 1,564±0,773 балла, боль в горле в покое составила 1,155±0,411 балла, жжение в горле — 0,582±0,581 балла. К 3-му визиту отмечено существенное снижение выраженности всех симптомов: боль при глотании — 0,455±0,644 балла, боль в горле в покое — 0,309±0,520 балла, жжение в горле — 0,109±0,391 балла. На 4-м визите все симптомы фарингеальной парестезии отсутствовали (рис. 2).

Анализ обобщенной оценки показал, что болевые ощущения с симптомами фарингеальной парестезии и без таковых на 1-м визите отмечены у всех 110 пациентов с наличием хронической патологии глотки и миндалин (100%). На 3-м визите болевые ощущения в группе пациентов с наличием хронической патологии глотки и миндалин регистрировали у 34 (30,9%) пациентов, только симптомы фарингеальной парестезии отмечали у 20 (18,2%) пациентов. Болевые ощущения полностью отсутствовали на 3-м визите у 56 (50,9%) пациентов. К концу исследования на 4-м визите только симптомы фарингеальной парестезии отмечались лишь у 1 (0,9%) пациента в группе с хронической патологией глотки и миндалин (рис. 3).
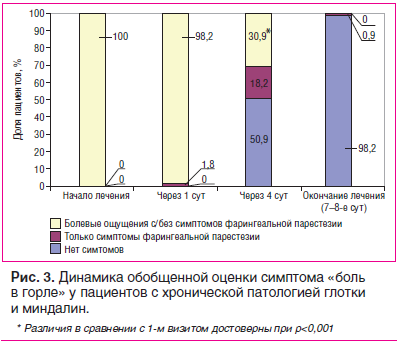
Количественная оценка местных признаков острого воспаления по данным фарингоскопии для характеристики гиперемии и отека на 1-м визите составляла в среднем 1,600±0,666 и 1,573±0,613 балла соответственно. Наличие лимфоидных гранул задней стенки глотки и боковых столбов на 1-м визите в среднем составило 0,591±0,668 балла. Уже к 3-му визиту было отмечено достоверное снижение выраженности всех признаков острого воспаления по данным фарингоскопии. К концу исследования средние показатели наличия отека слизистой оболочки глотки, а также лимфоидных гранул задней стенки глотки и боковых столбов достоверно снизились на 1,555 и 0,573 балла соответственно и составили в обоих случаях 0,018±0,134 балла. Гиперемия достоверно снизилась на 1,591 балла, достигнув значения 0,009±0,095 балла (рис. 4).

За весь период проведения исследования нежелательных явлений и нежелательных реакций зарегистрировано не было.








.gif)



