Когда речь идет о функциональных нарушениях как нозологической единице, обычно подразумеваются нарушения моторной функции, однако вполне правомерно говорить о других функциональных нарушениях, например, связанных с нарушениями секреции.
К функциональным относятся состояния желудочно–кишечного тракта, заключающиеся в несовершенстве моторной функции (физиологический гастроэзофагеальный рефлюкс, нарушение аккомодации желудка и антропилорической моторики, дискинезии тонкой и толстой кишки) и секреции (значительная вариабельность активности желудочной, панкреатической и кишечной липазы, низкая активность пепсина, незрелость дисахаридаз, в частности, лактазы), лежащие в основе синдромов срыгиваний, кишечных колик, метеоризма, диспепсии, не связанные с органическими причинами и не влияющие на состояние здоровья ребенка [7–8].
Дисфункции желудочно–кишечного тракта у детей раннего возраста клинически наиболее часто проявляются следующими синдромами: синдром срыгивания; синдром кишечной колики (метеоризм в сочетании со схваткообразными болями в животе и криком); синдром нерегулярного стула со склонностью к запорам и периодическими периодами послабления [3].
Классификация функциональных расстройств в рамках Римского Консенсуса в третьей редакции в педиатрической своей части претерпела существенные изменения. Имевшие место в Римском II Консенсусе детские функциональные расстройства разделены на «Функциональные расстройства: новорожденные и дети младшего возраста» (категория G) и «Функциональные расстройства: дети и подростки» (категория H) [9–11].
G. Функциональные расстройства: новорожденные и дети младшего возраста (дети до 4 лет)
• G1. Младенческая регургитация
• G2. Младенческий руминационный синдром
• G3. Синдром циклической рвоты
• G4. Младенческая колика
• G5. Функциональная диарея
• G6. Младенческая затрудненная дефекация (дисхезия)
• G7. Функциональный запор
Н. Функциональные расстройства: дети и подростки (от 4 до 18 лет)
H1. Рвота и аэрофагия
• H1a. Подростковый руминационный синдром
• H1b. Синдром циклической рвоты
• H1c. Аэрофагия
• H3. Запор и недержание (кала)
• H3a. Функциональный запор
• H3b. Недержание кала без его задержки
H2. Функциональные пищеварительные расстройства, связанные с абдоминальной болью
• H2a. Функциональная диспепсия
• H2b. Синдром раздраженного кишечника
• H2c. Абдоминальная мигрень
• H2d. Детская функциональная абдоминальная боль
• H2d1. Синдром детской функциональной абдоминальной боли
Одним из частых вариантов функциональных расстройств является регургитация (срыгивание), которая у новорожденных всегда относится к функциональным заболеваниям. При этом имеет место обратный заброс пищевого химуса вскоре после проглатывания съеденной пищи.
Срыгивание расценивается как физиологическое состояние в том случае, если оно носит:
– редкий, необильный характер,
– возникает не позже одного часа после кормления.
Тревожными, требующими дополнительного обследования и проведения дифференциально–диагностического поиска являются срыгивания, если они:
– возникают более двух раз в сутки,
– появляются через час и позднее после еды,
– носят обильный характер.
Следует, однако, отметить, что мнение о том, что срыгивания у детей раннего возраста исчезают по мере их роста без каких–либо последствий, не подтверждается данными проведенных исследований (рис. 1).
Так, например, оценке риска развития ГЭРБ у детей более старшего возраста посвящена работа Martin A.J. et al. [13]. В этом исследовании впервые была прослежена взаимосвязь частых срыгиваний на первом году жизни и вероятность развития типичных симптомов ГЭРБ у этих детей в дальнейшем. Всего в исследование было включено 693 ребенка, которые наблюдались с первого года жизни в течение 9 лет. Были подтверждены данные Nelson et al. [14,15] о том, что наиболее часто дети срыгивают в возрасте 3–4 месяцев – 41% детей. При дальнейшем наблюдении детей с частыми срыгиваниями (>90 дней за первые 2 года жизни) было показано, что они к 9–10–летнему возрасту чаще страдают от типичных проявлений ГЭРБ (рис. 1). Риск развития кислой отрыжки у этих детей больше в 4,7 раз, риск изжоги – в 4,6 раз, риск повторной рвоты – в 2,7 раз. Таким образом, можно говорить о том, что частые срыгивания на первом году жизни ребенка являются предпосылкой для дальнейшего развития ГЭРБ в более старшем возрасте.
Другим вариантом функциональной диспепсии является кишечная колика. У детей первого года жизни диагноз функциональной абдоминальной боли не ставится, а состояние с похожими симптомами называют детскими коликами (от греческого «коликос», что означает «боль в толстой кишке»). В первые три месяца жизни более чем у 70% детей отмечаются функциональные кишечные колики. Среди основных причин кишечных колик называются: морфофункциональная незрелость периферической иннервации кишечника, дис¬функ¬ция центральной регуляции, поздний старт ферментативной системы органов ЖКТ, повышенное газообразование, синдром мальабсорбции, нарушения становления микробиоценоза кишечника, характер питания матери. Нельзя исключить из причин и аллергические, и псевдоаллергические реакции, переход с естественного вскармливания на искусственное, включение в рацион пищевых добавок. Возникновение болевого синдрома преимущественно связывается с нарушением двигательной функции кишечника. Сущность данных рефлексов в том, что спустя 1–10 мин после приема пищи возникает периодическое повышение моторной активности кишки, которое сопровождается гиперемией и секрецией слизистой оболочки. Гастроцекальный рефлекс вызывает массивную моторную деятельность одновременно всех сегментов толстой кишки и возникает после каждого приема пищи. Другая составляющая боли при кишечной колике обусловлена повышенным газообразованием и растяжением стенки кишечника. Ряд авторов считают, что детские колики обусловлены несовершенством нервной регуляции деятельности кишечника, отмечают также незрелость ферментных систем у новорожденного и, как следствие – усиление бродильных процессов.
Для диагностики кишечной колики у младенцев используют так называемое «правило трёх» – плач в течение 3 и более часов в сутки, не менее 3 дней в неделю, на протяжении 3 недель подряд. Клинически у детей отмечаются боли спастического характера. Приступ, как правило, начинается неожиданно, на фоне полного благополучия, чаще во время или вскоре после кормления, сопровождается длительным плачем. Ребенок пронзительно кричит, беспокоится, сучит ножками, стопы часто холодные на ощупь, руки прижаты к туловищу. Живот вздут и напряжен, возможны нечастые срыгивания. Однако для функциональных колик не характерны болезненность при пальпации живота, напряжение мышц брюшной стенки и затруднение при глубокой пальпации. Как правило, заметное облегчение наступает сразу после дефекации или отхождения газов. Вне приступа кишечной колики дети имеют хороший аппетит, прибавляют в весе, сохраняют общий позитивный эмоциональный настрой. Необходимо помнить, что диагноз кишечной колики устанавливается только после того, как были исключены более грозные состояния, сопровождающиеся возникновением абдоминальной боли.
Классификация функциональной диспепсии базируется на оценке ведущего клинического синдрома. Различают три варианта функциональной диспепсии:
– язвенноподобный,
– дискинетический,
– неспецифический [1].
Согласно данным обследования 3926 пациентов, проведенного Grainger SL et al., функциональная диспепсия более чем в половине случаев (в общей сложности у 57%) проявляется либо только нарушениями моторики (13%), либо в сочетании их с другими клиническими проявлениями (44%) (рис. 2).
К нарушениям гастродуоденальной моторики, выявляемым у пациентов с функциональной диспепсией, относят:
– гастропарез (ослабление моторно–эвакуаторной функции желудка);
– нарушение антродуоденальной координации;
– ослабление постпрандиальной моторики антрального отдела;
– нарушение распределения пищи внутри желудка (расстройство релаксации желудка, нарушенная аккомодация пищи в теле желудка);
– нарушения циклической активности желудка в межпищеварительном периоде – желудочные дисритмии (тахигастрия, брадигастрия, антральная фибрилляция);
– дуоденогастральный рефлюкс [1].
Собственные результаты
Целью исследования явилось на основе данных клинического и инструментального (эзофагогастродуоденоскопия, суточная рН–метрия) обследования оценить характер нарушений моторики верхних отделов пищеварительного тракта у детей с ГЭРБ и обосновать целесообразность включения прокинетиков в схемы лечения данной патологии.
Нами были обследованы 62 ребенка (20 девочек и 42 мальчика в возрасте от 9 до 17 лет), которые находились на стационарном лечении в гастроэнтерологическом отделении клиники детских болезней ММА имени И.М. Сеченова по поводу различных заболеваний ЖКТ. Всем детям был проведен суточный мониторинг рН в пищеводе и желудке для оценки функционального состояния верхних отделов ЖКТ. Для оценки тяжести воспалительных изменений слизистой оболочки пищевода, желудка и двенадцатиперстной кишки всем детям была проведена эзофагогастродуоденоскопия (ЭГДС).
Для диагностики нарушений моторики верхних отделов ЖКТ наиболее информативна суточная рН–метрия. Данный метод позволяет выявить наличие патологических гастроэзофагеальных (ГЭР) и дуодено–гастральных (ДГР) рефлюксов, их частоту, длительность и особенности возникновения (связь с приемами пищи, положением тела), сопоставить появление жалоб с эпизодами рефлюкса, оценить эффективность проводимой терапии.
24–часовое мониторирование рН проводилось при помощи аппарата «Гастроскан 24» (Исток–Система, Россия), трансназального трехэлектродного рН–зонда и компьютерной системы. Исследование выполнялось до назначения антисекреторных препаратов, антацидные препараты отменяли не позднее, чем за 24 часа до исследования. Зонд устанавливали в I положение: нижний электрод располагался в теле желудка, средний – в кардиальном отделе желудка, верхний – на расстоянии 5 см выше нижнего пищеводного сфинктера. После окончания исследования данные с прибора передавались в базу данных персонального компьютера, где производилась их расшифровка [16].
Для оценки результатов рН–метрии в пищеводе использовали критерии, разработанные T.R. DeMeester et al. [17]. Патологический кислый ГЭР (КГЭР) диагностировали в тех случаях, когда общая продолжительность снижения внутрипищеводного рН ниже 4,0 составляла более 4,5% времени исследования, а индекс DeMeester превышал 14,7.
Подъемы рН в пищеводе выше 7,5 более 27 раз в сутки расценивались, как патологический щелочной ГЭР. Также при оценке щелочных ГЭР учитывались такие показатели, как процент времени с рН более 7,5, число эпизодов щелочных ГЭР длительностью более 5 минут, наиболее продолжительный щелочной ГЭР [18,19].
У части детей показатели суточного мониторинга pH в пищеводе соответствовали как критериям патологического кислого, так и патологического щелочного ГЭР. В таких случаях давалось заключение о наличии патологического смешанного рефлюкса.
Для диагностики патологических ДГР Гнусаевым С.Ф. с соавт. (2003) была разработана оценка степени выраженности ДГР в баллах по графику колебаний рН в антральном отделе за ночной период (с 22.00 до 7.00 часов) [19]:
0 баллов – отсутствие колебаний рН выше 5 в ночное время;
1 балл – ДГР кратковременные, единичные, занимают не более 1/4 части анализируемого периода;
2 балла – ДГР возникают в основном в предутренние часы, занимают не более 1/2 части исследуемого времени;
3 балла – ДГР возникают на протяжении всей ночи, занимают более 1/2 части анализируемого периода.
По данным ЭГДС у всех детей был выявлен эзофагит (классификация по G. Tytgat в модификацмм Приворотского В.Ф.) [20]: I степени – у 17 детей, II степени – у 36 детей, III степени – у 4 детей и у 4 подростков морфологически был подтвержден пищевод Барретта (эзофагит IV степени).
Исходя из эндоскопической картины в пищеводе все дети были разделены на 2 группы: первая (n=18) – дети с катаральным эзофагитом (I степень), вторая группа (n=44) – дети с эрозивным эзофагитом (ЭЭ) (II, III и IV степени).
При эндоскопическом исследовании у всех детей были выявлены воспалительные изменения разной степени выраженности в пищеводе, желудке и двенадцатиперстной кишке. В группе детей с эрозивными эзофагитами большинство детей были с эзофагитом II степени (единичные эрозии) – 81,8%. Эзофагит III и IV степени обнаружен в 9,1 и 9,1% случаев соответственно. Эзофагит IV степени устанавливался после морфологического исследования биопсий слизистой оболочки из области атипичных очагов. У всех 4 пациентов морфологически был подтвержден диагноз пищевод Барретта, желудочная метаплазия. В группе детей с эрозивным эзофагитом достоверно чаще выявлялись нарушения моторики в области кардио–эзофагеального перехода в виде недостаточности кардии и гастроэзофагеального рефлюкса (52,3% против 22,2%, р<0,05).
Эрозивный гастрит в группе больных с неэрозивным эзофагитом не выявлялся, в то время как в группе детей с эрозивным эзофагитом в 6,8% случаев были выявлены эрозии в желудке. Эрозивный дуоденит в группе детей с эрозивным эзофагитом выявлялся в три раза чаще (18,2%), чем у детей с неэрозивным эзофагитом (5,6%). Причем у одного больного отмечалось наличие множественных эрозий в пищеводе (эзофагит III степени) в сочетании с эрозиями в антральном отделе желудка и луковице 12–перстной кишки.
Нарушения моторики в пилоро–дуоденальной зоне по данным ЭГДС в виде дуодено–гастрального рефлюкса отмечались примерно у половины больных в обеих группах: у 52,6% детей с эрозивным и у 55,6% детей с катаральным эзофагитом.
Таким образом, по данным ЭГДС воспалительные изменения слизистой оболочки верхних отделов ЖКТ и нарушения моторики в зоне кардиоэзофагеального перехода были более выраженными в группе детей с эрозивным эзофагитом.
При проведении суточного мониторинга рН в пищеводе в группе детей с неэрозивным эзофагитом физиологический ГЭР зафиксирован у 8 больных (45%), патологические ГЭР – у 10 (55%). Кислый ГЭР отмечался у 4 (22%), щелочной – у 6 детей (33%). Смешанных ГЭР в группе детей без эрозий в пищеводе не отмечалось.
При проведении суточного мониторинга рН в пищеводе в группе детей с эрозивным эзофагитом физиологический ГЭР зафиксирован у 19 больных (43%), у 25 (57%) отмечались патологические ГЭР. Среди детей с патологическим ГЭР кислый вариант отмечался у 8 (18%), щелочной – у 10 (23%), а смешанный – у 7 больных (16%).
При анализе рН–грамм в теле желудка ДГР 2–3 балла [Гнусаев с соавт., 2003] отмечался у 43 из 66 обследованных детей (65%).
В группе детей с неэрозивным эзофагитом ДГР зафиксирован у 11 детей (61%). При этом сочетание ДГР с физиологическим ГЭР отмечалось у 3 из 6 детей (50%), с патологическим кислым ГЭР – у 1 из 4 детей (25%), с патологическим щелочным ГЭР – у 7 из 8 больных (88%).
При проведении суточного мониторинга рН в теле желудка в группе детей с эрозивным эзофагитом ДГР зафиксирован у 32 детей (73%). При этом сочетание ДГР с физиологическим ГЭР отмечалось у 14 из 19 детей (74%), с патологическим кислым ГЭР – у 5 из 8 (63%), с патологическим щелочным ГЭР – у 7 из 10 больных (70%), а среди детей со смешанным ГЭР – у 6 из 7 (86%).
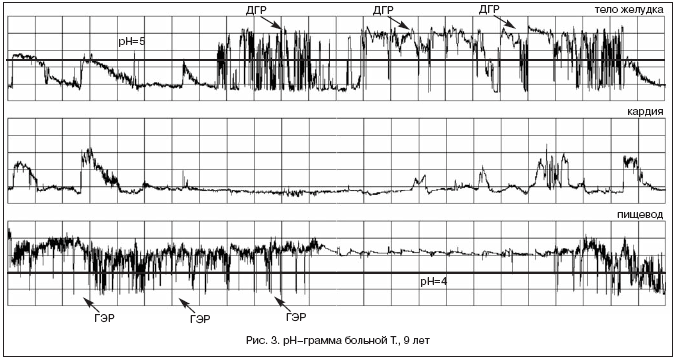
На рисунке 3 представлены данные суточного мониторинга рН в пищеводе и желудке больной Т. 9 лет с жалобами на изжогу и отрыжку, эрозивным эзофагитом по данным ЭГДС. В пищеводе отмечаются множественные ГЭР с рН<4 преимущественно в дневное время. Процент времени с рН<4 в пищеводе – 7% за сутки (при норме до 4,5%), общее количество щелочных ГЭР с рН<4 составило 88 (при норме до 47). В теле желудка в вечернее и ночное время регистрируются множественные подъемы рН>5, занимающие большую часть суток, что соответствует критериям патологического ДГР [18,19].
На рисунке 4 представлены данные суточного мониторинга рН в пищеводе и желудке больной Р. 11 лет с жалобами на срыгивания, изжогу, отрыжку, катаральным эзофагитом и признаками грыжи пищеводного отверстия диафрагмы по данным ЭГДС. В пищеводе отмечаются множественные щелочные ГЭР с рН>7,5 в дневное время. Процент времени с рН>7,5 в пищеводе составил 70% за сутки (при норме до 16%), общее количество щелочных ГЭР с рН>7,5 – 295 (при норме до 27). В теле желудка отмечаются подъемы рН>5, занимающие более 1/2 части ночного времени, что соответствует критериям патологического ДГР [18,19].
Таким образом, по данным суточной рН–метрии более чем у половины детей как с эрозивной, так и с неэрозивной формой ГЭРБ, выявлены патологические ГЭР, причем наиболее часто – щелочные. У большинства пациентов выявлялись ДГР. При этом наиболее часто ДГР сочетались с патологическим щелочным и смешанным ГЭР. Наличие смешанных ГЭР среди детей с эрозивным эзофагитом косвенно подтверждает более выраженные нарушения моторики верхних отделов пищеварительного тракта (в том числе и в пилоро–дуоденальной зоне) у таких детей. Все это свидетельствует о значительных нарушениях моторики верхних отделов ЖКТ у детей с ГЭРБ, что необходимо учитывать при лечении данной патологии.
Эффективным препаратом, используемым в педиатрической практике, является домперидон (Мотилиум). По своей химической структуре он относится к производным бензимидазола, является высокоселективным блокатором периферических допаминовых рецепторов (D) 2 типа и в отличие от метоклопрамида лишен многих побочных эффектов ввиду отсутствия проникновения препарата через гематоэнцефалический барьер. Подавляя влияние дофамина, домперидон увеличивает спонтанную активность желудка, повышает давление нижнего пищеводного сфинктера и активирует перистальтику пищевода и антрального отдела желудка. Препарат также усиливает частоту, амплитуду и продолжительность сокращений двенадцатиперстной кишки и уменьшает время пассажа пищевых масс по тонкой кишке. Домперидон оказывает противорвотный эффект, который обусловлен подавлением активности хеморецепторных триггерных зон, расположенных на дне четвертого желудочка вне пределов гематоэнцефалического барьера. При его применении практически не отмечены экстрапирамидные реакции у детей. Также обнаружено позитивное влияние домперидона при запорах у детей: он приводит к нормализации процесса дефекации. Мотилиум назначается в дозе от 0,25 мг/кг (в виде суспензии и таблеток) 3–4 раза в сутки за 30–60 минут до приема пищи и перед сном.
После приема внутрь Мотилиум быстро абсорбируется в желудочно–кишечном тракте. Максимальная концентрация в крови достигается через 0,5–1 часа. Подвергается интенсивному метаболизму в стенке кишечника и печени (путем гидроксилирования и N–дезалкилирования) с образованием гидроксидомперидона и 2,3–дигидро–2–оксо–1–H–бензимидазол–1–пропионовой кислоты соответственно. Время полувыведения после однократной дозы – 7 часов и увеличивается при хронической почечной недостаточности. 31% выводится почками, из них 1% – в неизмененном виде и 66% – кишечником (в неизмененном виде 10%).
Мотилиум относится к прокинетикам II поколения и в отличие от прокинетиков I поколения: Церукала, Реглана и др. (активное вещество метоклопрамид) плохо проникает через гематоэнцефалический барьер. Поэтому препарат не вызывает экстрапирамидальных расстройств: Мотилиум реже и в меньшей степени, чем Церукал и Реглан, вызывает такие побочные эффекты, как сонливость, утомляемость, усталость, слабость, головные боли, повышенную тревожность, растерянность, шум в ушах.
У детей Мотилиум показан при синдроме срыгивания, циклической рвоте, гастроэзофагеальных рефлюксах и других нарушениях моторики верхних отделов пищеварительного тракта.
Мотилиум применяют при лечении многих заболеваний ЖКТ, обычно в комплексе с антисекреторными и другими лекарствами. Наиболее часто его назначают при:
• гастроэзофагеальной рефлюксной болезни;
• ахалазии кардии;
• дуоденогастральном рефлюксе;
• хронических гастритах со снижением моторно–эвакуаторной функции желудка;
• гастроптозе;
• язвенной болезни желудка с нормальной и пониженной кислотностью и ослаблением мышечного тонуса и перистальтики;
• атонии и гипотонии желудка и двенадцатиперстной кишки, развившихся в послеоперационном периоде (гастропарез);
• гипокинетическом типе дискенизии желчевыводящих путей.
Лекарственные формы Мотилиума:
• таблетки для рассасывания
• таблетки, покрытые оболочкой
• суспензия для приема внутрь
Одна таблетка для рассасывания или таблетка, покрытая оболочкой, содержит 10 мг домперидона. Суспензия для приема внутрь содержит 1 мг домперидона в 1 мл. Таблетки, покрытые оболочкой, показаны для взрослых и детей с массой тела более 35 кг.
Таблетки для рассасывания показаны для взрослых и детей старше 5 лет. Детям в возрасте до 5 лет рекомендуется использовать Мотилиум в форме суспензии.
При диспепсии взрослым и детям назначают по 10 мг 3 раза/сут. за 15–30 мин. до приема пищи и в случае необходимости – перед сном. Максимальная суточная доза – 80 мг. При необходимости для взрослых и детей в возрасте старше 12 лет дозу можно удвоить. Детям препарат в форме суспензии назначают из расчета 2,5 мл/10 кг массы тела (что соответствует 250 мкг/кг массы тела) 3 раза/сут. до приема пищи и в случае необходимости – перед сном. При тошноте и рвоте взрослым и детям старше 12 лет назначают по 20 мг 3–4 раза/сут. до приема пищи и перед сном. Детям в возрасте от 5 до 12 лет назначают по 10 мг 3–4 раза/сут. до приема пищи и перед сном. Препарат в форме суспензии назначают из расчета 5 мл/10 кг массы тела (что соответствует 500 мкг/кг массы тела) 3–4 раза/сут. до приема пищи и перед сном. Эта доза достигается двукратным наполнением пипетки. В последнее время появилась удобная форма Мотилиума – таблетки для рассасывания. Препарат не нужно запивать, он растворяется на языке.
Эффективность применения Мотилиума в сочетании с ингибитором протонной помпы при лечении детей с ГЭРБ демонстрирует следующий клинический случай.
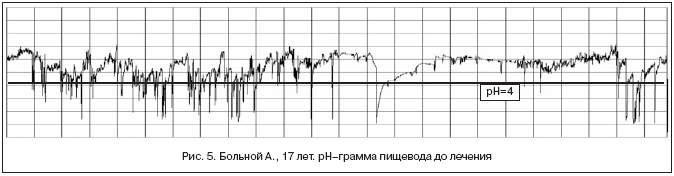
На рисунках 5 и 6 представлены данные рН–метрии в пищеводе больного А., 17 лет с ЭЭ на фоне длительного течения ГЭРБ до лечения и после курса ИПП (эзомепразол) в сочетании с прокинетиком (домперидон). Исходная рН–грамма соответствует по критериям DeMeester патологическому кислому ГЭР. После проведенной терапии общее время с рН<4 в пищеводе уменьшилось с 7 до 2% за сутки, число рефлюксов с рН<4 сократилось с 47 до 16, а индекс DeMeester составил 7,43 (табл. 1). Полученные данные показывают эффективность использования прокинетика в комплексной терапии ГЭРБ.
Таким образом, домперидон является эффективным и безопасным прокинетиком, который может быть рекомендован к применению в педиатрической практике для комплексного лечения детей с нарушениями моторики верхних отделов пищеварительного тракта.
![Рис. 1. Риск развития симптомов ГЭРБ у детей в возрасте 9–10 лет с частыми срыгиваниями в раннем анамнезе [Martin, 2002]](/data/articles/Image/t18/n1/1-1.gif)
![Рис. 2. Варианты функциональной диспепсии по Grainger S.L. et al. [12]](/data/articles/Image/t18/n1/1-2.gif)



Литература
1. Шабалов Н.П. “Детские болезни” СПб, Сотис, 1993, с.240–248
2. Эрдес С.И., Мухаметова Е.М. Абдоминальная боль у детей и пути ее терапии. Гастроревью. Педиатрия. Сборник избранных статей, 2009. С. – 21–24.
3. Эрдес С.И. Актуальные проблемы абдоминальной патологии у детей. Вопросы современной педиатрии, 2009.–Т.8, №2. – С.68–76.
4. С.В.Бельмер, Т.В.Гасилина, А.И.Хавкин, А.С.Эйберман. Функциональные нарушения органов пищеварения у детей. М., 2005.– 36 с.
5. Печкуров Д.В., Щербаков П.Л., Канганова Т.И. Синдром диспепсии у детей: современные подходы к диагностике и лечению. Информационно–методические материалы для педиатров, гастроэнтерологов и семейных врачей. Самара, 2005. 20с.
6. Бельмер С.В., Гасилина Т.В., Хавкин А.И., Пономарева А.П. Функциональные нарушения верхних отделов пищеварительного тракта у детей. Лечащий врач, 2005.– №8.
7. Детская гастроэнтерология. Руководство на компакт–диске. Под общей редакцией С.В. Бельмера и А.И. Хавкина. Москва, 2001 г., 692 MB.
8. Хавкин А.И. «Функциональные нарушения желудочно–кишечного тракта у детей раннего возраста» Пособие для врачей, Москва, 2001г. стр.16–17.
9. Пиманов C.И., Силивончик Н.Н. Римский III Консенсус: избранные разделы и комментарии. Пособие для врачей. Витебск: Издательство ВГМУ, 2006.–160с.
10. Drossman D.A. The functional gastrointestinal disorders and the Rome III process. Gastroenterology 2006; 130: 1377–1390.
11. Thompson W.G. The road to Rome. Gastroenterology 2006; 130: 1552–1556
12. Grainger S.L., Klass H.J., Rake M.O., et al: Review article: prevalence of dyspepsia: the epidemiology of overlapping symptoms. Postgrad Med J 1994; 70: 154–161
13. Martin A.J., Pratt N., Kennedy J.D., et al. Natural history and familial relationships of infant spilling to 9 years of age. Pediatrics 2002; 109:1061.
14. Nelson S.P., Chen E.H., Syniar G.M., et al. Prevalence of symptoms of gastroesophageal reflux during infancy. A pediatric practice–based survey. Pediatric Practice Research Group. Arch Pediatr Adolesc Med 1997; 151: 569–72.
15. Nelson S.P., Chen E.H., Syniar G.M., et al. One–year follow–up of symptoms of gastroesophageal reflux during infancy. Pediatric Practice Research Group. Pediatrics 1998; 102: E67.
16. Рапопорт С.И., Лакшин А.А., Ракитин Б.В., Трифонов М.М. рН–метрия пищевода и желудка при заболеваниях верхних отделов пищеварительного тракта. Под ред. Ф.И. Комарова М.: ИД Медпрактика<М, 2005.
17. DeMeester T.R., Chandrasoma P. Updated guidelines for diagnosis and treatment of gastroesophageal reflux disease. Annu. Rev. Med. 1999; 50: 469–506.
18. Гнусаев С.Ф., Иванова И.И, Апенченко Ю.С. Диагностика гастроэзофагеального рефлюкса при заболеваниях верхних отделов пищеварительного тракта у детей у детей (пособие для врачей). М.: Тверская гос. мед. акад., 2003.
19. Пахомовская Н.Л. Клиническое значение суточной рН<метрии при ГЭРБ у детей: Автореф. дисс… канд. мед. наук. М., 2006.
20. Приворотский В.Ф., Луппова Н.Е. Проект рабочего протокола диагностики и лечения гастроэзофагеальной рефлюксной болезни. Вопр. дет. диетологии. 2004; 2(1): 87–92.











