–Ґ—А–∞—Е–µ–Њ–±—А–Њ–љ—Е–Є–∞–ї—М–љ–∞—П —Б–ї–Є–Ј—М —П–≤–ї—П–µ—В—Б—П —Б–Њ–≤–Њ–Ї—Г–њ–љ—Л–Љ –њ—А–Њ–і—Г–Ї—В–Њ–Љ —Б–µ–Ї—А–µ—В–Њ—А–љ–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є –±–Њ–Ї–∞–ї–Њ–≤–Є–і–љ—Л—Е –Ї–ї–µ—В–Њ–Ї —Н–њ–Є—В–µ–ї–Є—П, –њ–Њ–і—Б–ї–Є–Ј–Є—Б—В—Л—Е –ґ–µ–ї–µ–Ј —В—А–∞—Е–µ–Є –Є –±—А–Њ–љ—Е–Њ–≤, –∞ —В–∞–Ї–ґ–µ –Ї–ї–µ—В–Њ–Ї –Ъ–ї–∞—А–∞. –Ю–±—Л—З–љ–Њ –≤ —В—А–∞—Е–µ–Њ–±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–Љ —Б–µ–Ї—А–µ—В–µ –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞—О—В—Б—П —В–∞–Ї–ґ–µ –Ї–ї–µ—В–Њ—З–љ—Л–µ —Н–ї–µ–Љ–µ–љ—В—Л (–∞–ї—М–≤–µ–Њ–ї—П—А–љ—Л–µ –Љ–∞–Ї—А–Њ—Д–∞–≥–Є –Є –ї–Є–Љ—Д–Њ—Ж–Є—В—Л), —Б—Г—А—Д–∞–Ї—В–∞–љ—В, –њ—А–Њ–і—Г–Ї—В—Л –і–µ–≥–µ–љ–µ—А–∞—Ж–Є–Є –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ –Є —Н–њ–Є—В–µ–ї–Є–Њ—Ж–Є—В–Њ–≤, –∞ —В–∞–Ї–ґ–µ –њ–ї–∞–Ј–Љ–µ–љ–љ—Л–µ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В—Л, –њ–Њ–њ–∞–і–∞—О—Й–Є–µ –Ј–∞ —Б—З–µ—В —Н–Ї—Б—Б—Г–і–∞—Ж–Є–Є –Є–ї–Є —В—А–∞–љ—Б—Б—Г–і–∞—Ж–Є–Є [1]. –Т —Б–Њ—Б—В–∞–≤–µ —Б–µ–Ї—А–µ—В–∞ –≤—Л–і–µ–ї—П—О—В –і–≤–∞ –Ї–Њ–ї–ї–Њ–Є–і–љ—Л—Е —Б–ї–Њ—П – –љ–Є–ґ–љ–Є–є (–≤–љ—Г—В—А–µ–љ–љ–Є–є) –Є –≤–µ—А—Е–љ–Є–є (–љ–∞—А—Г–ґ–љ—Л–є). –Э–Є–ґ–љ–Є–є —Б–ї–Њ–є, –±–Њ–ї–µ–µ –ґ–Є–і–Ї–Є–є (–Ј–Њ–ї—М), –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ –≤ –≤–Є–і–µ –љ–µ–њ—А–µ—А—Л–≤–љ–Њ–є –њ–Њ–і–≤–Є–ґ–љ–Њ–є –њ–ї–µ–љ–Ї–Є –љ–∞ —А–µ—Б–љ–Є—З–Ї–∞—Е –Љ–µ—А—Ж–∞—В–µ–ї—М–љ–Њ–≥–Њ —Н–њ–Є—В–µ–ї–Є—П. –Ч–Њ–ї—М –њ—А–Њ–і—Г—Ж–Є—А—Г–µ—В—Б—П –≤ –±—А–Њ–љ—Е–Є–Њ–ї–∞—Е –Є –∞–ї—М–≤–µ–Њ–ї–∞—Е. –Т –љ–µ–Љ –љ–∞—Е–Њ–і—П—В—Б—П –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є –∞–Ї—В–Є–≤–љ—Л–µ –≤–µ—Й–µ—Б—В–≤–∞, —Д–µ—А–Љ–µ–љ—В—Л, –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ—Л, –Ї–Њ—В–Њ—А—Л–µ –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞—О—В –Ј–∞—Й–Є—В–љ—Г—О —Д—Г–љ–Ї—Ж–Є—О —Б–ї–Є–Ј–Є. –Ш–Љ–µ–љ–љ–Њ –≤ —Н—В–Њ–Љ —Б–ї–Њ–µ —А–µ—Б–љ–Є—З–Ї–Є –Љ–µ—А—Ж–∞—В–µ–ї—М–љ–Њ–≥–Њ —Н–њ–Є—В–µ–ї–Є—П —Б–Њ–≤–µ—А—И–∞—О—В —Б–≤–Њ–Є –Ї–Њ–ї–µ–±–∞—В–µ–ї—М–љ—Л–µ –і–≤–Є–ґ–µ–љ–Є—П –Є –њ–µ—А–µ–і–∞—О—В –Ї–Є–љ–µ—В–Є—З–µ—Б–Ї—Г—О —Н–љ–µ—А–≥–Є—О –љ–∞—А—Г–ґ–љ–Њ–Љ—Г —Б–ї–Њ—О —В—А–∞—Е–µ–Њ–±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ —Б–µ–Ї—А–µ—В–∞. –С–ї–∞–≥–Њ–і–∞—А—П —Н—В–Њ–Љ—Г —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Г–Ї–Њ—А–∞—З–Є–≤–∞–µ—В—Б—П –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–≥–Њ –Ї–Њ–љ—В–∞–Ї—В–∞ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ —Б –Ї–ї–µ—В–Ї–∞–Љ–Є —Б–ї–Є–Ј–Є—Б—В—Л—Е –Њ–±–Њ–ї–Њ—З–µ–Ї –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є –Є, —Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –Ј–∞—В—А—Г–і–љ—П–µ—В—Б—П –Є–љ–≤–∞–Ј–Є—П –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є –≤ —В—А–∞—Е–µ–Њ–±—А–Њ–љ—Е–Є–∞–ї—М–љ—Л–є —Н–њ–Є—В–µ–ї–Є–є. –Э–∞—А—Г–ґ–љ—Л–є —Б–ї–Њ–є —В—А–∞—Е–µ–Њ–±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ —Б–µ–Ї—А–µ—В–∞ – –±–Њ–ї–µ–µ –њ–ї–Њ—В–љ—Л–є, –≤—П–Ј–Ї–Њ—Н–ї–∞—Б—В–Є—З–љ—Л–є, –љ–µ—А–∞—Б—В–≤–Њ—А–Є–Љ—Л–є (–≥–µ–ї—М). –У–µ–ї—М —Д–Њ—А–Љ–Є—А—Г–µ—В—Б—П –њ–Њ –Љ–µ—А–µ –њ—А–Њ–і–≤–Є–ґ–µ–љ–Є—П –Ј–Њ–ї—П –Њ—В —В–µ—А–Љ–Є–љ–∞–ї—М–љ—Л—Е –±—А–Њ–љ—Е–Є–Њ–ї –≤ –њ—А–Њ–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–Љ –љ–∞–њ—А–∞–≤–ї–µ–љ–Є–Є –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ —Б–Љ–µ—И–Є–≤–∞–љ–Є—П –Ј–Њ–ї—П —Б —Б–µ–Ї—А–µ—В–∞–Љ–Є –±–Њ–Ї–∞–ї–Њ–≤–Є–і–љ—Л—Е –Є —Б–µ—А–Њ–Љ—Г–Ї–Њ–Є–і–љ—Л—Е –Ї–ї–µ—В–Њ–Ї. –У–µ–ї—М –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ —И–Є—А–Њ–Ї–Њ–є —Б–µ—В—М—О –≥–ї–Є–Ї–Њ–њ—А–Њ—В–µ–Є–љ–Њ–≤, —Б—Ж–µ–њ–ї–µ–љ–љ—Л—Е –њ–Њ–њ–µ—А–µ—З–љ—Л–Љ–Є –і–Є—Б—Г–ї—М—Д–Є–і–љ—Л–Љ–Є «–Љ–Њ—Б—В–Є–Ї–∞–Љ–Є». –Я–µ—А–µ–Љ–µ—Й–µ–љ–Є–µ –≥–µ–ї—П —Б —Б–Њ–і–µ—А–ґ–∞—Й–Є–Љ–Є—Б—П –≤ –љ–µ–Љ –Ї–Њ–Љ–Њ—З–Ї–∞–Љ–Є —Б–ї–Є–Ј–Є –Є –Њ—Б–µ–≤—И–Є–Љ–Є –Є–Ј –≤–і—Л—Е–∞–µ–Љ–Њ–≥–Њ –≤–Њ–Ј–і—Г—Е–∞ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–∞–Љ–Є –Є —З—Г–ґ–µ—А–Њ–і–љ—Л–Љ–Є —З–∞—Б—В–Є—Ж–∞–Љ–Є —Б—В–∞–љ–Њ–≤–Є—В—Б—П –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–Љ —В–Њ–ї—М–Ї–Њ –њ–Њ—Б–ї–µ —А–∞–Ј—А—Л–≤–∞ –њ–Њ–њ–µ—А–µ—З–љ—Л—Е –і–Є—Б—Г–ї—М—Д–Є–і–љ—Л—Е —Б–≤—П–Ј–µ–є –Љ–µ–ґ–і—Г –≥–ї–Є–Ї–Њ–њ—А–Њ—В–µ–Є–љ–∞–Љ–Є.
–°–Ї–Њ—А–Њ—Б—В—М –≤—Л–≤–µ–і–µ–љ–Є—П —В—А–∞—Е–µ–Њ–±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–є —Б–ї–Є–Ј–Є –Є–Ј –љ–Є–ґ–љ–Є—Е –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є –Ј–∞–≤–Є—Б–Є—В –љ–µ —В–Њ–ї—М–Ї–Њ –Њ—В —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Љ–µ—А—Ж–∞—В–µ–ї—М–љ–Њ–≥–Њ —Н–њ–Є—В–µ–ї–Є—П, –љ–Њ –Є –Њ—В —А–µ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–≤–Њ–є—Б—В–≤ —Б–∞–Љ–Њ–≥–Њ —Б–µ–Ї—А–µ—В–∞. –Т –љ–Њ—А–Љ–∞–ї—М–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е —В—А–∞—Е–µ–Њ–±—А–Њ–љ—Е–Є–∞–ї—М–љ–∞—П —Б–ї–Є–Ј—М –љ–∞ 90% —Б–Њ—Б—В–Њ–Є—В –Є–Ј –≤–Њ–і—Л, –љ–∞—Е–Њ–і—П—Й–µ–є—Б—П –±–Њ–ї—М—И–µ–є —З–∞—Б—В—М—О –≤ —Б—В—А—Г–Ї—В—Г—А–љ–Њ–Љ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–µ —Б –≥–ї–Є–Ї–Њ–њ—А–Њ—В–µ–Є–љ–∞–Љ–Є. –°–Њ–і–µ—А–ґ–∞–љ–Є–µ –њ–Њ—Б–ї–µ–і–љ–Є—Е –≤ —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Г—Б–ї–Њ–≤–Є—П—Е –љ–µ –њ—А–µ–≤—Л—И–∞–µ—В 3–6% [1]. –Ш–Ј–Љ–µ–љ–µ–љ–Є–µ —Е–Є–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ—Б—В–∞–≤–∞ —Б–ї–Є–Ј–Є –њ—А–Є–≤–Њ–і–Є—В –Ї –љ–∞—А—Г—И–µ–љ–Є—О –µ–µ —Д–Є–Ј–Є—З–µ—Б–Ї–Є—Е —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї, —В–∞–Ї–Є—Е –Ї–∞–Ї –≤—П–Ј–Ї–Њ—Б—В—М, —Н–ї–∞—Б—В–Є—З–љ–Њ—Б—В—М, —В–µ–Ї—Г—З–µ—Б—В—М, —З—В–Њ –Љ–Њ–ґ–µ—В –њ—А–Є–≤–µ—Б—В–Є –Ї —Б–љ–Є–ґ–µ–љ–Є—О —Г—А–Њ–≤–љ—П –Љ—Г–Ї–Њ—Ж–Є–ї–Є–∞—А–љ–Њ–≥–Њ –Ї–ї–Є—А–µ–љ—Б–∞ –і–∞–ґ–µ –њ—А–Є —Б–Њ—Е—А–∞–љ–µ–љ–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Љ–µ—А—Ж–∞—В–µ–ї—М–љ–Њ–≥–Њ —Н–њ–Є—В–µ–ї–Є—П.
–Т–Њ—Б–њ–∞–ї–µ–љ–Є–µ —В—А–∞—Е–µ–Є –Є –±—А–Њ–љ—Е–Њ–≤ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –Ї–Њ–Љ–њ–µ–љ—Б–∞—В–Њ—А–љ—Л–Љ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ —Б–ї–Є–Ј–µ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П —Б –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ—Л–Љ –Є–Ј–Љ–µ–љ–µ–љ–Є–µ–Љ —Б–Њ—Б—В–∞–≤–∞ —В—А–∞—Е–µ–Њ–±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ —Б–µ–Ї—А–µ—В–∞ – –≤ –љ–µ–Љ —Г–Љ–µ–љ—М—И–∞–µ—В—Б—П —Г–і–µ–ї—М–љ—Л–є –≤–µ—Б –≤–Њ–і—Л –Є –њ–Њ–≤—Л—И–∞–µ—В—Б—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –Љ—Г—Ж–Є–љ–Њ–≤ (–љ–µ–є—В—А–∞–ї—М–љ—Л—Е –Є –Ї–Є—Б–ї—Л—Е –≥–ї–Є–Ї–Њ–њ—А–Њ—В–µ–Є–љ–Њ–≤). –≠—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О –≤—П–Ј–Ї–Њ—Б—В–Є –Љ–Њ–Ї—А–Њ—В—Л –Є –µ–µ –Ј–∞—Б—В–Њ—О –≤ –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В—П—Е. –£—Е—Г–і—И–µ–љ–Є—О –Љ—Г–Ї–Њ—Ж–Є–ї–Є–∞—А–љ–Њ–≥–Њ –Ї–ї–Є—А–µ–љ—Б–∞ –њ—А–Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є–Є —В–∞–Ї–ґ–µ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—В —Б—В—А—Г–Ї—В—Г—А–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤ –Ї–ї–µ—В–Ї–∞—Е –Љ–µ—А—Ж–∞—В–µ–ї—М–љ–Њ–≥–Њ —Н–њ–Є—В–µ–ї–Є—П (–љ–∞—А—Г—И–µ–љ–Є–µ —Г–ї—М—В—А–∞—Б—В—А—Г–Ї—В—Г—А—Л —А–µ—Б–љ–Є—З–µ–Ї –Є –Є—Е –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–µ–љ–љ–Њ–є –Њ—А–Є–µ–љ—В–∞—Ж–Є–Є, –і–µ—Б—В—А—Г–Ї—Ж–Є—П –Ї–ї–µ—В–Њ—З–љ—Л—Е –Њ—А–≥–∞–љ–µ–ї–ї –Є –і—А.). –Я—А–Є —В–∞–Ї–Є—Е —Г—Б–ї–Њ–≤–Є—П—Е –Є–Љ–µ–љ–љ–Њ –Ї–∞—И–µ–ї—М —П–≤–ї—П–µ—В—Б—П –Ї–Њ–Љ–њ–µ–љ—Б–∞—В–Њ—А–љ—Л–Љ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–Љ –Њ—З–Є—Й–µ–љ–Є—П –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є.
–Ь–µ—Е–∞–љ–Є–Ј–Љ —А–∞–Ј–≤–Є—В–Є—П –Ї–∞—И–ї—П —Б–≤—П–Ј–∞–љ —Б —А–∞–Ј–і—А–∞–ґ–µ–љ–Є–µ–Љ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –±–ї—Г–ґ–і–∞—О—Й–µ–≥–Њ –љ–µ—А–≤–∞, —Б–Ї–Њ–љ—Ж–µ–љ—В—А–Є—А–Њ–≤–∞–љ–љ—Л—Е –≤ –Њ–±–ї–∞—Б—В–Є —А–µ—Д–ї–µ–Ї—Б–Њ–≥–µ–љ–љ—Л—Е –Ј–Њ–љ, –Ї –Ї–Њ—В–Њ—А—Л–Љ –Њ—В–љ–Њ—Б—П—В—Б—П —Б–ї–Є–Ј–Є—Б—В–∞—П –Њ–±–Њ–ї–Њ—З–Ї–∞ –≥–Њ—А—В–∞–љ–Є, –±–Є—Д—Г—А–Ї–∞—Ж–Є—П —В—А–∞—Е–µ–Є, –Ї—А—Г–њ–љ—Л–µ –±—А–Њ–љ—Е–Є. –Я—А–Є —Н—В–Њ–Љ –Є–Љ–µ–µ—В –Ј–љ–∞—З–µ–љ–Є–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –Ї–∞–Ї –љ–∞ «–±—Л—Б—В—А—Л–µ» –Є–ї–Є –Є—А—А–Є—В–∞—В–Є–≤–љ—Л–µ —А–µ—Ж–µ–њ—В–Њ—А—Л –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Є—Е –Є —Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е —А–∞–Ј–і—А–∞–ґ–Є—В–µ–ї–µ–є, —В–∞–Ї –Є –љ–∞ «–Љ–µ–і–ї–µ–љ–љ—Л–µ» –°-—А–µ—Ж–µ–њ—В–Њ—А—Л –Љ–µ–і–Є–∞—В–Њ—А–Њ–≤ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П [2]. –°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –≤ –±—А–Њ–љ—Е–∞—Е —Г–±—Л–≤–∞–µ—В –њ–Њ –Љ–µ—А–µ —Г–Љ–µ–љ—М—И–µ–љ–Є—П –Є—Е –і–Є–∞–Љ–µ—В—А–∞. –Т —В–µ—А–Љ–Є–љ–∞–ї—М–љ—Л—Е –±—А–Њ–љ—Е–∞—Е –Ї–∞—И–ї–µ–≤—Л–µ —А–µ—Ж–µ–њ—В–Њ—А—Л –Њ—В—Б—Г—В—Б—В–≤—Г—О—В, —З—В–Њ –Њ–±—К—П—Б–љ—П–µ—В –њ—А–Є—З–Є–љ—Г –Њ—В—Б—Г—В—Б—В–≤–Є—П –Ї–∞—И–ї—П –њ—А–Є –Є—Е –Є–Ј–±–Є—А–∞—В–µ–ї—М–љ–Њ–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–Є –њ—А–Є –љ–∞–ї–Є—З–Є–Є —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –і—Л—Е–∞—В–µ–ї—М–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є [3]. –Ъ–∞—И–µ–ї—М –Љ–Њ–ґ–µ—В –±—Л—В—М —В–∞–Ї–ґ–µ –≤—Л–Ј–≤–∞–љ —А–∞–Ј–і—А–∞–ґ–µ–љ–Є–µ–Љ —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, —Б–Ї–Њ–љ—Ж–µ–љ—В—А–Є—А–Њ–≤–∞–љ–љ—Л—Е –≤ –Њ–±–ї–∞—Б—В–Є –љ–∞—А—Г–ґ–љ–Њ–≥–Њ —Б–ї—Г—Е–Њ–≤–Њ–≥–Њ –њ—А–Њ—Е–Њ–і–∞, —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –њ—А–Є–і–∞—В–Њ—З–љ—Л—Е –њ–∞–Ј—Г—Е –љ–Њ—Б–∞ –Є –≥–ї–Њ—В–Ї–Є, –∞ —В–∞–Ї–ґ–µ —А–µ—Д–ї–µ–Ї—Б–Њ–≥–µ–љ–љ—Л—Е –Ј–Њ–љ, —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ—Л—Е –љ–∞ –њ–ї–µ–≤—А–µ, –њ–∞—А–Є–µ—В–∞–ї—М–љ–Њ–є –±—А—О—И–Є–љ–µ, –і–Є–∞—Д—А–∞–≥–Љ–µ, –њ–µ—А–Є–Ї–∞—А–і–µ. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –≤—А–∞—З-–њ–µ–і–Є–∞—В—А –љ–µ –і–Њ–ї–ґ–µ–љ –Ј–∞–±—Л–≤–∞—В—М –Њ —В–Њ–Љ, —З—В–Њ –Ї–∞—И–µ–ї—М –Љ–Њ–ґ–µ—В —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—В—М –Є –і—А—Г–≥–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є –њ–∞—В–Њ–ї–Њ–≥–Є—О —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л, –ґ–µ–ї—Г–і–Њ—З–љ–Њ-–Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞, –¶–Э–° –Є –і—А.
–Ъ–∞—И–µ–ї—М – —З–∞—Б—В—Л–є –Є –≤ –њ–Њ–і–∞–≤–ї—П—О—Й–µ–Љ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –Њ–±—П–Ј–∞—В–µ–ї—М–љ—Л–є —Б–Є–Љ–њ—В–Њ–Љ –њ—А–Є —А–∞–Ј–ї–Є—З–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –Њ—А–≥–∞–љ–Њ–≤ –і—Л—Е–∞–љ–Є—П. –Ю–і–љ–∞–Ї–Њ —В–Њ–ї—М–Ї–Њ –Ї–Њ–љ—Б—В–∞—В–∞—Ж–Є—П —Б–Є–Љ–њ—В–Њ–Љ–∞ –Ї–∞—И–ї—П –љ–µ –Є–Љ–µ–µ—В —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ–≥–Њ –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ј–љ–∞—З–µ–љ–Є—П. –Ю–±—П–Ј–∞—В–µ–ї—М–љ–∞ –њ–Њ–і—А–Њ–±–љ–∞—П —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–∞ –Ї–∞—И–ї—П —Б —Г–Ї–∞–Ј–∞–љ–Є–µ–Љ —З–∞—Б—В–Њ—В—Л, –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є, —В–µ–Љ–±—А–∞, –њ–µ—А–Є–Њ–і–Є—З–љ–Њ—Б—В–Є, –љ–∞–ї–Є—З–Є—П –Є —Б–≤–Њ–є—Б—В–≤ –Љ–Њ–Ї—А–Њ—В—Л –Є –і—А. –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є. –Ґ–∞–Ї–Њ–є –і–µ—В–∞–ї—М–љ—Л–є –∞–љ–∞–ї–Є–Ј –њ–Њ–Ј–≤–Њ–ї—П–µ—В –≤—Л—П–≤–Є—В—М —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–µ —З–µ—А—В—Л –Ї–∞—И–ї—П, —Е–∞—А–∞–Ї—В–µ—А–љ—Л–µ –і–ї—П –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Є –Њ–њ—А–µ–і–µ–ї–Є—В—М —В–∞–Ї—В–Є–Ї—Г –ї–µ—З–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–∞ [4].
–Т –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –≥–ї—Г–±–Є–љ—Л –Є —Б–Є–ї—Л –Ї–∞—И–ї—П —А–∞–Ј–ї–Є—З–∞—О—В –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –Ї–∞—И–µ–ї—М –Є –њ–Њ–Ї–∞—И–ї–Є–≤–∞–љ–Є–µ (—Б–ї–∞–±—Л–є, –Ї–Њ—А–Њ—В–Ї–Є–є –Є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ—Л–є –Ї–∞—И–µ–ї—М). –Я–Њ–Ї–∞—И–ї–Є–≤–∞–љ–Є–µ —Е–∞—А–∞–Ї—В–µ—А–љ–Њ, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –і–ї—П —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –љ–Њ—Б–Њ–≥–ї–Њ—В–Ї–Є (—А–Є–љ–Є—В, –∞–і–µ–љ–Њ–Є–і–Є—В, —Д–∞—А–Є–љ–≥–Є—В), –љ–∞—З–∞–ї—М–љ–Њ–є —Б—В–∞–і–Є–Є —В—Г–±–µ—А–Ї—Г–ї–µ–Ј–∞ –ї–µ–≥–Ї–Є—Е, –њ–ї–µ–≤—А–Є—В–∞.
–Т –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —В–µ–Љ–±—А–∞ –Є —В–Њ–љ–∞–ї—М–љ–Њ—Б—В–Є –Ї–∞—И–ї—П —А–∞–Ј–ї–Є—З–∞—О—В —Б–ї–µ–і—Г—О—Й–Є–µ –µ–≥–Њ —А–∞–Ј–љ–Њ–≤–Є–і–љ–Њ—Б—В–Є: «–ї–∞—О—Й–Є–є», «—Е—А–Є–њ–ї—Л–є», –±–Є—В–Њ–љ–∞–ї—М–љ—Л–є, –≤–Є–±—А–Є—А—Г—О—Й–Є–є, –∞—Д–Њ–љ–Є—З–µ—Б–Ї–Є–є (–±–µ–Ј–Ј–≤—Г—З–љ—Л–є), –њ—А–Є —Н—В–Њ–Љ –Ј–≤—Г–Ї–Њ–≤—Л–µ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –Є–Љ–µ—О—В –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Г—О –љ–Њ–Ј–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О —Б–њ–µ—Ж–Є—Д–Є—З–љ–Њ—Б—В—М (—В–∞–±–ї. 1).
–Ю–і–љ–Њ–є –Є–Ј –≤–∞–ґ–љ—Л—Е —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї –Ї–∞—И–ї—П —П–≤–ї—П–µ—В—Б—П –µ–≥–Њ –њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ—Б—В—М. –Т –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –Є –Ї–∞—З–µ—Б—В–≤–∞ –Њ–±—А–∞–Ј—Г—О—Й–µ–є—Б—П –≤ –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В—П—Е –Љ–Њ–Ї—А–Њ—В—Л —А–∞–Ј–ї–Є—З–∞—О—В —Б—Г—Е–Њ–є –Є –≤–ї–∞–ґ–љ—Л–є –Ї–∞—И–µ–ї—М. –Я—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ—Б—В—М –Ї–∞—И–ї—П –Ј–∞–≤–Є—Б–Є—В –Ї–∞–Ї –Њ—В —Е–∞—А–∞–Ї—В–µ—А–∞ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, —В–∞–Ї –Є –Њ—В —Д–∞–Ј—Л –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ (—В–∞–±–ї. 2).
–Ъ–∞—И–µ–ї—М –Љ–Њ–ґ–µ—В –±—Л—В—М –њ—А–Њ—П–≤–ї–µ–љ–Є–µ–Љ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –Ї–∞–Ї –≤ –≤–µ—А—Е–љ–Є—Е (—А–Њ—В–Њ-–љ–Њ—Б–Њ–≥–ї–Њ—В–Ї–∞, –≥–Њ—А—В–∞–љ—М), —В–∞–Ї –Є –љ–Є–ґ–љ–Є—Е (—В—А–∞—Е–µ—П, –±—А–Њ–љ—Е–Є) –Њ—В–і–µ–ї–∞—Е —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞.
–І–∞—Б—В–Њ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –Ї–∞—И–ї—П —Г –і–µ—В–µ–є —Б–≤—П–Ј–∞–љ–Њ —Б –Њ—Б—В—А—Л–Љ —А–Є–љ–Є—В–Њ–Љ –Є–ї–Є –љ–∞–Ј–Њ—Д–∞—А–Є–љ–≥–Є—В–Њ–Љ. –Т —Б–≤—П–Ј–Є —Б –Ј–∞–ї–Њ–ґ–µ–љ–љ–Њ—Б—В—М—О –љ–Њ—Б–∞ –њ—А–Є —Н—В–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –і—Л—Е–∞–љ–Є–µ –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–µ—В—Б—П –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —З–µ—А–µ–Ј —А–Њ—В, —З—В–Њ –≤–µ–і–µ—В –Ї –њ–Њ–і—Б—Г—И–Є–≤–∞–љ–Є—О —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –≤–µ—А—Е–љ–Є—Е –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є, —З—В–Њ, –љ–∞—А—П–і—Г —Б–Њ —Б—В–µ–Ї–∞–љ–Є–µ–Љ —Б–ї–Є–Ј–Є –њ–Њ –Ј–∞–і–љ–µ–є —Б—В–µ–љ–Ї–µ –≥–ї–Њ—В–Ї–Є, –њ—А–Є–≤–Њ–і–Є—В –Ї –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—О –Ї–∞—И–ї—П. –£—Б–Є–ї–µ–љ–Є–µ –Ї–∞—И–ї—П –Њ–±—Л—З–љ–Њ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –љ–Њ—З—М—О –Є —Г—В—А–Њ–Љ. –Я—А–Є –ї–∞—А–Є–љ–≥–Є—В–µ, –Є—Б—В–Є–љ–љ–Њ–Љ –Є –ї–Њ–ґ–љ–Њ–Љ –Ї—А—Г–њ–µ –Ї–∞—И–µ–ї—М –Љ–Њ–ґ–µ—В –±—Л—В—М –Њ–і–љ–Є–Љ –Є–Ј –њ–µ—А–≤—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –і–∞–љ–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є. –Я—А–Є —Н—В–Њ–Љ –Њ–љ –Њ–±—Л—З–љ–Њ —Б—Г—Е–Њ–є –Є –≥—А—Г–±—Л–є («–ї–∞—О—Й–Є–є»), —З–∞—Б—В–Њ —Б–Њ—З–µ—В–∞–µ—В—Б—П —Б –∞—Д–Њ–љ–Є–µ–є –Є –Њ—Е—А–Є–њ–ї–Њ—Б—В—М—О –≥–Њ–ї–Њ—Б–∞ –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –Њ—В–µ–Ї–∞ –≥–Њ–ї–Њ—Б–Њ–≤—Л—Е —Б–≤—П–Ј–Њ–Ї –Є —Б–ї–Є–Ј–Є—Б—В–Њ–є –≥–Њ—А—В–∞–љ–Є. –Р—Г—Б–Ї—Г–ї—М—В–∞—В–Є–≤–љ–∞—П –Ї–∞—А—В–Є–љ–∞ –њ—А–Є –њ–Њ—А–∞–ґ–µ–љ–Є–Є –≤–µ—А—Е–љ–Є—Е –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –њ–Њ—П–≤–ї–µ–љ–Є–µ–Љ –ґ–µ—Б—В–Ї–Њ–≥–Њ –і—Л—Е–∞–љ–Є—П –Є —З–∞—Б—В–Њ —Е—А–Є–њ–Њ–≤ –њ—А–Њ–≤–Њ–і–љ–Њ–≥–Њ —Е–∞—А–∞–Ї—В–µ—А–∞, –Є—Б—З–µ–Ј–∞—О—Й–Є—Е –њ–Њ –Љ–µ—А–µ —Б—В–Є—Е–∞–љ–Є—П –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П.
–Я—А–Є –±—А–Њ–љ—Е–Є—В–∞—Е –Ї–∞—И–µ–ї—М –Љ–Њ–ґ–µ—В –±—Л—В—М —А–∞–Ј–ї–Є—З–љ—Л–Љ –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Е–∞—А–∞–Ї—В–µ—А–∞ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –Є —Б—В–∞–і–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Т –і–µ–±—О—В–µ –Њ—Б—В—А–Њ–≥–Њ –±—А–Њ–љ—Е–Є—В–∞ —З–∞—Й–µ –Њ—В–Љ–µ—З–∞–µ—В—Б—П —Б—Г—Е–Њ–є –Љ–∞–ї–Њ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ—Л–є –Ї–∞—И–µ–ї—М —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–є –µ–≥–Њ —В—А–∞–љ—Б—Д–Њ—А–Љ–∞—Ж–Є–µ–є –≤ –±–Њ–ї–µ–µ –≤–ї–∞–ґ–љ—Л–є, –≥–ї—Г–±–Њ–Ї–Є–є. –Я—А–Є —Н—В–Њ–Љ, –µ—Б–ї–Є –≤ –њ–µ—А–≤—Л–µ –і–љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –∞—Г—Б–Ї—Г–ї—М—В–∞—В–Є–≤–љ–∞—П –Ї–∞—А—В–Є–љ–∞ –≤ –ї–µ–≥–Ї–Є—Е —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є–µ–Љ —Б—Г—Е–Є—Е —А–∞—Б—Б–µ—П–љ–љ—Л—Е —Е—А–Є–њ–Њ–≤, —В–Њ –њ–Њ –Љ–µ—А–µ –њ–Њ—П–≤–ї–µ–љ–Є—П –Љ–Њ–Ї—А–Њ—В—Л –≤ –ї–µ–≥–Ї–Є—Е –љ–∞—З–Є–љ–∞—О—В –≤—Л—Б–ї—Г—И–Є–≤–∞—В—М—Б—П —А–∞–Ј–љ–Њ–Ї–∞–ї–Є–±–µ—А–љ—Л–µ –≤–ї–∞–ґ–љ—Л–µ —Е—А–Є–њ—Л, —Г–Љ–µ–љ—М—И–∞—О—Й–Є–µ—Б—П –Є–ї–Є –Є—Б—З–µ–Ј–∞—О—Й–Є–µ –њ—А–Є –Њ—В–Ї–∞—И–ї–Є–≤–∞–љ–Є–Є. –Я—А–Є —А–∞–Ј–≤–Є—В–Є–Є –Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ–Њ–≥–Њ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞ –Ј–∞ —Б—З–µ—В —Б—Г–ґ–µ–љ–Є—П –њ—А–Њ—Б–≤–µ—В–∞ –±—А–Њ–љ—Е–Њ–≤ –њ–Њ—П–≤–ї—П—О—В—Б—П —Б—Г—Е–Є–µ —Б–≤–Є—Б—В—П—Й–Є–µ —Е—А–Є–њ—Л. –Ъ–∞—И–µ–ї—М —Б—В–∞–љ–Њ–≤–Є—В—Б—П –њ—А–Є—Б—В—Г–њ–Њ–Њ–±—А–∞–Ј–љ—Л–Љ, —Б—Г—Е–Є–Љ, –љ–∞–≤—П–Ј—З–Є–≤—Л–Љ. –Т –і–µ–±—О—В–µ –њ–љ–µ–≤–Љ–Њ–љ–Є–Є, –Ї–Њ–≥–і–∞ –Њ—Б–љ–Њ–≤–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –њ—А–Њ—Ж–µ—Б—Б –ї–Њ–Ї–∞–ї–Є–Ј—Г–µ—В—Б—П –≤ –∞–ї—М–≤–µ–Њ–ї–∞—Е, –Ї–∞—И–µ–ї—М –Њ–±—Л—З–љ–Њ –љ–µ —П–≤–ї—П–µ—В—Б—П –Њ—Б–љ–Њ–≤–љ—Л–Љ —Б–Є–Љ–њ—В–Њ–Љ–Њ–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є –Њ—В–Љ–µ—З–∞–µ—В—Б—П –љ–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–µ –њ–Њ–Ї–∞—И–ї–Є–≤–∞–љ–Є–µ. –Т –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –Њ–±—К–µ–Љ–∞ –њ–Њ—А–∞–ґ–µ–љ–Є—П –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ–µ –≤ –њ–µ—А–≤—Л–µ –і–љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Љ–Њ–ґ–µ—В –і–Њ–Љ–Є–љ–Є—А–Њ–≤–∞—В—М –і—Л—Е–∞—В–µ–ї—М–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ–Є —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ–Є –Є–љ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–Є –Є —Е–∞—А–∞–Ї—В–µ—А–љ—Л–Љ–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ–Є, –≤—Л—П–≤–ї—П–µ–Љ—Л–Љ–Є –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –∞—Г—Б–Ї—Г–ї—М—В–∞—Ж–Є–Є –Є –њ–µ—А–Ї—Г—Б—Б–Є–Є –ї–µ–≥–Ї–Є—Е – –ї–Њ–Ї–∞–ї—М–љ–Њ–µ –Њ—Б–ї–∞–±–ї–µ–љ–Є–µ –ї–µ–≥–Њ—З–љ–Њ–≥–Њ –і—Л—Е–∞–љ–Є—П —Б –љ–∞–ї–Є—З–Є–µ–Љ –Ї—А–µ–њ–Є—В–Є—А—Г—О—Й–Є—Е —Е—А–Є–њ–Њ–≤, –њ—А–Є—В—Г–њ–ї–µ–љ–Є–µ –њ–µ—А–Ї—Г—В–Њ—А–љ–Њ–≥–Њ –Ј–≤—Г–Ї–∞ –љ–∞–і –Њ–±–ї–∞—Б—В—М—О –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П. –°—Г—Е–Њ–є –љ–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ—Л–є –Ї–∞—И–µ–ї—М, –≤–Њ–Ј–љ–Є–Ї–∞—О—Й–Є–є –љ–∞ –≥–ї—Г–±–Њ–Ї–Њ–Љ –≤–і–Њ—Е–µ, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–Є–є—Б—П –±–Њ–ї—М—О –≤ –Њ–±–ї–∞—Б—В–Є –≥—А—Г–і–љ–Њ–є –Ї–ї–µ—В–Ї–Є, —В–Є–њ–Є—З–µ–љ –і–ї—П –њ–ї–µ–≤—А–Є—В–∞.
–°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –њ–Њ—А–∞–ґ–µ–љ–Є–µ –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–≥–Њ —Е–∞—А–∞–Ї—В–µ—А–∞ —З–∞—Й–µ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –њ–Њ—П–≤–ї–µ–љ–Є–µ–Љ –Њ—Б—В—А–Њ–≥–Њ –Ї–∞—И–ї—П, –њ—А–Њ–і–Њ–ї–ґ–∞—О—Й–µ–≥–Њ—Б—П –љ–µ –±–Њ–ї–µ–µ 3 –Љ–µ—Б. –Я—А–Є —Н—В–Њ–Љ –њ—А–Є —А—П–і–µ –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –љ–∞–±–ї—О–і–∞–µ—В—Б—П –Ј–∞—В—П–ґ–љ–Њ–є (–±–Њ–ї–µ–µ 2 –љ–µ–і.) –Ї–∞—И–µ–ї—М. –Ґ–∞–Ї, –њ—А–Є—Б—В—Г–њ–Њ–Њ–±—А–∞–Ј–љ—Л–є –Є–Ј–љ—Г—А—П—О—Й–Є–є –Ї–∞—И–µ–ї—М —Г –і–µ—В–µ–є, –Њ—Б–Њ–±–µ–љ–љ–Њ –њ–µ—А–≤–Њ–≥–Њ –≥–Њ–і–∞ –ґ–Є–Ј–љ–Є, —Е–∞—А–∞–Ї—В–µ—А–µ–љ –і–ї—П –Ї–Њ–Ї–ї—О—И–∞. –Т —Н—В–Њ–Љ —Б–ї—Г—З–∞–µ –Њ–љ –њ–Њ—Б—В–µ–њ–µ–љ–љ–Њ —Г—Б–Є–ї–Є–≤–∞–µ—В—Б—П, –њ—А–Є–Њ–±—А–µ—В–∞—П —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–є —Б–њ–∞–Ј–Љ–∞—В–Є—З–µ—Б–Ї–Є–є —Е–∞—А–∞–Ї—В–µ—А, —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—Й–Є–є—Б—П –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ–Љ —Б–µ—А–Є–є –Ї–∞—И–ї–µ–≤—Л—Е —В–Њ–ї—З–Ї–Њ–≤, –±—Л—Б—В—А–Њ —Б–ї–µ–і—Г—О—Й–Є—Е –љ–∞ –≤—Л–і–Њ—Е–µ –і—А—Г–≥ –Ј–∞ –і—А—Г–≥–Њ–Љ. –Т—Б–ї–µ–і –Ј–∞ –Ї–∞—И–ї–µ–≤—Л–Љ–Є —В–Њ–ї—З–Ї–∞–Љ–Є –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –≥–ї—Г–±–Њ–Ї–Є–є —Б—Г–і–Њ—А–Њ–ґ–љ—Л–є —Б–≤–Є—Б—В—П—Й–Є–є –≤–і–Њ—Е, –Ј–∞ –Ї–Њ—В–Њ—А—Л–Љ —Б–љ–Њ–≤–∞ —Б–ї–µ–і—Г—О—В –≤—Л–і—Л—Е–∞—В–µ–ї—М–љ—Л–µ —В–Њ–ї—З–Ї–Є, –∞ –Ј–∞—В–µ–Љ –≤–љ–Њ–≤—М —Б—Г–і–Њ—А–Њ–ґ–љ—Л–є –≤–і–Њ—Е –Є —В.–і. –Ф–ї–Є—В–µ–ї—М–љ—Л–є —Б—Г—Е–Њ–є –Ї–∞—И–µ–ї—М, —З–∞—Б—В–Њ –Њ–њ—А–µ–і–µ–ї—П–µ–Љ—Л–є –Ї–∞–Ї –Ї–∞—И–µ–ї—М «—Б—В–∞–Ї–Ї–∞—В–Њ» – –Њ—В—А—Л–≤–Є—Б—В—Л–є, –Ј–≤–Њ–љ–Ї–Є–є, —Б–ї–µ–і—Г—О—Й–Є–є –њ—А–Є—Б—В—Г–њ–∞–Љ–Є, –љ–Њ –±–µ–Ј —А–µ–њ—А–Є–Ј – –Љ–Њ–ґ–µ—В –љ–∞–±–ї—О–і–∞—В—М—Б—П –њ—А–Є —Е–ї–∞–Љ–Є–і–Є–є–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є.
–Ч–∞—В—П–ґ–љ–Њ–є –Ї–∞—И–µ–ї—М –љ–µ—А–µ–і–Ї–Њ –≤—Л–Ј—Л–≤–∞–µ—В—Б—П –Ј–∞—В–µ–Ї–∞–љ–Є–µ–Љ —Б–ї–Є–Ј–Є –≤ –≥–Њ—А—В–∞–љ—М –Є–Ј –љ–Њ—Б–Њ–≥–ї–Њ—В–Ї–Є –њ—А–Є —А–∞–Ј–≤–Є—В–Є–Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –≤ –њ—А–Є–і–∞—В–Њ—З–љ—Л—Е –њ–∞–Ј—Г—Е–∞—Е –љ–Њ—Б–∞, –і–ї–Є—В–µ–ї—М–љ–Њ —В–µ–Ї—Г—Й–µ–Љ –љ–∞–Ј–Њ—Д–∞—А–Є–љ–≥–Є—В–µ, –∞–і–µ–љ–Њ–Є–і–Є—В–µ, –≥–Є–њ–µ—А—В—А–Њ—Д–Є–Є –∞–і–µ–љ–Њ–Є–і–Њ–≤. –Ю—В–ї–Є—З–Є—В–µ–ї—М–љ–Њ–є –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—М—О –Ї–∞—И–ї—П –≤ –і–∞–љ–љ–Њ–Љ —Б–ї—Г—З–∞–µ —П–≤–ї—П–µ—В—Б—П –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–µ –µ–≥–Њ –њ–Њ—П–≤–ї–µ–љ–Є–µ –≤ –љ–Њ—З–љ–Њ–µ –≤—А–µ–Љ—П.
–Ф–ї–Є—В–µ–ї—М–љ—Л–є –њ–Њ—Б—В–Њ—П–љ–љ—Л–є –Ї–∞—И–µ–ї—М (–±–Њ–ї–µ–µ 3 –Љ–µ—Б.) –љ–∞–±–ї—О–і–∞–µ—В—Б—П –њ—А–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –Њ—А–≥–∞–љ–Њ–≤ –і—Л—Е–∞–љ–Є—П. –Ґ–∞–Ї, –њ—А–Є –ї–µ–≥–Њ—З–љ–Њ–є —Д–Њ—А–Љ–µ –Љ—Г–Ї–Њ–≤–Є—Б—Ж–Є–і–Њ–Ј–∞ –Ї–∞—И–µ–ї—М —П–≤–ї—П–µ—В—Б—П –Њ–і–љ–Є–Љ –Є–Ј –Њ—Б–љ–Њ–≤–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Я—А–Є —Н—В–Њ–Љ —Е–∞—А–∞–Ї—В–µ—А –Ї–∞—И–ї—П –Љ–µ–љ—П–µ—В—Б—П –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Б—В–∞–і–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є —Б—В–µ–њ–µ–љ–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П –±—А–Њ–љ—Е–Њ–ї–µ–≥–Њ—З–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л. –Т –љ–∞—З–∞–ї—М–љ–Њ–є —Б—В–∞–і–Є–Є –Љ—Г–Ї–Њ–≤–Є—Б—Ж–Є–і–Њ–Ј–∞ —Б –Љ–Є–љ–Є–Љ–∞–ї—М–љ—Л–Љ–Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є –Ї–∞—И–µ–ї—М –љ–µ–њ–Њ—Б—В–Њ—П–љ–љ—Л–є, –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –њ–Њ —Г—В—А–∞–Љ, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –Њ—В—Е–Њ–ґ–і–µ–љ–Є–µ–Љ –љ–µ–±–Њ–ї—М—И–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –Љ–Њ–Ї—А–Њ—В—Л. –Ю–і–љ–∞–Ї–Њ —З—А–µ–Ј–Љ–µ—А–љ–∞—П –≤—П–Ј–Ї–Њ—Б—В—М –Љ–Њ–Ї—А–Њ—В—Л –Ј–∞—В—А—Г–і–љ—П–µ—В –µ–µ —Н–≤–∞–Ї—Г–∞—Ж–Є—О –Є –њ—А–Є–≤–Њ–і–Є—В –Ї –±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–Љ—Г –Ј–∞—Б–µ–ї–µ–љ–Є—О –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ –і–µ—А–µ–≤–∞, —А–∞–Ј–≤–Є—В–Є—О –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П —Б –Ј–∞–Ї–Њ–љ–Њ–Љ–µ—А–љ—Л–Љ –Њ—В–µ–Ї–Њ–Љ –Є –Є–љ—Д–Є–ї—М—В—А–∞—Ж–Є–µ–є —Б—В–µ–љ–Ї–Є –±—А–Њ–љ—Е–Њ–≤. –Ъ–∞—И–µ–ї—М –њ—А–Є —Н—В–Њ–Љ —Б—В–∞–љ–Њ–≤–Є—В—Б—П –њ–Њ—Б—В–Њ—П–љ–љ—Л–Љ, –Љ—Г—З–Є—В–µ–ї—М–љ—Л–Љ, –њ—А–Є—Б—В—Г–њ–Њ–Њ–±—А–∞–Ј–љ—Л–Љ –Є –Љ–∞–ї–Њ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ—Л–Љ. –Я—А–Є—Б—В—Г–њ—Л –Ї–∞—И–ї—П —Б —В—А—Г–і–љ–Њ–Њ—В–і–µ–ї—П–µ–Љ–Њ–є –≤—П–Ј–Ї–Њ–є, –≥—Г—Б—В–Њ–є, —Б–ї–Є–Ј–Є—Б—В–Њ-–≥–љ–Њ–є–љ–Њ–є –Љ–Њ–Ї—А–Њ—В–Њ–є –Њ–±—Л—З–љ–Њ –≤–Њ–Ј–љ–Є–Ї–∞—О—В –њ–Њ —Г—В—А–∞–Љ –Є –њ—А–Є —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –љ–∞–≥—А—Г–Ј–Ї–µ.
–Ъ–∞—И–µ–ї—М —П–≤–ї—П–µ—В—Б—П –Њ–і–љ–Є–Љ –Є–Ј –њ–Њ—Б—В–Њ—П–љ–љ—Л—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –њ–Њ—А–Њ–Ї–Њ–≤ —А–∞–Ј–≤–Є—В–Є—П —В—А–∞—Е–µ–Є –Є –±—А–Њ–љ—Е–Њ–≤. –Ъ –≥—А—Г–њ–њ–µ —В–∞–Ї–Є—Е –њ–Њ—А–Њ–Ї–Њ–≤ –Њ—В–љ–Њ—Б—П—В—Б—П —Б–Є–љ–і—А–Њ–Љ –Ь—Г–љ—М–µ-–Ъ—Г–љ–∞ (—В—А–∞—Е–µ–Њ–±—А–Њ–љ—Е–Њ–і–Є–ї–∞—В–∞—Ж–Є—П), —В—А–∞—Е–µ–Њ–±—А–Њ–љ—Е–Њ–Љ–∞–ї—П—Ж–Є—П, —Б–Є–љ–і—А–Њ–Љ –Т–Є–ї—М—П–Љ—Б–∞––Ъ–µ–Љ–њ–±–µ–ї–∞ –Є –і—А.
–Я—А–Є —Б–Є–љ–і—А–Њ–Љ–µ –Ь—Г–љ—М–µ-–Ъ—Г–љ–∞ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ —А–∞—Б—И–Є—А–µ–љ–Є–µ –њ—А–Њ—Б–≤–µ—В–∞ —В—А–∞—Е–µ–Є –Є –±—А–Њ–љ—Е–Њ–≤ –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –≤—А–Њ–ґ–і–µ–љ–љ–Њ–є –∞–љ–Њ–Љ–∞–ї–Є–Є –Љ—Л—И–µ—З–љ–Њ–є –Є —Н–ї–∞—Б—В–Є—З–љ–Њ–є —В–Ї–∞–љ–Є. –£ –і–µ—В–µ–є —Б —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –Ь—Г–љ—М–µ-–Ъ—Г–љ–∞ –љ–∞–±–ї—О–і–∞–µ—В—Б—П –њ–Њ—Б—В–Њ—П–љ–љ—Л–є –≤–ї–∞–ґ–љ—Л–є –Ї–∞—И–µ–ї—М —Б –≤—Л–і–µ–ї–µ–љ–Є–µ–Љ –±–Њ–ї—М—И–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ —Б–ї–Є–Ј–Є—Б—В–Њ-–≥–љ–Њ–є–љ–Њ–є –Є–ї–Є –≥–љ–Њ–є–љ–Њ–є –Љ–Њ–Ї—А–Њ—В—Л. –Ш–љ–Њ–≥–і–∞ –Ї–∞—И–µ–ї—М –≤–Є–±—А–Є—А—Г—О—Й–Є–є, —З—В–Њ —Б—З–Є—В–∞–µ—В—Б—П —В–Є–њ–Є—З–љ—Л–Љ –і–ї—П —Н—В–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞.
–Я—А–Є —В—А–∞—Е–µ–Њ–±—А–Њ–љ—Е–Њ–Љ–∞–ї—П—Ж–Є–Є –Є –±—А–Њ–љ—Е–Њ–Љ–∞–ї—П—Ж–Є–Є – –≤—А–Њ–ґ–і–µ–љ–љ–Њ–є —Б–ї–∞–±–Њ—Б—В–Є —Б—В–µ–љ–Њ–Ї —В—А–∞—Е–µ–Є –Є–ї–Є –Ї—А—Г–њ–љ—Л—Е –±—А–Њ–љ—Е–Њ–≤, —Б–≤—П–Ј–∞–љ–љ–Њ–є —Б –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –Љ—П–≥–Ї–Њ—Б—В—М—О –Є—Е —Е—А—П—Й–µ–≤–Њ–≥–Њ –Ї–∞—А–Ї–∞—Б–∞, – –Њ—В–Љ–µ—З–∞—О—В—Б—П —Б–Є–Љ–њ—В–Њ–Љ—Л —В—П–ґ–µ–ї–Њ–≥–Њ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ–≥–Њ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –±—А–Њ–љ—Е–Є—В–∞ —Б –њ–Њ—Б—В–Њ—П–љ–љ—Л–Љ –≤–ї–∞–ґ–љ—Л–Љ –Ї–∞—И–ї–µ–Љ.
–Ф–ї—П —Б–Є–љ–і—А–Њ–Љ–∞ –Ъ–∞—А—В–∞–≥–µ–љ–µ—А–∞ – –≤—А–Њ–ґ–і–µ–љ–љ–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—Й–µ–≥–Њ—Б—П –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л–Љ–Є –њ–Њ—А–Њ–Ї–∞–Љ–Є –≤–љ—Г—В—А–µ–љ–љ–Є—Е –Њ—А–≥–∞–љ–Њ–≤ –Є —З–∞—Б—В—Л–Љ –Є—Е –Њ–±—А–∞—В–љ—Л–Љ —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–Є–µ–Љ, – —В–∞–Ї–ґ–µ —Е–∞—А–∞–Ї—В–µ—А–љ—Л –њ—А–Є–Ј–љ–∞–Ї–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –±—А–Њ–љ—Е–Њ–ї–µ–≥–Њ—З–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л. –†–∞–Ј–≤–Є—В–Є–µ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –њ—А–Є —Н—В–Њ–Љ —Б–≤—П–Ј–∞–љ–Њ —Б –і–Є—Б—Д—Г–љ–Ї—Ж–Є–µ–є —А–µ—Б–љ–Є—В—З–∞—В–Њ–≥–Њ —Н–њ–Є—В–µ–ї–Є—П –±—А–Њ–љ—Е–Њ–≤, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї –љ–∞—А—Г—И–µ–љ–Є—О –Љ—Г–Ї–Њ—Ж–Є–ї–Є–∞—А–љ–Њ–≥–Њ –Ї–ї–Є—А–µ–љ—Б–∞. –С—А–Њ–љ—Е–Њ–ї–µ–≥–Њ—З–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –њ—А–Є —Б–Є–љ–і—А–Њ–Љ–µ –Ъ–∞—А—В–∞–≥–µ–љ–µ—А–∞ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—В—Б—П –њ–Њ—Б—В–Њ—П–љ–љ—Л–Љ –Ї–∞—И–ї–µ–Љ —Б —В—А—Г–і–љ–Њ–Њ—В–і–µ–ї—П–µ–Љ–Њ–є —Б–ї–Є–Ј–Є—Б—В–Њ–є –Є–ї–Є —Б–ї–Є–Ј–Є—Б—В–Њ-–≥–љ–Њ–є–љ–Њ–є –Љ–Њ–Ї—А–Њ—В–Њ–є.
–Ф–ї–Є—В–µ–ї—М–љ—Л–є –Ї–∞—И–µ–ї—М –Љ–Њ–ґ–µ—В –±—Л—В—М –µ–і–Є–љ—Б—В–≤–µ–љ–љ—Л–Љ —Б–Є–Љ–њ—В–Њ–Љ–Њ–Љ –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–є –∞—Б—В–Љ—Л. –Т –њ–∞—В–Њ–≥–µ–љ–µ–Ј–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –≤–µ–і—Г—Й–µ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ–µ—В —А–∞–Ј–≤–Є—В–Є–µ –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –Є, –Ї–∞–Ї —Б–ї–µ–і—Б—В–≤–Є–µ, –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –±—А–Њ–љ—Е–Њ—Б–њ–∞–Ј–Љ–∞, –Њ—В–µ–Ї–∞ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –±—А–Њ–љ—Е–Њ–≤ –Є –њ–Њ–≤—Л—И–µ–љ–љ–Њ–є –њ—А–Њ–і—Г–Ї—Ж–Є–Є –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ —Б–µ–Ї—А–µ—В–∞. –Т –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –Ї–∞—А—В–Є–љ–∞ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —В–Є–њ–Є—З–љ–∞ – –Њ–і—Л—И–Ї–∞, —Б–≤–Є—Б—В—П—Й–µ–µ –і—Л—Е–∞–љ–Є–µ, –Ї–∞—И–µ–ї—М, –њ—А–Є—Б—В—Г–њ—Л —Г–і—Г—И—М—П. –Ю–і–љ–∞–Ї–Њ –Ј–∞—В—А—Г–і–љ–µ–љ–Є–µ –≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –≤—Л–Ј—Л–≤–∞—О—В –Њ—В–і–µ–ї—М–љ—Л–µ —Б–ї—Г—З–∞–Є –∞—Б—В–Љ—Л, –Ї–Њ–≥–і–∞ –Ї–∞—И–µ–ї—М –Њ–Ї–∞–Ј—Л–≤–∞–µ—В—Б—П –і–Њ–Љ–Є–љ–Є—А—Г—О—Й–Є–Љ –Є–ї–Є –і–∞–ґ–µ –µ–і–Є–љ—Б—В–≤–µ–љ–љ—Л–Љ —Б–Є–Љ–њ—В–Њ–Љ–Њ–Љ –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–є –Њ–±—Б—В—А—Г–Ї—Ж–Є–Є [5]. –Э–µ—А–µ–і–Ї–Њ –Ї–∞—И–µ–ї—М –њ—А–Є –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–є –∞—Б—В–Љ–µ –љ–Њ—Б–Є—В –љ–Њ—З–љ–Њ–є —Е–∞—А–∞–Ї—В–µ—А, –Љ–Њ–ґ–µ—В –њ—А–Њ–≤–Њ—Ж–Є—А–Њ–≤–∞—В—М—Б—П –≥–ї—Г–±–Њ–Ї–Є–Љ –≤–і–Њ—Е–Њ–Љ, –≤–і—Л—Е–∞–љ–Є–µ–Љ —Е–Њ–ї–Њ–і–љ–Њ–≥–Њ –≤–Њ–Ј–і—Г—Е–∞, —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –љ–∞–≥—А—Г–Ј–Ї–Њ–є –≤—Б–ї–µ–і—Б—В–≤–Є–µ —А–∞–Ј–≤–Є—В–Є—П –≥–Є–њ–µ—А—А–µ–∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –±—А–Њ–љ—Е–Њ–≤.
–Я—А–Є —А–∞–Ј–і—А–∞–ґ–µ–љ–Є–Є –Њ–±–ї–∞—Б—В–Є –±–Є—Д—Г—А–Ї–∞—Ж–Є–Є —В—А–∞—Е–µ–Є —Г–≤–µ–ї–Є—З–µ–љ–љ—Л–Љ–Є –ї–Є–Љ—Д–∞—В–Є—З–µ—Б–Ї–Є–Љ–Є —Г–Ј–ї–∞–Љ–Є —Б—А–µ–і–Њ—Б—В–µ–љ–Є—П, –Њ–њ—Г—Е–Њ–ї—М—О, –∞–љ–µ–≤—А–Є–Ј–Љ–Њ–є –∞–Њ—А—В—Л –і–ї–Є—В–µ–ї—М–љ—Л–є –Ї–∞—И–µ–ї—М —З–∞—Б—В–Њ –љ–Њ—Б–Є—В –±–Є—В–Њ–љ–∞–ї—М–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А (–љ–Є–Ј–Ї–Є–є, –Ј–∞—В–µ–Љ –≤—Л—Б–Њ–Ї–Є–є —В–Њ–љ). –Я—А–Є —Н—В–Њ–Љ –њ—А–Є —Д–Є–Ј–Є–Ї–∞–ї—М–љ–Њ–Љ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Љ–Њ–≥—Г—В –Њ–њ—А–µ–і–µ–ї—П—В—М—Б—П —Б–Є–Љ–њ—В–Њ–Љ—Л –Ъ–Њ—А–∞–љ—М–Є (–њ—А–Є—В—Г–њ–ї–µ–љ–Є–µ –њ–µ—А–Ї—Г—В–Њ—А–љ–Њ–≥–Њ –Ј–≤—Г–Ї–∞ –≤ –Њ–±–ї–∞—Б—В–Є V–VI –≥—А—Г–і–љ—Л—Е –њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤ –њ—А–Є —Г–≤–µ–ї–Є—З–µ–љ–љ—Л—Е –ї–Є–Љ—Д–∞—В–Є—З–µ—Б–Ї–Є—Е —Г–Ј–ї–∞—Е –Ј–∞–і–љ–µ–≥–Њ —Б—А–µ–і–Њ—Б—В–µ–љ–Є—П), –Р—А–Ї–∞–≤–Є–љ–∞ (–њ—А–Є—В—Г–њ–ї–µ–љ–Є–µ –њ–Њ –њ–µ—А–µ–і–љ–µ–є –њ–Њ–і–Љ—Л—И–µ—З–љ–Њ–є –ї–Є–љ–Є–Є –њ—А–Є –љ–∞–ї–Є—З–Є–Є —Г–≤–µ–ї–Є—З–µ–љ–љ—Л—Е –њ—А–Є–Ї–Њ—А–љ–µ–∞–ї—М–љ—Л—Е –ї–Є–Љ—Д–∞—В–Є—З–µ—Б–Ї–Є—Е —Г–Ј–ї–Њ–≤) –Є –і—А.
–Т —Б–ї—Г—З–∞–µ –≤–љ–µ–Ј–∞–њ–љ–Њ–≥–Њ –њ–Њ—П–≤–ї–µ–љ–Є—П –њ—А–Є—Б—В—Г–њ–Њ–Њ–±—А–∞–Ј–љ–Њ–≥–Њ –Ї–Њ–Ї–ї—О—И–µ–њ–Њ–і–Њ–±–љ–Њ–≥–Њ –Ї–∞—И–ї—П, –љ–µ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–µ–≥–Њ—Б—П —А–µ–њ—А–Є–Ј–∞–Љ–Є –Є —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ–Є –Ю–†–Т–Ш, –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Є—Б–Ї–ї—О—З–µ–љ–Є–µ –∞—Б–њ–Є—А–∞—Ж–Є–Є –Є–љ–Њ—А–Њ–і–љ–Њ–≥–Њ —В–µ–ї–∞. –Т —А—П–і–µ —Б–ї—Г—З–∞–µ–≤ –і–∞–љ–љ–Њ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П —В–Є–њ–Є—З–љ–Њ–є –∞—Г—Б–Ї—Г–ї—М—В–∞—В–Є–≤–љ–Њ–є –Ї–∞—А—В–Є–љ–Њ–є, –Ї–Њ–≥–і–∞ –Њ—В–Љ–µ—З–∞–µ—В—Б—П –Њ—Б–ї–∞–±–ї–µ–љ–Є–µ –і—Л—Е–∞–љ–Є—П –љ–∞–і –Њ–і–љ–Є–Љ –ї–µ–≥–Ї–Є–Љ, —З–∞—Б—В–Њ —Б –њ–Њ—П–≤–ї–µ–љ–Є–µ–Љ —Г–і–ї–Є–љ–µ–љ–љ–Њ–≥–Њ —Б–≤–Є—Б—В—П—Й–µ–≥–Њ –≤—Л–і–Њ—Е–∞, –њ—А–Є —Н—В–Њ–Љ –Љ–Њ–ґ–µ—В –Њ—В–Љ–µ—З–∞—В—М—Б—П –Њ–і—Л—И–Ї–∞ —Б–Љ–µ—И–∞–љ–љ–Њ–≥–Њ —Е–∞—А–∞–Ї—В–µ—А–∞, —Г—Б–Є–ї–Є–≤–∞—О—Й–∞—П—Б—П –њ—А–Є –њ–µ—А–µ–Љ–µ–љ–µ –њ–Њ–ї–Њ–ґ–µ–љ–Є—П —В–µ–ї–∞. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Ї–∞—И–µ–ї—М —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –ї—О–±—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞, –њ—А–Є —Н—В–Њ–Љ —В—Й–∞—В–µ–ї—М–љ–Њ —Б–Њ–±—А–∞–љ–љ—Л–є –∞–љ–∞–Љ–љ–µ–Ј, –∞–љ–∞–ї–Є–Ј –≤—Б–µ—Е —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї –Ї–∞—И–ї—П –Є —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –±—Г–і—Г—В —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞—В—М –±–Њ–ї–µ–µ —В–Њ—З–љ–Њ–Љ—Г –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—О –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞, —З—В–Њ –њ–Њ–Љ–Њ–ґ–µ—В —Б–≤–µ—Б—В–Є –Ї –Љ–Є–љ–Є–Љ—Г–Љ—Г –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М –њ—А–Њ–≤–µ–і–µ–љ–Є—П –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л—Е –ї–∞–±–Њ—А–∞—В–Њ—А–љ–Њ-–Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –Є —А–∞–Ј—А–∞–±–Њ—В–∞—В—М —В–∞–Ї—В–Є–Ї—Г –≤–µ–і–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–∞.
–•—А–Њ–љ–Є—З–µ—Б–Ї–∞—П –∞—Б–њ–Є—А–∞—Ж–Є—П –њ–Є—Й–Є –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –њ—А–Є —В—А–∞—Е–µ–Њ–њ–Є—Й–µ–≤–Њ–і–љ–Њ–Љ —Б–≤–Є—Й–µ, –≥–∞—Б—В—А–Њ—Н–Ј–Њ—Д–∞–≥–µ–∞–ї—М–љ–Њ–Љ —А–µ—Д–ї—О–Ї—Б–µ, –∞ —В–∞–Ї–ґ–µ –њ—А–Є –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є—Е –њ–Њ—А–∞–ґ–µ–љ–Є—П—Е –¶–Э–° (–±—Г–ї—М–±–∞—А–љ—Л–µ –Є–ї–Є –њ—Б–µ–≤–і–Њ–±—Г–ї—М–±–∞—А–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П). –•–∞—А–∞–Ї—В–µ—А–љ—Л–Љ –њ—А–Є–Ј–љ–∞–Ї–Њ–Љ —Н—В–Є—Е –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є–є —П–≤–ї—П–µ—В—Б—П –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –њ—А–Є—Б—В—Г–њ–Њ–≤ —Г–і—Г—И—М—П, —Ж–Є–∞–љ–Њ–Ј–∞, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–Є—Е—Б—П –њ—А–Є—Б—В—Г–њ–Њ–Љ —Б–Є–ї—М–љ–Њ–≥–Њ –Ї–∞—И–ї—П –≤–Њ –≤—А–µ–Љ—П –Є–ї–Є —Б—А–∞–Ј—Г –њ–Њ—Б–ї–µ –µ–і—Л.
–Э–∞—А—П–і—Г —Б –±–Њ–ї–µ–Ј–љ—П–Љ–Є –Њ—А–≥–∞–љ–Њ–≤ –і—Л—Е–∞–љ–Є—П –Ї–∞—И–µ–ї—М –Љ–Њ–ґ–µ—В –±—Л—В—М —Б–Є–Љ–њ—В–Њ–Љ–Њ–Љ «–≤–љ–µ–ї–µ–≥–Њ—З–љ–Њ–є» –њ–∞—В–Њ–ї–Њ–≥–Є–Є. –Ю–љ –Љ–Њ–ґ–µ—В —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—В—М —В–µ—З–µ–љ–Є–µ —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –Њ—Б–Њ–±–µ–љ–љ–Њ –≤ —Б–ї—Г—З–∞–µ —А–∞–Ј–≤–Є—В–Є—П —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є —Б —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ–Љ –Ј–∞—Б—В–Њ–є–љ—Л—Е —П–≤–ї–µ–љ–Є–є –≤ –Љ–∞–ї–Њ–Љ –Ї—А—Г–≥–µ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П. –Т —В–∞–Ї–Њ–Љ —Б–ї—Г—З–∞–µ –њ–Њ—П–≤–ї–µ–љ–Є–µ –Ї–∞—И–ї—П, –љ–∞—А—П–і—Г —Б –љ–∞—А–∞—Б—В–∞–љ–Є–µ–Љ –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П, –±—Г–і–µ—В –њ—А–Њ–≤–Њ—Ж–Є—А–Њ–≤–∞—В—М—Б—П –±–µ—Б–њ–Њ–Ї–Њ–є—Б—В–≤–Њ–Љ —А–µ–±–µ–љ–Ї–∞, –њ–ї–∞—З–µ–Љ, —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –љ–∞–≥—А—Г–Ј–Ї–Њ–є. –Я–Њ–Љ–Є–Љ–Њ —Е–∞—А–∞–Ї—В–µ—А–љ—Л—Е –∞—Г—Б–Ї—Г–ї—М—В–∞—В–Є–≤–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є —Б–Њ —Б—В–Њ—А–Њ–љ—Л —Б–µ—А–і—Ж–∞ –≤ –ї–µ–≥–Ї–Є—Е –Љ–Њ–≥—Г—В –≤—Л—Б–ї—Г—И–Є–≤–∞—В—М—Б—П –љ–µ–Њ–±–Є–ї—М–љ—Л–µ –Љ–µ–ї–Ї–Њ–њ—Г–Ј—Л—А—З–∞—В—Л–µ –Є–ї–Є –Ї—А–µ–њ–Є—В–Є—А—Г—О—Й–Є–µ —Е—А–Є–њ—Л, –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –≤ –љ–Є–ґ–љ–Є—Е –Њ—В–і–µ–ї–∞—Е, —Б—В–Њ–є–Ї–Њ —Б–Њ—Е—А–∞–љ—П—О—Й–Є–µ—Б—П –њ–Њ—Б–ї–µ –Њ—В–Ї–∞—И–ї–Є–≤–∞–љ–Є—П.
–Э–µ–Ї–Њ—В–Њ—А—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –ґ–µ–ї—Г–і–Њ—З–љ–Њ-–Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ –Љ–Њ–≥—Г—В —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—В—М—Б—П –Ї–∞—И–ї–µ–Љ (—Б—В–µ–љ–Њ–Ј –њ–Є—Й–µ–≤–Њ–і–∞, –≥—А—Л–ґ–∞ –њ–Є—Й–µ–≤–Њ–і–љ–Њ–≥–Њ –Њ—В–≤–µ—А—Б—В–Є—П –і–Є–∞—Д—А–∞–≥–Љ—Л, –њ–Њ–і–і–Є–∞—Д—А–∞–≥–Љ–∞–ї—М–љ—Л–є –∞–±—Б—Ж–µ—Б—Б, –≥–∞—Б—В—А–Њ—Н–Ј–Њ—Д–∞–≥–µ–∞–ї—М–љ—Л–є —А–µ—Д–ї—О–Ї—Б). –°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –і–ї–Є—В–µ–ї—М–љ—Л–є –Ї–∞—И–µ–ї—М –љ–∞ —Д–Њ–љ–µ –Ј–∞—В—П–ґ–љ–Њ–≥–Њ –Є —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–µ–≥–Њ —В–µ—З–µ–љ–Є—П –Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ–Њ–≥–Њ –±—А–Њ–љ—Е–Є—В–∞ –Љ–Њ–ґ–µ—В –±—Л—В—М –µ–і–Є–љ—Б—В–≤–µ–љ–љ—Л–Љ –њ—А–Њ—П–≤–ї–µ–љ–Є–µ–Љ –У–≠–†. –Т –і–∞–љ–љ–Њ–Љ —Б–ї—Г—З–∞–µ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ–±—А–∞—В–Є—В—М –≤–љ–Є–Љ–∞–љ–Є–µ –љ–∞ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–µ —Б–Є–Љ–њ—В–Њ–Љ—Л –Є –∞–љ–∞–Љ–љ–µ—Б—В–Є—З–µ—Б–Ї–Є–µ –і–∞–љ–љ—Л–µ, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–Є–µ —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–Њ —Г—Б—В–∞–љ–Њ–≤–Є—В—М –њ—А–∞–≤–Є–ї—М–љ—Л–є –і–Є–∞–≥–љ–Њ–Ј (—Г–Ї–∞–Ј–∞–љ–Є–µ –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ –љ–∞ —З–∞—Б—В—Л–µ —Б—А—Л–≥–Є–≤–∞–љ–Є—П –њ–Њ—Б–ї–µ –Ї–Њ—А–Љ–ї–µ–љ–Є—П, —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–Є–µ –Њ—В–Є—В—Л, –њ–Њ—Б—В–Њ—П–љ–љ–∞—П –Љ–Њ–ї–Њ—З–љ–Є—Ж–∞ —Б–ї–Є–Ј–Є—Б—В–Њ–є –њ–Њ–ї–Њ—Б—В–Є —А—В–∞, —А–∞–Ј–≤–Є—В–Є–µ –±—А–Њ–љ—Е–Њ–Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Ю–†–Т–Ш). –Ъ–∞—И–µ–ї—М –≤–Њ –≤—А–µ–Љ—П –њ—А–Є–µ–Љ–∞ –њ–Є—Й–Є –Љ–Њ–ґ–µ—В –љ–∞–±–ї—О–і–∞—В—М—Б—П –њ—А–Є –і–Є—Б—Д–∞–≥–Є–Є –љ–∞ —Д–Њ–љ–µ –њ–Њ—А–∞–ґ–µ–љ–Є—П —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л, –∞ —В–∞–Ї–ґ–µ –њ—А–Є —В—А–∞—Е–µ–Њ–њ–Є—Й–µ–≤–Њ–і–љ—Л—Е —Б–≤–Є—Й–∞—Е, –Ї–Њ–≥–і–∞ –Њ–љ —З–∞—Б—В–Њ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –Њ—В–і–µ–ї–µ–љ–Є–µ–Љ –Њ–±–Є–ї—М–љ–Њ–є –њ–µ–љ–Є—Б—В–Њ–є –Љ–Њ–Ї—А–Њ—В—Л. –Т –і–∞–љ–љ–Њ–Љ —Б–ї—Г—З–∞–µ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—О –њ—А–∞–≤–Є–ї—М–љ–Њ–≥–Њ –і–Є–∞–≥–љ–Њ–Ј–∞ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–Њ–µ –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –±—А–Њ–љ—Е–Њ—Б–Ї–Њ–њ–Є–Є.
–Ю—Б–Њ–±–Њ–≥–Њ –≤–љ–Є–Љ–∞–љ–Є—П –Ј–∞—Б–ї—Г–ґ–Є–≤–∞–µ—В –њ—Б–Є—Е–Њ–≥–µ–љ–љ—Л–є –Ї–∞—И–µ–ї—М. –Ю–љ –Њ–±—Л—З–љ–Њ —Б—Г—Е–Њ–є, —Б –Љ–µ—В–∞–ї–ї–Є—З–µ—Б–Ї–Є–Љ –Њ—В—В–µ–љ–Ї–Њ–Љ; –љ–∞–±–ї—О–і–∞–µ—В—Б—П —В–Њ–ї—М–Ї–Њ –≤ –і–љ–µ–≤–љ–Њ–µ –≤—А–µ–Љ—П –Є –Є—Б—З–µ–Ј–∞–µ—В –≤–Њ —Б–љ–µ. –Х–≥–Њ –Њ—В–ї–Є—З–Є—В–µ–ї—М–љ–∞—П –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—М – —А–µ–≥—Г–ї—П—А–љ–Њ—Б—В—М –Є –≤—Л—Б–Њ–Ї–∞—П —З–∞—Б—В–Њ—В–∞ (–і–Њ 4–8 —А–∞–Ј/–Љ–Є–љ.), –њ—А–µ–Ї—А–∞—Й–µ–љ–Є–µ –≤–Њ –≤—А–µ–Љ—П –µ–і—Л –Є —А–∞–Ј–≥–Њ–≤–Њ—А–Њ–≤. –Я—Б–Є—Е–Њ–≥–µ–љ–љ—Л–є –Ї–∞—И–µ–ї—М –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –Њ–±—Л—З–љ–Њ –Ї–∞–Ї —А–µ–∞–Ї—Ж–Є—П –љ–∞ —Б—В—А–µ—Б—Б–Њ–≤—Л–µ —Б–Є—В—Г–∞—Ж–Є–Є –≤ —Б–µ–Љ—М–µ, —И–Ї–Њ–ї–µ. –Ь–∞–ї–µ–љ—М–Ї–Є–µ –і–µ—В–Є –љ–µ—А–µ–і–Ї–Њ –Ї–∞—И–ї—П—О—В –њ—А–Є —Б—В—А–µ—Б—Б–µ, –Њ—Б–Њ–±–µ–љ–љ–Њ —З—В–Њ–±—Л –і–Њ–±–Є—В—М—Б—П —Б–≤–Њ–Є—Е —Ж–µ–ї–µ–є. –Э–∞–њ—А–Є–Љ–µ—А, –Ї–∞—И–µ–ї—М –Љ–Њ–ґ–µ—В —Г—Б–Є–ї–Є–≤–∞—В—М—Б—П –і–Њ –Є –≤–Њ –≤—А–µ–Љ—П –Њ—Б–Љ–Њ—В—А–∞ –≤—А–∞—З–∞, –њ—А–µ–Ї—А–∞—Й–∞—П—Б—М –њ–Њ –µ–≥–Њ –Њ–Ї–Њ–љ—З–∞–љ–Є–Є (—Б–љ—П—В–Є–µ «—Б—В—А–µ—Б—Б–∞ –Њ–ґ–Є–і–∞–љ–Є—П»). –Я—А–Є—З–Є–љ–Њ–є –Ј–∞–Ї—А–µ–њ–ї–µ–љ–Є—П –Ї–∞—И–ї–µ–≤–Њ–≥–Њ —А–µ—Д–ї–µ–Ї—Б–∞ —Г —А–µ–±–µ–љ–Ї–∞ –Љ–Њ–≥—Г—В –±—Л—В—М –њ–Њ–≤—Л—И–µ–љ–љ–∞—П —В—А–µ–≤–Њ–ґ–љ–Њ—Б—В—М —А–Њ–і–Є—В–µ–ї–µ–є, –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –Є—Е –≤–љ–Є–Љ–∞–љ–Є—П –љ–∞ —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–∞—Е [–Ґ–∞—В–Њ—З–µ–љ–Ї–Њ –Т.–Ъ. –Ф–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ–∞—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Ї–∞—И–ї—П —Г –і–µ—В–µ–є. –Ь.: –Э–¶–Ч–Ф –і–µ—В–µ–є –†–Р–Ь–Э, 2006]. –Ъ–∞—И–µ–ї—М –Љ–Њ–ґ–µ—В —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—В—М —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л–є –∞–ї–Ї–∞–ї–Њ–Ј, —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Й–Є—В–Њ–≤–Є–і–љ–Њ–є –ґ–µ–ї–µ–Ј—Л, –≤–Њ–Ј–љ–Є–Ї–∞—В—М –њ—А–Є –Љ–µ–љ–Є–љ–≥–Є—В–µ, –Њ–њ—Г—Е–Њ–ї—П—Е –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ [3].
–Ф–µ—В—П–Љ, –Њ–±—А–∞—В–Є–≤—И–Є–Љ—Б—П –њ–Њ –њ–Њ–≤–Њ–і—Г –Ї–∞—И–ї—П, –љ–∞–Ј–љ–∞—З–∞–µ—В—Б—П –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –≤–Ї–ї—О—З–∞—О—Й–µ–µ –њ—А–Њ–≥—А–∞–Љ–Љ—Г –Љ–Є–љ–Є–Љ—Г–Љ – –њ—А–Є –Њ—Б—В—А–Њ–Љ –Є –Љ–∞–Ї—Б–Є–Љ—Г–Љ – –њ—А–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–Љ –Ї–∞—И–ї–µ. –Я–Њ—Б–ї–µ —Б–±–Њ—А–∞ –∞–љ–∞–Љ–љ–µ–Ј–∞ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П (—Е–∞—А–∞–Ї—В–µ—А –ґ–∞–ї–Њ–±, —Г—В–Њ—З–љ–µ–љ–Є–µ –і–Є–љ–∞–Љ–Є–Ї–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤), –∞–љ–∞–Љ–љ–µ–Ј–∞ –ґ–Є–Ј–љ–Є (—Б–≤–µ–і–µ–љ–Є—П –Њ –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ–Њ—Б—В–Є, —А–∞–љ–µ–µ –њ–µ—А–µ–љ–µ—Б–µ–љ–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е, –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤), –Њ—Ж–µ–љ–Ї–Є –Њ–±—Й–µ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П, –Њ—Б–Љ–Њ—В—А–∞, —Д–Є–Ј–Є–Ї–∞–ї—М–љ–Њ–≥–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П (–∞—Г—Б–Ї—Г–ї—М—В–∞—Ж–Є—П, –њ–µ—А–Ї—Г—Б—Б–Є—П) –љ–∞–Ј–љ–∞—З–∞–µ—В—Б—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј –Ї—А–Њ–≤–Є, –њ–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ – –Ї–Њ–љ—Б—Г–ї—М—В–∞—Ж–Є—П –Њ—В–Њ—А–Є–љ–Њ–ї–∞—А–Є–љ–≥–Њ–ї–Њ–≥–∞. –І–µ—А–µ–Ј 3–5 –і–љ–µ–є –њ—А–Њ–≤–Њ–і–Є—В—Б—П –њ–Њ–≤—В–Њ—А–љ—Л–є –Њ—Б–Љ–Њ—В—А –њ–∞—Ж–Є–µ–љ—В–∞ —Б —Ж–µ–ї—М—О —А–µ—И–µ–љ–Є—П –≤–Њ–њ—А–Њ—Б–∞ –Њ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ—Б—В–Є –і–Њ–Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є —В–µ—А–∞–њ–Є–Є. –Я—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –њ—А–Њ–≤–Њ–і–Є—В—Б—П —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Є–і–∞—В–Њ—З–љ—Л—Е –њ–∞–Ј—Г—Е –љ–Њ—Б–∞, –≥—А—Г–і–љ–Њ–є –Ї–ї–µ—В–Ї–Є. –Я—А–Є –Ї–∞—И–ї–µ, —Б–Њ—Е—А–∞–љ—П—О—Й–µ–Љ—Б—П –±–Њ–ї–µ–µ 2–3 –љ–µ–і., —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ—Л–Љ —П–≤–ї—П–µ—В—Б—П —Б–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Ї—А–Њ–≤–Є –і–ї—П –Є—Б–Ї–ї—О—З–µ–љ–Є—П –Љ–Є–Ї–Њ–њ–ї–∞–Ј–Љ–µ–љ–љ–Њ–є, —Е–ї–∞–Љ–Є–і–Є–є–љ–Њ–є, –Ї–Њ–Ї–ї—О—И–љ–Њ–є, –њ–љ–µ–≤–Љ–Њ—Ж–Є—Б—В–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є, –≥–ї–Є—Б—В–љ–Њ–є –Є–љ–≤–∞–Ј–Є–Є (–∞—Б–Ї–∞—А–Є–і–Њ–Ј–∞). –Я—А–Њ–≥—А–∞–Љ–Љ–∞ –Љ–∞–Ї—Б–Є–Љ—Г–Љ –≤–Ї–ї—О—З–∞–µ—В –∞–ї–ї–µ—А–≥–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Б –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ–Љ –Њ–±—Й–µ–≥–Њ –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ–∞ –Х –Є —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є—Е –∞–љ—В–Є—В–µ–ї –±—Л—В–Њ–≤–Њ–≥–Њ, –њ—Л–ї—М—Ж–µ–≤–Њ–≥–Њ, –Љ–Є–Ї—А–Њ–±–љ–Њ–≥–Њ, –≥—А–Є–±–Ї–Њ–≤–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞, –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Є –≤–љ–µ—И–љ–µ–≥–Њ –і—Л—Е–∞–љ–Є—П, –њ—А–Њ–±—Г —Б –±—А–Њ–љ—Е–Њ–ї–Є—В–Є–Ї–∞–Љ–Є, –Ї–Њ–Љ–њ—М—О—В–µ—А–љ—Г—О —В–Њ–Љ–Њ–≥—А–∞—Д–Є—О –≥—А—Г–і–љ–Њ–є –Ї–ї–µ—В–Ї–Є, —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Њ—А–≥–∞–љ–Њ–≤ –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є —Б –њ—А–Њ–≤–µ–і–µ–љ–Є–µ–Љ –≤–Њ–і–љ–Њ-—Б–Є—Д–Њ–љ–љ–Њ–є –њ—А–Њ–±—Л, —Н–Ј–Њ—Д–∞–≥–Њ–≥–∞—Б—В—А–Њ–і—Г–Њ–і–µ–љ–Њ—Б–Ї–Њ–њ–Є—О –Є —В.–і. [4].
–Ю—Б–љ–Њ–≤–Њ–є —В–µ—А–∞–њ–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–Є—Е—Б—П –Ї–∞—И–ї–µ–Љ, —П–≤–ї—П–µ—В—Б—П —Н—В–Є–Њ—В—А–Њ–њ–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ. –Т –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Е–∞—А–∞–Ї—В–µ—А–∞ –Ї–∞—И–ї—П –љ–∞–Ј–љ–∞—З–∞—О—В—Б—П –њ—А–Њ—В–Є–≤–Њ–Ї–∞—И–ї–µ–≤—Л–µ –Є–ї–Є –Њ—В—Е–∞—А–Ї–Є–≤–∞—О—Й–Є–µ –њ—А–µ–њ–∞—А–∞—В—Л. –Я—А–Њ—В–Є–≤–Њ–Ї–∞—И–ї–µ–≤—Л–µ —Б—А–µ–і—Б—В–≤–∞ –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В —Б–Њ–±–Њ–є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л, –њ–Њ–і–∞–≤–ї—П—О—Й–Є–µ –Ї–∞—И–ї–µ–≤–Њ–є —А–µ—Д–ї–µ–Ї—Б. –С–ї–∞–≥–Њ–і–∞—А—П —Б–љ–Є–ґ–µ–љ–Є—О —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ —В—А–∞—Е–µ–Њ–±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ –і–µ—А–µ–≤–∞ –Є–ї–Є –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ —Г–≥–љ–µ—В–µ–љ–Є—П –Ї–∞—И–ї–µ–≤–Њ–≥–Њ —Ж–µ–љ—В—А–∞ –њ—А–Њ–і–Њ–ї–≥–Њ–≤–∞—В–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –њ—А–Њ—В–Є–≤–Њ–Ї–∞—И–ї–µ–≤—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Я–Њ–Ї–∞–Ј–∞–љ–Є–µ–Љ –і–ї—П –љ–∞–Ј–љ–∞—З–µ–љ–Є—П —Н—В–Є—Е —Б—А–µ–і—Б—В–≤ —П–≤–ї—П–µ—В—Б—П —Б—Г—Е–Њ–є –Љ—Г—З–Є—В–µ–ї—М–љ—Л–є –Ї–∞—И–µ–ї—М, –≤—Б—В—А–µ—З–∞—О—Й–Є–є—Б—П –њ—А–Є –Њ—Б—В—А–Њ–Љ –ї–∞—А–Є–љ–≥–Є—В–µ, —В—А–∞—Е–µ–Є—В–µ, –±—А–Њ–љ—Е–Є—В–µ, —Б—Г—Е–Њ–Љ –њ–ї–µ–≤—А–Є—В–µ —Г –±–Њ–ї—М–љ—Л—Е –≥—А–Є–њ–њ–Њ–Љ, –Ю–†–Т–Ш. –Я—А–Њ—В–Є–≤–Њ–Ї–∞—И–ї–µ–≤—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ—Л –њ—А–Є –≤–ї–∞–ґ–љ–Њ–Љ –Ї–∞—И–ї–µ. –Ш—Е –њ–Њ–і—А–∞–Ј–і–µ–ї—П—О—В –љ–∞ –њ—А–µ–њ–∞—А–∞—В—Л —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–≥–Њ (–љ–∞—А–Ї–Њ—В–Є—З–µ—Б–Ї–Є–µ –Є –љ–µ–љ–∞—А–Ї–Њ—В–Є—З–µ—Б–Ї–Є–µ –њ—А–µ–њ–∞—А–∞—В—Л) –Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П. –Э–∞—А–Ї–Њ—В–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—В–Є–≤–Њ–Ї–∞—И–ї–µ–≤—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –≤ –і–µ—В—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ, –≤–≤–Є–і—Г –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є —А–∞–Ј–≤–Є—В–Є—П –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є, —Г–≥–љ–µ—В–µ–љ–Є—П –і—Л—Е–∞—В–µ–ї—М–љ–Њ–≥–Њ —Ж–µ–љ—В—А–∞, –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –љ–µ –њ—А–Є–Љ–µ–љ—П—О—В. –£ –і–µ—В–µ–є —Б—В–∞—А—И–µ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ –≤ —Б–ї—Г—З–∞–µ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є —Н—В–Є –ї–µ–Ї–∞—А—Б—В–≤–∞ –њ—А–Є–Љ–µ–љ—П—О—В—Б—П –≤ –Љ–∞–ї—Л—Е –і–Њ–Ј–∞—Е –≤ –≤–Є–і–µ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤ (—В–∞–±–ї. 3).
–Я—А–Њ—В–Є–≤–Њ–Ї–∞—И–ї–µ–≤—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –њ–Њ–Ї–∞–Ј–∞–љ—Л –њ—А–Є –љ–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–Љ, –Љ—Г—З–Є—В–µ–ї—М–љ–Њ–Љ, –љ–∞–≤—П–Ј—З–Є–≤–Њ–Љ —Б—Г—Е–Њ–Љ –Ї–∞—И–ї–µ, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—Й–µ–Љ –љ–∞—А—Г—И–µ–љ–Є—О —Б–љ–∞, –∞–њ–њ–µ—В–Є—В–∞ –Є –љ–µ–≥–∞—В–Є–≤–љ–Њ –≤–ї–Є—П—О—Й–µ–Љ –љ–∞ –Ї–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є —А–µ–±–µ–љ–Ї–∞. –Я—А–Є —Н—В–Њ–Љ –ґ–µ–ї–∞—В–µ–ї—М–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –љ–µ–љ–∞—А–Ї–Њ—В–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—В–Є–≤–Њ–Ї–∞—И–ї–µ–≤—Л–µ —Б—А–µ–і—Б—В–≤–∞ (—В–∞–±–ї. 4).
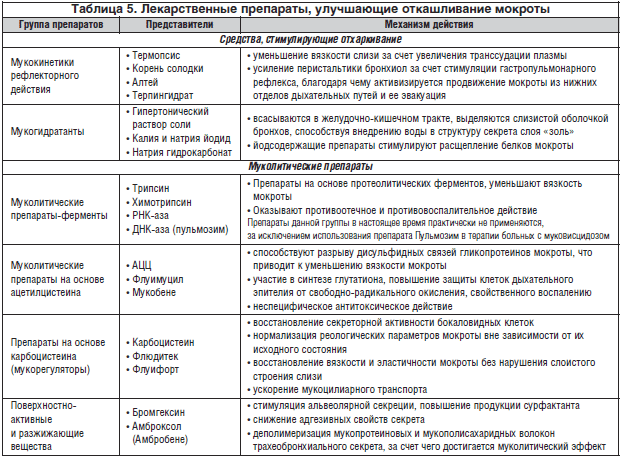
–Ю—В—Е–∞—А–Ї–Є–≤–∞—О—Й–Є–µ –њ—А–µ–њ–∞—А–∞—В—Л —И–Є—А–Њ–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –≤ –њ–µ–і–Є–∞—В—А–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –њ—А–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –≤–µ—А—Е–љ–Є—Е –Є –љ–Є–ґ–љ–Є—Е –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є. –°—А–µ–і–Є –Њ—В—Е–∞—А–Ї–Є–≤–∞—О—Й–Є—Е —Б—А–µ–і—Б—В–≤ –≤—Л–і–µ–ї—П—О—В —Б–ї–µ–і—Г—О—Й–Є–µ –≥—А—Г–њ–њ—Л [1, 4, 6–8] (—В–∞–±–ї. 5):
• –Љ—Г–Ї–Њ–≥–Є–і—А–∞—В–∞–љ—В—Л (–њ—А–µ–њ–∞—А–∞—В—Л, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—Й–Є–µ –≤–љ–µ–і—А–µ–љ–Є—О –≤–Њ–і—Л –≤ —Б—В—А—Г–Ї—В—Г—А—Г —Б–µ–Ї—А–µ—В–∞ —Б–ї–Њ—П «–Ј–Њ–ї—М» – –≥–Є–њ–µ—А—В–Њ–љ–Є—З–µ—Б–Ї–Є–є —А–∞—Б—В–≤–Њ—А —Б–Њ–ї–Є, –Ї–∞–ї–Є—П –Є –љ–∞—В—А–Є—П –є–Њ–і–Є–і);
• –Њ—В—Е–∞—А–Ї–Є–≤–∞—О—Й–Є–µ –Љ—Г–Ї–Њ–Ї–Є–љ–µ—В–Є–Ї–Є – –њ—А–µ–њ–∞—А–∞—В—Л, —Б–Њ–і–µ—А–ґ–∞—Й–Є–µ –∞–ї–Ї–∞–ї–Њ–Є–і—Л –Є–ї–Є —Б–∞–њ–Њ–љ–Є–љ—Л, —Г—Б–Є–ї–Є–≤–∞—О—Й–Є–µ –њ–µ—А–Є—Б—В–∞–ї—М—В–Є–Ї—Г –±—А–Њ–љ—Е–Є–Њ–ї –Ј–∞ —Б—З–µ—В —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є –≥–∞—Б—В—А–Њ–њ—Г–ї—М–Љ–Њ–љ–∞—А–љ–Њ–≥–Њ —А–µ—Д–ї–µ–Ї—Б–∞, –±–ї–∞–≥–Њ–і–∞—А—П —З–µ–Љ—Г –∞–Ї—В–Є–≤–Є–Ј–Є—А—Г–µ—В—Б—П –њ—А–Њ–і–≤–Є–ґ–µ–љ–Є–µ –Љ–Њ–Ї—А–Њ—В—Л –Є–Ј –љ–Є–ґ–љ–Є—Е –Њ—В–і–µ–ї–Њ–≤ –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є –Є –µ–µ —Н–≤–∞–Ї—Г–∞—Ж–Є—П (—В–µ—А–Љ–Њ–њ—Б–Є—Б, –Ї–Њ—А–µ–љ—М —Б–Њ–ї–Њ–і–Ї–Є, –≥–≤–∞–є—Д–µ–љ–µ–Ј–Є–љ, –∞–ї—В–µ–є, —В–µ—А–њ–Є–љ–≥–Є–і—А–∞—В –Є —В.–і.)
• –Љ—Г–Ї–Њ–ї–Є—В–Є–Ї–Є (–њ—А–µ–њ–∞—А–∞—В—Л, —А–∞–Ј–ґ–Є–ґ–∞—О—Й–Є–µ –Љ–Њ–Ї—А–Њ—В—Г –Є –Є–Ј–Љ–µ–љ—П—О—Й–Є–µ –≤—П–Ј–Ї–Њ—Б—В—М —Б–µ–Ї—А–µ—В–∞ –њ—Г—В–µ–Љ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –µ–≥–Њ —Д–Є–Ј–Є–Ї–Њ-—Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е —Б—А–µ–і—Б—В–≤ – –∞—Ж–µ—В–Є–ї—Ж–Є—Б—В–µ–Є–љ, —Ж–Є—Б—В–µ–Є–љ, –Љ–µ—В–Є–ї—Ж–Є—Б—В–µ–Є–љ);
• –Љ—Г–Ї–Њ—А–µ–≥—Г–ї—П—В–Њ—А—Л (–њ—А–µ–њ–∞—А–∞—В—Л, —А–µ–≥—Г–ї–Є—А—Г—О—Й–Є–µ –≤—Л—А–∞–±–Њ—В–Ї—Г —Б–µ–Ї—А–µ—В–∞ –ґ–µ–ї–µ–Ј–Є—Б—В—Л–Љ–Є –Ї–ї–µ—В–Ї–∞–Љ–Є – –Ї–∞—А–±–Њ—Ж–Є—Б—В–µ–Є–љ, —Б—В–µ–њ—А–Њ–љ–Є–љ, –ї–µ—В–Њ—Б—В–µ–Є–љ);
• –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–Њ-–∞–Ї—В–Є–≤–љ—Л–µ –Є —А–∞–Ј–ґ–Є–ґ–∞—О—Й–Є–µ –≤–µ—Й–µ—Б—В–≤–∞ (–њ—А–µ–њ–∞—А–∞—В—Л, –Є–Ј–Љ–µ–љ—П—О—Й–Є–µ –∞–і–≥–µ–Ј–Є—О —Б–µ–Ї—А–µ—В–∞ – –±—А–Њ–Љ–≥–µ–Ї—Б–Є–љ, –∞–Љ–±—А–Њ–Ї—Б–Њ–ї).
–Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Љ—Г–Ї–Њ–≥–Є–і—А–∞–љ—В–Њ–≤ –Є –Љ—Г–Ї–Њ–Ї–Є–љ–µ—В–Є–Ї–Њ–≤ –љ–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –њ—А–Є –Њ—Б—В—А—Л—Е –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–Њ—Ж–µ—Б—Б–∞—Е –≤ –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В—П—Е, –Ї–Њ–≥–і–∞ –µ—Й–µ –љ–µ—В –≤—Л—А–∞–ґ–µ–љ–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –≤ –±–Њ–Ї–∞–ї–Њ–≤–Є–і–љ—Л—Е –Ї–ї–µ—В–Ї–∞—Е –Є –Љ–µ—А—Ж–∞—В–µ–ї—М–љ–Њ–Љ —Н–њ–Є—В–µ–ї–Є–Є, –њ—А–Є –љ–∞–ї–Є—З–Є–Є –Љ–∞–ї–Њ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–≥–Њ –Ї–∞—И–ї—П [9]. –Ъ –Њ—Б–љ–Њ–≤–љ—Л–Љ –љ–µ–і–Њ—Б—В–∞—В–Ї–∞–Љ –Њ—В—Е–∞—А–Ї–Є–≤–∞—О—Й–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –і–∞–љ–љ—Л—Е –≥—А—Г–њ–њ –Љ–Њ–ґ–љ–Њ –Њ—В–љ–µ—Б—В–Є –Ї–Њ—А–Њ—В–Ї—Г—О –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –і–µ–є—Б—В–≤–Є—П –Є —З–∞—Б—В—Г—О –њ—А–Њ–≤–Њ–Ї–∞—Ж–Є—О —А–≤–Њ—В–љ–Њ–≥–Њ —А–µ—Д–ї–µ–Ї—Б–∞ —Г –і–µ—В–µ–є –њ—А–Є –њ—А–µ–≤—Л—И–µ–љ–Є–Є –і–Њ–њ—Г—Б—В–Є–Љ–Њ–є —А–∞–Ј–Њ–≤–Њ–є –і–Њ–Ј—Л. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –і–∞–љ–љ—Л–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞ –Љ–Њ–≥—Г—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–≤–µ–ї–Є—З–Є—В—М –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –Љ–Њ–Ї—А–Њ—В—Л, –Ї–Њ—В–Њ—А—Г—О –±—Л–≤–∞–µ—В —В—А—Г–і–љ–Њ –Њ—В–Ї–∞—И–ї—П—В—М –і–µ—В—П–Љ —А–∞–љ–љ–µ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞, —З—В–Њ –≤ —А—П–і–µ —Б–ї—Г—З–∞–µ–≤ –Љ–Њ–ґ–µ—В —Г—Б—Г–≥—Г–±–Є—В—М —В—П–ґ–µ—Б—В—М —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є.
–Т—Л—Б–Њ–Ї–Њ—Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ–Є –Є –±–µ–Ј–Њ–њ–∞—Б–љ—Л–Љ–Є –≤ –њ–µ–і–Є–∞—В—А–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –Ј–∞—А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–ї–Є —Б–µ–±—П –Љ—Г–Ї–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–µ –њ—А–µ–њ–∞—А–∞—В—Л, –Ї–Њ—В–Њ—А—Л–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ —А–∞–Ј–ґ–Є–ґ–∞—О—В –Љ–Њ–Ї—А–Њ—В—Г, —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –љ–µ —Г–≤–µ–ї–Є—З–Є–≤–∞—П –µ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ. –Ъ –і–∞–љ–љ–Њ–є –≥—А—Г–њ–њ–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤ –Њ—В–љ–Њ—Б—П—В—Б—П –Љ—Г–Ї–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–µ –њ—А–µ–њ–∞—А–∞—В—Л-—Д–µ—А–Љ–µ–љ—В—Л, –њ—А–µ–њ–∞—А–∞—В—Л –љ–∞ –Њ—Б–љ–Њ–≤–µ –∞—Ж–µ—В–Є–ї—Ж–Є—Б—В–µ–Є–љ–∞ –Є –Ї–∞—А–±–Њ—Ж–Є—Б—В–µ–Є–љ–∞, –∞ —В–∞–Ї–ґ–µ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–Њ-–∞–Ї—В–Є–≤–љ—Л–µ –Є —А–∞–Ј–ґ–Є–ґ–∞—О—Й–Є–µ –≤–µ—Й–µ—Б—В–≤–∞ (–±—А–Њ–Љ–≥–µ–Ї—Б–Є–љ, –∞–Љ–±—А–Њ–Ї—Б–Њ–ї). –Ь—Г–Ї–Њ–ї–Є—В–Є–Ї–Є –Љ–Њ–≥—Г—В –±—Л—В—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ—Л –Ї–∞–Ї –њ—А–Є –Њ—Б—В—А—Л—Е, —В–∞–Ї –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –±—А–Њ–љ—Е–Њ–ї–µ–≥–Њ—З–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–Є—Е—Б—П –њ—А–Њ–і—Г–Ї—В–Є–≤–љ—Л–Љ –Ї–∞—И–ї–µ–Љ —Б –Њ—В—Е–Њ–ґ–і–µ–љ–Є–µ–Љ –≥—Г—Б—В–Њ–є –≤—П–Ј–Ї–Њ–є –Љ–Њ–Ї—А–Њ—В—Л, –Њ—Б–Њ–±–µ–љ–љ–Њ —Г –і–µ—В–µ–є —А–∞–љ–љ–µ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞, —Г –Ї–Њ—В–Њ—А—Л—Е –њ–Њ–≤—Л—И–µ–љ–љ–∞—П –≤—П–Ј–Ї–Њ—Б—В—М –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ —Б–µ–Ї—А–µ—В–∞ —П–≤–ї—П–µ—В—Б—П –Њ–і–љ–Є–Љ –Є–Ј –Њ—Б–љ–Њ–≤–љ—Л—Е –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–∞–Ј–≤–Є—В–Є—П –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –≤ –љ–Є–ґ–љ–Є—Е –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В—П—Е. –Я—А–µ–њ–∞—А–∞—В—Л –љ–∞ –Њ—Б–љ–Њ–≤–µ –њ—А–Њ—В–µ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є—Е —Д–µ—А–Љ–µ–љ—В–Њ–≤ —Г–Љ–µ–љ—М—И–∞—О—В –≤—П–Ј–Ї–Њ—Б—В—М –Љ–Њ–Ї—А–Њ—В—Л –Є –Њ–Ї–∞–Ј—Л–≤–∞—О—В –њ—А–Њ—В–Є–≤–Њ–Њ—В–µ—З–љ–Њ–µ –Є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ. –Ш–Ј –і–∞–љ–љ–Њ–є –≥—А—Г–њ–њ—Л –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П —В–Њ–ї—М–Ї–Њ –њ—Г–ї—М–Љ–Њ–Ј–Є–Љ –≤ —В–µ—А–∞–њ–Є–Є –±–Њ–ї—М–љ—Л—Е —Б –Љ—Г–Ї–Њ–≤–Є—Б—Ж–Є–і–Њ–Ј–Њ–Љ. –Р—Ж–µ—В–Є–ї—Ж–Є—Б—В–µ–Є–љ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —А–∞–Ј—А—Л–≤—Г –і–Є—Б—Г–ї—М—Д–Є–і–љ—Л—Е —Б–≤—П–Ј–µ–є –≥–ї–Є–Ї–Њ–њ—А–Њ—В–µ–Є–љ–Њ–≤ –Љ–Њ–Ї—А–Њ—В—Л, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–Љ–µ–љ—М—И–µ–љ–Є—О –µ–µ –≤—П–Ј–Ї–Њ—Б—В–Є. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Є–Љ–µ—О—В—Б—П –і–∞–љ–љ—Л–µ, —Г–Ї–∞–Ј—Л–≤–∞—О—Й–Є–µ –љ–∞ —Г—З–∞—Б—В–Є–µ –∞—Ж–µ—В–Є–ї—Ж–Є—Б—В–µ–Є–љ–∞ –≤ —Б–Є–љ—В–µ–Ј–µ –≥–ї—Г—В–∞—В–Є–Њ–љ–∞, —З—В–Њ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –њ–Њ–≤—Л—И–µ–љ–Є—О –Ј–∞—Й–Є—В—Л –Ї–ї–µ—В–Њ–Ї –і—Л—Е–∞—В–µ–ї—М–љ–Њ–≥–Њ —Н–њ–Є—В–µ–ї–Є—П –Њ—В —Б–≤–Њ–±–Њ–і–љ–Њ-—А–∞–і–Є–Ї–∞–ї—М–љ–Њ–≥–Њ –Њ–Ї–Є—Б–ї–µ–љ–Є—П, —Б–≤–Њ–є—Б—В–≤–µ–љ–љ–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—О. –Я—А–µ–њ–∞—А–∞—В—Л –љ–∞ –Њ—Б–љ–Њ–≤–µ –Ї–∞—А–±–Њ—Ж–Є—Б—В–µ–Є–љ–∞ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—В –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—О —Б–µ–Ї—А–µ—В–Њ—А–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –±–Њ–Ї–∞–ї–Њ–≤–Є–і–љ—Л—Е –Ї–ї–µ—В–Њ–Ї —Н–њ–Є—В–µ–ї–Є—П —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞, –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є —А–µ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ –Љ–Њ–Ї—А–Њ—В—Л –Є —Г—Б–Ї–Њ—А–µ–љ–Є—О –Љ—Г–Ї–Њ—Ж–Є–ї–Є–∞—А–љ–Њ–≥–Њ —В—А–∞–љ—Б–њ–Њ—А—В–∞ [1].
–Я—А–Є –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–Є —В–∞–Ї—В–Є–Ї–Є —В–µ—А–∞–њ–Є–Є –Ї–∞—И–ї—П —Г –і–µ—В–µ–є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Г—З–Є—В—Л–≤–∞—В—М –≤–Њ–Ј—А–∞—Б—В–љ—Л–µ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є —А–µ–∞–≥–Є—А–Њ–≤–∞–љ–Є—П —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ –љ–∞ –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ-–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–є –њ—А–Њ—Ж–µ—Б—Б. –Т–≤–Є–і—Г —В–Њ–≥–Њ, —З—В–Њ –Њ–і–љ–Є–Љ –Є–Ј —Д–∞–Ї—В–Њ—А–Њ–≤, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—Й–Є—Е –Ј–∞—В—П–ґ–љ–Њ–Љ—Г —В–µ—З–µ–љ–Є—О —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є —Г –і–µ—В–µ–є —А–∞–љ–љ–µ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞, –Љ–Њ–ґ–µ—В —П–≤–Є—В—М—Б—П –і–µ—Д–Є—Ж–Є—В –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –Є –≤—Л–±—А–Њ—Б–∞ —Б—Г—А—Д–∞–Ї—В–∞–љ—В–∞, –Њ—Б–Њ–±—Л–є –Є–љ—В–µ—А–µ—Б –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –≤—Л–Ј—Л–≤–∞—О—В –њ—А–µ–њ–∞—А–∞—В—Л –љ–∞ –Њ—Б–љ–Њ–≤–µ –∞–Љ–±—А–Њ–Ї—Б–Њ–ї–∞ [4].
–Р–Љ–±—А–Њ–Ї—Б–Њ–ї —П–≤–ї—П–µ—В—Б—П –∞–Ї—В–Є–≤–љ—Л–Љ N-–і–µ–Љ–µ—В–Є–ї–Є—А–Њ–≤–∞–љ–љ—Л–Љ –Љ–µ—В–∞–±–Њ–ї–Є—В–Њ–Љ –±—А–Њ–Љ–≥–µ–Ї—Б–Є–љ–∞ –Є –Њ–±–ї–∞–і–∞–µ—В —Б–µ–Ї—А–µ—В–Њ–Љ–Њ—В–Њ—А–љ—Л–Љ, —Б–µ–Ї—А–µ—В–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–Љ –Є –Њ—В—Е–∞—А–Ї–Є–≤–∞—О—Й–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ. –Р–Љ–±—А–Њ–Ї—Б–Њ–ї —Б—В–Є–Љ—Г–ї–Є—А—Г–µ—В –Ї–ї–µ—В–Ї–Є –ґ–µ–ї–µ–Ј —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –±—А–Њ–љ—Е–Њ–≤, —Г–≤–µ–ї–Є—З–Є–≤–∞—П —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ —Б–ї–Є–Ј–Є—Б—В–Њ–≥–Њ —Б–µ–Ї—А–µ—В–∞, –Є —В–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ –Є–Ј–Љ–µ–љ—П–µ—В –љ–∞—А—Г—И–µ–љ–љ–Њ–µ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є–µ —Б–µ—А–Њ–Ј–љ–Њ–≥–Њ –Є —Б–ї–Є–Ј–Є—Б—В–Њ–≥–Њ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ –Љ–Њ–Ї—А–Њ—В—Л. –Р–Љ–±—А–Њ–Ї—Б–Њ–ї —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ —Б–ї–Є–Ј–Є—Б—В–Њ–≥–Њ —Б–µ–Ї—А–µ—В–∞ –Є –≤—Л–і–µ–ї–µ–љ–Є–µ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–Њ-–∞–Ї—В–Є–≤–љ–Њ–≥–Њ –≤–µ—Й–µ—Б—В–≤–∞ (—Б—Г—А—Д–∞–Ї—В–∞–љ—В–∞) –≤ –∞–ї—М–≤–µ–Њ–ї–∞—Е –Є –±—А–Њ–љ—Е–∞—Е. –Я—А–µ–њ–∞—А–∞—В –њ–Њ–≤—Л—И–∞–µ—В –і–≤–Є–≥–∞—В–µ–ї—М–љ—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Љ–µ—А—Ж–∞—В–µ–ї—М–љ–Њ–≥–Њ —Н—А–Є—В–µ–ї–Є—П, —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В –Љ—Г–Ї–Њ—Ж–Є–ї–Є–∞—А–љ—Л–є —В—А–∞–љ—Б–њ–Њ—А—В –Љ–Њ–Ї—А–Њ—В—Л. –Ф–µ–є—Б—В–≤–Є–µ –∞–Љ–±—А–Њ–Ї—Б–Њ–ї–∞ –њ—А–Є –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–Љ –њ—А–Є–µ–Љ–µ –љ–∞—Б—В—Г–њ–∞–µ—В —З–µ—А–µ–Ј 30 –Љ–Є–љ., –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –і–µ–є—Б—В–≤–Є—П —Б–Њ—Б—В–∞–≤–ї—П–µ—В 6–12 —З –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –і–Њ–Ј—Л. –Р–Љ–±—А–Њ–Ї—Б–Њ–ї –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –њ–Њ–ї–љ–Њ—Б—В—М—О –∞–±—Б–Њ—А–±–Є—А—Г–µ—В—Б—П –Є–Ј –Ц–Ъ–Ґ, –і–Њ—Б—В–Є–≥–∞—П –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –≤ –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є —З–µ—А–µ–Ј 1–3 —З. –Я–µ—А–Є–Њ–і –њ–Њ–ї—Г–≤—Л–≤–µ–і–µ–љ–Є—П –∞–Љ–±—А–Њ–Ї—Б–Њ–ї–∞ –Є–Ј –њ–ї–∞–Ј–Љ—Л —Б–Њ—Б—В–∞–≤–ї—П–µ—В 7–12 —З.
–Ф–µ–є—Б—В–≤–Є–µ –∞–Љ–±—А–Њ–Ї—Б–Њ–ї–∞ —Е–Њ—А–Њ—И–Њ –Є–Ј—Г—З–µ–љ–Њ –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є –њ–Њ—Б–ї–µ–і–љ–Є—Е 20 –ї–µ—В –њ—А–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –≤–µ—А—Е–љ–Є—Е –Є –љ–Є–ґ–љ–Є—Е –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є –Ї–∞–Ї —Г –і–µ—В–µ–є, —В–∞–Ї –Є —Г –≤–Ј—А–Њ—Б–ї—Л—Е. –Р–Љ–±—А–Њ–Ї—Б–Њ–ї —И–Є—А–Њ–Ї–Њ –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П –њ—А–Є –Њ—Б—В—А–Њ–Љ –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–Љ –±—А–Њ–љ—Е–Є—В–µ, –њ–љ–µ–≤–Љ–Њ–љ–Є–Є. –Ґ–∞–Ї, D. Olivieri –Є —Б–Њ–∞–≤—В. (1987) –њ—А–Њ–≤–µ–ї–Є 6-–Љ–µ—Б—П—З–љ–Њ–µ –Љ—Г–ї—М—В–Є—Ж–µ–љ—В—А–Њ–≤–Њ–µ –і–≤–Њ–є–љ–Њ–µ —Б–ї–µ–њ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, —Ж–µ–ї—М—О –Ї–Њ—В–Њ—А–Њ–≥–Њ —П–≤–Є–ї–Њ—Б—М –Є–Ј—Г—З–µ–љ–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –∞–Љ–±—А–Њ–Ї—Б–Њ–ї–∞ –≤ –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є–Є —А–µ—Ж–Є–і–Є–≤–Њ–≤ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –±—А–Њ–љ—Е–Є—В–∞ —Г –≤–Ј—А–Њ—Б–ї—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –С—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Г–ґ–µ —З–µ—А–µ–Ј 2 –Љ–µ—Б. —В–µ—А–∞–њ–Є–Є –∞–Љ–±—А–Њ–Ї—Б–Њ–ї–Њ–Љ —Г 67,2% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ—Л –љ–µ –±—Л–ї–Њ –Њ–±–Њ—Б—В—А–µ–љ–Є–є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –±—А–Њ–љ—Е–Є—В–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–Њ–є (50,4%). –І–µ—А–µ–Ј 6 –Љ–µ—Б. —В–µ—А–∞–њ–Є–Є –і–Њ–ї—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –љ–µ –Є–Љ–µ–≤—И–Є—Е –Њ–±–Њ—Б—В—А–µ–љ–Є–є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –±—А–Њ–љ—Е–Є—В–∞, —Б–Њ—Б—В–∞–≤–Є–ї–∞ 45,5% (–Њ—Б–љ–Њ–≤–љ–∞—П –≥—А—Г–њ–њ–∞), –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ – 14,4% (—А–∞–Ј–ї–Є—З–Є—П —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ—Л). –Р–≤—В–Њ—А–∞–Љ–Є –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М —Н–њ–Є–Ј–Њ–і–Њ–≤ –Њ–±–Њ—Б—В—А–µ–љ–Є—П —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –±—А–Њ–љ—Е–Є—В–∞, –Ї–∞–Ї –Є –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –±—Л–ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –Љ–µ–љ—М—И–µ –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞–Љ–±—А–Њ–Ї—Б–Њ–ї–∞ –њ—А–Є–≤–Њ–і–Є–ї–Њ –Ї –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –±–Њ–ї–µ–µ –±—Л—Б—В—А–Њ–Љ—Г –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—О –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П (—Г–Љ–µ–љ—М—И–µ–љ–Є—О —З–∞—Б—В–Њ—В—Л –Ї–∞—И–ї—П, –ї–Є–Ї–≤–Є–і–∞—Ж–Є–Є –Њ–і—Л—И–Ї–Є –Є –∞—Г—Б–Ї—Г–ї—М—В–∞—В–Є–≤–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –≤ –ї–µ–≥–Ї–Є—Е) [10].
J.–°. Peralta –Є —Б–Њ–∞–≤—В. (1987) –њ—А–Њ–≤–µ–ї–Є —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ –Є–Ј—Г—З–µ–љ–Є—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –∞–Љ–±—А–Њ–Ї—Б–Њ–ї–∞ –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ–Њ–Љ –≤ —В–µ—А–∞–њ–Є–Є –Њ–±–Њ—Б—В—А–µ–љ–Є–є –Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ–Њ–≥–Њ –±—А–Њ–љ—Е–Є—В–∞ —Г –≤–Ј—А–Њ—Б–ї—Л—Е [11]. –Я–∞—Ж–Є–µ–љ—В—Л –±—Л–ї–Є —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ—Л –љ–∞ –і–≤–µ –≥—А—Г–њ–њ—Л: –Њ—Б–љ–Њ–≤–љ–∞—П – –њ–Њ–ї—Г—З–∞–ї–Є —В–µ—А–∞–њ–Є—О –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ–Њ–Љ –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –∞–Љ–±—А–Њ–Ї—Б–Њ–ї–Њ–Љ, –Ї–Њ–љ—В—А–Њ–ї—М–љ–∞—П –—В–Њ–ї—М–Ї–Њ –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ–Њ–Љ. –Т —А–∞–љ–µ–µ –њ—А–Њ–≤–µ–і–µ–љ–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –∞–Љ–±—А–Њ–Ї—Б–Њ–ї –њ—А–Є —Б–Њ–≤–Љ–µ—Б—В–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —Б –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ–Њ–Љ —Б–њ–Њ—Б–Њ–±–µ–љ –Њ–±–ї–µ–≥—З–∞—В—М –µ–≥–Њ –њ—А–Њ–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –≤ –ї–µ–≥–Њ—З–љ—Г—О —В–Ї–∞–љ—М –Є –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–µ –і–µ—А–µ–≤–Њ [12, 13]. –Т —Е–Њ–і–µ –і–∞–љ–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Г–ґ–µ –љ–∞ 3-–є –і–µ–љ—М —В–µ—А–∞–њ–Є–Є –Љ–µ–ґ–і—Г –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є –Њ–±–µ–Є—Е –≥—А—Г–њ–њ –Њ—В–Љ–µ—З–∞–ї–Є—Б—М –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–µ —А–∞–Ј–ї–Є—З–Є—П –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ—Л –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –±—Л—Б—В—А–µ–µ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Г–ї—Г—З—И–µ–љ–Є–µ —Е–∞—А–∞–Ї—В–µ—А–∞ –Ї–∞—И–ї—П, –Є—Б—З–µ–Ј–љ–Њ–≤–µ–љ–Є–µ –Њ–і—Л—И–Ї–Є, –∞ —В–∞–Ї–ґ–µ –Є–Ј–Љ–µ–љ–µ–љ–Є–µ —Е–∞—А–∞–Ї—В–µ—А–∞ –Љ–Њ–Ї—А–Њ—В—Л (–Њ—В –≥–љ–Њ–є–љ–Њ–є –і–Њ –њ—А–Њ–Ј—А–∞—З–љ–Њ–є —Б–ї–Є–Ј–Є—Б—В–Њ–є). –Ъ–Њ–ї–Є—З–µ—Б—В–≤–Њ –і–љ–µ–≤–љ–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –Љ–Њ–Ї—А–Њ—В—Л –±—Л–ї–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –±–Њ–ї—М—И–µ –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ (—А<0,01). –Я—А–Є –±–∞–Ї—В–µ—А–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–Љ –∞–љ–∞–ї–Є–Ј–µ –Љ–Њ–Ї—А–Њ—В—Л –Ї 3-–Љ—Г –і–љ—О —В–µ—А–∞–њ–Є–Є —Н—А–∞–і–Є–Ї–∞—Ж–Є—П –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є –Њ—В–Љ–µ—З–∞–ї–∞—Б—М —Г 80% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –Є 31% – –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л. –Т —Е–Њ–і–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –і–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –≤ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –≤ –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–Љ —Б–µ–Ї—А–µ—В–µ –Љ–µ–ґ–і—Г –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є –Њ—Б–љ–Њ–≤–љ–Њ–є –Є –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ –≤—Л—П–≤–ї–µ–љ–Њ –љ–µ –±—Л–ї–Њ, –Њ–і–љ–∞–Ї–Њ, –µ—Б–ї–Є —Г—З–Є—В—Л–≤–∞—В—М —А–∞–Ј–ї–Є—З–љ–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Љ–Њ–Ї—А–Њ—В—Л, –Ї–ї–Є—А–µ–љ—Б –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –±—Л–ї –≤—Л—И–µ [11].
–Т–ї–Є—П–љ–Є–µ –Љ—Г–Ї–Њ–ї–Є—В–Є–Ї–Њ–≤ –љ–∞ –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–ї–Њ—Б—М —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ–Є –љ–µ—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –ї–µ–≥–Ї–Є—Е [14]: –±—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ –і–≤–Њ–є–љ–Њ–µ —Б–ї–µ–њ–Њ–µ –њ–ї–∞—Ж–µ–±–Њ-–Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –≤ –Ї–Њ—В–Њ—А–Њ–Љ –њ—А–Є–љ—П–ї–Є —Г—З–∞—Б—В–Є–µ 60 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ–Є –љ–µ—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –ї–µ–≥–Ї–Є—Е. –С–Њ–ї—М–љ—Л–µ –±—Л–ї–Є —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ—Л –љ–∞ 3 –≥—А—Г–њ–њ—Л, –њ–Њ–ї—Г—З–∞–≤—И–Є–µ –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ –Є–ї–Є —Н—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ, –Є–ї–Є —Ж–µ—Д—Г—А–Њ–Ї—Б–Є–Љ –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –њ–ї–∞—Ж–µ–±–Њ –Є–ї–Є –∞–Љ–±—А–Њ–Ї—Б–Њ–ї–Њ–Љ –≤ —В–µ—З–µ–љ–Є–µ 7 –і–љ–µ–є. –Т —Е–Њ–і–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Њ—Ж–µ–љ–Є–≤–∞–ї–∞—Б—М –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ –≤ –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–Љ —Б–µ–Ї—А–µ—В–µ –Є –Ї—А–Њ–≤–Є –љ–∞ 1-–є –Є 7-–є –і–µ–љ—М —В–µ—А–∞–њ–Є–Є. –Я—А–Є —Б–Њ—З–µ—В–∞–љ–љ–Њ–Љ –њ—А–Є–µ–Љ–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞ —Б –∞–Љ–±—А–Њ–Ї—Б–Њ–ї–Њ–Љ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –µ–≥–Њ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –≤ –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–Љ —Б–µ–Ї—А–µ—В–µ (–љ–Њ –љ–µ –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ), —З—В–Њ —Г–Ї–∞–Ј—Л–≤–∞–µ—В –љ–∞ —Б–Є–љ–µ—А–≥–Є–Ј–Љ –і–µ–є—Б—В–≤–Є—П –і–∞–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ–Є –љ–µ—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –ї–µ–≥–Ї–Є—Е. –Р–љ–∞–ї–Њ–≥–Є—З–љ—Л–µ –і–∞–љ–љ—Л–µ –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л P.C. Braga –Є —Б–Њ–∞–≤—В. (1985), F. Fraschini –Є —Б–Њ–∞–≤—В. (1986) [15, 16].
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є N. Princioi (1986) –Є–Ј—Г—З–∞–ї–∞—Б—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —Б–Њ–≤–Љ–µ—Б—В–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –Є –Љ—Г–Ї–Њ–ї–Є—В–Є–Ї–Њ–≤ —Г –і–µ—В–µ–є —Б –њ–љ–µ–≤–Љ–Њ–љ–Є—П–Љ–Є [17]. –Т —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Г—З–∞—Б—В–≤–Њ–≤–∞–ї–Є 120 –і–µ—В–µ–є –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 1 –Љ–µ—Б. –і–Њ 11 –ї–µ—В. –Ф–µ—В–Є –±—Л–ї–Є —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ—Л –љ–∞ –і–≤–µ –≥—А—Г–њ–њ—Л. –Ю—Б–љ–Њ–≤–љ–∞—П –≥—А—Г–њ–њ–∞ –і–µ—В–µ–є (60) –≤ —В–µ—З–µ–љ–Є–µ 10 –і–љ–µ–є –њ–Њ–ї—Г—З–∞–ї–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї (–∞–Љ–њ–Є—Ж–Є–ї–ї–Є–љ –Є–ї–Є –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ –Є–ї–Є —Н—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ) –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –∞–Љ–±—А–Њ–Ї—Б–Њ–ї–Њ–Љ –≤ –і–Њ–Ј–µ 1,5–2 –Љ–≥/–Ї–≥/—Б—Г—В. –Ъ–Њ–љ—В—А–Њ–ї—М–љ—Г—О –≥—А—Г–њ–њ—Г —Б–Њ—Б—В–∞–≤–Є–ї–Є 60 –і–µ—В–µ–є, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–ї—Г—З–∞–ї–Є —В–Њ–ї—М–Ї–Њ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є. –£ –≤—Б–µ—Е –і–µ—В–µ–є –Ї –Љ–Њ–Љ–µ–љ—В—Г –Њ–Ї–Њ–љ—З–∞–љ–Є—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–љ–µ–≤–Љ–Њ–љ–Є—П —А–∞–Ј—А–µ—И–Є–ї–∞—Б—М. –Ш—Б—З–µ–Ј–љ–Њ–≤–µ–љ–Є–µ –Ї–∞—И–ї—П, —Г–ї—Г—З—И–µ–љ–Є–µ —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ –љ–∞—Б—В—Г–њ–∞–ї–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –±—Л—Б—В—А–µ–µ (–і–Њ—Б—В–Њ–≤–µ—А–љ—Л–µ —А–∞–Ј–ї–Є—З–Є—П –Њ—В–Љ–µ—З–∞–ї–Є—Б—М —Г–ґ–µ –љ–∞ 3-–є –і–µ–љ—М —В–µ—А–∞–њ–Є–Є) –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ.
–Р–Љ–±—А–Њ–Ї—Б–Њ–ї –љ–µ –њ—А–Њ–≤–Њ—Ж–Є—А—Г–µ—В –±—А–Њ–љ—Е–Њ–Њ–±—Б—В—А—Г–Ї—Ж–Є—О. –Ф–Њ–Ї–∞–Ј–∞–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Д—Г–љ–Ї—Ж–Є–Є –≤–љ–µ—И–љ–µ–≥–Њ –і—Л—Е–∞–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е —Б –±—А–Њ–љ—Е–Њ–Њ–±—Б—В—А—Г–Ї—Ж–Є–µ–є –Є —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –≥–Є–њ–Њ–Ї—Б–µ–Љ–Є–Є –љ–∞ —Д–Њ–љ–µ –µ–≥–Њ –њ—А–Є–µ–Љ–∞. –Я–Њ–Ї–∞–Ј–∞–љ–Є–µ–Љ –і–ї—П –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –∞–Љ–±—А–Њ–Ї—Б–Њ–ї–∞ —П–≤–ї—П–µ—В—Б—П –±—А–Њ–љ—Е–Є–∞–ї—М–љ–∞—П –∞—Б—В–Љ–∞. –Т 1986 –≥. G. Melilio –Є —Б–Њ–∞–≤—В. –і–Њ–Ї–∞–Ј–∞–ї–Є –≤–ї–Є—П–љ–Є–µ –∞–Љ–±—А–Њ–Ї—Б–Њ–ї–∞ –љ–∞ –≥–Є–њ–µ—А—А–µ–∞–Ї—В–Є–≤–љ–Њ—Б—В—М –±—А–Њ–љ—Е–Њ–≤ [18]. –Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ —Д–Њ—Б—Д–∞—В–Є–і–Є–ї—Е–Њ–ї–Є–љ –≤ —Б–Њ—Б—В–∞–≤–µ —Б—Г—А—Д–∞–Ї—В–∞–љ—В–∞ –Є–≥—А–∞–µ—В –≤–∞–ґ–љ—Г—О —А–Њ–ї—М –≤ —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А–Њ–≤–∞–љ–Є–Є β-–∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, —Б–њ–Њ—Б–Њ–±–µ–љ —Г–≤–µ–ї–Є—З–Є–≤–∞—В—М –Є—Е –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –≤ –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–Љ –і–µ—А–µ–≤–µ [19]. –Ы–Є–Ј–Њ—Д–Њ—Б—Д–∞—В–Є–і–Є–ї—Е–Њ–ї–Є–љ, –љ–∞–Њ–±–Њ—А–Њ—В, —Г—Б–Є–ї–Є–≤–∞–µ—В –≥–Є–њ–µ—А—А–µ–∞–Ї—В–Є–≤–љ–Њ—Б—В—М –±—А–Њ–љ—Е–Њ–≤ –Ј–∞ —Б—З–µ—В —Г–≤–µ–ї–Є—З–µ–љ–Є—П –њ—А–Њ–љ–Є—Ж–∞–µ–Љ–Њ—Б—В–Є –Ї–ї–µ—В–Њ—З–љ—Л—Е –Љ–µ–Љ–±—А–∞–љ [20]. –Р–Љ–±—А–Њ–Ї—Б–Њ–ї —Б–њ–Њ—Б–Њ–±–µ–љ —Г—Б–Є–ї–Є–≤–∞—В—М –њ—А–Њ–і—Г–Ї—Ж–Є—О —Д–Њ—Б—Д–∞—В–Є–і–Є–ї—Е–Њ–ї–Є–љ–∞ –∞–ї—М–≤–µ–Њ–ї–Њ—Ж–Є—В–∞–Љ–Є II —В–Є–њ–∞ –Є —В–µ–Љ —Б–∞–Љ—Л–Љ –≤–ї–Є—П—В—М –љ–∞ –≥–Є–њ–µ—А—А–µ–∞–Ї—В–Є–≤–љ–Њ—Б—В—М –±—А–Њ–љ—Е–Њ–≤ –Ј–∞ —Б—З–µ—В, –≤–Њ-–њ–µ—А–≤—Л—Е, —Б–Њ–Ј–і–∞–љ–Є—П «–Ј–∞—Й–Є—В–љ–Њ–≥–Њ —Б–ї–Њ—П», –њ–Њ–Ї—А—Л–≤–∞—О—Й–µ–≥–Њ —А–µ—Ж–µ–њ—В–Њ—А—Л –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ –і–µ—А–µ–≤–∞, –≤–Њ-–≤—В–Њ—А—Л—Е, —Г—Б–Ї–Њ—А–µ–љ–Є—П –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –ї–Є–Ј–Њ—Д–Њ—Б—Д–∞—В–Є–і–Є–ї—Е–Њ–ї–Є–љ–∞. –Т –і–∞–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Њ—Ж–µ–љ–Є–≤–∞–ї–∞—Б—М —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –±—А–Њ–љ—Е–Њ–≤ –њ—А–Њ—В–Є–≤–Њ—Б—В–Њ—П—В—М —А–∞–Ј–і—А–∞–ґ–∞—О—Й–Є–Љ –∞–≥–µ–љ—В–∞–Љ –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –∞–Љ–±—А–Њ–Ї—Б–Њ–ї–∞ – —В–µ–Љ —Б–∞–Љ—Л–Љ –њ—А–Њ–Є–Ј–≤–µ–і–µ–љ–∞ –њ–Њ–њ—Л—В–Ї–∞ –Њ—Ж–µ–љ–Є—В—М –≤–ї–Є—П–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞ –љ–∞ –≥–Є–њ–µ—А—А–µ–∞–Ї—В–Є–≤–љ–Њ—Б—В—М –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ –і–µ—А–µ–≤–∞. –Т –Ї–∞—З–µ—Б—В–≤–µ –њ—А–Њ–≤–Њ—Ж–Є—А—Г—О—Й–µ–≥–Њ –∞–≥–µ–љ—В–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї—Б—П –Љ–µ—В–∞—Е–Њ–ї–Є–љ –≤ —А–∞–Ј–ї–Є—З–љ–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –њ—А–Є–љ—П–ї–Є —Г—З–∞—Б—В–Є–µ 11 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–є –∞—Б—В–Љ–Њ–є. –Я—А–Њ–≤–Њ–Ї–∞—Ж–Є–Њ–љ–љ—Л–µ —В–µ—Б—В—Л —Б –Љ–µ—В–∞—Е–Њ–ї–Є–љ–Њ–Љ –±—Л–ї–Є –њ—А–Њ–≤–µ–і–µ–љ—Л –і–≤–∞–ґ–і—Л –і–Њ –љ–∞—З–∞–ї–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б 3-–і–љ–µ–≤–љ—Л–Љ –Є–љ—В–µ—А–≤–∞–ї–Њ–Љ, –∞ —В–∞–Ї–ґ–µ –љ–∞ 14-–є –Є 28-–є –і–љ–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –Т —Е–Њ–і–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ–Њ—Б–ї–µ —В–µ—А–∞–њ–Є–Є –∞–Љ–±—А–Њ–Ї—Б–Њ–ї–Њ–Љ –і–Њ–Ј–∞ –Љ–µ—В–∞—Е–Њ–ї–Є–љ–∞, —Б–њ–Њ—Б–Њ–±–љ–∞—П –≤—Л–Ј–≤–∞—В—М –±—А–Њ–љ—Е–Њ—Б–њ–∞–Ј–Љ (–њ—А–Њ–≤–Њ–Ї–∞—Ж–Є–Њ–љ–љ–∞—П –і–Њ–Ј–∞), —Б—В–∞–ї–∞ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –≤—Л—И–µ, —З–µ–Љ –і–Њ –љ–∞—З–∞–ї–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, —З—В–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤–Њ–≤–∞–ї–Њ –Њ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–∞ —Б–љ–Є–ґ–∞—В—М –≥–Є–њ–µ—А—А–µ–∞–Ї—В–Є–≤–љ–Њ—Б—В—М –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–≥–Њ –і–µ—А–µ–≤–∞ –≤ –Њ—В–≤–µ—В –љ–∞ —А–∞–Ј–і—А–∞–ґ–∞—О—Й–Є–µ —Б—В–Є–Љ—Г–ї—Л. –Ф–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –Љ–µ–ґ–і—Г –њ—А–Њ–≤–Њ–Ї–∞—Ж–Є–Њ–љ–љ–∞–Љ–Є –і–Њ–Ј–∞–Љ–Є –Љ–µ—В–∞—Е–Њ–ї–Є–љ–∞ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –њ–ї–∞—Ж–µ–±–Њ –≤—Л—П–≤–ї–µ–љ–Њ –љ–µ –±—Л–ї–Њ [18].
–Р–Љ–±—А–Њ–Ї—Б–Њ–ї —Б–њ–Њ—Б–Њ–±–µ–љ –Њ–Ї–∞–Ј—Л–≤–∞—В—М –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ. –Ю–љ —Б–њ–Њ—Б–Њ–±–µ–љ –Є–љ–≥–Є–±–Є—А–Њ–≤–∞—В—М –њ—А–Њ–і—Г–Ї—Ж–Є—О –Є–љ—В–µ—А–ї–µ–є–Ї–Є–љ–∞ 1 (–Ш–Ы-1) –Є —Д–∞–Ї—В–Њ—А–∞ –љ–µ–Ї—А–Њ–Ј–∞ –Њ–њ—Г—Е–Њ–ї–Є –∞–ї—М—Д–∞ (–§–Э–Ю-α) [21]. –Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –Ш–Ы-1 –Є –§–Э–Ю-α –Є–≥—А–∞—О—В –≤–∞–ґ–љ—Г—О —А–Њ–ї—М –≤ —А–∞–Ј–≤–Є—В–Є–Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞. –°—А–µ–і–Є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —В–Њ–ї—М–Ї–Њ —Г –≥–ї—О–Ї–Њ–Ї–Њ—А—В–Є–Ї–Њ—Б—В–µ—А–Њ–Є–і–Њ–≤ –і–Њ–Ї–∞–Ј–∞–љ–∞ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —Г–Љ–µ–љ—М—И–∞—В—М —Б–Є–љ—В–µ–Ј –і–∞–љ–љ—Л—Е –њ—А–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Љ–µ–і–Є–∞—В–Њ—А–Њ–≤ –Ї–ї–µ—В–Ї–∞–Љ–Є —Б–Є—Б—В–µ–Љ—Л –Љ–Њ–љ–Њ–љ—Г–Ї–ї–µ–∞—А–љ—Л—Е —Д–∞–≥–Њ—Ж–Є—В–Њ–≤ [22]. –Т —Е–Њ–і–µ –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–≥–Њ J.A. Kern –Є —Б–Њ–∞–≤—В. (1988) –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –і–Њ–Ї–∞–Ј–∞–љ–∞ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –∞–Љ–±—А–Њ–Ї—Б–Њ–ї–∞ —Г–Љ–µ–љ—М—И–∞—В—М —Б–Є–љ—В–µ–Ј –Ш–Ы-1 –Є –§–Э–Ю-α –Ї–ї–µ—В–Ї–∞–Љ–Є –Љ–Њ–љ–Њ—Ж–Є—В–∞—А–љ–Њ-–Љ–∞–Ї—А–Њ—Д–∞–≥–∞–ї—М–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л, —В–µ–Љ —Б–∞–Љ—Л–Љ —Б–љ–Є–ґ–∞—П —Б—В–µ–њ–µ–љ—М –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –њ—А–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–Њ—Ж–µ—Б—Б–∞—Е. –Я—А–Є –≤—Л—П—Б–љ–µ–љ–Є–Є –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞ –і–∞–љ–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –∞–Љ–±—А–Њ–Ї—Б–Њ–ї–∞ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ—А–µ–њ–∞—А–∞—В –і–µ–є—Б—В–≤—Г–µ—В –∞–љ–∞–ї–Њ–≥–Є—З–љ–Њ —Б—В–µ—А–Њ–Є–і–љ—Л–Љ –≥–Њ—А–Љ–Њ–љ–∞–Љ [23].
–Р–Љ–±—А–Њ–Ї—Б–Њ–ї —Б–њ–Њ—Б–Њ–±–µ–љ –Є–љ–≥–Є–±–Є—А–Њ–≤–∞—В—М –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є–µ –≥–Є—Б—В–∞–Љ–Є–љ–∞, –ї–µ–є–Ї–Њ—В—А–Є–µ–љ–Њ–≤ –Є —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤ –Є–Ј –ї–µ–є–Ї–Њ—Ж–Є—В–Њ–≤ –Є —В—Г—З–љ—Л—Е –Ї–ї–µ—В–Њ–Ї [24]. –Ф–∞–љ–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Г–Ї–∞–Ј–∞–ї–Њ –љ–∞ –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–µ –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ—Л–µ –Є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –∞–Љ–±—А–Њ–Ї—Б–Њ–ї–∞. –Т —Е–Њ–і–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –∞–Љ–±—А–Њ–Ї—Б–Њ–ї —Б–њ–Њ—Б–Њ–±–µ–љ —Г–Љ–µ–љ—М—И–∞—В—М –≤—Л–±—А–Њ—Б –≥–Є—Б—В–∞–Љ–Є–љ–∞ –Є–Ј —В—Г—З–љ—Л—Е –Ї–ї–µ—В–Њ–Ї –њ–Њ–і –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ–Љ —А–∞–Ј–ї–Є—З–љ—Л—Е –Є–Љ–Љ—Г–љ–љ—Л—Е –Є –љ–µ–Є–Љ–Љ—Г–љ–љ—Л—Е —Б—В–Є–Љ—Г–ї–Њ–≤, —В–µ–Љ —Б–∞–Љ—Л–Љ –≤–ї–Є—П—П –љ–∞ —А–∞–Ј–≤–Є—В–Є–µ —А–µ–∞–Ї—Ж–Є–Є –≥–Є–њ–µ—А—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –љ–µ–Љ–µ–і–ї–µ–љ–љ–Њ–≥–Њ —В–Є–њ–∞. –Т–Њ–Ј–і–µ–є—Б—В–≤—Г—П –љ–∞ –±–∞–Ј–Њ—Д–Є–ї—Л, –Љ–Њ–љ–Њ—Ж–Є—В—Л –Є –љ–µ–є—В—А–Њ—Д–Є–ї—Л, –∞–Љ–±—А–Њ–Ї—Б–Њ–ї —Б–њ–Њ—Б–Њ–±–µ–љ –≤–ї–Є—П—В—М –љ–∞ –њ–Њ–Ј–і–љ—О—О —Д–∞–Ј—Г –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П, –≤ —В.—З. –Є –≤ —В–Ї–∞–љ—П—Е –Ј–∞ –њ—А–µ–і–µ–ї–∞–Љ–Є –ї–µ–≥–Ї–Є—Е. –Т –±–∞–Ј–Њ—Д–Є–ї–∞—Е –∞–Љ–±—А–Њ–Ї—Б–Њ–ї –Є–љ–≥–Є–±–Є—А—Г–µ—В –љ–µ —В–Њ–ї—М–Ї–Њ –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є–µ –≥–Є—Б—В–∞–Љ–Є–љ–∞, –љ–Њ –Є –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –Є–љ—В–µ—А–ї–µ–є–Ї–Є–љ–Њ–≤ 1 –Є 3. –Т–Њ–Ј–і–µ–є—Б—В–≤—Г—П –љ–∞ –≥—А–∞–љ—Г–ї–Њ—Ж–Є—В—Л, –њ—А–µ–њ–∞—А–∞—В —Б–њ–Њ—Б–Њ–±–µ–љ —Г–Љ–µ–љ—М—И–∞—В—М –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –≤ –љ–Є—Е —Б—Г–њ–µ—А–Њ–Ї—Б–Є–і-–∞–љ–Є–Њ–љ–∞ –Є LT B4. –Т –∞–љ–∞–ї–Њ–≥–Є—З–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –∞–Љ–±—А–Њ–Ї—Б–Њ–ї —Б–њ–Њ—Б–Њ–±–µ–љ —Г–Љ–µ–љ—М—И–∞—В—М –њ—А–Њ–і—Г–Ї—Ж–Є—О –§–Э–Ю-α, –Є–љ—В–µ—А–ї–µ–є–Ї–Є–љ–∞ 2, –Є–љ—В–µ—А—Д–µ—А–Њ–љ–∞-–≥–∞–Љ–Љ–∞ –Љ–Њ–љ–Њ–љ—Г–Ї–ї–µ–∞—А–љ—Л–Љ–Є –Ї–ї–µ—В–Ї–∞–Љ–Є [25, 26], –Ї—А–Њ–Љ–µ —В–Њ–≥–Њ, –Њ–љ —Б–њ–Њ—Б–Њ–±–µ–љ –Є–љ–≥–Є–±–Є—А–Њ–≤–∞—В—М –∞–Ї—В–Є–≤–∞—Ж–Є—О –§–Ы –Р2 [27, 28].
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –љ–∞ —А–Њ—Б—Б–Є–є—Б–Ї–Њ–Љ —А—Л–љ–Ї–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –∞–Љ–±—А–Њ–Ї—Б–Њ–ї–∞ –Љ–љ–Њ–≥–Њ, –Њ–і–Є–љ –Є–Ј –љ–Є—Е –і–Њ—Б—В—Г–њ–µ–љ –њ–Њ–і –љ–µ–Љ–µ—Ж–Ї–Њ–є —В–Њ—А–≥–Њ–≤–Њ–є –Љ–∞—А–Ї–Њ–є –Р–Љ–±—А–Њ–±–µ–љ–µ. –Я—А–µ–њ–∞—А–∞—В –≤—Л–њ—Г—Б–Ї–∞–µ—В—Б—П –Ї–∞–Ї –≤ —Д–Њ—А–Љ–µ —Б–Є—А–Њ–њ–∞ –Є —В–∞–±–ї–µ—В–Њ–Ї, —В–∞–Ї –Є –≤ –≤–Є–і–µ —А–∞—Б—В–≤–Њ—А–∞ –і–ї—П –њ—А–Є–µ–Љ–∞ –≤–љ—Г—В—А—М –Є –Є–љ–≥–∞–ї—П—Ж–Є–є, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –µ–≥–Њ —Г –і–µ—В–µ–є —А–∞–Ј–ї–Є—З–љ—Л—Е –≤–Њ–Ј—А–∞—Б—В–љ—Л—Е –≥—А—Г–њ–њ. –Т –≤–Є–і–µ —Б–Є—А–Њ–њ–∞, —Б–Њ–і–µ—А–ґ–∞—Й–µ–≥–Њ 0,3 –≥ –∞–Љ–±—А–Њ–Ї—Б–Њ–ї–∞ –≤ 100 –Љ–ї, –њ—А–µ–њ–∞—А–∞—В —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –њ—А–Є–љ–Є–Љ–∞—В—М –њ–Њ—Б–ї–µ –µ–і—Л, –Ј–∞–њ–Є–≤–∞—П –і–Њ—Б—В–∞—В–Њ—З–љ—Л–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ–Љ –ґ–Є–і–Ї–Њ—Б—В–Є:
• –і–µ—В—П–Љ –і–Њ 2 –ї–µ—В —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ–Љ–∞—П –і–Њ–Ј–∞ —Б–Њ—Б—В–∞–≤–ї—П–µ—В 2,5 –Љ–ї —Б–Є—А–Њ–њ–∞ 2 —А–∞–Ј–∞/—Б—Г—В. (15 –Љ–≥ –∞–Љ–±—А–Њ–Ї—Б–Њ–ї–∞ –≤ —Б—Г—В.);
• –і–µ—В—П–Љ –Њ—В 2 –і–Њ 6 –ї–µ—В – 2,5 –Љ–ї —Б–Є—А–Њ–њ–∞ 3 —А–∞–Ј–∞/—Б—Г—В. (22,5 –Љ–≥ –∞–Љ–±—А–Њ–Ї—Б–Њ–ї–∞ –≤ —Б—Г—В.);
• –і–µ—В—П–Љ –Њ—В 6 –і–Њ 12 –ї–µ—В – 5 –Љ–ї —Б–Є—А–Њ–њ–∞ 2–3 —А–∞–Ј–∞/—Б—Г—В. (30–45 –Љ–≥ –∞–Љ–±—А–Њ–Ї—Б–Њ–ї–∞ –≤ —Б—Г—В.);
• –≤–Ј—А–Њ—Б–ї—Л–Љ –Є –і–µ—В—П–Љ —Б—В–∞—А—И–µ 12 –ї–µ—В – –≤ –њ–µ—А–≤—Л–µ 2–3 –і–љ—П –ї–µ—З–µ–љ–Є—П —Б–ї–µ–і—Г–µ—В –њ—А–Є–љ–Є–Љ–∞—В—М –њ–Њ 10 –Љ–ї —Б–Є—А–Њ–њ–∞ 3 —А–∞–Ј–∞/—Б—Г—В. (90 –Љ–≥ –∞–Љ–±—А–Њ–Ї—Б–Њ–ї–∞ –≤ —Б—Г—В.). –Я—А–Є –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —В–µ—А–∞–њ–Є–Є –≤–Ј—А–Њ—Б–ї—Л–µ –Љ–Њ–≥—Г—В —Г–≤–µ–ї–Є—З–Є—В—М –і–Њ–Ј—Г –і–Њ 20 –Љ–ї —Б–Є—А–Њ–њ–∞ 2 —А–∞–Ј–∞/—Б—Г—В. (120 –Љ–≥ –∞–Љ–±—А–Њ–Ї—Б–Њ–ї–∞ –≤ —Б—Г—В.). –Т –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–µ –і–љ–Є –і–Њ–Ј–∞ –њ—А–µ–њ–∞—А–∞—В–∞ —Б–љ–Є–ґ–∞–µ—В—Б—П –і–Њ 10 –Љ–ї —Б–Є—А–Њ–њ–∞ 2 —А–∞–Ј–∞/—Б—Г—В. (60 –Љ–≥ –∞–Љ–±—А–Њ–Ї—Б–Њ–ї–∞ –≤ —Б—Г—В.).
–°–Є—А–Њ–њ –Р–Љ–±—А–Њ–±–µ–љ–µ –љ–µ —Б–Њ–і–µ—А–ґ–Є—В –Ј–∞–≥—Г—Б—В–Є—В–µ–ї–Є –Є –Ї–Њ–љ—Б–µ—А–≤–∞–љ—В—Л, —З—В–Њ —П–≤–ї—П–µ—В—Б—П –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–Љ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ–Љ —Б —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–∞.
–Ф–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П –і–Њ–ї–ґ–љ–∞ –њ–Њ–і–±–Є—А–∞—В—М—Б—П –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ–Њ –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —В–µ—З–µ–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є —Б—В—А–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї–Є—А–Њ–≤–∞—В—М—Б—П –≤—А–∞—З–Њ–Љ.




–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –Ъ–Њ—А–Њ–≤–Є–љ–∞ –Э.–Р., –Ч–∞—Е–∞—А–Њ–≤–∞ –Ш.–Э., –Ч–∞–њ–ї–∞—В–љ–Є–Ї–Њ–≤ –Р.–Ы., –Ю–≤—Б—П–љ–љ–Є–Ї–Њ–≤–∞ –Х.–Ь. –Ъ–∞—И–µ–ї—М —Г –і–µ—В–µ–є. –Я—А–Њ—В–Є–≤–Њ–Ї–∞—И–ї–µ–≤—Л–µ –Є –Њ—В—Е–∞—А–Ї–Є–≤–∞—О—Й–Є–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞ –≤ –њ–µ–і–Є–∞—В—А–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ. –Я–Њ—Б–Њ–±–Є–µ –і–ї—П –≤—А–∞—З–µ–є. –Ь., 2000. 56 —Б.
2. –Ґ–∞—В–Њ—З–µ–љ–Ї–Њ –Т. –Ъ. –Ф–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ–∞—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Ї–∞—И–ї—П —Г –і–µ—В–µ–є –Є –µ–≥–Њ –ї–µ—З–µ–љ–Є–µ // –Ы–µ—З–∞—Й–Є–є –≤—А–∞—З. 2008. вДЦ 3. –°. 15–19.
3. –®–Љ–µ–ї–µ–≤ –Х.–Ш. –Ъ–∞—И–µ–ї—М –њ—А–Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –ї–µ–≥–Ї–Є—Е: –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Є –ї–µ—З–µ–љ–Є–µ. –Ь.: –¶–Э–Ш–Ш–Ґ, 2009.
4. –Ч–∞—Е–∞—А–Њ–≤–∞ –Ш.–Э., –Ф–Љ–Є—В—А–Є–µ–≤–∞ –Ѓ.–Р. –Ъ–∞—И–µ–ї—М —Г –і–µ—В–µ–є: –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ–∞—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Є —В–∞–Ї—В–Є–Ї–∞ –ї–µ—З–µ–љ–Є—П // Consilium medicum. –Я—А–Є–ї–Њ–ґ–µ–љ–Є–µ «–Я–µ–і–Є–∞—В—А–Є—П». 2010. вДЦ 1. –°. 31–37.
5. –У–µ–њ–њ–µ –Э.–Р., –°–љ–µ–≥–Њ—Ж–Ї–∞—П –Ь.–Э. –Ъ–∞—И–µ–ї—М —Г –і–µ—В–µ–є. –Т–Њ–њ—А–Њ—Б—Л –Є –Њ—В–≤–µ—В—Л. –Я–Њ—Б–Њ–±–Є–µ –і–ї—П –≤—А–∞—З–µ–є. –Ь.: –Ь–Ь–Р –Є–Љ. –Ш.–Ь.–°–µ—З–µ–љ–Њ–≤–∞. 17 —Б.
6. –°–∞–Љ—Б—Л–≥–Є–љ–∞ –У.–Р. –Ю–± –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –Љ—Г–Ї–Њ–ї–Є—В–Є–Ї–Њ–≤ –≤ –ї–µ—З–µ–љ–Є–Є –Ї–∞—И–ї—П —Г –і–µ—В–µ–є// –Ґ—А—Г–і–љ—Л–є –њ–∞—Ж–Є–µ–љ—В. 2004. –Ґ. 2, вДЦ 9. –°. 39–42.
7. –Ъ–ї—П—З–Ї–Є–љ–∞ –Ш.–Ы. –Х—Й–µ —А–∞–Ј –Њ –Љ—Г–Ї–Њ–ї–Є—В–Є–Ї–∞—Е // Consilium medicum. –Ґ.10. вДЦ 3. –°. 121–124.
8. –У–µ–њ–њ–µ –Э.–Р., –°–љ–µ–≥–Њ—Ж–Ї–∞—П –Ь.–Э. –Т–Њ–њ—А–Њ—Б—Л –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є —В–µ—А–∞–њ–Є–Є –Ї–∞—И–ї—П —Г –і–µ—В–µ–є // Consilium medicum. –Я—А–Є–ї–Њ–ґ–µ–љ–Є–µ «–Я–µ–і–Є–∞—В—А–Є—П». вДЦ 2. –°.19–22.
9. –Ъ–Њ—Б–µ–љ–Ї–Њ –Ш.–Ь. –Ь—Г–Ї–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–µ –њ—А–Є–њ–∞—А–∞—В—Л –≤ —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ // Consilium medicum. –Я—А–Є–ї–Њ–ґ–µ–љ–Є–µ «–Я–µ–і–Є–∞—В—А–Є—П». 2010. вДЦ 1. –°. 52–58.
10. Olivieri D., Zavattini G., Daniotti G. et al. Ambroxol for the prevention of chronic bronchitis exacerbations, long-term multicenter trial // Respiration. 1987. Vol. 51( Suppl.1). P. 42–51.
11. Peralta J., Paderoso J.J., Corazza C. et al. Ambtoxol plus amoxicillin in the treatment of exacerbation of chronic bronchitis //Arzneim.-Forsch.// Drug Res. 1987. Vol. 37 (II), вДЦ.8.
12. Spatolo J., Paderoso J.J., Wiemeyer J.C.M. et al. // Arzneim.-Forsch.// Drug Res. 1987. Vol. 37 (II). P. 965.
13. Gene R., Paderoso J.J., Corazza C., Lasala M.B. et al. // Arzneim.-Forsch.// Drug Res. 1987. Vol. 37 (II). P. 967.
14. Franschini F., Scaglione F. et al. Effects of a mucolytic agent on the bioavailability of antibiotics in patients with chronic respiratory diseases // Current therapeutic research. 1988.Vol. 43, вДЦ 4.
15. Braga P.C., Scaglione F., Scarpazza G. et al. //Comparison of amoxicillin combined with carbocisteine an amoxicillin alone in pathological bronchial secretions and pulmonary tissue // Int. J. Clin. Pharmacol. Res. 1985. Vol. 5. P. 331–340.
16. Fraschini F., D’orsi S., Falchi M. et al. Therapy of respiratory tract infections joined to hypersecretion: criteria for the combined use of antibiotics and mucolytics // Curr. Ther. Res. 1986. Vol. 40. P. 941–947.
17. Princioi N., Zavattini G., Daniotti S. Possibility of interaction among antibiotics and mucolytics in children // Int. J.Clin.Pharm.Res. 1986.VI (5). P. 369–372.
18. Melilio G., Cocco G. Ambroxol decreases bronchial hyperreactivity // Eur. J. Respir. Dis. 1986. Vol. 69. P. 316–320.
19. Strittmatter W.J., Hirata F., Axelrod J. Phospholipid methylation unmasks cryptic beta-adrenergic receptors in rat reticulocytes // Science. 1979. Vol. 204. P. 1205–1207.
20. Nath P., Joshi S.P., Agrawal K.P. Biochemical correlates of airway hyperreactivity in guinea pigs: role of lysophosphotidyl choline // J. Allergy Clin. Immunol. 1983. Vol. 72. P. 351–358.
21. Bianchi M., Mantovani A., Erroi A. et al. Ambroxol inhibits interleukin 1 and tumor necrosis factor production in human mononuclear cells // Agents and actions. 1990.Vol. 31.
22. Snyder D.S., Unanue E.R. Corticosteroids inhibit murine macrophage Ia expression and interleukin 1 production // J. Immunol. 1982. Vol. 129. P. 1803–1805.
23. Kern J.A., Lamb R.J. et al. Dexamethasone inhibition of interleukin 1 beta production by human monocytes. Posttranscriptional mechanisms // J. Clin. Invest. 1988. Vol. 81. P. 237–244.
24. Gibbs B.F., Schmutzler W. et al. Ambroxol inhibits the release of histamine, leukotrienes and cytokines from human leukocytes and mast cells // Inflamm.res.48. 1999. P. 86–93.
25. Pairel M., Engelmann P. et al. Ambroxol improves the broncho-spasmolytic activity of clenbuterol in guinea-pig // J. Pharm. Pharmacol. 1997. Vol. 49. P. 184–186.
26. Pfeifer S., Zissel G., Kienst K. Reduction of cytokine release of blood bronchoalveolar mononuclear cells by ambroxol // Eur. J. Res. 1997. Vol. 2. P. 129–132.
27. Pairel M., Engelmann P. et al. Ambroxol improves the broncho-spasmolytic activity of clenbuterol in guinea-pig // J. Pharm. Pharmacol. 1997. Vol. 49. P. 184–186.
28. Heath M.F., Jacbson W. The inhibition of lysosomal phospholipase A from rabbit lung by ambroxol and its consequences for pulmonary surfactant // Lung. 1985. Vol. 163. P. 337–344.











