–Т –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–Є, –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–Љ —В–µ—З–µ–љ–Є–Є –Є –Є—Б—Е–Њ–і–µ –њ–µ—А–Є–љ–∞—В–∞–ї—М–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є —Г –љ–Њ–≤–Њ—А–Њ–ґ–і–µ–љ–љ—Л—Е –і–µ—В–µ–є —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Г—О —А–Њ–ї—М –Є–≥—А–∞–µ—В —Б–Њ—Б—В–Њ—П–љ–Є–µ –Є–Љ–Љ—Г–љ–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л [4–5], –њ–Њ—Н—В–Њ–Љ—Г –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є —В–∞–Ї–Є—Е –±–Њ–ї—М–љ—Л—Е –љ–µ–Љ–∞–ї–Њ–≤–∞–ґ–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ–µ—В –Є–Љ–Љ—Г–љ–Њ—В—А–Њ–њ–љ–∞—П —В–µ—А–∞–њ–Є—П.
–Ф–ї—П –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –Њ–±—К–µ–Љ–∞ –Є –≤–Є–і–∞ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –≤–∞–ґ–љ–Њ —Г—З–Є—В—Л–≤–∞—В—М –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –Є—Е —А–∞–Ј–≤–Є—В–Є—П –Є –≤–ї–Є—П–љ–Є–µ –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–≤ –љ–∞ –Є–Љ–Љ—Г–љ–љ—Г—О —Б–Є—Б—В–µ–Љ—Г –љ–Њ–≤–Њ—А–Њ–ґ–і–µ–љ–љ–Њ–≥–Њ —А–µ–±–µ–љ–Ї–∞.
–°–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –њ–Њ–і—Е–Њ–і—Л –Ї –Є–Љ–Љ—Г–љ–Њ–Љ–Њ–і—Г–ї–Є—А—Г—О—Й–µ–є —В–µ—А–∞–њ–Є–Є –њ–µ—А–Є–љ–∞—В–∞–ї—М–љ—Л—Е –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є –≤–Ї–ї—О—З–∞—О—В –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Є–Љ–Љ—Г–љ–Њ–±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П, —В–∞–Ї–Є—Е –Ї–∞–Ї –њ—А–µ–њ–∞—А–∞—В—Л —А–µ–Ї–Њ–Љ–±–Є–љ–∞–љ—В–љ—Л—Е —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤, –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ–Њ–≤, —Б —Г—З–µ—В–Њ–Љ –Є—Е –Ј–љ–∞—З–Є–Љ–Њ—Б—В–Є –≤ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П [6].
–Ъ–Є–њ—Д–µ—А–Њ–љ® —Б—Г–њ–њ–Њ–Ј–Є—В–Њ—А–Є–Є –і–ї—П –≤–∞–≥–Є–љ–∞–ї—М–љ–Њ–≥–Њ –Є–ї–Є —А–µ–Ї—В–∞–ї—М–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—О –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–≥–Њ –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ–Њ–≤–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ (–Ъ–Ш–Я) –≤ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ 60 –Љ–≥, —Б–Њ–і–µ—А–ґ–∞—Й–µ–≥–Њ –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ—Л —В—А–µ—Е –Њ—Б–љ–Њ–≤–љ—Л—Е –Ї–ї–∞—Б—Б–Њ–≤ – G, –Р –Є –Ь, –Є —А–µ–Ї–Њ–Љ–±–Є–љ–∞–љ—В–љ–Њ–≥–Њ —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Њ–≥–Њ –Є–љ—В–µ—А—Д–µ—А–Њ–љ–∞ –∞–ї—М—Д–∞–2b, –љ–µ –Љ–µ–љ–µ–µ 500 —В—Л—Б. –Ь–Х.
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є –њ—А–∞–Ї—В–Є–Ї–∞ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ъ–Є–њ—Д–µ—А–Њ–љ–∞® –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –≤ –њ—А–µ–њ–∞—А–∞—В–µ —Б–Њ—З–µ—В–∞–µ—В—Б—П –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–µ, –њ—А–Њ—В–Є–≤–Њ–≤–Є—А—Г—Б–љ–Њ–µ, –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–µ –Є –Є–Љ–Љ—Г–љ–Њ–Љ–Њ–і—Г–ї–Є—А—Г—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ. –Я—А–Њ—В–Є–≤–Њ–≤–Є—А—Г—Б–љ—Л–є –Є –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В—Л –њ—А–µ–њ–∞—А–∞—В–∞ –њ—А–Њ—П–≤–ї—П—О—В—Б—П –Ї–∞–Ї –≤–Њ –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ–Њ–є, —В–∞–Ї –Є –≤–љ–µ–Ї–ї–µ—В–Њ—З–љ–Њ–є —Б—А–µ–і–µ –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –Ј–∞ —Б—З–µ—В –њ—А—П–Љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –љ–∞ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –Ї–ї–µ—В–Њ—З–љ–Њ–≥–Њ –Є –≥—Г–Љ–Њ—А–∞–ї—М–љ–Њ–≥–Њ –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞ [10]. –®–Є—А–Њ–Ї–Є–є —Б–њ–µ–Ї—В—А –∞–љ—В–Є—В–µ–ї –≤ —Б–Њ—Б—В–∞–≤–µ –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ–Њ–≤ –Ъ–Ш–Я–∞ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ—А–µ–њ–∞—А–∞—В—Г –∞–Ї—В–Є–≤–љ–Њ –і–µ–є—Б—В–≤–Њ–≤–∞—В—М –љ–∞ —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–љ—Л–µ –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤.
–¶–µ–ї—М—О —А–∞–±–Њ—В—Л —П–≤–Є–ї–Њ—Б—М –Є–Ј—Г—З–µ–љ–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –Ъ–Є–њ—Д–µ—А–Њ–љ–∞® –≤ —В–µ—А–∞–њ–Є–Є –њ–µ—А–Є–љ–∞—В–∞–ї—М–љ—Л—Е –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є —Г –љ–Њ–≤–Њ—А–Њ–ґ–і–µ–љ–љ—Л—Е –і–µ—В–µ–є —Б –Ј–∞–і–µ—А–ґ–Ї–Њ–є –≤–љ—Г—В—А–Є—Г—В—А–Њ–±–љ–Њ–≥–Њ —А–∞–Ј–≤–Є—В–Є—П.
–Ь–∞—В–µ—А–Є–∞–ї—Л –Є –Љ–µ—В–Њ–і—Л
–Я–Њ–і –љ–∞–±–ї—О–і–µ–љ–Є–µ–Љ –љ–∞—Е–Њ–і–Є–ї–Є—Б—М 32 –і–Њ–љ–Њ—И–µ–љ–љ—Л—Е –љ–Њ–≤–Њ—А–Њ–ґ–і–µ–љ–љ—Л—Е —А–µ–±–µ–љ–Ї–∞ —Б –Ј–∞–і–µ—А–ґ–Ї–Њ–є –≤–љ—Г—В—А–Є—Г—В—А–Њ–±–љ–Њ–≥–Њ —А–∞–Ј–≤–Є—В–Є—П, —Г –Ї–Њ—В–Њ—А—Л—Е –±—Л–ї–Є –і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞–љ—Л –њ–µ—А–Є–љ–∞—В–∞–ї—М–љ—Л–µ –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є – —Ж–Є—В–Њ–Љ–µ–≥–∞–ї–Њ–≤–Є—А—Г—Б–љ–∞—П (–¶–Ь–Т–Ш), —Е–ї–∞–Љ–Є–і–Є–є–љ–∞—П –Є –Љ–Є–Ї—Б—В––Є–љ—Д–µ–Ї—Ж–Є—П (—Е–ї–∞–Љ–Є–і–Є–є–љ–Њ–—Ж–Є—В–Њ–Љ–µ–≥–∞–ї–Њ–≤–Є—А—Г—Б–љ–∞—П). –Ф–Є–∞–≥–љ–Њ–Ј –Є–љ—Д–µ–Ї—Ж–Є–є –≤–µ—А–Є—Д–Є—Ж–Є—А–Њ–≤–∞–ї–Є –Љ–µ—В–Њ–і–∞–Љ–Є –њ–Њ–ї–Є–Љ–µ—А–∞–Ј–љ–Њ–є —Ж–µ–њ–љ–Њ–є —А–µ–∞–Ї—Ж–Є–Є (–Я–¶–†) –Є –Є–Љ–Љ—Г–љ–Њ—Д–µ—А–Љ–µ–љ—В–љ–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ (–Ш–§–Р). –Ш–і–µ–љ—В–Є—Д–Є–Ї–∞—Ж–Є—П –Ф–Э–Ъ Cytomegalovirus, Chlamydia trachomatis –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–ї–∞—Б—М –≤ –Њ–±—А–∞–Ј—Ж–∞—Е –Ї—А–Њ–≤–Є –Љ–µ—В–Њ–і–Њ–Љ –Я–¶–†––∞–Љ–њ–ї–Є—Д–Є–Ї–∞—Ж–Є–Є –љ–∞ —В–µ—А–Љ–Њ—Ж–Є–Ї–ї–µ—А–µ «Gradient Palm Cycler» («Corbett Research», –Р–≤—Б—В—А–∞–ї–Є—П). –Ф–µ—В–µ–Ї—Ж–Є—П –њ—А–Њ–і—Г–Ї—В–Њ–≤ –Я–¶–†––∞–Љ–њ–ї–Є—Д–Є–Ї–∞—Ж–Є–Є –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М –Љ–µ—В–Њ–і–∞–Љ–Є —Д–Њ—А–µ–Ј–∞ –Є —Д–ї—О–Њ—А–µ—Б—Ж–µ–љ—Ж–Є–Є –љ–∞ –∞–њ–њ–∞—А–∞—В–µ Molecular Imager Gel Doc–XR 170–8170 (Bio–RAD) —Б –њ–Њ–Љ–Њ—Й—М—О –љ–∞–±–Њ—А–∞ —А–µ–∞–≥–µ–љ—В–Њ–≤ «–Р–Љ–њ–ї–Є –°–µ–љ—Б» (–§–У–£–Э «–¶–Э–Ш–Ш–≠» –†–Њ—Б–њ–Њ—В—А–µ–±–љ–∞–і–Ј–Њ—А–∞, –≥. –Ь–Њ—Б–Ї–≤–∞). –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–Њ–≤–Њ–і–Є–ї–Є—Б—М –љ–∞ –±–∞–Ј–µ –Я–¶–†––ї–∞–±–Њ—А–∞—В–Њ—А–Є–Є –†–µ—Б–њ—Г–±–ї–Є–Ї–∞–љ—Б–Ї–Њ–≥–Њ –Ї–Њ–ґ–љ–Њ––≤–µ–љ–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –і–Є—Б–њ–∞–љ—Б–µ—А–∞ –Ь–Ч –£–і–Љ—Г—А—В—Б–Ї–Њ–є –†–µ—Б–њ—Г–±–ї–Є–Ї–Є.
–°–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–µ –∞–љ—В–Є—В–µ–ї–∞ –Ї–ї–∞—Б—Б–∞ G –Є M –Ї –≤—Л—И–µ–њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л–Љ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П–Љ –Њ–њ—А–µ–і–µ–ї—П–ї–Є—Б—М –Љ–µ—В–Њ–і–Њ–Љ –Ш–§–Р. –°–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–Њ–≤–Њ–і–Є–ї–Є—Б—М –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –ї–∞–±–Њ—А–∞—В–Њ—А–Є–Є –†–µ—Б–њ—Г–±–ї–Є–Ї–∞–љ—Б–Ї–Њ–є –і–µ—В—Б–Ї–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї—М–љ–Є—Ж—Л –Ь–Ч –£–і–Љ—Г—А—В—Б–Ї–Њ–є –†–µ—Б–њ—Г–±–ї–Є–Ї–Є –љ–∞ –Є–Љ–Љ—Г–љ–Њ—Д–µ—А–Љ–µ–љ—В–љ–Њ–Љ –∞–љ–∞–ї–Є–Ј–∞—В–Њ—А–µ «Digiscan» (–Р–≤—Б—В—А–Є—П) —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –љ–∞–±–Њ—А–∞ —А–µ–∞–≥–µ–љ—В–Њ–≤ «–Т–µ–Ї—В–Њ—А––С–µ—Б—В» (–≥. –Э–Њ–≤–Њ—Б–Є–±–Є—А—Б–Ї).
–Я–∞—Ж–Є–µ–љ—В—Л –±—Л–ї–Є —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ—Л –љ–∞ –і–≤–µ –≥—А—Г–њ–њ—Л: –Њ—Б–љ–Њ–≤–љ–∞—П – 17 –љ–Њ–≤–Њ—А–Њ–ґ–і–µ–љ–љ—Л—Е –і–µ—В–µ–є, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –≤ —Б–Њ—Б—В–∞–≤–µ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Ъ–Є–њ—Д–µ—А–Њ–љ®; –≥—А—Г–њ–њ–∞ —Б—А–∞–≤–љ–µ–љ–Є—П – 15 –љ–Њ–≤–Њ—А–Њ–ґ–і–µ–љ–љ—Л—Е –і–µ—В–µ–є, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–ї—Г—З–∞–ї–Є —В–Њ–ї—М–Ї–Њ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ—Г—О —В–µ—А–∞–њ–Є—О.
–Я—А–µ–њ–∞—А–∞—В –Ъ–Є–њ—Д–µ—А–Њ–љ® –љ–∞–Ј–љ–∞—З–∞–ї—Б—П –њ–Њ—Б–ї–µ –≤–µ—А–Є—Д–Є–Ї–∞—Ж–Є–Є –Є–љ—Д–µ–Ї—Ж–Є–Є (–≤ –≤–Њ–Ј—А–∞—Б—В–µ 12,7±1,4 –і–љ—П) –њ–Њ 1/2 —Б–≤–µ—З–Є —А–µ–Ї—В–∞–ї—М–љ–Њ 1 —А–∞–Ј/—Б—Г—В. –≤ —В–µ—З–µ–љ–Є–µ 10 –і–љ–µ–є.
–£ –і–µ—В–µ–є –Њ–±–µ–Є—Е –≥—А—Г–њ–њ –≤ –і–Є–љ–∞–Љ–Є–Ї–µ (10–14 –і–љ–µ–є –Є 20–24 –і–љ—П) –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ—Л –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Є–љ—В–µ—А–ї–µ–є–Ї–Є–љ–∞–4 (IL–4) –Є –Є–љ—В–µ—А—Д–µ—А–Њ–љ–∞–γ (IFN–γ) –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є; —Б–µ–Ї—А–µ—В–Њ—А–љ–Њ–≥–Њ IgA (sIgA) –Є —Б—Л–≤–Њ—А–Њ—В–Њ—З–љ—Л—Е IgA, Ig–Ь, IgG –≤ –Ї–Њ–њ—А–Њ—Д–Є–ї—М—В—А–∞—В–∞—Е.
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Г—А–Њ–≤–љ–µ–є IL–4 –Є IFN–γ –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –Љ–µ—В–Њ–і–Њ–Љ —В–≤–µ—А–і–Њ—Д–∞–Ј–љ–Њ–≥–Њ –Є–Љ–Љ—Г–љ–Њ—Д–µ—А–Љ–µ–љ—В–љ–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ (—В–µ—Б—В–—Б–Є—Б—В–µ–Љ—Л –Ш–§–Р–IL–4» –Є «–Ш–§–Р–IFN–gamma» –њ—А–Њ–Є–Ј–≤–Њ–і—Б—В–≤–∞ «–Ю–Ю–Ю «–¶–Є—В–Њ–Ї–Є–љ», –≥. –°–∞–љ–Ї—В––Я–µ—В–µ—А–±—Г—А–≥). –Р–љ–∞–ї–Є–Ј—Л –њ—А–Њ–≤–Њ–і–Є–ї–Є –≤ –ї–∞–±–Њ—А–∞—В–Њ—А–Є–Є –Є–Љ–Љ—Г–љ–Њ–≥–µ–љ–µ—В–Є–Ї–Є –§–У–£ «–Ь–µ–і–Є–Ї–Њ––≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–є –љ–∞—Г—З–љ—Л–є —Ж–µ–љ—В—А –†–Р–Ь–Э», –≥. –Ь–Њ—Б–Ї–≤–∞.
–Ъ–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–µ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ sIgA, —Б—Л–≤–Њ—А–Њ—В–Њ—З–љ—Л—Е IgA, Ig–Ь, IgG –≤ –Ї–Њ–њ—А–Њ—Д–Є–ї—М—В—А–∞—В–∞—Е –њ—А–Њ–≤–Њ–і–Є–ї–Є –Љ–µ—В–Њ–і–Њ–Љ —А–∞–і–Є–∞–ї—М–љ–Њ–є –Є–Љ–Љ—Г–љ–Њ–і–Є—Д—Д—Г–Ј–Є–Є (G. Mancini, –Р. Carbonara, 1965) –≤ –Ь–Њ—Б–Ї–Њ–≤—Б–Ї–Њ–Љ –Э–Ш–Ш —Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є–Є –Є –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є–Є –Є–Љ. –У.–Э. –У–∞–±—А–Є—З–µ–≤—Б–Ї–Њ–≥–Њ. –Т —А–∞–±–Њ—В–µ –њ—А–Є–Љ–µ–љ—П–ї–Є 2 —В–Є–њ–∞ –∞–љ—В–Є—Б—Л–≤–Њ—А–Њ—В–Њ–Ї: –∞–љ—В–Є—Б—Л–≤–Њ—А–Њ—В–Ї—Г –Ї α–—Ж–µ–њ–Є, –Ї–Њ—В–Њ—А–∞—П –≤—Л—П–≤–ї—П–µ—В —Б—Л–≤–Њ—А–Њ—В–Њ—З–љ—Л–є –Є —Б–µ–Ї—А–µ—В–Њ—А–љ—Л–є IgA, –Є –∞–љ—В–Є—Б—Л–≤–Њ—А–Њ—В–Ї—Г —Б —Б–µ–Ї—А–µ—В–Њ—А–љ–Њ–Љ—Г –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В—Г (sc), –Ї–Њ—В–Њ—А–∞—П –Њ–њ—А–µ–і–µ–ї—П–µ—В —В–Њ–ї—М–Ї–Њ —Б–µ–Ї—А–µ—В–Њ—А–љ—Л–є IgA. –Я—А–Њ–Є–Ј–≤–Њ–і–Є—В–µ–ї—М –∞–љ—В–Є—Б—Л–≤–Њ—А–Њ—В–Њ–Ї – –Ь–Њ—Б–Ї–Њ–≤—Б–Ї–Є–є –Э–Ш–Ш –≤–∞–Ї—Ж–Є–љ –Є —Б—Л–≤–Њ—А–Њ—В–Њ–Ї –Є–Љ. –Ш.–Ш. –Ь–µ—З–љ–Є–Ї–Њ–≤–∞.
–Ь–∞—В–µ–Љ–∞—В–Є—З–µ—Б–Ї—Г—О –Њ–±—А–∞–±–Њ—В–Ї—Г –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –њ—А–Њ–≤–Њ–і–Є–ї–Є –њ–Њ –Њ–±—Й–µ–њ—А–Є–љ—П—В—Л–Љ –Љ–µ—В–Њ–і–∞–Љ –≤–∞—А–Є–∞—Ж–Є–Њ–љ–љ–Њ–є —Б—В–∞—В–Є—Б—В–Є–Ї–Є. –Т—Л—З–Є—Б–ї—П–ї–Є —Б—А–µ–і–љ–Є–µ –≤–µ–ї–Є—З–Є–љ—Л –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є (–Ь), —Б—В–∞–љ–і–∞—А—В–љ—Л–µ –Њ—И–Є–±–Ї–Є —Б—А–µ–і–љ–Є—Е –≤–µ–ї–Є—З–Є–љ (m) –Є —Б—А–µ–і–љ–µ–µ –Ї–≤–∞–і—А–∞—В–Є—З–љ–Њ–µ –Њ—В–Ї–ї–Њ–љ–µ–љ–Є–µ (σ). –Ф–Њ—Б—В–Њ–≤–µ—А–љ–Њ—Б—В—М —А–∞–Ј–ї–Є—З–Є–є –Љ–µ–ґ–і—Г —Б—А–µ–і–љ–Є–Љ–Є –≤–µ–ї–Є—З–Є–љ–∞–Љ–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –≤ —Б—А–∞–≤–љ–Є–≤–∞–µ–Љ—Л—Е –≥—А—Г–њ–њ–∞—Е –Њ—Ж–µ–љ–Є–≤–∞–ї–Є —Б –њ–Њ–Љ–Њ—Й—М—О –Ї—А–Є—В–µ—А–Є—П –°—В—М—О–і–µ–љ—В–∞ – t. –†–∞–Ј–ї–Є—З–Є—П —Б—А–∞–≤–љ–Є–≤–∞–µ–Љ—Л—Е –≤–µ–ї–Є—З–Є–љ –њ—А–Є–Ј–љ–∞–≤–∞–ї–Є —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ–Є –њ—А–Є –≤–µ—А–Њ—П—В–љ–Њ—Б—В–Є 95% (—А<0,05) –Є –≤—Л—И–µ. –°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї—Г—О –Њ–±—А–∞–±–Њ—В–Ї—Г –њ–Њ–ї—Г—З–µ–љ–љ–Њ–≥–Њ –Љ–∞—В–µ—А–Є–∞–ї–∞ –њ—А–Њ–≤–Њ–і–Є–ї–Є —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –ї–Є—Ж–µ–љ–Ј–Є–Њ–љ–љ–Њ–є –њ—А–Њ–≥—А–∞–Љ–Љ—Л «BioStat 2009».
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Є –Њ–±—Б—Г–ґ–і–µ–љ–Є–µ
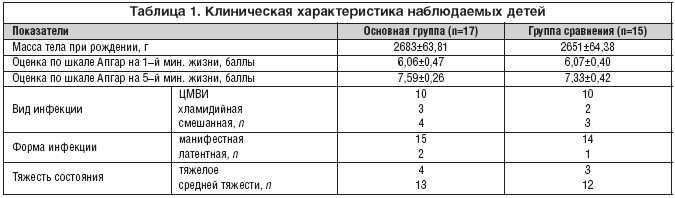
–Ф–µ—В–Є –Њ–±–µ–Є—Е –≥—А—Г–њ–њ –±—Л–ї–Є —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ—Л –њ–Њ –Њ—Б–љ–Њ–≤–љ—Л–Љ –њ–∞—А–∞–Љ–µ—В—А–∞–Љ – –≥–µ—Б—В–∞—Ж–Є–Њ–љ–љ–Њ–Љ—Г –≤–Њ–Ј—А–∞—Б—В—Г, –∞–љ—В—А–Њ–њ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є–Љ –і–∞–љ–љ—Л–Љ, —Б–Њ—Б—В–Њ—П–љ–Є—О –њ—А–Є —А–Њ–ґ–і–µ–љ–Є–Є –Є –≤ –і–Є–љ–∞–Љ–Є–Ї–µ, –≤–Є–і—Г –Є —Д–Њ—А–Љ–µ –Є–љ—Д–µ–Ї—Ж–Є–Є (—В–∞–±–ї. 1).
–£ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ –і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞–љ—Л –Љ–∞–љ–Є—Д–µ—Б—В–љ—Л–µ —Д–Њ—А–Љ—Л –њ–µ—А–Є–љ–∞—В–∞–ї—М–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є. –°—А–µ–і–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є –Є–љ—Д–µ–Ї—Ж–Є–є –њ—А–µ–Њ–±–ї–∞–і–∞–ї–∞ –њ–љ–µ–≤–Љ–Њ–љ–Є—П (60,0% –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ; 71,4% –≤ –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П). –Я–Њ—А–∞–ґ–µ–љ–Є–µ –≤–µ—А—Е–љ–Є—Е –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є –≤—Л—П–≤–ї–µ–љ–Њ —Г 20,0% –љ–Њ–≤–Њ—А–Њ–ґ–і–µ–љ–љ—Л—Е –і–µ—В–µ–є –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ—Л –Є 21,4% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≥—А—Г–њ–њ—Л —Б—А–∞–≤–љ–µ–љ–Є—П, –≥–µ–њ–∞—В–Є—В I —Б—В–µ–њ–µ–љ–Є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є – —Г 20,0 –Є 7,1% –і–µ—В–µ–є —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ. –°–Њ—Б—В–Њ—П–љ–Є–µ —А–∞—Б—Ж–µ–љ–Є–≤–∞–ї–Њ—Б—М –Ї–∞–Ї —В—П–ґ–µ–ї–Њ–µ —Г 1/5 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ –Ї–∞–ґ–і–Њ–є –≥—А—Г–њ–њ–µ.
–Ш–љ—Д–µ–Ї—Ж–Є—П –њ—А–Њ—В–µ–Ї–∞–ї–∞ –≤ –ї–∞—В–µ–љ—В–љ–Њ–є —Д–Њ—А–Љ–µ —Г 2 –±–Њ–ї—М–љ—Л—Е –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –Є 1 —А–µ–±–µ–љ–Ї–∞ –≤ –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П. –Ш—Е —Б–Њ—Б—В–Њ—П–љ–Є–µ —А–∞—Б—Ж–µ–љ–Є–≤–∞–ї–Њ—Б—М –Ї–∞–Ї —Б—А–µ–і–љ–µ–—В—П–ґ–µ–ї–Њ–µ, —З—В–Њ –±—Л–ї–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–µ–є –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є.
–Ф–ї—П –Њ—Ж–µ–љ–Ї–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –Ъ–Є–њ—Д–µ—А–Њ–љ–∞® –≤ —В–µ—А–∞–њ–Є–Є –њ–µ—А–Є–љ–∞—В–∞–ї—М–љ—Л—Е –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є –њ—А–Њ–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ—Л —Б—Г—В–Њ—З–љ–∞—П –њ—А–Є–±–∞–≤–Ї–∞ –≤ –≤–µ—Б–µ –Ј–∞ –њ–µ—А–Є–Њ–і –ї–µ—З–µ–љ–Є—П, –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Ї—Г—А—Б–Њ–≤ –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–є –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є –љ–Њ–≤–Њ—А–Њ–ґ–і–µ–љ–љ—Л—Е –і–µ—В–µ–є. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –і–Њ –Є –њ–Њ—Б–ї–µ –Њ–Ї–Њ–љ—З–∞–љ–Є—П –Ї—Г—А—Б–∞ –Ъ–Є–њ—Д–µ—А–Њ–љ–∞® –њ—А–Њ–≤–µ–і–µ–љ–∞ –Њ—Ж–µ–љ–Ї–∞ –Њ–±—Й–µ–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Є —Г—А–Њ–≤–љ–µ–є —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤ –Ї—А–Њ–≤–Є, –∞ —В–∞–Ї–ґ–µ –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ–Њ–≤ –≤ –Ї–Њ–њ—А–Њ—Д–Є–ї—М—В—А–∞—В–µ.
–С—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ, —З—В–Њ —Г –і–µ—В–µ–є, –њ–Њ–ї—Г—З–Є–≤—И–Є—Е –≤ —Б–Њ—Б—В–∞–≤–µ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є 10––і–љ–µ–≤–љ—Л–є –Ї—Г—А—Б –Ъ–Є–њ—Д–µ—А–Њ–љ–∞®, –Њ—В–Љ–µ—З–∞–ї–∞—Б—М –Ј–љ–∞—З–Є–Љ–Њ –±–Њ–ї—М—И–∞—П —Б—А–µ–і–љ–µ—Б—Г—В–Њ—З–љ–∞—П –њ—А–Є–±–∞–≤–Ї–∞ –≤ –≤–µ—Б–µ –Ј–∞ –њ–µ—А–Є–Њ–і –ї–µ—З–µ–љ–Є—П (35,06±2,92 –≥, –≤ –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П – 26,20±2,65 –≥, —А<0,05). –Ф–µ—В—П–Љ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ—Л –њ–Њ—В—А–µ–±–Њ–≤–∞–ї–Њ—Б—М –Љ–µ–љ—М—И–µ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Ї—Г—А—Б–Њ–≤ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є – 1,24±0,24 –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –≥—А—Г–њ–њ—Л —Б—А–∞–≤–љ–µ–љ–Є—П – 2,73±0,42 (—А<0,01). –°—А–µ–і–љ—П—П –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є —Г –љ–Њ–≤–Њ—А–Њ–ґ–і–µ–љ–љ—Л—Е –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ—Л —Б–Њ—Б—В–∞–≤–Є–ї–∞ – 22,0±1,59 –і–љ–µ–є, –≤ –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П – 29,8±3,42 –і–љ–µ–є (—А<0,05).
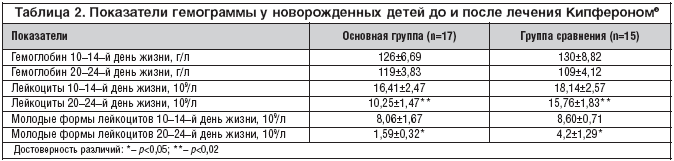
–£ –љ–Њ–≤–Њ—А–Њ–ґ–і–µ–љ–љ—Л—Е –і–µ—В–µ–є, –њ–Њ–ї—Г—З–Є–≤—И–Є—Е –Ї—Г—А—Б –Ъ–Є–њ—Д–µ—А–Њ–љ–∞®, –Њ—В–Љ–µ—З–∞–ї–∞—Б—М –±–Њ–ї–µ–µ –±—Л—Б—В—А–∞—П –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –≥–µ–Љ–Њ–≥—А–∞–Љ–Љ—Л (—В–∞–±–ї. 2): –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ –љ–Њ—А–Љ–∞–ї—М–љ–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –ї–µ–є–Ї–Њ—Ж–Є—В–Њ–≤ –≤ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –Ї—А–Њ–≤–Є – –і–Њ 10,25±1,47x109/–ї (—А<0,02), —Б –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ–Љ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ–≥–Њ —З–Є—Б–ї–∞ –Љ–Њ–ї–Њ–і—Л—Е —Д–Њ—А–Љ –љ–µ–є—В—А–Њ—Д–Є–ї–Њ–≤.
–Ш—Б—Е–Њ–і–љ—Л–є —Г—А–Њ–≤–µ–љ—М —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤ –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –і–µ—В–µ–є –Њ–±–µ–Є—Е –≥—А—Г–њ–њ –љ–µ –Є–Љ–µ–ї –Ј–љ–∞—З–Є–Љ—Л—Е –Њ—В–ї–Є—З–Є–є –Є –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ –≤ —В–∞–±–ї–Є—Ж–µ 3.
–£ –љ–Њ–≤–Њ—А–Њ–ґ–і–µ–љ–љ—Л—Е –і–µ—В–µ–є —Б –њ–µ—А–Є–љ–∞—В–∞–ї—М–љ—Л–Љ–Є –Є–љ—Д–µ–Ї—Ж–Є—П–Љ–Є —Г—А–Њ–≤–µ–љ—М –Є–љ—В–µ—А—Д–µ—А–Њ–љ–∞– –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –і–Њ –ї–µ—З–µ–љ–Є—П —Б–Њ—Б—В–∞–≤–Є–ї 115,28±13,50 –њ–Ї–≥/–Љ–ї. –£ –і–µ—В–µ–є, –њ–Њ–ї—Г—З–Є–≤—И–Є—Е –Ї—Г—А—Б –Ъ–Є–њ—Д–µ—А–Њ–љ–∞®, –µ–≥–Њ —Г—А–Њ–≤–µ–љ—М —Б—В–∞–ї –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –љ–Є–ґ–µ –Є —Б–Њ—Б—В–∞–≤–Є–ї 76,03±7,87 –њ–Ї–≥/–Љ–ї (—А<0,05). –Ш–љ—В–µ—А—Д–µ—А–Њ–љ– –Њ–±–ї–∞–і–∞–µ—В –њ—А–Њ—В–Є–≤–Њ–≤–Є—А—Г—Б–љ—Л–Љ –Є —Г–љ–Є–Ї–∞–ї—М–љ—Л–Љ –Є–Љ–Љ—Г–љ–Њ–Љ–Њ–і—Г–ї–Є—А—Г—О—Й–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ. –Ю–љ –Њ–њ–Њ—Б—А–µ–і—Г–µ—В –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–µ –Љ–µ–ґ–і—Г –Ґ––ї–Є–Љ—Д–Њ—Ж–Є—В–∞–Љ–Є –Є –Љ–∞–Ї—А–Њ—Д–∞–≥–∞–Љ–Є, —Г—Б–Є–ї–Є–≤–∞–µ—В —Ж–Є—В–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Ї–ї–µ—В–Њ–Ї –Є–Љ–Љ—Г–љ–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л, –Є–≥—А–∞–µ—В –≤–∞–ґ–љ—Г—О —А–Њ–ї—М –≤ –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–Ї–µ –Є —Б–Њ–Ј—А–µ–≤–∞–љ–Є–Є –Ґ––ї–Є–Љ—Д–Њ—Ж–Є—В–Њ–≤, –∞–Ї—В–Є–≤–Є—А—Г–µ—В —Б–Є—Б—В–µ–Љ—Г –µ—Б—В–µ—Б—В–≤–µ–љ–љ—Л—Е –Ї–Є–ї–ї–µ—А–љ—Л—Е –Ї–ї–µ—В–Њ–Ї, –Њ–±–ї–∞–і–∞—О—Й–Є—Е –љ–µ—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Њ–є —Ж–Є—В–Њ—В–Њ–Ї—Б–Є—З–љ–Њ—Б—В—М—О, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ–Њ–і–∞–≤–ї—П—В—М —А–∞–Ј–≤–Є—В–Є–µ –Є–љ—Д–µ–Ї—Ж–Є–Є, –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М, –≤—Л–Ј–≤–∞–љ–љ—Г—О –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ—Л–Љ–Є –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П–Љ–Є, –љ–∞ —А–∞–љ–љ–Є—Е —Б—В–∞–і–Є—П—Е [6–8]. –°–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–љ—П IFN–γ —Г –і–µ—В–µ–є –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ—Л –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –і–Є–љ–∞–Љ–Є–Ї–Њ–є –Љ–Њ–ґ–µ—В —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤–Њ–≤–∞—В—М –Њ —Б—В–Є—Е–∞–љ–Є–Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –Є –њ–Њ–і–∞–≤–ї–µ–љ–Є–Є —А–∞–Ј–Љ–љ–Њ–ґ–µ–љ–Є—П –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ—Л—Е –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є, —П–≤–ї—П—О—Й–Є—Е—Б—П –Є–љ–і—Г–Ї—В–Њ—А–∞–Љ–Є —Б–Є–љ—В–µ–Ј–∞ IFN–γ. –Т –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М IFN–γ –Њ—Б—В–∞–ї—Б—П –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –љ–µ–Є–Ј–Љ–µ–љ–љ—Л–Љ (112,11±29,51 –њ–Ї–≥/–Љ–ї).
–Ш–љ—В–µ—А–ї–µ–є–Ї–Є–љ–4, —П–≤–ї—П—П—Б—М –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ —Ж–Є—В–Њ–Ї–Є–љ–Њ–Љ, –њ—А–Є–љ–Є–Љ–∞–µ—В —Г—З–∞—Б—В–Є–µ –≤ –Є–Љ–Љ—Г–љ–љ–Њ–Љ –Њ—В–≤–µ—В–µ –Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е —А–µ–∞–Ї—Ж–Є—П—Е. –Я–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Є—Б—Е–Њ–і–љ—Л–Љ (4,27±0,47 –њ–Ї–≥/–Љ–ї), —Г—А–Њ–≤–µ–љ—М IL–4 —Г –і–µ—В–µ–є —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –Є –±–µ–Ј –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ъ–Є–њ—Д–µ—А–Њ–љ–∞® –≤ —В–µ—А–∞–њ–Є–Є –Є–Љ–µ–ї —В–µ–љ–і–µ–љ—Ж–Є—О –Ї —Б–љ–Є–ґ–µ–љ–Є—О (3,28±0,56 –Є 3,20±0,63 –њ–Ї–≥/–Љ–ї), –љ–Њ –±–µ–Ј –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–є —А–∞–Ј–љ–Є—Ж—Л –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е.
–Я–µ—А–≤–Њ–є –ї–Є–љ–Є–µ–є —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Њ–є –Ј–∞—Й–Є—В—Л —Б–ї–Є–Ј–Є—Б—В—Л—Е –Ї–Є—И–µ—З–љ–Є–Ї–∞ –Є –і–Њ–Љ–Є–љ–Є—А—Г—О—Й–Є–Љ –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ–Њ–Љ —П–≤–ї—П–µ—В—Б—П —Б–µ–Ї—А–µ—В–Њ—А–љ—Л–є IgA (sIgA), —Б–Є–љ—В–µ–Ј–Є—А—Г–µ–Љ—Л–є –њ–ї–∞–Ј–Љ–∞—В–Є—З–µ—Б–Ї–Є–Љ–Є –Ї–ї–µ—В–Ї–∞–Љ–Є —Б–ї–Є–Ј–Є—Б—В–Њ–є –≤ –Ї–Њ–Њ–њ–µ—А–∞—Ж–Є–Є —Б —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л–Љ–Є –Ї–ї–µ—В–Ї–∞–Љ–Є, –Њ–±—А–∞–Ј—Г—О—Й–Є–Љ–Є —Б–µ–Ї—А–µ—В–Њ—А–љ—Л–є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В –і–∞–љ–љ–Њ–≥–Њ –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ–∞. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П —Б –≥–ї–Є–Ї–Њ–Ї–∞–ї–Є–Ї—Б–Њ–Љ sIgA —Г–і–µ—А–ґ–Є–≤–∞–µ—В—Б—П –Њ–Ї–Њ–ї–Њ —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї, –њ–Њ–і–∞–≤–ї—П—П –Ї–Њ–ї–Њ–љ–Є–Ј–∞—Ж–Є—О —Н–њ–Є—В–µ–ї–Є—П –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л–Љ–Є –∞–≥–µ–љ—В–∞–Љ–Є –Є —Б–і–µ—А–ґ–Є–≤–∞—П –њ—А–Є—В–Њ–Ї —А–∞—Б—В–≤–Њ—А–Є–Љ—Л—Е –∞–љ—В–Є–≥–µ–љ–Њ–≤ [9].
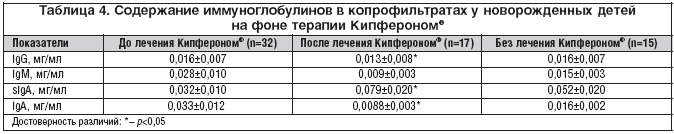
–Я—А–Є –∞–љ–∞–ї–Є–Ј–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є sIgA –≤ –Ї–Њ–њ—А–Њ—Д–Є–ї—М—В—А–∞—В–∞—Е —Г –љ–Њ–≤–Њ—А–Њ–ґ–і–µ–љ–љ—Л—Е –і–µ—В–µ–є —Б –њ–µ—А–Є–љ–∞—В–∞–ї—М–љ—Л–Љ–Є –Є–љ—Д–µ–Ї—Ж–Є—П–Љ–Є –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ, —З—В–Њ –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –Ъ–Є–њ—Д–µ—А–Њ–љ–Њ–Љ® –њ—А–Њ–Є—Б—Е–Њ–і–Є–ї–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ –њ–Њ–≤—Л—И–µ–љ–Є–µ –µ–≥–Њ —Г—А–Њ–≤–љ—П (—Б 0,032±0,010 –і–Њ 0,079±0,020 –Љ–≥/–Љ–ї, —А<0,05). –Т –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П –≤—Л—П–≤–ї–µ–љ–∞ –∞–љ–∞–ї–Њ–≥–Є—З–љ–∞—П —В–µ–љ–і–µ–љ—Ж–Є—П, –љ–Њ –±–µ–Ј –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–є —А–∞–Ј–љ–Є—Ж—Л (—Б 0,032±0,010 –і–Њ 0,052±0,020 –Љ–≥/–Љ–ї) (—В–∞–±–ї. 4).
–°—Л–≤–Њ—А–Њ—В–Њ—З–љ—Л–µ –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ—Л –љ–µ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—О—В –ї–Њ–Ї–∞–ї—М–љ–Њ–є –Ј–∞—Й–Є—В—Л. –Ю–љ–Є –љ–∞–Ї–∞–њ–ї–Є–≤–∞—О—В—Б—П –≤ –Ї–Є—И–µ—З–љ–Є–Ї–µ —В–Њ–ї—М–Ї–Њ –њ—А–Є –љ–∞–ї–Є—З–Є–Є –≤—Л—Б–Њ–Ї–Є—Е —Г—А–Њ–≤–љ–µ–є –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є. –°—Л–≤–Њ—А–Њ—В–Њ—З–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞ –њ—А–Њ–љ–Є–Ї–∞—О—В –≤ –њ—А–Њ—Б–≤–µ—В –Ї–Є—И–µ—З–љ–Є–Ї–∞ –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –њ–∞—Б—Б–Є–≤–љ–Њ–є —В—А–∞–љ—Б—Б—Г–і–∞—Ж–Є–Є –Є–љ—В–µ—А—Б—В–Є—Ж–Є–∞–ї—М–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є —З–µ—А–µ–Ј –њ–Њ–Ї—А–Њ–≤–љ—Л–є —Н–њ–Є—В–µ–ї–Є–є. –Я—А–Њ–љ–Є—Ж–∞–µ–Љ–Њ—Б—В—М —Б–ї–Є–Ј–Є—Б—В—Л—Е –і–ї—П —Б—Л–≤–Њ—А–Њ—В–Њ—З–љ—Л—Е –±–µ–ї–Ї–Њ–≤, –њ–Њ—Б—В—Г–њ–∞—О—Й–Є—Е –≤ —Б–µ–Ї—А–µ—В—Л, —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П –њ—А–Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–Њ—Ж–µ—Б—Б–∞—Е.
–Т –≥—А—Г–њ–њ–µ –і–µ—В–µ–є, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –ї–µ—З–µ–љ–Є–µ –Ъ–Є–њ—Д–µ—А–Њ–љ–Њ–Љ®, –Ј–∞—Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–Њ –Ј–љ–∞—З–Є–Љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–љ—П —Б—Л–≤–Њ—А–Њ—В–Њ—З–љ–Њ–≥–Њ IgA (c 0,033±0,012 –і–Њ 0,0088±0,003 –Љ–≥/–Љ–ї, —А<0,05) –Є —Г—А–Њ–≤–љ—П IgG (c 0,016±0,007 –і–Њ 0,013±0,008 –Љ–≥/–Љ–ї, —А<0,05) –≤ –Ї–Њ–њ—А–Њ—Д–Є–ї—М—В—А–∞—В–µ. –Т –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П —Г—А–Њ–≤–µ–љ—М —Б—Л–≤–Њ—А–Њ—В–Њ—З–љ–Њ–≥–Њ IgA —В–∞–Ї–ґ–µ –Є–Љ–µ–ї —В–µ–љ–і–µ–љ—Ж–Є—О –Ї —Б–љ–Є–ґ–µ–љ–Є—О (—А>0,05), –∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М IgG –Њ—Б—В–∞–ї—Б—П –љ–µ–Є–Ј–Љ–µ–љ–љ—Л–Љ.
–£ –і–µ—В–µ–є –Њ–±–µ–Є—Е –≥—А—Г–њ–њ –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –ї–µ—З–µ–љ–Є—П –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Б–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–љ—П IgM (—Б 0,028±0,010 –і–Њ 0,009±0,003 –Љ–≥/–Љ–ї –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –Є –і–Њ 0,015±0,003 –Љ–≥/–Љ–ї –≤ –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П) –≤ –Ї–Њ–њ—А–Њ—Д–Є–ї—М—В—А–∞—В–µ, –љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–є —А–∞–Ј–љ–Є—Ж—Л –≤ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П—Е –љ–µ –≤—Л—П–≤–ї–µ–љ–Њ.
–Т—Л—П–≤–ї–µ–љ–љ—Л–µ —Б–і–≤–Є–≥–Є –≤ —Б–Њ–і–µ—А–ґ–∞–љ–Є–Є –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ–Њ–≤ –≤ –Ї–Њ–њ—А–Њ—Д–Є–ї—М—В—А–∞—В–∞—Е –Љ–Њ–≥—Г—В —А–∞—Б—Ж–µ–љ–Є–≤–∞—В—М—Б—П –Ї–∞–Ї —А–µ–Ј—Г–ї—М—В–∞—В –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –Ъ–Є–њ—Д–µ—А–Њ–љ® –љ–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Љ–µ—Б—В–љ–Њ–≥–Њ –љ–µ—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Њ–≥–Њ –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞.
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ —В–Њ–Љ, —З—В–Њ –≤–Ї–ї—О—З–µ–љ–Є–µ –Ъ–Є–њ—Д–µ—А–Њ–љ–∞® –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ—Г—О —В–µ—А–∞–њ–Є—О –њ–µ—А–Є–љ–∞—В–∞–ї—М–љ—Л—Е –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є —Г –і–Њ–љ–Њ—И–µ–љ–љ—Л—Е –љ–Њ–≤–Њ—А–Њ–ґ–і–µ–љ–љ—Л—Е –і–µ—В–µ–є —Б –Ј–∞–і–µ—А–ґ–Ї–Њ–є –≤–љ—Г—В—А–Є—Г—В—А–Њ–±–љ–Њ–≥–Њ —А–∞–Ј–≤–Є—В–Є—П –њ–Њ–≤—Л—И–∞–µ—В —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –±–Њ–ї–µ–µ –±—Л—Б—В—А–Њ–Љ—Г —Г–ї—Г—З—И–µ–љ–Є—О —Б–Њ—Б—В–Њ—П–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є —Б–Њ–Ї—А–∞—Й–µ–љ–Є—О —Б—А–Њ–Ї–Њ–≤ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є.
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Є–Љ–Љ—Г–љ–љ–Њ–≥–Њ —Б—В–∞—В—Г—Б–∞ —Г –і–µ—В–µ–є, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Ъ–Є–њ—Д–µ—А–Њ–љ®, –≤—Л—П–≤–Є–ї–Њ –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—О –њ—А–Њ–і—Г–Ї—Ж–Є–Є IFN–γ, –њ–Њ–≤—Л—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П —Б–µ–Ї—А–µ—В–Њ—А–љ–Њ–≥–Њ IgA –≤ –Ї–Њ–њ—А–Њ—Д–Є–ї—М—В—А–∞—В–µ –Є —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П —Б—Л–≤–Њ—А–Њ—В–Њ—З–љ—Л—Е IgG. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Ъ–Є–њ—Д–µ—А–Њ–љ–∞® —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Г–Љ–µ–љ—М—И–µ–љ–Є—О –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –Ї–Є—И–µ—З–љ–Є–Ї–∞, –Њ —З–µ–Љ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П IgA –≤ –Ї–Њ–њ—А–Њ—Д–Є–ї—М—В—А–∞—В–∞—Е.

–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –°–∞–≤–µ–љ–Ї–Њ–≤–∞ –Ь.–°., –Э–Є—Б–µ–≤–Є—З –Э.–Ш. –•–ї–∞–Љ–Є–і–Є–Њ–Ј —Г –і–µ—В–µ–є –њ–µ—А–≤–Њ–≥–Њ –≥–Њ–і–∞ –ґ–Є–Ј–љ–Є // –Ф–µ—В—Б–Ї–Є–µ –Є–љ—Д–µ–Ї—Ж–Є–Є. 2007. вДЦ 3. –°. 23–30.
2. –Ч–∞–њ–ї–∞—В–љ–Є–Ї–Њ–≤ –Р.–Ы., –Ъ–Њ—А–Њ–≤–Є–љ–∞ –Э.–Р., –Ъ–Њ—А–љ–µ–≤–∞ –Ь.–Ѓ. –Є –і—А. –Т–љ—Г—В—А–Є—Г—В—А–Њ–±–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є: –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞, –ї–µ—З–µ–љ–Є–µ, –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ // –Ы–µ—З–∞—Й–Є–є –≤—А–∞—З. 2005. вДЦ 8. –°. 54–62.
3. Stiehm E.R., Ochs H.D., Winkelstein J.A. Immunologic Disorders in Infant and Children. 5th Ed. 2004.
4. –С–Њ—З–∞—А–Њ–≤–∞ –Ш.–Ш., –С–∞—И–∞–Ї–Є–љ –Э.–§., –Р–Ї—Б–µ–љ–Њ–≤ –Р.–Э. –Є –і—А. –Т–ї–Є—П–љ–Є–µ —Г—А–Њ–≥–µ–љ–Є—В–∞–ї—М–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є –Љ–∞—В–µ—А–Є –љ–∞ –Ї–ї–Є–љ–Є–Ї–Њ––Є–Љ–Љ—Г–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О –∞–і–∞–њ—В–∞—Ж–Є—О –љ–Њ–≤–Њ—А–Њ–ґ–і–µ–љ–љ–Њ–≥–Њ // –Т–Њ–њ—А–Њ—Б—Л –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–є –њ–µ–і–Є–∞—В—А–Є–Є. 2006. –Ґ. 1. вДЦ 4. –°. 16.
5. –Ґ–∞–±–Њ–ї–Є–љ –Т.–Р., –Т–Њ–ї–Њ–і–Є–љ –Э.–Э., –Ф–µ–≥—В—П—А–µ–≤–∞ –Ь.–Т. –Є –і—А. –Р–Ї—В—Г–∞–ї—М–љ—Л–µ –≤–Њ–њ—А–Њ—Б—Л –њ–µ—А–Є–љ–∞—В–∞–ї—М–љ–Њ–є –Є–Љ–Љ—Г–љ–Њ–ї–Њ–≥–Є–Є // Intern. J.Immunorehabilitation. 1997. вДЦ 6. –†. 112–122.
6. –Р–≤–і–µ–µ–≤–∞ –Ц.–Ш., –Р–ї–њ–∞—В–Њ–≤–∞ –Ш.–Р., –Ь–µ–і—Г–љ–Є—Ж—Л–љ –Э.–Т. –Я—А–µ–њ–∞—А–∞—В—Л —Б–Є—Б—В–µ–Љ—Л —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤ // –¶–Є—В–Њ–Ї–Є–љ—Л –Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ. 2002. –Ґ. 1 вДЦ 2. –°. 33.
7. Feghali C.A., Wright T.M. Cytokines In Acute and Chronic Inflammation // Frontiers in Bioscience 2. 1997. вДЦ 2. –†. 12–26.
8. –Х—А—И–Њ–≤ –§. –Ш., –Ъ–Є—Б–µ–ї–µ–≤ –Ю.–Ш. –Ш–љ—В–µ—А—Д–µ—А–Њ–љ—Л –Є –Є—Е –Є–љ–і—Г–Ї—В–Њ—А—Л (–Њ—В –Љ–Њ–ї–µ–Ї—Г–ї –і–Њ –ї–µ–Ї–∞—А—Б—В–≤). –Ь., 2005.
9. –•–∞–Є—В–Њ–≤ –†.–Ь. –§–Є–Ј–Є–Њ–ї–Њ–≥–Є—П –Є–Љ–Љ—Г–љ–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л. –Ь., 2001. 223 —Б.
10. –Ъ–Њ–љ–і—А–∞—И–Є–љ –Ѓ.–Ш. –Э–Њ–≤—Л–є –њ—А–Њ—В–Є–≤–Њ–≤–Є—А—Г—Б–љ—Л–є –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–є –Є–Љ–Љ—Г–љ–Њ–Љ–Њ–і—Г–ї–Є—А—Г—О—Й–Є–є –њ—А–µ–њ–∞—А–∞—В –Ъ–Є–њ—Д–µ—А–Њ–љ@ // –†—Г—Б—Б–Ї–Є–є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–є –ґ—Г—А–љ–∞–ї. 2006. –Ґ. 14. вДЦ 4. –°. 318–319.











