
–Ф–µ–є—Б—В–≤–Є–µ –њ—А–Њ–±–Є–Њ—В–Є–Ї–Њ–≤ –Љ–љ–Њ–≥–Њ–њ–ї–∞–љ–Њ–≤–Њ –Є –љ–µ —Б–≤–Њ–і–Є—В—Б—П –Ї –њ—А–Њ—Б—В–Њ–Љ—Г –Ј–∞—Б–µ–ї–µ–љ–Є—О –Ї–Є—И–µ—З–љ–Є–Ї–∞ [2]. –Я—А–Њ–±–Є–Њ—В–Є–Ї–Є –≤–ї–Є—П—О—В –љ–∞ —Б–Њ—Б—В–∞–≤ –Є —Д—Г–љ–Ї—Ж–Є—О –Ї–Њ–Љ–Љ–µ–љ—Б–∞–ї—М–љ–Њ–є –Љ–Є–Ї—А–Њ–±–Є–Њ—В—Л:
вАҐ –Љ–Њ–і—Г–ї–Є—А—Г—О—В –Њ—В–≤–µ—В —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї –Є —Б–Є—Б—В–µ–Љ—Л –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞,
вАҐ –≤–Њ—Б—Б—В–∞–љ–∞–≤–ї–Є–≤–∞—О—В —Ж–µ–ї–Њ—Б—В–љ–Њ—Б—В—М –Ї–Є—И–µ—З–љ–Њ–≥–Њ –±–∞—А—М–µ—А–∞ –њ–Њ—Б—А–µ–і—Б—В–≤–Њ–Љ —Б–љ–Є–ґ–µ–љ–Є—П —В—А–∞–љ—Б–ї–Њ–Ї–∞—Ж–Є–Є –±–∞–Ї—В–µ—А–Є–є –Є –Љ–∞–Ї—А–Њ–Љ–Њ–ї–µ–Ї—Г–ї,
вАҐ —Г–Љ–µ–љ—М—И–∞—О—В –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –ґ–µ–ї—Г–і–Ї–∞ [16],
вАҐ –Є–љ–≥–Є–±–Є—А–Є—А—Г—О—В –њ–∞—В–Њ–≥–µ–љ–љ—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –±–∞–Ї—В–µ—А–Є–є –њ—Г—В–µ–Љ –њ—А–Њ–і—Г–Ї—Ж–Є–Є –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е –њ–µ–њ—В–Є–і–Њ–≤ –Є –Ї–Њ—А–Њ—В–Ї–Њ—Ж–µ–њ–Њ—З–µ—З–љ—Л—Е –ґ–Є—А–љ—Л—Е –Ї–Є—Б–ї–Њ—В, —Б–љ–Є–ґ–∞—О—В –ї–Њ–Ї–∞–ї—М–љ—Г—О —А–Э –≤ –њ—А–Њ—Б–≤–µ—В–µ –Ї–Є—И–µ—З–љ–Є–Ї–∞, —Б–Њ–Ј–і–∞–≤–∞—П –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–µ —Г—Б–ї–Њ–≤–Є—П –і–ї—П —А–∞–Ј–≤–Є—В–Є—П –њ–∞—В–Њ–≥–µ–љ–Њ–≤,
вАҐ —Б—В–Є–Љ—Г–ї–Є—А—Г—О—В –њ—А–Њ–і—Г–Ї—Ж–Є—О —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ–Њ–≥–Њ –Љ—Г—Ж–Є–љ–∞, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї —Б–љ–Є–ґ–µ–љ–Є—О —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –њ–∞—В–Њ–≥–µ–љ–Њ–≤ –Ї –њ—А–Є–Ї—А–µ–њ–ї–µ–љ–Є—О –Ї —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л–Љ –Ї–ї–µ—В–Ї–∞–Љ,
вАҐ —Б–љ–Є–ґ–∞—О—В –∞–і–≥–µ–Ј–Є—О –Є –Є–љ–≥–Є–±–Є—А—Г—О—В —А–Њ—Б—В –Э. pylori –љ–∞ —Н–њ–Є—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Ї–∞—Е –ґ–µ–ї—Г–і–Ї–∞ –Ј–∞ —Б—З–µ—В –≤—Л—А–∞–±–Њ—В–Ї–Є –ї–∞–Ї—В–∞—В–∞ [6] –Є –±–∞–Ї—В–µ—А–Є–Њ—Ж–Є–љ–Њ–≤ [2], –Є–љ–≥–Є–±–Є—А—Г—О—В —Г—А–µ–∞–Ј—Г –Э. pylori [9].
–†—П–і –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –і–µ–Љ–Њ–љ—Б—В—А–Є—А—Г–µ—В –≤—Л—Б–Њ–Ї—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–Њ–±–Є–Њ—В–Є–Ї–Њ–≤ –љ–µ —В–Њ–ї—М–Ї–Њ –≤ –Ї–∞—З–µ—Б—В–≤–µ –∞–і—К—О–≤–∞–љ—В–љ–Њ–є [7, 8, 14, 17, 19, 20, 22], –љ–Њ –Є –≤ –≤–Є–і–µ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –Є–љ—Д–µ–Ї—Ж–Є–Є –Э. pylori [13, 18]. –Т –†–Њ—Б—Б–Є–Є –≤ 2014 –≥. –њ–Њ—П–≤–Є–ї—Б—П –•–µ–ї–Є–љ–Њ—А–Љ, —Б–Њ–і–µ—А–ґ–∞—Й–Є–є –≤ —Б–≤–Њ–µ–Љ —Б–Њ—Б—В–∞–≤–µ —Б—Г–±—Б—В–∞–љ—Ж–Є—О PylopassвДҐ вАУ —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–є —И—В–∞–Љ–Љ Lactobacillus reuteri, —Б–њ–Њ—Б–Њ–±–љ—Л–є —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є –Ї–Њ–∞–≥—А–µ–≥–Є—А–Њ–≤–∞—В—М —Б –Э. pylori, –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ —З–µ–≥–Њ —Б–≤—П–Ј–∞–љ–љ—Л–є –њ–∞—В–Њ–≥–µ–љ –љ–µ –Љ–Њ–ґ–µ—В –њ—А–Є—Б–Њ–µ–і–Є–љ–Є—В—М—Б—П –Ї —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–µ –ґ–µ–ї—Г–і–Ї–∞ –Є –≤—Л–≤–Њ–і–Є—В—Б—П –Є–Ј –љ–µ–≥–Њ –µ—Б—В–µ—Б—В–≤–µ–љ–љ—Л–Љ –њ—Г—В–µ–Љ [1].
–¶–µ–ї—М—О –љ–∞—И–µ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –±—Л–ї–Њ –Њ–њ—А–µ–і–µ–ї–Є—В—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —Б—А–µ–і—Б—В–≤–∞ –•–µ–ї–Є–љ–Њ—А–Љ –≤ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –Є–љ—Д–µ–Ї—Ж–Є–Є –Э. pylori —Г –і–µ—В–µ–є, –∞ —В–∞–Ї–ґ–µ –Њ—Ж–µ–љ–Є—В—М –≤–ї–Є—П–љ–Є–µ –љ–∞ —З–∞—Б—В–Њ—В—Г –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є –Є –њ—А–Њ—Ж–µ–љ—В —Н—А–∞–і–Є–Ї–∞—Ж–Є–Є –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б–Њ —Б—В–∞–љ–і–∞—А—В–љ–Њ–є –∞–љ—В–Є—Е–µ–ї–Є–Ї–Њ–±–∞–Ї—В–µ—А–љ–Њ–є —Б—Е–µ–Љ–Њ–є.
–Я–Њ–і –љ–∞—И–Є–Љ –љ–∞–±–ї—О–і–µ–љ–Є–µ–Љ –љ–∞—Е–Њ–і–Є–ї–Њ—Б—М 49 –і–µ—В–µ–є (20 –і–µ–≤–Њ—З–µ–Ї –Є 29 –Љ–∞–ї—М—З–Є–Ї–Њ–≤) –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 9 –і–Њ 17 –ї–µ—В —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ–Є –Э–†-–∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –≥–∞—Б—В—А–Њ–і—Г–Њ–і–µ–љ–∞–ї—М–љ–Њ–є –Ј–Њ–љ—Л: 47 –і–µ—В–µ–є (96%) —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ –≥–∞—Б—В—А–Њ–і—Г–Њ–і–µ–љ–Є—В–Њ–Љ, 2 —З–µ–ї–Њ–≤–µ–Ї–∞ —Б —П–Ј–≤–µ–љ–љ–Њ–є –±–Њ–ї–µ–Ј–љ—М—О –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є (–Ф–Я–Ъ) (4%), —А–∞–љ–µ–µ –љ–µ –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —Н—А–∞–і–Є–Ї–∞—Ж–Є–Њ–љ–љ—Г—О —В–µ—А–∞–њ–Є—О. –Т—Б–µ–Љ –і–µ—В—П–Љ –±—Л–ї–∞ –≤—Л–њ–Њ–ї–љ–µ–љ–∞ —Д–Є–±—А–Њ—Н–Ј–Њ—Д–∞–≥–Њ–≥–∞—Б—В—А–Њ–і—Г–Њ–і–µ–љ–Њ—Б–Ї–Њ–њ–Є—П (–§–≠–У–Ф–°) –њ–Њ –Њ–±—Й–µ–њ—А–Є–љ—П—В–Њ–є –Љ–µ—В–Њ–і–Є–Ї–µ —Б–Њ –≤–Ј—П—В–Є–µ–Љ –±–Є–Њ–њ—В–∞—В–Њ–≤ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –∞–љ—В—А–∞–ї—М–љ–Њ–≥–Њ –Њ—В–і–µ–ї–∞, —В–µ–ї–∞ –ґ–µ–ї—Г–і–Ї–∞ –Є –Ф–Я–Ъ –Є –Є—Е –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ–Љ. –Я—А–Є –Њ—Ж–µ–љ–Ї–µ –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–∞—Б—М –≤–Є–Ј—Г–∞–ї—М–љ–Њ-–∞–љ–∞–ї–Њ–≥–Њ–≤–∞—П —И–Ї–∞–ї–∞ (–Т–Р–®) (–Р—А—Г–Є–љ –Ы.–Ш., 1996), –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –Ї–Њ—В–Њ—А–Њ–є –Њ–њ—А–µ–і–µ–ї—П–ї–∞—Б—М —Б—В–µ–њ–µ–љ—М (–ї–µ–≥–Ї–∞—П, —Г–Љ–µ—А–µ–љ–љ–∞—П, –≤—Л—А–∞–ґ–µ–љ–љ–∞—П) –Љ–Њ–љ–Њ–љ—Г–Ї–ї–µ–∞—А–љ–Њ–є –Є –љ–µ–є—В—А–Њ—Д–Є–ї—М–љ–Њ–є –Є–љ—Д–Є–ї—М—В—А–∞—Ж–Є–Є, –∞—В—А–Њ—Д–Є–Є –ґ–µ–ї–µ–Ј, –Ї–Є—И–µ—З–љ–Њ–є –Љ–µ—В–∞–њ–ї–∞–Ј–Є–Є, –∞ —В–∞–Ї–ґ–µ –њ—А–Њ–≤–Њ–і–Є–ї–Є—Б—М –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–∞—П –Њ—Ж–µ–љ–Ї–∞ –Њ–±—Б–µ–Љ–µ–љ–µ–љ–љ–Њ—Б—В–Є —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –±–∞–Ї—В–µ—А–Є—П–Љ–Є –Э–†, –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ –µ–µ —Д–Њ—А–Љ (–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–∞—П, –Ї–Њ–Ї–Ї–Њ–≤–∞—П), –Є—Е –њ—А–Њ—Ж–µ–љ—В–љ–Њ–≥–Њ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є—П –Є –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–є –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є (–≤ —П–Љ–Ї–∞—Е, –љ–∞ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є).
–†–∞–Ј–і–µ–ї–µ–љ–Є–µ –љ–∞ –≥—А—Г–њ–њ—Л –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –≤—Л–±—А–∞–љ–љ–Њ–є —Б—Е–µ–Љ–Њ–є —В–µ—А–∞–њ–Є–Є. –Т 1-—О –≥—А—Г–њ–њ—Г –≤–Њ—И–ї–Є 17 –і–µ—В–µ–є —Б –љ–µ–њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ—Л–Љ –∞–љ–∞–Љ–љ–µ–Ј–Њ–Љ –Є —Г–Љ–µ—А–µ–љ–љ–Њ –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ —Е–∞—А–∞–Ї—В–µ—А–Њ–Љ –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –ґ–∞–ї–Њ–±. –Т —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ–µ –≤ –і–∞–љ–љ–Њ–є –≥—А—Г–њ–њ–µ –њ—А–µ–Њ–±–ї–∞–і–∞–ї —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ—Л–є –≥–∞—Б—В—А–Є—В —Г–Љ–µ—А–µ–љ–љ–Њ–є —Б—В–µ–њ–µ–љ–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є (64,5%) –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ—Л–Љ –і—Г–Њ–і–µ–љ–Є—В–Њ–Љ (88,2%). –Т—Б–µ –і–µ—В–Є –≤ —В–µ—З–µ–љ–Є–µ 4 –љ–µ–і. –њ–Њ–ї—Г—З–∞–ї–Є –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є—О –•–µ–ї–Є–љ–Њ—А–Љ–Њ–Љ вАУ 1 –Ї–∞–њ—Б—Г–ї—Г (200 –Љ–≥) –≤ –і–µ–љ—М, –≤–Њ –≤—А–µ–Љ—П –µ–і—Л, –Ј–∞–њ–Є–≤–∞—П –љ–µ–±–Њ–ї—М—И–Є–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ–Љ –≤–Њ–і—Л.
–Т –≥—А—Г–њ–њ—Г —Б—А–∞–≤–љ–µ–љ–Є—П –≤–Њ—И–ї–Є 16 –і–µ—В–µ–є, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Ї–ї–∞—Б—Б–Є—З–µ—Б–Ї—Г—О —Б—Е–µ–Љ—Г —Н—А–∞–і–Є–Ї–∞—Ж–Є–Є. –Т —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ–Є ESPGHAN –Є NASPGHAN, –Њ–њ—В–Є–Љ–∞–ї—М–љ—Л–Љ–Є —Б—З–Є—В–∞—О—В—Б—П —Б—Е–µ–Љ—Л, –њ—А–µ–і—Б—В–∞–≤–ї—П—О—Й–Є–µ —Б–Њ–±–Њ–є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—О –Є–љ–≥–Є–±–Є—В–Њ—А–∞ –њ—А–Њ—В–Њ–љ–љ–Њ–є –њ–Њ–Љ–њ—Л —Б 2 –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ–Є: –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ + –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ / –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ + –Љ–µ—В—А–Њ–љ–Є–і–∞–Ј–Њ–ї / –Ї–ї–∞—А–Є—В—А–Њ–Љ–Є—Ж–Є–љ + –Љ–µ—В—А–Њ–љ–Є–і–∞–Ј–Њ–ї [9]. –Ф–Њ–±–∞–≤–ї–µ–љ–Є–µ –Ї —Б—В–∞–љ–і–∞—А—В–љ–Њ–є —В—А–Њ–є–љ–Њ–є —В–µ—А–∞–њ–Є–Є –≤–Є—Б–Љ—Г—В–∞ —В—А–Є–Ї–∞–ї–Є—П –і–Є—Ж–Є—В—А–∞—В–∞ –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Г–≤–µ–ї–Є—З–Є—В—М –µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М, —Б–Њ–≥–ї–∞—Б–љ–Њ –љ–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ [3].
–Ь—Л –≤—Л–±—А–∞–ї–Є —Б—Е–µ–Љ—Г —Н—А–∞–і–Є–Ї–∞—Ж–Є–Є –Њ–Љ–µ–њ—А–∞–Ј–Њ–ї + –∞–Љ–Њ–Ї—Б–Є—Ж–Є–ї–ї–Є–љ + –Љ–µ—В—А–Њ–љ–Є–і–∞–Ј–Њ–ї + –њ—А–µ–њ–∞—А–∞—В—Л —Б–Њ–ї–µ–є –≤–Є—Б–Љ—Г—В–∞. –Я—А–µ–њ–∞—А–∞—В—Л –љ–∞–Ј–љ–∞—З–∞–ї–Є—Б—М –≤ –≤–Њ–Ј—А–∞—Б—В–љ–Њ–є –і–Њ–Ј–Є—А–Њ–≤–Ї–µ. –Я—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М —В–µ—А–∞–њ–Є–Є —Б–Њ—Б—В–∞–≤–Є–ї–∞ 10 –і–љ–µ–є. –£ –≤—Б–µ—Е –і–µ—В–µ–є –і–∞–љ–љ–Њ–є –≥—А—Г–њ–њ—Л –Є–Љ–µ–ї –Љ–µ—Б—В–Њ –і–ї–Є—В–µ–ї—М–љ—Л–є –∞–љ–∞–Љ–љ–µ–Ј –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –ґ–∞–ї–Њ–± —А–∞–Ј–љ–Њ–є —Б—В–µ–њ–µ–љ–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є (–Њ—В —Г–Љ–µ—А–µ–љ–љ–Њ–є –і–Њ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–є). –Т —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ–µ –њ—А–µ–Њ–±–ї–∞–і–∞–ї–Є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ—Л–є –≥–∞—Б—В—А–Є—В —Г–Љ–µ—А–µ–љ–љ–Њ–є —Б—В–µ–њ–µ–љ–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є (50%), –Њ—З–∞–≥–Њ–≤—Л–є –∞–љ—В—А–∞–ї—М–љ—Л–є –≥–∞—Б—В—А–Є—В (25%), —Н—А–Њ–Ј–Є–≤–љ—Л–є –∞–љ—В—А–∞–ї—М–љ—Л–є –≥–∞—Б—В—А–Є—В (18,8%) –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ—Л–Љ –і—Г–Њ–і–µ–љ–Є—В–Њ–Љ (81,2%).
–Т 3-–є –≥—А—Г–њ–њ–µ 16 –і–µ—В–µ–є –њ–Њ–ї—Г—З–∞–ї–Є –≤—Л—И–µ—Г–Ї–∞–Ј–∞–љ–љ—Г—О —Б—Е–µ–Љ—Г —Н—А–∞–і–Є–Ї–∞—Ж–Є–Є –≤ —В–µ—З–µ–љ–Є–µ 10 –і–љ–µ–є –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –•–µ–ї–Є–љ–Њ—А–Љ–Њ–Љ. –Я—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М —В–µ—А–∞–њ–Є–Є –њ–Њ—Б–ї–µ–і–љ–Є–Љ —Б–Њ—Б—В–∞–≤–Є–ї–∞ 4 –љ–µ–і. –Т –і–∞–љ–љ—Г—О –≥—А—Г–њ–њ—Г –±—Л–ї–Є –≤–Ї–ї—О—З–µ–љ—Л –і–µ—В–Є —Б –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ–Є –ґ–∞–ї–Њ–±–∞–Љ–Є –Є –і–ї–Є—В–µ–ї—М–љ—Л–Љ –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –∞–љ–∞–Љ–љ–µ–Ј–Њ–Љ, –љ–Њ —В–∞–Ї–ґ–µ –љ–µ –њ–Њ–ї—Г—З–∞–≤—И–Є–µ —А–∞–љ–µ–µ —Н—А–∞–і–Є–Ї–∞—Ж–Є–Њ–љ–љ—Г—О —В–µ—А–∞–њ–Є—О. –Т —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ–µ –њ—А–µ–Њ–±–ї–∞–і–∞–ї–Є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ—Л–є –≥–∞—Б—В—А–Є—В (68,8%), —Н—А–Њ–Ј–Є–≤–љ—Л–є –∞–љ—В—А–∞–ї—М–љ—Л–є –≥–∞—Б—В—А–Є—В (25%) –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ—Л–Љ –і—Г–Њ–і–µ–љ–Є—В–Њ–Љ (100%). –£ –і–≤—Г—Е –і–µ—В–µ–є (12,5%) –±—Л–ї–∞ –і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞–љ–∞ —П–Ј–≤–∞ –ї—Г–Ї–Њ–≤–Є—Ж—Л –Ф–Я–Ъ –±–µ–Ј –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є—П.
–Ф–ї—П –Њ—Ж–µ–љ–Ї–Є –і–Є–љ–∞–Љ–Є–Ї–Є –ґ–∞–ї–Њ–± –±—Л–ї –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ –Њ–њ—А–Њ—Б–љ–Є–Ї –њ–Њ —Б–ї–µ–і—Г—О—Й–Є–Љ —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ: –±–Њ–ї—М –≤ –ґ–Є–≤–Њ—В–µ, –Њ—В—А—Л–ґ–Ї–∞, –Є–Ј–ґ–Њ–≥–∞, —В–Њ—И–љ–Њ—В–∞, —А–≤–Њ—В–∞, –љ–∞—А—Г—И–µ–љ–Є—П –і–µ—Д–µ–Ї–∞—Ж–Є–Є, –Є–Ј–Љ–µ–љ–µ–љ–Є–µ –≤–Ї—Г—Б–∞, —Б—Л–њ—М –љ–∞ —В–µ–ї–µ. –Ш–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М –њ—А–Њ—П–≤–ї–µ–љ–Є—П —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є —А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–ї–∞—Б—М —Б–∞–Љ–Є–Љ –њ–∞—Ж–Є–µ–љ—В–Њ–Љ –њ–µ—А–µ–і –љ–∞—З–∞–ї–Њ–Љ, –≤ —В–µ—З–µ–љ–Є–µ –≤—Б–µ–є —В–µ—А–∞–њ–Є–Є (10 –і–љ–µ–є) –Є –њ–Њ—Б–ї–µ –µ–µ –Ј–∞–≤–µ—А—И–µ–љ–Є—П –њ—А–Є –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–Љ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є. –Ф–Є–љ–∞–Љ–Є–Ї–∞ —Б–Њ—Б—В–Њ—П–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ї 10-–Љ—Г –і–љ—О –њ—А–Њ–≤–µ–і–µ–љ–Є—П —В–µ—А–∞–њ–Є–Є –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –љ–∞ —А–Є—Б—Г–љ–Ї–µ 1.
–°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –≤ –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є —Б—Е–µ–Љ —Н—А–∞–і–Є–Ї–∞—Ж–Є–Є –Љ—Л –љ–µ –≤—Л—П–≤–Є–ї–Є, –љ–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –•–µ–ї–Є–љ–Њ—А–Љ, –±—Л—Б—В—А–µ–µ –Ї—Г–њ–Є—А–Њ–≤–∞–ї–∞—Б—М –ґ–µ–ї—Г–і–Њ—З–љ–Њ-–Ї–Є—И–µ—З–љ–∞—П —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–∞, —А–µ–ґ–µ –Њ—В–Љ–µ—З–∞–ї–Є—Б—М –≤–Ї—Г—Б–Њ–≤—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞, –Њ—В—Б—Г—В—Б—В–≤–Њ–≤–∞–ї–Є —Г—Б–Є–ї–µ–љ–Є–µ –±–Њ–ї–µ–є –≤ –ґ–Є–≤–Њ—В–µ –Є –Є–Ј–Љ–µ–љ–µ–љ–Є–µ —Е–∞—А–∞–Ї—В–µ—А–∞ —Б—В—Г–ї–∞.
–° —Ж–µ–ї—М—О –Њ—Ж–µ–љ–Ї–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —В–µ—А–∞–њ–Є–Є (–љ–µ —А–∞–љ–µ–µ —З–µ–Љ —З–µ—А–µ–Ј 6 –љ–µ–і. –њ–Њ—Б–ї–µ –µ–µ –Ј–∞–≤–µ—А—И–µ–љ–Є—П) –≤—Л–њ–Њ–ї–љ—П–ї–∞—Б—М –њ–Њ–≤—В–Њ—А–љ–∞—П –§–≠–У–Ф–° —Б–Њ –≤–Ј—П—В–Є–µ–Љ –±–Є–Њ–њ—В–∞—В–Њ–≤ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –∞–љ—В—А–∞–ї—М–љ–Њ–≥–Њ –Њ—В–і–µ–ї–∞, —В–µ–ї–∞ –ґ–µ–ї—Г–і–Ї–∞ –Є –Ф–Я–Ъ. –Ф–ї—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є H. pylori –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є—Б—М –±—Л—Б—В—А—Л–є —Г—А–µ–∞–Ј–љ—Л–є –•–µ–ї–њ–Є–ї-—В–µ—Б—В (–Ю–Ю–Ю ¬Ђ–Р–Ь–Р¬ї, –°–∞–љ–Ї—В-–Я–µ—В–µ—А–±—Г—А–≥, –†–Њ—Б—Б–Є—П), —Г–≥–ї–µ—А–Њ–і–љ—Л–є 13–° –і—Л—Е–∞—В–µ–ї—М–љ—Л–є —В–µ—Б—В 13C UBT (HeliforceTM, Beijing Richen-force Science Technology Co., Ltd., China), –•–µ–ї–Є–Ї-—В–µ—Б—В —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Є–љ–і–Є–Ї–∞—В–Њ—А–љ—Л—Е –•–µ–ї–Є–Ї-—В—А—Г–±–Њ–Ї (–Ю–Ю–Ю ¬Ђ–Р–Ь–Р¬ї, –°–∞–љ–Ї—В-–Я–µ—В–µ—А–±—Г—А–≥, –†–Њ—Б—Б–Є—П), –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±–Є–Њ–њ—В–∞—В–Њ–≤ —Б –Њ—Ж–µ–љ–Ї–Њ–є –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –њ–Њ –Т–Р–® –Р—А—Г–Є–љ–∞ –Ы.–Ш.
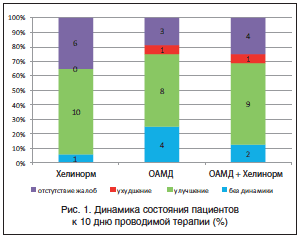
–°–Њ–≥–ї–∞—Б–љ–Њ –і–∞–љ–љ—Л–Љ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–≥–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, —Г—Б–њ–µ—И–љ–∞—П —Н—А–∞–і–Є–Ї–∞—Ж–Є—П –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є —Б—В–∞–љ–і–∞—А—В–љ–Њ–є —В–µ—А–∞–њ–Є–Є H. pylori –±—Л–ї–∞ –і–Њ—Б—В–Є–≥–љ—Г—В–∞ —Г 68,75% –і–µ—В–µ–є 2-–є –≥—А—Г–њ–њ—Л. –Ь–Њ–љ–Њ—В–µ—А–∞–њ–Є—П –•–µ–ї–Є–љ–Њ—А–Љ–Њ–Љ –≤ 1-–є –≥—А—Г–њ–њ–µ –±—Л–ї–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–∞ –≤ 50% —Б–ї—Г—З–∞–µ–≤, –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б–Њ —Б—Е–µ–Љ–Њ–є –Ї–≤–∞–і—А–Њ—В–µ—А–∞–њ–Є–Є вАУ –≤ 60% —Б–ї—Г—З–∞–µ–≤ –≤ 3-–є –≥—А—Г–њ–њ–µ. –Ш–Ј–љ–∞—З–∞–ї—М–љ–Њ –≥—А—Г–њ–њ—Л –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±—Л–ї–Є –љ–µ–Њ–і–љ–Њ—А–Њ–і–љ—Л, —В. –Ї. —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–µ –Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ —В–µ—А–∞–њ–Є–Є –њ—А–Њ–≤–Њ–і–Є–ї–Є—Б—М –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –Њ–±—К–µ–Ї—В–Є–≤–љ–Њ–≥–Њ —Б—В–∞—В—Г—Б–∞ –Є –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –≤ –≥—А—Г–њ–њ–∞—Е, –њ—А–Є–Љ–µ–љ—П–≤—И–Є—Е –•–µ–ї–Є–љ–Њ—А–Љ, –љ–∞ —Д–Њ–љ–µ —Е–Њ—А–Њ—И–µ–є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П —А–µ–ґ–µ –Њ—В–Љ–µ—З–∞–ї–Є—Б—М –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є, –Є –≤ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є —Г–Љ–µ–љ—М—И–Є–ї–Є—Б—М –њ—А–Њ—П–≤–ї–µ–љ–Є—П –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –ґ–µ–ї—Г–і–Ї–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–Њ–є (—А–Є—Б. 1).
–Э–∞—И–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ–і—В–≤–µ—А–і–Є–ї–Њ, —З—В–Њ –•–µ–ї–Є–љ–Њ—А–Љ –Њ–±–ї–∞–і–∞–µ—В –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –∞–љ—В–Є—Е–µ–ї–Є–Ї–Њ–±–∞–Ї—В–µ—А–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О –Є —Е–Њ—А–Њ—И–Є–Љ –њ—А–Њ—Д–Є–ї–µ–Љ –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є, —З—В–Њ –Њ—З–µ–љ—М –≤–∞–ґ–љ–Њ –≤ –і–µ—В—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ. –Х–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –≤ –Ї–∞—З–µ—Б—В–≤–µ –∞–і—К—О–≤–∞–љ—В–∞ –∞–љ—В–Є—Е–µ–ї–Є–Ї–Њ–±–∞–Ї—В–µ—А–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Г –і–µ—В–µ–є –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П –≤–µ—Б—М–Љ–∞ –њ–µ—А—Б–њ–µ–Ї—В–Є–≤–љ—Л–Љ, –Њ—Б–Њ–±–µ–љ–љ–Њ –≤ —Б–ї—Г—З–∞—П—Е –≤—Л—П–≤–ї–µ–љ–љ–Њ–≥–Њ –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–Є—П –Э. pylori –±–µ–Ј –∞–±—Б–Њ–ї—О—В–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞–љ–Є–є –Ї —Н—А–∞–і–Є–Ї–∞—Ж–Є–Є. –Я—А–Є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–Њ–Љ –≥–∞—Б—В—А–Є—В–µ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є—П –•–µ–ї–Є–љ–Њ—А–Љ–Њ–Љ –Є–Љ–µ–µ—В –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –њ–µ—А–µ–і —Б—В–∞–љ–і–∞—А—В–љ–Њ–є —В–µ—А–∞–њ–Є–µ–є, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –ї—Г—З—И–µ –Ї—Г–њ–Є—А—Г–µ—В –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П –Є –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –ґ–µ–ї—Г–і–Ї–∞, —З—В–Њ —П–≤–ї—П–µ—В—Б—П –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —Б–љ–Є–ґ–µ–љ–Є—П —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –∞—В—А–Њ—Д–Є—З–µ—Б–Ї–Њ–≥–Њ –≥–∞—Б—В—А–Є—В–∞ –≤ –і–Њ–ї–≥–Њ—Б—А–Њ—З–љ–Њ–є –њ–µ—А—Б–њ–µ–Ї—В–Є–≤–µ.











