В развитии хронической патологии ЖКТ, в силу цикличности течения процесса, наиболее актуальными являются продление ремиссии и предупреждение обострения болезни. Эта цель достижима при условии восстановления иммунной функции нормальной микрофлоры с помощью эффективной коррекции нарушенного микробиоценоза. В связи с этим крайне важным является поиск новых подходов к лечению хронических диарей, обеспечивающих одновременно купирование абдоминального синдрома, восстановление местного иммунитета системы пищеварения и общий иммуномодулирующий эффект.
Рецидивирующие, длительно или тяжело текущие заболевания ЖКТ, сопровождающиеся нарушением микробного пейзажа кишечника, являются показанием для введения в комплексную терапию иммуномодулирующих препаратов.
Наиболее перспективным и общепризнанным является использование иммунных препаратов, разработанных на основе иммуноглобулинов человека с высоким содержанием антибактериальных и антивирусных антител и генно–инженерного интерферона, что обеспечивает развитие активной сопротивляемости организма воздействию инфекционных агентов. Одним из таких новых отечественных препаратов, получивших в последние годы широкий спрос у специалистов и населения, стал Кипферон® суппозитории для вагинального или ректального введения (Кипферон®) Препарат содержит в себе иммуноглобулины трех основных классов – IgG, IgA и IgM и рекомбинантный человеческий интерферон альфа–2b. В одном суппозитории Кипферона® содержится 500.000 МЕ интерферона и 60 мг КИП. Кипферон® сочетает в себе антихламидийное, антибактериальное, противовирусное, противовоспалительное и иммуномодулирующее действие. Эффект препарата проявляется как во внутриклеточной, так и внеклеточной среде организма в результате непосредственного воздействия на возбудителей заболевания и прямой стимуляции местного и общего иммунитета. Все это обусловливает мощную терапевтическую и профилактическую направленность препарата Кипферон® [4,6,7].
Цель данного исследования – оценить эффективность применения препарата Кипферон® суппозитории в лечении хронических диарей у детей с патологией тонкой кишки.
Критерии включения детей в исследование:
• дети с хронической диареей, госпитализированные в соматический стационар;
• возраст ребенка (от 1 месяца до 5 лет).
Применялись следующие методы исследования: анамнез, клиническое обследование и динамическое наблюдение, лабораторные анализы (общий анализ крови, мочи, копроскопия, анализ кала на дисбактериоз), по показаниям – дополнительные лабораторные и инструментальные методы обследования в объеме стандартов диагностики основного заболевания.
Исследование выполнено на базе диагностического и отделения раннего возраста ГУ ОДКБ Н.Новгорода.
Под наблюдением находилось 62 ребенка в возрасте от 1 до 60 месяцев, средний возраст – 22,3±1,9 мес. Более половины детей (52%) имели возраст от 1 до 3 лет, мальчиков – 29 (47%) , девочек – 33 (53%).
Все обследуемые дети случайным методом (метод простой рандомизации) были разделены на 2 группы.
1 группа (основная) включала в себя 42 ребенка (20 мальчиков – 48% и 22 девочки – 52%), которые получали препарат Кипферон® суппозитории. Курс лечения длился от 5 до 14 дней. Суппозитории вводились в прямую кишку по 1–2 свече в сутки в зависимости от возраста (детям до 2–х лет по 1 свече 1 раз в сутки, старше 2–х лет по 1 свече 2 раза в сутки). Кипферон® назначался в составе комплексной терапии, включающей в зависимости от характера заболевания инфузионную терапию, антибактериальные, десенсибилизирующие, седативные, ферментные, биологические препараты, витамины, минералы и др.
2 группа (сравнения) состояла из 20 детей (9 мальчиков – 45% и 11 девочек – 55%), не получавших Кипферон® суппозитории.
У взятых под наблюдение детей с хронической диареей диагностированы: затяжной и хронический энтерит, целиакия, пострезекционный энтерит и муковисцидоз. Дети из обеих групп были сопоставимы по возрасту, полу, диагнозу, сопутствующей патологии, срокам госпитализации и характеру преморбидного фона (р=0,883) (табл. 1, 2).
Состояние детей обеих групп при поступлении оценивалось как очень тяжелое – у 2 (3,2%) больных, тяжелое – у 8 (13%), средней тяжести – у 48 (77,4%) пациентов, удовлетворительное – у 4 (6,4%) детей. Длительность госпитализации составляла от 7 до 57 дней, в среднем – 18,91±1,48 дней. Впервые госпитализировано – 34 (55%) ребенка. Подавляющее большинство детей (84%) – жители области.
Клиническая характеристика
обследуемых групп детей
Основная группа (42 ребенка)
При поступлении в стационар подавляющее большинство детей (83,3%) предъявляли жалобы на сниженный аппетит (45,2%), неустойчивый (чаще разжиженный – 57%), непереваренный (71,4%) стул, недостаточные весовые прибавки, метеоризм (43%), боли в животе, беспокойство, повышенную возбудимость, раздражительность, проявления атопического дерматита. Общее состояние лишь у 2 (4,8%) детей оценивалось как удовлетворительное; у 33 (78,5%) – как средней тяжести и у 7 (16,7%) больных как тяжелое.
Гипотрофия 1 степени диагностирована у 12 (29%) детей; гипотрофия 2 степени – у 9 (21%), гипотрофия 3 степени – у 4 (9,5%) больных; гипостатура – у 2 (4,8%) детей. Нормальное физическое развитие отмечено у 15 (35,7%) пациентов.
Нервно–психическое развитие у 23 (54,8%) детей соответствовало первой группе, у 14 (33,3%) больных – второй, у 4 (9,5%) детей – третьей группе и у 1 (2,4%) ребенка – четвертой.
При изучении анамнеза выявлено, что 35 (83,3%) пациентов были доношенными, средняя масса их тела при рождении – 3315,5±72,6 г (колебания от 2310 до 4000 г). Причем 5 (14,3%) детей имели внутриутробную гипотрофию (масса тела при рождении менее 2800 г). Соответственно 7 (16,7%) детей родились недоношенными со средней массой тела – 2101,4±236,4 г (колебания от 970 до 2860 г).
На момент госпитализации 3 (7,1%) ребенка находились на естественном вскармливании, 17 (40,5%) детей – на искусственном, 14 (33,3%) пациентов получали диету, соответствующую заболеванию, и 8 (19,1%) – питание по возрасту. Примечательно, что половина детей (56%) получали адаптированные молочные или лечебные смеси, остальные больные – неадаптированные (коровье и козье молоко, кефир) или и те и другие смеси одновременно.
Первые признаки заболевания у 11 (26,2%) детей появились с рождения, у 7 (16,7%) – в периоде новорожденности, у 6 (14,3%) больных – в первые 6 месяцев, у 14 (33,3%) – от 6 до 12 месяцев и у 4 (9,5%) пациентов – после года. Основная масса детей заболели на первом году жизни.
Группа сравнения (20 детей)
При поступлении в стационар большинство детей (80%) предъявляли жалобы на сниженный аппетит (35%), неустойчивый (чаще разжиженный – 55%), непереваренный (40%) стул, недостаточные весовые прибавки, метеоризм (20%), боли в животе, беспокойство, повышенную возбудимость, раздражительность, проявления атопического дерматита.
Общее состояние у 2 (10%) детей оценивалось как удовлетворительное; у 15 (75%) как средней тяжести и у 3 (15%) больных как тяжелое.
Хроническое расстройство питания выявлено у 13 (65%) детей, причем гипотрофия 1 степени – у 9 (45%); гипотрофия 2 степени – у 2 (10%); гипотрофия 3 степени – у 2 (10%) больных. Нормальное физическое развитие отмечено у 7 (35%) детей.
Нервно–психическое развитие у 7 (35%) детей соответствовало первой группе, у 10 (50%) больных – второй, у 3 (15%) детей – третьей группе.
При изучении анамнеза выявлено, что 18 пациентов (90%) были доношенными, средняя масса тела их при рождении 3265,44±437,1 (колебания от 2500 до 4100 г), из них 3 ребенка (16,7%) имели внутриутробную гипотрофию (масса тела менее 2800 г). Соответственно 2 детей (10%) родились недоношенными со средней массой тела – 2640 г (колебания от 2630 до 2650 г).
На момент госпитализации на естественном вскармливании не было ни одного ребенка, на искусственном – 6 (30%), 9 (45%) пациентов получали диету соответствующую заболеванию и 5 (25%) больных получали питание по возрасту. Более половины детей (69%) получали адаптированные молочные или лечебные смеси, остальные больные – неадаптированные (коровье и козье молоко, кефир) или и те и другие смеси одновременно.
Первые признаки заболевания у 3 (15%) детей появились с рождения, у 2 (10%) – в периоде новорожденности, у 8 (40%) больных – в первые 6 месяцев, у 7 (35%) – от 6 до 12 месяцев.
Оценка эффективности Кипферона®
На фоне лечения Кипфероном® у всех детей нормализовался аппетит (до лечения он был снижен у 45,2% детей; р=0,026). Срыгиваний, рвоты, поносов, задержки стула, аллергических реакций не выявлено ни у одного ребенка.
Перед выпиской половина детей, получавших Кипферон®, имели нормальное физическое развитие (до лечения таких детей было только 35,7%), уменьшилось количество больных с гипотрофией 2 и 3 степени. Общее состояние детей оценивалось как удовлетворительное (57%) и средней тяжести (43%), что существенно отличалось от состояния этих больных при поступлении (р=0,001 и р=0,0006 соответственно). У всех пациентов исчезли боли в животе, у подавляющего большинства (95,2%) – метеоризм (р=0,003), в 72% случаев нормализовался характер стула (р=0,003).
В группе сравнения на фоне базисного лечения у 5 детей появились боли в животе, у двоих – рвота, у троих отмечено ухудшение характера стула в виде учащения или разжижения
Сравнительный анализ
лабораторных показателей
В общем анализе крови анемия отмечена у 7 (16,7%) детей основной и у 5 (25%) группы сравнения. После лечения среди детей основной группы анемия сохранилась у 10% пациентов, в группе сравнения – у 46% детей (р=0,0032). Хотя средний уровень гемоглобина как в основной (121,42±1,92 г/л), так и в группе сравнения (119,16±3,99 г/л) существенно не различался.
Изменения в моче при госпитализации отмечались у каждого третьего ребенка обеих групп в виде слизи, солей (оксалаты, ураты). После лечения содержание примесей в моче в обеих группах уменьшилось в 1,5 раза.
Изменения в копрограмме выявлены у большинства детей обеих групп (у 69% больных основной и у 55% контрольной, р=0,772). После применения Кипферона® изменения в кале сохранялись у 53% детей; в группе сравнения число детей с измененной копроскопией увеличилось до 67%, хотя результаты статистически не значимы (р>0,05).
До лечения в основной группе низкий уровень детрита в кале (<4+) был у 62% детей, что говорит о нарушении переваривающей способности кишечника, после лечения таких детей стало 53% (р>0,05). Хотя результаты статистически не значимы, видна существенная положительная динамика изучаемых показателей.
В группе сравнения низкий уровень детрита в кале (<4+) выявлен у 55% обследованных детей в начале госпитализации и у 53,3% перед выпиской (р>0,05).
Стеаторея до лечения, в виде нейтрального жира, жирных кислот, мылов выявлена у 69% детей основной группы и у 45% группы сравнения. После лечения в основной группе отмечена статистически значимая положительная динамика в уменьшении числа детей со стеатореей до 27,8% (р=0,003). В группе сравнения, напротив, число больных со стеатореей увеличилось до 66,7%, что статистически значимо в сравнении с основной группой (р1–2=0,006).
В копрограмме детей обеих групп у каждого третьего встречались мышечные волокна, крахмал, растительная клетчатка, как до, так и после лечения, что подтверждает нарушение переваривания и всасывания в кишечнике, связанное с основным заболеванием, массивной медикаментозной терапией и тяжелым состоянием детей по основному и сопутствующим заболеваниям.
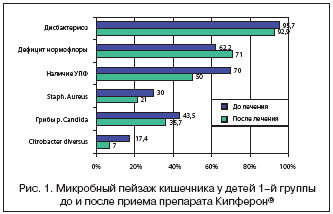
При анализе кала на дисбактериоз кишечника выявлено нарушение микробного пейзажа у подавляющего большинства (95,7% – в основной и 84,6% – в группе сравнения) обследуемых детей. Более чем у половины больных (62,2% основной и 61,5% сравнения) имело место отсутствие или дефицит нормофлоры кишечника (бифидо–, лактобактерии, кишечная палочка с нормальными ферментативными свойствами). У подавляющего большинства детей дисбактериоз кишечника был обусловлен наличием условно–патогенной флоры (70% в основной и 61,5% в группе сравнения). Из УПФ в 30% случаев в обеих группах из кала высевался золотистый стафилококк; в 43,5% основной и в 23,1% контрольной группы – грибы рода Candida; в 17,4% основной и 15,4% контрольной группы – бактерии Citrobacter diversus; в единичных случаях – протей; E. coli с измененными ферментативными свойствами, гемолитические E. coli. Необходимо отметить, что у каждого пятого ребенка дисбактериоз кишечника был обусловлен дефицитом или отсутствием отдельных представителей нормальной кишечной флоры. Примечателен тот факт, что почти в 30% случаев условно–патогенной флоре сопутствовали сапрофитный и эпидермальный стафилококки.
На фоне приема Кипферона® значительно улучшился микробный пейзаж кишечника у больных основной группы. Имелась тенденция к уменьшению количества УПФ с 70 до 50% (р=0,064) за счет золотистого стафилококка, грибов рода Candida, микробов рода Citrobacter. Полностью исчезли E. coli с измененными ферментативными свойствами, гемолитические E. coli, транзиторная флора. Ни у одного ребенка не зарегистрировано полного отсутствия нормофлоры кишечника. Достоверно увеличился удельный вес дисбактериозов 1 степени, обусловленных лишь дефицитом нормофлоры (с 17,4 до 42,9%, р=0,034). Однако отсутствие дисбактериоза кишечника отмечено только у 7,1% детей (рис. 1).
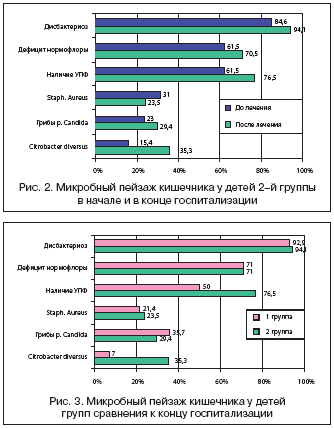
В группе сравнения после лечения следует отметить некоторую отрицательную динамику, проявляющуюся в нарастании доли детей, имеющих нарушенный микробный пейзаж кишечника (с 84,6 до 94,1%). Дисбактериоз кишечника у этих детей был обусловлен наличием УПФ в 76,5% наблюдений, дефицитом или отсутствием нормофлоры – в 17,6%, что существенно отличается от основной группы (50 и 42,9% соответственно, р=0,06). Увеличилось число больных, имеющих или не имеющих дефицит отдельных представителей нормофлоры с 61,5 до 70,5%. Отмечен рост грибов рода Candida с 23 до 29,4% (р>0,05), бактерий рода Citrobacter 15,4 до 35,3% (р=0,001). Сохранялись E. coli с измененными ферментативными свойствами, гемолитические E. coli, транзиторная флора (рис. 2).
Таким образом, видна существенная разница в составе кишечной микрофлоры в сравниваемых группах. Дети, получавшие в комплексной терапии Кипферон®, имели явное преимущество в позитивной динамике микробного пейзажа кишечника, что проявлялось статистически значимым снижением УПФ и появлением более легких дисбактериозов кишечника, обусловленных лишь дефицитом отдельных представителей нормофлоры (рис. 3).
Переносимость Кипферона®
Проведенные исследования показали хорошую переносимость препарата всеми детьми. Ни у одного ребенка не было зарегистрировано нежелательных эффектов. Необходимо отметить удобство применения препарата, в том числе у эмоционально неустойчивых и негативно относящихся к приему лекарств детей. Ни у среднего медицинского персонала, ни у родителей введение Кипферона® не вызывало никаких затруднений.
Выводы
1. Назначение Кипферона® детям с хронической диареей в соматическом отделении многопрофильной больницы позволяет существенно улучшить их общее состояние.
2. Применение Кипферона® в составе комплексной терапии хронических диарей сопровождается положительными изменениями в состоянии кишечной микрофлоры и процессах пищеварения.
3. Препарат Кипферон® характеризуется хорошей переносимостью.
Исходя из полученных данных можно утверждать, что Кипферон® высоко эффективен в комплексной терапии больных с хроническими диареями, что проявляется улучшением общего состояния, клинической симптоматики, функционального состояния кишечника, микробного пейзажа.
В связи с вышеизложенным считаем целесообразным:
1. Включать Кипферон® в комплексную терапию больных с хронической диареей, как с профилактической, так и с лечебной целью.
2. Продолжительность профилактического курса применения Кипферона® должна быть 5 дней, лечебного – до 10 дней.


Литература
1. Хромова С.С., Кафарская Л.И., Ефимов Б.А. Иммунитет у детей: от рождения к колонизации кишечника // Вопросы детской диетологии. – 2006. – Т. 4, № 1. – С. 15–19.
2. Хавкин А.И. Микробиоценоз кишечника и иммунитет // РМЖ. – 2003. Т. 11, № 3. – С. 3–7.
3. Мухина Ю.Г., Дубровская М.И., Кафарская Л.И. Иммунная система и микрофлора кишечника у детей. Обоснование функционального питания // Фарматека. – 2006. № 2. – С. 22–28.
4. Опыт применения Кипферона в практике педиатра. Факты и комментарии. Под ред. Г. В. Римарчук. Сборник статей. – М., 2008. – С. 32.
5. Щеплягина Л.А., Чернов В.М., Круглова И.В., Делягин В.М. Возрастные особенности иммунитета у детей. Лекция для врачей. – М., 2008. – С. 36.
6. Кондрашин Ю.И., Денисов А.К., Мигранова О.М. О практике применения нового отечественного иммунотропного препарата «Кипферон, суппозитории» при вирусно–бакткриальных инфекций // РМЖ. – 2006. Т.14, № 19. – С. 1361–1363.
7. Применение иммунобиологического препарата «Кипферон, суппозитории» для вагинального или ректального введения при лечении детей с различной инфекционной патологией. Пособие для врачей. М., – 2007. – С. 30.











