У пациентов с острым бронхитом и продуктивным кашлем раннее назначение секретолитических и отхаркивающих препаратов с целью восстановления мукоцилиарного клиренса является важной мерой профилактики суперинфекции. Особое значение это имеет у детей. Такие лекарственные растения, как тимьян и плющ, способствуют эффективному откашливанию благодаря разжижению вязкой бронхиальной слизи и улучшению транспортной функции ресничек [1]. В двойном–слепом исследовании, включавшем взрослых с острым бронхитом и продуктивным кашлем, ежедневно оценивали частоту приступов кашля с помощью ручного счетчика. Показано, что назначение жидкого экстракта травы тимьяна и листьев плюща сопровождалось быстрым и выраженным уменьшением количества приступов кашля [3]. У детей, особенно младшего возраста, самостоятельный точный подсчет эпизодов кашля не представляется возможным, так как счетчик будет использоваться скорее как игрушка. Постмаркетинговые наблюдательные (обсервационные) исследования в соответствии с Германским Законом о лекарственных препаратах (§ 67, абзац 6) дают возможность не только защитить детей от непредвиденных побочных эффектов лекарственных препаратов, но и повысить эффективность и безопасность лекарственных средств. Основной целью данного постмаркетингового наблюдательного исследования (ПНИ) было показать безопасность амбулаторного лечения жидким экстрактом травы тимьяна и листьев плюща (сиропом Бронхипрет®) у детей и подростков в соответствующих возрасту дозах.
Методы
Дизайн исследования
Данное проспективное ПНИ проводили в 60 медицинских офисах частнопрактикующих врачей–педиатров и семейных врачей в Германии с начала ноября 2005 г. по начало марта 2006 г. В соответствии с наблюдательным (обсервационным) характером исследования не требовалось проведение диагностических и лечебных мероприятий, которые бы выходили за рамки стандартных процедур при остром бронхите у детей и подростков. Такие ПНИ не вызывают сомнений с точки зрения этики.
Критерии включения
В ПНИ включали пациентов женского и мужского пола в возрасте 2–17 лет с диагнозом острого бронхита (ICD–10: J20) и наличием продуктивного кашля в течение 2 дней и более. Пациенты должны были иметь 10 и более эпизодов кашля в сутки, предшествующих началу лечения (по оценке родителей или подростков с 13 лет) и оценку 5 баллов и более по шкале тяжести бронхита (Bronchitis Severity Score, BSS) [3]. Эпизодом кашля считали три или более следующих друг за другом кашлевых толчка, не разделенных вдохом.
Лечение
Пациенты принимали сироп от кашля в соответствующих возрасту дозировках (2–5 лет: 3 x 3,2 мл; 6–11 лет: 3 x 4,3 мл, 12–17 лет: 3 x 5,4 мл), согласно действующей инструкции по применению препарата [2]. Длительность терапии зависела от течения заболевания у каждого пациента. Разрешалось применение любых других препаратов, все назначения должны были быть документированы.
В 100,0 г сиропа Бронхипрет® содержатся действу-ющие компоненты: 15,0 г жидкого экстракта травы тимьяна (1:2–2,5; экстрагирующее вещество по DAB [Германская фармакопея, Deutsches Arzneibuch]), 1,5 г жидкого экстракта листьев плюща (1:1; экстрагирующее вещество: этанол 70% в объемном отношении) и 7% этанол (в объемном отношении). Вспомогательные вещества: сироп мальтитный; калия сорбат и вода очищенная.
Сбор данных/длительность наблюдения
Длительность наблюдения в рамках ПНИ составляла в среднем 10 дней. Было запланировано три эпизода оценки состояния и регистрации данных в обычные для заболевания временные промежутки:
• при первом визите к врачу в начале заболевания (исходные данные, день 0);
• промежуточная оценка на 2–м визите (4–й день);
• заключительная оценка на 3–м визите (10–й день).
Сбор данных проводили с помощью стандартизированных историй болезни в соответствии с планом наблюдения.
Критерии оценки
На 1–м визите регистрировали демографические данные, критерии включения, сопутствующие заболевания, предшествующую терапию и температуру тела. Первичным критерием оценки эффективности препарата в исследовании являлось изменение клинической симптоматики по шкале BSS в среднем через 4 (визит 2) или 10 дней (визит 3) по сравнению с исходным состоянием (на визите 1). Вторичными критериями оценки эффективности являлись изменение частоты приступов кашля (по оценке родителей/подростков) за сутки, оценивавшееся по утрам (визиты 2 и 3), по сравнению с исходной (визит 1), а также ответ на терапию (доля ответивших на терапию (респондеры) = пациенты с выздоровлением или улучшением и доля не ответивших на терапию (нон–респондеры) = пациенты без изменений или с ухудшением).
На визитах 2 и 3 регистрировали изменение сопутствующей терапии и течения сопутствующих заболеваний. Для оценки переносимости оценивали частоту нежелательных явлений (НЯ), переносимость препарата в целом, по мнению врача и родителей/подростков, на 3–м визите и динамику температуры тела (визиты 2 и 3). Долю принятых пациентами доз препарата (комплайентность) оценивали по зафиксированным данным о регулярности приема ежедневных доз.
Контроль качества
Чтобы обеспечить точную диагностику и правильное лечение детей и подростков, в исследовании участвовали исключительно врачи–педиатры и семейные врачи. Перед началом исследования примерно 80% врачей посещались и инструктировались мониторами независимой контрактной исследовательской организации, оставшиеся 20% врачей получали инструкции по телефону. Во время ПНИ ход исследования контролировали по телефону. После сбора данных с помощью компьютерной обработки оценивали их полноту и достоверность. В случайной выборке, включавшей 2,5% всех пациентов, проводили сверку данных ПНИ с исходными историями болезни. Мониторирование ПНИ, планирование, регистрация данных и статистический анализ проводились специалистами вышеуказанной контрактной исследовательской организации.
Статистика
Описательный анализ данных проводили с помощью SAS®, версии 8.2, по предварительно установленному плану статистического анализа. Сопутствующие заболевания и НЯ обозначали в соответствии со словарем MedDRA, версии 9.0, сопутствующие заболевания кодировали в соответствии с классификацией ВОЗ (WHO–DRL, от сентября 2003 г.).
Результаты
Исследуемая популяция
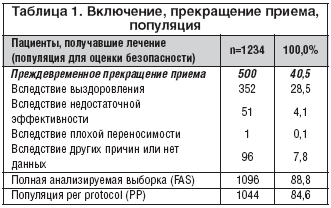
В статистический анализ (вся популяция и стратификация по разным возрастным группам) вошли данные 1234 пациентов, получавших терапию жидким экстрактом травы тимьяна и листьев плюща (611 [49,5%] девочек, 623 [50,5%] мальчиков в возрасте от 7 мес. до 17 лет, из них 12 детей младшего возраста [<2 лет], 372 дошкольника [2–5 лет], 438 школьников [6–11 лет] и 412 подростков [12–17 лет]). Для включения в полную анализируемую выборку (FAS) достаточные данные имелись у 1096 пациентов (88,8%). В этой выборке в случае отсутствия оценки по шкале BSS использовали предыдущую оценку. Популяция per protocol (PP) включала полные данные 1044 пациентов (84,6%) (табл. 1). Данные пациента исключали из полной анализируемой выборки в случае несоответствия пациента критериям включения (менее 10 эпизодов кашля, отмеченных в день перед 1–м визитом, и/или оценка <5 баллов по шкале BSS на 1–м визите), и/или отсутствия оценки по шкале BSS на 2–м или 3–м визите (исключение: выздоровление или прекращение приема препарата из–за его неэффективности). В популяции PP недостающую оценку по шкале BSS заменяли предыдущей только у тех пациентов, которые преждевременно прекратили лечение из–за выздоровления или неэффективности терапии. Самой частой причиной преждевременного прекращения терапии являлось успешное лечение (выздоровление: n=352; 28,5%); только в одном случае (0,1%) причиной прекращения терапии явилась плохая переносимость. У 51 пациента (4,1%) причиной прекращения лечения стала недостаточная эффективность. 95 пациентов (7,7%) не явились на контрольный визит. 734 пациента (59,5%) принимали препарат до конца периода наблюдения (табл. 1). Из 1234 пациентов, включенных в анализ, на 2 визит явились 1177 (данные промежуточной оценки) и на 3–й визит – 1151 (данные заключительной оценки). Биометрический анализ данных по переносимости проводили по вышеописанным четырем возрастным группам (< 2 лет: n=12; 2–5 лет: n=272; 6–11 лет: n=438; 12–17 лет: n=412). При оценке эффективности группа детей младшего возраста отсутствовала, так как немногочисленные пациенты в возрасте менее 2 лет были отнесены к возрастной группе «от 2 до 5 лет».
Лечение
В целом 973 пациента (78,8%) получали монотерапию экстрактом травы тимьяна и листьев плюща, 135 пациентов (10,9%) – экстракт в комбинации с антибиотиками и 126 пациентов (10,2%) – экстракт в комбинации с другими препаратами (преимущественно назальными средствами и средствами от простуды).
Дозы и отношение к терапии
Дозы препарата соответствовали рекомендованным в инструкции по применению препарата для возрастных групп «от 2 до 5 лет», «от 6 до 11 лет» и «от 12 до 17 лет». Дети младше 2 лет, как правило, получали такие же дозы, как в группе «от 2 до 5 лет». Отношение пациентов к терапии было очень хорошим во всех возрастных группах. 91,0% – 94,8% родителей или подростков сообщали о регулярном приеме назначенных дозировок.
Динамика критерия оценки эффективности
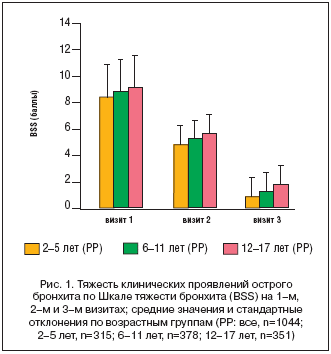
Клиническая симптоматика (шкала тяжести бронхита, Bronchitis Severity Score [BSS]). При исходном обследовании средняя суммарная оценка по шкале BSS составила 8,8±3,0 балла (PP). Как при монотерапии экстрактом травы тимьяна и листьев плюща (исходная оценка по BSS 8,9 балла), так и при сопутствующем лечении антибиотиками (исходная оценка по BSS 8,9 балла) отмечено быстрое и выраженное уменьшение клинической симптоматики. По данным промежуточной оценки, в среднем после 4 дней лечения средний балл BSS по всем группам уменьшился почти вдвое (4,8±2,9 балла). К моменту заключительной оценки в среднем через 10 дней терапии отмечено дальнейшее уменьшение BSS на 1,3±2,2 балла (PP). На рисунке 1 представлено снижение BSS под отдельности в каждой из трех возрастных групп (PP) (средние значения и стандартные отклонения) с 1–й по 3–й визиты.
Кашель
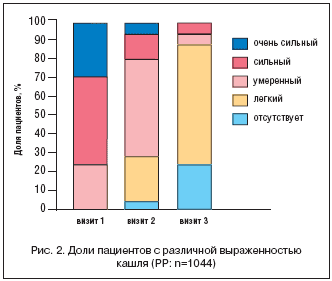
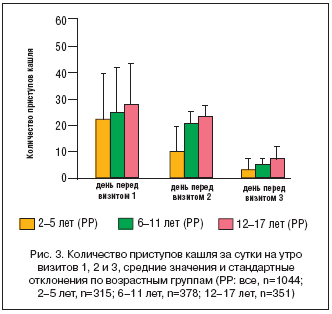
Показано клинически значимое уменьшение выраженности кашля (отдельный показатель в шкале BSS) (рис. 2). Суточное количество эпизодов кашля значительно уменьшилось на 81,3% с 25,1 (±24,2) в начале лечения до 4,7 (±10,8) в конце. На рисунке 3 представлено выраженное уменьшение количества эпизодов кашля с 1–го по 3–й визит по 3 возрастным группам (PP) (средние значения и стандартные отклонения).
Ответ на лечение, по мнению врачей
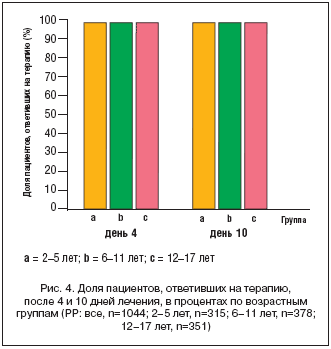
У большинства пациентов при заключительной оценке отмечено выздоровление (n=675 [64,7%]) или улучшение (n=306 [29,3%]) (частота ответа на лечение: 94,0%; PP). Уже после 4 дней лечения 898 пациентов (86,0%) были отнесены в группу ответивших на терапию. Частота ответа на лечение в 3 возрастных группах составила от 92,0% до 96,5% (рис. 4). 52 пациента (5,0%) были расценены как не ответившие на терапию.
Переносимость
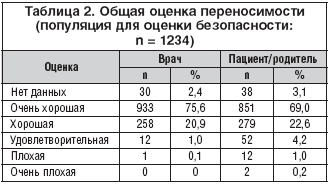
У двух пациенток (0,2%) из 1234 отмечены преходящие, нетяжелые нежелательные явления (НПД) с возможной связью с терапией. Одна двенадцатилетняя девочка, получавшая экстракт травы тимьяна и листьев плюща, в первый день лечения жаловалась на боли в животе. У другой девочки в возрасте 9 лет, получавшей также антибиотики, отмечена легкая тошнота на второй день терапии. В дальнейшем этой пациентке была назначена терапия по поводу мочевой инфекции. Переносимость препарата была хорошей или очень хорошей в 96,5% случаев (табл. 2). Подъем температуры тела более чем на 1,5°C по сравнению с исходной температурой в начале наблюдения зарегистрирован на 4–й и 10–й день соответственно у 12 (1,0%) и 9 (0,7%) из 1234 пациентов.
Обсуждение
Результаты данного постмаркетингового наблюдательного исследования, включавшего крупную выборку больных, показали, что комбинация жидкого экстракта травы тимьяна и листьев плюща является эффективным и безопасным средством лечения острого бронхита с продуктивным кашлем у маленьких детей и подростков. Десятидневный курс лечения соответствующими возрасту дозами препарата обеспечивал отчетливое уменьшение тяжести симптомов или выздоровление при очень хорошей переносимости. Методика данного постмаркетингового наблюдательного исследования во многом согласовалась с методикой проведенного в 2006 г. рандомизированного двойного–слепого исследования применения жидкого экстракта травы тимьяна и листьев плюща у 361 взрослого [3]. Это подтверждающее клиническое исследование продемонстрировало статистически и клинически значимое превосходство комбинации травы тимьяна и листьев плюща над плацебо при десятидневном лечении острого бронхита с продуктивным кашлем. Показан более быстрый и полный регресс клинической симптоматики (BSS). Оценка по шкале BSS уменьшилась на 6,6 балла. Количество эпизодов кашля уменьшилось на 68,7%. Кроме того, показана значительно более высокая частота ответа на терапию травой тимьяна и листьями плюща после четырех дней (83,0% по сравнению с 53,9% при приеме плацебо) и 10 дней лечения (96,2% по сравнению с 74,7%) при сходной переносимости. Даже с учетом открытого дизайна постмаркетингового наблюдательного исследования продемонстрированное в нем уменьшение оценки по шкале BSS на 7,5 балла, а также снижение числа эпизодов кашля на 81,3% вполне согласовалось с результатами подтверждающего рандомизированного исследования. Частота ответа на терапию 94,0% также была сопоставима с частотой в контролируемом исследовании (96,2%). Самой высокой была частота ответа на терапию у детей младше 6 лет (96,5%), несколько ниже – в средней (93,7%) и старшей (92,0%) возрастных группах, что соответствовало отношению к терапии в исследуемых возрастных группах. У детей младше 6 лет, которые, безусловно, принимали препарат под контролем родителей, отмечена самая высокая комплайентность (94,8%), которая снижалась в более старших возрастных группах до 94,3% у детей до 11 лет и 91,7% у подростков с 12 лет.
Пациенты ПНИ и контролируемого исследования имели сходную тяжесть заболевания до начала лечения (BSS, количество эпизодов кашля за сутки). Это свидетельствует о репрезентативности выборки пациентов с острым бронхитом и продуктивным кашлем. Следует подчеркнуть, что отмеченный хороший терапевтический эффект препарата не сопровождался значительными нежелательными явлениями. Напротив, при частоте нежелательных явлений 0,2% следует говорить об очень хорошей переносимости препарата. Таким образом, исследуемый сироп от кашля заслуживает более широкого применения у детей.
по материалам статьи O. Marzian «Behandlung der akuten Bronchitis bei Kindern und Jugendlichen
Anwendungsbeobachtung bestatigt Nutzen
und Unbedenklichkeit einer Fluussigextrakt-Kombination
aus Thymiankraut und Efeublattern».
MMW–Fortschritte der Medizin Originalien,
Nr. II/2007 (149. Jg.), S. 69–74
Литература:
1. Behandlungsprobleme Husten und Bronchitis. Teil II: Auswurffordernde und krampflosende Mittel.
Zeitschrift fur Phytotherapie 27 (2006), 27–30.
2. Bionorica AG: Fachinformation Bronchipret® Saft. Status Juli 2002. Bundesverband der Pharmazeutischen Industrie e.V., Fachinfo–Service.
3. Kemmerich, B., Eberhardt, R., Stammer, H.: Efficacy and tolerability of a fluid extract combination of thyme herb and ivy leaves and matched placebo in adults suffering from acute bronchitis with productive cough. A prospective, double–blind, placebocontrolled clinical trial. Arzneim.–Forsch./Drug Res. 56 (2006), 652–660.











