–Я–Њ–≤—Л—И–µ–љ–Є–µ —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л —В–µ–ї–∞ —П–≤–ї—П–µ—В—Б—П –Њ–і–љ–Є–Љ –Є–Ј –≤–∞–ґ–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –≤ –і–µ—В—Б–Ї–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–µ. –Ы–Є—Е–Њ—А–∞–і–Њ—З–љ—Л–µ —Б–Њ—Б—В–Њ—П–љ–Є—П —Г –і–µ—В–µ–є – –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В—Л–є –њ–Њ–≤–Њ–і –Њ–±—А–∞—Й–µ–љ–Є–є –Ї –≤—А–∞—З—Г, —Е–Њ—В—П –і–Њ–≤–Њ–ї—М–љ–Њ —З–∞—Б—В–Њ –Љ–љ–Њ–≥–Є–µ —А–Њ–і–Є—В–µ–ї–Є –њ—Л—В–∞—О—В—Б—П —Б–љ–Є–Ј–Є—В—М –њ–Њ–≤—Л—И–µ–љ–љ—Г—О —В–µ–Љ–њ–µ—А–∞—В—Г—А—Г —В–µ–ї–∞ —Г –і–µ—В–µ–є —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ, –њ—А–Є–Љ–µ–љ—П—П –ґ–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–Є–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞, –Њ—В–њ—Г—Б–Ї–∞–µ–Љ—Л–µ –±–µ–Ј —А–µ—Ж–µ–њ—В–∞ –≤—А–∞—З–∞ [6,7]. –Ґ–∞–Ї–ґ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л–Љ–Є –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —П–≤–ї—П—О—В—Б—П –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П —Г –і–µ—В–µ–є, –Њ–њ—А–µ–і–µ–ї—П—О—Й–Є–µ –љ–µ—А–µ–і–Ї–Њ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є —В–µ—З–µ–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –њ—А–Њ—В–µ–Ї–∞—О—Й–Є—Е —Б –ї–Є—Е–Њ—А–∞–і–Ї–Њ–є, –Є –њ–Њ–≤—Л—И–∞—О—Й–Є–µ —А–Є—Б–Ї –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є—Е —А–µ–∞–Ї—Ж–Є–є –љ–∞ –њ—А–Є–Љ–µ–љ—П–µ–Љ—Л–µ –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В—Л. –Т–Њ–њ—А–Њ—Б—Л —Н—В–Є–Њ–њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ –≥–Є–њ–µ—А—В–µ—А–Љ–Є–Є –Є —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –њ–Њ–і—Е–Њ–і—Л –Ї —В–µ—А–∞–њ–Є–Є –ї–Є—Е–Њ—А–∞–і–Њ—З–љ—Л—Е —Б–Њ—Б—В–Њ—П–љ–Є–є –і–Њ —Б–Є—Е –њ–Њ—А —П–≤–ї—П—О—В—Б—П –∞–Ї—В—Г–∞–ї—М–љ—Л–Љ–Є –њ—А–Њ–±–ї–µ–Љ–∞–Љ–Є –њ–µ–і–Є–∞—В—А–Є–Є.
–Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—В—М —В–µ–Љ–њ–µ—А–∞—В—Г—А—Г —В–µ–ї–∞ –љ–∞ –њ–Њ—Б—В–Њ—П–љ–љ–Њ–Љ —Г—А–Њ–≤–љ–µ, –≤–љ–µ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —В–µ–Љ–њ–µ—А–∞—В—Г—А–љ—Л—Е –Ї–Њ–ї–µ–±–∞–љ–Є–є –≤–љ–µ—И–љ–µ–є —Б—А–µ–і—Л (–≥–Њ–Љ–Њ–є–Њ—В–µ—А–Љ–љ–Њ—Б—В—М), –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Њ—А–≥–∞–љ–Є–Ј–Љ—Г —Б–Њ—Е—А–∞–љ—П—В—М –≤—Л—Б–Њ–Ї—Г—О –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –Є –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В –Ї–Њ–ї–µ–±–∞–љ–Є–є —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л –Њ–Ї—А—Г–ґ–∞—О—Й–µ–є —Б—А–µ–і—Л. –У–Њ–Љ–Њ–є–Њ—В–µ—А–Љ–љ–Њ—Б—В—М —Г —З–µ–ї–Њ–≤–µ–Ї–∞ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–∞ –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ –љ–∞–ї–Є—З–Є–µ–Љ —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ —В–µ—А–Љ–Њ—А–µ–≥—Г–ї—П—Ж–Є–Є, —В.–µ. —А–µ–≥—Г–ї—П—Ж–Є–Є —В–µ–њ–ї–Њ–њ—А–Њ–і—Г–Ї—Ж–Є–Є –Є —В–µ–њ–ї–Њ–Њ—В–і–∞—З–Є. –Ъ–Њ–љ—В—А–Њ–ї—М –Ј–∞ —Г—А–∞–≤–љ–Њ–≤–µ—И–Є–≤–∞–љ–Є–µ–Љ –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ —В–µ–њ–ї–Њ–њ—А–Њ–і—Г–Ї—Ж–Є–Є –Є —В–µ–њ–ї–Њ–Њ—В–і–∞—З–Є –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–µ—В—Б—П —Ж–µ–љ—В—А–Њ–Љ —В–µ—А–Љ–Њ—А–µ–≥—Г–ї—П—Ж–Є–Є, —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ—Л–Љ –≤ –њ—А–µ–Њ–њ—В–Є—З–µ—Б–Ї–Њ–є –Њ–±–ї–∞—Б—В–Є –њ–µ—А–µ–і–љ–µ–є —З–∞—Б—В–Є –≥–Є–њ–Њ—В–∞–ї–∞–Љ—Г—Б–∞. –Ш–љ—Д–Њ—А–Љ–∞—Ж–Є—П –Њ —В–µ–Љ–њ–µ—А–∞—В—Г—А–љ–Њ–Љ –±–∞–ї–∞–љ—Б–µ –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –њ–Њ—Б—В—Г–њ–∞–µ—В –≤ —Ж–µ–љ—В—А —В–µ—А–Љ–Њ—А–µ–≥—Г–ї—П—Ж–Є–Є, –≤–Њ––њ–µ—А–≤—Л—Е, —З–µ—А–µ–Ј –љ–µ–є—А–Њ–љ—Л —Ж–µ–љ—В—А–∞ —В–µ—А–Љ–Њ—А–µ–≥—Г–ї—П—Ж–Є–Є, —А–µ–∞–≥–Є—А—Г—О—Й–Є–µ –љ–∞ –Є–Ј–Љ–µ–љ–µ–љ–Є–µ —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л –Ї—А–Њ–≤–Є –Є, –≤–Њ––≤—В–Њ—А—Л—Е, –Њ—В –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е —В–µ—А–Љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –≤ –Њ—Б—Г—Й–µ—Б—В–≤–ї–µ–љ–Є–Є –≥–Є–њ–Њ—В–∞–ї–∞–Љ–Є—З–µ—Б–Ї–Њ–є —А–µ–≥—Г–ї—П—Ж–Є–Є —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л —В–µ–ї–∞ —Г—З–∞—Б—В–≤—Г—О—В –Є –ґ–µ–ї–µ–Ј—Л –≤–љ—Г—В—А–µ–љ–љ–µ–є —Б–µ–Ї—А–µ—Ж–Є–Є, –≥–ї–∞–≤–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Й–Є—В–Њ–≤–Є–і–љ–∞—П –ґ–µ–ї–µ–Ј–∞ –Є –љ–∞–і–њ–Њ—З–µ—З–љ–Є–Ї–Є. –С–ї–∞–≥–Њ–і–∞—А—П –Ї–Њ–Њ—А–і–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л–Љ –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ —В–µ–њ–ї–Њ–њ—А–Њ–і—Г–Ї—Ж–Є–Є –Є —В–µ–њ–ї–Њ–Њ—В–і–∞—З–Є –њ–Њ–і–і–µ—А–ґ–Є–≤–∞–µ—В—Б—П –њ–Њ—Б—В–Њ—П–љ—Б—В–≤–Њ —В–µ–њ–ї–Њ–≤–Њ–≥–Њ –≥–Њ–Љ–µ–Њ—Б—В–∞–Ј–∞ –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ (—А–Є—Б.1).
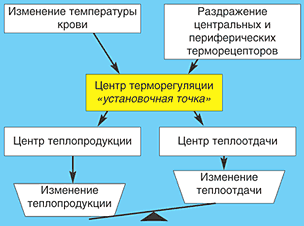
–†–Є—Б. 1. –Ь–µ—Е–∞–љ–Є–Ј–Љ—Л —В–µ—А–Љ–Њ—А–µ–≥—Г–ї—П—Ж–Є–Є
–≠—В–Є–Њ–њ–∞—В–Њ–≥–µ–љ–µ–Ј –ї–Є—Е–Њ—А–∞–і–Ї–Є–Т –Њ—В–≤–µ—В –љ–∞ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ —А–∞–Ј–ї–Є—З–љ—Л—Е –њ–∞—В–Њ–≥–µ–љ–љ—Л—Е —А–∞–Ј–і—А–∞–ґ–Є—В–µ–ї–µ–є –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –њ–µ—А–µ—Б—В—А–Њ–є–Ї–∞ —В–µ–Љ–њ–µ—А–∞—В—Г—А–љ–Њ–≥–Њ –≥–Њ–Љ–µ–Њ—Б—В–∞–Ј–∞, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–∞—П –љ–∞ –њ–Њ–≤—Л—И–µ–љ–Є–µ —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л —В–µ–ї–∞ —Б —Ж–µ–ї—М—О –њ–Њ–≤—Л—И–µ–љ–Є—П –µ—Б—В–µ—Б—В–≤–µ–љ–љ–Њ–є —А–µ–∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Њ—А–≥–∞–љ–Є–Ј–Љ–∞. –Ґ–∞–Ї–Њ–µ –њ–Њ–≤—Л—И–µ–љ–Є–µ —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л –љ–∞–Ј—Л–≤–∞—О—В –ї–Є—Е–Њ—А–∞–і–Ї–Њ–є. –Ы–Є—Е–Њ—А–∞–і–Ї–∞ —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞–µ—В—Б—П, –Ї–∞–Ї –Ј–∞—Й–Є—В–љ–Њ––њ—А–Є—Б–њ–Њ—Б–Њ–±–Є—В–µ–ї—М–љ–∞—П —А–µ–∞–Ї—Ж–Є—П –Њ—А–≥–∞–љ–Є–Ј–Љ–∞, –≤–Њ–Ј–љ–Є–Ї–∞—О—Й–∞—П –≤ –Њ—В–≤–µ—В –љ–∞ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –њ–∞—В–Њ–≥–µ–љ–љ—Л—Е —А–∞–Ј–і—А–∞–ґ–Є—В–µ–ї–µ–є –Є —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—Й–∞—П—Б—П –њ–µ—А–µ—Б—В—А–Њ–є–Ї–Њ–є –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ —В–µ—А–Љ–Њ—А–µ–≥—Г–ї—П—Ж–Є–Є, –њ—А–Є–≤–Њ–і—П—Й–Є—Е –Ї –њ–Њ–≤—Л—И–µ–љ–Є—О —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л —В–µ–ї–∞ –Є —Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–Є—Е –µ—Б—В–µ—Б—В–≤–µ–љ–љ—Г—О —А–µ–∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Њ—А–≥–∞–љ–Є–Ј–Љ–∞. –С–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –ї–Є—Е–Њ—А–∞–і–Ї–Є –Ј–∞–Ї–ї—О—З–∞–µ—В—Б—П –≤ –њ–Њ–≤—Л—И–µ–љ–Є–Є –Є–Љ–Љ—Г–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –Ј–∞—Й–Є—В—Л. –Я–Њ–≤—Л—И–µ–љ–Є–µ —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л —В–µ–ї–∞ –њ—А–Є–≤–Њ–і–Є—В –Ї —Г—Б–Є–ї–µ–љ–Є—О —Д–∞–≥–Њ—Ж–Є—В–Њ–Ј–∞, —Г–≤–µ–ї–Є—З–µ–љ–Є—О —Б–Є–љ—В–µ–Ј–∞ –Є–љ—В–µ—А—Д–µ—А–Њ–љ–Њ–≤, –∞–Ї—В–Є–≤–∞—Ж–Є–Є –Є –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–Ї–µ –ї–Є–Љ—Д–Њ—Ж–Є—В–Њ–≤ –Є —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є –∞–љ—В–Є—В–µ–ї–Њ–≥–µ–љ–µ–Ј–∞. –Я–Њ–≤—Л—И–µ–љ–љ–∞—П —В–µ–Љ–њ–µ—А–∞—В—Г—А–∞ —В–µ–ї–∞ –њ—А–µ–њ—П—В—Б—В–≤—Г–µ—В —А–∞–Ј–Љ–љ–Њ–ґ–µ–љ–Є—О –≤–Є—А—Г—Б–Њ–≤, –Ї–Њ–Ї–Ї–Њ–≤ –Є –і—А—Г–≥–Є—Е –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤.
–Т –Њ—В–≤–µ—В –љ–∞ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ —А–∞–Ј–ї–Є—З–љ—Л—Е –њ–∞—В–Њ–≥–µ–љ–љ—Л—Е —А–∞–Ј–і—А–∞–ґ–Є—В–µ–ї–µ–є –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –њ–µ—А–µ—Б—В—А–Њ–є–Ї–∞ —В–µ–Љ–њ–µ—А–∞—В—Г—А–љ–Њ–≥–Њ –≥–Њ–Љ–µ–Њ—Б—В–∞–Ј–∞, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–∞—П –љ–∞ –њ–Њ–≤—Л—И–µ–љ–Є–µ —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л —В–µ–ї–∞ —Б —Ж–µ–ї—М—О –њ–Њ–≤—Л—И–µ–љ–Є—П –µ—Б—В–µ—Б—В–≤–µ–љ–љ–Њ–є —А–µ–∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Њ—А–≥–∞–љ–Є–Ј–Љ–∞. –Ґ–∞–Ї–Њ–µ –њ–Њ–≤—Л—И–µ–љ–Є–µ —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л –љ–∞–Ј—Л–≤–∞—О—В –ї–Є—Е–Њ—А–∞–і–Ї–Њ–є. , –≤–Њ–Ј–љ–Є–Ї–∞—О—Й–∞—П –≤ –Њ—В–≤–µ—В –љ–∞ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –њ–∞—В–Њ–≥–µ–љ–љ—Л—Е —А–∞–Ј–і—А–∞–ґ–Є—В–µ–ї–µ–є –Є —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—Й–∞—П—Б—П –њ–µ—А–µ—Б—В—А–Њ–є–Ї–Њ–є –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ —В–µ—А–Љ–Њ—А–µ–≥—Г–ї—П—Ж–Є–Є, –њ—А–Є–≤–Њ–і—П—Й–Є—Е –Ї –њ–Њ–≤—Л—И–µ–љ–Є—О —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л —В–µ–ї–∞ –Є —Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–Є—Е –µ—Б—В–µ—Б—В–≤–µ–љ–љ—Г—О —А–µ–∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Њ—А–≥–∞–љ–Є–Ј–Љ–∞. –С–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –ї–Є—Е–Њ—А–∞–і–Ї–Є –Ј–∞–Ї–ї—О—З–∞–µ—В—Б—П –≤ –њ–Њ–≤—Л—И–µ–љ–Є–Є –Є–Љ–Љ—Г–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –Ј–∞—Й–Є—В—Л. –Я–Њ–≤—Л—И–µ–љ–Є–µ —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л —В–µ–ї–∞ –њ—А–Є–≤–Њ–і–Є—В –Ї —Г—Б–Є–ї–µ–љ–Є—О —Д–∞–≥–Њ—Ж–Є—В–Њ–Ј–∞, —Г–≤–µ–ї–Є—З–µ–љ–Є—О —Б–Є–љ—В–µ–Ј–∞ –Є–љ—В–µ—А—Д–µ—А–Њ–љ–Њ–≤, –∞–Ї—В–Є–≤–∞—Ж–Є–Є –Є –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–Ї–µ –ї–Є–Љ—Д–Њ—Ж–Є—В–Њ–≤ –Є —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є –∞–љ—В–Є—В–µ–ї–Њ–≥–µ–љ–µ–Ј–∞. –Я–Њ–≤—Л—И–µ–љ–љ–∞—П —В–µ–Љ–њ–µ—А–∞—В—Г—А–∞ —В–µ–ї–∞ –њ—А–µ–њ—П—В—Б—В–≤—Г–µ—В —А–∞–Ј–Љ–љ–Њ–ґ–µ–љ–Є—О –≤–Є—А—Г—Б–Њ–≤, –Ї–Њ–Ї–Ї–Њ–≤ –Є –і—А—Г–≥–Є—Е –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤.–Ы–Є—Е–Њ—А–∞–і–Ї–∞ –њ—А–Є–љ—Ж–Є–њ–Є–∞–ї—М–љ–Њ –Њ—В–ї–Є—З–∞–µ—В—Б—П –Њ—В –њ–Њ–≤—Л—И–µ–љ–Є—П —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л —В–µ–ї–∞ –њ—А–Є –њ–µ—А–µ–≥—А–µ–≤–∞–љ–Є–Є –Њ—А–≥–∞–љ–Є–Ј–Љ–∞, –≤–Њ–Ј–љ–Є–Ї–∞—О—Й–µ–≥–Њ –Њ—В —А–∞–Ј–ї–Є—З–љ—Л—Е –њ—А–Є—З–Є–љ: –њ—А–Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ –њ–Њ–≤—Л—И–µ–љ–Є–Є —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л –Њ–Ї—А—Г–ґ–∞—О—Й–µ–є —Б—А–µ–і—Л, –∞–Ї—В–Є–≤–љ–Њ–є –Љ—Л—И–µ—З–љ–Њ–є —А–∞–±–Њ—В–µ –Є –і—А. –Я—А–Є –њ–µ—А–µ–≥—А–µ–≤–µ —Б–Њ—Е—А–∞–љ—П–µ—В—Б—П —Г—Б—В–∞–љ–Њ–≤–Ї–∞ —Ж–µ–љ—В—А–∞ —В–µ—А–Љ–Њ—А–µ–≥—Г–ї—П—Ж–Є–Є –љ–∞ –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—О —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –њ—А–Є –ї–Є—Е–Њ—А–∞–і–Ї–µ —Ж–µ–љ—В—А —В–µ—А–Љ–Њ—А–µ–≥—Г–ї—П—Ж–Є–Є —Ж–µ–ї–µ–љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ –њ–µ—А–µ—Б—В—А–∞–Є–≤–∞–µ—В «—Г—Б—В–∞–љ–Њ–≤–Њ—З–љ—Г—О —В–Њ—З–Ї—Г» –љ–∞ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–є —Г—А–Њ–≤–µ–љ—М —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л —В–µ–ї–∞.
–Я–Њ—Б–Ї–Њ–ї—М–Ї—Г –ї–Є—Е–Њ—А–∞–і–Ї–∞ —П–≤–ї—П–µ—В—Б—П –љ–µ—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Њ–є –Ј–∞—Й–Є—В–љ–Њ––њ—А–Є—Б–њ–Њ—Б–Њ–±–Є—В–µ–ї—М–љ–Њ–є —А–µ–∞–Ї—Ж–Є–µ–є –Њ—А–≥–∞–љ–Є–Ј–Љ–∞, —В–Њ –њ—А–Є—З–Є–љ—Л, –µ–µ –≤—Л–Ј—Л–≤–∞—О—Й–Є–µ, –≤–µ—Б—М–Љ–∞ —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–љ—Л. –Э–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –ї–Є—Е–Њ—А–∞–і–Ї–∞ –≤—Б—В—А–µ—З–∞–µ—В—Б—П –њ—А–Є –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –±–Њ–ї–µ–Ј–љ—П—Е, —Б—А–µ–і–Є –Ї–Њ—В–Њ—А—Л—Е –і–Њ–Љ–Є–љ–Є—А—Г—О—В –Њ—Б—В—А—Л–µ —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –≤–µ—А—Е–љ–Є—Е –Є –љ–Є–ґ–љ–Є—Е –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є. –Ы–Є—Е–Њ—А–∞–і–Ї–∞ –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–≥–Њ –≥–µ–љ–µ–Ј–∞ —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –≤ –Њ—В–≤–µ—В –љ–∞ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –≤–Є—А—Г—Б–Њ–≤, –±–∞–Ї—В–µ—А–Є–є –Є –њ—А–Њ–і—Г–Ї—В–Њ–≤ –Є—Е —А–∞—Б–њ–∞–і–∞. –Я–Њ–≤—Л—И–µ–љ–Є–µ —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л —В–µ–ї–∞ –љ–µ–Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–≥–Њ —Е–∞—А–∞–Ї—В–µ—А–∞ –Љ–Њ–ґ–µ—В –±—Л—В—М —А–∞–Ј–ї–Є—З–љ–Њ–≥–Њ –≥–µ–љ–µ–Ј–∞: —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–≥–Њ (–Ї—А–Њ–≤–Њ–Є–Ј–ї–Є—П–љ–Є–µ, –Њ–њ—Г—Е–Њ–ї—М, —В—А–∞–≤–Љ–∞, –Њ—В–µ–Ї –Љ–Њ–Ј–≥–∞), –њ—Б–Є—Е–Њ–≥–µ–љ–љ–Њ–≥–Њ (–љ–µ–≤—А–Њ–Ј, –њ—Б–Є—Е–Є—З–µ—Б–Ї–Є–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞, —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–µ –љ–∞–њ—А—П–ґ–µ–љ–Є–µ), —А–µ—Д–ї–µ–Ї—В–Њ—А–љ–Њ–≥–Њ (–±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ –њ—А–Є –Љ–Њ—З–µ–Ї–∞–Љ–µ–љ–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є), —Н–љ–і–Њ–Ї—А–Є–љ–љ–Њ–≥–Њ (–≥–Є–њ–µ—А—В–Є—А–µ–Њ–Ј, —Д–µ–Њ—Е—А–Њ–Љ–Њ—Ж–Є—В–Њ–Љ–∞), —А–µ–Ј–Њ—А–±—В–Є–≤–љ–Њ–≥–Њ (—Г—И–Є–±, –љ–µ–Ї—А–Њ–Ј, –∞—Б–µ–њ—В–Є—З–µ—Б–Ї–Њ–µ –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ, –≥–µ–Љ–Њ–ї–Є–Ј), –∞ —В–∞–Ї–ґ–µ –љ–∞ –≤–≤–µ–і–µ–љ–Є–µ –љ–µ–Ї–Њ—В–Њ—А—Л—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ (—Н—Д–µ–і—А–Є–љ–∞, –Ї—Б–∞–љ—В–Є–љ–Њ–≤—Л—Е –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л—Е, –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –Є –і—А.).
–Ъ–∞–ґ–і—Л–є –Є–Ј –≤–∞—А–Є–∞–љ—В–Њ–≤ –ї–Є—Е–Њ—А–∞–і–Ї–Є –Є–Љ–µ–µ—В –Ї–∞–Ї –Њ–±—Й–Є–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л —А–∞–Ј–≤–Є—В–Є—П, —В–∞–Ї –Є —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–µ —З–µ—А—В—Л [3,4]. –£—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –Є–љ—В–µ–≥—А–∞–ї—М–љ—Л–Љ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–Љ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ –ї–Є—Е–Њ—А–∞–і–Ї–Є —П–≤–ї—П–µ—В—Б—П —А–µ–∞–Ї—Ж–Є—П —Д–∞–≥–Њ—Ж–Є—В–Њ–≤ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –Ї—А–Њ–≤–Є –Є/–Є–ї–Є —В–Ї–∞–љ–µ–≤—Л—Е –Љ–∞–Ї—А–Њ—Д–∞–≥–Њ–≤ –љ–∞ –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Г—О –Є–љ–≤–∞–Ј–Є—О –Є–ї–Є –љ–µ–Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л–є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–є –њ—А–Њ—Ж–µ—Б—Б. –Я–µ—А–≤–Є—З–љ—Л–µ –њ–Є—А–Њ–≥–µ–љ—Л, –Ї–∞–Ї –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л–µ, —В–∞–Ї –Є –љ–µ–Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л–µ, —В–Њ–ї—М–Ї–Њ –Є–љ–Є—Ж–Є–Є—А—Г—О—В —А–∞–Ј–≤–Є—В–Є–µ –ї–Є—Е–Њ—А–∞–і–Ї–Є, —Б—В–Є–Љ—Г–ї–Є—А—Г—П –Ї–ї–µ—В–Ї–Є –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –Ї —Б–Є–љ—В–µ–Ј—Г –≤—В–Њ—А–Є—З–љ—Л—Е –Љ–µ–і–Є–∞—В–Њ—А–Њ–≤––њ–Є—А–Њ–≥–µ–љ–Њ–≤. –Ш—Б—В–Њ—З–љ–Є–Ї–Њ–Љ –≤—В–Њ—А–Є—З–љ—Л—Е –њ–Є—А–Њ–≥–µ–љ–Њ–≤ —Б—В–∞–љ–Њ–≤—П—В—Б—П –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –Ї–ї–µ—В–Ї–Є —Д–∞–≥–Њ—Ж–Є—В–Є—А—Г—О—Й–Є—Е –Љ–Њ–љ–Њ–љ—Г–Ї–ї–µ–∞—А–Њ–≤. –Т—В–Њ—А–Є—З–љ—Л–µ –њ–Є—А–Њ–≥–µ–љ—Л – –љ–µ–Њ–і–љ–Њ—А–Њ–і–љ–∞—П –≥—А—Г–њ–њ–∞ –њ—А–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤ (–Є–љ—В–µ—А–ї–µ–є–Ї–Є–љ—Л 1, 6, —Д–∞–Ї—В–Њ—А –љ–µ–Ї—А–Њ–Ј–∞ –Њ–њ—Г—Е–Њ–ї–Є –∞–ї—М—Д–∞ –Є –і—А.), –Њ–і–љ–∞–Ї–Њ –Њ—Б–љ–Њ–≤–љ—Г—О –Є–љ–Є—Ж–Є–Є—А—Г—О—Й—Г—О —А–Њ–ї—М –≤ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–µ –ї–Є—Е–Њ—А–∞–і–Ї–Є –Є–≥—А–∞–µ—В –Є–љ—В–µ—А–ї–µ–є–Ї–Є–љ–1 (–Ш–Ы–1).
–Ш–Ы–1 – –Њ—Б–љ–Њ–≤–љ–Њ–є –Љ–µ–і–Є–∞—В–Њ—А –Љ–µ–ґ–Ї–ї–µ—В–Њ—З–љ–Њ–≥–Њ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П –Њ—Б—В—А–Њ–є —Д–∞–Ј—Л –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П. –С–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Н—Д—Д–µ–Ї—В—Л –µ–≥–Њ —З—А–µ–Ј–≤—Л—З–∞–є–љ–Њ —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–љ—Л. –Я–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ –Ш–Ы–1 –Є–љ–Є—Ж–Є–Є—А—Г–µ—В—Б—П –∞–Ї—В–Є–≤–∞—Ж–Є—П –Є –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є—П –Ґ––ї–Є–Љ—Д–Њ—Ж–Є—В–Њ–≤, —Г—Б–Є–ї–Є–≤–∞–µ—В—Б—П –њ—А–Њ–і—Г–Ї—Ж–Є—П –Ш–Ы–2, –њ–Њ–≤—Л—И–∞–µ—В—Б—П —Н–Ї—Б–њ—А–µ—Б—Б–Є—П –Ї–ї–µ—В–Њ—З–љ—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤. –Ш–Ы–1 —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є–Є –Т––Ї–ї–µ—В–Њ–Ї –Є —Б–Є–љ—В–µ–Ј—Г –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ–Њ–≤, —Б—В–Є–Љ—Г–ї–Є—А—Г–µ—В —Б–Є–љ—В–µ–Ј –±–µ–ї–Ї–Њ–≤ –Њ—Б—В—А–Њ–є —Д–∞–Ј—Л –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П (–°–†–С, –Ї–Њ–Љ–њ–ї–µ–Љ–µ–љ—В–∞ –Є –і—А.), –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤ –Є –њ—А–µ–і—И–µ—Б—В–≤–µ–љ–љ–Є–Ї–Њ–≤ –≥–µ–Љ–Њ–њ–Њ—Н–Ј–∞ –≤ –Ї–Њ—Б—В–љ–Њ–Љ –Љ–Њ–Ј–≥–µ. –Ш–Ы–1 –Њ–±–ї–∞–і–∞–µ—В –њ—А—П–Љ—Л–Љ —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –љ–∞ –Ї–ї–µ—В–Ї–Є, –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л–µ –≤–Є—А—Г—Б–Њ–Љ.
–£—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –Ш–Ы–1 —П–≤–ї—П–µ—В—Б—П –Њ—Б–љ–Њ–≤–љ—Л–Љ –Љ–µ–і–Є–∞—В–Њ—А–Њ–Љ –≤ –Љ–µ—Е–∞–љ–Є–Ј–Љ–µ —А–∞–Ј–≤–Є—В–Є—П –ї–Є—Е–Њ—А–∞–і–Ї–Є –Є –±–ї–∞–≥–Њ–і–∞—А—П —Н—В–Њ–Љ—Г –≤ –ї–Є—В–µ—А–∞—В—Г—А–µ —З–∞—Б—В–Њ –Њ–±–Њ–Ј–љ–∞—З–∞–µ—В—Б—П, –Ї–∞–Ї —Н–љ–і–Њ–≥–µ–љ–љ—Л–є –Є–ї–Є –ї–µ–є–Ї–Њ—Ж–Є—В–∞—А–љ—Л–є –њ–Є—А–Њ–≥–µ–љ. –Т –љ–Њ—А–Љ–∞–ї—М–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е –Ш–Ы–1 –љ–µ –њ—А–Њ–љ–Є–Ї–∞–µ—В —З–µ—А–µ–Ј –≥–µ–Љ–∞—В–Њ—Н–љ—Ж–µ—Д–∞–ї–Є—З–µ—Б–Ї–Є–є –±–∞—А—М–µ—А. –Ю–і–љ–∞–Ї–Њ –њ—А–Є –љ–∞–ї–Є—З–Є–Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П (–Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–≥–Њ –Є–ї–Є –љ–µ–Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–≥–Њ) –Ш–Ы–1 –і–Њ—Б—В–Є–≥–∞–µ—В –њ—А–µ–Њ–њ—В–Є—З–µ—Б–Ї–Њ–є –Њ–±–ї–∞—Б—В–Є –њ–µ—А–µ–і–љ–µ–є —З–∞—Б—В–Є –≥–Є–њ–Њ—В–∞–ї–∞–Љ—Г—Б–∞ –Є –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤—Г–µ—В —Б —А–µ—Ж–µ–њ—В–Њ—А–∞–Љ–Є –љ–µ–є—А–Њ–љ–Њ–≤ —Ж–µ–љ—В—А–∞ —В–µ—А–Љ–Њ—А–µ–≥—Г–ї—П—Ж–Є–Є. –Я—А–Є —Н—В–Њ–Љ –∞–Ї—В–Є–≤–Є–Ј–Є—А—Г–µ—В—Б—П —Ж–Є–Ї–ї–Њ–Њ–Ї—Б–Є–≥–µ–љ–∞–Ј–∞ (–¶–Ю–У), —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О —Б–Є–љ—В–µ–Ј–∞ –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–∞ –Х1 –Є –њ–Њ–≤—Л—И–µ–љ–Є—О –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П —Ж–Є–Ї–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –∞–і–µ–љ–Њ–Ј–Є–љ–3,5––Љ–Њ–љ–Њ—Д–Њ—Б—Д–∞—В–∞ (—Ж–Р–Ь–§). –£–≤–µ–ї–Є—З–µ–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є —Ж–Р–Ь–§ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ–Њ–Љ—Г –љ–∞–Ї–Њ–њ–ї–µ–љ–Є—О –Є–Њ–љ–Њ–≤ –Ї–∞–ї—М—Ж–Є—П, –Є–Ј–Љ–µ–љ–µ–љ–Є—О —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є–є Na/Ca –Є –њ–µ—А–µ—Б—В—А–Њ–є–Ї–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Ж–µ–љ—В—А–Њ–≤ —В–µ–њ–ї–Њ–њ—А–Њ–і—Г–Ї—Ж–Є–Є –Є —В–µ–њ–ї–Њ–Њ—В–і–∞—З–Є. –£—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–µ—В—Б—П –љ–Њ–≤—Л–є —Г—А–Њ–≤–µ–љ—М —В–µ–Љ–њ–µ—А–∞—В—Г—А–љ–Њ–≥–Њ –≥–Њ–Љ–µ–Њ—Б—В–∞–Ј–∞ – –љ–∞ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Њ–є —В–Њ—З–Ї–µ, –њ–Њ–≤—Л—И–∞–µ—В—Б—П —В–µ–њ–ї–Њ–њ—А–Њ–і—Г–Ї—Ж–Є—П, —Б–љ–Є–ґ–∞–µ—В—Б—П —В–µ–њ–ї–Њ–Њ—В–і–∞—З–∞ (—А–Є—Б. 2). –Я–Њ–≤—Л—И–µ–љ–Є–µ —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л —В–µ–ї–∞ –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П –Ј–∞ —Б—З–µ—В –Є–Ј–Љ–µ–љ–µ–љ–Є—П –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤, —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —В–Њ–љ—Г—Б–∞, –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞, –њ–Њ—В–Њ–Њ—В–і–µ–ї–µ–љ–Є—П, —Б–Є–љ—В–µ–Ј–∞ –≥–Њ—А–Љ–Њ–љ–Њ–≤ –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л –Є –љ–∞–і–њ–Њ—З–µ—З–љ–Є–Ї–Њ–≤, —Б–Њ–Ї—А–∞—В–Є—В–µ–ї—М–љ–Њ–≥–Њ —В–µ—А–Љ–Њ–≥–µ–љ–µ–Ј–∞ (–Љ—Л—И–µ—З–љ–Њ–µ –і—А–Њ–ґ–∞–љ–Є–µ) –Є –і—А—Г–≥–Є—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ [1,3].
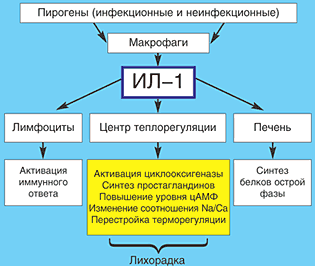
–†–Є—Б. 2. –Я–∞—В–Њ–≥–µ–љ–µ–Ј –ї–Є—Е–Њ—А–∞–і–Ї–Є
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –Ї–∞—А—В–Є–љ–∞–Ы–Є—Е–Њ—А–∞–і–Њ—З–љ—Л–є –њ—А–Њ—Ж–µ—Б—Б –Њ–±—Л—З–љ–Њ –њ—А–Њ—В–µ–Ї–∞–µ—В –≤ —В—А–Є —Б—В–∞–і–Є–Є. –Т –њ–µ—А–≤–Њ–є —Б—В–∞–і–Є–Є —В–µ–Љ–њ–µ—А–∞—В—Г—А–∞ –њ–Њ–≤—Л—И–∞–µ—В—Б—П –Ј–∞ —Б—З–µ—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є—П —В–µ–њ–ї–Њ–њ—А–Њ–і—Г–Ї—Ж–Є–Є –љ–∞–і —В–µ–њ–ї–Њ–Њ—В–і–∞—З–µ–є. –Т–Њ –≤—В–Њ—А–Њ–є – —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П —В–µ–њ–ї–Њ–Њ—В–і–∞—З–∞, –і–∞–ї—М–љ–µ–є—И–µ–≥–Њ –Є–Ј–Љ–µ–љ–µ–љ–Є—П —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л –≤ —В–µ—З–µ–љ–Є–µ –љ–µ–Ї–Њ—В–Њ—А–Њ–≥–Њ –≤—А–µ–Љ–µ–љ–Є (–і–љ–Є, —З–∞—Б—Л) –љ–µ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В. –Т —В—А–µ—В—М–µ–є, –њ–Њ—Б–ї–µ –њ—А–µ–Ї—А–∞—Й–µ–љ–Є—П –і–µ–є—Б—В–≤–Є—П –њ–Є—А–Њ–≥–µ–љ–Њ–≤, «—Г—Б—В–∞–љ–Њ–≤–Њ—З–љ–∞—П —В–Њ—З–Ї–∞» —Ж–µ–љ—В—А–∞ —В–µ—А–Љ–Њ—А–µ–≥—Г–ї—П—Ж–Є–Є –Њ–њ—Г—Б–Ї–∞–µ—В—Б—П –і–Њ –љ–Њ—А–Љ–∞–ї—М–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П. –Ґ–µ–њ–ї–Њ–Њ—В–і–∞—З–∞ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П –Ј–∞ —Б—З–µ—В —А–∞—Б—И–Є—А–µ–љ–Є—П –Ї–Њ–ґ–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤, –Њ–±–Є–ї—М–љ–Њ–≥–Њ –њ–Њ—В–Њ–Њ—В–і–µ–ї–µ–љ–Є—П, —З–∞—Б—В–Њ–≥–Њ –і—Л—Е–∞–љ–Є—П. –°–љ–Є–ґ–µ–љ–Є–µ —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л –Љ–Њ–ґ–µ—В –±—Л—В—М –њ–Њ—Б—В–µ–њ–µ–љ–љ—Л–Љ (–ї–Є—В–Є—З–µ—Б–Ї–Є–Љ) –Є–ї–Є –±—Л—Б—В—А—Л–Љ (–Ї—А–Є—В–Є—З–µ—Б–Ї–Є–Љ). –Х—Б–ї–Є –Ї—А–Є—В–Є—З–µ—Б–Ї–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–µ–µ—Б—П —А–µ–Ј–Ї–Є–Љ —А–∞—Б—И–Є—А–µ–љ–Є–µ–Љ —Б–Њ—Б—Г–і–Њ–≤, —Б–Њ—З–µ—В–∞–µ—В—Б—П —Б –Є–љ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–µ–є, —В–Њ –Љ–Њ–ґ–µ—В –≤–Њ–Ј–љ–Є–Ї–љ—Г—В—М –Њ–њ–∞—Б–љ—Л–є –і–ї—П –ґ–Є–Ј–љ–Є —А–µ–±–µ–љ–Ї–∞ –Ї–Њ–ї–ї–∞–њ—Б. –Э–∞–і–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Є–Ј––Ј–∞ —И–Є—А–Њ–Ї–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –љ–∞ —А–∞–љ–љ–Є—Е —Б—В–∞–і–Є—П—Е –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л—Е —Н—В–Є–Њ—В—А–Њ–њ–љ—Л—Е (–∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е) –Є –ґ–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–Є—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤ —В–Є–њ–Є—З–љ—Л–µ, –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л–µ —В–µ–Љ–њ–µ—А–∞—В—Г—А–љ—Л–µ –Ї—А–Є–≤—Л–µ –љ–∞ –њ—А–∞–Ї—В–Є–Ї–µ –њ—А–Є—Е–Њ–і–Є—В—Б—П –≤–Є–і–µ—В—М —А–µ–і–Ї–Њ.
–Т –њ–µ—А–≤–Њ–є —Б—В–∞–і–Є–Є —В–µ–Љ–њ–µ—А–∞—В—Г—А–∞ –њ–Њ–≤—Л—И–∞–µ—В—Б—П –Ј–∞ —Б—З–µ—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є—П —В–µ–њ–ї–Њ–њ—А–Њ–і—Г–Ї—Ж–Є–Є –љ–∞–і —В–µ–њ–ї–Њ–Њ—В–і–∞—З–µ–є. –Т–Њ –≤—В–Њ—А–Њ–є – —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П —В–µ–њ–ї–Њ–Њ—В–і–∞—З–∞, –і–∞–ї—М–љ–µ–є—И–µ–≥–Њ –Є–Ј–Љ–µ–љ–µ–љ–Є—П —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л –≤ —В–µ—З–µ–љ–Є–µ –љ–µ–Ї–Њ—В–Њ—А–Њ–≥–Њ –≤—А–µ–Љ–µ–љ–Є (–і–љ–Є, —З–∞—Б—Л) –љ–µ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В. –Т —В—А–µ—В—М–µ–є, –њ–Њ—Б–ї–µ –њ—А–µ–Ї—А–∞—Й–µ–љ–Є—П –і–µ–є—Б—В–≤–Є—П –њ–Є—А–Њ–≥–µ–љ–Њ–≤, «—Г—Б—В–∞–љ–Њ–≤–Њ—З–љ–∞—П —В–Њ—З–Ї–∞» —Ж–µ–љ—В—А–∞ —В–µ—А–Љ–Њ—А–µ–≥—Г–ї—П—Ж–Є–Є –Њ–њ—Г—Б–Ї–∞–µ—В—Б—П –і–Њ –љ–Њ—А–Љ–∞–ї—М–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П. –Ґ–µ–њ–ї–Њ–Њ—В–і–∞—З–∞ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П –Ј–∞ —Б—З–µ—В —А–∞—Б—И–Є—А–µ–љ–Є—П –Ї–Њ–ґ–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤, –Њ–±–Є–ї—М–љ–Њ–≥–Њ –њ–Њ—В–Њ–Њ—В–і–µ–ї–µ–љ–Є—П, —З–∞—Б—В–Њ–≥–Њ –і—Л—Е–∞–љ–Є—П. –°–љ–Є–ґ–µ–љ–Є–µ —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л –Љ–Њ–ґ–µ—В –±—Л—В—М –њ–Њ—Б—В–µ–њ–µ–љ–љ—Л–Љ (–ї–Є—В–Є—З–µ—Б–Ї–Є–Љ) –Є–ї–Є –±—Л—Б—В—А—Л–Љ (–Ї—А–Є—В–Є—З–µ—Б–Ї–Є–Љ). –Х—Б–ї–Є –Ї—А–Є—В–Є—З–µ—Б–Ї–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–µ–µ—Б—П —А–µ–Ј–Ї–Є–Љ —А–∞—Б—И–Є—А–µ–љ–Є–µ–Љ —Б–Њ—Б—Г–і–Њ–≤, —Б–Њ—З–µ—В–∞–µ—В—Б—П —Б –Є–љ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–µ–є, —В–Њ –Љ–Њ–ґ–µ—В –≤–Њ–Ј–љ–Є–Ї–љ—Г—В—М –Њ–њ–∞—Б–љ—Л–є –і–ї—П –ґ–Є–Ј–љ–Є —А–µ–±–µ–љ–Ї–∞ –Ї–Њ–ї–ї–∞–њ—Б. –Э–∞–і–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Є–Ј––Ј–∞ —И–Є—А–Њ–Ї–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –љ–∞ —А–∞–љ–љ–Є—Е —Б—В–∞–і–Є—П—Е –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л—Е —Н—В–Є–Њ—В—А–Њ–њ–љ—Л—Е (–∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е) –Є –ґ–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–Є—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤ —В–Є–њ–Є—З–љ—Л–µ, –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л–µ —В–µ–Љ–њ–µ—А–∞—В—Г—А–љ—Л–µ –Ї—А–Є–≤—Л–µ –љ–∞ –њ—А–∞–Ї—В–Є–Ї–µ –њ—А–Є—Е–Њ–і–Є—В—Б—П –≤–Є–і–µ—В—М —А–µ–і–Ї–Њ.–Ю—Б–Њ–±–Њ —Б–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –њ—А–Є –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–Љ —Г—А–Њ–≤–љ–µ –≥–Є–њ–µ—А—В–µ—А–Љ–Є–Є –ї–Є—Е–Њ—А–∞–і–Ї–∞ —Г –і–µ—В–µ–є –Љ–Њ–ґ–µ—В –њ—А–Њ—В–µ–Ї–∞—В—М –њ–Њ–—А–∞–Ј–љ–Њ–Љ—Г. –Ґ–∞–Ї, –µ—Б–ї–Є —В–µ–њ–ї–Њ–Њ—В–і–∞—З–∞ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В —В–µ–њ–ї–Њ–њ—А–Њ–і—Г–Ї—Ж–Є–Є, —Н—В–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ–± –∞–і–µ–Ї–≤–∞—В–љ–Њ–Љ —В–µ—З–µ–љ–Є–Є –ї–Є—Е–Њ—А–∞–і–Ї–Є –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –њ—А–Њ—П–≤–ї—П–µ—В—Б—П –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –љ–Њ—А–Љ–∞–ї—М–љ—Л–Љ —Б–∞–Љ–Њ—З—Г–≤—Б—В–≤–Є–µ–Љ —А–µ–±–µ–љ–Ї–∞, —А–Њ–Ј–Њ–≤–Њ–є –Є–ї–Є —Г–Љ–µ—А–µ–љ–љ–Њ –≥–Є–њ–µ—А–µ–Љ–Є—А–Њ–≤–∞–љ–љ–Њ–є –Њ–Ї—А–∞—Б–Ї–Њ–є –Ї–Њ–ґ–Є, –≤–ї–∞–ґ–љ–Њ–є –Є —В–µ–њ–ї–Њ–є –љ–∞ –Њ—Й—Г–њ—М («—А–Њ–Ј–Њ–≤–∞—П –ї–Є—Е–Њ—А–∞–і–Ї–∞»). –≠—В–Њ—В —В–Є–њ –ї–Є—Е–Њ—А–∞–і–Ї–Є —З–∞—Б—В–Њ –љ–µ —В—А–µ–±—Г–µ—В –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –ґ–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–Є—Е —Б—А–µ–і—Б—В–≤.
–Т —Б–ї—Г—З–∞–µ, –Ї–Њ–≥–і–∞ –њ—А–Є –њ–Њ–≤—Л—И–µ–љ–љ–Њ–є —В–µ–њ–ї–Њ–њ—А–Њ–і—Г–Ї—Ж–Є–Є —В–µ–њ–ї–Њ–Њ—В–і–∞—З–∞ –љ–µ–∞–і–µ–Ї–≤–∞—В–љ–∞ –Є–Ј––Ј–∞ –љ–∞—А—Г—И–µ–љ–Є—П –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П, —В–µ—З–µ–љ–Є–µ –ї–Є—Е–Њ—А–∞–і–Ї–Є –њ—А–Њ–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є –њ—А–Є —Н—В–Њ–Љ –Њ—В–Љ–µ—З–∞—О—В—Б—П –≤—Л—А–∞–ґ–µ–љ–љ—Л–є –Њ–Ј–љ–Њ–±, –±–ї–µ–і–љ–Њ—Б—В—М –Ї–Њ–ґ–љ—Л—Е –њ–Њ–Ї—А–Њ–≤–Њ–≤, –∞–Ї—А–Њ—Ж–Є–∞–љ–Њ–Ј, —Е–Њ–ї–Њ–і–љ—Л–µ —Б—В–Њ–њ—Л –Є –ї–∞–і–Њ–љ–Є («–±–ї–µ–і–љ–∞—П –ї–Є—Е–Њ—А–∞–і–Ї–∞»). –≠—В–Є –і–µ—В–Є, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –љ—Г–ґ–і–∞—О—В—Б—П –≤ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –ґ–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б —Б–Њ—Б—Г–і–Њ—А–∞—Б—И–Є—А—П—О—Й–Є–Љ–Є –Є –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л–Љ–Є —Б—А–µ–і—Б—В–≤–∞–Љ–Є (–Є–ї–Є –љ–µ–є—А–Њ–ї–µ–њ—В–Є–Ї–∞–Љ–Є).
–Ю–і–љ–Є–Љ –Є–Ј –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –≤–∞—А–Є–∞–љ—В–Њ–≤ –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–≥–Њ —В–µ—З–µ–љ–Є—П –ї–Є—Е–Њ—А–∞–і–Ї–Є —П–≤–ї—П–µ—В—Б—П –≥–Є–њ–µ—А—В–µ—А–Љ–Є—З–µ—Б–Ї–Њ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ —Г –і–µ—В–µ–є —А–∞–љ–љ–µ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞, –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ–Њ–µ –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л–Љ –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ–Љ, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–Є–Љ—Б—П —В–Њ–Ї—Б–Є–Ї–Њ–Ј–Њ–Љ. –Я—А–Є —Н—В–Њ–Љ –Њ—В–Љ–µ—З–∞–µ—В—Б—П —Б—В–Њ–є–Ї–Њ–µ (6 –Є –±–Њ–ї–µ–µ —З–∞—Б–Њ–≤) –Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ (–≤—Л—И–µ 40°–°) –њ–Њ–≤—Л—И–µ–љ–Є–µ —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л —В–µ–ї–∞, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–µ–µ—Б—П –љ–∞—А—Г—И–µ–љ–Є–µ–Љ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є, –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–Љ–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є –Є –њ—А–Њ–≥—А–µ—Б—Б–Є–≤–љ–Њ –љ–∞—А–∞—Б—В–∞—О—Й–µ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–µ–є –ґ–Є–Ј–љ–µ–љ–љ–Њ –≤–∞–ґ–љ—Л—Е –Њ—А–≥–∞–љ–Њ–≤ –Є —Б–Є—Б—В–µ–Љ [3,6]. –†–∞–Ј–≤–Є—В–Є–µ –ї–Є—Е–Њ—А–∞–і–Ї–Є –љ–∞ —Д–Њ–љ–µ –Њ—Б—В—А—Л—Е –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ—Л—Е –Њ–±–Љ–µ–љ–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є, –ї–µ–ґ–∞—Й–Є—Е –≤ –Њ—Б–љ–Њ–≤–µ —В–Њ–Ї—Б–Є–Ї–Њ–Ј–∞, –њ—А–Є–≤–Њ–і–Є—В –Ї –і–µ–Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є–Є —В–µ—А–Љ–Њ—А–µ–≥—Г–ї—П—Ж–Є–Є —Б —А–µ–Ј–Ї–Є–Љ –љ–∞—А–∞—Б—В–∞–љ–Є–µ–Љ —В–µ–њ–ї–Њ–њ—А–Њ–і—Г–Ї—Ж–Є–Є, –љ–µ–∞–і–µ–Ї–≤–∞—В–љ–Њ —Б–љ–Є–ґ–µ–љ–љ–Њ–є —В–µ–њ–ї–Њ–Њ—В–і–∞—З–µ–є. –Т—Б–µ —Н—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –≤—Л—Б–Њ–Ї–Є–Љ —А–Є—Б–Ї–Њ–Љ —А–∞–Ј–≤–Є—В–Є—П –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є –Є –Њ—В–µ–Ї–∞ –Љ–Њ–Ј–≥–∞, —З—В–Њ —В—А–µ–±—Г–µ—В —Б—А–Њ—З–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є –љ–µ–Њ—В–ї–Њ–ґ–љ–Њ–є —В–µ—А–∞–њ–Є–Є. –Я–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ –≤–≤–Њ–і–Є—В—Б—П –ґ–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–Є–є –њ—А–µ–њ–∞—А–∞—В, –њ—А–Њ–≤–Њ–і–Є—В—Б—П –ї–µ—З–µ–љ–Є–µ —В–Њ–Ї—Б–Є–Ї–Њ–Ј–∞, –њ—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є – –њ—А–Њ—В–Є–≤–Њ—Б—Г–і–Њ—А–Њ–ґ–љ–∞—П —В–µ—А–∞–њ–Є—П (–і–Є–∞–Ј–µ–њ–∞–Љ, –Њ–Ї—Б–Є–±—Г—В–Є—А–∞—В –љ–∞—В—А–Є—П).
–Я—А–Є–љ—Ж–Є–њ—Л –ї–µ—З–µ–љ–Є—П
–Т —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –†–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ–Є –Т–Ю–Ч «–Ы–µ—З–µ–љ–Є–µ –ї–Є—Е–Њ—А–∞–і–Ї–Є –њ—А–Є –Њ—Б—В—А—Л—Е —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є—П—Е —Г –і–µ—В–µ–є» (WHO, 1993) [18] –Є –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ—Л–Љ–Є —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ–Є [6] –ґ–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–Є–µ –њ—А–µ–њ–∞—А–∞—В—Л —Б–ї–µ–і—Г–µ—В –љ–∞–Ј–љ–∞—З–∞—В—М, –Ї–Њ–≥–і–∞ —В–µ–Љ–њ–µ—А–∞—В—Г—А–∞ —Г —А–µ–±–µ–љ–Ї–∞, –Є–Ј–Љ–µ—А–µ–љ–љ–∞—П —А–µ–Ї—В–∞–ї—М–љ–Њ, –њ—А–µ–≤—Л—И–∞–µ—В 39°–°. –Ш—Б–Ї–ї—О—З–µ–љ–Є–µ —Б–Њ—Б—В–∞–≤–ї—П—О—В –і–µ—В–Є —Б —А–Є—Б–Ї–Њ–Љ —А–∞–Ј–≤–Є—В–Є—П —Д–µ–±—А–Є–ї—М–љ—Л—Е —Б—Г–і–Њ—А–Њ–≥, –і–µ—В–Є —Б —В—П–ґ–µ–ї—Л–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ–Љ –ї–µ–≥–Њ—З–љ–Њ–є –Є–ї–Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л –Є –і–µ—В–Є –њ–µ—А–≤—Л—Е 2 –Љ–µ—Б—П—Ж–µ–≤ –ґ–Є–Ј–љ–Є. –Т –љ–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є –љ–∞—Г—З–љ–Њ––њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–є –њ—А–Њ–≥—А–∞–Љ–Љ–µ «–Ю—Б—В—А—Л–µ —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Г –і–µ—В–µ–є: –ї–µ—З–µ–љ–Є–µ –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞» (2002) –ґ–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–Є–µ —Б—А–µ–і—Б—В–≤–∞ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –і–∞–≤–∞—В—М –≤ —Б–ї–µ–і—Г—О—Й–Є—Е —Б–ї—Г—З–∞—П—Е:
1. –†–∞–љ–µ–µ –Ј–і–Њ—А–Њ–≤—Л–Љ –і–µ—В—П–Љ – –њ—А–Є —В–µ–Љ–њ–µ—А–∞—В—Г—А–µ —В–µ–ї–∞ –≤—Л—И–µ 39°–° –Є/–Є–ї–Є –њ—А–Є –Љ—Л—И–µ—З–љ–Њ–є –ї–Њ–Љ–Њ—В–µ –Є –≥–Њ–ї–Њ–≤–љ–Њ–є –±–Њ–ї–Є.
2. –Ф–µ—В—П–Љ —Б —Д–µ–±—А–Є–ї—М–љ—Л–Љ–Є —Б—Г–і–Њ—А–Њ–≥–∞–Љ–Є –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ – –њ—А–Є —В–µ–Љ–њ–µ—А–∞—В—Г—А–µ —В–µ–ї–∞ –≤—Л—И–µ 38–38,5°–°.
3. –Ф–µ—В—П–Љ —Б —В—П–ґ–µ–ї—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є —Б–µ—А–і—Ж–∞ –Є –ї–µ–≥–Ї–Є—Е – –њ—А–Є —В–µ–Љ–њ–µ—А–∞—В—Г—А–µ —В–µ–ї–∞ –≤—Л—И–µ 38,5°–°.
4. –Ф–µ—В—П–Љ –њ–µ—А–≤—Л—Е 3 –Љ–µ—Б—П—Ж–µ–≤ –ґ–Є–Ј–љ–Є – –њ—А–Є —В–µ–Љ–њ–µ—А–∞—В—Г—А–µ —В–µ–ї–∞ –≤—Л—И–µ 38°–°.
–£ —А–µ–±–µ–љ–Ї–∞ —Б –љ–µ–Њ—В—П–≥–Њ—Й–µ–љ–љ—Л–Љ –њ—А–µ–Љ–Њ—А–±–Є–і–љ—Л–Љ —Д–Њ–љ–Њ–Љ —В–µ–Љ–њ–µ—А–∞—В—Г—А–љ–∞—П —А–µ–∞–Ї—Ж–Є—П, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –Є–Љ–µ–µ—В –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А («—А–Њ–Ј–Њ–≤–∞—П –ї–Є—Е–Њ—А–∞–і–Ї–∞»), –љ–µ –њ—А–µ–≤—Л—И–∞–µ—В 39°–°, –Є –Њ—В –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤ –Љ–Њ–ґ–љ–Њ –≤–Њ–Ј–і–µ—А–ґ–∞—В—М—Б—П. –Т —Н—В–Є—Е —Б–ї—Г—З–∞—П—Е –њ–Њ–Ї–∞–Ј–∞–љ—Л –Њ–±–Є–ї—М–љ–Њ–µ –њ–Є—В—М–µ, –Љ–Њ–≥—Г—В –±—Л—В—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ—Л —Д–Є–Ј–Є—З–µ—Б–Ї–Є–µ –Љ–µ—В–Њ–і—Л –Њ—Е–ї–∞–ґ–і–µ–љ–Є—П (—А–µ–±–µ–љ–Ї–∞ —Б–ї–µ–і—Г–µ—В —А–∞—Б–Ї—А—Л—В—М –Є –Њ–±—В–µ—А–µ—В—М –≤–Њ–і–Њ–є –Ї–Њ–Љ–љ–∞—В–љ–Њ–є —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л, –Њ–і–µ–ґ–і–∞ –і–Њ–ї–ґ–љ–∞ –±—Л—В—М —Б–≤–Њ–±–Њ–і–љ–Њ–є, –ї–µ–≥–Ї–Њ–є, —В–µ–Љ–њ–µ—А–∞—В—Г—А–∞ –≤ –Ї–Њ–Љ–љ–∞—В–µ –љ–µ –±–Њ–ї–µ–µ 20°–°, –≤–Њ–Ј–Љ–Њ–ґ–љ–∞ –ї–µ—З–µ–±–љ–∞—П –≤–∞–љ–љ–∞ —Б —В–µ–Љ–њ–µ—А–∞—В—Г—А–Њ–є –љ–∞ 2°–° –љ–Є–ґ–µ —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л —В–µ–ї–∞).
–Ю—Б–љ–Њ–≤—Г —В–µ—А–∞–њ–Є–Є —Б–Њ—Б—В–∞–≤–ї—П–µ—В —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –ї–µ—З–µ–љ–Є–µ –Њ—Б–љ–Њ–≤–љ–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –ґ–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–∞—П —В–µ—А–∞–њ–Є—П –љ–Њ—Б–Є—В —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–є —Е–∞—А–∞–Ї—В–µ—А, –∞ —Г –і–µ—В–µ–є —Б –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є (–∞—В–Њ–њ–Є—З–µ—Б–Ї–Є–є –і–µ—А–Љ–∞—В–Є—В, –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є–є —А–Є–љ–Є—В) –Љ–Њ–ґ–µ—В —Б–Њ—З–µ—В–∞—В—М—Б—П —Б –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л–Љ–Є —Б—А–µ–і—Б—В–≤–∞–Љ–Є.
–Ц–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–Є–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞ (–∞–љ–∞–ї—М–≥–µ—В–Є–Ї–Є––∞–љ—В–Є–њ–Є—А–µ—В–Є–Ї–Є) –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –≤ –Љ–µ–і–Є—Ж–Є–љ–µ –±–Њ–ї–µ–µ 200 –ї–µ—В. –Ґ–∞–Ї, –≤ 1763 –≥–Њ–і—Г –±—Л–ї–Њ —Б–і–µ–ї–∞–љ–Њ –њ–µ—А–≤–Њ–µ –љ–∞—Г—З–љ–Њ–µ —Б–Њ–Њ–±—Й–µ–љ–Є–µ –Њ –ґ–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–µ–Љ –і–µ–є—Б—В–≤–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞, –њ–Њ–ї—Г—З–µ–љ–љ–Њ–≥–Њ –Є–Ј –Є–≤–Њ–≤–Њ–є –Ї–Њ—А—Л (Stone R.E.). –Я–Њ–Ј–ґ–µ –±—Л–ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –∞–Ї—В–Є–≤–љ—Л–Љ –љ–∞—З–∞–ї–Њ–Љ —Н—В–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ —П–≤–ї—П–µ—В—Б—П —Б–∞–ї–Є—Ж–Є–љ. –Я–Њ—Б—В–µ–њ–µ–љ–љ–Њ —Б–Є–љ—В–µ—В–Є—З–µ—Б–Ї–Є–µ –∞–љ–∞–ї–Њ–≥–Є —Б–∞–ї–Є—Ж–Є–љ–∞ (—Б–∞–ї–Є—Ж–Є–ї–∞—В –љ–∞—В—А–Є—П –Є –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞) –њ–Њ–ї–љ–Њ—Б—В—М—О –Ј–∞–Љ–µ–љ–Є–ї–Є –≤ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –њ—А–Є—А–Њ–і–љ—Л–µ —Б–Њ–µ–і–Є–љ–µ–љ–Є—П. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —Б–Њ–Ј–і–∞–љ–Њ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –≥—А—Г–њ–њ –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–Њ–≤––∞–љ—В–Є–њ–Є—А–µ—В–Є–Ї–Њ–≤, –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –Є–Ј –Ї–Њ—В–Њ—А—Л—Е –Њ—В–љ–Њ—Б—П—В—Б—П –Ї –≥—А—Г–њ–њ–µ –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л—Е –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ (–Э–Я–Т–Я).
–Т –Њ—Б–љ–Њ–≤–µ –ґ–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–µ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–Њ–≤––∞–љ—В–Є–њ–Є—А–µ—В–Є–Ї–Њ–≤ –ї–µ–ґ–∞—В –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л —Г–≥–љ–µ—В–µ–љ–Є—П —Б–Є–љ—В–µ–Ј–∞ –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤ –Ј–∞ —Б—З–µ—В —Б–љ–Є–ґ–µ–љ–Є—П –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Ж–Є–Ї–ї–Њ–Њ–Ї—Б–Є–≥–µ–љ–∞–Ј—Л (–¶–Ю–У). –£—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ —Б—Г—Й–µ—Б—В–≤—Г–µ—В 2 –Є–Ј–Њ—Д–µ—А–Љ–µ–љ—В–∞ –¶–Ю–У. –¶–Ю–У–1 –љ–∞–њ—А–∞–≤–ї—П–µ—В –њ—А–Њ—Ж–µ—Б—Б—Л –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –∞—А–∞—Е–Є–і–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –љ–∞ –Њ—Б—Г—Й–µ—Б—В–≤–ї–µ–љ–Є–µ —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Д—Г–љ–Ї—Ж–Є–є: –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤, –Њ–Ї–∞–Ј—Л–≤–∞—О—Й–Є—Е —Ж–Є—В–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –љ–∞ —Б–ї–Є–Ј–Є—Б—В—Г—О –ґ–µ–ї—Г–і–Ї–∞, –љ–∞ —А–µ–≥—Г–ї—П—Ж–Є—О —Д—Г–љ–Ї—Ж–Є–Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤, –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –Є –і—А. –¶–Ю–У–2 –Њ–±—А–∞–Ј—Г–µ—В—Б—П —В–Њ–ї—М–Ї–Њ –њ—А–Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–Њ—Ж–µ—Б—Б–∞—Е –њ–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤. –Я—А–Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є–Є –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ –∞—А–∞—Е–Є–і–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –∞–Ї—В–Є–≤–Є–Ј–Є—А—Г–µ—В—Б—П, –њ–Њ–≤—Л—И–∞–µ—В—Б—П —Б–Є–љ—В–µ–Ј –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤, –ї–µ–є–Ї–Њ—В—А–Є–µ–љ–Њ–≤, –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є–µ –±–Є–Њ–≥–µ–љ–љ—Л—Е –∞–Љ–Є–љ–Њ–≤, —Б–≤–Њ–±–Њ–і–љ—Л—Е —А–∞–і–Є–Ї–∞–ї–Њ–≤, NO –Є –і—А., —З—В–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞–µ—В —А–∞–Ј–≤–Є—В–Є–µ —А–∞–љ–љ–µ–є —Б—В–∞–і–Є–Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П. –С–ї–Њ–Ї–∞–і–∞ –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–∞–Љ–Є––∞–љ—В–Є–њ–Є—А–µ—В–Є–Ї–∞–Љ–Є –¶–Ю–У –≤ –¶–Э–° –њ—А–Є–≤–Њ–і–Є—В –Ї –ґ–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–µ–Љ—Г –Є –∞–љ–∞–ї—М–≥–µ–Ј–Є—А—Г—О—Й–µ–Љ—Г —Н—Д—Д–µ–Ї—В—Г (—Ж–µ–љ—В—А–∞–ї—М–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ), –∞ —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤ –≤ –Љ–µ—Б—В–µ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П – –Ї –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–Љ—Г –і–µ–є—Б—В–≤–Є—О –Є –Ј–∞ —Б—З–µ—В —Г–Љ–µ–љ—М—И–µ–љ–Є—П –±–Њ–ї–µ–≤–Њ–є —А–µ—Ж–µ–њ—Ж–Є–Є – –Ї –Њ–±–µ–Ј–±–Њ–ї–Є–≤–∞–љ–Є—О (–њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ) [1,2,3].
–Я—А–Є –≤—Л–±–Њ—А–µ –ґ–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–Є—Е —Б—А–µ–і—Б—В–≤ –і–ї—П –і–µ—В–µ–є –Њ—Б–Њ–±–µ–љ–љ–Њ –≤–∞–ґ–љ–Њ –Њ—А–Є–µ–љ—В–Є—А–Њ–≤–∞—В—М—Б—П –љ–∞ –њ—А–µ–њ–∞—А–∞—В—Л —Б –љ–∞–Є–Љ–µ–љ—М—И–Є–Љ —А–Є—Б–Ї–Њ–Љ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —В–Њ–ї—М–Ї–Њ –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї –Є –Є–±—Г–њ—А–Њ—Д–µ–љ –њ–Њ–ї–љ–Њ—Б—В—М—О –Њ—В–≤–µ—З–∞—О—В –Ї—А–Є—В–µ—А–Є—П–Љ –≤—Л—Б–Њ–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є. –Ю–љ–Є –Њ—Д–Є—Ж–Є–∞–ї—М–љ–Њ —А–µ–Ї–Њ–Љ–µ–љ–і—Г—О—В—Б—П –Т—Б–µ–Љ–Є—А–љ–Њ–є –Ю—А–≥–∞–љ–Є–Ј–∞—Ж–Є–µ–є –Ч–і—А–∞–≤–Њ–Њ—Е—А–∞–љ–µ–љ–Є—П –Є –љ–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ–Є –њ—А–Њ–≥—А–∞–Љ–Љ–∞–Љ–Є –≤ –Ї–∞—З–µ—Б—В–≤–µ –ґ–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–Є—Е —Б—А–µ–і—Б—В–≤ –≤ –њ–µ–і–Є–∞—В—А–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ [1,3,6,18]. –Я–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї –Є –Є–±—Г–њ—А–Њ—Д–µ–љ –Љ–Њ–≥—Г—В –љ–∞–Ј–љ–∞—З–∞—В—М—Б—П –і–µ—В—П–Љ —Б –њ–µ—А–≤—Л—Е –Љ–µ—Б—П—Ж–µ–≤ –ґ–Є–Ј–љ–Є (—Б 3–—Е––Љ–µ—Б—П—З–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞). –†–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–љ—Л–µ —А–∞–Ј–Њ–≤—Л–µ –і–Њ–Ј—Л: –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–∞ 10–15 –Љ–≥/–Ї–≥, –Є–±—Г–њ—А–Њ—Д–µ–љ–∞ – 5–10 –Љ–≥/–Ї–≥. –Я–Њ–≤—В–Њ—А–љ–Њ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –∞–љ—В–Є–њ–Є—А–µ—В–Є–Ї–Њ–≤ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –љ–µ —А–∞–љ–µ–µ, —З–µ–Љ —З–µ—А–µ–Ј 4–5 —З–∞—Б–Њ–≤, –љ–Њ –љ–µ –±–Њ–ї–µ–µ 4 —А–∞–Ј –≤ —Б—Г—В–Ї–Є [2,9].
–Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –Љ–µ—Е–∞–љ–Є–Ј–Љ –і–µ–є—Б—В–≤–Є—П —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —А–∞–Ј–ї–Є—З–µ–љ. –Я–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї –Њ–±–ї–∞–і–∞–µ—В –ґ–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–Є–Љ, –∞–љ–∞–ї—М–≥–µ–Ј–Є—А—Г—О—Й–Є–Љ –Є –Њ—З–µ–љ—М –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–Љ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ, —В.–Ї. –±–ї–Њ–Ї–Є—А—Г–µ—В –¶–Ю–У –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –≤ –¶–Э–° –Є –љ–µ –Њ–±–ї–∞–і–∞–µ—В –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ. –Ш–Љ–µ—О—В—Б—П –Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–∞ –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –≤–Њ–Ј—А–∞—Б—В–∞ —А–µ–±–µ–љ–Ї–∞, –Ї–Њ—В–Њ—А—Л–µ –Њ–њ—А–µ–і–µ–ї—П—О—В—Б—П –Ј—А–µ–ї–Њ—Б—В—М—О —Б–Є—Б—В–µ–Љ—Л —Ж–Є—В–Њ—Е—А–Њ–Љ–∞ –†–450. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Ј–∞–і–µ—А–ґ–Ї–∞ –≤—Л–≤–µ–і–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –Є –µ–≥–Њ –Љ–µ—В–∞–±–Њ–ї–Є—В–Њ–≤ –Љ–Њ–ґ–µ—В –Њ—В–Љ–µ—З–∞—В—М—Б—П –њ—А–Є –љ–∞—А—Г—И–µ–љ–Є–Є —Д—Г–љ–Ї—Ж–Є–є –њ–µ—З–µ–љ–Є –Є –њ–Њ—З–µ–Ї. –°—Г—В–Њ—З–љ–∞—П –і–Њ–Ј–∞ 60 –Љ–≥/–Ї–≥ —Г –і–µ—В–µ–є —П–≤–ї—П–µ—В—Б—П –±–µ–Ј–Њ–њ–∞—Б–љ–Њ–є, –љ–Њ –њ—А–Є –µ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–Є –Љ–Њ–ґ–µ—В –љ–∞–±–ї—О–і–∞—В—М—Б—П –≥–µ–њ–∞—В–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞. –Ю–њ–Є—Б–∞–љ —Б–ї—Г—З–∞–є —Д—Г–ї—М–Љ–Є–љ–∞–љ—В–љ–Њ–є –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є —Б –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–µ–є, –Ї–Њ–∞–≥—Г–ї–Њ–њ–∞—В–Є–µ–є –њ—А–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–Љ –њ—А–µ–≤—Л—И–µ–љ–Є–Є —А–Њ–і–Є—В–µ–ї—П–Љ–Є –і–Њ–Ј—Л –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–∞ (150 –Љ–≥/–Ї–≥) –≤ —В–µ—З–µ–љ–Є–µ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –і–љ–µ–є [14]. –Я—А–Є –љ–∞–ї–Є—З–Є–Є —Г —А–µ–±–µ–љ–Ї–∞ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –≥–ї—О–Ї–Њ–Ј–Њ–6–—Д–Њ—Б—Д–∞—В–і–µ–≥–Є–і—А–Њ–≥–µ–љ–∞–Ј—Л –Є —А–µ–і—Г–Ї—В–∞–Ј—Л –≥–ї—О—В–∞—В–Є–Њ–љ–∞ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–∞ –Љ–Њ–ґ–µ—В –≤—Л–Ј–≤–∞—В—М –≥–µ–Љ–Њ–ї–Є–Ј —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤, –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Г—О –≥–µ–Љ–Њ–ї–Є—В–Є—З–µ—Б–Ї—Г—О –∞–љ–µ–Љ–Є—О.
–Ш–±—Г–њ—А–Њ—Д–µ–љ –Њ–±–ї–∞–і–∞–µ—В –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ –ґ–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–Є–Љ, –∞–љ–∞–ї—М–≥–µ–Ј–Є—А—Г—О—Й–Є–Љ –Є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ. –Т –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Є–±—Г–њ—А–Њ—Д–µ–љ —В–∞–Ї –ґ–µ —Н—Д—Д–µ–Ї—В–Є–≤–µ–љ –њ—А–Є –ї–Є—Е–Њ—А–∞–і–Ї–µ, –Ї–∞–Ї –Є –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї [9,13,15]. –Т –і—А—Г–≥–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –ґ–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–Є–є —Н—Д—Д–µ–Ї—В –Є–±—Г–њ—А–Њ—Д–µ–љ–∞ –≤ –і–Њ–Ј–µ 7,5 –Љ–≥/–Ї–≥ –≤—Л—И–µ, —З–µ–Љ —Г –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–∞ –≤ –і–Њ–Ј–µ 10 –Љ–≥/–Ї–≥ –Є –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л (10 –Љ–≥/–Ї–≥) [10]. –≠—В–Њ –њ—А–Њ—П–≤–ї—П–ї–Њ—Б—М –±–Њ–ї—М—И–Є–Љ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л —З–µ—А–µ–Ј 4 —З–∞—Б–∞ –Є —Г –±–Њ–ї—М—И–µ–≥–Њ —З–Є—Б–ї–∞ –і–µ—В–µ–є. –Ґ–∞–Ї–Є–µ –ґ–µ –і–∞–љ–љ—Л–µ –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л –≤ –і–≤–Њ–є–љ–Њ–Љ —Б–ї–µ–њ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –≤ –њ–∞—А–∞–ї–ї–µ–ї—М–љ—Л—Е –≥—А—Г–њ–њ–∞—Е –њ—А–Є –њ–Њ–≤—В–Њ—А–љ–Њ–Љ –њ—А–Є–µ–Љ–µ –Є–±—Г–њ—А–Њ—Д–µ–љ–∞ 7 –Є 10 –Љ–≥/–Ї–≥ –Є –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–∞ 10 –Љ–≥/–Ї–≥ —Г –і–µ—В–µ–є –Њ—В 5 –Љ–µ—Б. –і–Њ 13 –ї–µ—В [20]. –Ш–±—Г–њ—А–Њ—Д–µ–љ –±–ї–Њ–Ї–Є—А—Г–µ—В –¶–Ю–У –Ї–∞–Ї –≤ –¶–Э–°, —В–∞–Ї –Є –≤ –Њ—З–∞–≥–µ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П (–њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є–є –Љ–µ—Е–∞–љ–Є–Ј–Љ), —З–µ–Љ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ –µ–≥–Њ –љ–µ —В–Њ–ї—М–Ї–Њ –∞–љ—В–Є–њ–Є—А–µ—В–Є—З–µ—Б–Ї–Є–є, –љ–Њ –Є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ —Г–Љ–µ–љ—М—И–∞–µ—В—Б—П —Д–∞–≥–Њ—Ж–Є—В–∞—А–љ–∞—П –њ—А–Њ–і—Г–Ї—Ж–Є—П –Љ–µ–і–Є–∞—В–Њ—А–Њ–≤ –Њ—Б—В—А–Њ–є —Д–∞–Ј—Л, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –Є –Ш–Ы–1 (—Н–љ–і–Њ–≥–µ–љ–љ–Њ–≥–Њ –њ–Є—А–Њ–≥–µ–љ–∞). –°–љ–Є–ґ–µ–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Ш–Ы–1 —В–∞–Ї–ґ–µ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л. –Ш–±—Г–њ—А–Њ—Д–µ–љ –њ—А–Њ—П–≤–ї—П–µ—В –і–≤–Њ–є–љ–Њ–µ –±–Њ–ї–µ—Г—В–Њ–ї—П—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ – –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–µ –Є —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–µ. –С–Њ–ї–µ—Г—В–Њ–ї—П—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ –њ—А–Њ—П–≤–ї—П–µ—В—Б—П —Г–ґ–µ –≤ –і–Њ–Ј–µ 5 –Љ–≥/–Ї–≥ –Є –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–Њ, —З–µ–Љ —Г –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–∞. –≠—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –Є–±—Г–њ—А–Њ—Д–µ–љ –њ—А–Є —Б–ї–∞–±–Њ–є –Є —Г–Љ–µ—А–µ–љ–љ–Њ–є –±–Њ–ї–Є –≤ –≥–Њ—А–ї–µ, –±–Њ–ї–Є –њ—А–Є —В–Њ–љ–Ј–Є–ї–ї–Є—В–∞—Е, –Њ—Б—В—А—Л—Е —Б—А–µ–і–љ–Є—Е –Њ—В–Є—В–∞—Е, –Ј—Г–±–љ–Њ–є –±–Њ–ї–Є [11].
–Ш–Ј–≤–µ—Б—В–љ–Њ–є —А–µ–∞–Ї—Ж–Є–µ–є —Г –і–µ—В–µ–є —П–≤–ї—П–µ—В—Б—П –≥–Є–њ–µ—А—В–µ—А–Љ–Є—П –њ–Њ—Б–ї–µ –Є–Љ–Љ—Г–љ–Є–Ј–∞—Ж–Є–Є. –Э–∞ –Љ–µ—Б—В–µ –≤–≤–µ–і–µ–љ–Є—П –≤–∞–Ї—Ж–Є–љ—Л –Љ–Њ–ґ–µ—В –њ–Њ—П–≤–ї—П—В—М—Б—П –≥–Є–њ–µ—А–µ–Љ–Є—П, –њ—А–Є–њ—Г—Е–ї–Њ—Б—В—М, –±–Њ–ї—М –≤ –Љ–µ—Б—В–µ –Є–љ—К–µ–Ї—Ж–Є–Є, —З—В–Њ –Є–љ–Њ–≥–і–∞ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л, –љ–µ–і–Њ–Љ–Њ–≥–∞–љ–Є–µ–Љ –Є –≥–Њ–ї–Њ–≤–љ–Њ–є –±–Њ–ї—М—О. –У–Є–њ–µ—А—В–µ—А–Љ–Є—П –њ–Њ—Б–ї–µ –Є–Љ–Љ—Г–љ–Є–Ј–∞—Ж–Є–Є —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞–µ—В—Б—П, –Ї–∞–Ї –њ–Њ–Ї–∞–Ј–∞–љ–Є–µ –і–ї—П –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Є–±—Г–њ—А–Њ—Д–µ–љ–∞ [22].
–Э–µ—Б–Љ–Њ—В—А—П –љ–∞ –≤—Л—Б–Њ–Ї—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–Њ–≤––∞–љ—В–Є–њ–Є—А–µ—В–Є–Ї–Њ–≤, –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Є—Е —Г –і–µ—В–µ–є –љ–µ –≤—Б–µ–≥–і–∞ –±–µ–Ј–Њ–њ–∞—Б–љ–Њ. –Ґ–∞–Ї, –≤ 70––µ –≥–Њ–і—Л –њ—А–Њ—И–ї–Њ–≥–Њ —Б—В–Њ–ї–µ—В–Є—П –њ–Њ—П–≤–Є–ї–Є—Б—М —Г–±–µ–і–Є—В–µ–ї—М–љ—Л–µ –і–∞–љ–љ—Л–µ, —З—В–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –њ—А–Є –≤–Є—А—Г—Б–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є—П—Е —Г –і–µ—В–µ–є –Љ–Њ–ґ–µ—В —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—В—М—Б—П —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –†–µ—П (Reye), —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—Й–Є–Љ—Б—П —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–µ–є –Є –ґ–Є—А–Њ–≤–Њ–є –і–µ–≥–µ–љ–µ—А–∞—Ж–Є–µ–є –≤–љ—Г—В—А–µ–љ–љ–Є—Е –Њ—А–≥–∞–љ–Њ–≤, –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –њ–µ—З–µ–љ–Є –Є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞. –Ю–≥—А–∞–љ–Є—З–µ–љ–Є—П, –≤–≤–µ–і–µ–љ–љ—Л–µ –≤ –°–®–Р –љ–∞ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л —Г –і–µ—В–µ–є, –њ—А–Є–≤–µ–ї–Є –Ї –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ—Г —Б–љ–Є–ґ–µ–љ–Є—О —З–∞—Б—В–Њ—В—Л —Б–Є–љ–і—А–Њ–Љ–∞ –†–µ—П (—Б 555 —Б–ї—Г—З–∞–µ–≤ –≤ 1980 –≥. –і–Њ 36 – –≤ 1987 –Є 2 – –≤ 1997 –≥.) [12]. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞ –њ–Њ–≤—Л—И–∞–µ—В —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є —Б–Њ —Б—В–Њ—А–Њ–љ—Л –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞, –љ–∞—А—Г—И–∞–µ—В —Б–≤–µ—А—В—Л–≤–∞–µ–Љ–Њ—Б—В—М –Ї—А–Њ–≤–Є, –њ–Њ–≤—Л—И–∞–µ—В –ї–Њ–Љ–Ї–Њ—Б—В—М —Б–Њ—Б—Г–і–Њ–≤, —Г –љ–Њ–≤–Њ—А–Њ–ґ–і–µ–љ–љ—Л—Е –Љ–Њ–ґ–µ—В –≤—Л—В–µ—Б–љ—П—В—М –±–Є–ї–Є—А—Г–±–Є–љ –Є–Ј –µ–≥–Њ —Б–≤—П–Ј–Є —Б –∞–ї—М–±—Г–Љ–Є–љ–∞–Љ–Є –Є —В–µ–Љ —Б–∞–Љ—Л–Љ —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞—В—М —А–∞–Ј–≤–Є—В–Є—О –±–Є–ї–Є—А—Г–±–Є–љ–Њ–≤–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є. –≠–Ї—Б–њ–µ—А—В—Л –Т–Ю–Ч –љ–µ —А–µ–Ї–Њ–Љ–µ–љ–і—Г—О—В –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –Ї–∞—З–µ—Б—В–≤–µ –ґ–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–µ–≥–Њ —Б—А–µ–і—Б—В–≤–∞ —Г –і–µ—В–µ–є –і–Њ 12 –ї–µ—В, —З—В–Њ –љ–∞—И–ї–Њ –Њ—В—А–∞–ґ–µ–љ–Є–µ –≤ –љ–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–Љ –§–Њ—А–Љ—Г–ї—П—А–µ (2002) [8]. –Я—А–Є–Ї–∞–Ј–Њ–Љ –§–∞—А–Љ–Ї–Њ–Љ–Є—В–µ—В–∞ –†–§ –Њ—В 25.03.99 –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –њ—А–Є –Њ—Б—В—А—Л—Е –≤–Є—А—Г—Б–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є—П—Е —А–∞–Ј—А–µ—И–µ–љ–Њ —Б 15––ї–µ—В–љ–µ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞. –Т–Љ–µ—Б—В–µ —Б —В–µ–Љ –њ–Њ–і –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –≤—А–∞—З–∞ –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞ –Љ–Њ–ґ–µ—В –њ—А–Є–Љ–µ–љ—П—В—М—Б—П –њ—А–Є —А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е.
–Ю–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ –љ–∞–Ї–∞–њ–ї–Є–≤–∞–ї–Є—Б—М –і–∞–љ–љ—Л–µ –Њ –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–∞—Е –Є –і—А—Г–≥–Є—Е –∞–љ—В–Є–њ–Є—А–µ—В–Є–Ї–Њ–≤. –Ґ–∞–Ї, –∞–Љ–Є–і–Њ–њ–Є—А–Є–љ –Є–Ј––Ј–∞ —Б–≤–Њ–µ–є –≤—Л—Б–Њ–Ї–Њ–є —В–Њ–Ї—Б–Є—З–љ–Њ—Б—В–Є –±—Л–ї –Є—Б–Ї–ї—О—З–µ–љ –Є–Ј –љ–Њ–Љ–µ–љ–Ї–ї–∞—В—Г—А—Л –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ [5]. –Ь–µ—В–∞–Љ–Є–Ј–Њ–ї (–∞–љ–∞–ї—М–≥–Є–љ, –і–Є–њ–Є—А–Њ–љ) –Љ–Њ–ґ–µ—В —Г–≥–љ–µ—В–∞—В—М –Ї—А–Њ–≤–µ—В–≤–Њ—А–µ–љ–Є–µ –≤–њ–Њ—В—М –і–Њ —А–∞–Ј–≤–Є—В–Є—П —Д–∞—В–∞–ї—М–љ–Њ–≥–Њ –∞–≥—А–∞–љ—Г–ї–Њ—Ж–Є—В–Њ–Ј–∞, —З—В–Њ —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞–ї–Њ —А–µ–Ј–Ї–Њ–Љ—Г –Њ–≥—А–∞–љ–Є—З–µ–љ–Є—О –µ–≥–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –≤–Њ –Љ–љ–Њ–≥–Є—Е —Б—В—А–∞–љ–∞—Е –Љ–Є—А–∞ (International Agranulocytosis and Aplastic Anaemia Study Group, 1986). –Ю–і–љ–∞–Ї–Њ –≤ —Г—А–≥–µ–љ—В–љ—Л—Е —Б–Є—В—Г–∞—Ж–Є—П—Е, —В–∞–Ї–Є—Е –Ї–∞–Ї –≥–Є–њ–µ—А—В–µ—А–Љ–Є—З–µ—Б–Ї–Є–є —Б–Є–љ–і—А–Њ–Љ, –Њ—Б—В—А—Л–µ –±–Њ–ї–Є –≤ –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ –Є –і—А—Г–≥–Є—Е, –љ–µ –њ–Њ–і–і–∞—О—Й–Є—Е—Б—П –Є–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –і–Њ–њ—Г—Б—В–Є–Љ–Њ –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Љ–µ—В–∞–Љ–Є–Ј–Њ–ї—Б–Њ–і–µ—А–ґ–∞—Й–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤.
–°—А–∞–≤–љ–µ–љ–Є–µ –≤ –і–≤–Њ–є–љ—Л—Е —Б–ї–µ–њ—Л—Е —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –њ—А–Є –Љ–љ–Њ–≥–Њ–Ї—А–∞—В–љ–Њ–Љ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –і–Њ–Ј—Л –ґ–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–Є—Е —Б—А–µ–і—Б—В–≤ –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ —З–∞—Б—В–Њ—В–∞ –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л—Е —П–≤–ї–µ–љ–Є–є —Б—Е–Њ–і–љ–∞ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Є–±—Г–њ—А–Њ—Д–µ–љ–∞ –Є –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–∞ (8–9%) [17]. –Т —Н—В–Њ–Љ –Ї—А—Г–њ–љ–Њ–Љ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –±–Њ–ї–µ–µ —З–µ–Љ —Г 80 —В—Л—Б—П—З –і–µ—В–µ–є –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Г –Є–±—Г–њ—А–Њ—Д–µ–љ–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–Њ–Љ –љ–µ –њ–Њ–≤—Л—И–∞–µ—В—Б—П —А–Є—Б–Ї –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є, —Б–≤—П–Ј–∞–љ–љ–Њ–є —Б –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ—Л–Љ–Є –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є—П–Љ–Є, –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О –Є–ї–Є –∞–љ–∞—Д–Є–ї–∞–Ї—Б–Є–µ–є. –Э–Є —Г –Њ–і–љ–Њ–≥–Њ –Є–Ј –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Є–±—Г–њ—А–Њ—Д–µ–љ, –љ–µ —А–∞–Ј–≤–Є–ї—Б—П —Б–Є–љ–і—А–Њ–Љ –†–µ—П.
–£ –і–µ—В–µ–є, –Њ—Б–Њ–±–µ–љ–љ–Њ —А–∞–љ–љ–µ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞, –Њ—Б—В—А—Л–µ —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –љ–µ—А–µ–і–Ї–Њ –њ—А–Њ—В–µ–Ї–∞—О—В —Б –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–є –Њ–±—Б—В—А—Г–Ї—Ж–Є–µ–є, —З—В–Њ —Б—В–∞–≤–Є—В –≤–Њ–њ—А–Њ—Б –Њ–± –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—П—Е –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –ґ–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Г —В–∞–Ї–Є—Е –і–µ—В–µ–є –Є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–Љ —А–Є—Б–Ї–µ –њ—А–Њ–≤–Њ–Ї–∞—Ж–Є–Є –±—А–Њ–љ—Е–Њ—Б–њ–∞–Ј–Љ–∞. –Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞ –Є –і—А—Г–≥–Є–µ –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л–µ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞ –Љ–Њ–≥—Г—В –њ—А–Њ–≤–Њ—Ж–Є—А–Њ–≤–∞—В—М –±—А–Њ–љ—Е–Њ—Б–њ–∞–Ј–Љ —Г –ї–Є—Ж —Б –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М—О –∞—Б–њ–Є—А–Є–љ–∞. –≠—В–Њ—В –Љ–µ—Е–∞–љ–Є–Ј–Љ —Б–≤—П–Ј—Л–≤–∞—О—В —Б –Є–љ–∞–Ї—В–Є–≤–∞—Ж–Є–µ–є –¶–Ю–У, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї –љ–∞—А—Г—И–µ–љ–Є—О –±–∞–ї–∞–љ—Б–∞ –Љ–µ–ґ–і—Г –ї–Є–њ–Є–і–љ—Л–Љ–Є –Љ–µ–і–Є–∞—В–Њ—А–∞–Љ–Є –≤ —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ–Њ–Љ —В—А–∞–Ї—В–µ —Б —Г–≥–љ–µ—В–µ–љ–Є–µ–Љ —Б–Є–љ—В–µ–Ј–∞ –Я–У–Х2, –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–∞ –Є —В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ–Њ–≤ –Є —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ —Б–Є–љ—В–µ–Ј–∞ –ї–µ–є–Ї–Њ—В—А–Є–µ–љ–Њ–≤ [21]. –Я—А–Є –њ—А–Є–µ–Љ–µ –∞—Ж–µ—В–∞–Љ–Є–љ–Њ—Д–µ–љ–∞ –±—А–Њ–љ—Е–Њ–Ї–Њ–љ—Б—В—А–Є–Ї—Ж–Є—О —Б–≤—П–Ј—Л–≤–∞—О—В —Б –Є—Б—В–Њ—Й–µ–љ–Є–µ–Љ –≥–ї—О—В–∞—В–Є–Њ–љ–∞ –≤ —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ–Њ–Љ —В—А–∞–Ї—В–µ –Є —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ–Њ–є –Ј–∞—Й–Є—В—Л. –Ю–і–љ–∞–Ї–Њ –і–∞–ґ–µ —Г –±–Њ–ї—М–љ—Л—Е —Б –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М—О –∞—Б–њ–Є—А–Є–љ–∞ –Є –∞—В–Њ–њ–Є—З–µ—Б–Ї–Є–Љ –Є–ї–Є –∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ—Л–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ–Љ –љ–µ –≤—Л—П–≤–ї–µ–љ–Њ —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є—Е –∞–љ—В–Є—В–µ–ї –Ї –∞—Б–њ–Є—А–Є–љ—Г. –Т –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –∞—Б–њ–Є—А–Є–љ–Њ–≤–Њ–є –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –≤–∞–ґ–љ—Г—О —А–Њ–ї—М –Є–≥—А–∞–µ—В –њ—А–∞–≤–Є–ї—М–љ–Њ —Б–Њ–±—А–∞–љ–љ—Л–є –∞–љ–∞–Љ–љ–µ–Ј –Є –Њ—Ж–µ–љ–Ї–∞ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є, —Б –љ–∞—Б—В–Њ—А–Њ–ґ–µ–љ–љ–Њ—Б—В—М—О —Г –±–Њ–ї—М–љ—Л—Е —Б —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ–Њ–є «–∞—Б–њ–Є—А–Є–љ–Њ–≤–Њ–є —В—А–Є–∞–і–Њ–є» – –±—А–Њ–љ—Е–Є–∞–ї—М–љ–∞—П –∞—Б—В–Љ–∞ (–Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, —В—П–ґ–µ–ї–∞—П), –љ–∞–Ј–∞–ї—М–љ—Л–µ –њ–Њ–ї–Є–њ—Л –Є –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –∞—Б–њ–Є—А–Є–љ–∞.
–Я—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –Є–±—Г–њ—А–Њ—Д–µ–љ–∞ –Є –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–∞ —Г –і–µ—В–µ–є —Б –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–є –∞—Б—В–Љ–Њ–є [17] –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Є–Ј 1879 –і–µ—В–µ–є –≤ —Б–≤—П–Ј–Є –Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л–Љ —В–µ—З–µ–љ–Є–µ–Љ –∞—Б—В–Љ—Л –±—Л–ї–Є –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ—Л —В–Њ–ї—М–Ї–Њ 18, –њ—А–Є—З–µ–Љ –њ—А–Є–Љ–µ—А–љ–Њ –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–µ —З–Є—Б–ї–Њ –і–µ—В–µ–є –њ–Њ–ї—Г—З–∞–ї–Њ –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї –Є –Є–±—Г–њ—А–Њ—Д–µ–љ. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Є–±—Г–њ—А–Њ—Д–µ–љ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –∞—Ж–µ—В–∞–Љ–Є–љ–Њ—Д–µ–љ–Њ–Љ –љ–µ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В —А–Є—Б–Ї –±—А–Њ–љ—Е–Њ—Б–њ–∞–Ј–Љ–∞ —Г –і–µ—В–µ–є —Б –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–є –∞—Б—В–Љ–Њ–є, –љ–µ –Є–Љ–µ—О—Й–Є—Е —Г–Ї–∞–Ј–∞–љ–Є—П –љ–∞ –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –∞—Б–њ–Є—А–Є–љ–∞, —З—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В –µ–≥–Њ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Г—О –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –і–ї—П –і–µ—В–µ–є —Б –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–є –∞—Б—В–Љ–Њ–є. –£ –і–µ—В–µ–є –њ–µ—А–≤—Л—Е 6 –Љ–µ—Б. –њ—А–Є –±—А–Њ–љ—Е–Є–Њ–ї–Є—В–µ –Є–±—Г–њ—А–Њ—Д–µ–љ —В–∞–Ї–ґ–µ –љ–µ –Њ–Ї–∞–Ј—Л–≤–∞–ї –±—А–Њ–љ—Е–Њ—Б–њ–∞—Б—В–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П. –£ –і–µ—В–µ–є –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –∞—Б–њ–Є—А–Є–љ–∞ –≤—Б—В—А–µ—З–∞–µ—В—Б—П –і–Њ–≤–Њ–ї—М–љ–Њ —А–µ–і–Ї–Њ, –Є –≤ —Н—В–Є—Е —Б–ї—Г—З–∞—П—Е –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Є–±—Г–њ—А–Њ—Д–µ–љ–∞ –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Њ.
–Ь—Л –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є –Є–±—Г–њ—А–Њ—Д–µ–љ (—Б—Г—Б–њ–µ–љ–Ј–Є—П «–Э—Г—А–Њ—Д–µ–љ –і–ї—П –і–µ—В–µ–є») –≤ –і–Њ–Ј–µ 7–10 –Љ–≥/–Ї–≥ —Г 52 –і–µ—В–µ–є —Б –Ю–†–Т–Ш –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 6 –Љ–µ—Б. –і–Њ 10 –ї–µ—В. –Ш–Ј –љ–Є—Е —Г 20 –Ю–†–Т–Ш –њ—А–Њ—В–µ–Ї–∞–ї–∞ –љ–∞ —Д–Њ–љ–µ –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–є –∞—Б—В–Љ—Л –ї–µ–≥–Ї–Њ–є –Є —Б—А–µ–і–љ–µ–є —В—П–ґ–µ—Б—В–Є –±–µ–Ј —Г–Ї–∞–Ј–∞–љ–Є–є –љ–∞ –∞—Б–њ–Є—А–Є–љ–Њ–≤—Г—О –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М; —Г 17 –і–µ—В–µ–є – –Ю–†–Т–Ш —Б –±—А–Њ–љ—Е–Њ–Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –Є —Г 15 –і–µ—В–µ–є – –Ю–†–Ч –≤–µ—А—Е–љ–Є—Е –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є. –Э—Г—А–Њ—Д–µ–љ –і–ї—П –і–µ—В–µ–є – —Н—В–Њ –±–µ–ї–∞—П, –љ–µ —Б–Њ–і–µ—А–ґ–∞—Й–∞—П —Б–∞—Е–∞—А–∞ —Б—Г—Б–њ–µ–љ–Ј–Є—П –і–ї—П –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞, —Б–Њ –≤–Ї—Г—Б–Њ–Љ –∞–њ–µ–ї—М—Б–Є–љ–∞, –Ї–Њ—В–Њ—А–∞—П –≤ –Ї–∞—З–µ—Б—В–≤–µ –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –Є–љ–≥—А–µ–і–Є–µ–љ—В–∞ —Б–Њ–і–µ—А–ґ–Є—В –Є–±—Г–њ—А–Њ—Д–µ–љ –≤ –і–Њ–Ј–µ 100 –Љ–≥/5 –Љ–ї. –£ 48 –і–µ—В–µ–є –њ–Њ–ї—Г—З–µ–љ —Е–Њ—А–Њ—И–Є–є –ґ–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–Є–є —Н—Д—Д–µ–Ї—В –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –њ–µ—А–≤–Њ–є –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞ –њ—А–Є –ї–Є—Е–Њ—А–∞–і–Ї–µ, –њ—А–µ–≤—Л—И–∞—О—Й–µ–є 38,5°–° –≤ –∞–Ї—Б–Є–ї–ї—П—А–љ–Њ–є –Њ–±–ї–∞—Б—В–Є. –С–Њ–ї—М—И–Є–љ—Б—В–≤—Г –і–µ—В–µ–є –њ—А–µ–њ–∞—А–∞—В –љ–∞–Ј–љ–∞—З–∞–ї–Є –љ–µ –±–Њ–ї–µ–µ 2 –і–љ–µ–є. –Я–Њ–±–Њ—З–љ—Л—Е –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є, –≤ —В.—З. —Г—Б–Є–ї–µ–љ–Є—П –Є–ї–Є –њ—А–Њ–≤–Њ–Ї–∞—Ж–Є–Є –±—А–Њ–љ—Е–Њ—Б–њ–∞–Ј–Љ–∞, –љ–µ –Њ—В–Љ–µ—З–∞–ї–Є. –£ 4 –і–µ—В–µ–є —Н—Д—Д–µ–Ї—В –Њ—В –њ—А–Є–µ–Љ–∞ –Є–±—Г–њ—А–Њ—Д–µ–љ–∞ –±—Л–ї –Љ–Є–љ–Є–Љ–∞–ї—М–љ—Л–Љ –Є –Ї—А–∞—В–Ї–Њ–≤—А–µ–Љ–µ–љ–љ—Л–Љ. –£ 2 –і–µ—В–µ–є –±—Л–ї –љ–∞–Ј–љ–∞—З–µ–љ –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї, —Г 2 –і—А—Г–≥–Є—Е –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–∞—Б—М –ї–Є—В–Є—З–µ—Б–Ї–∞—П —Б–Љ–µ—Б—М –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ. –Ш–Ј –њ–Њ–±–Њ—З–љ—Л—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є —Г —А–µ–±–µ–љ–Ї–∞ —Б –∞—В–Њ–њ–Є—З–µ—Б–Ї–Є–Љ –і–µ—А–Љ–∞—В–Є—В–Њ–Љ –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ–Њ –њ–Њ—П–≤–ї–µ–љ–Є–µ –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Њ–є —Б—Л–њ–Є.
–Т –ї–Є—В–µ—А–∞—В—Г—А–µ –Њ–њ–Є—Б–∞–љ—Л —Б–ї—Г—З–∞–Є –љ–∞—А—Г—И–µ–љ–Є—П –њ–Њ—З–µ—З–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є —Г –Њ—В–і–µ–ї—М–љ—Л—Е –±–Њ–ї—М–љ—Л—Е, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –Є–±—Г–њ—А–Њ—Д–µ–љ [19]. Lesko and Mitchell –≤ 1995 –≥–Њ–і—Г –њ—А–Њ–≤–µ–ї–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –і–ї—П –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П —Б—В–µ–њ–µ–љ–Є —А–Є—Б–Ї–∞ –њ–Њ–±–Њ—З–љ—Л—Е —П–≤–ї–µ–љ–Є–є –≤ –±–Њ–ї—М—И–Њ–Љ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –і–≤–Њ–є–љ–Њ–Љ —Б–ї–µ–њ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Є–±—Г–њ—А–Њ—Д–µ–љ–∞ –Є –∞—Ж–µ—В–∞–Љ–Є–љ–Њ—Д–µ–љ–∞ [16]. –Ф–µ—В–Є —Б —Д–µ–±—А–Є–ї—М–љ—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –њ–Њ–ї—Г—З–∞–ї–Є –Є–ї–Є 12 –Љ–≥/–Ї–≥ –∞—Ж–µ—В–∞–Љ–Є–љ–Њ—Д–µ–љ–∞, –Є–ї–Є –Є–±—Г–њ—А–Њ—Д–µ–љ –≤ –і–Њ–Ј–µ 5 –Є–ї–Є 10 –Љ–≥/–Ї–≥. –Э–Є —Г –Њ–і–љ–Њ–≥–Њ –Є–Ј –±–Њ–ї—М–љ—Л—Е –љ–µ –Њ—В–Љ–µ—З–µ–љ–Њ —А–∞–Ј–≤–Є—В–Є–µ –њ–Њ—З–µ—З–љ–Њ–є –Њ—Б—В—А–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є. –Т 1997 –≥. —В–µ –ґ–µ –∞–≤—В–Њ—А—Л —Г 84 000 –±–Њ–ї—М–љ—Л—Е –њ—А–Њ–≤–µ—А–Є–ї–Є –≥–Є–њ–Њ—В–µ–Ј—Г, —З—В–Њ –Ї—А–∞—В–Ї–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –∞–љ—В–Є–њ–Є—А–µ—В–Є–Ї–Њ–≤ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В —А–Є—Б–Ї –љ–∞—А—Г—И–µ–љ–Є–є –њ–Њ—З–µ—З–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є —Г –і–µ—В–µ–є [17]. –Ю—Б–љ–Њ–≤—Л–≤–∞—П—Б—М –љ–∞ —Н—В–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е, –∞–≤—В–Њ—А—Л —Б—З–Є—В–∞—О—В, —З—В–Њ –њ—А–Є –Ї—А–∞—В–Ї–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–Љ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –Є–±—Г–њ—А–Њ—Д–µ–љ–∞ –Є –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–∞ –љ–µ –њ–Њ–≤—Л—И–∞–µ—В—Б—П —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є —Б–Њ —Б—В–Њ—А–Њ–љ—Л –њ–Њ—З–µ–Ї. –Я–Њ–≤—Л—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –∞–Ј–Њ—В–∞ –Љ–Њ—З–µ–≤–Є–љ—Л –Є –Ї—А–µ–∞—В–Є–љ–Є–љ–∞ –≤—Б—В—А–µ—З–∞–ї–Њ—Б—М —Г –і–µ—В–µ–є, –Є—Б—Е–Њ–і–љ–Њ –Є–Љ–µ–≤—И–Є—Е —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Б–Њ —Б—В–Њ—А–Њ–љ—Л –њ–Њ—З–µ–Ї –≤ —Б–≤—П–Ј–Є —Б —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є (–њ–Њ—З–µ—З–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М, –≤—А–Њ–ґ–і–µ–љ–љ–∞—П —Б–µ—А–і–µ—З–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М, –њ–µ—З–µ–љ–Њ—З–љ–∞—П –і–Є—Б—Д—Г–љ–Ї—Ж–Є—П), –∞ —В–∞–Ї–ґ–µ –њ—А–Є–љ–Є–Љ–∞–µ–Љ—Л–Љ–Є –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–∞–Љ–Є (–љ–µ—Д—А–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є, —В–∞–Ї–Є–Љ–Є –Ї–∞–Ї —Ж–Є–Ї–ї–Њ—Б–њ–Њ—А–Є–љ, –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і—Л; –Є–Ј–Љ–µ–љ—П—О—Й–Є–Љ–Є —Б—Л–≤–Њ—А–Њ—В–Њ—З–љ—Г—О –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О –Ї–∞–ї–Є—П – –і–Є–≥–Њ–Ї—Б–Є–љ, –њ—А–µ–њ–∞—А–∞—В—Л –Ї–∞–ї–Є—П) –Є–ї–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ–Њ–є –і–µ–≥–Є–і—А–∞—В–∞—Ж–Є–Є.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –ґ–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–∞—П —В–µ—А–∞–њ–Є—П —Г –і–µ—В–µ–є –і–Њ–ї–ґ–љ–∞ –љ–∞–Ј–љ–∞—З–∞—В—М—Б—П —Б—В—А–Њ–≥–Њ –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ–Њ —Б —Г—З–µ—В–Њ–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є –∞–љ–∞–Љ–љ–µ—Б—В–Є—З–µ—Б–Ї–Є—Е –і–∞–љ–љ—Л—Е. –Я—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –ї—О–±–Њ–≥–Њ –∞–љ—В–Є–њ–Є—А–µ—В–Є–Ї–∞ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –≤–љ–Є–Љ–∞—В–µ–ї—М–љ–Њ –Њ–њ—А–µ–і–µ–ї—П—В—М –і–Њ–Ј—Г, –Є–Ј–±–µ–≥–∞—В—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —Б–Њ–і–µ—А–ґ–∞—Й–Є—Е –±–Њ–ї–µ–µ —З–µ–Љ –Њ–і–љ–Њ –ґ–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–µ–µ —Б—А–µ–і—Б—В–≤–Њ, –њ–Њ–љ–Є–Љ–∞—В—М —А–Њ–ї—М –і–µ–≥–Є–і—А–∞—В–∞—Ж–Є–Є –њ—А–Є —А–≤–Њ—В–µ, —Б–љ–Є–ґ–µ–љ–Є–Є –њ–Њ—В—А–µ–±–ї–µ–љ–Є—П –ґ–Є–і–Ї–Њ—Б—В–Є, –і–Є–∞—А–µ–µ. –Я—А–µ–њ–∞—А–∞—В–∞–Љ–Є –≤—Л–±–Њ—А–∞ –њ—А–Є –ї–Є—Е–Њ—А–∞–і–Ї–µ –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ––≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –≥–µ–љ–µ–Ј–∞ —Г –і–µ—В–µ–є —П–≤–ї—П—О—В—Б—П –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї –Є –Є–±—Г–њ—А–Њ—Д–µ–љ. –Э–µ–і–Њ–њ—Г—Б—В–Є–Љ–Њ –Ї—Г—А—Б–Њ–≤–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞–љ—В–Є–њ–Є—А–µ—В–Є–Ї–Њ–≤ –±–µ–Ј —Г—В–Њ—З–љ–µ–љ–Є—П –њ—А–Є—З–Є–љ –ї–Є—Е–Њ—А–∞–і–Ї–Є.
1. –Т–µ—В—А–Њ–≤ –Т.–Я., –Ф–ї–Є–љ –Т.–Т. –Є —Б–Њ–∞–≤—В. –†–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞–љ—В–Є–њ–Є—А–µ—В–Є–Ї–Њ–≤ —Г –і–µ—В–µ–є. –Я–Њ—Б–Њ–±–Є–µ –і–ї—П –≤—А–∞—З–µ–є. –Ь.,2002. 23—Б.
2. –У–Њ—Б—Г–і–∞—А—Б—В–≤–µ–љ–љ—Л–є —А–µ–µ—Б—В—А –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤.– –Ь.: –Ь–Ч –†–§, 2000.
3. –Ъ–Њ—А–Њ–≤–Є–љ–∞ –Э.–Р., –Ч–∞–њ–ї–∞—В–љ—В–Ї–Њ–≤ –Р.–Ы. –Є —Б–Њ–∞–≤—В. –Ы–Є—Е–Њ—А–∞–і–Ї–∞ —Г –і–µ—В–µ–є. –†–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л–є –≤—Л–±–Њ—А –ґ–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–Є—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤. –†—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –і–ї—П –≤—А–∞—З–µ–є. –Ь., 2000, 67—Б.
4. –Ы–Њ—Г—А–Є–љ –Ь.–Ш. –Ы–Є—Е–Њ—А–∞–і–Ї–∞ —Г –і–µ—В–µ–є. –Я–µ—А. —Б –∞–љ–≥–ї. – –Ь.: –Ь–µ–і–Є—Ж–Є–љ–∞, 1985. – 255—Б.
5. –Ь–∞—И–Ї–Њ–≤—Б–Ї–Є–є –Ь.–Ф. –Ы–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞. –Т –і–≤—Г—Е —З–∞—Б—В—З—Е. – 12 –Є–Ј–і., –њ–µ—А–µ—А–∞–±. –Є –і–Њ–њ. –Ь.:–Ь–µ–і–Є—Ж–Є–љ–∞, 1993. – –І.1 – —Б.199–200.
6. –Ю—Б—В—А—Л–µ —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Г –і–µ—В–µ–є: –ї–µ—З–µ–љ–Є–µ –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞. –Э–∞—Г—З–љ–Њ––њ—А–∞–Ї—В–Є—З–µ—Б–Ї–∞—П –њ—А–Њ–≥—А–∞–Љ–Љ–∞ –Ь., 2002.
7. –Ґ–∞—В–Њ—З–µ–љ–Ї–Њ –Т.–Ъ. –†–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –ґ–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–Є—Е —Б—А–µ–і—Б—В–≤ —Г –і–µ—В–µ–є. –†—Г—Б—Б–Ї–Є–є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–є –ґ—Г—А–љ–∞–ї, 2000 – вДЦ3. —Б—В—А 40–42.
8. –§–µ–і–µ—А–∞–ї—М–љ–Њ–µ —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –і–ї—П –≤—А–∞—З–µ–є –њ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—О –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤ (—Д–Њ—А–Љ—Г–ї—П—А–љ–∞—П —Б–Є—Б—В–µ–Љ–∞): –≤—Л–њ—Г—Б–Ї –®. –У–≠–Ю–Ґ–Р–† –Ь–Х–Ф–Ш–¶–Ш–Э–Р.2002–325,462 —Б.
9. Aksoylar S, et al. Evaluation of sponging and antipyretic medication to reduce body temperature in febrile children. Acta Paediatrica Japonica 1997; 39: 215–217.
10. Autret E, et al. Evaluation of ibuprofen versus aspirin and paracetamol on efficacy and comfort in children with fever. EurJ Clin 1997; 51: 367–371.
11. Bertin, L., G. Pons, et al. Randomized, double–blind, multicenler, controlled Trial of ibuprofen versus acetaminophen (paracetamol) and placebo for treatment of symptoms of tonsillitis and pharyngitis in children. J Pediatr 1991, 119(5): 811–4.
12. –°enter for Disiese Control: National Reye syndrom Surveillance – United States // New England J. Med. – 1999. –N340. – P.1377.
13. Czaykowski D, et al. Evaluation of the antipyretic efficacy of single dose ibuprofen suspension compared to acetaminophen elixir in febrile children. Pediatric Research, April 1994; Vol. 35, No.4, Part 2, Abstr. 829.
14. Henretig F. Fever In: Fleisher G. Ludwig S ed. Textbook of pediatric emergency medicine. 3 d ed. Baltimore: Williams & Wilkins, 1993; 202–9.
15. Kelley MT, Walson P.D, Edge H et al. Pharmacokinetics and pharmacodynamics of ibuprofen isomers and acetaminophen in febrile children. Clin. Pharmacol. Ther. 1992; 52: 181–9.
16. Lesko SM, Mitchell AA. An assessment of the safety of pediatric ibuprofen: a practitioner–based randomized clinical trial. JAMA 1995;–273.–929–33.
17. Lesko SM, Mitchell AA. Renal function after short–term ibuprofen use in infants and children. Pediatrics 1997.–100.–954–7.
18. The management of fever in young children with acute respiratory infections in developing countries/ WHO/ARI/93.90/, Geneva 1993.
19. Marcia L. Buck Ibuprofen–associated Renal Toxicity in Children Pediatric Pharmacotherapy. A Monthly Review for Health Care Professionals of the Children’s Medical Center 2000.– V 6 – N 4.
20. Sidler J, et al. A double–blind comparison of ibuprofen and paracetamol in juvenile pyrexia. Br. J. Clin. Pract. 1–990; 44(Suppl. 70): 22–25.
21. Szczeklic A., Sanak M Genetic mechanisms in aspirin0induced asthma. Am J Respir Crit Care Med 2000< –161.–pS142–146.
22. Van der Walt JH, Roberton DM. Anaesthesia and recently vaccinated children. Paediatr. Anaesth., 1996; 6 (2): 135–41.












