Аллергическими заболеваниями во всем мире страдают около 500 млн человек. В развивающихся странах рост заболеваемости опережает аналогичные показатели развитых стран, приобретая особое социальное значение. Распространенность бронхиальной астмы в разных странах и разных возрастных группах колеблется от 33 до 150‰, атопического дерматита – от 37 до 250‰. Даже если аллергическое заболевание протекает не в тяжелой форме, оно существенно сказывается на общественной и профессиональной деятельности, неблагоприятно влияет на школьную успеваемость, требует больших экономических затрат от общества и семьи. Изменяется и структура возможных причинных факторов. Если раньше контактная аллергия у детей и подростков была казуистической редкостью, то в настоящее время нарастает частота аллергии на никель за–за ношения подростками металлических пряжек и цепочек на голом теле и в нередких случаях – после пирсинга.
Чаще регистрируется аллергия на латекс. Латекс выступает как контактный и ингаляционный аллерген. Особенно часто данный вид аллергии регистрируется у персонала операционных, у оперированных, урологических пациентов. Признаком латексной аллергии может быть периоральная уртикария после надувания воздушных шариков. В 30% случаев – перекрестная реакция с бананами.
С учетом распространенности аллергии, полиморфизма ее проявлений задача по ее выявлению и подбору первого этапа терапии возлагается на врачей первичного звена медицинской службы: педиатров, терапевтов, специалистов по семейной медицине.
Респираторную аллергию следует исключать при наличии следующих признаков:
• респираторные симптомы не сопровождаются лихорадкой. Отделяемое из носа водянистого характера;
• регистрируются признаки атопии;
• в индивидуальном анамнезе есть указания на атопический дерматит или непереносимость отдельных видов пищи;
• в семейном анамнезе есть случаи атопического дерматита, экземы, аллергического ринита или астмы;
• ухудшение состояния развивается сезонно или после экспозиции с определенным веществом, растением или животным;
• антибиотики малоэффективны;
• облегчение приносят антигистаминные препараты и бронходилататоры.
Следует подчеркнуть, что диагностика аллергических состояний – прежде всего клиническая задача.
Клинические симптомы и состояния, требующие подтверждения или исключения аллергии (атопии)
Анафилаксия. Может быть аллергической, но может быть и токсического характера, например, на укус овода.
Бронхиальная астма. У детей младшего возраста чаще инфекционная. У старших – аллергического характера (до 70%).
Конъюнктивит. Рецидивирующее течение, особенно сезонное – показатель аллергического генеза.
Ринит. При хроническом рините исключить аллергию на домашних клещей.
Отек Квинке. Может быть аллергический, но чаще – генетически опосредованная иммунная реакция.
Крапивница. Аллергический генез не чаще чем в 5% случаев.
Атопический дерматит. Аллергия – одно из проявлений, реже – причина.
Гастроэнтеритические симптомы. Боли в животе, колики, диарея могут быть обусловлены аллергией, но чаще – иными причинами (непереносимость трегаллоза – углевода грибов, возрастная непереносимость лактозы и т.д.).
Мигрень. Пусковым механизмом может быть пища, но проблема не в аллергии, а в освобождении биогенных аминов.
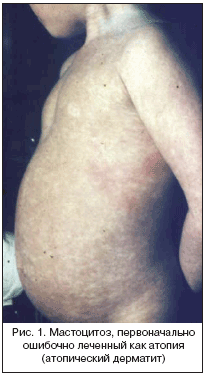
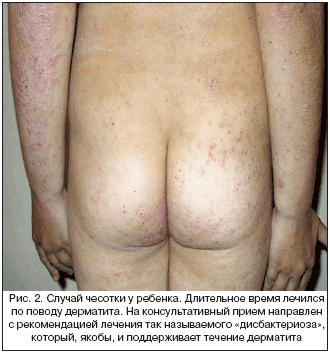
Как аллергические реакции воспринимаются мастоцитоз (крапивница, чаще – генетически детерминирована, а не аллергическая реакция), вегетативные реакции, реакции раздражения (в т.ч. артифициальные), инфекции (рис. 1 и 2).
С осторожностью следует трактовать лабораторные признаки атопии, которые обнаруживаются у 30–40% людей, но аллергические реакции фиксируются всего у 10%. Достоверность диагностики пищевой аллергии методами RAST или PRIST:
• Отрицательный результат – 90%.
• Положительный результат – 25% (!).
Из этого следует, что ¾ положительных результатов, на основании которых педиатрами нередко накладываются жесткие ограничения диеты, ошибочны.
Достоверность определения причинных факторов аллергии по концентрации иммуноглобулина Е (IgE):
• 80–90% – пыльцевая аллергия, аллергия на домашнюю пыль, животных (за исключением собак), пчел, ос;
• 25–50% – пищевые аллергены, аллергены собак, плесневых грибков;
• 20–30% – пенициллин, токсические вещества из внешней среды.
Специфический IgG (и IgG4) часто ложноположительный: до 30% здоровых детей младшего возраста имеют специфические IgG и IgG4 к коровьему молоку, видимо, как результат широкого распространения искусственного вскармливания. По мнению S. Illing [1], специфический IgG есть смысл определять только в динамике для оценки течения аллергии на яд насекомых.
Наряду с собственно аллергическими состояниями существует большое число заболеваний и реакций (например, некоторые токсические: ожоги растениями и т.д.), протекающих со схожими клиническими проявлениями за счет высвобождения гистамина и гистаминоподобных продуктов. Это ставит перед специалистами задачу выбора препарата, оптимальным образом сочетающего эффективность и приемлемую стоимость.
Обоснование выбора Супрастинекса
В середине 90–х годов XX века в практику внедрили второе поколение антигистаминных препаратов (лоратадин, цетиризин), ставших препаратами выбора в лечении атопии у детей и взрослых [2,3]. Седативный эффект в этой группе значительно ниже, чем у препаратов первого поколения. Дальнейшее совершенствование препаратов второго поколения привело к синтезу левоцетиризина (Супрастинекс) – изомера цетиризина, обладающего большим сродством к рецепторам. Распространенность атопических заболеваний, вероятность стремительного развития симптоматики требуют предоставления пациентам препаратов, которые бы позволили им самостоятельно регулировать активность заболевания, не дожидаясь визита к врачу, и при этом не снижая степень собственной работоспособности [4,5]. И если в описаниях антигистаминных препаратов указывают на возможность или невозможность после их приема вождения автомобиля, то почему–то не вспоминают, что ребенок должен учиться и много двигаться.
Механизм действия Супрастинекса
(левоцетиризина)
Цетиризин – метаболит гидроксизина – представителя первого поколения пиперазиновых антигистаминных препаратов. Супрастинекс – активный R–энантиомер (левовращающий) цетиризина и, по сравнению с последним, с двухкратной аффинностью к Н1–рецепторам. Если цетиризин в дозе 5–10 мг при энтодермальном введении гистамина значительно подавляет образование волдырей и эритемы, вызванных этим введением, то Супрастинекс (левоцетиризин) в дозе 5 мг блокирует данные реакции на протяжении 24 ч [6,7]. Супрастинекс практически не оказывает антихолинергического и антисеротонического действия, не взаимодействует с адренергическими 5–НТ–рецепторами. Крайне важно, что в противоположность многим другим антигистаминным препаратам Супрастинекс не влияет на длительность интервала QT, т.е. не может быть причиной синдрома внезапной смерти [8].
Фармакокинетика
Супрастинекс быстро всасывается из кишечника, максимальная концентрация в плазме достигается уже через 1 ч после приема препарата. Супрастинекс способен проникать через гематоэнцефалический барьер. Но в мозге он связывается только с 30–50% Н1–рецепторов, а на периферии – с 90%. 50–80% дозы Супрастинекса выделяется с мочой в неизменном виде, экскретируясь клубочками и активно секретируясь канальцами. Клиренс Супрастинекса полностью коррелирует с креатининовым [5,7], а фармакокинетика выгодно отличается от множества других антигистаминных препаратов. В частности, пиковая концентрация Супрастинекса (левоцетиризина) в плазме регистрируется уже через 0,9 ч после приема против 3 ч для дезлоратадина. Стабильная терапевтическая концентрация в плазме достигается для дезлоратадина через 6 сут., фексофенамида – через 3 сут., мизоластина – через 2–3 сут., Супрастинекса – уже на 2–е сут. [9].
Результаты клинических исследований
Эффективность Супрастинекса по сравнению с цетиризином и плацебо была первоначально доказана по результатам проспективных рандомизированных двойных слепых плацебо–контролируемых исследований [10]. Для достижения эффекта требовалось либо 10 мг цетиризина, либо 5 мг Супрастинекса (левоцетиризина) в сутки [11,12], что свидетельствует в пользу последнего.
Безопасность Супрастинекса (левоцетиризина) была изучена у 510 детей в возрасте от 12 до 24 мес. в рамках исследований по раннему предупреждению астмы у детей с атопией (EPAAC). По результатам рандомизированного двойного слепого плацебо–контролируемого исследования было показано, что прием дважды в сутки 0,125 мг Супрастинекса на протяжении 18 мес. сопровождался минимальными побочными реакциями у небольшого числа детей [13], что позволяет использовать препарат для снижения риска формирования бронхиальной астмы [14] у детей с атопическим дерматитом, обрывая так называемый «атопический марш». Эффективность Супрастинекса (левоцетиризина), позволяющая использовать его в минимальных дозах в качестве монопрепарата, а не в комплексе с иными средствами, резко снижает затраты на лечение [15].
Побочные действия
Самое частое побочное действие – дозозависимая сонливость, но она регистрируется только в первый день лечения и значительно реже, чем у препаратов первого поколения. Более того, побочные эффекты, явно связанные с медикаментами, были зарегистрированы у пациентов, леченных Супрастинексом (левоцетиризином), реже, чем при назначении плацебо (5,1 против 6,3%). Побочные реакции заставили прервать прием Супрастинекса всего у 0,5% детей и у 1% – в контрольной группе [5,7,13].
Заключение
Широкая распространенность аллергических реакций, изменение спектра аллергенов ставят перед лечащим врачом задачу выбора эффективных препаратов с быстрым эффектом, возможностью длительного приема без ограничения активности и когнитивных способностей и минимальным риском побочных действий. Супрастинекс (левоцетиризин) относится к безрецептурным препаратам и может по рекомендациям врача использоваться пациентами для самостоятельного контроля симптомов атопии. Малая вероятность сонливости и других побочных действий, способность подавлять секрецию провоспалительных цитокинов [16,17], ингибировать аллергические реакции на введение гистамина, специфических аллергенов, при холодовой аллергии, уменьшение бронхоспазма при астме, значительное смягчение проявлений сезонного и персистирующего аллергического ринита, хронической идиопатической крапивницы, отека Квинке, зудящих дерматозов, аллергических реакций на прием пищи, лекарственных средств, укусы насекомых выводит обсуждаемый препарат на первую линию терапии.
Литература
1. Illing S., Spranger St. (Hrsg.) // Padiatrie. JungjohanVerlaggesellschaft. – Stuttgart, 1993. – S. 442–449.
2. Фризин Д.В., Бастракова Т.А., Фризин В.В. Цетиризин в лечении детей с атопическим дерматитом. http://www.dermatology.ru/collections/tsetirizin–v–lechenii–detei–s–atopicheskim–dermatitom.
3. Bachert C. A review of the efficacy of desloratadine, fexofenadine and levocetirizine in the treatment of nasal congestion in patients with allergic rhinitis // Clin. Ther. – 2009. – Vol. 31. – P. 921–944.
4. Singh–Franco D., Ghin H., Robles G. et al. Levocetirizine for the treatment of allergic rhinitis and chronic idiopathic urticaria in adults and children // Clin. Ther. – 2009. – Vol. 31. – P. 1664–1687.
5. Levocetirizine. Drug Facts and Comparisons 4.0. Efacts [online]. 2010. Available from Wolters Kluwer Health, Inc. (accessed 4/19/10).
6. Buck L. Cetirizine and Levocetirizine Use in Children // Pediatr. Pharm. – 2010. – Vol. 16. – P. 225–234.
7. Xyzal® (Levocetirizine) prescribing information. UCB, Inc., August 2009. Available at www.xyzal.com (accessed 5/15/10).
8. Schmidt B., Sreeram N., Brockmeier K. Verlangerung des QTc–IntervallsimOberflachen–Ekg // Padiatrische Praxis. – 2009. – Bd. 73. – S. 279–286.
9. Molimard M., Diquet B., Benedetti M. Comparison of pharmacokinetic and metabolism of desloratadine, fexofenadine, levoceterizine and mizolastine in humans // Fundamental and Clinical Pharmacology. – 2004. – Vol. 18. – P. 399–411.
10. Lee C., Sun J., Lu K. et al. The comparison of cetirizine, levocetirizine and placebo for the treatment of childhood perennial allergic rhinitis. // Pediatr. Allergy Immunol. – 2009. – Vol. 20. – P. 493–499.
11. deBlic J., Wahn U., Billard E. et al. Levocetirizine in children: evidenced efficacy and safety n a 6–week randomized seasonal allergic rhinitis trial // Pediatr. Allergy Immunol. – 2005. – Vol. 16. – P. 267–275.
12. Potter P. Pediatric Levocetirizine Study Group. Efficacy and safety of levocetirizine on symptoms and health–related quality of life of children with perennial allergic rhinitis: a double–blind, placebo–controlled randomized clinical trial // Ann. Allergy, Asthma and Immunolog. – 2005. – Vol. 95. – P. 175–180.
13. Simons F. Early Prevention of Asthma in Atopic Children Study Group. Safety of levocetirizine treatment in young atopic children: an 18–month study // Pediatr. Allergy and Immunolog. – 2007. – Vol. 18. – P. 535–542.
14. Warner J. A double–blinded, randomized, placebo–controlled trial of cetirizine in preventing the onset of asthma in children with atopic dermatitis: 18 months treatment and 18 months posttreatment follow–up // J. Allergy Clin. Immunol. – 2001. – Vol. 108. – P. 929–937.
15. Bousquet J., Demerteau N., Mullol J. et al. Cost associated with persistent allergic rhinitis are reduced by levocetirizine // Allergy. – 2005. – Vol. 60. – P. 788–794.
16. Cranswick N., Turzikova J., Fuchs M., Hulhoven R. Levocetirizine in 1–2 year old children: pharmacokinetic and pharmacodynamics profile // Int. J. Clin. Pharmacol. Ther. – 2005. – Vol. 43. – P. 172–177.
17. Fadia M., Arifhodzic N., Al–Awadh R., Heines D. Intrecellular cytokine production in children with atopic dermatitis: effect of levocetirizine treatment // Pediatrijadanas. – 2009. – Vol. 5. – P. 161–171.











